Producido a partir de plasma humano procedente de donantes humanos.
|
|
|
- Juan Rey Navarro
- hace 7 años
- Vistas:
Transcripción
1 1. NOMBRE DEL MEDICAMENTO Flebogamma DIF 50 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina humana normal (IgIV) Un ml contiene: Inmunoglobulina humana normal 50 mg (La pureza es de al menos 97% IgG) Cada vial de 10 ml contiene: 0,5 g de inmunoglobulina humana normal Cada vial de 50 ml contiene: 2,5 g de inmunoglobulina humana normal Cada vial de 100 ml contiene: 5 g de inmunoglobulina humana normal Cada vial de 200 ml contiene: 10 g de inmunoglobulina humana normal Cada vial de 400 ml contiene: 20 g de inmunoglobulina humana normal El porcentaje de subclases IgG es (valores aproximados): IgG 1 66,6% IgG 2 28,5% IgG 3 2,7% IgG 4 2,2% El contenido máximo de IgA es de 50 microgramos/ml. Producido a partir de plasma humano procedente de donantes humanos. Excipiente con efecto conocido: Un ml contiene 50 mg de D-sorbitol. Para consultar la lista completa de excipientes, ver sección FORMA FARMACÉUTICA Solución para perfusión. La solución es transparente o ligeramente opalescente, incolora o de color amarillo pálido. Flebogamma DIF es isotónico, con una osmolalidad de 240 a 370 mosm/kg. 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Flebogamma DIF está indicado para: Tratamiento de reposición en adultos, niños y adolescentes (2-18 años) en: - Síndromes de inmunodeficiencia primaria con producción de anticuerpos deteriorada (ver sección 4.4). 1
2 - Hipogammaglobulinemia e infecciones bacterianas recurrentes en pacientes con leucemia linfocítica crónica en los que los antibióticos profilácticos no han dado resultado. - Hipogammaglobulinemia e infecciones bacterianas recurrentes en pacientes con mieloma múltiple en fase estacionaria y que no respondieron a la inmunización neumocócica. - Hipogammaglobulinemia en pacientes después de un trasplante alogénico de células madre. - SIDA congénito con infecciones bacterianas recurrentes. Inmunomodulación en adultos, niños y adolescentes (2-18 años) en: - Trombocitopenia inmune primaria, en pacientes con riesgo elevado de sufrir hemorragia o en pacientes antes de someterse a cirugía para corregir el recuento de plaquetas. - Síndrome de Guillain Barré. - Enfermedad de Kawasaki. 4.2 Posología y forma de administración El tratamiento de reposición debe iniciarse y monitorizarse bajo la supervisión de un médico con experiencia en el tratamiento de inmunodeficiencias. Posología La dosis y el régimen de dosificación dependen de la indicación. En el tratamiento de reposición puede ser necesario individualizar la dosificación para cada paciente, dependiendo de su respuesta clínica y farmacocinética. A título informativo se indica el siguiente régimen de dosificación. Tratamiento de reposición en síndromes de inmunodeficiencia primaria El régimen de dosificación debe alcanzar un nivel de IgG pre-infusión (medido antes de la siguiente perfusión) de por lo menos 5 a 6 g/l. Se requieren de tres a seis meses desde el inicio del tratamiento para establecer el estado estacionario. La dosis inicial recomendada es de 0,4-0,8 g/kg en una única administración, seguida de al menos 0,2 g/kg cada tres o cuatro semanas. La dosis requerida para conseguir un nivel pre-infusión de 5-6 g/l es de aproximadamente 0,2-0,8 g/kg/mes. El intervalo de dosificación cuando se ha conseguido el estado estacionario varía de 3 a 4 semanas. Los niveles pre-infusión deben medirse y valorarse junto con la incidencia de la infección. Para reducir el nivel de infección, puede ser necesario incrementar la dosis a fin de alcanzar los niveles pre-infusión superiores. Hipogammaglobulinemia e infecciones bacterianas recurrentes en pacientes con leucemia linfocítica crónica en los que los antibióticos profilácticos no han dado resultado; hipogammaglobulinemia e infecciones bacterianas recurrentes en pacientes con mieloma múltiple en fase estacionaria, que no respondieron a la inmunización de neumocócica; niños y adolescentes con SIDA congénito e infecciones bacterianas recurrentes La dosis recomendada es de 0,2-0,4 g/kg cada tres o cuatro semanas. 2
3 Hipogammaglobulinemia en pacientes después de un trasplante alogénico de células madre hematopoyéticas La dosis recomendada es de 0,2-0,4 g/kg cada tres o cuatro semanas. Los niveles pre-infusión deben mantenerse por encima de 5 g/l. Trombocitopenia inmune primaria Existen dos regímenes alternativos de tratamiento: 0,8 a 1 g/kg administrados el primer día; esta dosis puede repetirse una vez en los tres días siguientes 0,4 g/kg administrados diariamente durante 2-5 días. El tratamiento puede repetirse en caso de recidiva. Síndrome de Guillain Barré 0,4 g/kg/día durante 5 días. Enfermedad de Kawasaki Deben administrarse 1,6-2,0 g/kg divididos en varias dosis durante 2-5 días o 2,0 g/kg en dosis única. Los pacientes deben recibir tratamiento concomitante con ácido acetilsalicílico. La posología recomendada se detalla en la siguiente tabla: Indicación Dosis Frecuencia de perfusión Tratamiento de reposición en inmunodeficiencia primaria - dosis inicial: 0,4-0,8 g/kg - dosis cada 3-4 semanas para obtener un posteriores: nivel de IgG pre-infusión de al menos 0,2-0,8 g/kg 5-6 g/l Tratamiento de reposición en inmunodeficiencia secundaria SIDA congénito Hipogammaglobulinemia (< 4 g/l) en pacientes después de un trasplante alogénico de células madre hematopoyéticas 0,2-0,4 g/kg 0,2-0,4 g/kg 0,2-0,4 g/kg cada 3-4 semanas para obtener un nivel de IgG pre-infusión de al menos 5-6 g/l cada 3-4 semanas cada 3-4 semanas para obtener un nivel de IgG pre-infusión por encima de 5 g/l. 3
4 Inmunomodulación: Trombocitopenia inmune primaria Síndrome de Guillain Barré Enfermedad de Kawasaki Población pediátrica 0,8-1 g/kg o 0,4 g/kg/d 0,4 g/kg/d 1,6-2 g/kg o 2 g/kg el 1 er día, pudiéndose repetir una vez dentro de los 3 días siguientes de 2-5 días durante 5 días en varias dosis durante 2-5 días, junto con ácido acetilsalicílico en una dosis, junto con ácido acetilsalicílico Flebogamma DIF 50 mg/ml está contraindicado en niños de 0 a 2 años (ver sección 4.3). La posología en niños y adolescentes (2-18) no es diferente de la de los adultos, puesto que la posología para cada indicación va asociada al peso corporal y se ajusta al resultado clínico de las condiciones arriba indicadas. Forma de administración Por vía intravenosa. Flebogamma DIF 50 mg/ml debe administrarse por vía intravenosa a una velocidad inicial de 0,01-0,02 ml/kg/min durante los primeros treinta minutos. Si se tolera bien (ver sección 4.4), la velocidad de administración puede aumentarse gradualmente hasta un máximo de 0,1 ml/kg/min. 4.3 Contraindicaciones Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1 (ver sección 4.4). Hipersensibilidad a inmunoglobulinas humanas, especialmente en pacientes con anticuerpos anti-iga. Intolerancia a la fructosa (ver sección 4.4). En bebés y niños pequeños (0-2 años), la intolerancia hereditaria a la fructosa (IHF) puede no haber sido diagnosticada y podría ser fatal, por lo que no deben recibir este medicamento. 4.4 Advertencias y precauciones especiales de empleo Sorbitol Cada ml de este medicamento contiene 50 mg de sorbitol. Aquellos pacientes que padezcan problemas hereditarios poco comunes de intolerancia a la fructosa no deben tomar este medicamento. En personas de más de 2 años de edad con IHF, se desarrolla una aversión espontánea a la fructosa que contienen algunos alimentos y que puede dar lugar a la aparición de algunos síntomas (tales como vómitos, trastornos gastrointestinales, apatía, retardo de altura y peso). Por lo tanto, es necesario un historial detallado con respecto a los síntomas de la IHF para cada paciente antes de recibir Flebogamma DIF. En el caso de que se hubiera administrado sin haber realizado dicha comprobación y se sospeche de la presencia de intolerancia a la fructosa, se deberá detener inmediatamente la 4
5 perfusión, proceder a reestablecer el nivel normal de glicemia y a estabilizar la función orgánica mediante cuidados intensivos. No son de esperar interferencias en la determinación de los niveles de glucosa en sangre. Determinadas reacciones adversas graves pueden estar relacionadas con la velocidad de administración. La velocidad de administración recomendada descrita en la sección 4.2 debe respetarse estrictamente. Los pacientes deben ser monitorizados y vigilados minuciosamente por si aparece algún síntoma durante el periodo de perfusión. Determinadas reacciones adversas pueden producirse de forma más frecuente: - en caso de una elevada velocidad de perfusión, - en pacientes que reciben inmunoglobulina humana normal por primera vez o, en casos poco frecuentes, al cambiar de producto de inmunoglobulina humana normal o cuando ha transcurrido un largo periodo desde la perfusión anterior. Con frecuencia, las posibles complicaciones pueden evitarse, comprobando que: - los pacientes no sean sensibles a la inmunoglobulina humana normal, inyectando primero el medicamento lentamente (a una velocidad inicial de 0,01-0,02 ml/kg/min). - durante todo el periodo de perfusión, se vigile minuciosamente la presencia de cualquier síntoma en los pacientes. En particular, los pacientes tratados por primera vez con inmunoglobulina humana normal, pacientes que han cambiado de producto IgIV o cuando ha transcurrido un largo periodo de tiempo desde la perfusión anterior, deben monitorizarse durante la primera perfusión y durante la primera hora después de la primera perfusión a fin de detectar posibles reacciones adversas. Se debe observar al resto de pacientes al menos durante 20 minutos después de la administración. En caso de que se produzcan reacciones adversas, se reducirá la velocidad de administración o se suspenderá la administración. El tratamiento adecuado depende de la naturaleza y gravedad de las reacciones adversas. En caso de shock, se debe proceder de acuerdo con el tratamiento médico estándar. En todos los pacientes, la administración de IgIV requiere: - una hidratación adecuada antes de iniciar la perfusión de IgIV - monitorizar la diuresis - monitorizar los niveles de creatinina sérica - evitar el uso concomitante de diuréticos del asa. Hipersensibilidad Las reacciones de hipersensibilidad son poco frecuentes y se pueden producir en pacientes con anticuerpos anti-iga. IgIV no está indicado en pacientes con deficiencia de IgA selectiva si ésta es la única alteración destacable. Raramente, la inmunoglobulina humana normal puede producir un descenso brusco de la presión arterial asociada con una reacción anafiláctica, incluso en pacientes que toleraron bien tratamientos anteriores con inmunoglobulina humana normal. Tromboembolismo Existen evidencias clínicas que asocian la administración de IgIV con la aparición de eventos tromboembólicos como el infarto de miocardio, accidente cerebro vascular (incluyendo ictus), embolismo pulmonar y trombosis venosa profunda, que se suponen que están relacionados con el incremento relativo de la viscosidad sanguínea por el alto flujo de la inmunoglobulina en pacientes de 5
6 riesgo. Se debe tener precaución al prescribir y perfundir una IgIV en pacientes obesos y en pacientes con factores de riesgo preexistentes de eventos trombóticos (como edad avanzada, hipertensión, diabetes mellitus y con historia de enfermedad vascular o eventos trombóticos, pacientes con trombofilia congénita o adquirida, pacientes con periodos prolongados de inmovilización, pacientes con hipovolemia grave y pacientes con enfermedades que incrementen la viscosidad de la sangre). En aquellos pacientes con riesgo de sufrir reacciones adversas tromboembólicas, se deben administrar los productos con IgIV a la mínima velocidad de perfusión y dosis practicable. Insuficiencia renal aguda Se han notificado casos de insuficiencia renal aguda en pacientes que recibieron tratamiento con IgIV. En la mayoría de casos, se han identificado los factores de riesgo, tales como insuficiencia renal preexistente, diabetes mellitus, hipovolemia, sobrepeso, tratamiento concomitante con fármacos nefrotóxicos o edad superior a 65 años. En caso de insuficiencia renal, debe considerarse suspender el tratamiento con IgIV. Mientras que los casos de disfunción renal y de insuficiencia renal aguda se han asociado con el uso de algunas IgIV comercializadas que emplean diversos excipientes como sacarosa, glucosa y maltosa, se ha observado que existe una acumulación de casos en aquellas que contienen sacarosa como estabilizante. En pacientes de riesgo debe considerarse el uso de productos IgIV que no contengan estos excipientes. Flebogamma DIF no contiene sacarosa, maltosa ni glucosa. En los pacientes con riesgo de presentar fallo renal agudo, los productos de IgIV deben ser administrados a la mínima concentración y velocidad de perfusión posible. Síndrome de meningitis aséptica Se ha notificado un síndrome de meningitis aséptica asociado al tratamiento con IgIV. La interrupción del tratamiento con IgIV ha hecho remitir el síndrome en unos días y sin secuelas. El síndrome suele aparecer desde varias horas a 2 días después del tratamiento con IgIV. Los estudios de líquido cefalorraquídeo suelen revelar pleocitosis con varios miles de células por mm 3, principalmente de la serie granulocítica, y niveles elevados de proteína con varios cientos de mg/dl. Este síndrome suele darse con más frecuencia asociado a altas dosis de IgIV (2 g/kg). Anemia hemolítica Los productos con IgIV pueden contener anticuerpos de grupos sanguíneos, pudiendo actuar como hemolisinas e inducir a la aglutinación in vivo de glóbulos rojos con inmunoglobulinas in vivo, causando una reacción antiglobulina directa positiva (test de Coombs) y, en raras ocasiones, una hemólisis. La anemia hemolítica puede desarrollarse tras el tratamiento con IgIV debido a una mayor captación de glóbulos rojos. Los pacientes que reciben IgIV deben ser monitorizados para la detección de signos clínicos y síntomas de hemólisis. (Ver sección 4.8) Interferencia con pruebas serológicas Después de la inyección de inmunoglobulina, el incremento transitorio de varios de los anticuerpos transferidos de forma pasiva a la sangre del paciente puede dar lugar a la aparición de falsos positivos en pruebas serológicas. La transmisión pasiva de anticuerpos de antígenos eritrocitarios, por ejemplo A, B, D, puede afectar a algunas pruebas serológicas de anticuerpos eritrocitarios, por ejemplo al test directo de antiglobulina (DAT, test directo de Coombs). 6
7 Agentes transmisibles Para prevenir la transmisión de enfermedades infecciosas cuando se administran medicamentos derivados de la sangre o plasma humanos, se toman medidas estándar como la selección de donantes, análisis de marcadores específicos de infecciones en las donaciones individuales y las mezclas de plasma, así como la inclusión de etapas en el proceso de fabricación para eliminar e inactivar virus. A pesar de esto, cuando se administran medicamentos derivados de la sangre o plasma humanos, no se puede excluir totalmente la posibilidad de transmisión de agentes infecciosos. Esto también se refiere a virus y agentes infecciosos emergentes o de naturaleza desconocida. Las medidas tomadas se consideran efectivas para los virus envueltos como el VIH, VHB y VHC, y para los virus no envueltos de la hepatitis A y el parvovirus B19. Existe experiencia clínica que confirma la ausencia de transmisión de hepatitis A o parvovirus B19 con inmunoglobulinas y también se asume que el contenido de anticuerposconstituye una importante contribución en cuanto a seguridad vírica. Es altamente recomendable que cada vez que se administre Flebogamma DIF a un paciente, se deje constancia del nombre del medicamento y del número de lote administrado a fin de mantener una relación entre el paciente y el lote del producto. Población pediátrica Se recomienda monitorizar las constantes vitales de los pacientes pediátricos cuando se administre Flebogamma DIF. 4.5 Interacción con otros medicamentos y otras formas de interacción Vacunas con virus vivos atenuados La administración de inmunoglobulinas puede alterar la eficacia de las vacunas con virus vivos atenuados tales como sarampión, rubéola, paperas y varicela durante un periodo de al menos 6 semanas y hasta 3 meses. Después de la administración de este producto, se debe dejar transcurrir un periodo de 3 meses antes de administrar vacunas con virus vivos atenuados. En el caso del sarampión, esta interacción puede llegar hasta 1 año. Por lo tanto, se deben controlar los niveles de anticuerpos en pacientes que vayan a recibir la vacuna del sarampión. Población pediátrica Se espera que las mismas interacciones mencionadas para los adultos puedan observarse en la población pediátrica. 4.6 Fertilidad, embarazo y lactancia Embarazo No se ha establecido la seguridad de este medicamento en ensayos clínicos controlados en cuanto a su uso durante el embarazo y, por lo tanto, debe administrarse con precaución en mujeres embarazadas y madres en periodo de lactancia. Se ha demostrado que los productos con IgIV atraviesan la placenta de manera más intensa después del tercer trimestre. La experiencia clínica con inmunoglobulinas indica que no son de esperar efectos perjudiciales durante el embarazo, en el feto o en el recién nacido. Lactancia Las inmunoglobulinas se excretan con la leche materna y pueden contribuir a proteger al neonato frente a los patógenos que acceden al organismo a través de las mucosas. 7
8 Fertilidad La experiencia clínica con inmunoglobulinas indica que no son de esperar efectos perjudiciales sobre la fertilidad. 4.7 Efectos sobre la capacidad para conducir y utilizar máquinas La capacidad para conducir y utilizar máquinas puede verse afectada por algunas reacciones adversas, tales como mareo, relacionadas con Flebogamma DIF. Los pacientes que hayan sufrido reacciones adversas durante el tratamiento deben esperar a que éstas desaparezcan para poder conducir o utilizar máquinas. 4.8 Reacciones adversas Resumen del perfil de seguridad Ocasionalmente, pueden producirse reacciones adversas tales como escalofríos, cefalea, mareos, fiebre, vómitos, reacciones alérgicas, nauseas, artralgia, presión sanguínea baja y leve dolor de espalda. Raramente, la inmunoglobulina humana normal puede causar una disminución repentina de la presión sanguínea y, en casos aislados, shock anafiláctico, incluso cuando los pacientes no mostraron hipersensibilidad en anteriores administraciones. Con la inmunoglobulina humana normal se han observado casos de meningitis aséptica reversible y casos raros de reacciones cutáneas transitorias. Se han observado reacciones hemolíticas reversibles, especialmente en pacientes de los grupos sanguíneos A, B y AB. Raramente, después de un tratamiento con IgIV de dosis elevada, el paciente puede desarrollar una anemia hemolítica que requiera transfusión (ver también Sección 4.4). Se ha observado un incremento en los niveles de creatinina sérica y/o insuficiencia renal aguda. Muy raramente: reacciones tromboembólicas tales como infarto de miocardio, accidente cerebro vascular, embolia pulmonar y trombosis venosa profunda. En cuanto a la seguridad con respecto a agentes transmisibles, ver sección 4.4. Tabla de las reacciones adversas La siguiente tabla sigue la clasificación de órganos del sistema MedDRA (SOC y nivel de término preferido). Las frecuencias se han evaluado de acuerdo con los siguientes criterios: - muy frecuentes (>1/10) - frecuentes (>1/100, <1/10) - poco frecuentes (>1/1.000, <1/100) - raras (>1/10.000, <1/1.000) - muy raras (<1/10.000) - frecuencia no conocida (no puede estimarse a partir de los datos disponibles). Las reacciones adversas se presentan en orden decreciente de gravedad dentro de cada frecuencia. 8
9 Frecuencia de reacciones adversas (RA) en estudios clínicos con Flebogamma DIF 50 mg/ml Clasificación de órganos del sistema MedDRA Trastornos del sistema nervioso Trastornos vasculares Trastornos respiratorios, torácicos y mediastínicos Trastornos gastrointestinales Trastornos de la piel y del tejido subcutáneo Trastornos musculoesqueléticos y del tejido conjuntivo Trastornos generales y alteraciones en el lugar de administración Reacción adversa Cefalea Mareo Hipotensión, hipertensión, hipertensión diastólica, fluctuaciones en la presión sanguínea Bronquitis, tos, dificultad respiratoria Diarrea, nauseas, vómitos, dolor abdominal, dolor abdominal superior Urticaria, erupción con prurito, dermatitis de contacto Dolor de espalda, artralgia, mialgia, calambres musculares Fiebre, reacción en el punto de perfusión Rigidez, astenia, dolor, inflamación en el punto de perfusión, edema en el punto de perfusión, dolor en el punto de perfusión, prurito en el punto de perfusión, hinchazón en el punto de perfusión, migración del implante Exploraciones complementarias Test de Coombs positivo, disminución de la presión sistólica de la sangre, incremento de la presión sistólica de la sangre, incremento de la temperatura corporal Frecuencia Frecuentes Frecuentes Descripción de las reacciones adversas seleccionadas Las reacciones adversas notificadas con más frecuencia desde que se autorizó el medicamento para ambas concentraciones fueron dolor en el pecho, eritema, aumento y disminución de la presión arterial, malestar, disnea, náuseas, vómitos, pirexia, dolor de espalda, cefalea y escalofríos. Población pediátrica Se evaluaron los resultados de seguridad obtenidos en 29 pacientes pediátricos ( 17 años) incluidos en los estudios de inmunodeficiencia primaria. Se observó que la proporción de cefalea, pirexia, taquicardias e hipotensión era mayor en niños que en adultos. La evaluación de las constantes vitales en los estudios clínicos realizados en la población pediátrica no mostró ningún patrón de cambios clínicamente relevante. Notificación de sospechas de reacciones adversas Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: Sobredosis La sobredosis puede provocar sobrecarga de fluidos e hiperviscosidad, particularmente en pacientes de riesgo, incluyendo ancianos o pacientes con insuficiencia renal. 9
10 Población pediátrica No hay datos en cuanto a la sobredosis con Flebogamma DIF en niños. Sin embargo, al igual que en la población adulta, la sobredosis puede provocar sobrecarga de fluidos e hiperviscosidad, como en otras inmunoglobulinas intravenosas. 5. PROPIEDADES FARMACOLÓGICAS 5.1 Propiedades farmacodinámicas Grupo farmacoterapéutico: sueros inmunes e inmunoglobulinas: inmunoglobulina humana normal para administración intravascular. Código ATC: J06BA02. La inmunoglobulina humana normal contiene principalmente inmunoglobulina G (IgG) con un amplio espectro de anticuerpos contra a agentes infecciosos. La inmunoglobulina humana normal contiene los anticuerpos IgG presentes en la población normal. Normalmente se prepara a partir de mezclas de plasma de no menos de 1000 donaciones. La distribución de subclases de la inmunoglobulina G es estrechamente proporcional a la del plasma humano nativo. Las dosis suficientes de este producto farmacéutico pueden restablecer las concentraciones anormalmente bajas de inmunoglobulina G hasta los valores normales. El mecanismo de acción en aquellas indicaciones distintas al tratamiento de reposición no se ha aclarado completamente, pero incluye efectos inmunomoduladores. En el ensayo clínico realizado con pacientes con PTI crónica se obtuvo un incremento significativo en los niveles medios de plaquetas (64.000/microlitros), aunque sin alcanzar los niveles normales. Se realizaron tres ensayos clínicos con Flebogamma DIF, dos de tratamiento de reposición en pacientes con inmunodeficiencia primaria (uno en adultos y en niños de más de 10 años y otro en niños de entre 2 y 16 años) y otro de inmunomodulación en pacientes adultos con púrpura trombocitopénica inmune. 5.2 Propiedades farmacocinéticas Inmediatamente después de su administración intravenosa, la inmunoglobulina está completamente biodisponible en la circulación del paciente. Se distribuye con relativa rapidez entre el plasma y el líquido extravascular, alcanzándose aproximadamente después de 3-5 días un equilibrio entre los compartimentos intravascular y extravascular. Flebogamma DIF 50 mg/ml tiene una semivida de días. Esta semivida puede variar según el paciente, sobre todo en casos de inmunodeficiencia primaria. Las IgG y los complejos IgG se catabolizan en las células del sistema retículo endotelial. Población pediátrica No se esperan diferencias en las propiedades farmacocinéticas en la población pediátrica. 5.3 Datos preclínicos sobre seguridad Se realizaron estudios de toxicidad a dosis única con ratas y cobayas. La ausencia de mortalidad en los estudios no-clínicos realizados con Flebogamma DIF con dosis de hasta 2500 mg/kg y la ausencia 10
11 total de reacciones adversas relevantes que afectaran al sistema respiratorio, circulatorio y nervioso central de los animales tratados demuestran la seguridad de Flebogamma DIF. Los estudios de toxicidad a dosis repetida y los estudios de toxicidad embrio-fetal no se pueden realizar debido a la inducción y a la interferencia con anticuerpos. No se han estudiado los efectos del medicamento sobre el sistema inmunitario del recién nacido. 6. DATOS FARMACÉUTICOS 6.1 Lista de excipientes D-sorbitol Agua para preparaciones inyectables 6.2 Incompatibilidades En ausencia de estudios de compatibilidad, este medicamento no debe mezclarse con otros. 6.3 Periodo de validez 2 años. 6.4 Precauciones especiales de conservación No conservar a temperatura superior a 30 ºC. No congelar. 6.5 Naturaleza y contenido del envase 10 ml, 50 ml, 100 ml, 200 ml o 400 ml de solución en viales (vidrio tipo II) con tapón (caucho clorobutilo). Tamaño del envase: 1 vial Puede que solamente estén comercializados algunos tamaños de envases. 6.6 Precauciones especiales de eliminación y otras manipulaciones El medicamento debe alcanzar la temperatura ambiente o corporal antes de su uso. La solución debe ser transparente o ligeramente opalescente e incolora o de color amarillo pálido. Las soluciones que estén turbias o presenten sedimentos no deben utilizarse. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local. 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Instituto Grifols, S.A. Can Guasc, 2 - Parets del Vallès Barcelona - España 11
12 8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN EU/1/07/404/ FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN Fecha de la primera autorización: 23 de Agosto de 2007 Fecha de la última renovación: 30 de Agosto de FECHA DE LA REVISIÓN DEL TEXTO 07/2014 La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos 12
Producido a partir de plasma humano procedente de donantes humanos.
 1. NOMBRE DEL MEDICAMENTO Flebogamma DIF 100 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina humana normal (IgIV) Un ml contiene: Inmunoglobulina humana normal 100
1. NOMBRE DEL MEDICAMENTO Flebogamma DIF 100 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina humana normal (IgIV) Un ml contiene: Inmunoglobulina humana normal 100
Un ml contiene 50 mg de inmunoglobulina humana normal, de los cuales al menos el 97% es IgG.
 1. NOMBRE DEL MEDICAMENTO Flebogamma 5% DIF solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 50 mg de inmunoglobulina humana normal, de los cuales al menos el 97% es IgG.
1. NOMBRE DEL MEDICAMENTO Flebogamma 5% DIF solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 50 mg de inmunoglobulina humana normal, de los cuales al menos el 97% es IgG.
Prospecto: información para el usuario. Plangamma 50 mg/ml solución para perfusión Inmunoglobulina humana normal (IgIV)
 Prospecto: información para el usuario Plangamma 50 mg/ml solución para perfusión Inmunoglobulina humana normal (IgIV) Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
Prospecto: información para el usuario Plangamma 50 mg/ml solución para perfusión Inmunoglobulina humana normal (IgIV) Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
Producido a partir de plasma humano procedente de donantes humanos.
 1. NOMBRE DEL MEDICAMENTO Flebogamma 10% DIF solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina humana normal (IgIV) Un ml contiene: Inmunoglobulina humana normal 100 mg
1. NOMBRE DEL MEDICAMENTO Flebogamma 10% DIF solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina humana normal (IgIV) Un ml contiene: Inmunoglobulina humana normal 100 mg
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Flebogamma DIF 50 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Flebogamma DIF 50 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina
0,5 g. 0,5 g. D-Sorbitol Agua inyectable cbp 10 ml 50 ml 100 ml 200 ml 400 ml
 INFORMACIÓN PARA PRESCRIBIR AMPLIA IPP-A 1. DENOMINACIÓN DISTINTIVA FLEBOGAMMA I.V. 5% 2. DENOMINACIÓN GENÉRICA Inmunoglobulina humana normal endovenosa 3. FORMA FARMACÉUTICA Y FORMULACIÓN Solución inyectable
INFORMACIÓN PARA PRESCRIBIR AMPLIA IPP-A 1. DENOMINACIÓN DISTINTIVA FLEBOGAMMA I.V. 5% 2. DENOMINACIÓN GENÉRICA Inmunoglobulina humana normal endovenosa 3. FORMA FARMACÉUTICA Y FORMULACIÓN Solución inyectable
100 UI 80 mg 95% IgG
 1. NOMBRE DEL MEDICAMENTO IGANTIBE 200 UI/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 100 UI/0,5 ml 600 UI/3 ml 1000 UI/5 ml Inmunoglobulina humana antihepatitis
1. NOMBRE DEL MEDICAMENTO IGANTIBE 200 UI/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 100 UI/0,5 ml 600 UI/3 ml 1000 UI/5 ml Inmunoglobulina humana antihepatitis
600 U.I. 480 mg 95% Ig. 67,5 mg 9,0 mg 3 ml. Solución inyectable con inmunoglobulinas, principalmente inmunoglobulina G (IgG).
 1. NOMBRE DEL MEDICAMENTO GAMMA ANTI-HEPATITIS B GRIFOLS 600 U.I. GAMMA ANTI-HEPATITIS B GRIFOLS 1000 U.I. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 600 U.I. 1000 U.I. Inmunoglobulina
1. NOMBRE DEL MEDICAMENTO GAMMA ANTI-HEPATITIS B GRIFOLS 600 U.I. GAMMA ANTI-HEPATITIS B GRIFOLS 1000 U.I. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 600 U.I. 1000 U.I. Inmunoglobulina
Terapia de reposición en adultos y niños en síndromes de inmunodeficiencia primaria tales como:
 1. NOMBRE DEL MEDICAMENTO IGAMPLIA 160 mg/ml SOLUCIÓN INYECTABLE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 320 mg/2 ml 800 mg/5 ml Inmunoglobulina humana normal (Proteínas humanas (Proporción
1. NOMBRE DEL MEDICAMENTO IGAMPLIA 160 mg/ml SOLUCIÓN INYECTABLE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 320 mg/2 ml 800 mg/5 ml Inmunoglobulina humana normal (Proteínas humanas (Proporción
Inmunoglobulina humana normal (IgIV) mg* *correspondiente al contenido en proteína humana, de la cual al menos el 98% es IgG.
 1. NOMBRE DEL MEDICAMENTO KIOVIG 100 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene: Inmunoglobulina humana normal (IgIV)...100 mg* *correspondiente al contenido
1. NOMBRE DEL MEDICAMENTO KIOVIG 100 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene: Inmunoglobulina humana normal (IgIV)...100 mg* *correspondiente al contenido
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
Inmunoglobulina humana normal (IgIV) mg* *correspondiente al contenido en proteína humana, de la cual al menos el 98% es IgG.
 1. NOMBRE DEL MEDICAMENTO KIOVIG 100 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene: Inmunoglobulina humana normal (IgIV)...100 mg* *correspondiente al contenido
1. NOMBRE DEL MEDICAMENTO KIOVIG 100 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene: Inmunoglobulina humana normal (IgIV)...100 mg* *correspondiente al contenido
FICHA TÉCNICA. Albutein 5% es una solución que contiene 50 g/l de proteína total, de las cuales al menos un 95% es albúmina humana.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Albutein 5% solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Albúmina humana. Albutein 5% es una solución que contiene 50 g/l de proteína total,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Albutein 5% solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Albúmina humana. Albutein 5% es una solución que contiene 50 g/l de proteína total,
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
FICHA TÉCNICA. Virus de la gripe fraccionados*, inactivados, que contienen antígenos equivalentes a:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VACUNA ANTIGRIPAL POLIVALENTE LETI VIRUS FRACCIONADOS SUSPENSIÓN INYECTABLE EN JERINGA PRECARGADA. Vacuna antigripal de virus fraccionados inactivados. 2. COMPOSICIÓN
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VACUNA ANTIGRIPAL POLIVALENTE LETI VIRUS FRACCIONADOS SUSPENSIÓN INYECTABLE EN JERINGA PRECARGADA. Vacuna antigripal de virus fraccionados inactivados. 2. COMPOSICIÓN
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en jeringa precargada Vacuna antidiftero-tetánica (adsorbida) para adultos y adolescentes. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en jeringa precargada Vacuna antidiftero-tetánica (adsorbida) para adultos y adolescentes. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA
 La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA VARICELA Definición: La varicela es una enfermedad infecciosa causada por un virus llamado Varicela zoster (VVZ). Cuando se produce la reactivación
La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA VARICELA Definición: La varicela es una enfermedad infecciosa causada por un virus llamado Varicela zoster (VVZ). Cuando se produce la reactivación
FICHA TECNICA. Adultos en prediálisis o en diálisis: 1 dosis (40 µg) de 1 ml en cada inyección.
 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 40 mg Vacuna recombinante antihepatitis B. FICHA TECNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 40microgramos/ ml, suspensión inyectable
1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 40 mg Vacuna recombinante antihepatitis B. FICHA TECNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 40microgramos/ ml, suspensión inyectable
- Como disolvente de medicamentos en polvo o liofilizados, previamente a su administración. - Como diluyente de soluciones y/o medicamentos.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO HIPRAVIAR-BPL2 Emulsión inyectable para aves 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de vacuna
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO HIPRAVIAR-BPL2 Emulsión inyectable para aves 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de vacuna
IGAMAD 750 UI/ml SOLUCIÓN INYECTABLE EN JERINGA PRECARGADA. 213 mg 95% IgG. Cloruro sódico 4 mg 5 mg 6 mg
 1. NOMBRE DEL MEDICAMENTO IGAMAD 750 UI/ml SOLUCIÓN INYECTABLE EN JERINGA PRECARGADA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 1000 UI/1,33 ml 1250 UI/1,67 ml 1500 UI/2 ml Inmunoglobulina
1. NOMBRE DEL MEDICAMENTO IGAMAD 750 UI/ml SOLUCIÓN INYECTABLE EN JERINGA PRECARGADA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 1000 UI/1,33 ml 1250 UI/1,67 ml 1500 UI/2 ml Inmunoglobulina
Ficha Técnica. La solución contiene un 20% de proteína, de la que al menos el 95% es albúmina humana.
 Ficha Técnica 1 Denominación del medicamento ALBÚMINA HUMANA 20% Baxter, Solución para perfusión intravenosa 2 Composición cualitativa y cuantitativa Albúmina humana. La solución contiene un 20% de proteína,
Ficha Técnica 1 Denominación del medicamento ALBÚMINA HUMANA 20% Baxter, Solución para perfusión intravenosa 2 Composición cualitativa y cuantitativa Albúmina humana. La solución contiene un 20% de proteína,
Vacuna frente al papilomavirus humano. (Comentarios a las fichas técnicas)
 Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Medicamento con autorización anulada
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO ImmunoGam 312 UI/ml, solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene 312
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO ImmunoGam 312 UI/ml, solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene 312
Cepa derivada de A/California/7/2009 (H1N1)pdm09: (NYMC X-181) 15 microgramos HA** Cepa derivada de A/Victoria/361/2011 (H3N2): (IVR-165)
 1. NOMBRE DEL MEDICAMENTO CHIROFLU, suspensión inyectable en jeringa precargada Vacuna antigripal de antígeno de superficie, inactivado. (CAMPAÑA 2012/2013) 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Antígenos
1. NOMBRE DEL MEDICAMENTO CHIROFLU, suspensión inyectable en jeringa precargada Vacuna antigripal de antígeno de superficie, inactivado. (CAMPAÑA 2012/2013) 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Antígenos
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO Hodernal 800 mg/ml solución oral Parafina líquida 1. NOMBRE DEL MEDICAMENTO Hodernal 800 mg/ml solución oral. 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO Hodernal 800 mg/ml solución oral Parafina líquida 1. NOMBRE DEL MEDICAMENTO Hodernal 800 mg/ml solución oral. 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
La actividad específica de Trypsan es 0,5 mg de alfa-1-antitripsina activa/mg de proteína. Para información sobre excipientes, ver 6.1.
 FOLLETO DE INFORMACIÓN AL PROFESIONAL 1. NOMBRE DEL MEDICAMENTO Trypsan 0,5 g Polvo liofilizado para solución inyectable con solvente Trypsan 1 g Polvo liofilizado para solución inyectable con solvente
FOLLETO DE INFORMACIÓN AL PROFESIONAL 1. NOMBRE DEL MEDICAMENTO Trypsan 0,5 g Polvo liofilizado para solución inyectable con solvente Trypsan 1 g Polvo liofilizado para solución inyectable con solvente
ENOXPRIM. Solución inyectable. Solución inyectable estéril, libre de pirógenos, contenida en jeringas pre-llenadas listas para usarse.
 ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
FICHA TECNICA ROPHYLAC
 FICHA TECNICA ROPHYLAC RHOPHYLAC Solución INYECTABLE 300 mcg/2 Ml Jeringa de vidrio (Vidrio de Clase 1) prellenada con 2 ml de solución inyectable (1500 UI de inmunoglobulina anti D Indicaciones: Profilaxis
FICHA TECNICA ROPHYLAC RHOPHYLAC Solución INYECTABLE 300 mcg/2 Ml Jeringa de vidrio (Vidrio de Clase 1) prellenada con 2 ml de solución inyectable (1500 UI de inmunoglobulina anti D Indicaciones: Profilaxis
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA. Rhophylac 300 microgramos / 2 ml de solución inyectable en jeringa precargada.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Rhophylac 300 microgramos / 2 ml de solución inyectable en jeringa precargada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Cada jeringa precargada
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Rhophylac 300 microgramos / 2 ml de solución inyectable en jeringa precargada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Cada jeringa precargada
FICHA TÉCNICA. Por sobre: Acetato de calcio, 2,5 g (equivale a 635 mg de calcio), almidón de maíz, manitol (E421)
 FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
FICHA TÉCNICA. Tratamiento de la incontinencia urinaria asociada a la insuficiencia del esfínter uretral en la perra.
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
Inflexal V, suspensión inyectable Vacuna antigripal (antígeno de superficie, inactivado, virosoma). Campaña 2013/2014
 RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Inflexal V, suspensión inyectable Vacuna antigripal (antígeno de superficie, inactivado, virosoma). Campaña 2013/2014 2. COMPOSICIÓN
RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Inflexal V, suspensión inyectable Vacuna antigripal (antígeno de superficie, inactivado, virosoma). Campaña 2013/2014 2. COMPOSICIÓN
Octalbin 200 mg/ml solución para perfusión
 Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BOVILIS BVD Suspensión inyectable para bovino. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por dosis
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BOVILIS BVD Suspensión inyectable para bovino. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por dosis
La osmolaridad calculada de la solución es de 154 mosm/l y el ph de 4,5-7,0. El contenido teórico en sodio y en cloruro es de 77 mmol/l.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Cloruro de Sodio Grifols 0,45% solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml de solución contienen: Cloruro de sodio, 0,45 g La osmolaridad
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Cloruro de Sodio Grifols 0,45% solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml de solución contienen: Cloruro de sodio, 0,45 g La osmolaridad
PROSPECTO: INFORMACIÓN PARA EL USUARIO. CITICOLINA Normon 1000 mg solución inyectable EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO CITICOLINA Normon 1000 mg solución inyectable EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información importante
PROSPECTO: INFORMACIÓN PARA EL USUARIO CITICOLINA Normon 1000 mg solución inyectable EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información importante
FICHA TECNICA. Tratamiento de la intoxicación por Amanita phalloides.
 FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Eurican MHPPi 2 -LR Liofilizado y suspensión para suspensión inyectable 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Eurican MHPPi 2 -LR Liofilizado y suspensión para suspensión inyectable 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Glucosamina KERN PHARMA 1.500 mg polvo para solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Glucosamina KERN PHARMA 1.500 mg polvo para solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre
Prospecto: información para el usuario
 Prospecto: información para el usuario Mucosan 6 mg/ml jarabe Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
Prospecto: información para el usuario Mucosan 6 mg/ml jarabe Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO KIOVIG 100 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina humana
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO KIOVIG 100 mg/ml solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Inmunoglobulina humana
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR
 INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR 1. NOMBRE DEL MEDICAMENTO Disolgas 257,5 mg cápsulas blandas 2. PRINCIPIO(S) ACTIVO(S) 3. LISTA DE EXCIPIENTES Amarillo anaranjado S (E 110), azorrubina
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR 1. NOMBRE DEL MEDICAMENTO Disolgas 257,5 mg cápsulas blandas 2. PRINCIPIO(S) ACTIVO(S) 3. LISTA DE EXCIPIENTES Amarillo anaranjado S (E 110), azorrubina
FICHA TÉCNICA. 1. NOMBRE COMERCIAL DEL MEDICAMENTO Rhesuman Berna P 1250 UI (250 µg) polvo liofilizado y disolvente para solución inyectable
 FICHA TÉCNICA 1. NOMBRE COMERCIAL DEL MEDICAMENTO Rhesuman Berna P 1250 UI (250 µg) polvo liofilizado y disolvente para solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa:
FICHA TÉCNICA 1. NOMBRE COMERCIAL DEL MEDICAMENTO Rhesuman Berna P 1250 UI (250 µg) polvo liofilizado y disolvente para solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa:
Anexo III. Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos
 Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable
 FICHA TÉCNICA VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable 1. NOMBRE DEL MEDICAMENTO VAXIGRIP, suspensión inyectable en jeringa precargada Vacuna antiinfluenza de virus fraccionados,
FICHA TÉCNICA VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable 1. NOMBRE DEL MEDICAMENTO VAXIGRIP, suspensión inyectable en jeringa precargada Vacuna antiinfluenza de virus fraccionados,
FICHA TÉCNICA. Azelastina hidrocloruro al 0,05% (0,5 mg/ml). Cada gota contiene 0,015 mg de azelastina hidrocloruro
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Azelastina MABO 0,5 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Azelastina hidrocloruro al 0,05% (0,5
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Azelastina MABO 0,5 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Azelastina hidrocloruro al 0,05% (0,5
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
PROSPECTO: INFORMACIÓN PARA EL USUARIO. ACETILCISTEÍNA BEXAL 100 mg polvo para solución oral EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO ACETILCISTEÍNA BEXAL 100 mg polvo para solución oral EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto, ya
PROSPECTO: INFORMACIÓN PARA EL USUARIO ACETILCISTEÍNA BEXAL 100 mg polvo para solución oral EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto, ya
Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp
 Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp Enf. María Guadalupe Vega Jefe de Piso Unidad de Terapia Intensiva Hospital General Las Américas, Ecatepec
Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp Enf. María Guadalupe Vega Jefe de Piso Unidad de Terapia Intensiva Hospital General Las Américas, Ecatepec
1. Qué es Actithiol Mucolítico adultos y para qué se utiliza
 Introducción PROSPECTO: INFORMACIÓN PARA EL USUARIO Actithiol Mucolítico adultos 50 mg/ml solución oral Carbocisteína Lea todo el prospecto detenidamente porque contiene información importante para usted.
Introducción PROSPECTO: INFORMACIÓN PARA EL USUARIO Actithiol Mucolítico adultos 50 mg/ml solución oral Carbocisteína Lea todo el prospecto detenidamente porque contiene información importante para usted.
FICHA TÉCNICA. ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
Alivio de los sofocos que aparecen durante la menopausia como consecuencia de la deprivación estrogénica.
 1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
4.2 Indicaciones de uso, especificando las especies a las que va destinado
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Loxicom 5 mg/ml solución inyectable para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Principio activo: Meloxicam Excipientes:
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Loxicom 5 mg/ml solución inyectable para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Principio activo: Meloxicam Excipientes:
FICHA TÉCNICA. Vispring 500 microgramos/ml colirio en solución en envases unidosis
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Vispring 500 microgramos/ml colirio en solución en envases unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de colirio en solución contiene: Tetrizolina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Vispring 500 microgramos/ml colirio en solución en envases unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de colirio en solución contiene: Tetrizolina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Plasbumin 20 % solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Plasbumin 20 % solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Albúmina humana. Solución de 200 g de proteínas plasmáticas/l con un 95% como mínimo
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Plasbumin 20 % solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Albúmina humana. Solución de 200 g de proteínas plasmáticas/l con un 95% como mínimo
SERPIENTES Definición:
 SERPIENTES Definición: Las serpientes u ofidios son reptiles caracterizados por la ausencia de extremidades y un cuerpo muy alargado. En España hay solo dos familias de serpientes venenosas: las víboras
SERPIENTES Definición: Las serpientes u ofidios son reptiles caracterizados por la ausencia de extremidades y un cuerpo muy alargado. En España hay solo dos familias de serpientes venenosas: las víboras
Prospecto: información para el usuario. LIZIPADOL 20 mg pastillas para chupar Ambroxol hidrocloruro
 Prospecto: información para el usuario LIZIPADOL 20 mg pastillas para chupar Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
Prospecto: información para el usuario LIZIPADOL 20 mg pastillas para chupar Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
THIPENTHAL. TIOPENTAL SÓDICO 1 g INYECTABLE. VENTA BAJO RECETA ARCHIVADA (Lista III) FÓRMULA CUALI Y CUANTITATIVA. Cada frasco ampolla contiene:
 THIPENTHAL TIOPENTALSÓDICO1g INYECTABLE VENTABAJORECETAARCHIVADA(ListaIII) FÓRMULACUALIYCUANTITATIVA Cadafrascoampollacontiene: Tiopentalsódicoestéril 1g ACCIÓNTERAPÉUTICA: Anestésicogeneral,barbitúrico.CódigoATC:N01AF03.
THIPENTHAL TIOPENTALSÓDICO1g INYECTABLE VENTABAJORECETAARCHIVADA(ListaIII) FÓRMULACUALIYCUANTITATIVA Cadafrascoampollacontiene: Tiopentalsódicoestéril 1g ACCIÓNTERAPÉUTICA: Anestésicogeneral,barbitúrico.CódigoATC:N01AF03.
CENAVUL Suspensión inyectable
 Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VERSIFEL FeLV suspensión inyectable para gatos 2. COMPOSICIÓN
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VERSIFEL FeLV suspensión inyectable para gatos 2. COMPOSICIÓN
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
TASIGNA (NILOTINIB) INFORMACIÓN DE SEGURIDAD PARA EL PACIENTE
 TASIGNA (NILOTINIB) INFORMACIÓN DE SEGURIDAD PARA EL PACIENTE Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), julio 2015 Índice
TASIGNA (NILOTINIB) INFORMACIÓN DE SEGURIDAD PARA EL PACIENTE Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), julio 2015 Índice
FICHA TÉCNICA. Solución estéril inyectable por vía intramuscular (preferiblemente) o subcutánea. Pneumo 23 es un líquido transparente e incoloro.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO PNEUMO 23, solución inyectable en jeringa precargada Vacuna antineumocócica de polisacáridos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml contiene:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO PNEUMO 23, solución inyectable en jeringa precargada Vacuna antineumocócica de polisacáridos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml contiene:
PROSPECTO. CEFTRIAXONA REIG JOFRÉ 1 g IM. Polvo y disolvente para solución inyectable. E.F.G. Ceftriaxona (D.C.I.)
 PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Fevaxyn Pentofel, suspensión inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Fevaxyn Pentofel, suspensión inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. Niños menores de 1 año: no se ha establecido la seguridad y eficacia de Thrombocid Forte en niños menores de 1 año.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Thrombocid Forte 5 mg/g pomada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene: Pentosano polisulfato sódico...5 mg Excipientes: Alcohol
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Thrombocid Forte 5 mg/g pomada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene: Pentosano polisulfato sódico...5 mg Excipientes: Alcohol
Para la lista completa de excipientes, véase la sección Indicaciones de uso, especificando las especies de destino
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Emeprid 1 mg/ml solución oral para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Emeprid 1 mg/ml solución oral para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO DICLOVET 50 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO DICLOVET 50 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
1. Tratamiento del estreñimiento 2. Tratamiento de la encefalopatia hepática (encefalopatía porto-sistémica); coma hepático
 1. NOMBRE DEL MEDICAMENTO Lactulosa Resolution 3,3 g/5 ml, solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 5 mililitros de solución oral contienen 3,3 g de lactulosa Para la lista completa
1. NOMBRE DEL MEDICAMENTO Lactulosa Resolution 3,3 g/5 ml, solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 5 mililitros de solución oral contienen 3,3 g de lactulosa Para la lista completa
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Amorolfina Isdin 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Amorolfina Isdin 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de Amorolfina ISDIN contiene 55,74 mg de clorhidrato de amorolfina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Amorolfina Isdin 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de Amorolfina ISDIN contiene 55,74 mg de clorhidrato de amorolfina
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. ANTISHMANIA 300 mg/ml solución inyectable para perros
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMACIÓN DEL MEDICAMENTO VETERINARIO ANTISHMANIA 300 mg/ml solución inyectable para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA (ES,
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMACIÓN DEL MEDICAMENTO VETERINARIO ANTISHMANIA 300 mg/ml solución inyectable para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA (ES,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA 3. FORMA FARMACÉUTICA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO. 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextrometorfano
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextrometorfano
Vacuna antigripal de antígeno de superficie, inactivado, con adyuvante MF59C.1.
 1. NOMBRE DEL MEDICAMENTO CHIROMAS, suspensión inyectable en jeringa precargada Vacuna antigripal de antígeno de superficie, inactivado, con adyuvante MF59C.1. (CAMPAÑA 2014/2015) 2. COMPOSICIÓN CUALITATIVA
1. NOMBRE DEL MEDICAMENTO CHIROMAS, suspensión inyectable en jeringa precargada Vacuna antigripal de antígeno de superficie, inactivado, con adyuvante MF59C.1. (CAMPAÑA 2014/2015) 2. COMPOSICIÓN CUALITATIVA
Enfermedad de Kawasaki
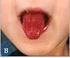 www.printo.it/pediatric-rheumatology/ar/intro Enfermedad de Kawasaki Versión de 2016 2. DIAGNÓSTICO Y TRATAMIENTO 2.1 Cómo se diagnostica? El diagnóstico de la enfermedad de Kawasaki se realiza en base
www.printo.it/pediatric-rheumatology/ar/intro Enfermedad de Kawasaki Versión de 2016 2. DIAGNÓSTICO Y TRATAMIENTO 2.1 Cómo se diagnostica? El diagnóstico de la enfermedad de Kawasaki se realiza en base
Prospecto: información para el usuario
 Prospecto: información para el usuario Grafalon 20 mg/ml concentrado para solución para perfusión Inmunoglobulina anti-linfocitos T humanos de conejo Lea todo el prospecto detenidamente Conserve este prospecto.
Prospecto: información para el usuario Grafalon 20 mg/ml concentrado para solución para perfusión Inmunoglobulina anti-linfocitos T humanos de conejo Lea todo el prospecto detenidamente Conserve este prospecto.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BERIGLOBINA P 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BERIGLOBINA P 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Composición cualitativa Inmunoglobulina humana normal 2.2 Composición cuantitativa 1 ml contiene: Proteína
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BERIGLOBINA P 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Composición cualitativa Inmunoglobulina humana normal 2.2 Composición cuantitativa 1 ml contiene: Proteína
PROSPECTO: INFORMACIÓN PARA EL PACIENTE BISOLVON MUCOLÍTICO INFANTIL 0,8 MG/ML JARABE. Bromhexina hidrocloruro
 PROSPECTO: INFORMACIÓN PARA EL PACIENTE BISOLVON MUCOLÍTICO INFANTIL 0,8 MG/ML JARABE Bromhexina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
PROSPECTO: INFORMACIÓN PARA EL PACIENTE BISOLVON MUCOLÍTICO INFANTIL 0,8 MG/ML JARABE Bromhexina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Bioselenium 25 mg/ml suspensión cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sulfuro de selenio,
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Bioselenium 25 mg/ml suspensión cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sulfuro de selenio,
Vacuna antigripal de antígeno de superficie, inactivado, con adyuvante MF59C.1.
 1. NOMBRE DEL MEDICAMENTO CHIROMAS, suspensión inyectable en jeringa precargada Vacuna antigripal de antígeno de superficie, inactivado, con adyuvante MF59C.1. (CAMPAÑA 2012/2013) 2. COMPOSICIÓN CUALITATIVA
1. NOMBRE DEL MEDICAMENTO CHIROMAS, suspensión inyectable en jeringa precargada Vacuna antigripal de antígeno de superficie, inactivado, con adyuvante MF59C.1. (CAMPAÑA 2012/2013) 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA. La duración estimada del tratamiento será de dos semanas.
 FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS)_Agosto_2016
 KEYTRUDA (pembrolizumab) Información para pacientes Keytruda es un medicamento biológico Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios
KEYTRUDA (pembrolizumab) Información para pacientes Keytruda es un medicamento biológico Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. RESINCALCIO polvo para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RESINCALCIO polvo para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 g de polvo para suspensión oral contienen 99,75 g de poliestireno sulfonato
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RESINCALCIO polvo para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 g de polvo para suspensión oral contienen 99,75 g de poliestireno sulfonato
Inmunizaciones Esc. "José Ma. Vargas"
 Inmunizaciones Esc. "José Ma. Vargas" 2016 Objetivos de la clase 1.- Generalidades: Definición, Antecedentes Históricos. 2.- Tipos de Inmunizaciones: a) Inmunización Activa: - Principios generales - Vías
Inmunizaciones Esc. "José Ma. Vargas" 2016 Objetivos de la clase 1.- Generalidades: Definición, Antecedentes Históricos. 2.- Tipos de Inmunizaciones: a) Inmunización Activa: - Principios generales - Vías
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA. Gotas Óticas. Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g.
 DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
FICHA TÉCNICA. KETOISDIN 400 mg óvulos está indicado en adultos para el tratamiento local de
 1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
Prospecto: Información para el paciente. Rhophylac 300 microgramos / 2 ml de solución inyectable en jeringa precargada Inmunoglobulina Humana Anti-D
 Prospecto: Información para el paciente Rhophylac 300 microgramos / 2 ml de solución inyectable en jeringa precargada Inmunoglobulina Humana Anti-D Lea todo el prospecto detenidamente antes de empezar
Prospecto: Información para el paciente Rhophylac 300 microgramos / 2 ml de solución inyectable en jeringa precargada Inmunoglobulina Humana Anti-D Lea todo el prospecto detenidamente antes de empezar
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO IMIZOL 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO IMIZOL 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/18
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/18 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Oncept IL-2 liofilizado y disolvente para suspensión inyectable para gatos. 2. COMPOSICIÓN
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/18 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Oncept IL-2 liofilizado y disolvente para suspensión inyectable para gatos. 2. COMPOSICIÓN
Se recomiendan las siguientes modificaciones en caso de disfunción renal.
 1. NOMBRE DEL MEDICAMENTO ACICLOVIR TEDEC 25 mg/ml solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla contiene: Aciclovir (D.O.E.) 250 mg Para excipientes, ver 6.1. 3. FORMA
1. NOMBRE DEL MEDICAMENTO ACICLOVIR TEDEC 25 mg/ml solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla contiene: Aciclovir (D.O.E.) 250 mg Para excipientes, ver 6.1. 3. FORMA
