FORMULACIÓN QUÍMICA INORGÁNICA 3º ESO
|
|
|
- Elisa Domínguez Robles
- hace 6 años
- Vistas:
Transcripción
1 FORMULACIÓN QUÍMICA INORGÁNICA A continuación tienes un esquema de los compuestos inorgánicos que aprenderemos a formular: I. SUSTANCIAS SIMPLES II. COMPUESTOS BINARIOS A. CON OXÍGENO ÓXIDOS BÁSICOS ÓXIDOS ÁCIDOS O ANHÍDRIDOS HIDRUROS METÁLICOS B. CON HIDRÓGENO HALUROS DE HIDRÓGENO HIDRUROS VOLÁTILES C. SALES BINARIAS SALES HIDRÁCIDAS SALES VOLÁTILES III. COMPUESTOS TERNARIOS A. HIDRÓXIDOS O BASES de halógenos B. OXOÁCIDOS de los grupos IIIA, IVA, VA, VIA de metales de transición (Mn y Cr) C. SALES NEUTRAS U OXISALES Este curso nosotros aprenderemos a formular compuestos binarios con oxígeno e hidrógeno y los hidróxidos o bases. La formulación es el conjunto de normas donde se utilizan los símbolos de los elementos químicos y unos números llamados subíndices, que representan la fórmula de un determinado compuesto químico. Los compuestos químicos pueden ser binarios, ternarios, etc, según estén formados por 2 elementos diferentes, 3 elementos diferentes, etc.
2 1. NORMAS GENERALES DE FORMULACIÓN DE COMPUESTOS INORGÁNICOS ORDEN EN EL QUE SE DISPONEN LOS SÍMBOLOS DE LOS ELEMENTOS EN LOS COMPUESTOS Se escribe siempre en primer lugar el símbolo del elemento o radical menos electronegativo (metal o elemento más a la izquierda en el sistema periódico (SP) o grupo que actúe como tal) y a continuación el del elemento o radical más electronegativo, no metal o elemento más a la derecha del SP. Sin embargo, al nombrarlos se hace en orden inverso (empezando a nombrar por la derecha). Como norma general se puede decir que se escribe a la izquierda en una fórmula el elemento que se encuentra más a la izquierda en el sistema periódico. Si aparecen dos elementos del mismo grupo en la fórmula, se sitúa en primer lugar el elemento que se encuentre más abajo en el grupo. La posición del hidrógeno varía en función del elemento con el que se combine: se sitúa a la derecha cuando se combina con los metales y con los no metales B, Si, C, Sb, As, P o N, y a la izquierda cuando se combina con Te, Se, S, At, I, Br, Cl, O o F. El oxígeno se sitúa siempre a la derecha en la fórmula excepto cuando se combina con el flúor (porque éste es más electronegativo que el oxígeno). En las combinaciones de dos no metales se escribe en primer lugar el símbolo del elemento que aparece antes en la siguiente lista: B, Si, C, Sb, As, P, N, H, Te, Se, S, At, I, Br, Cl, O, F SUBÍNDICES Para formular los compuestos binarios se ponen los símbolos de los elementos que los constituyan en el orden que corresponda (el más electronegativo se sitúa a la derecha) y se ponen como subíndices las valencias intercambiadas. El subíndice 1 no se escribe. Siempre que todos los subíndices de un compuesto sean divisibles por el mismo número deben simplificarse (excepto en los peróxidos). PREFIJOS Y SUFIJOS En la nomenclatura de Stock, la valencia se indica con un número romano entre paréntesis. Si un elemento actúa con su única valencia se prescinde de poner este número. En la nomenclatura sistemática suelen emplearse los siguientes prefijos numéricos para indicar el número de átomos de un elemento dado que aparece en un compuesto: Mono 1 Di 2 Tri 3 Tetra 4 Penta 5 Hexa 6 Hepta 7 Etc. Cuando en el nombre de un compuesto aparece dos veces el prefijo mono, siempre se prescinde del segundo. Ejemplo: CO se denomina monóxido de carbono y no monóxido de monocarbono (el elemento de la izquierda nunca lleva mono). Isabel Martos Martínez. Colegio Herma 2
3 En la nomenclatura tradicional se emplean prefijos y sufijos para distinguir la valencia con la que está actuando un elemento. El empleo de éstos se hace según el siguiente criterio: Una valencia: Dos valencias: Tres valencias: Cuatro valencias: -ICO -OSO (menor) -ICO (mayor) HIPO...OSO (menor) -OSO -ICO (mayor) HIPO...OSO (menor) -OSO - ICO PER...ICO (mayor) Los prefijos META- y ORTO- hacen referencia al contenido de agua en los oxoácidos. META- expresa que se ha añadido una sola molécula de agua ORTO- que se ha añadido más de una (dos en los oxoácidos de los elementos con valencias pares y tres en los de valencias impares). RAÍCES IRREGULARES El nombre de los compuestos que forman algunos elementos se obtiene a partir de la raíz latina del nombre de dicho elemento en vez de hacerse con la raíz castellana. A continuación se citan esos casos irregulares: Compuesto de Raíz Ejemplo Azufre (S) Sulfur- Ácido sulfúrico Cobre (Cu) Cupr- Sulfato cúprico Estaño (Sn) Estann- Óxido estánnico Hierro (Fe) Ferr- Hidróxido férrico Manganeso (Mn) Mangan- Hidruro manganoso Nitrógeno (N) Nitr- Ácido nítrico Plata (Ag) Argent- Cloruro argéntico Plomo (Pb) Plumb- Nitrato plumboso SÍMBOLOS Y VALENCIAS Para formular correctamente es imprescindible conocer perfectamente el nombre y el símbolo de los elementos químicos, así como la valencia o valencias con las que puede actuar. NÚMERO DE OXIDACIÓN O VALENCIA DE UN ELEMENTO Los átomos se unen entre sí mediante enlaces para formar moléculas. Dichos enlaces se originan captando, cediendo o compartiendo electrones entre los átomos que lo forman. Se llama número de oxidación de un elemento al número de electrones cedidos, captados o compartidos por un átomo en su combinación química con otro para formar un enlace: al átomo que capta electrones se le asigna un número de oxidación negativo, mientras que al átomo que cede los electrones en el enlace se le asigna un número de oxidación positivo. Isabel Martos Martínez. Colegio Herma 3
4 La valencia es la capacidad de combinación de un elemento con otros elementos de la tabla periódica. La valencia se suele expresar con un número sin signo que se corresponde con el número de oxidación del elemento. NÚMEROS DE OXIDACIÓN PRINCIPALES Los números de oxidación de la mayoría de los elementos se pueden deducir teniendo en cuenta el número del grupo en el que están de la siguiente manera: Números de oxidación positivos: Los elementos que están en un grupo impar tienen todos los números de oxidación impares desde el 1 hasta el número del grupo. Los elementos que están en un grupo par tienen todos los números de oxidación pares desde el 2 hasta el número del grupo. Este criterio sólo es válido si se emplea la numeración antigua de los periodos, en la que se empleaban los números romanos del I al VIII para nombrar a los ocho grupos representativos, es decir, pertenecientes a los bloques s y p del sistema periódico (los dos primeros y los seis últimos) y, por lo tanto, no es aplicable a los elementos de transición. Números de oxidación negativos: Corresponde al número de electrones que puede captar (-) o ceder (+) el elemento al combinarse con otro elemento. El número de oxidación principal de cada elemento se corresponde con el número de electrones que le faltan (-) o le sobran (+) para que su última capa quede completa, adquiriendo la configuración del gas noble más cercano, de su mismo periodo o del anterior (regla del octete). Por ejemplo, un elemento del grupo V tiene 5 electrones en su última capa y, por tanto, le faltan tres electrones para completar los 8, por lo que su número de oxidación principal es -3. NÚMEROS DE OXIDACIÓN Y EXCEPCIONES Grupo Nº oxidación Excepciones Grupo I (1) +1 Hidrógeno +1, -1 Grupo II (2) +2 Grupo III (13) +1, +3 Boro +3 Grupo IV (14) +2, +4-4 Grupo V (15) +1, +3, +5 Nitrógeno +1, +2, +3, +4, +5, -3 Grupo VI (16) +2, +4, +6 Oxigeno -2 Grupo VII (17) +1, +3, +5, +7 Flúor -1 Elementos de transición: Sus números de oxidación no son deducibles mediante un método tan sencillo y es preciso tener en cuenta otros conceptos más complejos para ello. Sus números de oxidación son siempre positivos. Valencias +1 y +2 Valencias +1 y +3 Valencias +2 y +3 Valencia +1 Valencia +2 Valencias +2 y +4 Valencias +2, +3 y +6 Cu, Hg Au Fe, Co, Ni Ag Zn, Cd Pt, Ge, Sn, Pb, Pd Cr Isabel Martos Martínez. Colegio Herma 4
5 Valencias +2, +3, +4, +6 y +7 Mn Las valencias o números de oxidación más frecuentes quedan resumidos en la siguiente tabla: GRUPO VALENCIA ELEMENTOS IA Alcalinos 1 H, Li, Na, K, Rb, Cs, Fr IIA Alcalinotérreos 2 Be, Mg, Ca, Sr, Ba, Ra IIA Boroideos 3 B, Al IVA Carbonoideos 4, 2 C, Sn, Pb 4 Si, Ge VA Nitrogenoideos 5,3 P, As 1,2,3,4,5 N VIA Anfígenos -2 O 2, 4, 6 S, Se, Te VIIA Halógenos -1 F 1, 3, 5, 7 Cl, Br, I IB 1, 2 Cu 1 Ag 1, 3 Au IIB 2 Zn, Cd 2, 1 Hg VIII Triadas 2,3 Fe, Co, Ni 2,4 Pd, Pt Transición 2, 3, 6 Cr 2, 3, 4, 6, 7 Mn DETERMINACIÓN DEL NÚMERO DE OXIDACIÓN DE UN ELEMENTO Como hemos visto, muchos elementos pueden actuar con varios números de oxidación diferentes. Para determinar con qué número de oxidación está actuando un elemento se deben tener en cuenta las siguientes reglas: Isabel Martos Martínez. Colegio Herma 5
6 El número de oxidación de un átomo en un elemento libre es cero. El número de oxidación de un ion monoatómico es su propia carga. En toda molécula la suma de los números de oxidación es igual a cero. El oxígeno actúa siempre con número de oxidación 2. Existen dos excepciones a esta regla: los peróxidos, en los que el oxígeno actúa con valencia 1; y cuando se combina con el flúor, con el que tiene +2. El hidrógeno combinado con un no metal tiene valencia +1 y con un metal 1. Cuando se unen un metal y un no metal, el metal actúa con número de oxidación positivo y el no metal con número de oxidación negativo. El número de oxidación positivo de un elemento es, como máximo, igual al número de electrones corticales del último nivel y el negativo es, como máximo, igual al número de electrones que le faltan para completar dicho nivel y adquirir en ambos caso la estructura de gas noble. 2. FORMULACIÓN DE COMPUESTOS INORGÁNICOS I. SUSTANCIAS SIMPLES Las sustancias simples son moléculas formadas por átomos de un mismo elemento. Algunos elementos, cuando se encuentran en estado gaseoso, se presentan como moléculas diatómicas. Los más frecuentes son: H 2 O 2 N 2 F 2 Cl 2 Br 2 I 2 dihidrógeno, hidrógeno gas o hidrógeno molecular dioxígeno, oxígeno gas u oxígeno molecular dinitrógeno, nitrógeno gas o nitrógeno molecular diflúor, flúor gas o flúor molecular dicloro, cloro gas o cloro molecular dibromo, bromo gas o bromo molecular diyodo, yodo gas o yodo molecular. El oxígeno se puede presentar también en forma de molécula triatómica O 3 (trioxígeno u ozono). Los gases nobles son siempre monoatómicos, y se nombran como tales, ya que en la naturaleza se encuentran en forma atómica: He helio Ar argón Xe xenón Otros elementos pueden formar agrupaciones constituidas por más de dos átomos. Las más conocidas son: las de azufre, que se representan por Sx (poliazufre) el P 4 fósforo blanco o tetrafósforo. Isabel Martos Martínez. Colegio Herma 6
7 Por último, muchos elementos forman mallas de gran número de átomos. Es el caso de los metales y otras sustancias simples como el grafito y el diamante (dos formas del carbono). En este caso, se representan simplemente por el símbolo del elemento. Fe hierro Mg magnesio Ni níquel Co cobalto II. COMPUESTOS BINARIOS Las combinaciones químicas más sencillas son las realizadas entre 2 elementos diferentes, por ello se llaman combinaciones binarias, y los compuestos que resultan, COMPUESTOS BINARIOS. II.1 COMPUESTOS BINARIOS CON OXÍGENO: ÓXIDOS Si uno de los elementos que se combina es el OXÍGENO tendremos los ÓXIDOS. Son compuestos formados por la combinación del oxígeno con cualquiera de los demás elementos de la tabla periódica. Si el elemento que se combina con el oxígeno es un METAL, se formarán loa ÓXIDOS BÁSICOS. Si el elemento que se combina es un NO METAL se formarán los ÓXIDOS ÁCIDOS, llamados también ANHÍDRIDOS, y que suelen ser gaseosos o muy volátiles. Formulación: M 2 Om Donde 2: es la valencia del oxígeno que la toma el metal o no metal m: es la valencia del elemento metálico o no metálico que la toma el oxígeno Pasos a seguir: 1. se escribe el símbolo del metal con su valencia positiva 2. se escribe el oxígeno con su valencia negativa, que es 2 3. se intercambian las valencias 4. si se puede se simplifica Ca 2+ + O 2- Ca 2 O 2 CaO Na 1+ + O 2- Na 2 O NOMENCLATURA DE STOCK - La valencia se indica con un número romano entre paréntesis. Se nombra de la siguiente forma: Óxido + de + nombre elemento + (Valencia en números romanos) Ej: CuO óxido de Cobre (II) Cu 2 O óxido de Cobre (I) - Si un elemento actúa con su única valencia se prescinde de poner este número. CaO óxido de Calcio Isabel Martos Martínez. Colegio Herma 7
8 Al 2 O 3 óxido de Aluminio - Sólo se indicará el número de valencia cuando el elemento posea varias de ellas. Ca O Fe O Fe2O3 Cl2O Cl2O3 Cl2O5 Cl2O7 Óxido de calcio Óxido de hierro (II) Óxido de hierro (III) Óxido de cloro (I) Óxido de cloro (III) Óxido de cloro (V) Óxido de cloro (VII) NOMENCLATURA SISTEMÁTICA - Como se indicó anteriormente, suelen emplearse los siguientes prefijos numéricos para indicar el número de átomos de un elemento dado que aparece en un compuesto: Mono 1 Di 2 Tri 3 Tetra 4 Penta 5 Hexa 6 Hepta 7, etc. De este modo se nombra a los compuestos como: prefijo + óxido de + prefijo + nombre de elemento Ej: Al 2 O 3 Trióxido de dialuminio - Cuando en el nombre de un compuesto aparece en el segundo elemento el prefijo mono, siempre se prescinde de él. Ej: CO 2 Dióxido de carbono Ej: CO se denomina monóxido de carbono y no monóxido de monocarbono. Ca O Monóxido de calcio ( Fe O Monóxido de hierro Fe2O3 Trióxido de dihierro Cl2O Monóxido de dicloro Cl2O3 Trióxido de dicloro Cl2O5 Pentaóxido de dicloro Cl2O7 Heptaóxido de dicloro NOMENCLATURA TRADICIONAL Como se indicó anteriormente, en la nomenclatura tradicional se emplean prefijos y sufijos para distinguir la valencia con la que está actuando un elemento. El empleo de éstos se hace según el siguiente criterio: Isabel Martos Martínez. Colegio Herma 8
9 Una valencia: Dos valencias: Tres valencias: Cuatro valencias: -ICO -OSO (menor) -ICO (mayor) HIPO...OSO (menor) -OSO -ICO (mayor) HIPO...OSO (menor) -OSO - ICO PER...ICO (mayor) Los óxidos ácidos vendrán precedidos por la palabra anhídrido en esta nomenclatura. Ej: Ca O Óxido cálcico Fe O Óxido ferroso Fe2O3 Óxido férrico Cl2O Anhídrido hipocloroso Cl2O3 Anhídrido cloroso Cl2O5 Anhídrido clórico Cl2O7 Anhídrido perclórico Ejemplos con las tres nomenclaturas (stock/sistemática/tradicional) SO Cl 2 O P 2 O 5 Br 2 O 7 CO 2 II.1 óxido de azufre (II)/monóxido de azufre/anhídrido hiposulfuroso óxido de cloro (I)/monóxido de dicloro/anhídrdo hipocloroso óxido de fósforo (V)/pentaóxido de difósforo/anh. fosfórico óxido de bromo (VII)/ heptaóxido de dibromo/anh. perbrómico óxido de carbono (IV)/dióxido de carbono/anh. carbónico COMPUESTOS BINARIOS CON HIDRÓGENO HIDRUROS METÁLICOS Son compuestos binarios donde el hidrogeno actúa como no metal y se combina con elementos metálicos. Formulación: MHm Donde: M: es el símbolo del elemento metálico que toma la valencia del hidríogeno -1, que no se indica como subíndice. H: símbolo del hidrógeno que toma la valencia del metal (m) NOMENCLATURA DE STOCK - La valencia se indica con números romanos entre paréntesis. Se nombra de la siguiente forma: Hidruro de + nombre del elemento (Valencia en sistema romano) Isabel Martos Martínez. Colegio Herma 9
10 Ej: CuH 2 Hidruro de Cobre (II) CuH Hidruro de Cobre (I) - Si un elemento actúa con su única valencia se prescinde de poner este número. CaH 2 Hidruro de Calcio AlH 3 Hidruro de Aluminio - Sólo se indicará el número de valencia cuando el elemento posea varias de ellas. Sr H2 Ni H2 Ni H3 Hidruro de estroncio Hidruro de níquel (II) Hidruro de níquel (III) NOMENCLATURA SISTEMÁTICA prefijo + hidruro de + nombre del elemento Ej: AlH 3 Trihidruro de aluminio Sr H2 Dihidruro de estroncio Ni H2 Dihidruro de níquel Ni H3 Trihidruro de níquel NOMENCLATURA TRADICIONAL Hidruro + nombre del metal terminado en. -ico para la valencia mayor -oso para la valencia menor Ej: CuH 2 Hidruro cúprico CuH Hidruro cuproso Sr H2 Hidruro estróncico Ni H2 Hidruro niqueloso Ni H3 Hidruro niquélico -ico si es monovalente - Si un elemento actúa con su única valencia termina en -ico. CaH 2 Hidruro cálcico AlH 3 Hidruro alumínico HALUROS DE HIDRÓGENO O ÁCIDOS HIDRÁCIDOS Combinaciones binarias del hidrógeno con los elementos F, Cl, Br, I, S, Se y Te que son no metales. En disolución acuosa estos compuestos se comportan como ácidos, y se nombrarán como Ácidos Hidrácidos. En estos compuestos el H actúa con valencia positiva +1 y se sitúa a la izquierda. El no metal actuará con su valencia negativa, que será, -1 para F, Cl, Br y I, y -2 para S, Se y Te. Isabel Martos Martínez. Colegio Herma 10
11 Formulación: HmX Donde: m: es la valencia del no metal que la toma el hidrógeno X: es el símbolo del no metal que toma la valencia +1 del hidrógeno y, por tanto, no se indica como subíndice NOMENCLATURA SISTEMÁTICA haluro de + prefijo + hidrógeno Haluro: fluoruro, cloruro, seleniuro, sulfuro, etc, de hidrógeno Ej: H 2 Te Telururo de dihidrógeno o telururo de hidrógeno simplemente. H Cl Cloruro de hidrógeno H Br Bromuro de hidrógeno H2S Sulfuro de hidrógeno NOMENCLATURA TRADICIONAL Estos compuestos son conocidos por sus nombres tradicionales cuando están en disolución: ácido fluorhídrico, clorhídrico, sulfhídrico, bromhídrico, yodhídrico, selenhídrico o telurhídrico. H Cl H Br H2S Ácido clorhídrico Ácido bromhídrico Ácido sulfhídrico HIDRUROS VOLÁTILES Combinaciones binarias del hidrógeno con los elementos N, P, As, Sb, C, Si, B donde el hidrógeno actúa como no metal (se sitúa a la derecha) y por tanto con valencia negativa -1. Son todos gaseosos. En estos compuestos los no metales se sitúan a la izquierda del compuesto y actúan con las siguientes valencias: B, N, P, AS, Sb: valencia +3 C, Si: Valencia +4 Formulación: XHm Donde: X: es el no metal que toma la valencia del hidrógeno y no se indica como subíndice m: subíndice que toma el hidrógeno de la valencia del no metal NOMENCLATURA SISTEMÁTICA prefijo + hidruro de + nombre del elemento Ej: PH 3 trihidruro de fósforo. NOMENCLATURA STOCK Isabel Martos Martínez. Colegio Herma 11
12 prefijo + hidruro + de + nombre del elemento No es necesario colocar la valencia entre paréntesis ya que el otro elemento solo actúa con una valencia. Ej: PH 3 Trihidruro de fósforo N H3 Trihidruro de nitrógeno P H3 Trihidruro de fósforo C H4 Tetrahidruro de carbono B H3 Trihidruro de boro NOTA: Estos compuestos son conocidos por sus nombres tradicionales: BH 3 CH 4 SiH 4 NH 3 PH 3 AsH 3 SbH 3 Borano Metano Silano Amoniaco Fosfina Arsina Estibina II.3 SALES BINARIAS SALES NEUTRAS Combinaciones binarias de un metal con un no metal distinto del oxígeno y el hidrógeno. Formulación: MxXm Donde: NOMENCLATURA DE STOCK M: es el símbolo del metal que toma la valencia del no metal como subíndice X: es el símbolo del no metal que toma la valencia del metal como subíndice No metal terminado en uro + nombre del metal + (valencia en números romanos) Ej: CuS Sulfuro de Cobre (II) Cu 2 S Sulfuro de Cobre (I) Ca F2 Au2S Au2S3 Fluoruro de calcio Sulfuro de oro (I) Sulfuro de oro (III) Si un elemento actúa con su única valencia se prescinde de poner este número. CaS AlCl 3 Sulfuro de Calcio Cloruro de Aluminio - Sólo se indicará el número de valencia cuando el elemento posea varias de ellas. Isabel Martos Martínez. Colegio Herma 12
13 NOMENCLATURA SISTEMÁTICA mono-, di-, tri- + no metal terminado en -uro + de + nombre del metal Haluro: fluoruro, bromuro, seleniuro, sulfuro. Ej: PCl 3 Tricloruro de fósforo. Au2S Monosulfuro de dioro Au2S3 Trisulfuro de dioro - Cuando en el nombre de un compuesto aparece en el segundo elemento el prefijo mono, siempre se prescinde de él. Ej: CCl 4 Tetracloruro de carbono, no se dice de monocarbono Ca F2 Difluoruro de calcio NOMENCLATURA TRADICIONAL Nombre del no metal terminado en uro + metal terminado en ico/-oso Si el metal actúa con valencia única: terminación en ico Si el metal actúa con más de una valencia: terminación en -ico para la mayor terminación en oso para la menor Ca F2 Au2S Au2S3 Fluoruro cálcico Sulfuro auroso Sulfuro aúrico SALES VOLÁTILES Combinaciones binarias de dos no metales. Son también fluoruros, cloruros, bromuros, yoduros, sulfuros, seleniuros, telururos, nitruros, fosfuros, arseniuros, carburos y siliciuros. En estos compuestos, el no metal que está más a la izquierda o más bajo en la tabla si es que son del mismo grupo, actúa con cualquiera de sus valencias positivas, y el no metal de la derecha con su correspondiente valencia negativa. Formulación: YmXn Donde: Y: símbolo del no metal más a la izquierda del SP m: subíndice que toma el elemento del no metal de la derecha X: símbolo del no metal más a la derecha del SP n: subíndice que toma el elemento del no metal de la izquierda La nomenclatura será la misma que para las sales neutras. Ejemplos: BF 3 Trifluoruro de boro o flururo de boro Isabel Martos Martínez. Colegio Herma 13
14 CI 4 Tetrayoduro de Carbono o yoduro de carbono (IV) III. COMPUESTOS TERNARIOS III.1 HIDRÓXIDOS O BASES Combinaciones ternarias de un metal con el grupo hidróxido (OH) -1. Aunque sean compuestos ternarios, su formulación y nomenclatura son idénticas a las de los compuestos binarios, ya que el grupo (OH) actúa como un único elemento con valencia -1. NOMENCLATURA STOCK Hidróxido de + nombre del metal + (valencia del en números romanos) Be(OH) 2 Sn(OH) 2 Sn(OH) 4 Hidróxido de berilio Hidróxido de estaño (II) Hidróxido de estaño (IV) NOMENCLATURA SISTEMÁTICA Se anteponen prefijos numéricos, mono-, di-, tri-, etc, a la palabra hidróxido en función del subíndice que lleve y se le añade el nombre del metal. prefijo + hidróxido + de + nombre del metal Be(OH)2 Sn(OH)2 Sn(OH)4 Dihidróxido de berilio Dihidróxido de estaño Tetrahidróxido de estaño NOMENCLATURA TRADICIONAL Hidróxido + nombre del metal con la terminación: Si es monovalente: -ico Si es divalente: -ico para la mayor -oso para la menor Be(OH) 2 Hidróxido berílico Sn(OH) 2 Hidróxido estannoso Sn(OH) 4 Hidróxido estánnico Isabel Martos Martínez. Colegio Herma 14
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos. 13 millones!!!
 La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
Química General Básica. Nomenclatura de Compuestos Inorgánicos
 Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN Y NOMENCLATURA
 1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
Para nombrar compuestos químicos según esta nomenclatura se utilizan los prefijos: MONO_, DI_, TRI_, TETRA_, PENTA_, HEXA_, HEPTA_...
 3. NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos
3. NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos
1.- CONCEPTOS PREVIOS
 TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
Lo primero que hay que conocer para formular y nombrar los compuestos químicos es el número de oxidación de cada elemento.
 Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
PROGRAMA TOTAL FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA)
 FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
QUÍMICA INORGÁNICA. Elementos Símbolo Valencia Elemento Símbolo Valencia. Hidrógeno H Oxigeno O -2. Flúor F -1 Nitrógeno N
 QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
Trióxido de dihierro
 Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
M m+ + X n- M n X m. Qué es formular un compuesto binario?
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Trióxido de dihierro
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS.
 QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
Trióxido de dihierro
 COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
Nomenclatura Inorgánica
 Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Formulación Inorgánica
 Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Metal y no. metal. sodio. cloruro de COMPUESTOS IES RIBERA DE CASTILLA. Óxidos. Peróxidos. que los binarios) Pág 1
 FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS BINARIOS Igual que todas las personas tenemos un nombre, también cada compuesto químico tiene el suyo. Es importante conocer la fórmula y el nombre de los compuestos
FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS BINARIOS Igual que todas las personas tenemos un nombre, también cada compuesto químico tiene el suyo. Es importante conocer la fórmula y el nombre de los compuestos
SUMARIO FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS INTRODUCCIÓN SUSTANCIAS SIMPLES
 Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
Número de oxidación. Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo
 FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
Formulación: Introducción y compuesto binarios. Teoría. Compuestos binarios y ternarios
 Compuestos binarios y ternarios 1. Compuestos binarios son aquellos que están formados por dos elementos diferentes. Ejemplos: - NaH está formado por dos elementos el Na y el H - Cl 2 O está formado por
Compuestos binarios y ternarios 1. Compuestos binarios son aquellos que están formados por dos elementos diferentes. Ejemplos: - NaH está formado por dos elementos el Na y el H - Cl 2 O está formado por
TEMA 5.- Formulación y nomenclatura
 Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
Tema 1 : Nomenclatura y formulación Química Inorgánica
 Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Formación de compuestos inorgánicos binarios y ternarios
 Formación de compuestos inorgánicos binarios y ternarios Números de oxidación (valencia) Cuando los átomos se unen intercambian o comparten electrones; en general lo hacen de forma tal que completan su
Formación de compuestos inorgánicos binarios y ternarios Números de oxidación (valencia) Cuando los átomos se unen intercambian o comparten electrones; en general lo hacen de forma tal que completan su
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
NOMENCLATURA DE ÁCIDOS Y BASES
 COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS CON OXÍGENO El oxígeno se combina con todos los elementos excepto con los gases nobles. En estos compuestos el oxígeno actúa
RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS CON OXÍGENO El oxígeno se combina con todos los elementos excepto con los gases nobles. En estos compuestos el oxígeno actúa
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Símbolos y números de oxidación Reglas para conocer el número de oxidación de un elemento. a. El número de oxidación del hidrógeno en sus compuestos es +1, excepto en los hidruros
NOMENCLATURA INORGÁNICA Símbolos y números de oxidación Reglas para conocer el número de oxidación de un elemento. a. El número de oxidación del hidrógeno en sus compuestos es +1, excepto en los hidruros
Nomenclatura de Compuestos Inorgánicos
 Repartido Nomenclatura Compuestos Inorgánicos Química 1 B.D. Prof. Javier Ponce Ecuaciones Químicas: Una ecuación química es la representación de una reacción química. En toda ecuación química se verifica
Repartido Nomenclatura Compuestos Inorgánicos Química 1 B.D. Prof. Javier Ponce Ecuaciones Químicas: Una ecuación química es la representación de una reacción química. En toda ecuación química se verifica
INSTITUTO EDUCACIÓN SECUNDARIA POLITÉCNICO. CARTAGENA. 3º E.S.O.
 Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
FORMULACIÓN INORGÁNICA. Departamento de Física y Química 3º ESO
 FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA FORMULACIÓN Una fórmula química es la representación escrita de una molécula o compuesto iónico. Para expresar una fórmula química se utilizan los símbolos de los elementos que
FORMULACIÓN Y NOMENCLATURA FORMULACIÓN Una fórmula química es la representación escrita de una molécula o compuesto iónico. Para expresar una fórmula química se utilizan los símbolos de los elementos que
M m+ + X n-! M n X m EJERCICIOS/ESTUDIO. Qué es formular un compuesto binario?
 EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS
 EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (3.º ESO)
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA
 5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. CLASIFICACIÓN DE LOS ELEMENTOS QUÍMICOS. 1.1. METALES Y NO METALES En términos generales, se clasifican como: METALES: Poseen brillo metálico.
5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. CLASIFICACIÓN DE LOS ELEMENTOS QUÍMICOS. 1.1. METALES Y NO METALES En términos generales, se clasifican como: METALES: Poseen brillo metálico.
Ejemplo 2.- Cuando tiene 4 valencias como el Cl, I, Br, Fluor se usa HIPO-OSO e HIPER-ICO
 FUNCIONES QUÍMICAS INORGANICAS 1. FUNCION QUIMICA.- Es el conjunto de compuestos que tienen ciertas propiedades en común, como por ejemplo un átomo común para todos. Las funciones químicas pueden ser inorgánicas
FUNCIONES QUÍMICAS INORGANICAS 1. FUNCION QUIMICA.- Es el conjunto de compuestos que tienen ciertas propiedades en común, como por ejemplo un átomo común para todos. Las funciones químicas pueden ser inorgánicas
Óxido de hierro (III)
 COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
DEPARTAMENTO DE FÍSICA Y QUÍMICA
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied Chemistry).
 4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
Formulación Inorgánica
 Formulación Inorgánica Sustancias elementales: Son las que están constituidas por átomos de un elemento, constituyen la molécula del elemento. A. Sustancias monoatómicas: Se representan y nombran igual
Formulación Inorgánica Sustancias elementales: Son las que están constituidas por átomos de un elemento, constituyen la molécula del elemento. A. Sustancias monoatómicas: Se representan y nombran igual
11 Dióxido de carbono. 12 Trióxido de monoazufre. 13 Pentaóxido de difósforo. 14 Dióxido de monoselenio. 15 Dióxido de selenio. 16 Óxido de dimercurio
 1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
Óxido de hierro(iii)
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
Apuntes de refuerzo 1 de 5
 Apuntes de refuerzo 1 de 5 1º. Para averiguar el nombre de gran número de compuestos necesitamos conocer el número de oxidacin de los elementos del compuesto. Procedemos según las reglas estudiadas. Se
Apuntes de refuerzo 1 de 5 1º. Para averiguar el nombre de gran número de compuestos necesitamos conocer el número de oxidacin de los elementos del compuesto. Procedemos según las reglas estudiadas. Se
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO
 PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO Para superar la materia, el alumno deberá realizar las actividades que se indican a continuación. Se realizarán en un cuaderno destinado únicamente
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO Para superar la materia, el alumno deberá realizar las actividades que se indican a continuación. Se realizarán en un cuaderno destinado únicamente
ÓXIDOS EJEMPLOS EJERCICICIOS. Br 2 O As 2 O 3 B 2 O 3 SnO 2 Cl 2 O 3 As 2 O 5 P 2 O 3. SeO 2 TeO 3 P 2 O 5. Óxido selenioso
 ÓXIDOS EJEMPLOS Fórmula N. Sistemática N. Stock N. tradicional CO Monóxido de carbono Óxido de carbono (I) Óxido carbonoso CO 2 Dióxido de carbono Óxido de carbono (II) Óxido carbónico SO Monóxido de azufre
ÓXIDOS EJEMPLOS Fórmula N. Sistemática N. Stock N. tradicional CO Monóxido de carbono Óxido de carbono (I) Óxido carbonoso CO 2 Dióxido de carbono Óxido de carbono (II) Óxido carbónico SO Monóxido de azufre
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO
 EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN
 QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN Rafael Jiménez Prieto FORMULACIÓN INORGÁNICA FORMULACIÓN INORGÁNICA VALENCIAS MÁS COMUNES DE LOS ELEMENTOS QUÍMICOS TIPOS DE COMPUESTOS Consideraciones generales
QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN Rafael Jiménez Prieto FORMULACIÓN INORGÁNICA FORMULACIÓN INORGÁNICA VALENCIAS MÁS COMUNES DE LOS ELEMENTOS QUÍMICOS TIPOS DE COMPUESTOS Consideraciones generales
Combinaciones Binarias
 Combinaciones Binarias Se llama combinaciones binarias a los compuestos formados por átomos de dos elementos diferentes. Antes de estudiar los diferentes tipos de combinaciones binarias veremos unas normas
Combinaciones Binarias Se llama combinaciones binarias a los compuestos formados por átomos de dos elementos diferentes. Antes de estudiar los diferentes tipos de combinaciones binarias veremos unas normas
Ejercicios de la unidad didáctica 4.- Formulación y nomenclatura.
 Nombre y apellidos: Ejercicios de la unidad didáctica 4.- Formulación y nomenclatura. 1 Los elementos que debes conocer este curso están recogidos en las siguientes tablas. Complétalas escribiendo los
Nombre y apellidos: Ejercicios de la unidad didáctica 4.- Formulación y nomenclatura. 1 Los elementos que debes conocer este curso están recogidos en las siguientes tablas. Complétalas escribiendo los
TEMA 4: Formulación inorgánica
 TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES. Número de oxidación. + 1 Li, Na, K, Rb, Cs y Ag
 1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
Calcio(2+) Hierro(3+)
 CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y INORGÁNICA (IUPAC 2005) 0 COLEGIO COLÓN MARISTAS HUELVA CURSO ACADÉMICO 2015-2016 ÍNDICE 1. COMPUESTOS BINARIOS.. 2 1.1 ÓXIDOS 2 1.2 HALUROS DE OXÍGENO... 3 1.3 PERÓXIDOS...4 1.4 HIDRUROS..
FORMULACIÓN Y INORGÁNICA (IUPAC 2005) 0 COLEGIO COLÓN MARISTAS HUELVA CURSO ACADÉMICO 2015-2016 ÍNDICE 1. COMPUESTOS BINARIOS.. 2 1.1 ÓXIDOS 2 1.2 HALUROS DE OXÍGENO... 3 1.3 PERÓXIDOS...4 1.4 HIDRUROS..
metal + H 2 hidruro metálico
 Hidruros metálicos Compuestos binarios formados por la combinación del hidrógeno con metales, especialmente con los del grupo IA y IIA (con excepción del berilio, del manganeso). En los Hidruros el metal
Hidruros metálicos Compuestos binarios formados por la combinación del hidrógeno con metales, especialmente con los del grupo IA y IIA (con excepción del berilio, del manganeso). En los Hidruros el metal
REPASO: FORMULACIÓN INORGÁNICA
 COMPUESTOS BINARIOS REPASO: FORMULACIÓN INORGÁNICA OXÍGENO + METAL ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos excepto
COMPUESTOS BINARIOS REPASO: FORMULACIÓN INORGÁNICA OXÍGENO + METAL ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos excepto
FORMULACIÓN INORGÁNICA
 1 FORMULACIÓN INORGÁNICA Hay tres métodos para poder nombrar cualquier compuesto, el tradicional, el de Stock y la sistemática. Para saber manejar los tres métodos lo mejor es empezar por el más complicado
1 FORMULACIÓN INORGÁNICA Hay tres métodos para poder nombrar cualquier compuesto, el tradicional, el de Stock y la sistemática. Para saber manejar los tres métodos lo mejor es empezar por el más complicado
TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS ÍNDICE 1. Tipos de nomenclatura 2. Compuestos binarios 2.1. Combinaciones con hidrógeno 2.2. Combinaciones con oxígeno 2.3. Sales
TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS ÍNDICE 1. Tipos de nomenclatura 2. Compuestos binarios 2.1. Combinaciones con hidrógeno 2.2. Combinaciones con oxígeno 2.3. Sales
OXIDOS METÁLICOS O BÁSICOS. Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos
 OXIDOS METÁLICOS O BÁSICOS Nomenclatura Stock Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos Hg +1 O -2 = Hg2O = óxido de mercurio (I) Hg +2 O
OXIDOS METÁLICOS O BÁSICOS Nomenclatura Stock Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos Hg +1 O -2 = Hg2O = óxido de mercurio (I) Hg +2 O
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA I. SUSTANCIAS SIMPLES II. COMPUESTOS BINARIOS A. CON OXÍGENO ÓXIDOS BÁSICOS ÓXIDOS ÁCIDOS O ANHÍDRIDOS HIDRUROS METÁLICOS B. CON HIDRÓGENO HALUROS DE HIDRÓGENO HIDRUROS VOLÁTILES
FORMULACIÓN QUÍMICA INORGÁNICA I. SUSTANCIAS SIMPLES II. COMPUESTOS BINARIOS A. CON OXÍGENO ÓXIDOS BÁSICOS ÓXIDOS ÁCIDOS O ANHÍDRIDOS HIDRUROS METÁLICOS B. CON HIDRÓGENO HALUROS DE HIDRÓGENO HIDRUROS VOLÁTILES
CUADERNO DE FORMULACIÓN 4º ESO. Dep. de Física y Química - Curso 2011/12
 CUADERNO DE FORMULACIÓN 4º ESO 5. FORMULACIÓN INORGÁNICA. 5.1.- CONCEPTOS BÁSICOS. Para evitar la confusión que supondría designar a los distintos elementos con un nombre diferente según el idioma empleado,
CUADERNO DE FORMULACIÓN 4º ESO 5. FORMULACIÓN INORGÁNICA. 5.1.- CONCEPTOS BÁSICOS. Para evitar la confusión que supondría designar a los distintos elementos con un nombre diferente según el idioma empleado,
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
CONFERENCIA No. 1 Página 1 de 4. DE: Septiembre 7 del 2015 A : Septiembre 25 del 2015
 CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO METALES
 CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
Un elemento es una sustancia que no puede descomponerse en sustancias más simples, y está compuesta por una sola clase de átomos.
 Elementos químicos en Costa Rica Elementos Químicos en Costa Rica Un elemento es una sustancia que no puede descomponerse en sustancias más simples, y está compuesta por una sola clase de átomos. La mayoría
Elementos químicos en Costa Rica Elementos Químicos en Costa Rica Un elemento es una sustancia que no puede descomponerse en sustancias más simples, y está compuesta por una sola clase de átomos. La mayoría
Compuesto N. Stock N. tradicional N. sistemática. óxido de hierro (III) óxido férrico trióxido de dihierro
 Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Ti: +,+,+ en los hidruros no metálicos. +,+ en los óxidos, hidróxidos, hidruros metálicos. Cr: +,+ en las sales binarias. Mn:
 Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
Universidad Técnica Nacional
 Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
H, Li, Na, K, Rb, Cs, Fr 1. Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2. B, Al 3. N, P, As, Sb 1, 3, 5. F, Cl, Br, I 1, 3, 5, 7. C, Si, Ge, Sn, Pb 2, 4 O 2
 H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
Como en los óxidos, pero cambiando la palabra óxido por peróxido. Ej: Cs 2 O 2 : peróxido de cesio
 Sustancias simples Formadas por átomos de un mismo elemento. Se nombran usando un prefijo indicando el número de átomos seguido del nombre del elemento. Sustancia Nombre sistemático Nombre común H Monohidrógeno
Sustancias simples Formadas por átomos de un mismo elemento. Se nombran usando un prefijo indicando el número de átomos seguido del nombre del elemento. Sustancia Nombre sistemático Nombre común H Monohidrógeno
COMPUESTOS BINARIOS: están formados por átomos de dos elementos diferentes. Se escribe primero el menos electronegativo. (NaCl cloruro de sodio).
 NOMENCLATURA La Química se apoya en la organización La Unión Internacional de Química Pura y Aplicada (IUPAC) para establecer las reglas para nombrar los compuestos. Esta parte de la química se llama nomenclatura.
NOMENCLATURA La Química se apoya en la organización La Unión Internacional de Química Pura y Aplicada (IUPAC) para establecer las reglas para nombrar los compuestos. Esta parte de la química se llama nomenclatura.
UD 2 ENLACE QUÍMICO Y FUERZAS INTERMOLECULARES FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
FORMULACIÓN DE QUÍMICA INORGÁNICA 3ºESO
 Euclides Enseñanza Sociedad Cooperativa Andaluza Colegio Privado Concertado Arboleda C/ Reina Victoria 2. 41020 Sevilla Telf. 954 408126 Fax 954 440186 www.colegioarboleda.es arboleda@aces-andalucia.org
Euclides Enseñanza Sociedad Cooperativa Andaluza Colegio Privado Concertado Arboleda C/ Reina Victoria 2. 41020 Sevilla Telf. 954 408126 Fax 954 440186 www.colegioarboleda.es arboleda@aces-andalucia.org
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA 1. SUSTANCIAS SIMPLES El número de oxidación de un elemento en una sustancia simple es cero. Se nombran utilizando prefijos numerales que indican el número de átomos del elemento,
FORMULACIÓN INORGÁNICA 1. SUSTANCIAS SIMPLES El número de oxidación de un elemento en una sustancia simple es cero. Se nombran utilizando prefijos numerales que indican el número de átomos del elemento,
Compuestos binarios (combinaciones de dos elementos) HIDRUROS METÁLICOS= Metal - Hidrógeno. X H m. H : - 1 Metales: el suyo. FeH 3
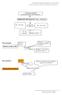 HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales
 Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales 2 de 12 Tipo de compuesto Relaciona estos compuestos:
Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales 2 de 12 Tipo de compuesto Relaciona estos compuestos:
FORMULA LOS SIGUIENTES COMPUESTOS. 1) Óxido crómico: CrO 3. 2) Trióxido de difósforo: P 2 O 3. 3) Óxido de cromo (III): Cr 2 O 3
 FORMULA LOS SIGUIENTES COMPUESTOS 1) Óxido crómico: CrO 3 2) Trióxido de difósforo: P 2 O 3 3) Óxido de cromo (III): Cr 2 O 3 4) Óxido de hierro (II): FeO 5) Pentaóxido de dinitrógeno: N 2 O 5 6) Óxido
FORMULA LOS SIGUIENTES COMPUESTOS 1) Óxido crómico: CrO 3 2) Trióxido de difósforo: P 2 O 3 3) Óxido de cromo (III): Cr 2 O 3 4) Óxido de hierro (II): FeO 5) Pentaóxido de dinitrógeno: N 2 O 5 6) Óxido
Reglas generales. n Se nombra electronegativo de electropositivo. n Fórmula electropositivo electronegativo
 nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
REACCIONES QUÍMICAS. Ocurren en la naturaleza. Se expresan por ECUACIONES QUÍMICAS
 REACCIONES QUÍMICAS Ocurren en la naturaleza Se expresan por ECUACIONES QUÍMICAS NaCl + AgNO 3 AgCl + NaNO 3 REACTIVOS PRODUCTOS ECUACIÓN QUÍMICA Estequiométrica (ecuación balanceada) Representar una reacción
REACCIONES QUÍMICAS Ocurren en la naturaleza Se expresan por ECUACIONES QUÍMICAS NaCl + AgNO 3 AgCl + NaNO 3 REACTIVOS PRODUCTOS ECUACIÓN QUÍMICA Estequiométrica (ecuación balanceada) Representar una reacción
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. A medida que fueron conociéndose los diferentes elementos químicos de la tabla periódica se vio que el número era relativamente pequeño si se compara con la gran variedad
FORMULACIÓN DE QUÍMICA INORGÁNICA. A medida que fueron conociéndose los diferentes elementos químicos de la tabla periódica se vio que el número era relativamente pequeño si se compara con la gran variedad
Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas
 D EPA R T A M ENTO D E FÍSICA Y Q UÍM ICA Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas José Manuel Ramírez Fernández Valencias y estados, grados o números de oxidación Con
D EPA R T A M ENTO D E FÍSICA Y Q UÍM ICA Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas José Manuel Ramírez Fernández Valencias y estados, grados o números de oxidación Con
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
Compuestos inorgánicos: su nomenclatura
 Compuestos inorgánicos: su nomenclatura Por: Cristina Andrade Guevara La carnalita (cloruro doble de potasio y magnesio) y la silvina (cloruro de potasio), así como el azogue (mercurio) y el cinabrio (sulfuro
Compuestos inorgánicos: su nomenclatura Por: Cristina Andrade Guevara La carnalita (cloruro doble de potasio y magnesio) y la silvina (cloruro de potasio), así como el azogue (mercurio) y el cinabrio (sulfuro
