Formulación y nomenclatura en química inorgánica para P.M.A.R. 1
|
|
|
- Marcos Cortés Sáez
- hace 6 años
- Vistas:
Transcripción
1 Formulación y nomenclatura en química inorgánica para P.M.A.R. 1 INTRODUCCIÓN LAS VALENCIAS Cuando los átomos se combinan entre sí para formar compuestos, lo hacen en ciertas proporciones que son fijas para cada tipo de compuesto. Estas proporciones están relacionadas con la distribución que tienen los electrones de la última capa de los átomos. A esta capa se le llama capa de valencia, y a los electrones que se encuentran en ella 'electrones de valencia'. De esta manera, podemos decir que la valencia de un elemento es un número que indica en qué proporción se combina con otros átomos. Esta valencia puede ser positiva -cuando un átomo se une a otro que atrae a los electrones más que él- o negativa -si el átomo con el que se combina a los electrones menos que él-. Además, un mismo elemento puede combinarse de distintas maneras con otros, dando lugar a que un elemento pueda tener más de una valencia. Incluso un átomo puede actuar con valencia positiva o negativa dependiendo de cuál sea el otro átomo con el que se combina. Es necesario memorizar la tabla de valencias que aparece al final de los apuntes. Vamos a considerar que cualquier elemento que tenga una valencia negativa es un elemento no metálico, y un elemento que no tiene valencias negativas es un metal. LA NOMENCLATURA STOCK En la nomenclatura Stock, la valencia de los elementos se indica con números romanos, y se pone entre paréntesis después del nombre del elemento, por ejemplo, cobre(ii). Cuando un elemento tiene una sola valencia, ésta no se indica. Así, los compuestos de litio llevan al final siempre la terminación 'litio', y no 'litio(i)', porque el litio sólo puede actuar con valencia +1. LA NOMENCLATURA DE COMPOSICIÓN La nomenclatura de composición se basa en leer la fórmula tal y como se escribe, empezando desde el final y yendo hacia el principio. Cada vez que nos encontremos con un número en la fórmula, éste se indica con un prefijo como los de la tabla. Número Prefijo Número Prefijo 1 mono 5 penta 2 di 6 hexa 3 tri 7 hepta 4 tetra 8 octa Hay que tener en cuenta que el prefijo 'mono' nunca se utiliza para el elemento que va al principio de la fórmula, y que sólo se usa para el elemento que va al final cuando el elemento que va al principio tiene más de una valencia.
2 2 Formulación y nomenclatura en química inorgánica para P.M.A.R. ELEMENTOS a) Fórmula Los elementos son sustancias formadas por un solo tipo de átomos. Su fórmula general es: En donde E es el símbolo del elemento y n es el número de átomos que se agrupan. Los elementos metálicos se representan sólo con el símbolo del elemento: Fe, K, Mn, Los elementos no metálicos gaseosos (excepto los gases nobles) están formados casi siempre por moléculas de dos átomos: H 2, N 2, O 2, F 2, Cl 2, Br 2, I 2 Hay algunos elementos que pueden unirse formando moléculas con distinto número de átomos, como el azufre (S 2, S 6, S 8, ), el fósforo (P 4) o el oxígeno (O 2, O 3). b) Nombre Los elementos se nombran utilizando la nomenclatura de composición, indicando el número de átomos que forma la molécula, seguido del nombre del elemento: prefijo correspondiente a n + nombre del elemento Si el elemento no forma moléculas, como los metales, el nombre es únicamente el nombre del elemento. c) Ejemplos Fórmula Nombre Nombre aceptado O 2 Dioxígeno oxígeno O 3 Trioxígeno ozono Au Oro - S 8 Octaazufre -
3 Formulación y nomenclatura en química inorgánica para P.M.A.R. 3 COMPUESTOS BINARIOS Como indica su nombre, los compuestos binarios están formados por átomos de dos elementos diferentes. De los dos elementos, el que va la final de la fórmula siempre actúa con valencia negativa, mientras que el que va al principio actúa siempre con valencia positiva. La fórmula se obtiene escribiendo los dos elementos uno a continuación de otro, escribiendo sus valencias sin signo y poniéndoselas como subíndice al átomo contrario. Si es posible, hay que simplificar estos subíndices de manera que no tengan divisores comunes. El nombre tiene dos partes: una general, que indica el tipo de compuesto y que es debida al átomo que aparece al final de la fórmula y otra específica que indica el elemento que aparece al principio. Vamos a estudiar ahora las familias de compuestos una por una. ÓXIDOS Son compuestos en los que el elemento que aparece al final de la fórmula es el oxígeno que actúa con su valencia negativa (-2). a) Fórmula Su fórmula general es: E2On donde E es el símbolo del elemento que se combina con el oxígeno y n es su valencia. Hay que recordar que los subíndices deben simplificarse cuando sea posible. b) Nombre Para el nombre se pueden utilizar la nomenclatura de composición y la de Stock. Composición Se lee la fórmula tal como está escrita, comenzando por el final e indicando los números con los prefijos. El oxígeno se lee como óxido. El profijo mono no se utiliza para el elemento que va al principio de la fórmula, y sólo se usa con el oxígeno si el elemento que lo acompaña tiene más de una valencia positiva: prefijo del oxígeno + óxido de + prefijo del elemento + nombre del elemento
4 4 Formulación y nomenclatura en química inorgánica para P.M.A.R. Stock En la nomenclatura de Stock, estos compuestos se nombran comenzando con las palabras óxido de, seguidas del nombre del elemento que acompaña al oxígeno y de la valencia de éste último escrita con números romanos y entre paréntesis. La valencia del elemento es el número que va en el oxígeno, a no ser que la fórmula esté simplificada. En ese caso, la valencia es el doble del número que va con el oxígeno. La valencia sólo se indica si el elemento que va acompañando al oxígeno tiene más de una valencia positiva: óxido de + nombre del elemento + valencia con números romanos y entre paréntesis c) Dado el nombre poner la fórmula Supongamos que nos piden formular el dióxido de silicio. Lo primero que tenemos que tener en cuenta es que el nombre está en la nomenclatura de composición, por lo que debemos escribir, de derecha a izquierda, lo que nos dice el nombre: d i ó x i d o d e s i l i c i o SiO 2 Supongamos ahora que nos piden formular el óxido de azufre(vi). Sabemos que está escrito en la nomenclatura de Stock. Es un óxido (valencia -2) con el azufre (valencia +6). Se escribe el símbolo del azufre, el del oxígeno, y, como subíndices, las valencias cambiadas de sitio: S 2O 6 Como las valencias son pares, se simplifican: SO 3 d) Dada la fórmula, poner el nombre Nos piden nombrar el compuesto de fórmula Hg 2O. En la nomenclatura de composición, la fórmula se lee desde el final hacia el principio tal cual está escrita: monóxido de dimercurio Se utiliza el prefijo mono porque el mercurio tiene dos valencias diferentes (+1 y +2). En la nomenclatura de Stock, se indica la valencia del mercurio con números romanos y entre paréntesis. En este caso, la valencia del mercurio es +1 (es el subíndice del oxígeno). Como el mercurio tiene dos valencias, hay que indicarla: e) Ejemplos óxido de mercurio(i) Fórmula Composición Stock PtO 2 dióxido de platino óxido de platino(iv) Cl 2O 7 heptaóxido de dicloro óxido de cloro(vii) K 2O óxido de dipotasio óxido de potasio PtO 2 dióxido de platino óxido de platino(iv)
5 Formulación y nomenclatura en química inorgánica para P.M.A.R. 5 HIDRUROS Los hidruros son compuestos binarios en los que el elemento que va al final de la fórmula es el hidrógeno, que actúa con su valencia negativa (-1). a) Fórmula Su fórmula general es: donde E es el símbolo del elemento que se combina con el hidrógeno y n es su valencia. Estos compuestos no pueden simplificarse porque la valencia del hidrógeno es -1. b) Nombre Para el nombre se pueden utilizar la nomenclatura de composición, la de Stock y, en algunos casos, la de sustitución. Composición EHn Se lee la fórmula tal como está escrita, comenzando por el final e indicando los números con los prefijos. prefijo del hidrógeno + hidruro de + nombre del elemento Stock En la nomenclatura de Stock, estos compuestos se nombran comenzando con las palabras hidruro de, seguidas del nombre del elemento que acompaña al hidrógeno y de la valencia de éste último escrita con números romanos y entre paréntesis si el elemento tiene más de una valencia positiva. hidruro de + nombre del elemento + valencia con números romanos y entre paréntesis Sustitución Los hidruros de elementos no metálicos se suelen nombrar también utilizando la nomenclatura de sustitución, que es, en ocasiones, más utilizada que las otras dos. Los nombres de estos compuestos son: Compuesto Nombre Compuesto Nombre BH 3 borano NH 3 amoniaco (azano) CH 4 metano PH 3 fosfano SiH 4 silano AsH 3 arsano GeH 4 germano SbH 3 estibano
6 6 Formulación y nomenclatura en química inorgánica para P.M.A.R. c) Dado el nombre poner la fórmula Supongamos que nos piden formular el dihidruro de hierro. Lo primero que tenemos que tener en cuenta es que el nombre está en la nomenclatura de composición, por lo que debemos escribir, de derecha a izquierda, lo que nos dice el nombre: d i h i d r u r o d e h i e r r o FeH 2 Supongamos ahora que nos piden formular el hidruro de oro(iii). Sabemos que está escrito en la nomenclatura de Stock. Escribimos el símbolo del oro, el del hidrógeno y, como subíndice del hidrógeno, la valencia del oro: AuH 3 d) Dada la fórmula, poner el nombre Nos piden nombrar el compuesto de fórmula PH 3. En la nomenclatura de composición, la fórmula se lee desde el final hacia el principio tal cual está escrita: trihidruro de fósforo En la nomenclatura de Stock, es necesario indicar la valencia del fósforo porque tiene tres valencias positivas (+1, +3 y +5): e) Ejemplos hidruro de fósforo(iii) Este compuesto también puede nombrarse por la nomenclatura de sustitución: fosfano Fórmula Composición Stock Sustitución HgH 2 dihidruro de mercurio hidruro de mercurio(ii) - LiH hidruro de litio hidruro de litio - CrH 3 trihidruro de cromo hidruro de cromo(iii) - CH 4 tetrahidruro de carbono hidruro de carbono metano
7 Formulación y nomenclatura en química inorgánica para P.M.A.R. 7 HALUROS Son combinaciones entre un metal y un no metal. En ellas, el no metal siempre actúa con valencia negativa y el metal con valencia positiva. El metal se escribe en la fórmula en primer lugar y en no metal va al final de la fórmula. a) Fórmula Su fórmula general es: MnXm donde M es el símbolo del metal, X el del no metal, m es la valencia del metal y n la del no metal. Los subíndices deben simplificarse siempre que sea posible. b) Nombre Para el nombre se pueden utilizar la nomenclatura de composición y la de Stock. Composición Se lee la fórmula tal como está escrita, comenzando por el final e indicando los números con los prefijos. El nombre del no metal (el elemento que va al final de la fórmula) se termina en uro. prefijo del no metal + nombre del no metal + -uro de + prefijo del metal + nombre del metal Stock En la nomenclatura de Stock, estos compuestos se nombran comenzando con el nombre del no metal (el elemento que va al final de la fórmula) con la terminación uro, la preposición de y, finalmente, el nombre del metal y la valencia de éste último escrita con números romanos y entre paréntesis (si el metal tiene más de una valencia positiva). nombre del no metal + -uro de + nombre del metal + valencia con números romanos y entre paréntesis c) Dado el nombre poner la fórmula Supongamos que nos piden formular el trisulfuro de dialuminio. Lo primero que tenemos que tener en cuenta es que el nombre está en la nomenclatura de composición, por lo que debemos escribir, de derecha a izquierda, lo que nos dice el nombre: t r i s u l f u r o d e d i a l u m i n i o Al 2S 3 Supongamos ahora que nos piden formular el bromuro de magnesio. Está escrito en la nomenclatura de Stock (no está la valencia del magnesio porque sólo tiene una, +2). Escribimos el símbolo del magnesio, el del bromo y, como subíndice del magnesio la valencia negativa del bromo (-1) y como subíndice del bromo la valencia del magnesio: MgBr 2
8 8 Formulación y nomenclatura en química inorgánica para P.M.A.R. d) Dada la fórmula, poner el nombre Nos dan la fórmula CoSe, y nos piden el nombre del compuesto. En la nomenclatura de composición se lee la fórmula desde el final hacia el principio: monoseleniuro de cobalto Es necesario utilizar el prefijo mono para el selenio porque el cobalto tiene dos valencias positivas (+2 y +3). En la nomenclatura de Stock es necesario determinar la valencia del cobalto. Como el elemento que va al final de la fórmula es el selenio, cuya valencia negativa es -2, debería aparecer un 2 como subíndice del cobalto. Este número no aparece, lo que indica que la fórmula está simplificada. De las dos valencias del cobalto, la que permite simplificar la fórmula es +2, con lo que el nombre sería: e) Ejemplos seleniuro de cobalto(ii) Fórmula Composición Stock AuCl monocloruro de oro cloruro de oro(i) H 2S sulfuro de dihidrógeno sulfuro de hidrógeno Fe 2Te 3 tritelururo de dihierro telururo de hierro(iii) Ag 3N nitruro de tetraplata nitruro de plata VALENCIAS DE ALGUNOS ELEMENTOS QUÍMICOS Alcalinos (+1) Li Na K Rb Cs Fr Alcalino-térreos (+2) Be Mg Ca Sr Ba Ra Térreos B (+3, -3) Al (+3) Ga (+3) In (+1, +3) Tl (+1, +3) Carbonoideos C (+4, -4) Si (+4, -4) Ge (+2, +4) Sn (+2, +4) Pb (+2, +4) Pnictógenos N (+1, +3, +5, -3) P (+1, +3, +5, -3) As (+3, +5, -3) Sb (+3, +5, -3) Bi (+3, +5) Calcógenos O (-2) S (+2, +4, +6, -2) Se (+2, +4, +6, -2) Te (+2, +4, +6, -2) Po (+2, +4, +6) Halógenos F (-1) Cl (+1, +3, +5, +7, -1) Br (+1, +3, +5, +7, -1) I (+1, +3, +5, +7, -1) At (+1, +3, +5, +7, -1) Amonio NH4 + (+1) Hidrógeno H (+1, -1) Cr Mn Fe Co Ni Cu Zn (+3, +6) (+2, +3, +4, +6, +7) (+2, +3) (+2, +3) (+2, +3) (+1, +2) (+2) Pd Ag Cd (+2, +4) (+1) (+2) Pt Au Hg (+2, +4) (+1, +3) (+1, +2)
9 Formulación y nomenclatura en química inorgánica para la E.S.O. 9 EJERCICIOS ÓXIDOS Trióxido de cromo Óxido de plata Óxido de níquel(iii) Monóxido de mercurio Pentaóxido de dinitrógeno BaO SO 2 I 2O 5 Li 2O Al 2O 3 HIDRUROS Dihidruro de magnesio Hidruro de estaño(iv) Fosfano Hexahidruro de cromo Trihidruro de aluminio EJERCICIO COMBINADO NaH SiI 4 PdO 2 AsH 3 SnO 2 MnH 4 As 2O 5 AsN MgH 2 PoCl 4 SeO 2 I 2O 3 GeS 2 SnSe 2 N 2O HBr AsCl 5 FeO K 3N Br 2O AuH CO 2 H 2S Ni 2Te 3 CoH 2 BH 3 CoH 2 FeH 3 CH 4 KH HALUROS Monobromuro de oro Cloruro de hidrógeno Trisulfuro de dialuminio Seleniuro de calcio Carburo de tetraplata NH 4I H 2S Cu 3N 2 CdBr 2 PbCl 4 Óxido de dilitio Arseniuro de carbono Óxido de galio Monóxido de plomo Trihidruro de indio Trióxido de selenio Bromuro de hidrógeno Antimoniuro de germanio(iv) Carburo de tetraamonio Monóxido de nitrógeno Fosfuro de amonio Arsano Tetracloruro de paladio Hidruro de antimonio(iii) Fluoruro de cobalto(ii) Óxido de manganeso(iv) Telururo de dihidrógeno Amoniaco Trióxido de diboro Telururo de estroncio Hidruro de arsénico(iii) Yoduro de hidrógeno Dióxido de azufre Siliciuro de talio(i) Hidruro de bismuto(iii)
Lo primero que hay que conocer para formular y nombrar los compuestos químicos es el número de oxidación de cada elemento.
 Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
INSTITUTO EDUCACIÓN SECUNDARIA POLITÉCNICO. CARTAGENA. 3º E.S.O.
 Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos. 13 millones!!!
 La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
FORMULACIÓN Y NOMENCLATURA
 1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
Química General Básica. Nomenclatura de Compuestos Inorgánicos
 Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA)
 FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
11 Dióxido de carbono. 12 Trióxido de monoazufre. 13 Pentaóxido de difósforo. 14 Dióxido de monoselenio. 15 Dióxido de selenio. 16 Óxido de dimercurio
 1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied Chemistry).
 4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
M m+ + X n- M n X m. Qué es formular un compuesto binario?
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
M m+ + X n-! M n X m EJERCICIOS/ESTUDIO. Qué es formular un compuesto binario?
 EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
Óxido de hierro (III)
 COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
Óxido de hierro(iii)
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS.
 QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
1.- CONCEPTOS PREVIOS
 TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO
 EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
DEPARTAMENTO DE FÍSICA Y QUÍMICA
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
QUÍMICA INORGÁNICA. Elementos Símbolo Valencia Elemento Símbolo Valencia. Hidrógeno H Oxigeno O -2. Flúor F -1 Nitrógeno N
 QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
3.5. FORMULACIÓN Y NOMENCLATURA II
 3.5. FORMULACIÓN Y NOMENCLATURA II 3.5.1. HIDRUROS METÁLICOS. Los compuestos binarios son aquellos en los que únicamente intervienen dos tipos de átomos, es decir, que están formados por sólo dos elementos
3.5. FORMULACIÓN Y NOMENCLATURA II 3.5.1. HIDRUROS METÁLICOS. Los compuestos binarios son aquellos en los que únicamente intervienen dos tipos de átomos, es decir, que están formados por sólo dos elementos
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
Formulación de Química Inorgánica
 Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
PROGRAMA TOTAL FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
H, Li, Na, K, Rb, Cs, Fr 1. Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2. B, Al 3. N, P, As, Sb 1, 3, 5. F, Cl, Br, I 1, 3, 5, 7. C, Si, Ge, Sn, Pb 2, 4 O 2
 H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
SUMARIO FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS INTRODUCCIÓN SUSTANCIAS SIMPLES
 Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
QUÍMICA INORGÁNICA 3º E.S.O.
 QUÍMICA INORGÁNICA 3º E.S.O. Formulación y nomenclatura. Normas de la IUPAC (2005) 1 2 CONCEPTOS GENERALES 1. NORMAS PARA ESCRIBIR LAS FÓRMULAS Se escriben juntos los símbolos de los átomos, el más electronegativo
QUÍMICA INORGÁNICA 3º E.S.O. Formulación y nomenclatura. Normas de la IUPAC (2005) 1 2 CONCEPTOS GENERALES 1. NORMAS PARA ESCRIBIR LAS FÓRMULAS Se escriben juntos los símbolos de los átomos, el más electronegativo
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
Calcio(2+) Hierro(3+)
 CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
Número de oxidación. Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo
 FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
Se conocen como sales binarias a las combinaciones de un metal con un no. metal o de dos no metales entre sí. En los compuestos de un metal y un no
 4.2. COMPUESTOS BINARIOS. 4.2.1. METAL Y NO METAL. Se conocen como sales binarias a las combinaciones de un metal con un no metal o de dos no metales entre sí. En los compuestos de un metal y un no metal,
4.2. COMPUESTOS BINARIOS. 4.2.1. METAL Y NO METAL. Se conocen como sales binarias a las combinaciones de un metal con un no metal o de dos no metales entre sí. En los compuestos de un metal y un no metal,
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA
 5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. CLASIFICACIÓN DE LOS ELEMENTOS QUÍMICOS. 1.1. METALES Y NO METALES En términos generales, se clasifican como: METALES: Poseen brillo metálico.
5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. CLASIFICACIÓN DE LOS ELEMENTOS QUÍMICOS. 1.1. METALES Y NO METALES En términos generales, se clasifican como: METALES: Poseen brillo metálico.
Formulación Inorgánica
 Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Combinaciones Binarias
 Combinaciones Binarias Se llama combinaciones binarias a los compuestos formados por átomos de dos elementos diferentes. Antes de estudiar los diferentes tipos de combinaciones binarias veremos unas normas
Combinaciones Binarias Se llama combinaciones binarias a los compuestos formados por átomos de dos elementos diferentes. Antes de estudiar los diferentes tipos de combinaciones binarias veremos unas normas
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA FORMULACIÓN Una fórmula química es la representación escrita de una molécula o compuesto iónico. Para expresar una fórmula química se utilizan los símbolos de los elementos que
FORMULACIÓN Y NOMENCLATURA FORMULACIÓN Una fórmula química es la representación escrita de una molécula o compuesto iónico. Para expresar una fórmula química se utilizan los símbolos de los elementos que
Un átomo de sodio (Na) y otro de cloro(cl) Dos átomos de hidrógeno (H) y uno de oxígeno (O)
 Símbolos Un elemento químico es aquel compuesto químico que no puede ser descompuesto en otros más simples. Se conocen más de cien elementos químicos, aunque en la naturaleza sólo aparecen noventa, los
Símbolos Un elemento químico es aquel compuesto químico que no puede ser descompuesto en otros más simples. Se conocen más de cien elementos químicos, aunque en la naturaleza sólo aparecen noventa, los
Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales
 Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales 2 de 12 Tipo de compuesto Relaciona estos compuestos:
Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales 2 de 12 Tipo de compuesto Relaciona estos compuestos:
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN (3.º ESO) Nomenclatura de compuestos binarios usando números de oxidación
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN Nomenclatura de compuestos binarios usando números de oxidación La nomenclatura de composición permite usar los números de oxidación para
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN Nomenclatura de compuestos binarios usando números de oxidación La nomenclatura de composición permite usar los números de oxidación para
Tema 1 : Nomenclatura y formulación Química Inorgánica
 Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Acuerdo 286. Química. Nomenclatura Inorgánica. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Nomenclatura Inorgánica Recopiló: M.C. Macaria Hernández Chávez Nomenclatura química inorgánica La Química tiene un lenguaje propio para nombrar las sustancias puras, ya sean simples
Acuerdo 286 Química Nomenclatura Inorgánica Recopiló: M.C. Macaria Hernández Chávez Nomenclatura química inorgánica La Química tiene un lenguaje propio para nombrar las sustancias puras, ya sean simples
FORMULACIÓN INORGÁNICA:
 FORMULACIÓN INORGÁNICA: Formular un compuesto consiste en expresar la fórmula química de dicho compuesto. Es decir, indicar qué tipo de átomos (qué elementos) están presentes en la molécula (o en la red
FORMULACIÓN INORGÁNICA: Formular un compuesto consiste en expresar la fórmula química de dicho compuesto. Es decir, indicar qué tipo de átomos (qué elementos) están presentes en la molécula (o en la red
ACTIVIDADES FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 ACTIVIDADES FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA EJERCICIOS PROPUESTOS 1. Indica los diferentes átomos que existen en estos compuestos y el número de oxidación con que actúan. a) FeS b) Mg(OH)
ACTIVIDADES FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA EJERCICIOS PROPUESTOS 1. Indica los diferentes átomos que existen en estos compuestos y el número de oxidación con que actúan. a) FeS b) Mg(OH)
http://recursos-itaca.blogspot.com.es/ Formulación Inorgánica 1º) Nombra los compuestos siguientes por las tres nomenclaturas:
 1º) Nombra los compuestos siguientes por las tres nomenclaturas: COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + METAL-- ÓXIDOS BÁSICOS OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos
1º) Nombra los compuestos siguientes por las tres nomenclaturas: COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + METAL-- ÓXIDOS BÁSICOS OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos
ESTRUCTURA INTERNA DE LA MATERIA. LOS ÁTOMOS
 1. DE DEMÓCRITO A DALTON ESTRUCTURA INTERNA DE LA MATERIA. LOS ÁTOMOS Hasta dónde podemos dividir una sustancia? Tomamos un terrón de azúcar y lo partimos por la mitad. Elegimos una de las dos mitades
1. DE DEMÓCRITO A DALTON ESTRUCTURA INTERNA DE LA MATERIA. LOS ÁTOMOS Hasta dónde podemos dividir una sustancia? Tomamos un terrón de azúcar y lo partimos por la mitad. Elegimos una de las dos mitades
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
UD 2 ENLACE QUÍMICO Y FUERZAS INTERMOLECULARES FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
REACCIONES QUÍMICAS. Ocurren en la naturaleza. Se expresan por ECUACIONES QUÍMICAS
 REACCIONES QUÍMICAS Ocurren en la naturaleza Se expresan por ECUACIONES QUÍMICAS NaCl + AgNO 3 AgCl + NaNO 3 REACTIVOS PRODUCTOS ECUACIÓN QUÍMICA Estequiométrica (ecuación balanceada) Representar una reacción
REACCIONES QUÍMICAS Ocurren en la naturaleza Se expresan por ECUACIONES QUÍMICAS NaCl + AgNO 3 AgCl + NaNO 3 REACTIVOS PRODUCTOS ECUACIÓN QUÍMICA Estequiométrica (ecuación balanceada) Representar una reacción
Boletín de Actividades (VII) INICIACIÓN A LA FORMULACIÓN Y NOMENCLATURA INORGÁNICA. LiH --
 www.colegioelatabal.es/ciencias/ Boletín de Actividades (VII) INICIACIÓN A LA FORMULACIÓN Y NOMENCLATURA INORGÁNICA. 1. Formula y/o nombra las siguientes combinaciones binarias del hidrógeno: Fórmula N.
www.colegioelatabal.es/ciencias/ Boletín de Actividades (VII) INICIACIÓN A LA FORMULACIÓN Y NOMENCLATURA INORGÁNICA. 1. Formula y/o nombra las siguientes combinaciones binarias del hidrógeno: Fórmula N.
FORMULACIÓN INORGÁNICA
 1 FORMULACIÓN INORGÁNICA Hay tres métodos para poder nombrar cualquier compuesto, el tradicional, el de Stock y la sistemática. Para saber manejar los tres métodos lo mejor es empezar por el más complicado
1 FORMULACIÓN INORGÁNICA Hay tres métodos para poder nombrar cualquier compuesto, el tradicional, el de Stock y la sistemática. Para saber manejar los tres métodos lo mejor es empezar por el más complicado
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO METALES
 CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
FORMULACIÓN (4º ESO)
 FORMULACIÓN (4º ESO) Valencia. Es un número entero que representa el número de electrones que un átomo pone en juego cuando forma un compuesto determinado. NO METALES H (1) -1 +1 METALES Li, Na, K, Rb,
FORMULACIÓN (4º ESO) Valencia. Es un número entero que representa el número de electrones que un átomo pone en juego cuando forma un compuesto determinado. NO METALES H (1) -1 +1 METALES Li, Na, K, Rb,
FORMULACIÓN -TEORIA ÓXIDOS. Son combinaciones binarias con oxígeno. Unidos con metales o no metales más.
 FORMULACIÓN -TEORIA ÓXIDOS Son combinaciones binarias con oxígeno. Unidos con metales o no metales más. Formulación: Se escribe el nombre del metal o no metal y luego se intercambian las valencias, se
FORMULACIÓN -TEORIA ÓXIDOS Son combinaciones binarias con oxígeno. Unidos con metales o no metales más. Formulación: Se escribe el nombre del metal o no metal y luego se intercambian las valencias, se
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO
 APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA Para poder formular y nombrar los
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA Para poder formular y nombrar los
Juan Mª García Bruna Manuel Ortega García José Mª Valderas Jiménez
 Juan Mª García Bruna Manuel Ortega García José Mª Valderas Jiménez Formulación - 3º de ESO Departamento de Física y Química - IES Sierra Mágina FORMULACIÓN Y NOMENCLATURA INORGÁNICA Todas las sustancias
Juan Mª García Bruna Manuel Ortega García José Mª Valderas Jiménez Formulación - 3º de ESO Departamento de Física y Química - IES Sierra Mágina FORMULACIÓN Y NOMENCLATURA INORGÁNICA Todas las sustancias
Universidad Técnica Nacional
 Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Trióxido de dihierro
 OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1) excepto halógenos X no m Metal + Oxígeno = Óxido metálico Fe 2 O 3 ; Li 2 O ; CaO ; Ag
OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1) excepto halógenos X no m Metal + Oxígeno = Óxido metálico Fe 2 O 3 ; Li 2 O ; CaO ; Ag
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17
 FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
Nomenclatura Inorgánica
 Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y INORGÁNICA (IUPAC 2005) 0 COLEGIO COLÓN MARISTAS HUELVA CURSO ACADÉMICO 2015-2016 ÍNDICE 1. COMPUESTOS BINARIOS.. 2 1.1 ÓXIDOS 2 1.2 HALUROS DE OXÍGENO... 3 1.3 PERÓXIDOS...4 1.4 HIDRUROS..
FORMULACIÓN Y INORGÁNICA (IUPAC 2005) 0 COLEGIO COLÓN MARISTAS HUELVA CURSO ACADÉMICO 2015-2016 ÍNDICE 1. COMPUESTOS BINARIOS.. 2 1.1 ÓXIDOS 2 1.2 HALUROS DE OXÍGENO... 3 1.3 PERÓXIDOS...4 1.4 HIDRUROS..
Nomenclatura de compuestos inorgánicos
 1 Nomenclatura de compuestos inorgánicos De pequeños nos comunicamos con otras personas aprendiendo el nombre de los objetos que nos rodean. Conforme vamos creciendo aprendemos a hablar y utilizamos el
1 Nomenclatura de compuestos inorgánicos De pequeños nos comunicamos con otras personas aprendiendo el nombre de los objetos que nos rodean. Conforme vamos creciendo aprendemos a hablar y utilizamos el
Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno:
 Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno: 1) Ácido clorhídrico 2) Sulfuro de hidrógeno 3) Estibano 4) Agua u oxidano 5) Trihidruro de fósforo 6) Hidruro de estaño(iv)
Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno: 1) Ácido clorhídrico 2) Sulfuro de hidrógeno 3) Estibano 4) Agua u oxidano 5) Trihidruro de fósforo 6) Hidruro de estaño(iv)
Compuestos binarios (combinaciones de dos elementos) HIDRUROS METÁLICOS= Metal - Hidrógeno. X H m. H : - 1 Metales: el suyo. FeH 3
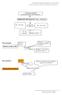 HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
FORMULACIÓN DE QUÍMICA INORGÁNICA 3ºESO
 Euclides Enseñanza Sociedad Cooperativa Andaluza Colegio Privado Concertado Arboleda C/ Reina Victoria 2. 41020 Sevilla Telf. 954 408126 Fax 954 440186 www.colegioarboleda.es arboleda@aces-andalucia.org
Euclides Enseñanza Sociedad Cooperativa Andaluza Colegio Privado Concertado Arboleda C/ Reina Victoria 2. 41020 Sevilla Telf. 954 408126 Fax 954 440186 www.colegioarboleda.es arboleda@aces-andalucia.org
7.-GENERALIDADES EN LA FORMULACIÓN Y NOMENCLATURA SUSTANCIAS BINARIAS
 7.-GENERALIDADES EN LA FORMULACIÓN Y NOMENCLATURA SUSTANCIAS BINARIAS Estas sustancias son las formadas por la unión de dos elementos químicos como por ejemplo NaH, Co 2 O 3, Li 2 S y PCl 3. Para escribir
7.-GENERALIDADES EN LA FORMULACIÓN Y NOMENCLATURA SUSTANCIAS BINARIAS Estas sustancias son las formadas por la unión de dos elementos químicos como por ejemplo NaH, Co 2 O 3, Li 2 S y PCl 3. Para escribir
ÓXIDOS EJEMPLOS EJERCICICIOS. Br 2 O As 2 O 3 B 2 O 3 SnO 2 Cl 2 O 3 As 2 O 5 P 2 O 3. SeO 2 TeO 3 P 2 O 5. Óxido selenioso
 ÓXIDOS EJEMPLOS Fórmula N. Sistemática N. Stock N. tradicional CO Monóxido de carbono Óxido de carbono (I) Óxido carbonoso CO 2 Dióxido de carbono Óxido de carbono (II) Óxido carbónico SO Monóxido de azufre
ÓXIDOS EJEMPLOS Fórmula N. Sistemática N. Stock N. tradicional CO Monóxido de carbono Óxido de carbono (I) Óxido carbonoso CO 2 Dióxido de carbono Óxido de carbono (II) Óxido carbónico SO Monóxido de azufre
NOMENCLATURA DE ÁCIDOS Y BASES
 COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA 0. Introducción. Existen tres tipos de nomenclaturas que nos permiten nombrar los compuestos químicos inorgánicos: A. Nomenclatura Sistemática (normas propuestas por la Unión
FORMULACIÓN Y NOMENCLATURA 0. Introducción. Existen tres tipos de nomenclaturas que nos permiten nombrar los compuestos químicos inorgánicos: A. Nomenclatura Sistemática (normas propuestas por la Unión
REPASO: FORMULACIÓN INORGÁNICA
 COMPUESTOS BINARIOS REPASO: FORMULACIÓN INORGÁNICA OXÍGENO + METAL ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos excepto
COMPUESTOS BINARIOS REPASO: FORMULACIÓN INORGÁNICA OXÍGENO + METAL ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos excepto
 FORMULACIÓN Inorgánica_ DEPARTAMENTO DE FÍSICA Y QUÍMICA http://www.juntadeandalucia.es/educacion/portalaverroes/contenidosdigitales/contenido/ndoiand-20080324-0007-las-formulas-quimicas http://agrega.juntadeandalucia.es//repositorio/28082013/c0/es-an_2013082813_9115336/ndoiand-20080324-0007/index.html
FORMULACIÓN Inorgánica_ DEPARTAMENTO DE FÍSICA Y QUÍMICA http://www.juntadeandalucia.es/educacion/portalaverroes/contenidosdigitales/contenido/ndoiand-20080324-0007-las-formulas-quimicas http://agrega.juntadeandalucia.es//repositorio/28082013/c0/es-an_2013082813_9115336/ndoiand-20080324-0007/index.html
EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS DEL OXÍGENO 1.- Cl 2 O 7 2.- FeO 3.- N 2 O 4.- SO 3 1.- NOMBRA LOS SIGUIENTES COMPUESTOS: 6.- Br 2 O 7.- P 2 O 5 8.- CO 2 9.- I 2 O 5 5.-
EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS DEL OXÍGENO 1.- Cl 2 O 7 2.- FeO 3.- N 2 O 4.- SO 3 1.- NOMBRA LOS SIGUIENTES COMPUESTOS: 6.- Br 2 O 7.- P 2 O 5 8.- CO 2 9.- I 2 O 5 5.-
Física y Química 4º ESO: guía interactiva para la resolución de ejercicios
 Formulación y nomenclatura Física y Química 4º ESO: guía interactiva para la resolución de ejercicios I.E.S. Élaios Departamento de Física y Química SÍMBOLOS QUÍMICOS Y NÚMEROS DE OXIDACIÓN Los elementos
Formulación y nomenclatura Física y Química 4º ESO: guía interactiva para la resolución de ejercicios I.E.S. Élaios Departamento de Física y Química SÍMBOLOS QUÍMICOS Y NÚMEROS DE OXIDACIÓN Los elementos
Un elemento es una sustancia que no puede descomponerse en sustancias más simples, y está compuesta por una sola clase de átomos.
 Elementos químicos en Costa Rica Elementos Químicos en Costa Rica Un elemento es una sustancia que no puede descomponerse en sustancias más simples, y está compuesta por una sola clase de átomos. La mayoría
Elementos químicos en Costa Rica Elementos Químicos en Costa Rica Un elemento es una sustancia que no puede descomponerse en sustancias más simples, y está compuesta por una sola clase de átomos. La mayoría
Ejercicios y respuestas del apartado: Tabla periódica. Grupos y períodos. Metales, no metales y gases nobles
 Ejercicios y respuestas del apartado: Tabla periódica. Grupos y períodos. Metales, no metales y gases nobles Elementos de la tabla periódica (1) 1. Grupo de los halógenos: ---------> Símbolos: (1), (2),
Ejercicios y respuestas del apartado: Tabla periódica. Grupos y períodos. Metales, no metales y gases nobles Elementos de la tabla periódica (1) 1. Grupo de los halógenos: ---------> Símbolos: (1), (2),
COMPUESTOS BINARIOS Y DERIVADOS
 FORMULACIÓN INORGÁNICA SEGÚN LAS REGLAS DE LA IUPAC 005 COMPUESTOS BINARIOS Y DERIVADOS Dentro de este tipo de compuestos hay: sustancias moleculares: Amoniaco NH, Cloruro de hidrógeno HCl, aunque puedan
FORMULACIÓN INORGÁNICA SEGÚN LAS REGLAS DE LA IUPAC 005 COMPUESTOS BINARIOS Y DERIVADOS Dentro de este tipo de compuestos hay: sustancias moleculares: Amoniaco NH, Cloruro de hidrógeno HCl, aunque puedan
ísica y uímica FORMULACIÓN Y NOMENCLATURA Nombre Óxido de bario Óxido de sodio Óxido de plata Fórmula
 Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
5) Cuando un metal y un no metal reaccionan el tiende a perder electrones y el tiende a ganar electrones.
 Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. A medida que fueron conociéndose los diferentes elementos químicos de la tabla periódica se vio que el número era relativamente pequeño si se compara con la gran variedad
FORMULACIÓN DE QUÍMICA INORGÁNICA. A medida que fueron conociéndose los diferentes elementos químicos de la tabla periódica se vio que el número era relativamente pequeño si se compara con la gran variedad
Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas
 D EPA R T A M ENTO D E FÍSICA Y Q UÍM ICA Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas José Manuel Ramírez Fernández Valencias y estados, grados o números de oxidación Con
D EPA R T A M ENTO D E FÍSICA Y Q UÍM ICA Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas José Manuel Ramírez Fernández Valencias y estados, grados o números de oxidación Con
FORMULACIÓN INORGÁNICA CURSO 2012-2013 DPTO. FÍSICA Y QUÍMICA IES. ALMINARES
 A) SUSTANCIAS SIMPLES - Los elementos gaseosos suelen encontrarse en forma de moléculas diatómicas. Ej: H 2, O 2, N 2, Cl 2,... Algunas excepciones son el ozono ( O 3 ), azufre ( S 8 )... - Los metales
A) SUSTANCIAS SIMPLES - Los elementos gaseosos suelen encontrarse en forma de moléculas diatómicas. Ej: H 2, O 2, N 2, Cl 2,... Algunas excepciones son el ozono ( O 3 ), azufre ( S 8 )... - Los metales
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 4º ESO
 EJERCICIOS DE FORMULACIÓN Y DE QUÍMICA INORGÁNICA 4º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido de disodio Óxido de sodio
EJERCICIOS DE FORMULACIÓN Y DE QUÍMICA INORGÁNICA 4º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido de disodio Óxido de sodio
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA 1. SUSTANCIAS SIMPLES El número de oxidación de un elemento en una sustancia simple es cero. Se nombran utilizando prefijos numerales que indican el número de átomos del elemento,
FORMULACIÓN INORGÁNICA 1. SUSTANCIAS SIMPLES El número de oxidación de un elemento en una sustancia simple es cero. Se nombran utilizando prefijos numerales que indican el número de átomos del elemento,
CONFERENCIA No. 1 Página 1 de 4. DE: Septiembre 7 del 2015 A : Septiembre 25 del 2015
 CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
Trabajo de repaso. Física y Química
 Departamento de Física y Química IES Salvador Allende Trabajo de repaso De Física y Química Nombre del alumno: Curso: Objetivo del trabajo: ayudar a preparar la asignatura durante el verano Fecha de entrega
Departamento de Física y Química IES Salvador Allende Trabajo de repaso De Física y Química Nombre del alumno: Curso: Objetivo del trabajo: ayudar a preparar la asignatura durante el verano Fecha de entrega
EL SISTEMA PERIÓDICO
 EL SISTEMA PERIÓDICO CONTENIDOS. 1.- Primeras clasificaciones de los elementos químicos. 2.- Clasificaciones de Meyer y Mendeleiev. 3.- Clasificación actual de los elementos químicos. 4.- Tabla periódica
EL SISTEMA PERIÓDICO CONTENIDOS. 1.- Primeras clasificaciones de los elementos químicos. 2.- Clasificaciones de Meyer y Mendeleiev. 3.- Clasificación actual de los elementos químicos. 4.- Tabla periódica
Ejercicios de la unidad didáctica 4.- Formulación y nomenclatura.
 Nombre y apellidos: Ejercicios de la unidad didáctica 4.- Formulación y nomenclatura. 1 Los elementos que debes conocer este curso están recogidos en las siguientes tablas. Complétalas escribiendo los
Nombre y apellidos: Ejercicios de la unidad didáctica 4.- Formulación y nomenclatura. 1 Los elementos que debes conocer este curso están recogidos en las siguientes tablas. Complétalas escribiendo los
APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O
 APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O Colegio Cardenal Spínola Huelva FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con
APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O Colegio Cardenal Spínola Huelva FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con
GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA.
 1 GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA. 1. Estado de Oxidación Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y
1 GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA. 1. Estado de Oxidación Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y
