Chatham y la Fábrica de Esmeraldas
|
|
|
- Teresa Castellanos Roldán
- hace 6 años
- Vistas:
Transcripción
1 Chatham y la Fábrica de Esmeraldas Desde tiempos inmemoriales la humanidad ha vivido fascinada por la idiosincrasia de una serie de materiales geológicos cuya belleza, rareza, brillo o transparencia sobresalían sobre los demás. Fueron denominados piedras preciosas, atesoradas por reyes como símbolo de poder e imbuidas de tal halo de trascendencia que aún hoy su posesión es causa de guerras. Los alquimistas pasaron siglos intentando reproducirlas y cuando la alquimia se convirtió en química los científicos centraron sus esfuerzos en conocer su composición y estructura con el fin de sintetizarlas y crearlas a su antojo. Las primeras gemas sintéticas de las que se tiene constancia datan del siglo XIX, se trata de rubíes de procedencia incierta los cuales se creen resultado de la fusión de otros de menor tamaño. Estas piezas se sabe sirvieron de inspiración a los químicos franceses Edmond Frémy y Auguste Verneuil para desarrollar sus métodos, siendo el de este último un éxito y un hito en la gemología. Con el conocimiento de que zafiros y rubíes son ambos el mismo mineral de óxido de aluminio llamado corindón (Al₂O₃) Verneuil ideó en 1902 un horno para fabricarlos. En él la materia prima (aluminio puro) en forma de polvo fino se coloca en un contenedor con una abertura en la parte inferior, a través de esta apertura el polvo puede escapar cuando se hace vibrar. Mientras el polvo sale, se suministra oxígeno al horno, dicho oxígeno viaja junto con el polvo por un tubo estrecho el cual está situado dentro de un tubo más grande, en el que se suministra también hidrógeno. En el punto donde el tubo estrecho se abre al mayor, se produce la combustión, con una llama de por lo menos 2000 C. El polvo pasa a través de la llama, y se derrite en gotitas pequeñas, que entran en una varilla de soporte. Poco a poco las gotas forman un aglomerado en la barra. En el extremo se forma con el tiempo la semilla del cristal. A medida que más gotas caen en la punta un solo cristal, llamado bola, comienza a formarse, la barra se mueve lentamente hacia abajo, permitiendo a la base de la bola cristalizar mientras el otro extremo se mantiene líquido.
2 Corindones y espinelas sintetizados por el método de Verneuil ( Por otra parte, el color que en los minerales y en este caso concreto en los corindones depende tan sólo de pequeñas trazas de elementos ajenos a los que conforman su estructura cristalina, se consigue por la simple adición de escasas cantidades de diversos óxidos, tales como el de cromo para un rubí rojo, o el óxido férrico y dióxido de titanio para un zafiro azul.
3 Diagrama simplificado del proceso de Verneuil ( Ahora bien, el método de Verneuil no funciona para obtener algunas gemas como las esmeraldas. La razón es que la esmeralda con una fórmula química más compleja (Be₃Al₂(SiO₃)₆::Cr) es un silicato de berilo y aluminio coloreado por cromo y es bastante difícil disolver todos sus componentes al mismo tiempo (algunos de ellos se evaporan antes de que los otros se hayan disuelto). Sin embargo Chatham un brillante químico estadounidense que desarrolló un particular interés por la creación de gemas sintéticas a muy temprana edad no cesaría en su empeño hasta conseguir sintetizarlas. Durante su adolescencia trató de crear diamantes sintéticos a través de la disolución de grafito en hierro fundido. Por desgracia, cuando trató de producir un enfriamiento rápido por medio de la inmersión en nitrógeno líquido, la explosión que resultó de esto, destruyó las ventanas de todo su vecindario en San Francisco. Por este incidente tanto su padre como la policía de San Francisco insistieron
4 en que volcara su atención en el desarrollo de cristales de esmeralda. En 1930 cultivó cristales de berilo incoloro y para 1935 cultivó su primera esmeralda, un cristal de un quilate, que se encuentra actualmente en el museo Smithsoniano. La clave del método fue un diluyente especial llamado flux constituido por la combinación de ciertos químicos como óxido de litio, óxido de molibdeno y óxido de vanadio; que mantienen su estado líquido aún a altas temperaturas. La receta secreta del flux permitió que todos los componentes se disolvieran al mismo tiempo. Así pues, Chatham suspendió pequeños cristales en el flux caliente como base para el crecimiento de nuevos cristales; todo ello contenido en un crisol o recipiente adecuado para la fusión de sustancias a muy alta temperatura. En el crisol abierto (a presión ambiental) y a una temperatura de unos C se colocan, separados, fragmentos de SiO₂ y de Al₂O₃+ BeO. Por otra parte, las semillas de cristalización, sobre las que se pretende que se formen los cristales de esmeralda se sitúan en el centro del crisol, separadas de la sílice por una rejilla de platino. A la temperatura citada, el óxido de vanadio que constituye la mezcla se funde y disuelve la sílice, la alúmina, el óxido de berilio y los compuestos portadores de cromo. Esquema de fabricación de esmeraldas sintéticas "flux" (
5 Al descender la temperatura, a razón de unos 4 C por hora, se forman cristales de esmeralda sobre las semillas. En algunos aspectos, las piedras creadas por Chatham llegan a ser superiores a las esmeraldas naturales; debido a que éstas últimas, pueden presentar muchas fracturas e inclusiones. Mientras que las de Chatham no poseen ninguno de estos defectos. Así mismo, nuestro fabricante de esmeraldas no sólo fue un brillante e inquieto científico, sino que además fue un hombre de negocios muy astuto. Creo una compañía para la comercialización de sus esmeraldas y desarrolló la tecnología para crear rubíes, alejandritas, y zafiros azules y naranjas. Chatham murió en 1983, pero su hijo heredó sus negocios y tan sólo unos años después del fallecimiento, su compañía logró crear diamantes en el laboratorio, realizando así su mayor anhelo y esta vez sin destruir los cristales de todo un vecindario. Carla P. Yanes es licenciada en Geología por la Universidad de Granada. Además, participó en la promoción de 2014 del curso de Edafología, Química Agrícola y Biología Vegetal de la Unesco en la EEZ de Granada. Para saber más: Gemas de ayer, de hoy y de mañana: introducción al estudio de las piedras preciosas. Joaquín Solans Huguet.
Cristalización artificial de rubíes
 Cristalización artificial de rubíes Mª Victoria López-Acevedo Cornejo Se denomina rubí a la variedad noble del corindón, de color rojo sangre. Es la más valiosa de todas las piedras preciosas naturales
Cristalización artificial de rubíes Mª Victoria López-Acevedo Cornejo Se denomina rubí a la variedad noble del corindón, de color rojo sangre. Es la más valiosa de todas las piedras preciosas naturales
6.1. LA INDUSTRIA QUÍMICA BÁSICA.
 6. LA QUÍMICA EN SOCIEDAD. 6.1. LA INDUSTRIA QUÍMICA BÁSICA. 6.1.1. METALURGIA. No podríamos imaginar el mundo moderno sin metales, ya que entran en la composición de miles de aparatos e instrumentos que
6. LA QUÍMICA EN SOCIEDAD. 6.1. LA INDUSTRIA QUÍMICA BÁSICA. 6.1.1. METALURGIA. No podríamos imaginar el mundo moderno sin metales, ya que entran en la composición de miles de aparatos e instrumentos que
Las piedras preciosas: un arcoiris de color
 Las piedras preciosas: un arcoiris de color Ricardo Rafael Contreras* Las piedras preciosas o materiales gemológicos, han sido utilizados por las diversas culturas en función de su belleza, durabilidad
Las piedras preciosas: un arcoiris de color Ricardo Rafael Contreras* Las piedras preciosas o materiales gemológicos, han sido utilizados por las diversas culturas en función de su belleza, durabilidad
MODULO ESPECTRO VISIBLE. LABORATORIO GEMOLÓGICO MLLOPIS
 7.3 ESPECTRO VISIBLE Como dijimos al principio de este mismo módulo, la luz blanca que nos llega del sol es la suma de todas las longitudes de onda comprendidas entre los 700 y los 400 nm aproximadamente.
7.3 ESPECTRO VISIBLE Como dijimos al principio de este mismo módulo, la luz blanca que nos llega del sol es la suma de todas las longitudes de onda comprendidas entre los 700 y los 400 nm aproximadamente.
Sabes cuál es el nombre de esta gema de origen orgánico?
 Empecemos! Amigos y amigas, hemos llegado al final de este semestre! Y nos despediremos explorando las bondades que nos provee la naturaleza y que el ser humano ha sabido aprovechar para su beneficio y
Empecemos! Amigos y amigas, hemos llegado al final de este semestre! Y nos despediremos explorando las bondades que nos provee la naturaleza y que el ser humano ha sabido aprovechar para su beneficio y
Ciencias de la Tierra FS001
 1 Ciencias de la Tierra FS001 001_02_01 - Rocas Ígneas UNIVERSIDAD NACIONAL AUTÓNOMA DE HONDURAS FACULTAD DE CIENCIAS ESCUELA DE FÍSICA LUIS VARGAS & HEYDI MARTÍNEZ Ciclo de la Roca 2 Clasificación de
1 Ciencias de la Tierra FS001 001_02_01 - Rocas Ígneas UNIVERSIDAD NACIONAL AUTÓNOMA DE HONDURAS FACULTAD DE CIENCIAS ESCUELA DE FÍSICA LUIS VARGAS & HEYDI MARTÍNEZ Ciclo de la Roca 2 Clasificación de
Curso Académico Nombre del Curso Gemología Tipo de Curso Curso de Formación Continua Número de créditos 12,00 ECTS
 GEMOLOGÍA Datos básicos del Curso Curso Académico 2012-2013 Nombre del Curso Gemología Tipo de Curso Curso de Formación Continua Número de créditos 12,00 ECTS Dirección Unidad organizadora Departamento
GEMOLOGÍA Datos básicos del Curso Curso Académico 2012-2013 Nombre del Curso Gemología Tipo de Curso Curso de Formación Continua Número de créditos 12,00 ECTS Dirección Unidad organizadora Departamento
Curso Académico Nombre del Curso Gemología Tipo de Curso Curso de Formación Especializada Número de créditos 15,00 ECTS
 GEMOLOGÍA Datos básicos del Curso Curso Académico 2011-2012 Nombre del Curso Gemología Tipo de Curso Curso de Formación Especializada Número de créditos 15,00 ECTS Dirección Unidad organizadora Departamento
GEMOLOGÍA Datos básicos del Curso Curso Académico 2011-2012 Nombre del Curso Gemología Tipo de Curso Curso de Formación Especializada Número de créditos 15,00 ECTS Dirección Unidad organizadora Departamento
TEMA 5. Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS
 TEMA 5 Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS La primera clasificación de los elementos fue la que distinguió entre metales y no metales y se basaba en el aspecto que presentaban los elementos
TEMA 5 Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS La primera clasificación de los elementos fue la que distinguió entre metales y no metales y se basaba en el aspecto que presentaban los elementos
Física y Química: guía interactiva para la resolución de ejercicios
 Física y Química: guía interactiva para la resolución de ejercicios CLASIFICACIÓN DE LA MATERIA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 (a) En un vaso tenemos alcohol que calentamos
Física y Química: guía interactiva para la resolución de ejercicios CLASIFICACIÓN DE LA MATERIA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 (a) En un vaso tenemos alcohol que calentamos
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO.
 LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO. Prácticamente todos los elementos conocidos, metales y no metales, reaccionan o son oxidados por el oxígeno formando
LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO. Prácticamente todos los elementos conocidos, metales y no metales, reaccionan o son oxidados por el oxígeno formando
Cátedra de Geoquímica - TP N 9 Regla de fases I
 La regla de las fases permite interpretar y seguir los cursos de cristalización y fusión en sistemas de dos y tres componentes (regla de fases I y II, respectivamente). La formulación de la regla es la
La regla de las fases permite interpretar y seguir los cursos de cristalización y fusión en sistemas de dos y tres componentes (regla de fases I y II, respectivamente). La formulación de la regla es la
-Estructura del átomo. Explícala y realiza un dibujo.
 2. Polis y urbe: la ciudad como teatro de un mundo civilizado. 2.1. La ciudad como escenario; escenas de la ciudad 2.1.2. TRAMOYA URBANA. ESTRUCTURA DE LA MATERIA Alguien en la prehistoria se dio cuenta
2. Polis y urbe: la ciudad como teatro de un mundo civilizado. 2.1. La ciudad como escenario; escenas de la ciudad 2.1.2. TRAMOYA URBANA. ESTRUCTURA DE LA MATERIA Alguien en la prehistoria se dio cuenta
UNAM Facultad de Química Curso Química General 1 Grupo 8 COLECCIÓN DE EJERCICIOS UNIDAD 1
 UNAM Facultad de Química Curso Química General 1 Grupo 8 COLECCIÓN DE EJERCICIOS UNIDAD 1 1. En un libro aparece la siguiente definición de Química: La Química es la ciencia que tiene por objeto el estudio
UNAM Facultad de Química Curso Química General 1 Grupo 8 COLECCIÓN DE EJERCICIOS UNIDAD 1 1. En un libro aparece la siguiente definición de Química: La Química es la ciencia que tiene por objeto el estudio
CLASIFICACIÓN DE LOS MATERIALES
 METALES FERROSOS CLASIFICACIÓN DE LOS MATERIALES MATERIALES METÁLICOS NO METÁLICOS FÉRRICOS Aceros, fundiciones, hierro dulce NO FÉRRICOS Metales ligeros, metales pesados, aleaciones, etc.. NATURALES Seda,
METALES FERROSOS CLASIFICACIÓN DE LOS MATERIALES MATERIALES METÁLICOS NO METÁLICOS FÉRRICOS Aceros, fundiciones, hierro dulce NO FÉRRICOS Metales ligeros, metales pesados, aleaciones, etc.. NATURALES Seda,
Física y Química (4º ESO): Estructura del átomo y enlaces químicos 11
 Física y Química (4º ESO): Estructura del átomo y enlaces químicos 11 EL ENLACE QUÍMICO 10.- Concepto y naturaleza del enlace químico Se denomina enlace químico al conjunto de fuerzas que mantiene unidos
Física y Química (4º ESO): Estructura del átomo y enlaces químicos 11 EL ENLACE QUÍMICO 10.- Concepto y naturaleza del enlace químico Se denomina enlace químico al conjunto de fuerzas que mantiene unidos
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
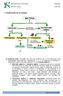 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
UNAM Facultad de Química Curso Química General 1 Grupo 14 COLECCIÓN DE EJERCICIOS UNIDAD 1
 UNAM Facultad de Química Curso Química General 1 Grupo 14 COLECCIÓN DE EJERCICIOS UNIDAD 1 1. En un libro aparece la siguiente definición de Química: La Química es la ciencia que tiene por objeto el estudio
UNAM Facultad de Química Curso Química General 1 Grupo 14 COLECCIÓN DE EJERCICIOS UNIDAD 1 1. En un libro aparece la siguiente definición de Química: La Química es la ciencia que tiene por objeto el estudio
VIDRIOS. Ilse Itzel Ramírez Barbosa Cecilia Ruiz Alemán
 VIDRIOS Ilse Itzel Ramírez Barbosa Cecilia Ruiz Alemán 1 Qué es un vidrio? Es un sólido inorgánico fundido que se ha enfriado sin experimentar cristalización. Los vidrios son deformables por al aplicarles
VIDRIOS Ilse Itzel Ramírez Barbosa Cecilia Ruiz Alemán 1 Qué es un vidrio? Es un sólido inorgánico fundido que se ha enfriado sin experimentar cristalización. Los vidrios son deformables por al aplicarles
UNIONES ENTRE ÁTOMOS. EL ENLACE QUÍMICO. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 UNIONES ENTRE ÁTOMOS. EL ENLACE QUÍMICO Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción En la naturaleza, son muy pocos los átomos que se encuentran libres y aislados, sólo los átomos de
UNIONES ENTRE ÁTOMOS. EL ENLACE QUÍMICO Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción En la naturaleza, son muy pocos los átomos que se encuentran libres y aislados, sólo los átomos de
1. Formación de núcleos estables en el fundido. ( Nucleacion ).
 PROPIEDADES DE LOS MATERIALES. UNIDAD. IMPERFECCIONES EN SOLIDOS. Proceso de Solidificación. Es un proceso físico que consiste en el cambio de estado de materia de líquido a solido producido por la disminución
PROPIEDADES DE LOS MATERIALES. UNIDAD. IMPERFECCIONES EN SOLIDOS. Proceso de Solidificación. Es un proceso físico que consiste en el cambio de estado de materia de líquido a solido producido por la disminución
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA - (TIPO I)
 PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA - (TIPO I) Las preguntas de este tipo constan de un enunciado y de cuatro posibilidades de respuesta, entre las cuales debe escoger la que considere
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA - (TIPO I) Las preguntas de este tipo constan de un enunciado y de cuatro posibilidades de respuesta, entre las cuales debe escoger la que considere
3º ESO Física y Química A. Puebla T3: Sustancias puras y mezclas. FICHA 2: LA MATERIA. COMO SE PRESENTA
 FICHA 2: LA MATERIA. COMO SE PRESENTA 1. Lee detenidamente las siguientes descripciones (de A a E) y clasifica como elemento o compuesto las sustancias: A) Caliza. Se coloca en un matraz varias piedras
FICHA 2: LA MATERIA. COMO SE PRESENTA 1. Lee detenidamente las siguientes descripciones (de A a E) y clasifica como elemento o compuesto las sustancias: A) Caliza. Se coloca en un matraz varias piedras
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO. Dpto. de Física y Química. R. Artacho
 4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Enlace químico en las sustancias 2. Tipos de enlace entre átomos 3. Enlace iónico 4. Enlace covalente
4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Enlace químico en las sustancias 2. Tipos de enlace entre átomos 3. Enlace iónico 4. Enlace covalente
CLASIFICACIÓN DE LOS MATERIALES
 METALES FERROSOS CLASIFICACIÓN DE LOS MATERIALES MATERIALES METÁLICOS NO METÁLICOS FÉRRICOS Aceros, fundiciones, hierro dulce NO FÉRRICOS Metales ligeros, metales pesados, aleaciones, etc.. NATURALES Seda,
METALES FERROSOS CLASIFICACIÓN DE LOS MATERIALES MATERIALES METÁLICOS NO METÁLICOS FÉRRICOS Aceros, fundiciones, hierro dulce NO FÉRRICOS Metales ligeros, metales pesados, aleaciones, etc.. NATURALES Seda,
Clase N 7. Mineralogía
 Pre-Universitario Manuel Guerrero Ceballos Clase N 7 Mineralogía ICAL ATACAMA Módulo Plan Común Síntesis De La Clase Anterior Compuestos Binarios Cuaternarios Compuestos oxigenados Compuestos hidrogenados
Pre-Universitario Manuel Guerrero Ceballos Clase N 7 Mineralogía ICAL ATACAMA Módulo Plan Común Síntesis De La Clase Anterior Compuestos Binarios Cuaternarios Compuestos oxigenados Compuestos hidrogenados
NORMA TÉCNICA COLOMBIANA 623
 NORMA TÉCNICA NTC COLOMBIANA 623 1972-11-02 MATERIALES REFRACTARIOS. CLASIFICACIÓN GENERAL E: REFRACTORY MATERIAL. GENERAL CLASSIFICATION CORRESPONDENCIA: DESCRIPTORES: material refractario; producto refractario;
NORMA TÉCNICA NTC COLOMBIANA 623 1972-11-02 MATERIALES REFRACTARIOS. CLASIFICACIÓN GENERAL E: REFRACTORY MATERIAL. GENERAL CLASSIFICATION CORRESPONDENCIA: DESCRIPTORES: material refractario; producto refractario;
Este es un modelo de examen, en el examen real usted debe identificar los datos que necesita para resolver el problema, por lo tanto usted debe en
 Este es un modelo de examen, en el examen real usted debe identificar los datos que necesita para resolver el problema, por lo tanto usted debe en algunos problemas inventarse datos para poder resolver
Este es un modelo de examen, en el examen real usted debe identificar los datos que necesita para resolver el problema, por lo tanto usted debe en algunos problemas inventarse datos para poder resolver
Web-page:
 GUÍA - PARALELO CEPRE UNI ESTADOS DE AGREGACIÓN MOLECULAR SÓLIDOS Y LÍQUIDOS I. Colocar (A) si la propiedad corresponde a un sólido amorfo y (C) si la propiedad corresponde a un sólido cristalino: 1. Poseen
GUÍA - PARALELO CEPRE UNI ESTADOS DE AGREGACIÓN MOLECULAR SÓLIDOS Y LÍQUIDOS I. Colocar (A) si la propiedad corresponde a un sólido amorfo y (C) si la propiedad corresponde a un sólido cristalino: 1. Poseen
COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10
 COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10 NOTA: ALGUNAS DE LAS PREGUNTAS PRESENTES EN ESTE CUESTIONARIO SON PREGUNTAS LIBERADAS POR EL ICFES ENTRE LOS AÑOS DE 2009 A 2011. Como
COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10 NOTA: ALGUNAS DE LAS PREGUNTAS PRESENTES EN ESTE CUESTIONARIO SON PREGUNTAS LIBERADAS POR EL ICFES ENTRE LOS AÑOS DE 2009 A 2011. Como
PROPIEDADES DE LA MATERIA. Prof. Jackeline Ruttell torres Química Febrero 2017
 PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
PROGRAMA ANALÍTICO. Correlativas para cursar: Regulares: Aprobadas: Correlativas para rendir: Regulares: Aprobadas:
 PROGRAMA ANALÍTICO ASIGNATURA: Refractarios y Cerámicos ESPECIALIDAD: Metalurgia PLAN: 95 Adecuado (Ordenanza Nº 1058) NIVEL: Cuarto MODALIDAD: Anual DICTADO: Anual HORAS:4.hs semanales ÁREA: Tecnologías
PROGRAMA ANALÍTICO ASIGNATURA: Refractarios y Cerámicos ESPECIALIDAD: Metalurgia PLAN: 95 Adecuado (Ordenanza Nº 1058) NIVEL: Cuarto MODALIDAD: Anual DICTADO: Anual HORAS:4.hs semanales ÁREA: Tecnologías
MINERALOGÍA Profesora: Priscilla Guzmán C.
 MINERALOGÍA Profesora: Priscilla Guzmán C. Habilidades Conocimiento. Comprensión. Aplicación. Contenidos Definición de mineral. Propiedades físicas y químicas de los minerales. Definición de roca y clasificación.
MINERALOGÍA Profesora: Priscilla Guzmán C. Habilidades Conocimiento. Comprensión. Aplicación. Contenidos Definición de mineral. Propiedades físicas y químicas de los minerales. Definición de roca y clasificación.
CATALOGO DE PRODUCTOS
 CATALOGO DE PRODUCTOS 2017 INDICE HISTORIA HISTORIA DATOS Peso Color Transparencia Brillo Corte Mejoramiento Precio Certificado productos Royal Premium Medium Standard Basic Colombia Greenstones es la
CATALOGO DE PRODUCTOS 2017 INDICE HISTORIA HISTORIA DATOS Peso Color Transparencia Brillo Corte Mejoramiento Precio Certificado productos Royal Premium Medium Standard Basic Colombia Greenstones es la
UNIDAD 3: EL ENLACE QUÍMICO
 UNIDAD 3: EL ENLACE QUÍMICO 1.- REGLA DEL OCTETO Casi todas las sustancias que encontramos en la naturaleza están formadas por átomos unidos. Las fuerzas que mantienen unidos los átomos en las distintas
UNIDAD 3: EL ENLACE QUÍMICO 1.- REGLA DEL OCTETO Casi todas las sustancias que encontramos en la naturaleza están formadas por átomos unidos. Las fuerzas que mantienen unidos los átomos en las distintas
Resolución Directoral N INACAL/DN ( )
 Resolución Directoral N 008-2017-INACAL/DN (2017-04-01) El Centro de Información y Documentación (CID) del Inacal, con el objetivo de ofrecer a los usuarios en general productos informativos actualizados,
Resolución Directoral N 008-2017-INACAL/DN (2017-04-01) El Centro de Información y Documentación (CID) del Inacal, con el objetivo de ofrecer a los usuarios en general productos informativos actualizados,
Sus caracteristicas principales son:
 Los materiales cerámicos son materiales que tienen tanto compuestos de elementos metálicos como no metálicos, que están unidos por enlaces iónicos y/o covalentes. Sus caracteristicas principales son: Su
Los materiales cerámicos son materiales que tienen tanto compuestos de elementos metálicos como no metálicos, que están unidos por enlaces iónicos y/o covalentes. Sus caracteristicas principales son: Su
Instrucciones: Lee el siguiente texto y contesta los ejercicios propuestos.
 Instrucciones: Lee el siguiente texto y contesta los ejercicios propuestos. I. Propiedades y cambios físicos y químicos. QUÍMICA 1 El azúcar, el agua y el aluminio son sustancias diferentes. Toda sustancia
Instrucciones: Lee el siguiente texto y contesta los ejercicios propuestos. I. Propiedades y cambios físicos y químicos. QUÍMICA 1 El azúcar, el agua y el aluminio son sustancias diferentes. Toda sustancia
Química: el estudio del cambio. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Química: el estudio del cambio Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. ACLARACIÓN IMPORTANTE: Esta presentación ha sido diseñada por los creativos de
Química: el estudio del cambio Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. ACLARACIÓN IMPORTANTE: Esta presentación ha sido diseñada por los creativos de
El color que presentan los minerales es otra propiedad que permite distinguir
 4.2.2.3. COLOR. El color que presentan los minerales es otra propiedad que permite distinguir los minerales. El color no sólo depende de la composición del mineral, también se ve influido por las impurezas
4.2.2.3. COLOR. El color que presentan los minerales es otra propiedad que permite distinguir los minerales. El color no sólo depende de la composición del mineral, también se ve influido por las impurezas
LAS ROCAS ÍGNEAS LAS ROCAS ÍGNEAS
 LAS ROCAS ÍGNEAS Geología a Aplicada a la Geografía a FísicaF LAS ROCAS ÍGNEAS Geología a FísicaF CONTENIDO Cristalización de un magma. Texturas ígneas. Composiciones ígneas. Denominación de las rocas
LAS ROCAS ÍGNEAS Geología a Aplicada a la Geografía a FísicaF LAS ROCAS ÍGNEAS Geología a FísicaF CONTENIDO Cristalización de un magma. Texturas ígneas. Composiciones ígneas. Denominación de las rocas
Interacciones entre los átomos, o MODELOS DE ENLACE
 Interacciones entre los átomos, o MODELOS DE ENLACE Las Sustancias Químicas (realidad) Y los enlaces... (el modelo ) Cómo clasificamos a a las sustancias? Por qué es importante clasificarlas? Por estado
Interacciones entre los átomos, o MODELOS DE ENLACE Las Sustancias Químicas (realidad) Y los enlaces... (el modelo ) Cómo clasificamos a a las sustancias? Por qué es importante clasificarlas? Por estado
 http://www-g.eng.cam.ac.uk/mmg/teaching/phasediagrams/index4.html COMPOSICION QUIMICA Y CANTIDADES RELATIVAS DE CADA FASE EVOLUCION DE LA MICROESTRUCTURA DURANTE EL ENFRIAMIENTO LENTO DE UNA COMPOSICION
http://www-g.eng.cam.ac.uk/mmg/teaching/phasediagrams/index4.html COMPOSICION QUIMICA Y CANTIDADES RELATIVAS DE CADA FASE EVOLUCION DE LA MICROESTRUCTURA DURANTE EL ENFRIAMIENTO LENTO DE UNA COMPOSICION
ENLACE QUÍMICO 2º BACH EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. H-CHO H C = O : CH 3 OH H C O H H H H C O C H H H CH 3 OCH 3
 EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
Capítulo 3. Azufre Producción de Ácido Sulfúrico Producción de azufre y ácido sulfúrico Proceso Frash. Definición
 Figura 30 Esquema del proceso de producción de Gas Natural Sustituto GNS (Reimert, 2003) Capítulo 3 Azufre Producción de Ácido Sulfúrico 1.3. Producción de azufre y ácido sulfúrico 1.3.1. Proceso Frash.
Figura 30 Esquema del proceso de producción de Gas Natural Sustituto GNS (Reimert, 2003) Capítulo 3 Azufre Producción de Ácido Sulfúrico 1.3. Producción de azufre y ácido sulfúrico 1.3.1. Proceso Frash.
Una aleación es una mezcla homo génea, de propiedades metálicas, que está compuesta de dos o más elementos, de los cuales, al menos uno es un metal.
 Una aleación es una mezcla homo génea, de propiedades metálicas, que está compuesta de dos o más elementos, de los cuales, al menos uno es un metal. Las aleaciones están constituidas por elementos metálicos:
Una aleación es una mezcla homo génea, de propiedades metálicas, que está compuesta de dos o más elementos, de los cuales, al menos uno es un metal. Las aleaciones están constituidas por elementos metálicos:
MATERIALES DE LA CORTEZA TERRESTRE: MINERALES
 MATERIALES DE LA CORTEZA TERRESTRE: MINERALES CONTENIDO Minerales: componentes básicos b de las rocas. Composición n de los minerales. Estructura de los minerales. Propiedades físicas f de los minerales.
MATERIALES DE LA CORTEZA TERRESTRE: MINERALES CONTENIDO Minerales: componentes básicos b de las rocas. Composición n de los minerales. Estructura de los minerales. Propiedades físicas f de los minerales.
Cambios en la Materia. Sra. Anlinés Sánchez Otero
 Cambios en la Materia Sra. Anlinés Sánchez Otero Cambios en la Materia Cambios Físicos Químicos Cambios Físicos Alteran la sustancia sin modificar su composición. Se utilizan para separar mezclas e identificar
Cambios en la Materia Sra. Anlinés Sánchez Otero Cambios en la Materia Cambios Físicos Químicos Cambios Físicos Alteran la sustancia sin modificar su composición. Se utilizan para separar mezclas e identificar
DETERMINACIÓN DE PUNTO DE FUSIÓN
 DETERMINACIÓN DE PUNTO DE FUSIÓN La pureza e identidad de una sustancia orgánica puede quedar establecida cuando sus constantes físicas (punto de fusión, punto de ebullición, color, densidad, índice de
DETERMINACIÓN DE PUNTO DE FUSIÓN La pureza e identidad de una sustancia orgánica puede quedar establecida cuando sus constantes físicas (punto de fusión, punto de ebullición, color, densidad, índice de
ACTIVIDAD DE INTERPRETASCION EN LA MEDICION
 1 ACTIVIDAD DE INTERPRETASCION EN LA MEDICION 1. El sulfuro de hierro es una sustancia sólida a temperatura ambiente y está compuesta de hierro y azufre. Estas sustancias tienen las siguientes propiedades:
1 ACTIVIDAD DE INTERPRETASCION EN LA MEDICION 1. El sulfuro de hierro es una sustancia sólida a temperatura ambiente y está compuesta de hierro y azufre. Estas sustancias tienen las siguientes propiedades:
Química General I. Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Escuela de Química Departamento de Química General
 Química General I Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Escuela de Química Departamento de Química General Química: el estudio del cambio Copyright The McGraw-Hill
Química General I Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Escuela de Química Departamento de Química General Química: el estudio del cambio Copyright The McGraw-Hill
Química. Tema 2. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Química Tema 2 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Contenido: Tema 2. Materia y energía Átomos y moléculas Propiedades extensivas e intensivas Estado
Química Tema 2 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Contenido: Tema 2. Materia y energía Átomos y moléculas Propiedades extensivas e intensivas Estado
LOS MINERALES Y LAS ROCAS
 BIOLOGÍA Y GEOLOGÍA (1º ESO) ADAPTACIÓN CURRICULAR LOS MINERALES Y LAS ROCAS Nombre: Curso: 1D.ESO En esta unidad vamos a estudiar: 1 1. Qué son los minerales? 2. Propiedades de los minerales 3. Qué son
BIOLOGÍA Y GEOLOGÍA (1º ESO) ADAPTACIÓN CURRICULAR LOS MINERALES Y LAS ROCAS Nombre: Curso: 1D.ESO En esta unidad vamos a estudiar: 1 1. Qué son los minerales? 2. Propiedades de los minerales 3. Qué son
La infinidad de cosas que nos rodean están constituidas de pequeñas partículas en movimiento.
 La infinidad de cosas que nos rodean están constituidas de pequeñas partículas en movimiento. Estas partículas no las podemos ver con nuestros ojos, pero las podemos imaginar así De los materiales que
La infinidad de cosas que nos rodean están constituidas de pequeñas partículas en movimiento. Estas partículas no las podemos ver con nuestros ojos, pero las podemos imaginar así De los materiales que
Obtención de hierro. Hematites (Fe2O3) Magnetita (Fe3O4) Siderita (FeCO3) Limonita (Fe2O3.H2O) Pirita (FeS2)
 Obtención de hierro Alrededor de nosotros hay numerosos objetos de hierro, acero o alguna otra aleación metálica que contiene hierro. Por lo tanto es poco probable que alguien no conozca sobre este metal.
Obtención de hierro Alrededor de nosotros hay numerosos objetos de hierro, acero o alguna otra aleación metálica que contiene hierro. Por lo tanto es poco probable que alguien no conozca sobre este metal.
Nombre de la signatura Óptica de Cristales Naturales. 3 er curso / 1 grupo
 Universidad de Murcia Curso Académico 2009/2010 Escuela de Óptica Diplomatura de Óptica y Optometría 1-Identificación 1.1. De la asignatura Nombre de la signatura Óptica de Cristales Naturales Código 9I0
Universidad de Murcia Curso Académico 2009/2010 Escuela de Óptica Diplomatura de Óptica y Optometría 1-Identificación 1.1. De la asignatura Nombre de la signatura Óptica de Cristales Naturales Código 9I0
PRIMERA CLASE: Definiciones Definición grupal Historia del material Estado del material Métodos de obtención Propiedades Generales Video
 ALUMINIO 2010 PRIMERA CLASE: Definiciones Definición grupal Historia del material Estado del material Métodos de obtención Propiedades Generales Video DEFINICION GRUPAL Elemento químico de número atómico
ALUMINIO 2010 PRIMERA CLASE: Definiciones Definición grupal Historia del material Estado del material Métodos de obtención Propiedades Generales Video DEFINICION GRUPAL Elemento químico de número atómico
Tema 3. Reacciones químicas
 Tema 3. Reacciones químicas 1. La respiración de los seres vivos Para mantener vivo tu organismo y realizar las funciones propias de la vida diaria, tu cuerpo consume alimentos. En el proceso de digestión,
Tema 3. Reacciones químicas 1. La respiración de los seres vivos Para mantener vivo tu organismo y realizar las funciones propias de la vida diaria, tu cuerpo consume alimentos. En el proceso de digestión,
Igual número de cationes y aniones. Ejemplos: cloruro de sodio (NaCl), cloruro de cesio (CsCl), blenda (ZnS), etc.
 6. MATERIALES CERÁMICOS 6.1 Estructura de los cerámicos Enlace atómico: parcial o totalmente iónico Iones metálicos: cationes (ceden sus electrones, +), aniones (aceptan electrones, - ). Estructuras cristalinas,
6. MATERIALES CERÁMICOS 6.1 Estructura de los cerámicos Enlace atómico: parcial o totalmente iónico Iones metálicos: cationes (ceden sus electrones, +), aniones (aceptan electrones, - ). Estructuras cristalinas,
A continuación tienes unas imágenes de minerales y el modelo cristalográfico que representa su estructura y su composición.
 Minerales Actividad 1 Recuerda Un mineral es una sustancia sólida, natural e inorgánica que se ha originado en unas condiciones de presión y temperatura determinadas. Los minerales poseen una composición
Minerales Actividad 1 Recuerda Un mineral es una sustancia sólida, natural e inorgánica que se ha originado en unas condiciones de presión y temperatura determinadas. Los minerales poseen una composición
Qué es el vidrio? Material amorfo obtenido
 Qué es el vidrio? Material amorfo obtenido por enfriamiento de una masa fundida, cualquiera que sea su composición química y la zona de temperatura en la que tenga lugar su solidificación Debido al aumento
Qué es el vidrio? Material amorfo obtenido por enfriamiento de una masa fundida, cualquiera que sea su composición química y la zona de temperatura en la que tenga lugar su solidificación Debido al aumento
LOS ESTADOS DE LA MATERIA
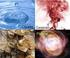 LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA
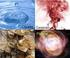 LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
Técnicas Fundamentales de Chocolatería EL TEMPERADO. Chef Gabriela Castillo
 Técnicas Fundamentales de Chocolatería EL TEMPERADO Chef Gabriela Castillo Temperar Chocolate Todo el chocolate que se usará para cubrir productos, bombones moldados, ganache, entre otros debe ser temperado.
Técnicas Fundamentales de Chocolatería EL TEMPERADO Chef Gabriela Castillo Temperar Chocolate Todo el chocolate que se usará para cubrir productos, bombones moldados, ganache, entre otros debe ser temperado.
Tiempo (minutos) Temperatura (ºC)
 EXAMEN FINAL 3º ESO. FÍSICA Y QUÍMICA. 1.- Al calentar un cierto sólido se ha obtenido la siguiente tabla de datos: Tiempo (minutos) 0 2 4 6 10 12 16 18 20 Temperatura (ºC) -5 0 5 10 20 20 20 25 30 Representa
EXAMEN FINAL 3º ESO. FÍSICA Y QUÍMICA. 1.- Al calentar un cierto sólido se ha obtenido la siguiente tabla de datos: Tiempo (minutos) 0 2 4 6 10 12 16 18 20 Temperatura (ºC) -5 0 5 10 20 20 20 25 30 Representa
TEMA 3: DIAGRAMAS DE EQUILIBRIO
 TEMA 3: DIAGRAMAS DE EQUILIBRIO 1.- Aleaciones Características Los metales puros tienen poca aplicación en la industria. La mayoría de ellos se combinan con otros metales o no metales para mejorar sus
TEMA 3: DIAGRAMAS DE EQUILIBRIO 1.- Aleaciones Características Los metales puros tienen poca aplicación en la industria. La mayoría de ellos se combinan con otros metales o no metales para mejorar sus
3. El sistema periódico de los elementos. 3. El sistema periódico de los elementos. 3. El sistema periódico de los elementos
 3. El sistema periódico de los elementos Clasificación de los elementos químicos en el siglo XIX: los químicos de la época tenían una idea vaga de los átomos; no conocían p + ni e -. Clasificaban los elementos
3. El sistema periódico de los elementos Clasificación de los elementos químicos en el siglo XIX: los químicos de la época tenían una idea vaga de los átomos; no conocían p + ni e -. Clasificaban los elementos
Los refractarios están compuestos principalmente de óxidos o compuestos como carburo de silicio que son estables a temperaturas elevadas.
 ASTM: define a los refractarios como materiales, generalmente no metálicos, utilizados para permanecer a altas temperaturas que proporcionan el revestimiento de hornos y reactores de alta temperatura.
ASTM: define a los refractarios como materiales, generalmente no metálicos, utilizados para permanecer a altas temperaturas que proporcionan el revestimiento de hornos y reactores de alta temperatura.
La materia y los cambios químicos 4. Sustancias puras y mezclas
 4. Sustancias puras y mezclas Materia Sustancias puras Formadas por un único tipo de componente Mezclas Formada por dos o más sustancias puras Elementos Formados por la misma clase de átomos Compuestos
4. Sustancias puras y mezclas Materia Sustancias puras Formadas por un único tipo de componente Mezclas Formada por dos o más sustancias puras Elementos Formados por la misma clase de átomos Compuestos
Guía del Curso Especialista en Tasaciones de Gemología y Joyería
 Guía del Curso Especialista en Tasaciones de Gemología y Joyería Modalidad de realización del curso: Titulación: A distancia y Online Diploma acreditativo con las horas del curso OBJETIVOS La gemología
Guía del Curso Especialista en Tasaciones de Gemología y Joyería Modalidad de realización del curso: Titulación: A distancia y Online Diploma acreditativo con las horas del curso OBJETIVOS La gemología
También existen en pequeñas proporciones gases como neón, kriptón, helio, xenón, hidrógeno, metano, etc.
 El aire es una mezcla de gases que constituye la atmósfera. CARACTERÍSTICAS - No presenta color ni olor. - Posee peso, aproximadamente: 1,3g por litro, está relacionado a la gravedad terrestre. - Por acción
El aire es una mezcla de gases que constituye la atmósfera. CARACTERÍSTICAS - No presenta color ni olor. - Posee peso, aproximadamente: 1,3g por litro, está relacionado a la gravedad terrestre. - Por acción
Estequiometría II. Química General I Lic. Oswaldo Martínez
 Estequiometría II Química General I 2012 Lic. Oswaldo Martínez Reactivo limitante Cuando se efectúa una reacción, los reactivos no están presentes en cantidades estequiométricas necesariamente, es decir,
Estequiometría II Química General I 2012 Lic. Oswaldo Martínez Reactivo limitante Cuando se efectúa una reacción, los reactivos no están presentes en cantidades estequiométricas necesariamente, es decir,
El uso de fertilizantes sintéticos, los cultivos agrícolas y la quema de carbón y petróleo han duplicado el ritmo al cual el
 ( ) La diferencia de temperatura de las distintas fracciones ( ) La diferencia de densidad de los distintos hidrocarburos que forman las fracciones ( ) La solubilidad de cada una de las fracciones 5 El
( ) La diferencia de temperatura de las distintas fracciones ( ) La diferencia de densidad de los distintos hidrocarburos que forman las fracciones ( ) La solubilidad de cada una de las fracciones 5 El
Son las fuerzas que mantienen unidos a los átomos entre sí para formar moléculas o cristales que son más estables que los átomos por separados..
 ENLACE QUÍMICO Son las fuerzas que mantienen unidos a los átomos entre sí para formar moléculas o cristales que son más estables que los átomos por separados.. Son de tipo eléctrico. Al formarse un enlace
ENLACE QUÍMICO Son las fuerzas que mantienen unidos a los átomos entre sí para formar moléculas o cristales que son más estables que los átomos por separados.. Son de tipo eléctrico. Al formarse un enlace
Métodos de separación de sistemas materiales sencillos
 Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
MATERIALES DE USO TÉCNICO V. EL VIDRIO
 MATERIALES DE USO TÉCNICO V. EL VIDRIO EL VIDRIO: El vidrio es un material inorgánico duro, frágil, transparente y amorfo que se encuentra en la naturaleza aunque también puede ser producido por el hombre.
MATERIALES DE USO TÉCNICO V. EL VIDRIO EL VIDRIO: El vidrio es un material inorgánico duro, frágil, transparente y amorfo que se encuentra en la naturaleza aunque también puede ser producido por el hombre.
PROGRAMA OFICIAL DE POSGRADO EN INGENIERÍA DEL AGUA Y DEL
 PROGRAMA OFICIAL DE POSGRADO EN INGENIERÍA DEL AGUA Y DEL TERRENO MÓDULO I.-INSTRUMENTACIÓN Y MÉTODOS DE ANÁLISIS QUÍMICO La Digestión como Método Químico de Extracción de Metales Pesados Ponente: Ángel
PROGRAMA OFICIAL DE POSGRADO EN INGENIERÍA DEL AGUA Y DEL TERRENO MÓDULO I.-INSTRUMENTACIÓN Y MÉTODOS DE ANÁLISIS QUÍMICO La Digestión como Método Químico de Extracción de Metales Pesados Ponente: Ángel
Crecimiento de Cristales de Sulfato de Cobre (II) pentahidratado CuSO 4 5H 2 O
 Crecimiento de Cristales de Sulfato de Cobre (II) pentahidratado CuSO 4 5H 2 O Materiales Hervidor de vidrio de ½ litro Cuchara metálica de mango largo 500 g de sulfato de cobre comercial Frasco de vidrio
Crecimiento de Cristales de Sulfato de Cobre (II) pentahidratado CuSO 4 5H 2 O Materiales Hervidor de vidrio de ½ litro Cuchara metálica de mango largo 500 g de sulfato de cobre comercial Frasco de vidrio
LAS ROCAS ÍGNEAS. Ignis= Fuego
 Ignis= Fuego LAS ROCAS ÍGNEAS Las rocas ígneas se originan por la cristalización del magma fundido e incandescente, que al ascender a la superficie terrestre se enfría y consolida. Magma LAS ROCAS ÍGNEAS
Ignis= Fuego LAS ROCAS ÍGNEAS Las rocas ígneas se originan por la cristalización del magma fundido e incandescente, que al ascender a la superficie terrestre se enfría y consolida. Magma LAS ROCAS ÍGNEAS
LA MATERIA Y SU DIVERSIDAD
 LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
La geosfera. Biología y Geología 1.º ESO
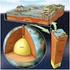 La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Biología y Geología 1.º ESO 2 Las capas de la geosfera Corteza continental Más de
La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Biología y Geología 1.º ESO 2 Las capas de la geosfera Corteza continental Más de
TEMA 2. CERAMICAS TRADICIONALES
 TEMA 2. CERAMICAS TRADICIONALES ESQUEMA: - Porcelanas - Esteatitas y Cordieritas 1 Porcelanas. Fabricación Barros como la kaolinita, silicato de aluminio hidratado: Al 2.2SiO 2.2H 2 O A 600ºC se pierde
TEMA 2. CERAMICAS TRADICIONALES ESQUEMA: - Porcelanas - Esteatitas y Cordieritas 1 Porcelanas. Fabricación Barros como la kaolinita, silicato de aluminio hidratado: Al 2.2SiO 2.2H 2 O A 600ºC se pierde
Rocas Ígneas. Introducción
 Rocas Ígneas Introducción Las rocas ígneas constituyen la mayor parte de la Corteza Terrestre. De hecho, con la excepción del Núcleo Exterior líquido, la porción sólida restante de nuestro planeta es básicamente
Rocas Ígneas Introducción Las rocas ígneas constituyen la mayor parte de la Corteza Terrestre. De hecho, con la excepción del Núcleo Exterior líquido, la porción sólida restante de nuestro planeta es básicamente
Práctica 4 y 5 Propiedades periódicas
 1 Nombres de los integrantes: Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 4 y 5 Propiedades periódicas Problema 1 Qué comportamiento
1 Nombres de los integrantes: Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 4 y 5 Propiedades periódicas Problema 1 Qué comportamiento
TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
Materiales Modernos «Cerámicas»
 Universidad Nacional Autónoma de Honduras del Valle de Sula Departamento de Química Materiales Modernos «Cerámicas» Asignatura: Química Inorgánica II Catedrática: Lic. Marina Sánchez Alumno Eli Francisco
Universidad Nacional Autónoma de Honduras del Valle de Sula Departamento de Química Materiales Modernos «Cerámicas» Asignatura: Química Inorgánica II Catedrática: Lic. Marina Sánchez Alumno Eli Francisco
METALES Y ALEACIONES. 1. Calcula la concentración de carbono en un acero que tiene 1200 Kg de hierro puro y 8,5 Kg de carbono. Solución: 0,70% de C
 METALES Y ALEACIONES 1. Calcula la concentración de carbono en un acero que tiene 1200 Kg de hierro puro y 8,5 Kg de carbono. Solución: 0,70% de C 2. Tenemos 2000 kg de acero, con una concentración del
METALES Y ALEACIONES 1. Calcula la concentración de carbono en un acero que tiene 1200 Kg de hierro puro y 8,5 Kg de carbono. Solución: 0,70% de C 2. Tenemos 2000 kg de acero, con una concentración del
La geosfera. La geosfera. Biología y Geología 1.º ESO
 La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Oxford University Press España, S. A. Biología y Geología 1.º ESO 2 Las capas de
La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Oxford University Press España, S. A. Biología y Geología 1.º ESO 2 Las capas de
MÉTODOS Y MATERIALES VI. MÉTODOS Y MATERIALES
 VI. MÉTODOS Y MATERIALES VI. MÉTODOS Y MATERIALES MÉTODOS Y MATERIALES 6.1. MATERIALES Los materiales fueron: ÿ 3 tipos de arena - sílica, provenientes de procesos diferentes formadas, por silicatos, bentonita
VI. MÉTODOS Y MATERIALES VI. MÉTODOS Y MATERIALES MÉTODOS Y MATERIALES 6.1. MATERIALES Los materiales fueron: ÿ 3 tipos de arena - sílica, provenientes de procesos diferentes formadas, por silicatos, bentonita
UNAM Facultad de Química Curso Intersemestral de Química General 1 Grupo 2 COLECCIÓN DE EJERCICIOS UNIDAD 1
 UNAM Facultad de Química Curso Intersemestral de Química General 1 Grupo 2 COLECCIÓN DE EJERCICIOS UNIDAD 1 1. Escribe la fórmula o el nombre de los siguientes compuestos, según se pide: i. Cromato de
UNAM Facultad de Química Curso Intersemestral de Química General 1 Grupo 2 COLECCIÓN DE EJERCICIOS UNIDAD 1 1. Escribe la fórmula o el nombre de los siguientes compuestos, según se pide: i. Cromato de
Ciencias Naturales 7mo Grado Proyecto Nº 5 febrero 2016 Profesor Melvyn García. Qué entiendes por materia? Qué propiedades caracterizan la materia?
 Ciencias Naturales 7mo Grado Proyecto Nº 5 febrero 2016 Profesor Melvyn García Qué entiendes por materia? Qué propiedades caracterizan la materia? Qué lograrás en este propósito 1? Analizar el concepto
Ciencias Naturales 7mo Grado Proyecto Nº 5 febrero 2016 Profesor Melvyn García Qué entiendes por materia? Qué propiedades caracterizan la materia? Qué lograrás en este propósito 1? Analizar el concepto
