Óxido de hierro(iii)
|
|
|
- Jorge Maidana Vera
- hace 9 años
- Vistas:
Transcripción
1 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número de átomos de oxígeno. Óxidos no metálicos: combinación de un no metal con el oxígeno. CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 Fórmula general: X no m Óxidos metálicos: combinación de un metal con el oxígeno. Fe 2 O 3 ; Li 2 O ; CaO ; Ag 2 O ; Al 2 O 3 N os de oxidación O : - 2 Metales: el suyo No metales: números de oxidación positivos Formulación: Compuesto nombrado según la nomenclatura sistemática: Trióxido de dihierro Nombre del elemento Prefijo numeral que indica el número de oxígenos Prefijo numeral que indica el número de átomos del elemento Fe 2 O 3 El elemento se escribe a la izquierda El oxígeno, como elemento más electronegativo, se escribe a la derecha Compuesto nombrado según la nomenclatura de Stock: Óxido de hierro(iii) Palabra "óxido" Fe 2 O 3 Nombre del metal con su número de oxidación en números romanos y entre paréntesis (si tiene varios). El número de oxidación del oxígeno (sin signo) se coloca como subíndice del metal. El número de oxidación del metal (sin signo) se coloca como subíndice del oxígeno Si los subíndices son divisibles por un mismo número es obligatorio simplificar. 1
2 ÓXIDOS Cuando los elementos que se combinan con el oxígeno tienen estado de oxidación fijo (alcalinos, alcalino-térreos, Ag, Zn, Al... etc), está permitido omitir los prefijos numerales (nomenclatura sistemática) o el número de oxidación escrito entre paréntesis (nomenclatura de Stock) en el nombre del óxido correspondiente, ya que como forman un único compuesto no existe ninguna ambigüedad: Óxido de sodio, óxido de calcio, óxido de plata... etc. En estos casos se debe tener especial cuidado a la hora de escribir la fórmula, ya que se debe tener en cuenta el estado de oxidación del elemento y formular el óxido correspondiente cruzando, como subíndices, los correspondientes números de oxidación. Si los subíndices resultantes son divisibles por un mismo número es obligatorio simplificar. Óxido de calcio El calcio es un metal alcalino-térreo con número de oxidación fijo: +2 Ca 2 O 2 Simplificar subíndices CaO El número de oxidación del oxígeno (sin signo) se coloca como subíndice del calcio. El número de oxidación del calcio (sin signo) se coloca como subíndice del oxígeno Nomenclatura: SO 2 Palabra óxido Solución (sistemática): Dióxido de azufre Prefijo numeral que indica el número de oxígenos. Nombre del elemento. Si hay un solo átomo del elemento no se pone el prefijo mono. Solución (Stock): Palabra óxido Óxido de azufre(iv) Nombre del elemento. Estado de oxidación entre paréntesis. Para obtener el estado de oxidación recordar que la suma algebraica de los estados de oxidación debe ser cero. Cuando el elemento tenga un único estado de oxidación se puede nombrar sin especificar el estado de oxidación entre paréntesis o sin poner ningún prefijo numeral, ya que el óxido es único: Na 2 O: Monóxido de disodio u óxido de sodio 2
3 PERÓXIDOS Los peróxidos son combinaciones binarias de un metal (generalmente alcalino o alcalino-térreo) con el grupo O 2 2-, grupo peróxido. El nombre de estos compuestos siempre incluye la palabra peróxido. Al agua oxigenada, o peróxido de hidrógeno, es el más conocido de esta clase de compuestos. El agua oxigenada se descompone con cierta facilidad dando oxígeno: 2 H 2 O > 2 H 2 O + O 2 BaO 2 ; CaO 2 ; Li 2 O 2 ;Ag 2 O 2 ;Na 2 O 2 ; Hg 2 O 2 Fórmula general: X no 2 La fórmula es simplificable, siempre que se respete la agrupación (O 2 ) N os de oxidación O : - 1 Metales: el suyo Nomenclatura: Peróxido de sodio Grupo peróxido O 2 2- a la derecha Peróxido de bario Metal a la izquierda Metal a la izquierda Na 2 O 2 Intercambiar n os de oxidación (sin signo). No es simplificable, ya que si dividimos los subíndices por dos, desaparecería la agrupacíón (O 2 ) Grupo peróxido O 2 2- a la derecha Truco para formular peróxidos: 1. Formular el óxido: Na Añadir un oxígeno más: Na 2 O 2 Tener en cuenta que no se puede simplificar si desaparece el grupo (O 2) Ba 2 (O 2 ) 2 = Ba 2 O 4 = BaO 2 Intercambiar n os de oxidación (sin signo). Es simplificable, ya que si dividimos los subíndices por dos sigue presente la agrupación (O 2 ) Nomenclatura: K 2 O 2 Palabra peróxido Nombre del elemento Peróxido de potasio 1
4 HIDRUROS Los hidruros son combinaciones de los metales con el hidrógeno. El nombre de estos compuestos siempre incluye la palabra hidruro que puede estar precedida de prefijos numerales indicadores del número de átomos de hidrógeno. AlH 3 ; LiH; CuH Fórmula general: X H m KH ; CaH 2 ; ZnH 2 N os de oxidación Formulación: Compuesto nombrado según la nomenclatura sistemática: H : - 1 Metales: el suyo Trihidruro de cobalto El hidrógeno en los hidruros funciona con -1. Esto nos indica que es más electronegativo que los metales. Por tanto, al escribir la fórmula, debe situarse a la derecha. Prefijo numeral que indica el número de hidrógenos Nombre del elemento CoH 3 El metal se escribe a la izquierda El hidrógeno, que es más electronegativo que los metales, se escribe a la derecha Compuesto nombrado según la nomenclatura de Stock: Hidruro de cobalto(iii) Prefijo numeral que indica el número de hidrógenos Nombre del metal con su número de oxidación en números romanos y entre paréntesis (si tiene varios). No dejar espacio entre el paréntesis y el nombre del metal. CoH 3 El número de oxidación del hidrógeno (sin signo) se coloca como subíndice del metal (al ser 1, se suprime) El número de oxidación del metal (sin número) se coloca como subíndice del oxígeno 1
5 HIDRUROS Cuando los elementos que se combinan con el hidrógeno tienen estado de oxidación fijo (alcalinos, alcalino-térreos, Ag, Zn, Al... etc), está permitido omitir los prefijos numerales en el nombre del hidruro correspondiente, ya que como forman un único compuesto no existe ninguna ambigüedad: Hidruro de sodio, hidruro de calcio, hidruro de plata... etc. En estos casos se debe tener especial cuidado a la hora de escribir la fórmula, ya que se debe tener en cuenta el estado de oxidación del elemento y formular el hidruro correspondiente cruzando, como subíndices, los correspondientes números de oxidación. Hidruro de aluminio El aluminio es un metal con número de oxidación fijo: +3 AlH 3 El número de oxidación del hidrógeno (sin signo) se coloca como subíndice del aluminio (al ser 1 se omite) El número de oxidación del aluminio (sin signo) se coloca como subíndice del hidrógeno. Nomenclatura: MgH 2 Palabra hidruro Solución (sistemática): Prefijo numeral que indica el número de hidrógenos Dihidruro de magnesio Nombre del metal Cuando el metal tenga un único estado de oxidación (como en este caso) se puede nombrar sin poner ningún prefijo numeral ya que el hidruro es único. Ejemplo: MgH 2 : Dihidruro de magnesio o hidruro de magnesio. Solución (Stock): Hidruro de magnesio Palabra "hidruro" Nombre del elemento. En esta caso no se especifica el estado de oxidación del metal, ya que es fijo. Las combinaciones binarias del hidrógeno con los elementos carbonoideos y nitrogenoideos no se nombran como hidruros. Todos ellos tienen nombres especiales no sistemáticos: 2 CH 4 : Metano
6 HIDRUROS Los hidruros del boro merecen una mención aparte por sus características especiales. La especie BH 3 (borano), no existe. El hidruro más sencillo es el B 2 H 6, llamado diborano. Las recomendaciones de la IUPAC indican que el número de átomos de boro se indique con un prefijo multiplicador, poniendo entre paréntesis el número de átomos de hidrógeno con el número arábigo apropiado: B 2 H 6 diborano(6) B 4 H 10 tetarborano(10) Las combinaciones binarias del hidrógeno con los no metales del grupo de los anfígenos y halógenos no se consideran hidruros. El halógeno o anfígeno, como son más electronegativos que el hidrógeno, funcionan con el estado de oxidación negativo y deberán situarse a la derecha a la hora de escribir la fórmula. Se nombran terminando en URO el nombre del halógeno o anfígeno. Los cuatro son gases y cuando se disuelven en agua se comportan como ácidos (ácidos hidrácidos) por lo que también pueden nombrase con la palabra ácido-nombre del elementoterminación HIDRICO. HF : Fluoruro de hidrógeno o ácido fluorhídrico HCl : Cloruro de hidrógeno o ácido clorhídrico HBr : Bromuro de hidrógeno o ácido bromhídrico HI : Yoduro de hidrógeno o ácido yodhídrico H 2 S : Sulfuro de hidrógeno o ácido sulfhídrico 3
7 NO METAL - NO METAL Los no metales pueden combinarse entre sí para dar compuestos binarios. La terminación URO del nombre del no metal más electronegativo (que se escribirá a la derecha) es característica de estos compuestos. SF 6 ; PCl 3 ; CCl 4 Fórmula general: Y n X m SiCl 4 ; PCl 5 ; CS 2 N os de oxidación El elemento más electronegativo funcionará con el estado de oxidación negativo El elemento menos electronegativo funcionará con el estado de oxidación positivo Formulación: Hexafluoruro de azufre Subíndice del flúor Nombre del otro no metal La terminación URO indica el no metal más electronegativo SF 6 El elemento menos electronegativo se escribe a la izquierda El elemento más electronegativo (el terminado en URO) se escribe a la derecha. Nomenclatura: CCl 4 Nombre del elemento más electronegativo (situado a la derecha) terminado en URO Tetracloruro de carbono Prefijo numeral que indica el número de átomos del elemento Nombre del elemento menos electronegativo (situado a la izquierda) 1
8 NO METAL - METAL Las combinaciones binarias no metal - metal reciben el nombre de sales haloideas. Los no metales pertenecen al grupo de los halógenos y anfígenos. La terminación en URO del no metal es característica de estos compuestos. KBr ; Fe 2 S 3 ; AgCl Fórmula general: M n X m NaCl ; CaI 2 ; PbS 2 N os de oxidación El no metal como es el elemento más electronegativo funcionará con el estado de oxidación negativo. Metal: el suyo Formulación: Compuesto nombrado según la nomenclatura sistemática: Tricloruro de niquel Subíndice del cloro Nombre del metal Terminación característica NiCl 3 El metal se escribe a la izquierda El no metal (terminación URO) se escribe a la derecha. Compuesto nombrado según la nomenclatura de Stock: Cloruro de niquel(iii) Nombre del no metal terminado en URO NiCl 3 Nombre del metal con el estado de oxidación en números romanos y entre paréntesis. Si el metal tiene estado de oxidación fijo, se suprime. El metal se escribe a la izquierda. Como subíndice se coloca el número de oxidación del no metal. El no metal (terminación URO) se escribe a la derecha. Como subíndice se coloca el número de oxidación del metal. 1
9 NO METAL - METAL Cuando los metales que se combinan tienen estado de oxidación fijo (alcalinos, alcalino-térreos, Ag, Zn, Al... etc), está permitido omitir los prefijos numerales (nomenclatura sistemática) o el estado de oxidación (Stock) en el nombre del compuesto, ya que no existe ninguna ambigüedad: Cloruro de sodio, sulfuro de magnesio, cloruro de plata... etc. En estos casos se debe tener especial cuidado a la hora de formular. Se debe de tener en cuenta el estado de oxidación del metal y del no metal y formular el compuesto correspondiente cruzando, como subíndices, los correspondientes números de oxidación. Si los subíndices resultantes son divisibles por un mismo número es obligatorio simplificar. Cloruro de aluminio Nombre sin prefijos numerales (sistemática). Estado de oxidación del metal sin especificar entre paréntesis (Stock). AlCl 3 El número de oxidación del no metal (sin signo) se coloca como subíndice del aluminio (en este caso, al ser 1, se omite) El número de oxidación del aluminio (sin signo) se coloca como subíndice del no metal. Nomenclatura: PbS 2 No metal terminado en URO Solución (sistemática): Prefijo numeral que indica el número de átomos del no metal Solución (Stock): Disulfuro de plomo No metal terminado en URO Sulfuro de plomo(iv) Nombre del metal Cuando el elemento tenga un único estado de oxidación se puede nombrar sin poner ningún prefijo numeral ya que el compuesto es único. Tampoco se especifica el estado de oxidación entre paréntesis. Ejemplo: AgCl: monocloruro de plata o cloruro de plata. Nombre del metal con el estado de oxidación entre paréntesis. No dejar espacio entre el paréntesis y el nombre del metal. 2
10 RESUMEN Resumen combinaciones binarias Para formular: Identificar los dos elementos que se combinan (para saber cuáles son examina el nombre del compuesto). Situar el más electronegativo a la derecha (funcionará con el estado de oxidación negativo). Guiarse por los prefijos numerales o el estado de oxidación para colocar los subíndices. Tener especial cuidado cuando en el nombre no figuren prefijos numerales. En ese caso se trata de un compuesto de un elemento con un único estado de oxidación. Situar ambos elementos juntos e intercambiar estados de oxidación, simplificando si es posible. Algunos ejemplos: Cinco átomos de oxígeno (más electronegativo) Dos átomos de fósforo Combinación oxígeno-fósforo Óxido de fósforo(v) Número de oxidación del fósforo. Pentaóxido de difósforo oxígeno y fósforo P 2 O 5 No hay prefijos numerales. Tampoco se especifica el estado de oxidación del metal Obtener los subíndices cruzando los estados de oxidación de ambos. Óxido de plata oxígeno y plata Ag 2 O También es correcto el nombre sistemático monóxido de diplata. No hay prefijos numerales. No se especifica el estado de oxidación del metal. El H funciona con -1 El calcio tiene un único número de oxidación:+2 Hidruro de calcio hidrógeno y calcio CaH 2 También es correcto el nombre sistemático dihidruro de calcio 1
11 RESUMEN hidrógeno y oro Estado de oxidación del oro Tres átomos de hidrógeno (más electronegativo) Un átomo de oro Hidruro de oro(iii) Trihidruro de oro hidrógeno y oro AuH 3 Dos átomos de cloro (más electronegativo) Dicloruro de níquel cloro y níquel Un átomo de níquel NiCl 2 cloro y níquel Cloruro de níquel(ii) Estado de oxidación del níquel Tres átomos de azufre (más electronegativo) Dos átomos de hierro azufre y hierro Estado de oxidación del hierro Trisulfuro de dihierro Sulfuro de hierro(iii) azufre y hierro Fe 2 S 3 No hay prefijos numerales ni se especifica el estado de oxidación del metal El cloro como es más electronegativo funciona con -1 El magnesio tiene un único estado de oxidación: +2 Cloruro de magnesio cloro y magnesio MgCl 2 También es correcto el nombre sistemático dicloruro de magnesio 2
12 RESUMEN Resumen combinaciones binarias Para nombrar: Identificar los dos elementos que se combinan (para saber cuáles son examina la fórmula del compuesto) El más electronegativo estará situado a la derecha. Si el elemento situado a la derecha no es oxígeno, termina su nombre en uro. Si el elemento situado a la derecha es el oxígeno usa la palabra óxido. Indica el número de átomos de cada elemento mediante prefijos (sistemática). Recuerda que si hay un solo átomo del segundo elemento que se nombra no se pone el prefijo "mono". Si el elemento tiene varios estados de oxidación debes indicar entre paréntesis con cual de ellos funciona en el compuesto. Ten en cuenta que existen algunas excepciones: NH 3 : Amoniaco CH 4 : Metano H 2 S : Ácido sulfhídrico Las combinaciones de los halógenos con el hidrógeno que se pueden nombrar como ácidos: HF : Ácido fluorhídrico HCl :Ácido clorhídrico HBr: Ácido bromhídrico HI: Ácido yodhídrico Algunos ejemplos Un átomo de azufre y tres de oxígeno SO 3 Trióxido de azufre Óxido de azufre(vi) azufre y oxígeno Un átomo de zinc y uno de oxígeno ZnO oxígeno y zinc Monóxido de zinc Óxido de zinc Como el zinc tiene un único estado de oxidación (+2) en este caso es correcto nombrar sin prefijos numerales. Tampoco se pone el estado de oxidación entre paréntesis: óxido de zinc. 3
13 RESUMEN Un átomo de magnesio y dos de hidrógeno MgH 2 hidrógeno y magnesio Dihidruro de magnesio Hidruro de magnesio Como el magnesio tiene un único estado de oxidación (+2) en este caso es correcto nombrar sin prefijos numerales. Tampoco se pone el estado de oxidación entre paréntesis: hidruro de magnesio Un átomo de oro y uno de hidrógeno AuH Monohidruro de oro Hidruro de oro(i) hidrógeno y oro Un átomo de azufre y dos de sodio Na 2 S azufre y sodio Monosulfuro de disodio Sulfuro de sodio Como el sodio tiene un único estado de oxidación (+1) en este caso es correcto nombrar sin prefijos numerales. Tampoco se pone el estado de oxidación entre paréntesis: sulfuro de sodio. Un átomo de plomo y dos de yodo PbI 2 yodo y plomo Diyoduro de plomo Yoduro de plomo(ii) 4
14 RESUMEN Apuntes creados por el I.E.S. La Magdalena Avilés. Asturias 5
Trióxido de dihierro
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
Óxido de hierro(iii)
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
Trióxido de dihierro
 COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
Óxido de hierro (III)
 COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
Trióxido de dihierro
 OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1) excepto halógenos X no m Metal + Oxígeno = Óxido metálico Fe 2 O 3 ; Li 2 O ; CaO ; Ag
OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1) excepto halógenos X no m Metal + Oxígeno = Óxido metálico Fe 2 O 3 ; Li 2 O ; CaO ; Ag
Trióxido de dihierro
 Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA 0. Introducción. Existen tres tipos de nomenclaturas que nos permiten nombrar los compuestos químicos inorgánicos: A. Nomenclatura Sistemática (normas propuestas por la Unión
FORMULACIÓN Y NOMENCLATURA 0. Introducción. Existen tres tipos de nomenclaturas que nos permiten nombrar los compuestos químicos inorgánicos: A. Nomenclatura Sistemática (normas propuestas por la Unión
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (3.º ESO)
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA. Son aquellas sustancias que están formadas por átomos de la misma clase.
 FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA Elementos químicos Son aquellas sustancias que están formadas por átomos de la misma clase. Símbolos Dalton se inventó una serie de símbolos
FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA Elementos químicos Son aquellas sustancias que están formadas por átomos de la misma clase. Símbolos Dalton se inventó una serie de símbolos
NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES. Número de oxidación. + 1 Li, Na, K, Rb, Cs y Ag. +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd
 NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu y Hg +1, +3 Au +2, +3 Fe, Co, Ni
NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu y Hg +1, +3 Au +2, +3 Fe, Co, Ni
Compuestos binarios (combinaciones de dos elementos) HIDRUROS METÁLICOS= Metal - Hidrógeno. X H m. H : - 1 Metales: el suyo. FeH 3
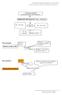 HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN (3.º ESO) Nomenclatura de compuestos binarios usando números de oxidación
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN Nomenclatura de compuestos binarios usando números de oxidación La nomenclatura de composición permite usar los números de oxidación para
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN Nomenclatura de compuestos binarios usando números de oxidación La nomenclatura de composición permite usar los números de oxidación para
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA
 EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA 1. Determina el número de oxidación del manganeso en los compuestos: MnO 2 Mn 2 O 3 2. Determina el número de oxidación del Cl en los compuestos: Cl 2 O 7 Cl 2
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA 1. Determina el número de oxidación del manganeso en los compuestos: MnO 2 Mn 2 O 3 2. Determina el número de oxidación del Cl en los compuestos: Cl 2 O 7 Cl 2
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
FORMULACION Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 FORMULACION Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y
FORMULACION Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y
1 HIDRUROS COMPUESTOS BINARIOS. Química Formulación y nomenclatura Adrián de la Torre Isidoro
 Química y nomenclatura Adrián de la Torre Isidoro Dependiendo del número de elementos que intervienen en un compuesto, estos se dividen en componentes binarios, sin tiene dos elementos; terciarios, si
Química y nomenclatura Adrián de la Torre Isidoro Dependiendo del número de elementos que intervienen en un compuesto, estos se dividen en componentes binarios, sin tiene dos elementos; terciarios, si
Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno:
 Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno: 1) Ácido clorhídrico 2) Sulfuro de hidrógeno 3) Estibano 4) Agua u oxidano 5) Trihidruro de fósforo 6) Hidruro de estaño(iv)
Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno: 1) Ácido clorhídrico 2) Sulfuro de hidrógeno 3) Estibano 4) Agua u oxidano 5) Trihidruro de fósforo 6) Hidruro de estaño(iv)
Trióxido de dihierro
 Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
1 FORMULACIÓN Y NOMENCLATURA QUÍMICA INORGÁNICA
 1 FRMULACIÓN Y NMENCLATURA QUÍMICA INRGÁNICA I 1 ELEMENTS Un elemento químico es la clase de átomos que tienen el mismo número atómico. Existen hasta 109 elementos químicos con los que se forma toda la
1 FRMULACIÓN Y NMENCLATURA QUÍMICA INRGÁNICA I 1 ELEMENTS Un elemento químico es la clase de átomos que tienen el mismo número atómico. Existen hasta 109 elementos químicos con los que se forma toda la
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
Formulación química inorgánica Compuestos binarios
 1/9 Los compuestos binarios son aquellos formados por dos elementos. A continuación se muestran las distintas combinaciones de dos elementos. Normas generales de formulación. Óxidos: Óxidos básicos y óxidos
1/9 Los compuestos binarios son aquellos formados por dos elementos. A continuación se muestran las distintas combinaciones de dos elementos. Normas generales de formulación. Óxidos: Óxidos básicos y óxidos
Trióxido de dihierro
 FORMULACIÓN QUÍMICA INORGÁNICA Combinaciones binarias (Combinaciones de dos elementos) OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1)
FORMULACIÓN QUÍMICA INORGÁNICA Combinaciones binarias (Combinaciones de dos elementos) OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1)
Lo primero que hay que conocer para formular y nombrar los compuestos químicos es el número de oxidación de cada elemento.
 Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO
 EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS METÁLICOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS METÁLICOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido
FORMULACIÓN INORGÁNICA. Departamento de Física y Química 3º ESO
 FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA I.B. Alonso de Covarrubias En química utilizamos fórmulas para representar elementos y compuestos. La IUPAC (Unión Internacional de Química Pura y Aplicada) es el
1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA I.B. Alonso de Covarrubias En química utilizamos fórmulas para representar elementos y compuestos. La IUPAC (Unión Internacional de Química Pura y Aplicada) es el
EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS DEL OXÍGENO 1.- Cl 2 O 7 2.- FeO 3.- N 2 O 4.- SO 3 1.- NOMBRA LOS SIGUIENTES COMPUESTOS: 6.- Br 2 O 7.- P 2 O 5 8.- CO 2 9.- I 2 O 5 5.-
EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS DEL OXÍGENO 1.- Cl 2 O 7 2.- FeO 3.- N 2 O 4.- SO 3 1.- NOMBRA LOS SIGUIENTES COMPUESTOS: 6.- Br 2 O 7.- P 2 O 5 8.- CO 2 9.- I 2 O 5 5.-
RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS CON OXÍGENO El oxígeno se combina con todos los elementos excepto con los gases nobles. En estos compuestos el oxígeno actúa
RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS CON OXÍGENO El oxígeno se combina con todos los elementos excepto con los gases nobles. En estos compuestos el oxígeno actúa
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
REPASO DE FORMULACIÓN INORGÁNICA
 REPASO DE FORMULACIÓN INORGÁNICA 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. Br 2 O 7. P 2 O 5 8. CO 2 9. I 2 O 5 10. MnO 2 11. Trióxido de dicromo 12. Óxido de nitrógeno (V) 13. Heptaóxido de dicloro
REPASO DE FORMULACIÓN INORGÁNICA 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. Br 2 O 7. P 2 O 5 8. CO 2 9. I 2 O 5 10. MnO 2 11. Trióxido de dicromo 12. Óxido de nitrógeno (V) 13. Heptaóxido de dicloro
SESIÓN 1 CÁLCULOS QUÍMICOS
 SESIÓN 1 CÁLCULOS QUÍMICOS I. CONTENIDOS: 1. Nomenclatura química. 2. atómica. 3. molecular. 4. Concepto mol. 5. El número de Avogadro. II. OBJETIVOS: Al término de la Sesión, el alumno: Recordará las
SESIÓN 1 CÁLCULOS QUÍMICOS I. CONTENIDOS: 1. Nomenclatura química. 2. atómica. 3. molecular. 4. Concepto mol. 5. El número de Avogadro. II. OBJETIVOS: Al término de la Sesión, el alumno: Recordará las
Indique el número de óxidos básicos y óxidos ácidos respectivamente en la siguiente tabla:
 EJERCICIO RESUELTO Ejercicio 1: Indique el número de óxidos básicos y óxidos ácidos respectivamente en la siguiente tabla: a) Fe 2 O 3 b) CO c) SO 3 d) CuO e) NO 2 f) Na 2 O g) MgO Solución: Comenzaremos
EJERCICIO RESUELTO Ejercicio 1: Indique el número de óxidos básicos y óxidos ácidos respectivamente en la siguiente tabla: a) Fe 2 O 3 b) CO c) SO 3 d) CuO e) NO 2 f) Na 2 O g) MgO Solución: Comenzaremos
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA 1. Valencia. 2. Combinaciones binarias del Oxígeno: Óxidos y peróxidos 3. Combinaciones binarias del Hidrógeno: Hidruros e Hidrácidos 4. Combinaciones binarias: sales haloideas y
FORMULACIÓN INORGÁNICA 1. Valencia. 2. Combinaciones binarias del Oxígeno: Óxidos y peróxidos 3. Combinaciones binarias del Hidrógeno: Hidruros e Hidrácidos 4. Combinaciones binarias: sales haloideas y
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Este libro se presenta para exponer, analizar y aplicar las reglas de formulación y nomenclatura recomendadas por la IUPAC para los compuestos inorgánicos,
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Este libro se presenta para exponer, analizar y aplicar las reglas de formulación y nomenclatura recomendadas por la IUPAC para los compuestos inorgánicos,
FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS.
 FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS. 1. ÓXIDOS. Son compuestos, formados por la unión del oxígeno y cualquier otro elemento de la tabla periódica (excepto los gases nobles que jamás
FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS. 1. ÓXIDOS. Son compuestos, formados por la unión del oxígeno y cualquier otro elemento de la tabla periódica (excepto los gases nobles que jamás
La IUPAC recomienda lo siguiente para formular los hidrácidos: Para los hidrácidos la nomenclatura tradicional y la sistemática coinciden:
 ACIDOS HIDRÁCIDOS: Son compuestos formados por HIDRÓGENO y un NO METAL de los grupos 6A y 7A. El hidrógeno presenta un estado de oxidación 1+ por lo que el no metal tomará un estado de oxidación negativo,
ACIDOS HIDRÁCIDOS: Son compuestos formados por HIDRÓGENO y un NO METAL de los grupos 6A y 7A. El hidrógeno presenta un estado de oxidación 1+ por lo que el no metal tomará un estado de oxidación negativo,
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA)
 FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
- Nomenclatura tradicional. Hoy está totalmente en desuso, pero es necesario conocerla para poder formular oxiácidos. La posibilidad de que un mismo
 NORMAS BÁSICAS SOBRE FORMULACIÓN - Se escribe siempre en primer lugar el símbolo del elemento (o grupo) que actúa con número de oxidación positivo, generalmente un metal y a continuación el símbolo del
NORMAS BÁSICAS SOBRE FORMULACIÓN - Se escribe siempre en primer lugar el símbolo del elemento (o grupo) que actúa con número de oxidación positivo, generalmente un metal y a continuación el símbolo del
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO
 EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Fórmula: primero se escribe el elemento menos electronegativo (orden decreciente: F, O, Cl, Br, I, S, Se, Te, H, N, P, As, Sb, C, Si, B )
 FORMULACIÓN INORGÁNICA Regla general para todos los compuestos: Fórmula: primero se escribe el elemento menos electronegativo (orden decreciente: F, O, Cl, Br, I, S, Se, Te, H, N, P, As, Sb, C, Si, B )
FORMULACIÓN INORGÁNICA Regla general para todos los compuestos: Fórmula: primero se escribe el elemento menos electronegativo (orden decreciente: F, O, Cl, Br, I, S, Se, Te, H, N, P, As, Sb, C, Si, B )
Formulación inorgánica
 Formulación inorgánica 1. Compuestos binarios con oxígeno (Óxidos) Combinaciones de cualquier elemento con el oxígeno. El elemento se coloca a la izquierda y el oxígeno a la derecha y se intercambian las
Formulación inorgánica 1. Compuestos binarios con oxígeno (Óxidos) Combinaciones de cualquier elemento con el oxígeno. El elemento se coloca a la izquierda y el oxígeno a la derecha y se intercambian las
TEMA 5.- Formulación y nomenclatura
 Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
FORMULA LOS SIGUIENTES COMPUESTOS. 1) Óxido crómico: CrO 3. 2) Trióxido de difósforo: P 2 O 3. 3) Óxido de cromo (III): Cr 2 O 3
 FORMULA LOS SIGUIENTES COMPUESTOS 1) Óxido crómico: CrO 3 2) Trióxido de difósforo: P 2 O 3 3) Óxido de cromo (III): Cr 2 O 3 4) Óxido de hierro (II): FeO 5) Pentaóxido de dinitrógeno: N 2 O 5 6) Óxido
FORMULA LOS SIGUIENTES COMPUESTOS 1) Óxido crómico: CrO 3 2) Trióxido de difósforo: P 2 O 3 3) Óxido de cromo (III): Cr 2 O 3 4) Óxido de hierro (II): FeO 5) Pentaóxido de dinitrógeno: N 2 O 5 6) Óxido
Ficha 1. CONCEPTOS BÁSICOS
 Ficha 1. CONCEPTOS BÁSICOS 1 4 LA TABLA PERIÓDICA Ejercicio 1. Las cosas están formadas a partir de: Protones Moléculas Elementos químicos Ejercicio 2. Los elementos químicos se representan ordenados en:
Ficha 1. CONCEPTOS BÁSICOS 1 4 LA TABLA PERIÓDICA Ejercicio 1. Las cosas están formadas a partir de: Protones Moléculas Elementos químicos Ejercicio 2. Los elementos químicos se representan ordenados en:
Metal y no. metal. sodio. cloruro de COMPUESTOS IES RIBERA DE CASTILLA. Óxidos. Peróxidos. que los binarios) Pág 1
 FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS BINARIOS Igual que todas las personas tenemos un nombre, también cada compuesto químico tiene el suyo. Es importante conocer la fórmula y el nombre de los compuestos
FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS BINARIOS Igual que todas las personas tenemos un nombre, también cada compuesto químico tiene el suyo. Es importante conocer la fórmula y el nombre de los compuestos
Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied Chemistry).
 4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
REPASO FORMULACIÓN INORGÁNICA 1
 REPASO FORMULACIÓN INORGÁNICA 1 IES TURANIANA Nombre: Fecha: RELACIÓN 1: ÓXIDOS Trióxido de azufre Dióxido de azufre Oxido de cobalto (II) Oxido de magnesio Oxido de estaño (II) Oxido de potasio Oxido
REPASO FORMULACIÓN INORGÁNICA 1 IES TURANIANA Nombre: Fecha: RELACIÓN 1: ÓXIDOS Trióxido de azufre Dióxido de azufre Oxido de cobalto (II) Oxido de magnesio Oxido de estaño (II) Oxido de potasio Oxido
1.ELEMENTOS QUÍMICOS: NOMBRES Y SÍMBOLOS
 1 1.ELEMENTOS QUÍMICOS: NOMBRES Y SÍMBOLOS Se denomina "elemento químico" a toda sustancia pura que no se puede descomponer en otras más sencillas. Sus nombres y símbolos son los vistos en el sistema periódico,
1 1.ELEMENTOS QUÍMICOS: NOMBRES Y SÍMBOLOS Se denomina "elemento químico" a toda sustancia pura que no se puede descomponer en otras más sencillas. Sus nombres y símbolos son los vistos en el sistema periódico,
TEMA 4: Formulación inorgánica
 TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
M m+ + X n- M n X m. Qué es formular un compuesto binario?
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Formulación y Nomenclatura
 Formulación y más metal NÚMEROS DE OXIDACIÓN DE LOS ELEMENTOS MÁS FRECUENTES: Hidrógeno (-1/+1) Niquel (+2/+3) Fósforo (-3/+3/+5) Litio (+1) Platino (+2/+4) Arsénico (-3/+3/+5) Sodio (+1) Cobre (+1/+2)
Formulación y más metal NÚMEROS DE OXIDACIÓN DE LOS ELEMENTOS MÁS FRECUENTES: Hidrógeno (-1/+1) Niquel (+2/+3) Fósforo (-3/+3/+5) Litio (+1) Platino (+2/+4) Arsénico (-3/+3/+5) Sodio (+1) Cobre (+1/+2)
EJERCICIOS DE FORMULACIÓN (QUÍMICA INORGÁNICA) EJERCICIOS POR GRUPOS DE COMPUESTOS. Óxidos metálicos
 EJERCICIOS DE FORMULACIÓN (QUÍMICA INORGÁNICA) EJERCICIOS POR GRUPOS DE COMPUESTOS Óxidos metálicos 1. Nombra los siguientes compuestos: 1. PbO 2 2. Ni 2 O 3 3. V 2 O 5 4. Cs 2 O 5. Bi 2 O 3 6. OsO 4 7.
EJERCICIOS DE FORMULACIÓN (QUÍMICA INORGÁNICA) EJERCICIOS POR GRUPOS DE COMPUESTOS Óxidos metálicos 1. Nombra los siguientes compuestos: 1. PbO 2 2. Ni 2 O 3 3. V 2 O 5 4. Cs 2 O 5. Bi 2 O 3 6. OsO 4 7.
Boletín de Actividades (VII) INICIACIÓN A LA FORMULACIÓN Y NOMENCLATURA INORGÁNICA. LiH --
 www.colegioelatabal.es/ciencias/ Boletín de Actividades (VII) INICIACIÓN A LA FORMULACIÓN Y NOMENCLATURA INORGÁNICA. 1. Formula y/o nombra las siguientes combinaciones binarias del hidrógeno: Fórmula N.
www.colegioelatabal.es/ciencias/ Boletín de Actividades (VII) INICIACIÓN A LA FORMULACIÓN Y NOMENCLATURA INORGÁNICA. 1. Formula y/o nombra las siguientes combinaciones binarias del hidrógeno: Fórmula N.
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA INTRODUCCIÓN. Las fórmulas representan a los compuestos químicos y constan de una agrupación de símbolos afectados de unos subíndices que nos indican la proporción en que
FORMULACIÓN QUÍMICA INORGÁNICA INTRODUCCIÓN. Las fórmulas representan a los compuestos químicos y constan de una agrupación de símbolos afectados de unos subíndices que nos indican la proporción en que
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
ísica y uímica FORMULACIÓN Y NOMENCLATURA Nombre Óxido de bario Óxido de sodio Óxido de plata Fórmula
 Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
FORMULACIÓN Y NOMENCLATURA
 1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales
 Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales 2 de 12 Tipo de compuesto Relaciona estos compuestos:
Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales 2 de 12 Tipo de compuesto Relaciona estos compuestos:
Número de oxidación. Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo
 FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos. 13 millones!!!
 La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
H, Li, Na, K, Rb, Cs, Fr 1. Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2. B, Al 3. N, P, As, Sb 1, 3, 5. F, Cl, Br, I 1, 3, 5, 7. C, Si, Ge, Sn, Pb 2, 4 O 2
 H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
Son compuestos binarios, resultan de la combinación de un metal más el oxígeno. Metal + Oxígeno =
 FUNCIÓN ÓXIDO BASICO U ÓXIDO Son compuestos binarios, resultan de la combinación de un metal más el oxígeno. Metal + Oxígeno = óxido NOMENCLATURA CLASICA.-Se nombra de acuerdo a: Primer caso: El no metal
FUNCIÓN ÓXIDO BASICO U ÓXIDO Son compuestos binarios, resultan de la combinación de un metal más el oxígeno. Metal + Oxígeno = óxido NOMENCLATURA CLASICA.-Se nombra de acuerdo a: Primer caso: El no metal
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
Ti: +,+,+ en los hidruros no metálicos. +,+ en los óxidos, hidróxidos, hidruros metálicos. Cr: +,+ en las sales binarias. Mn:
 Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
Trihidróxido de niquel
 COMBINACIONES TERNARIAS (4º ESO) HIDRÓXIDOS Los hidróxidos, aunque son combinaciones ternarias (tres elementos), se formulan y nombran como si fueran combinaciones binarias del ión (OH) - con metales.
COMBINACIONES TERNARIAS (4º ESO) HIDRÓXIDOS Los hidróxidos, aunque son combinaciones ternarias (tres elementos), se formulan y nombran como si fueran combinaciones binarias del ión (OH) - con metales.
11 Dióxido de carbono. 12 Trióxido de monoazufre. 13 Pentaóxido de difósforo. 14 Dióxido de monoselenio. 15 Dióxido de selenio. 16 Óxido de dimercurio
 1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
COMPUESTOS INORGÁNICOS
 COMPUESTOS INORGÁNICOS ELEMENTO METÁLICO NO METÁLICO con con metal oxígeno hidrógeno metal oxígeno hidrógeno ALEACIÓN ÓXIDO METÁLICO HIDRURO SAL HALOIDEA ÓXIDO NO METÁLICO ÁCIDO HIDRÁCIDO con H 2O con
COMPUESTOS INORGÁNICOS ELEMENTO METÁLICO NO METÁLICO con con metal oxígeno hidrógeno metal oxígeno hidrógeno ALEACIÓN ÓXIDO METÁLICO HIDRURO SAL HALOIDEA ÓXIDO NO METÁLICO ÁCIDO HIDRÁCIDO con H 2O con
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA 1. Elementos Químicos. 2. Valencia. 3. Combinaciones binarias del Oxígeno: Óxidos 4. Combinaciones binarias del Hidrógeno: Hidruros e Hidrácidos 5. Ácidos Oxácidos 6. Hidróxidos,
FORMULACIÓN INORGÁNICA 1. Elementos Químicos. 2. Valencia. 3. Combinaciones binarias del Oxígeno: Óxidos 4. Combinaciones binarias del Hidrógeno: Hidruros e Hidrácidos 5. Ácidos Oxácidos 6. Hidróxidos,
REACCIONES QUÍMICAS. Ocurren en la naturaleza. Se expresan por ECUACIONES QUÍMICAS
 REACCIONES QUÍMICAS Ocurren en la naturaleza Se expresan por ECUACIONES QUÍMICAS NaCl + AgNO 3 AgCl + NaNO 3 REACTIVOS PRODUCTOS ECUACIÓN QUÍMICA Estequiométrica (ecuación balanceada) Representar una reacción
REACCIONES QUÍMICAS Ocurren en la naturaleza Se expresan por ECUACIONES QUÍMICAS NaCl + AgNO 3 AgCl + NaNO 3 REACTIVOS PRODUCTOS ECUACIÓN QUÍMICA Estequiométrica (ecuación balanceada) Representar una reacción
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
QUÍMICA INORGÁNICA 3º E.S.O.
 QUÍMICA INORGÁNICA 3º E.S.O. Formulación y nomenclatura. Normas de la IUPAC (2005) 1 2 CONCEPTOS GENERALES 1. NORMAS PARA ESCRIBIR LAS FÓRMULAS Se escriben juntos los símbolos de los átomos, el más electronegativo
QUÍMICA INORGÁNICA 3º E.S.O. Formulación y nomenclatura. Normas de la IUPAC (2005) 1 2 CONCEPTOS GENERALES 1. NORMAS PARA ESCRIBIR LAS FÓRMULAS Se escriben juntos los símbolos de los átomos, el más electronegativo
1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 5. ESTRUCTURA DE LA MATERIA
 TEMA 5. ESTRUCTURA DE LA MATERIA - Cómo se combinan los átomos entre sí para formar moléculas y redes cristalinas? - Qué lenguaje utiliza la química? - Cuánto miden y cuánto pesan los átomos? - De qué
TEMA 5. ESTRUCTURA DE LA MATERIA - Cómo se combinan los átomos entre sí para formar moléculas y redes cristalinas? - Qué lenguaje utiliza la química? - Cuánto miden y cuánto pesan los átomos? - De qué
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
Compuestos Binarios- Óxidos-Hidruros-Hidrácidos-Sales Binarias. ÓXIDOS ( Metal/No Metal + O )
 Alcalinos + O Alcalino-Térreos + O Metales de Transición + O Térreos + O Carbonoideos + O ÓXIDOS ( Metal/No Metal + O ) Li 2 O monóxido de dilitio óxido de litio (I) Na 2 O monóxido de disodio óxido de
Alcalinos + O Alcalino-Térreos + O Metales de Transición + O Térreos + O Carbonoideos + O ÓXIDOS ( Metal/No Metal + O ) Li 2 O monóxido de dilitio óxido de litio (I) Na 2 O monóxido de disodio óxido de
ion hidrógeno Li + ion litio Mg 2+ ion cloruro F - ion fluoruro S 2- ion sulfuro H - ion hidruro P 3-
 I. IONES Conformados por uno o más átomos del mismo elemento, presentan carga positiva o MONOATÓMICOS: negativa. I.1 CATIONES: Presentan carga positiva. H + ion hidrógeno Li + ion litio Mg 2+ ion magnesio
I. IONES Conformados por uno o más átomos del mismo elemento, presentan carga positiva o MONOATÓMICOS: negativa. I.1 CATIONES: Presentan carga positiva. H + ion hidrógeno Li + ion litio Mg 2+ ion magnesio
M m+ + X n-! M n X m EJERCICIOS/ESTUDIO. Qué es formular un compuesto binario?
 EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
PROGRAMA TOTAL FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
3º de E.S.O. Física y Química Ejercicios de repaso para septiembre 2
 IES EL ESCORIAL 3º de ESO Física y Química Ejercicios de repaso para septiembre 2 Apellidos: Nombre: Curso: Fecha: 1 Indica para los siguientes científicos Dalton, Thomson, Rutherford y Bohr, sus descubrimientos
IES EL ESCORIAL 3º de ESO Física y Química Ejercicios de repaso para septiembre 2 Apellidos: Nombre: Curso: Fecha: 1 Indica para los siguientes científicos Dalton, Thomson, Rutherford y Bohr, sus descubrimientos
FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES. Número de oxidación. + 1 Li, Na, K, Rb, Cs y Ag
 1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
Trabajo para alumnos con el Ámbito Científico Matemático II de 3º ESO pendiente del curso anterior
 Trabajo para alumnos con el Ámbito Científico Matemático II de 3º ESO pendiente del curso anterior Los alumnos con ACM pendiente deberán realizar los siguientes ejercicios y entregarlos antes del día La
Trabajo para alumnos con el Ámbito Científico Matemático II de 3º ESO pendiente del curso anterior Los alumnos con ACM pendiente deberán realizar los siguientes ejercicios y entregarlos antes del día La
FORMULACIÓN INORGÁNICA. COMPUESTOS BINARIOS
 FORMULACIÓN INORGÁNICA. COMPUESTOS BINARIOS Frmular una sustancia cnsiste en escribir crrectamente su frmula. Nmbrar una sustancia cnsiste en asignarle su nmbre crrect atendiend a las características de
FORMULACIÓN INORGÁNICA. COMPUESTOS BINARIOS Frmular una sustancia cnsiste en escribir crrectamente su frmula. Nmbrar una sustancia cnsiste en asignarle su nmbre crrect atendiend a las características de
Para nombrar compuestos químicos según esta nomenclatura se utilizan los prefijos: MONO_, DI_, TRI_, TETRA_, PENTA_, HEXA_, HEPTA_...
 3. NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos
3. NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos
FORMULACIÓN EN QUÍMICA INORGÁNICA
 FRMULACIÓN EN QUÍMICA INRGÁNICA CMPUESTS BINARIS Y TERNARIS NMENCLATURA SISTEMÁTICA Y TRADICINAL NMENCLATURA SISTEMÁTICA Y TRADICINAL EJERCICIS DE APLICACIÓN www.lamanzanadenewton.com LA FRMULACIÓN INRGÁNICA
FRMULACIÓN EN QUÍMICA INRGÁNICA CMPUESTS BINARIS Y TERNARIS NMENCLATURA SISTEMÁTICA Y TRADICINAL NMENCLATURA SISTEMÁTICA Y TRADICINAL EJERCICIS DE APLICACIÓN www.lamanzanadenewton.com LA FRMULACIÓN INRGÁNICA
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
1. Completa (escribe también el nombre del compuesto con la nomenclatura que falta): FÓRMULA NOMBRE FÓRMULA NOMBRE. HCl. Ácido selenhídrico
 1. Completa (escribe también el nombre del compuesto con la nomenclatura que falta): FÓRMULA NOMBRE FÓRMULA NOMBRE BH 3 HCl Hidruro de cinc Amoníaco Hidruro de hierro (III) Dihidruro de estaño AlH 3 NiH
1. Completa (escribe también el nombre del compuesto con la nomenclatura que falta): FÓRMULA NOMBRE FÓRMULA NOMBRE BH 3 HCl Hidruro de cinc Amoníaco Hidruro de hierro (III) Dihidruro de estaño AlH 3 NiH
1.- CONCEPTOS PREVIOS
 TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
Nomenclatura Inorgánica
 Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
TRANSFORMACIONES Y REACCIONES QUÍMICAS
 TRANSFORMACIONES Y REACCIONES QUÍMICAS 1. TRANSFORMACIONES FÍSICAS Y QUÍMICAS a. Transformaciones físicas: Cambios que sufre la materia y que no alteran su naturaleza. (Ej.: el agua al congelarse) b. Transformaciones
TRANSFORMACIONES Y REACCIONES QUÍMICAS 1. TRANSFORMACIONES FÍSICAS Y QUÍMICAS a. Transformaciones físicas: Cambios que sufre la materia y que no alteran su naturaleza. (Ej.: el agua al congelarse) b. Transformaciones
ACTIVIDAD I. Desarrollo. MATERIA: todo lo que posee masa, inercia y ocupa un lugar en el espacio.
 ACTIVIDAD I ELEMENTOS Y COMPUESTOS NUMERO DE OXIDACION ACTIVIDAD I TEMARIO: Materia - Atomo - Elemento - Sustancia: elementos y compuestos - Mezclas - Molécula - Atomicidad - Símbolo de los elementos químicos
ACTIVIDAD I ELEMENTOS Y COMPUESTOS NUMERO DE OXIDACION ACTIVIDAD I TEMARIO: Materia - Atomo - Elemento - Sustancia: elementos y compuestos - Mezclas - Molécula - Atomicidad - Símbolo de los elementos químicos
DEPARTAMENTO DE FÍSICA Y QUÍMICA
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Apuntes de refuerzo 1 de 5
 Apuntes de refuerzo 1 de 5 1º. Para averiguar el nombre de gran número de compuestos necesitamos conocer el número de oxidacin de los elementos del compuesto. Procedemos según las reglas estudiadas. Se
Apuntes de refuerzo 1 de 5 1º. Para averiguar el nombre de gran número de compuestos necesitamos conocer el número de oxidacin de los elementos del compuesto. Procedemos según las reglas estudiadas. Se

 1 ALCALINOS 3 C3
1 ALCALINOS 3 C3