Capítulo 7 OXÍGENO SINGLETE
|
|
|
- Catalina Agüero Valverde
- hace 9 años
- Vistas:
Transcripción
1 Capítulo 7 OXÍGENO SINGLETE Como se detalló en el Capítulo 3, el oxígeno singlete es un estado electrónicamente excitado del oxígeno y es un agente fuertemente oxidante. La generación fotoquímica de esta especie consiste en la transferencia de energía desde una molécula electrónicamente excitada debido a la absorción de un cuanto de luz, denominada comúnmente sensibilizador, al oxígeno [Foote, 1991]. Como consecuencia de esta transferencia se regenera el sensibilizador en su estado basal y el oxígeno queda en su estado excitado singlete. Como parte de este trabajo se investigó la capacidad de las pterinas excitadas para generar oxígeno singlete. Aunque anteriormente ya se explicó la generación fotosensibilizada de oxígeno singlete, se plantea nuevamente en el presente Capítulo a fines de describir el método experimental utilizado para las determinación de rendimientos cuánticos de producción de oxígeno singlete (Φ ). El posible sensibilizador ( 1 Sens) es, en este caso, una molécula de pterina. Éste absorbe luz UV-A y se genera un estado excitado singlete ( 1 Sens*), el cual, mediante un cruzamiento intersistemas, genera cierta proporción de moléculas en estado triplete ( 3 Sens*) de mayor tiempo de vida (Ecuación 1). Este estado triplete del sensibilizador es el que tiene la capacidad de transferir su energía hacia el oxígeno molecular ( 3 O2) disuelto en el medio (Ecuación 2). 1 Sens hν 1 Sens* kisc 3 Sens* (1) 3 Sens* + 3 O 2 ket 1 Sens + 1 O 2 (2) 68
2 La desactivación del oxígeno singlete puede ocurrir en forma no radiativa (transferencia de energía al solvente) o radiativa (emitiendo luz) (Ecuaciones 3 y 4). En presencia de otra sustancia capaz de actuar como quencher (Q), deben considerarse el quenching químico o físico (Ecuaciones 5 y 6). Cabe aclarar que el rendimiento cuántico de fosforescencia es casi siempre despreciable respecto al rendimiento cuántico de desactivación por el solvente. 1 k O d 3 2 O 2 1 k e O 3 2 O 2 + h. ν (3) (4) Q + 1 O2 k r QO2 (5) Q + 1 O2 k q Q + 3 O2 (6) Método de detección de oxígeno singlete. El fundamento de la técnica empleada consiste en la medida de la luminiscencia del oxígeno singlete a 1270 nm, producido durante la irradiación continua de una solución de la sustancia que se quiere investigar [Krasnovsky, 1979; Kahn, 1980]. Como se describió anteriormente, el reemplazo del agua común por agua deuterada, o agua pesada (D2O), disminuye la velocidad de desactivación del estado singlete aproximadamente en un orden de magnitud debido a que las frecuencias vibracionales disminuyen. El resultado es un tiempo de vida mucho mayor en D 2 O que en H 2 O (de 3 a 4 µs en H 2 O a 62 µs en D 2 O [Foote y Clennan, 1995; Martínez et al, 2000]). Los estudios se realizan en soluciones preparadas en agua deuterada, D2O (Euriso-top, CAE, Saclay, France de 99.9 % de pureza isotópica), como solvente, en el cual se obtienen señales mayores que usando agua común, aumentando así la sensibilidad del método significativamente [Hurst y Schuster, 1983; Schmidt, 1989; Rodgers, 1983]. 69
3 El pd (-log [D + ]) fue medido con un ph-meter Schott CG 843P en combinación con un electrodo Blue Line 0.14 ph (Schott). Los valores de pd se calcularon aplicando la siguiente corrección a cada medida: pd= ph + 0,4 donde ph es el valor leído en el ph-meter [Salomaa et al, 1964]. El pd fue ajustado mediante el agregado de pequeños volúmenes (microlitros), con micropipeta, de soluciones concentradas de hidróxido de sodio deuterado, NaOD (CEA) y de ácido clorhídrico deuterado, DCl (Aldrich, 99.5%). Las soluciones a estudiar se prepararon de modo tal que la absorbancia a la longitud de onda de excitación fue siempre mayor a 0.6. El equipo cuenta con una lámpara de excitación Xe/Hg Osram de 1kW. El haz de luz pasa a través de un filtro de agua y un monocromador ISA Jobin-Yvon B204, de 6 nm de ancho de banda, antes de incidir en la celda que contiene la muestra. La mencionada celda, de 1x1 cm, es de cuarzo y puede contener aproximadamente 3,5 ml de solución. La luz emitida es colectada por un espejo. El haz pasa primero a través de un chopper calibrado a 11 Hz; luego pasa por un filtro tipo cut-off de 1000 nm y por un filtro de interferencia de 1271 nm, para incidir, finalmente, en un fotodiodo de Germanio ubicado en ángulo recto respecto al haz incidente. Este dispositivo de detección trabaja a 78 o C, por consiguiente, consta de un sistema de refrigeración que emplea una mezcla de CO 2 sólido y alcohol isopropílico para alcanzar dicha temperatura. El detector de Germanio está conectado a dos amplificadores (lock-in) los cuales envían, cada uno, una señal a un registrador Y-t y a un osciloscopio digital HP 54602B, 150 Mz. La longitud de onda de excitación se elige teniendo en cuenta los máximos de absorción de los sensibilizadores a estudiar y el espectro de emisión de la lámpara de excitación. Para las pterinas se utilizó, en todos los casos, luz de longitud de onda de 367 nm. La potencia de la luz incidente (F o, mw) se midió por medio de una termopila (Laser instrumentation, model 154). 70
4 Todas las medidas realizadas en el equipo de detección de oxígeno singlete utilizado en el presente trabajo se realizaron en el Instituto Engler Bunte de la Universidad de Karlsruhe, en el marco de un convenio de colaboración entre dicho Instituto y nuestros laboratorios (SECyT-BMFB). Cada medida se realizó registrando, primero, una línea de base sin irradiación, luego se iluminó la muestra y, por último, se realizó nuevamente una línea de base sin irradiación. Sistemáticamente se registraron señales durante nueve minutos totales repartidos en tres minutos para cada una de las tres etapas de la medida: se controla la línea de base tres minutos, se irradia durante tres minutos y se vuelve a controlar la línea de base tres minutos más. Además se tomaron los espectros de absorción antes y después de la irradiación en un espectrofotómetro Cary 5 (Varian). Este control se realizó para determinar si durante la iluminación de la muestra se producía transformación química de la misma. Cada señal es amplificada y registrada. Se obtienen dos registros de cada señal, debido a que, como se mencionó anteriormente, el equipo cuenta con dos amplificadores (Figura 7.1, corresponde a dos registros, rojo y azul, de la misma señal). Se (mv) Figura 7.1: Registros de una señal de oxígeno singlete. 71
5 Dado un conjunto de condiciones experimentales (longitud de onda de excitación, absorbancia de la solución a analizar a dicha longitud de onda, solvente, etc.) la diferencia entre el voltaje proveniente del detector, en presencia y ausencia de luz, es proporcional a la concentración de estado estacionario de oxígeno singlete presente en la solución durante la irradiació n. La obtención de este parámetro, que en adelante se llamará señal (Se) se muestra esquemáticamente en la Figura 7.1. La magnitud de esta diferencia se compara con la correspondiente a una referencia para determinar el rendimiento cuántico de producción de oxígeno singlete (Φ ) de una sustancia a un determinado pd. Determinación del rendimiento cuántico de producción de oxígeno singlete. El rendimiento cuántico de producción de oxígeno singlete (Φ ) puede definirse como la fracción de moléculas de oxígeno singlete producidas por cada cuanto de luz absorbido por el sensibilizador. Bajo condiciones de irradiación continua y teniendo en cuenta las ecuaciones 1 a 6 planteadas anteriormente puede escribirse la siguiente expresión para la concentración de estado estacionario de oxígeno singlete: Φ. I A [ 1 O 2 ] = (7) kd + (kq + kr) [Sens] donde Φ.I A (I A es la luz absorbida por el sensibilizador) es la velocidad de generación de oxígeno singlete (Ecuaciones 1 y 2) y k e fue despreciada por ser mucho menor que kd. Por otra parte, en esta expresión se considera una posible desactivación del oxígeno singlete por interacción con el propio sensibilizador. Por lo tanto, Q de las Ecuaciones 4 y 5 se reemplazó por Sens. Como ya se dijo, la señal obtenida para cada sustancia es proporcional a la cantidad de oxígeno singlete que se genera. Esta señal está relacionada con las 72
6 características del equipo, el sensibilizador y el medio acorde a la siguiente ecuación: Se = C k e (1/n 2 ) [ 1 O 2 ] = C k e (1/n 2 ) P o (1-10 -A ) Φ S 1 k d + (k q + k r ) [Sens] donde C es un factor de proporcionalidad que incluye la geometría y factores electrónicos del sistema de detección; P o es la tasa de fotones incidentes; A la absorbancia del sensibilizador a la longitud de onda de excitación (así el producto P o (1-10 -A ) representa la tasa de fotones absorbidos por el sensibilizador, es decir S I A ); Φ es el rendimiento cuántico de producción de oxígeno singlete por el sensibilizador; k e es la constante de desactivación radiativa del oxígeno singlete; (1/kd) el tiempo de vida del oxígeno singlete y n el índice de refracción del medio. Se utilizaron como referencias sustancias con rendimientos cuánticos de producción de oxígeno singlete conocidos (Φ R ). Se prepararon soluciones de las referencias en agua deuterada (D 2 O), con una absorbancia y un pd iguales a los de la solución de la sustancia cuyo rendimiento cuántico (Φ S ) se quiere determinar. De acuerdo al pd se utilizaron dos referencias diferentes: para el medio alcalino se eligió rosa de bengala, y para medio ácido fenalenona. La longitud de onda de R excitación fue 367 nm para todas las pterinas y la fenalenona (Φ = 0.975, en D 2 O) [Oliveros et al, 1991]. Para el rosa de bengala se irradió a 547 nm (Φ R = 0.76 en D2O) [Murasecco-Suardi et al, 1987; Neckers, 1989]. Los valores de absorbancia se fijaron entre 0.6 y 1.6. Se utilizaron celdas de cuarzo para fluorescencia de 1 cm por 1 cm. Si las señales luminosas son monitoreadas usando soluciones ópticamente comparables de la muestra y la referencia, la relación entre las señales de la emisión fosforescente del oxígeno singlete de la muestra (Se S ) y la referencia (Se R ) es proporcional a la relación entre los rendimientos cuánticos de producción de oxígeno singlete. Entonces el cociente entre la magnitud de ambas señales estará dado por la Ecuación (8): 73
7 Se S Se R = Φ S Φ R k d k d + k T S [Sens] S P0 P 0 R (1 10 -AS ) (1 10 -AR ) (8) donde el superíndice S se refiere al sensibilizador en estudio y el superíndice R se refiere a la referencia; k S T es la constante bimolecular de quenching total de oxígeno singlete por el sensibilizador (k S T = k S q + k S r ). La desactivación del oxígeno singlete por la referencia no fue considerada porque para las dos referencias utilizadas este fenómeno es despreciable. Los términos ke, n y C se mantienen constantes en ambas medidas y por lo tanto se anulan al formular el cociente. Debido a la diferencia entre la intensidad de la luz incidente (P o ) a las longitudes de onda de excitación de la muestra y la referencia (λ S y λ R ), a causa del espectro de emisión de la lámpara, es necesario introducir el factor de corrección P S o / P R o. Este factor pueden escribirse como F S 0. λ S / P R 0. λ R. La potencia de la luz incidente, F 0, se mide con una termopila Laser Instrumentation modelo 154. El otro factor que está presente en la ecuación (8), [(1 10 -AS ) / (1 10 -AR )], se origina en la diferente cantidad de fotones absorbidos por la muestra y por la referencia. Sin embargo, como se trabajó en condiciones tales que la absorbancia de ambas soluciones fue igual para cada experimento, este factor puede eliminarse. Teniendo en cuenta estas consideraciones y despejando Φ S de la Ecuación (8), se obtiene Φ S = Φ R Se S Se R F 0 R. λ R F0 X. λ X (kd + kt S [Sens]) kd (9) En aquellos casos en los cuales la referencia y la muestra se excitan a la misma longitud de onda, la Ecuación (9) se reduce a: Φ S = Φ R Se S Se R (kd + kt S [Sens]) k d (10) 74
8 En el presente trabajo de tesis, como ya se mencionó, se utilizaron dos referencias según el pd. En las medidas realizadas en medio ácido se empleó fenalenona como referencia y, en este caso, la muestra y la referencia se excitaron a 367 nm. Para los cálculos se empleó la Ecuación (10). En medio alcalino, en cambio, se utilizó rosa de bengala como referencia, y, en este caso, la referencia se excitó a 547 nm (debido a que a 367 nm su coeficiente de extinción molar es muy bajo) y la muestra a 367 nm. Por esta razón, no puede eliminarse el factor que corrige la diferencia de intensidad a diferentes longitudes de onda, entonces se utilizó la Ecuación (9). Esta claro, que para calcular los rendimientos cuánticos de producción de oxígeno singlete (Φ S ) es necesario conocer la constante bimolecular de quenching total de oxígeno singlete (k S T ). De lo contrario, se determina un rendimiento cuántico aparente (Φ ap ) dado por la siguiente ecuación: Se S F0 R. λ R Φ ap = Φ R (11) Se R F X 0. λ X donde: kd Φ ap = Φ S (kd + kt S [Sens]) Determinación de la constante de velocidad de quenching total de oxígeno singlete. Las constantes de velocidad de quenching total de oxígeno singlete (kt) se determinaron por análisis de Stern-Volmer del quenching de oxígeno singlete [Tournaire et al, 1993]. Se utilizó el mismo equipo y las mismas condiciones que para las medidas de producción de oxígeno singlete. El oxígeno singlete fue generado por fotosensibilización, utilizando rosa de bengala (RB) como 75
9 sensibilizador. Se irradió con luz de excitación de 547 nm, donde las pterinas no absorben. Se mantuvo constante la concentración de rosa de bengala y se varió la concentración de pterinas. La concentración de rosa de bengala fue tal que el quenching de oxígeno singlete por ella misma es despreciable comparado con la desactivación por el solvente. Se realizó un análisis de Stern-Volmer, en una gráfica de la relación entre las señales en ausencia (Se 0 ) y en presencia (Se) de quencher versus la concentración del mismo, de acuerdo a la ecuación: S e 0 / (S e ) = Φ e 0 / Φ e = 1 + k T τ [Q] (12) En el presente trabajo los quenchers utilizados fueron pterina, 6-carboxipterina, 6-formilpterina, neopterina, biopterina y ácido fólico. 76
Capítulo 5 ESPECTROSCOPÍA ELECTRÓNICA
 Capítulo 5 ESPECTROSCOPÍA ELECTRÓNICA Existen numerosas técnicas espectroscópicas que permiten estudiar los estados excitados de las moléculas orgánicas. En particular, los espectros de absorción y emisión
Capítulo 5 ESPECTROSCOPÍA ELECTRÓNICA Existen numerosas técnicas espectroscópicas que permiten estudiar los estados excitados de las moléculas orgánicas. En particular, los espectros de absorción y emisión
PRODUCCIÓN DE OXIGENO SINGLETE
 Capítulo 11 PRODUCCIÓN DE OXIGENO SINGLETE Como se detalló en el Capítulo 2 existen muchas moléculas orgánicas que pueden actuar como sensibilizadores y producir oxígeno singlete al iluminar soluciones
Capítulo 11 PRODUCCIÓN DE OXIGENO SINGLETE Como se detalló en el Capítulo 2 existen muchas moléculas orgánicas que pueden actuar como sensibilizadores y producir oxígeno singlete al iluminar soluciones
Capítulo 6 QUENCHING DE FLUORESCENCIA
 Capítulo 6 QUENCHING DE FLUORESCENCIA El fenómeno de quenching de fluorescencia se refiere a procesos que provocan una disminución de la intensidad de fluorescencia de una sustancia dada. El quenching
Capítulo 6 QUENCHING DE FLUORESCENCIA El fenómeno de quenching de fluorescencia se refiere a procesos que provocan una disminución de la intensidad de fluorescencia de una sustancia dada. El quenching
ESPECTROFOTÓMETROS UV- VISIBLE COMPONENTES
 ESPECTROFOTÓMETROS UV- VISIBLE COMPONENTES INSTRUMENTAL EL INSTRUMENTO QUE NORMALMENTE SE UTILIZA PARA MEDIR LA TRANSMITANCIA Y ABSORBANCIA ES EL ESPECTROFOTÓMETRO LOS COMPONENTES BÁSICOS DE UN ESPECTROFOTÓMETRO
ESPECTROFOTÓMETROS UV- VISIBLE COMPONENTES INSTRUMENTAL EL INSTRUMENTO QUE NORMALMENTE SE UTILIZA PARA MEDIR LA TRANSMITANCIA Y ABSORBANCIA ES EL ESPECTROFOTÓMETRO LOS COMPONENTES BÁSICOS DE UN ESPECTROFOTÓMETRO
PRÁCTICA 3 DETERMINACIÓN ESPECTROFOTOMÉTRICA DEL pk DE UN INDICADOR
 PRÁCTICA 3 DETERMINACIÓN ESPECTROFOTOMÉTRICA DEL pk DE UN INDICADOR Material Productos 2 matraces aforados de 250 ml Hidróxido de sodio en lentejas 2 matraces aforados de 25 ml Disolución de hidróxido
PRÁCTICA 3 DETERMINACIÓN ESPECTROFOTOMÉTRICA DEL pk DE UN INDICADOR Material Productos 2 matraces aforados de 250 ml Hidróxido de sodio en lentejas 2 matraces aforados de 25 ml Disolución de hidróxido
QUENCHING DE FLUORESCENCIA POR ANIONES
 Capítulo QUENCHING DE FLUORESCENCIA POR ANIONES Como se mencionó en el Capítulo 6 algunas sustancias pueden producir una disminución de la emisión fluorescente, siguiendo una comportamiento de Stern-Volmer.
Capítulo QUENCHING DE FLUORESCENCIA POR ANIONES Como se mencionó en el Capítulo 6 algunas sustancias pueden producir una disminución de la emisión fluorescente, siguiendo una comportamiento de Stern-Volmer.
PROCESOS FOTOSENSIBILIZADOS EN MOLÉCULAS SIMPLES Y BIOMOLÉCULAS
 Capítulo 3 PROCESOS FOTOSENSIBILIZADOS EN MOLÉCULAS SIMPLES Y BIOMOLÉCULAS Se denomina fotosensibilización a todo proceso por el cual una especie química sufre una alteración fotoquímica o fotofísica como
Capítulo 3 PROCESOS FOTOSENSIBILIZADOS EN MOLÉCULAS SIMPLES Y BIOMOLÉCULAS Se denomina fotosensibilización a todo proceso por el cual una especie química sufre una alteración fotoquímica o fotofísica como
Determinación de constantes de ionización
 Capítulo 5. Determinación de constantes de ionización Se determinaron las constantes de ionización de diversos compuestos mediante curvas de titulación ácido-base empleando métodos espectrofotométricos
Capítulo 5. Determinación de constantes de ionización Se determinaron las constantes de ionización de diversos compuestos mediante curvas de titulación ácido-base empleando métodos espectrofotométricos
3. a) Explique brevemente en qué consiste el efecto fotoeléctrico. b) Tienen la misma energía cinética todos los fotoelectrones emitidos?
 CUESTIONES 1. a) Enuncie la hipótesis de de Broglie. Depende la longitud de onda asociada a una partícula, que se mueve con una cierta velocidad, de su masa? b) Comente el significado físico y las implicaciones
CUESTIONES 1. a) Enuncie la hipótesis de de Broglie. Depende la longitud de onda asociada a una partícula, que se mueve con una cierta velocidad, de su masa? b) Comente el significado físico y las implicaciones
Espectros Atómicos. Química General I 2012
 Espectros Atómicos Química General I 2012 Estudios de las ondas Que es una onda? Es una alteración vibracional a través de la cual se transmite energía. Existen muchos tipos de ondas, por ejemplo, las
Espectros Atómicos Química General I 2012 Estudios de las ondas Que es una onda? Es una alteración vibracional a través de la cual se transmite energía. Existen muchos tipos de ondas, por ejemplo, las
Espectroscopía de Fluorescencia. Ana Denicola
 Espectroscopía de Fluorescencia Ana Denicola DIAGRAMA DE JABLONSKI (1898-1980) relajación vibracional S2 conversión interna IC relajación vibracional cruce intersistemas ISC S1 T1 k NR IC hυ A hυ F k NR
Espectroscopía de Fluorescencia Ana Denicola DIAGRAMA DE JABLONSKI (1898-1980) relajación vibracional S2 conversión interna IC relajación vibracional cruce intersistemas ISC S1 T1 k NR IC hυ A hυ F k NR
Módulo 5: La luz. Ondas electromagnéticas
 Módulo 5: La luz 1 Ondas electromagnéticas Partículas cargadas eléctricamente (cargas) en movimiento forman una corriente eléctrica Una corriente eléctrica que cambia (debida al movimiento) crea un campo
Módulo 5: La luz 1 Ondas electromagnéticas Partículas cargadas eléctricamente (cargas) en movimiento forman una corriente eléctrica Una corriente eléctrica que cambia (debida al movimiento) crea un campo
UNIVERSIDAD NACIONAL DE VILLA MERCEDES CARRERA DE KINESIOLOGIA Y FISIATRIA TRABAJO Y ENERGIA.
 TRABAJO Y ENERGIA. El problema fundamental de la Mecánica es describir como se moverán los cuerpos si se conocen las fuerzas aplicadas sobre él. La forma de hacerlo es aplicando la segunda Ley de Newton,
TRABAJO Y ENERGIA. El problema fundamental de la Mecánica es describir como se moverán los cuerpos si se conocen las fuerzas aplicadas sobre él. La forma de hacerlo es aplicando la segunda Ley de Newton,
MODELO ATÓMICO DE DALTON 1808
 ESTRUCTURA ATÓMICA MODELO ATÓMICO DE DALTON 1808 Sienta las bases para la estequiometría de composición y la estequiometría de reacción. 1. Un elemento se compone de partículas extremadamente pequeñas,
ESTRUCTURA ATÓMICA MODELO ATÓMICO DE DALTON 1808 Sienta las bases para la estequiometría de composición y la estequiometría de reacción. 1. Un elemento se compone de partículas extremadamente pequeñas,
Química Biológica TP 1: ESPECTROFOTOMETRIA.
 TP 1: ESPECTROFOTOMETRIA. Introducción Al observar una solución acuosa de un colorante a trasluz, observamos una leve coloración, la cual se debe a la interacción entre las moléculas del colorante y la
TP 1: ESPECTROFOTOMETRIA. Introducción Al observar una solución acuosa de un colorante a trasluz, observamos una leve coloración, la cual se debe a la interacción entre las moléculas del colorante y la
CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara
 CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara OBJETIVOS 1.- Estudiar la cinética de la reacción de hidrólisis ácida del acetato de metilo en disolución
CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara OBJETIVOS 1.- Estudiar la cinética de la reacción de hidrólisis ácida del acetato de metilo en disolución
PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA
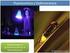 PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA Objetivos. La práctica se divide en dos partes. En la primera, se registran los espectros de absorción, fluorescencia y excitación de un conjunto de colorantes
PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA Objetivos. La práctica se divide en dos partes. En la primera, se registran los espectros de absorción, fluorescencia y excitación de un conjunto de colorantes
Distancias estelares. Magnitudes estelares
 Capítulo 5 Distancias estelares. Magnitudes estelares 5.1. Distancias estelares # Determinación de distancias esencial para estimar parámetros fundamentales en astrofísica: R, M, L,... Métodos directos:
Capítulo 5 Distancias estelares. Magnitudes estelares 5.1. Distancias estelares # Determinación de distancias esencial para estimar parámetros fundamentales en astrofísica: R, M, L,... Métodos directos:
CUADERNO DE PRÁCTICAS
 CUADERNO DE PRÁCTICAS ANÁLISIS INDUSTRIAL Área de Química Analítica Facultad de Ciencias Químicas Curso 2006/2007 Cuaderno de Prácticas 2006/2007 1 ÍNDICE *Práctica 1.- Práctica 2.- Determinación de Cu
CUADERNO DE PRÁCTICAS ANÁLISIS INDUSTRIAL Área de Química Analítica Facultad de Ciencias Químicas Curso 2006/2007 Cuaderno de Prácticas 2006/2007 1 ÍNDICE *Práctica 1.- Práctica 2.- Determinación de Cu
Las ecuaciones químicas
 Las reacciones químicas se representan escribiendo las fórmulas de los reactivos en el primer miembro de una ecuación y las de los productos en el segundo. El signo igual se sustituye por una flecha (
Las reacciones químicas se representan escribiendo las fórmulas de los reactivos en el primer miembro de una ecuación y las de los productos en el segundo. El signo igual se sustituye por una flecha (
Clasificación de Electrolitos
 8/11/14 Conductancia eléctrica Lalboratorio de Química Física I QUIM 451 http://www.usm.maine.edu/chy/manuals/114/text/conduct.html Ileana Nieves Martínez agosto 14 1 Clasificación de Electrolitos Electrolitos
8/11/14 Conductancia eléctrica Lalboratorio de Química Física I QUIM 451 http://www.usm.maine.edu/chy/manuals/114/text/conduct.html Ileana Nieves Martínez agosto 14 1 Clasificación de Electrolitos Electrolitos
Circuitos de RF y las Comunicaciones Analógicas. Capítulo X: Comunicación Banda Base
 Capítulo X: Comunicación Banda Base 173 174 10. COMUNICACION BANDA BASE 10.1 Introducción Transmitir una señal eléctrica sin ninguna traslación de su espectro se conoce como comunicación en banda base.
Capítulo X: Comunicación Banda Base 173 174 10. COMUNICACION BANDA BASE 10.1 Introducción Transmitir una señal eléctrica sin ninguna traslación de su espectro se conoce como comunicación en banda base.
PROBLEMARIO DE QUÍMICA ANALÍTICA II. Espectrometría UV-Visible
 UNIVERSIDAD DEL ZULIA FACULTAD EXPERIMENTAL DE CIENCIAS DEPARTAMENT DE QUIMICA UNIDAD ACADÉMICA DE QUÍMICA ANALÍTICA MATERIA: QUÍMICA ANALÍTICA II PRBLEMARI DE QUÍMICA ANALÍTICA II Espectrometría UV-Visible
UNIVERSIDAD DEL ZULIA FACULTAD EXPERIMENTAL DE CIENCIAS DEPARTAMENT DE QUIMICA UNIDAD ACADÉMICA DE QUÍMICA ANALÍTICA MATERIA: QUÍMICA ANALÍTICA II PRBLEMARI DE QUÍMICA ANALÍTICA II Espectrometría UV-Visible
(g) CO 2. (g) + 2 H 2. Procediendo en la misma forma con la segunda ecuación, obtenemos: (g) 3 CO 2. (g) + 4 H 2
 Para ajustar el oxígeno, escribiremos otro dos delante de la molécula de oxígeno gaseoso en los reactivos. De este modo, la ecuación ajustada del primer proceso es: CH (g) + 2 O 2 (g) CO 2 (g) + 2 H 2
Para ajustar el oxígeno, escribiremos otro dos delante de la molécula de oxígeno gaseoso en los reactivos. De este modo, la ecuación ajustada del primer proceso es: CH (g) + 2 O 2 (g) CO 2 (g) + 2 H 2
OTRAS PROPIEDADES: TÉRMICAS, ELÉCTRICAS, DIELÉCTRICAS, AISLANTES Y MAGNÉTICAS DE LOS MATERIALES
 OTRAS PROPIEDADES: TÉRMICAS, ELÉCTRICAS, DIELÉCTRICAS, AISLANTES Y MAGNÉTICAS DE LOS MATERIALES El comportamiento físico de los materiales se encuentra descrito por una gran variedad de propiedades eléctricas,
OTRAS PROPIEDADES: TÉRMICAS, ELÉCTRICAS, DIELÉCTRICAS, AISLANTES Y MAGNÉTICAS DE LOS MATERIALES El comportamiento físico de los materiales se encuentra descrito por una gran variedad de propiedades eléctricas,
ESPECTROFOTOMETRIA. BASES FISICAS
 ESPECTROFOTOMETRIA. BASES FISICAS Radiación Electromagnética y su Interacción con la Materia El principio de funcionamiento de la espectrofotometría se basa en el empleo de las interacciones entre la radiación
ESPECTROFOTOMETRIA. BASES FISICAS Radiación Electromagnética y su Interacción con la Materia El principio de funcionamiento de la espectrofotometría se basa en el empleo de las interacciones entre la radiación
IV. RESULTADOS Y DISCUSIÓN
 IV. RESULTADOS Y DISCUSIÓN IV. RESULTADOS Y DISCUSIÓN IV.1 Síntesis de Nanopartículas de Oro En primera instancia la obtención de las nanopartículas de oro es corroborada a simple vista mediante el cambio
IV. RESULTADOS Y DISCUSIÓN IV. RESULTADOS Y DISCUSIÓN IV.1 Síntesis de Nanopartículas de Oro En primera instancia la obtención de las nanopartículas de oro es corroborada a simple vista mediante el cambio
Tema 3: Ecuaciones químicas y concentraciones
 Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
Diseño Pasivo: Diseñando para la Iluminación Natural
 Diseño Pasivo: Diseñando para la Iluminación Natural Objetivo Al final del curso el participante tendrá un conocimiento más amplio de la importancia de la iluminación natural y su impacto en el diseño
Diseño Pasivo: Diseñando para la Iluminación Natural Objetivo Al final del curso el participante tendrá un conocimiento más amplio de la importancia de la iluminación natural y su impacto en el diseño
Práctica 5. Polarización de ondas electromagnéticas planas
 Polarización de ondas electromagnéticas planas 1 Práctica 5. Polarización de ondas electromagnéticas planas 1.- OBJETIVOS - Estudiar las características de la luz polarizada, comprobar experimentalmente
Polarización de ondas electromagnéticas planas 1 Práctica 5. Polarización de ondas electromagnéticas planas 1.- OBJETIVOS - Estudiar las características de la luz polarizada, comprobar experimentalmente
EL MODELO ATOMICO DE BOHR
 EL MODELO ATOMICO DE BOHR En 1913, Niels Bohr ideó un modelo atómico que explica perfectamente los espectros determinados experimentalmente para átomos hidrogenoides. Estos son sistemas formados solamente
EL MODELO ATOMICO DE BOHR En 1913, Niels Bohr ideó un modelo atómico que explica perfectamente los espectros determinados experimentalmente para átomos hidrogenoides. Estos son sistemas formados solamente
MOTORES DE CD INTRODUCCIÓN A LOS MOTORES DE CD. Los motores de CD son máquinas utilizadas
 INTRODUCCIÓN A LOS MOTORES DE CD Los motores de CD son máquinas utilizadas tanto como motores que como generadores de CD, es decir, físicamente es la misma máquina y únicamente difieren en la forma de
INTRODUCCIÓN A LOS MOTORES DE CD Los motores de CD son máquinas utilizadas tanto como motores que como generadores de CD, es decir, físicamente es la misma máquina y únicamente difieren en la forma de
SELECTIVIDAD: Física cuántica Física nuclear (Teoría)
 FÍSICA SELECTIVIDAD: Física cuántica Física nuclear (Teoría) Selectividad 2001 1. a) Qué significado tiene la expresión "longitud de onda asociada a una partícula"? b) Si la energía cinética de una partícula
FÍSICA SELECTIVIDAD: Física cuántica Física nuclear (Teoría) Selectividad 2001 1. a) Qué significado tiene la expresión "longitud de onda asociada a una partícula"? b) Si la energía cinética de una partícula
DETERMINACIÓN DE LA LEY EXPERIMENTAL DE RAPIDEZ. ESTUDIO DE LA CINÉTICA DE YODACIÓN DE LA ACETONA. Grupo: Equipo: Fecha: Nombre(s):
 DETERMINACIÓN DE LA LEY EXPERIMENTAL DE RAPIDEZ. ESTUDIO DE LA CINÉTICA DE YODACIÓN DE LA ACETONA. Grupo: Equipo: Fecha: Nombre(s): I. OBJETIVO GENERAL Comprender que la composición de un sistema reaccionante
DETERMINACIÓN DE LA LEY EXPERIMENTAL DE RAPIDEZ. ESTUDIO DE LA CINÉTICA DE YODACIÓN DE LA ACETONA. Grupo: Equipo: Fecha: Nombre(s): I. OBJETIVO GENERAL Comprender que la composición de un sistema reaccionante
PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA
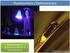 Práctica 3: Espectroscopia de Fluorescencia PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA Objetivos. La práctica se divide en dos partes. En la primera, se registran los espectros de absorción, fluorescencia
Práctica 3: Espectroscopia de Fluorescencia PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA Objetivos. La práctica se divide en dos partes. En la primera, se registran los espectros de absorción, fluorescencia
Capítulo II. Ecuaciones de los circuitos magnéticos
 Capítulo II. Ecuaciones de los circuitos magnéticos 2.1. Intensidad de Campo magnético Los campos magnéticos son el mecanismo fundamental para convertir energía eléctrica de corriente alterna de un nivel
Capítulo II. Ecuaciones de los circuitos magnéticos 2.1. Intensidad de Campo magnético Los campos magnéticos son el mecanismo fundamental para convertir energía eléctrica de corriente alterna de un nivel
ÓPTICA FÍSICA MODELO 2016
 ÓPTICA FÍSICA MODELO 2016 1- Un foco luminoso puntual está situado en el fondo de un recipiente lleno de agua cubierta por una capa de aceite. Determine: a) El valor del ángulo límite entre los medios
ÓPTICA FÍSICA MODELO 2016 1- Un foco luminoso puntual está situado en el fondo de un recipiente lleno de agua cubierta por una capa de aceite. Determine: a) El valor del ángulo límite entre los medios
Trabajo Práctico N o 1
 Trabajo Práctico N o 1 Reflexión y Refracción de la Luz Tomás Corti ([email protected]) Ramiro Olivera ([email protected]) Fabián Shalóm ([email protected]) Marzo de 2004 Cátedra
Trabajo Práctico N o 1 Reflexión y Refracción de la Luz Tomás Corti ([email protected]) Ramiro Olivera ([email protected]) Fabián Shalóm ([email protected]) Marzo de 2004 Cátedra
DETECTORES DE RADIACIÓN IONIZANTE
 DETECTORES DE RADIACIÓN IONIZANTE Nuevo símbolo ISO de advertencia por presencia de Radiación FENÓMENOS FÍSICOS UTILIZADOS PARA LA DETECCIÓN Ionización de los gases Excitación y luminiscencia de los
DETECTORES DE RADIACIÓN IONIZANTE Nuevo símbolo ISO de advertencia por presencia de Radiación FENÓMENOS FÍSICOS UTILIZADOS PARA LA DETECCIÓN Ionización de los gases Excitación y luminiscencia de los
Tema 7. Espectroscopia para el estudio de la materia
 Tema 7. Espectroscopia para el estudio de la materia 1. Introducción. Naturaleza dual de la radiación y la materia 2. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojos 4.
Tema 7. Espectroscopia para el estudio de la materia 1. Introducción. Naturaleza dual de la radiación y la materia 2. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojos 4.
INTRODUCCIÓN GENERAL Y OBJETIVOS
 Capítulo 1 INTRODUCCIÓN GENERAL Y OBJETIVOS La luz tiene un papel fundamental sobre los seres vivos. La energía de la radiación ultravioleta y visible del sol da lugar a fenómenos que permiten la continuidad
Capítulo 1 INTRODUCCIÓN GENERAL Y OBJETIVOS La luz tiene un papel fundamental sobre los seres vivos. La energía de la radiación ultravioleta y visible del sol da lugar a fenómenos que permiten la continuidad
SOLUCIONES. Lic. Sandra Williams Pinto Profesora de Química Colegio Instituto de Humanidades Alfredo Silva Santiago (Concepción)
 SOLUCIONES Dr. José Francisco Acuña Elgueta Docente de Química Facultad de Agronomía Universidad de Concepción Lic. Sandra Williams Pinto Profesora de Química Colegio Instituto de Humanidades Alfredo Silva
SOLUCIONES Dr. José Francisco Acuña Elgueta Docente de Química Facultad de Agronomía Universidad de Concepción Lic. Sandra Williams Pinto Profesora de Química Colegio Instituto de Humanidades Alfredo Silva
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez DEYMER GÓMEZ CORREA: 1 042 091 432
 UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: ESTEQUIOMETRÍA 2: RELACIÓN MASA- Fecha: 16/Febrero/2010 MASA. DEYMER GÓMEZ CORREA:
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: ESTEQUIOMETRÍA 2: RELACIÓN MASA- Fecha: 16/Febrero/2010 MASA. DEYMER GÓMEZ CORREA:
1. Introducción. e. V 0 = h. ν - φ (1)
 Efecto fotoeléctrico Juan Kamienkowski, Sebastián Romano y Matías Travizano, [email protected], [email protected], [email protected] Laboratorio 5, Departamento de física, UBA- 2002 Resumen En el presente
Efecto fotoeléctrico Juan Kamienkowski, Sebastián Romano y Matías Travizano, [email protected], [email protected], [email protected] Laboratorio 5, Departamento de física, UBA- 2002 Resumen En el presente
Introducción. Condensadores
 . Introducción Un condensador es un dispositivo que sirve para almacenar carga y energía. Está constituido por dos conductores aislados uno de otro, que poseen cargas iguales y opuestas. Los condensadores
. Introducción Un condensador es un dispositivo que sirve para almacenar carga y energía. Está constituido por dos conductores aislados uno de otro, que poseen cargas iguales y opuestas. Los condensadores
Determinación de proteínas
 Determinación de proteínas Curso EMA 2013 Ing. Agr. Marta del Puerto Métodos para determinar proteínas Se basan en: a. Propiedad de las proteínas de absorber luz en el UV absorción A=280nm a. Capacidad
Determinación de proteínas Curso EMA 2013 Ing. Agr. Marta del Puerto Métodos para determinar proteínas Se basan en: a. Propiedad de las proteínas de absorber luz en el UV absorción A=280nm a. Capacidad
UNIDADES DE CONCENTRACIÓN
 Colegio San Esteban Diácono Departamento de Ciencias Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León UNIDADES DE CONCENTRACIÓN 1. Porcentaje masa/masa (%m/m) Cantidad en masa (g) de un componente
Colegio San Esteban Diácono Departamento de Ciencias Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León UNIDADES DE CONCENTRACIÓN 1. Porcentaje masa/masa (%m/m) Cantidad en masa (g) de un componente
El agua calentada en microondas se enfría más rápido?
 El agua calentada en microondas se enfría más rápido? Primera parte Experiencia de Laboratorio, Física experimental II, 2009 Larregain, Pedro [email protected] Machado, Alejandro [email protected]
El agua calentada en microondas se enfría más rápido? Primera parte Experiencia de Laboratorio, Física experimental II, 2009 Larregain, Pedro [email protected] Machado, Alejandro [email protected]
PROCEDIMIENTO PARA DETERMINAR HIERRO EN HARINAS Y ALIMENTOS. Método Espectrofotometría de Absorción Atómica/Llama
 PRT-711.02-159 Página 1 de 6 1. OBJETIVO Cuantificación de hierro en harinas y alimentos sólidos por espectrofotometría de absorción atómica y vía seca. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento
PRT-711.02-159 Página 1 de 6 1. OBJETIVO Cuantificación de hierro en harinas y alimentos sólidos por espectrofotometría de absorción atómica y vía seca. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento
DETERMINACIÓN DE FLUORUROS EN AGUAS CON EL ELECTRODO SELECTIVO
 DETERMINACIÓN DE FLUORUROS EN AGUAS CON EL ELECTRODO SELECTIVO 1. OBLETIVO: 1 Llevar a cabo medidas de potenciales con un electrodo selectivo de iones fluoruro para determinar la concentración de este
DETERMINACIÓN DE FLUORUROS EN AGUAS CON EL ELECTRODO SELECTIVO 1. OBLETIVO: 1 Llevar a cabo medidas de potenciales con un electrodo selectivo de iones fluoruro para determinar la concentración de este
UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS LABORATORIO DE FÍSICA ASIGNATURA: ELECTRICIDAD Y MAGNETISMO
 UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS LABORATORIO DE FÍSICA ASIGNATURA: ELECTRICIDAD Y MAGNETISMO I. OBJETIVOS LABORATORIO 4: CAPACITANCIA Determinar, a partir de su geometría, la capacitancia
UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS LABORATORIO DE FÍSICA ASIGNATURA: ELECTRICIDAD Y MAGNETISMO I. OBJETIVOS LABORATORIO 4: CAPACITANCIA Determinar, a partir de su geometría, la capacitancia
Capítulo 10. Fotólisis de ácido fólico.
 Capítulo 10. Fotólisis de ácido fólico. En este capítulo se presentan los resultados de los experimentos realizados irradiando soluciones ligeramente ácidas de ácido fólico. En estas condiciones, según
Capítulo 10. Fotólisis de ácido fólico. En este capítulo se presentan los resultados de los experimentos realizados irradiando soluciones ligeramente ácidas de ácido fólico. En estas condiciones, según
FUNDAMENTOS CIENTIFICOS DEL METODO MONCAYO INSTITUTO DE INVESTIGACION MONCAYO ESPAÑA MEXICO - SUECIA
 FUNDAMENTOS CIENTIFICOS DEL METODO MONCAYO INSTITUTO DE INVESTIGACION MONCAYO ESPAÑA MEXICO - SUECIA ESPECTOFOTOMETRIA Permite determinar la concentración de un compuesto en una solución. Mide la cantidad
FUNDAMENTOS CIENTIFICOS DEL METODO MONCAYO INSTITUTO DE INVESTIGACION MONCAYO ESPAÑA MEXICO - SUECIA ESPECTOFOTOMETRIA Permite determinar la concentración de un compuesto en una solución. Mide la cantidad
CONDENSADOS DE LUZ LIQUIDA. Humberto Michinel Alvarez. Área de Óptica. Universidade de Vigo.
 CONDENSADOS DE LUZ LIQUIDA Humberto Michinel Alvarez Área de Óptica. Universidade de Vigo. 1. INTRODUCCIÓN Fue Albert Einstein quien en su "annus mirabilis" 1905 propuso por primera vez la idea de que
CONDENSADOS DE LUZ LIQUIDA Humberto Michinel Alvarez Área de Óptica. Universidade de Vigo. 1. INTRODUCCIÓN Fue Albert Einstein quien en su "annus mirabilis" 1905 propuso por primera vez la idea de que
Física 2 Biólogos y Geólogos. Reflexión y refracción de la luz
 Física 2 Biólogos y Geólogos Curso de Verano 2007 Guía de laboratorio N 1 Reflexión y refracción de la luz Objetivos Estudiar experimentalmente las leyes de la reflexión y de la refracción de la luz. Determinar
Física 2 Biólogos y Geólogos Curso de Verano 2007 Guía de laboratorio N 1 Reflexión y refracción de la luz Objetivos Estudiar experimentalmente las leyes de la reflexión y de la refracción de la luz. Determinar
CAPITULO 5 LA DETERMINACIÓN DEL INGRESO DE EQUILIBRIO
 Documento elaborado por Jaime Aguilar Moreno Docente área económica Universidad del Valle Sede Buga CAPITULO 5 LA DETERMINACIÓN DEL INGRESO DE EQUILIBRIO OBJETIVO DEL CAPÍTULO Lograr que el estudiante
Documento elaborado por Jaime Aguilar Moreno Docente área económica Universidad del Valle Sede Buga CAPITULO 5 LA DETERMINACIÓN DEL INGRESO DE EQUILIBRIO OBJETIVO DEL CAPÍTULO Lograr que el estudiante
Tecnologías de redes de datos. Medios de transmisión
 Tecnologías de redes de datos Medios de transmisión Contenido Introducción Tipos de medios Conceptos básicos Aplicaciones de los medios 2 Introducción Elementos fundamentales de un sistema de comunicaciones
Tecnologías de redes de datos Medios de transmisión Contenido Introducción Tipos de medios Conceptos básicos Aplicaciones de los medios 2 Introducción Elementos fundamentales de un sistema de comunicaciones
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA
 MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
MOVIMIENTO ARMÓNICO AMORTIGUADO
 MOVIMIENTO ARMÓNICO AMORTIGUADO OBJETIVO Medida experimental de la variación exponencial decreciente de la oscilación en un sistema oscilatorio de bajo amortiguamiento. FUNDAMENTO TEÓRICO A) SISTEMA SIN
MOVIMIENTO ARMÓNICO AMORTIGUADO OBJETIVO Medida experimental de la variación exponencial decreciente de la oscilación en un sistema oscilatorio de bajo amortiguamiento. FUNDAMENTO TEÓRICO A) SISTEMA SIN
Tema 6: Detectores de radiación
 Tema 6: Detectores de radiación 1. Detección de la radiación Detección: Conjunto de procedimientos necesarios para determinar las propiedades de las partículas (E, q, m) de la radiación Fundamental para
Tema 6: Detectores de radiación 1. Detección de la radiación Detección: Conjunto de procedimientos necesarios para determinar las propiedades de las partículas (E, q, m) de la radiación Fundamental para
Para poder comenzar con el análisis de la primera etapa, es necesario definir la
 Capítulo 1 1 Diseño del convertidor AC/DC 1.1 Justificación para los valores de entrada Para poder comenzar con el análisis de la primera etapa, es necesario definir la señal de entrada. nicialmente el
Capítulo 1 1 Diseño del convertidor AC/DC 1.1 Justificación para los valores de entrada Para poder comenzar con el análisis de la primera etapa, es necesario definir la señal de entrada. nicialmente el
CAPITULO IV EL SONIDO Y LOS SISTEMAS ACUSTICOS 4.1 INTRODUCCIÓN
 158 159 CAPIITULO IIV EL SONIIDO Y LOS SIISTEMAS ACUSTIICOS 4..1 IINTRODUCCIIÓN Conocemos como sonido a aquel fenómeno físico que estimula el sentido del oído. El sonido es una onda mecánica longitudinal
158 159 CAPIITULO IIV EL SONIIDO Y LOS SIISTEMAS ACUSTIICOS 4..1 IINTRODUCCIIÓN Conocemos como sonido a aquel fenómeno físico que estimula el sentido del oído. El sonido es una onda mecánica longitudinal
La ley de desplazamiento de Wien (Premio Nobel 1911):
 Trabajo de laboratorio Nro 1: Verificación de la ley de Stefan Boltzmann y determinación de la constante de Planck mediante el análisis de la radiación del cuerpo negro Introducción Toda superficie cuya
Trabajo de laboratorio Nro 1: Verificación de la ley de Stefan Boltzmann y determinación de la constante de Planck mediante el análisis de la radiación del cuerpo negro Introducción Toda superficie cuya
SERIE INFORMES TÉCNICOS Nº. 2 / 93 UTILIZACIÓN DE LA ESPECTROSCOPIA EN EL INFRARROJO CERCANO PARA EL ANÁLISIS DE FORRAJES Y MATERIAS PRIMAS
 UTILIZACIÓN DE LA ESPECTROSCOPIA EN EL INFRARROJO CERCANO PARA EL ANÁLISIS DE FORRAJES Y MATERIAS PRIMAS SERIE INFORMES TÉCNICOS Nº. 2 / 93 Instituto de Experimentación y Promoción Agraria. UTILIZACIÓN
UTILIZACIÓN DE LA ESPECTROSCOPIA EN EL INFRARROJO CERCANO PARA EL ANÁLISIS DE FORRAJES Y MATERIAS PRIMAS SERIE INFORMES TÉCNICOS Nº. 2 / 93 Instituto de Experimentación y Promoción Agraria. UTILIZACIÓN
FARMACOPEA MERCOSUR: MÉTODO GENERAL PARA ESPECTROFOTOMETRIA ULTRAVIOLETA Y VISIBLE
 MERCOSUL/XLIII SGT Nº 11/P.RES. Nº FARMACOPEA MERCOSUR: MÉTODO GENERAL PARA ESPECTROFOTOMETRIA ULTRAVIOLETA Y VISIBLE VISTO: El Tratado de Asunción, el Protocolo de Ouro Preto y las Resoluciones N 31/11
MERCOSUL/XLIII SGT Nº 11/P.RES. Nº FARMACOPEA MERCOSUR: MÉTODO GENERAL PARA ESPECTROFOTOMETRIA ULTRAVIOLETA Y VISIBLE VISTO: El Tratado de Asunción, el Protocolo de Ouro Preto y las Resoluciones N 31/11
CALIBRACIÓN DE ANALIZADORES DE DESFIBRILADOR
 Instituto Nacional de Tecnología Industrial Centro de Desarrollo e Investigación en Física y Metrología Procedimiento específico: PEE52 CALIBRACIÓN DE ANALIZADORES DE DESFIBRILADOR Revisión: Diciembre
Instituto Nacional de Tecnología Industrial Centro de Desarrollo e Investigación en Física y Metrología Procedimiento específico: PEE52 CALIBRACIÓN DE ANALIZADORES DE DESFIBRILADOR Revisión: Diciembre
CONCRECIÓN CURRICULAR FÍSICA Y QUÍMICA CURSO: 3º DE LA ESO
 CONCRECIÓN CURRICULAR FÍSICA Y QUÍMICA CURSO: 3º DE LA ESO CRITERIOS DE EVALUACIÓN COMPETENCIAS BÁSICAS CONTENIDOS OBJETIVOS DE ÁREA /MATERIA OBJETIVOS DE ETAPA Trabajar con orden, limpieza, exactitud
CONCRECIÓN CURRICULAR FÍSICA Y QUÍMICA CURSO: 3º DE LA ESO CRITERIOS DE EVALUACIÓN COMPETENCIAS BÁSICAS CONTENIDOS OBJETIVOS DE ÁREA /MATERIA OBJETIVOS DE ETAPA Trabajar con orden, limpieza, exactitud
ÁREA DE INGENIERÍA QUÍMICA Prof. Isidoro García García. Operaciones Básicas de Transferencia de Materia. Tema 1
 ÁREA DE INGENIERÍA QUÍMICA Operaciones Básicas de Transferencia de Materia Los procesos químicos modifican las condiciones de una determinada cantidad de materia: modificando su masa o composición modificando
ÁREA DE INGENIERÍA QUÍMICA Operaciones Básicas de Transferencia de Materia Los procesos químicos modifican las condiciones de una determinada cantidad de materia: modificando su masa o composición modificando
CAPÍTULO 5 ARREGLO EXPERIMENTAL 5.1 INTRODUCCIÓN 5.2 GENERACIÓN DE MICROONDAS
 CAPÍTULO 5 ARREGLO EXPERIMENTAL 5.1 INTRODUCCIÓN En este capítulo se presenta una técnica fotónica que permite medir la potencia de reflexión en una antena microstrip, como resultado de las señales de
CAPÍTULO 5 ARREGLO EXPERIMENTAL 5.1 INTRODUCCIÓN En este capítulo se presenta una técnica fotónica que permite medir la potencia de reflexión en una antena microstrip, como resultado de las señales de
IE1117 - Temas especiales II en máquinas eléctricas: Energía solar fotovoltaica. TAREA 3 Josué Otárola Sánchez
 IE1117 - Temas especiales II en máquinas eléctricas: Energía solar fotovoltaica TAREA 3 Josué Otárola Sánchez A84674 Ejercicio 2: Cambio de polaridad en la celda solar El montaje realizado se resume en
IE1117 - Temas especiales II en máquinas eléctricas: Energía solar fotovoltaica TAREA 3 Josué Otárola Sánchez A84674 Ejercicio 2: Cambio de polaridad en la celda solar El montaje realizado se resume en
REACCIONES REVERSIBLES. ASPECTOS PRÁCTICOS DEL EQUILIBRIO QUÍMICO
 III 1 PRÁCTICA 3 REACCIONES REVERSIBLES. ASPECTOS PRÁCTICOS DEL EQUILIBRIO QUÍMICO En esta experiencia estudiaremos, cualitativamente, algunos aspectos prácticos del euilibrio uímico. Para ello: Experimentaremos
III 1 PRÁCTICA 3 REACCIONES REVERSIBLES. ASPECTOS PRÁCTICOS DEL EQUILIBRIO QUÍMICO En esta experiencia estudiaremos, cualitativamente, algunos aspectos prácticos del euilibrio uímico. Para ello: Experimentaremos
2.- 1 1 2 51 2,5 MW 0,6 1) A
 Problemas Tema 4 Problema 1.- Un alternador de 2,5 MW, 50 Hz, tiene una constante del regulador de 1 MW/Hz. El generador tiene en vacío una frecuencia de 51 Hz. Calcular: 1) Cuál será la frecuencia a la
Problemas Tema 4 Problema 1.- Un alternador de 2,5 MW, 50 Hz, tiene una constante del regulador de 1 MW/Hz. El generador tiene en vacío una frecuencia de 51 Hz. Calcular: 1) Cuál será la frecuencia a la
CAPITULO II Espectroscopia del infrarrojo
 CAPITULO II Espectroscopia del infrarrojo 2.1 Región del infrarrojo Los enlaces químicos que unen entre sí a los átomos de una molécula, no son rígidos, sino que se comportan con efectos de elasticidad
CAPITULO II Espectroscopia del infrarrojo 2.1 Región del infrarrojo Los enlaces químicos que unen entre sí a los átomos de una molécula, no son rígidos, sino que se comportan con efectos de elasticidad
MANUAL DE LAB ELECTRICIDAD Y MAGNETISMO
 POTENCIA ELECTRICA EXPERIENCIA N 5 1. OBJETIVOS. 1. Mostrar la potencia eléctrica como función del voltaje y de la corriente, calculando y midiendo la potencia disipada en una resistencia conforme aumenta
POTENCIA ELECTRICA EXPERIENCIA N 5 1. OBJETIVOS. 1. Mostrar la potencia eléctrica como función del voltaje y de la corriente, calculando y midiendo la potencia disipada en una resistencia conforme aumenta
FOTOLUMINISCENCIA MOLECULAR
 FOTOLUMINISCENCIA MOLECULAR El término luminiscencia lo introdujo por primera vez el físico e historiador científico alemán Eilhard Wiedemann en el año 1888 Luminescencia es la emisión de luz de una sustancia
FOTOLUMINISCENCIA MOLECULAR El término luminiscencia lo introdujo por primera vez el físico e historiador científico alemán Eilhard Wiedemann en el año 1888 Luminescencia es la emisión de luz de una sustancia
Problemas de Óptica Física
 Problemas de Óptica Física Cte. de Planck: h= 6.6x10-34 J.s= 4.1x10-15 ev.s Velocidad de la luz en el vacío: c = 3x10 8 m/s Problema 1 Si se observa en una pantalla alejada el patrón de difracción al hacer
Problemas de Óptica Física Cte. de Planck: h= 6.6x10-34 J.s= 4.1x10-15 ev.s Velocidad de la luz en el vacío: c = 3x10 8 m/s Problema 1 Si se observa en una pantalla alejada el patrón de difracción al hacer
Medición de la constante de Planck Efecto fotoeléctrico Faraggi Marisa y Sapoznik Marysol
 Medición de la constante de Planck Efecto fotoeléctrico Faraggi Marisa y Sapoznik Marysol Laboratorio 5- Curso de verano 2001 Resumen En el siguiente informe se quiere determinar la constante de Planck,
Medición de la constante de Planck Efecto fotoeléctrico Faraggi Marisa y Sapoznik Marysol Laboratorio 5- Curso de verano 2001 Resumen En el siguiente informe se quiere determinar la constante de Planck,
TEMA 5 CINÉTICA QUÍMICA
 TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
Unidades de masa atómica
 Unidades de masa atómica La estructura química y las fórmulas químicas sirven para estudiar las relaciones de masa de átomos y moléculas. Estas relaciones ayudan a explicar la composición de los compuestos
Unidades de masa atómica La estructura química y las fórmulas químicas sirven para estudiar las relaciones de masa de átomos y moléculas. Estas relaciones ayudan a explicar la composición de los compuestos
Funciones de varias variables: problemas propuestos
 Funciones de varias variables: problemas propuestos BENITO J. GONZÁLEZ RODRÍGUEZ ([email protected]) DOMINGO HERNÁNDEZ ABREU ([email protected]) MATEO M. JIMÉNEZ PAIZ ([email protected]) M. ISABEL MARRERO RODRÍGUEZ
Funciones de varias variables: problemas propuestos BENITO J. GONZÁLEZ RODRÍGUEZ ([email protected]) DOMINGO HERNÁNDEZ ABREU ([email protected]) MATEO M. JIMÉNEZ PAIZ ([email protected]) M. ISABEL MARRERO RODRÍGUEZ
INTRODUCCION A LA ESPECTROSCOPIA DE ABSORCION MOLECULAR UV/VIS Y DE INFRARROJO CERCANO. Cap. 13
 INTRODUCCION A LA ESPECTROSCOPIA DE ABSORCION MOLECULAR UV/VIS Y DE INFRARROJO CERCANO Cap. 13 Medición de la absorbancia y la transmitancia Recipiente produce pérdidas por: reflexión (aire/pared, pared/solución)
INTRODUCCION A LA ESPECTROSCOPIA DE ABSORCION MOLECULAR UV/VIS Y DE INFRARROJO CERCANO Cap. 13 Medición de la absorbancia y la transmitancia Recipiente produce pérdidas por: reflexión (aire/pared, pared/solución)
PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA
 PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo
PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo
Tema 13: La materia Ciencias Naturales 1º ESO página 1. Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
 Tema 13: La materia Ciencias Naturales 1º ESO página 1 TEMA 13: LA MATERIA, BASE DEL UNIVERSO 1. Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
Tema 13: La materia Ciencias Naturales 1º ESO página 1 TEMA 13: LA MATERIA, BASE DEL UNIVERSO 1. Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
FÍSICA MODERNA FCA 04 ANDALUCÍA. partícula alfa. Escriba la reacción nuclear y determine las características del núclido X resultante.
 6. En la reacción del Li 3 con un neutrón se obtiene un núclido X y una partícula alfa. Escriba la reacción nuclear y determine las características del núclido X resultante. b) Calcule la energía liberada
6. En la reacción del Li 3 con un neutrón se obtiene un núclido X y una partícula alfa. Escriba la reacción nuclear y determine las características del núclido X resultante. b) Calcule la energía liberada
GUÍA DE PROBLEMAS. Cinética Química
 GUÍA DE PROBLEMAS 1) Deduzca las ecuaciones matemáticas que representan la cinética química para las reacciones de cero, primer y segundo orden. Asimismo, establezca la ecuación para cuando la concentración
GUÍA DE PROBLEMAS 1) Deduzca las ecuaciones matemáticas que representan la cinética química para las reacciones de cero, primer y segundo orden. Asimismo, establezca la ecuación para cuando la concentración
CÁLCULO DE LA CONSTANTE DE PROPORCIONALIDAD DE LA LEY DE COULOMB
 CÁLCULO DE LA CONSTANTE DE PROPORCIONALIDAD DE LA LEY DE COULOMB HÉCTOR BARCO R.,* EDILBERTO ROJAS C.* PC: Coulomb, Electrostática, Balanza, Torsión RESUMEN En este artículo se presentan los resultados
CÁLCULO DE LA CONSTANTE DE PROPORCIONALIDAD DE LA LEY DE COULOMB HÉCTOR BARCO R.,* EDILBERTO ROJAS C.* PC: Coulomb, Electrostática, Balanza, Torsión RESUMEN En este artículo se presentan los resultados
ESPECTROSCOPÍA ESPECTROSCOPÍA INFRARROJA INTERPRETACIÓN ESPECTRO IR
 ESPECTROSCOPÍA ESPECTROSCOPÍA INFRARROJA INTERPRETACIÓN ESPECTRO IR Espectroscopia infrarroja (Espectroscopia IR) es la rama de la espectroscopia que trata con la parte infrarroja del espectro electromagnético.
ESPECTROSCOPÍA ESPECTROSCOPÍA INFRARROJA INTERPRETACIÓN ESPECTRO IR Espectroscopia infrarroja (Espectroscopia IR) es la rama de la espectroscopia que trata con la parte infrarroja del espectro electromagnético.
Práctica 2 - Circuitos, instrumentos de medición, elementos de protección y detección de equipos en falla
 VIII curso de EEIBS -Práctica 2- Núcleo de Ingeniería Biomédica Facultades de Medicina e Ingeniería UdelaR. Práctica 2 - Circuitos, instrumentos de medición, elementos de protección y detección de equipos
VIII curso de EEIBS -Práctica 2- Núcleo de Ingeniería Biomédica Facultades de Medicina e Ingeniería UdelaR. Práctica 2 - Circuitos, instrumentos de medición, elementos de protección y detección de equipos
FLUORESCENCIA. TM. Franna Bacic TM. Pablo Cabrera TM. Carlos Zamorano BQ. Javiera villar
 FLUORESCENCIA 2014 TM. Franna Bacic TM. Pablo Cabrera TM. Carlos Zamorano BQ. Javiera villar Fluorescencia Es un fenómeno de luminiscencia. La fluorescencia es un proceso de emisión en el cual las moléculas
FLUORESCENCIA 2014 TM. Franna Bacic TM. Pablo Cabrera TM. Carlos Zamorano BQ. Javiera villar Fluorescencia Es un fenómeno de luminiscencia. La fluorescencia es un proceso de emisión en el cual las moléculas
Reacciones Oxido- Reducción (REDOX)
 Reacciones Oxido- Reducción (REDOX) Se llama Reacción Óxido-Reducción (REDOX) a una transferencia de electrones entre átomos. Por ejemplo: Cu +2 + e- Cu + Donde el signo + en el átomo de cobre que se encuentra
Reacciones Oxido- Reducción (REDOX) Se llama Reacción Óxido-Reducción (REDOX) a una transferencia de electrones entre átomos. Por ejemplo: Cu +2 + e- Cu + Donde el signo + en el átomo de cobre que se encuentra
TEMA 5 COMUNICACIONES ANALÓGICAS
 TEMA 5 COMUNICACIONES ANALÓGICAS Modulaciones angulares Introducen la información exclusivamente en la fase de una portadora, manteniendo constante la amplitud y(t )= A c cos[ω c t +ϕ(t)] La potencia media,
TEMA 5 COMUNICACIONES ANALÓGICAS Modulaciones angulares Introducen la información exclusivamente en la fase de una portadora, manteniendo constante la amplitud y(t )= A c cos[ω c t +ϕ(t)] La potencia media,
El brillo de los cuerpos celestes: Flujos, magnitudes y colores. Dr. Lorenzo Olguín R. Universidad de Sonora
 El brillo de los cuerpos celestes: Flujos, magnitudes y colores Dr. Lorenzo Olguín R. Universidad de Sonora Luminosidad y Flujo La luminosidad L de un objeto, es la cantidad de energía que emite por unidad
El brillo de los cuerpos celestes: Flujos, magnitudes y colores Dr. Lorenzo Olguín R. Universidad de Sonora Luminosidad y Flujo La luminosidad L de un objeto, es la cantidad de energía que emite por unidad
CINÉTICA DE LA REACCIÓN DEL COLORANTE AZUL BRILLANTE CON HIPOCLORITO DE SODIO
 Página: 1/5 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 6: CINÉTICA DE LA REACCIÓN DEL COLORANTE AZUL BRILLANTE CON HIPOCLORITO DE SODIO Bibliografía: Química General, Quinta Edición, K. Whitten, R. Davis, M.
Página: 1/5 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 6: CINÉTICA DE LA REACCIÓN DEL COLORANTE AZUL BRILLANTE CON HIPOCLORITO DE SODIO Bibliografía: Química General, Quinta Edición, K. Whitten, R. Davis, M.
Solución: a) Falso, porque la carga que se apiña en lo que se denomina núcleo es toda la carga positiva.
 ies menéndez tolosa 1 De las siguientes proposiciones, señala las que considere correctas: a) Todos los isótopos de un elemento tienen el mismo número de electrones. b) Dos isótopos de un elemento pueden
ies menéndez tolosa 1 De las siguientes proposiciones, señala las que considere correctas: a) Todos los isótopos de un elemento tienen el mismo número de electrones. b) Dos isótopos de un elemento pueden
LABORATORIO N 2 PREPARACIÓN DE SOLUCIONES
 LABORATORIO N 2 PREPARACIÓN DE SOLUCIONES I.- INTRODUCCIÓN A) Soluciones La materia puede presentarse en forma de mezclas o sustancias puras. Cuando una mezcla tiene una composición uniforme, en cualquier
LABORATORIO N 2 PREPARACIÓN DE SOLUCIONES I.- INTRODUCCIÓN A) Soluciones La materia puede presentarse en forma de mezclas o sustancias puras. Cuando una mezcla tiene una composición uniforme, en cualquier
