CURSO 2016 / Tema 3. Sistemas. materiales. Física y química para 2º ESO. Nombre..
|
|
|
- María Jesús Serrano Lagos
- hace 6 años
- Vistas:
Transcripción
1 CURSO 2016 / 2017 Tema 3. Sistemas materiales. Física y química para 2º ESO Nombre..
2 Índice general: 1. Concepto de mezcla. Tipos. 2. Las disoluciones. 3. Tipos de disoluciones Según el estado físico de los componentes Según la proporción entre los componentes. 4. Concentración de las disoluciones. 5. Técnicas de separación de mezclas Separación de mezclas heterogéneas Separación de mezclas homogéneas. En esta unidad vas a aprender que las sustancias pueden mezclarse de manera que, en unos casos, los componentes puedan observarse a simple vista, mientras que en otros seas incapaz de saber si estás ante una sustancia pura o ante una mezcla. Para empezar, vas a preparar una mezcla tan sencilla que puedes hacerla en casa. Toma un poco de arena y unas piedras, y mézclalas entre sí. Describe lo que observas. Se distinguen ambas sustancias a simple vista? Sabrías cómo separarlas? Ahora mezcla entre sí la arena con limaduras o polvo de hierro. Describe lo que observas. Se distinguen ambas sustancias a simple vista? Sabrías cómo separarlas? El método para separar una mezcla como esta se denomina imantación. Estas experiencias son sencillas, pero al final de la unidad vas a conocer otros métodos de separación de mezclas más complejos.
3 Los sistemas materiales se pueden clasificar en: Sustancia pura: es aquella en la que, sea cual sea su estado de agregación, sus propiedades, tanto físicas como químicas, son uniformes en cualquier parte de ella, caracterizándola y permitiendo diferenciarla de otras sustancias. El agua se puede descomponer, mediante un proceso químico, en hidrógeno y oxígeno, pero no hay ningún procedimiento que nos permita descomponer el hidrógeno y el oxígeno en otras sustancias más simples. Así dentro de las sustancias puras distinguimos dos tipos: Compuestos: son sustancias puras que se pueden descomponer en otras más simples por medio de un proceso químico. Elementos: son sustancias puras que nos e pueden descomponer en otras más simples por ningún procedimiento. Mezcla: es un sistema material en el que se han combinado dos o más sustancias puras cuya proporción puede ser variable. Podemos distinguir dos tipos de mezclas: Mezcla heterogénea: es una mezcla en la que es posible distinguir sus componentes por procedimientos ópticos. Sus partículas son superiores a 10-6 m. Sistemas coloidales: en el límite entre las mezclas heterogéneas y las homogéneas se encuentran los sistemas coloidales. Se trata de mezclas que tienen, al menos, dos fases, una de ellas finamente dividida en pequeñas partículas (entre 10-6 y 10-9 m) a las que rodea completamente la otra sustancia. Mezcla homogénea o disolución: es una mezcla en la que no es posible distinguir sus componentes por procedimientos ópticos convencionales. Las partículas de la fase dispersa son inferiores a 10-9 m.
4 I. Dibuja cómo son y cómo se encuentran las partículas en cada uno de los casos: SUSTANCIAS PURAS ELEMENTO COMPUESTO MEZCLAS HETEROGÉNEA COLOIDAL HOMOGÉNEA
5 En la siguiente tabla se indica los principales tipos de sistemas coloidales: FASE DISPERSA SÓLIDO LÍQUIDO GAS FASE DISPERSANTE SÓLIDO Geles, jalea Espumas, piedra pómez LÍQUIDO Soles, pintura Emulsiones, mahonesa Espumas, nata batida GAS ---- Aerosoles, espray ---- En este vídeo se muestran los diferentes tipos de coloides con muchos ejemplos. Incluso del efecto Tyndall. goo.gl/cazbx9 Una disolución es una mezcla homogénea de dos o más compuestos. Cuando una sustancia se disuelve en otra, se produce la separación y posterior dispersión de las partículas de uno de los componentes en el otro. El componente que está en menor proporción se denomina soluto. El componente que está en mayor proporción es el disolvente. Cuando los componentes de una disolución están en proporciones similares, el disolvente será aquella sustancia que se encuentre en el mismo estado de agregación que la disolución final.
6 II. Completa el cuadro: DISOLUCIÓN ESTADO DISOLUCIÓN ESTADO SOLUTO ESTADO DISOLVENTE Agua azucarada Alcohol sanitario Cava Aire Bronce Cómo se forman las disoluciones? Observa esta animación que permite ver cómo se disuelve un terrón de azúcar en agua a nivel molecular: goo.gl/qegckx
7 III. Qué ocurre si agitamos con una cuchara los componentes? IV. Qué sucede si aumentamos la temperatura del recipiente que los contiene?
8 3.1 SEGÚN EL ESTADO FÍSICO DE LOS COMPONENTES. V. Identifica las sustancias componentes de los ejemplos incluidos en la tabla anterior, busca información en textos o Internet. Disoluciones gaseosas: como las partículas de los gases se mueven libremente, se difunden entre sí con gran facilidad, y se consigue una mezcla homogénea con gran rapidez. El ejemplo más importante es el aire. Contiene una mezcla de gases en proporciones ligeramente variables: nitrógeno (78%), oxígeno (21%) y otros, como el dióxido de carbono (0,03%) y argón (0,93%). Disoluciones líquidas: las más importantes son las que implican al agua. Cuando las fuerzas con las que las moléculas del disolvente atraen a las partículas del sólido son mayores que las que ejercen ellas entre sí, consiguen separarlas y dispersarlas, formándose la disolución. Para que los líquidos formen una disolución
9 deben tener la propiedad de ser totalmente miscibles entre sí. Los gases se disuelven siempre en agua, en mayor o menor proporción, dependiendo de la presión que se les administre. Así se forman las bebidas carbónicas, como colas, tónicas, gaseosas, etc. El oxígeno disuelto en ríos y mares permite la vida animal y vegetal en su interior. Disoluciones sólidas: las más importantes son las aleaciones. Una aleación es una mezcla de metales que se obtiene agregando los componentes fundidos y enfriando la mezcla. Algunos ejemplos son el bronce, el acero y el latón. 3.2 SEGÚN LA PROPORCIÓN DE LOS COMPONENTES. La solubilidad es la máxima cantidad de solutos que se puede disolver en una determinada cantidad de disolvente. Es una proporción fija para cada pareja de soluto y disolvente a una temperatura determinada. La solubilidad se suele expresar en gramos de soluto por litro de disolvente (g/l). Hay diferentes tipos de disoluciones en función de la cantidad de soluto que vayas a disolver: Disolución diluida: en ella la cantidad de soluto es pequeña comparada con la solubilidad. Disolución concentrada: aquella en la que la cantidad de soluto es cercana a la solubilidad. Disolución saturada: aquella que no admite más cantidad de soluto sin añadir más disolvente a una determinada temperatura. La proporción entre soluto y disolvente es la máxima posible. En el fondo del recipiente aparece algo de soluto que ya no se puede disolver.
10 Según las características de cada soluto y de cada disolvente, la saturación se alcanzará antes o después. Se llama disolución sobresaturada a aquella que contiene más cantidad de soluto disuelto del que puede disolver. Se consigue aumentando la presión (en el caso de solutos gases) o la temperatura (en los solutos sólidos) y, luego, dejándola enfriar lentamente para conseguir que, al enfriarse, el exceso no precipite al fondo del vaso. Existen algunos factores que afectan a la solubilidad: Superficie de contacto: al aumentar, lo que se favorece por la pulverización del soluto, aumenta la rapidez de disolución porque las interacciones entre las partículas de soluto-disolvente son mayores. Agitación: al disolverse el soluto, las partículas deben difundirse por todo el disolvente. La agitación favorece la movilidad, aumentando la disolución. Temperatura: afecta a la rapidez y al grado de solubilidad. Al aumentar la temperatura se favorece el movimiento de las moléculas en la disolución. Además, provoca el aumento de la energía de las partículas que forman el soluto, lo que induce a una mayor facilidad de disgregación. En el caso de los gases, este mismo proceso de aumento de velocidad por aumento térmico provoca justamente lo contrario: que disminuya su solubilidad.
11 Presión: en el caso de solutos gases, su solubilidad es directamente proporcional a la presión. Es fácil observar cómo al abrir una botella que contiene una bebida con gas en su interior disminuye su presión y el gas abandona rápidamente la disolución, saliendo en forma de «explosión» de burbujas. En este vídeo se muestra la fabricación industrial de las bebidas carbónicas. goo.gl/4hcwjk Para conocer la composición concreta de una disolución emplearemos el concepto de concentración, que expresa de forma numérica la relación en que se encuentra el soluto frente al disolvente o la disolución. Concentración en porcentaje de masa Concentración % masa Masa g de soluto 100 Masa g de soluto Masa g de disolvente Concentración en porcentaje de volumen Concentración % volumen Volumen de soluto 100 Volumen de disolución Concentración en gramo por litro Concentración g/l Masa g de soluto 100 Volumen de disolución L
12 Ejemplo 1 Calcula la concentración en porcentaje de masa de una disolución de 20 g de cloruro de sodio (NaCl) en 0,3 L de agua (d=1kg/l). Ejemplo 2 Calcula la concentración expresada en porcentaje de volumen de una disolución preparada con 200 ml de alcohol etílico a la que hemos añadido agua hasta completar 500 ml de disolución. Ejemplo 3 Cuántos gramos de una disolución de cloruro sódico (NaCl) al 10 % en masa son necesarios para tener 20 g de NaCl puro?
13 Cuando dos o más sustancias se mezclan No hay reacción química Por tanto Sus propiedades químicas se conservan Entonces Se podrían volver a separar por procedimientos físicos 5.1 SEPARACIÓN DE MEZCLAS HETEROGÉNEAS. Filtración: se utiliza para separar líquidos y sólidos no solubles. Decantación: separar dos o más líquidos que no se mezclan. Centrifugación: separar líquidos y sólidos no solubles. Separación magnética: separar limaduras de hierro, por ejemplo.
14 5.2 SEPARACIÓN DE MEZCLAS HOMOGÉNEAS. Cristalización: un sólido soluble en el seno de un líquido. En estos casos, el compuesto que deseamos obtener debe ser soluble en un disolvente caliente y poco soluble en el mismo disolvente frío, siendo las impurezas que queremos separar insolubles en este mismo disolvente. Destilación: dos o más líquidos que se mezclan. Se basa en las distintas temperaturas de ebullición de las sustancias. Cromatografía: técnica empleada para reconocer las sustancias de una disolución, no para separarlas. Se basa en la distinta velocidad de difusión que sobre un mismo soporte tienen diferentes sustancias.
15 Actividades finales Actividades básicas 1 Indica cuáles de las siguientes mezclas son homogéneas y cuáles, heterogéneas: gaseosa, infusión de hierbas, batido de frutas, tazón de chocolate líquido y un cuenco lleno de arena y lentejas. 3 Cuáles de las siguientes mezclas son coloides: sangre, saliva, espuma de afeitar, jalea, ADN y amoniaco en agua. 4 Busca información en Internet acerca del rango de tamaño de las partículas existentes en el caso de mezclas homogéneas, heterogéneas y coloides. 5 Explica por qué unas sustancias no son capaces de disolver a otras. 6 Indica en qué tipo de disolución existe mayor proporción de soluto, en una disolución saturada o en una disolución muy concentrada? 7 Existen disoluciones con más de un soluto? Y con más de un disolvente? 8 Calcula la cantidad de una disolución de cloruro de potasio (KCl) al 15 % en masa que se necesita para obtener 12 g de soluto puro. Y si el caso fuera con una disolución de cloruro de sodio (NaCl)? 9 Calcula el porcentaje en masa que existe de cada componente de una disolución formada por 350 ml de agua y 15 g de azúcar. 10 Una disolución puede ser diluida y saturada al mismo tiempo? 11 Si la solubilidad del azúcar en agua es de 200 g/l a 20 ºC, qué cantidad de azúcar podremos disolver en 300 ml de agua a esa misma temperatura? 12 Escribe la diferencia entre una disolución saturada y otra sobresaturada. Cómo puedes transformar la sobresaturada en saturada? 13 Si quieres separar una mezcla de hierro en polvo con agua, qué método emplearías? 14 A partir de la gráfica indica cuál sería la solubilidad del clorato de potasio a 80 ºC.
16 15 Para tratar una herida, el médico te ha dicho que tienes que preparar una disolución de alcohol en agua al 35 %, si el alcohol del botiquín indica que es del 70 %, cómo lo harías? 16 Cuáles de las siguientes técnicas de separación de mezclas te permiten trabajar después con todos los componentes que hayas separado? A Cromatografía. B Recristalización. C Decantación. 17 Busca información en Internet e indica tres aleaciones importantes diferentes de las comentadas en la unidad. 18 En un experimento en el que destilas una disolución de sal común (cloruro de sodio) en agua, qué es lo que queda en el matraz de destilación cuando has separado toda el agua? 19 Qué método de separación de mezclas se está produciendo en la realidad en los terrenos que contienen salinas naturales? 20 Hemos visto en el texto que la solubilidad aumenta con la temperatura. Busca en Internet los valores de la solubilidad del cloruro sódico (NaCl) a distintas temperaturas y contesta, basándote en ello, la sal en las comidas se debe echar cuando están calientes o frías? Actividades de consolidación 21 Por qué al agitar una botella con una bebida carbónica los gases salen con más violencia que si no la agitas? 22 Los fabricantes de planchas indican que es mejor utilizar agua destilada en las planchas que agua del grifo, por qué crees que lo recomiendan?
17 23 Alguna vez habrás visto leche agria, en mal estado. Por qué ocurre eso? Qué fases eres capaz de observar en ella? 24 La cantidad de alcohol en las bebidas se expresa en grados. Qué significado tienen esos grados? 25 Explica detalladamente cómo prepararías 200 ml de una disolución de nitrato de sodio (NaNO3) al 12 % de masa si cuentas con un matraz de 100 ml. 26 Habrás observado que cuando sacas la ropa de la lavadora aparece húmeda pero sin gotear, por qué crees que pasa eso? Actividades avanzadas 27 A lo largo de un día cualquiera realizas tareas como estas: a) añades sal a la sopa, b) agregas azúcar a la leche, c) preparas un café, d) elaboras una mayonesa. Indica cuáles son disoluciones y cuáles coloides. 28 Se tiene una disolución de sal (NaCl) en agua al 20 % en masa. Si coges 100 g de ella, qué cantidad de sal obtendrás cuando se evapore todo el disolvente? 29 Si quieres preparar una disolución de hidróxido de potasio en agua de 2,5 g/l que contenga 20 g del soluto, qué cantidad de disolución debes obtener? 30 Si tienes una disolución al 30 % en masa, cuál sería la nueva concentración si añades agua suficiente hasta duplicar su volumen? 31 El amoniaco casero es una disolución de gas amoniaco en agua. Calcula la cantidad de amoniaco puro que contiene una botella casera que tiene un volumen de 0,25 L si su concentración es del 3 % en volumen. 32 Tienes una disolución de carbonato de sodio en agua (Na2CO3) del 25 %, a qué concentración equivale, expresada en g/l? 33 Qué cantidad de alcohol deberás añadir sobre agua para obtener 350 ml de disolución de alcohol en agua al 15 % en volumen? 34 Busca información en Internet y prepara un mural con las diferentes formas de contaminación medioambiental que provocan los coloides. 35 El agua de mar es una disolución de sal común en agua. En algunas poblaciones, como por ejemplo las islas, es preciso desalinizar el agua marina para conseguir agua potable. Busca información, y con ella explica las técnicas empleadas habitualmente para conseguirlo.
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
PROBLEMAS MEZCLAS Y DISOLUCIONES
 PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
Tema 7. Las mezclas. Introducción
 Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
FÍSICA Y QUÍMICA 2º ESO Tema 2: LA MATERIA Mezclas y Soluciones. Sustancias puras y mezclas
 Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
1. La materia: sustancias puras y mezclas
 RESUMEN de la UNIDAD 3. DIVERSIDAD DE LA MATERIA 1. La materia: sustancias puras y mezclas La principal clasificación que se hace de la materia es en sustancias puras y mezclas. Las sustancias puras tienen
RESUMEN de la UNIDAD 3. DIVERSIDAD DE LA MATERIA 1. La materia: sustancias puras y mezclas La principal clasificación que se hace de la materia es en sustancias puras y mezclas. Las sustancias puras tienen
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
LA DIVERSIDAD DE LA MATERIA
 Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia. Sistemas materiales Sustancias puras Mezclas Un solo componente Dos o mas componentes Simples Compuestas Homogénas Heterogénas Un solo tipo de átomo.
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia. Sistemas materiales Sustancias puras Mezclas Un solo componente Dos o mas componentes Simples Compuestas Homogénas Heterogénas Un solo tipo de átomo.
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
Disoluciones Químicas
 Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
CLASIFICACIÓN DE LA MATERIA
 Separación de sustancias Elementos y compuestos Fernández Monroy, Mª Ernestina; Gutiérrez Múzquiz, Félix A. y Marco Viñes, José Manuel Física y Química: guía interactiva para la resolución de ejercicios
Separación de sustancias Elementos y compuestos Fernández Monroy, Mª Ernestina; Gutiérrez Múzquiz, Félix A. y Marco Viñes, José Manuel Física y Química: guía interactiva para la resolución de ejercicios
TEMA 2: DIVERSIDAD DE LA MATERIA
 TEMA 2: DIVERSIDAD DE LA MATERIA 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.- Propiedades generales y características de la materia.
TEMA 2: DIVERSIDAD DE LA MATERIA 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.- Propiedades generales y características de la materia.
LA MATERIA Y SU DIVERSIDAD
 LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
Disoluciones y cálculos de concentraciones
 Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Clasificación de la materia
 Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA
 FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química.
 Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
U.D. 2 LA MATERIA. Para describir un cuerpo o un sistema material, necesitamos conocer sus propiedades. Así, distinguimos entre:
 U.D. 2 LA MATERIA 1. Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Para describir
U.D. 2 LA MATERIA 1. Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Para describir
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
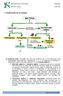 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
Tema 2: Dispersiones (1) Material preparado por VChan 1
 MATERIA: Cualquier cosa que ocupa espacio y tiene masa. Es todo lo que nos rodea. 2.1 Proceso de disolución Velocidad de disolución Material preparado por: Licda. Victoria Chan Escuela de Química/ ITCR
MATERIA: Cualquier cosa que ocupa espacio y tiene masa. Es todo lo que nos rodea. 2.1 Proceso de disolución Velocidad de disolución Material preparado por: Licda. Victoria Chan Escuela de Química/ ITCR
2. Métodos de separación de los componentes de una mezcla.
 TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso)
 Física y Química 4 ESO DISOLUCIONES Pág. 1 SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso) Pág. 2 DISOLUCIONES Física y Química 4 ESO DISOLUCIONES CONCEPTO DE DISOLUCIÓN. COMPONENTES DE UNA DISOLUCIÓN. Una
Física y Química 4 ESO DISOLUCIONES Pág. 1 SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso) Pág. 2 DISOLUCIONES Física y Química 4 ESO DISOLUCIONES CONCEPTO DE DISOLUCIÓN. COMPONENTES DE UNA DISOLUCIÓN. Una
TEMA 3.- Naturaleza de la. materia (II)
 TEMA 3.- Naturaleza de la 1.- Concepto de mezcla. Tipos. materia (II) ÍNDICE GENERAL 2.- Separación de los componentes de una mezcla. 2.1.- Separación de los componentes de mezclas heterogéneas. 2.1.1.-
TEMA 3.- Naturaleza de la 1.- Concepto de mezcla. Tipos. materia (II) ÍNDICE GENERAL 2.- Separación de los componentes de una mezcla. 2.1.- Separación de los componentes de mezclas heterogéneas. 2.1.1.-
1. Disoluciones una disolución es cualquier mezcla homogénea disolvente soluto Medidas de composición
 1. Disoluciones En general, una disolución es cualquier mezcla homogénea. Por ejemplo, el aire, mezcla de nitrógeno, oxígeno y otros gases en proporciones menores; o el bronce, que es una aleación metálica
1. Disoluciones En general, una disolución es cualquier mezcla homogénea. Por ejemplo, el aire, mezcla de nitrógeno, oxígeno y otros gases en proporciones menores; o el bronce, que es una aleación metálica
Escuela del Petróleo - Química
 Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
TEMA 3: Composición de la Materia
 TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
FyQ 1. IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química Unidad Didáctica 2
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
Disoluciones. Química General II 2011
 Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
03 DISOLUCIONES. 2 Observando la curva de solubilidad del clorato potásico, responder:
 03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN.
 MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
SOLUCIONES SOLIDA LIQUIDA GASEOSA. mezclas homogéneas de dos sustancias: SEGÚN EL ESTADO FISICO DEL SOLVENTE
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Sustituir fotografía. Sustituir texto
 Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Disoluciones. Qué es una mezcla? Concepto de Mezcla 12/05/2014
 Disoluciones Profesora: Karina Oñate Fuentes Asignatura: Química- Plan común Nivel: 2º año medio Qué es una mezcla? Los compuestos químicos pueden unirse para reaccionar o mezclarse. En el primer caso
Disoluciones Profesora: Karina Oñate Fuentes Asignatura: Química- Plan común Nivel: 2º año medio Qué es una mezcla? Los compuestos químicos pueden unirse para reaccionar o mezclarse. En el primer caso
TEMA 2: Diversidad de la materia. T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1
 TEMA 2: Diversidad de la materia T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1 ESQUEMA DE LA UNIDAD 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.-
TEMA 2: Diversidad de la materia T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1 ESQUEMA DE LA UNIDAD 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.-
Soluciones y unidades de concentración
 MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
Soluciones y unidades de concentración
 Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES.
 EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
DISOLUCIONES 1.- QUÉ ES UNA DISOLUCIÓN?
 DISOLUCIONES 1.- QUÉ ES UNA DISOLUCIÓN? Disoluciones, en química, mezclas homogéneas de dos o más sustancias. El soluto es el componente que se encuentra en distinto estado físico que la disolución; y
DISOLUCIONES 1.- QUÉ ES UNA DISOLUCIÓN? Disoluciones, en química, mezclas homogéneas de dos o más sustancias. El soluto es el componente que se encuentra en distinto estado físico que la disolución; y
2. MECANISMO DE DISOLUCIÓN Y DE HIDRATACIÓN DE IONES.
 1. QUÉ ES UNA DISOLUCIÓN? Disoluciones, en química, mezclas homogéneas de dos o más sustancias. El soluto es el componente que se encuentra en distinto estado físico que la disolución; y el disolvente
1. QUÉ ES UNA DISOLUCIÓN? Disoluciones, en química, mezclas homogéneas de dos o más sustancias. El soluto es el componente que se encuentra en distinto estado físico que la disolución; y el disolvente
Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas:
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas: Plomo ; acero ; mercurio ; óxido de hierro
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas: Plomo ; acero ; mercurio ; óxido de hierro
Acuerdo 286. Química. Disoluciones. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller DISOLUCIONES
 Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Clasificación de la materia
 Clasificación de la materia La materia puede estar en forma de sustancias puras o mezclas. Materia Sustancias Puras Mezclas Elemento Compuesto Homogéneas Heterogéneas Disoluciones Coloides Suspensiones
Clasificación de la materia La materia puede estar en forma de sustancias puras o mezclas. Materia Sustancias Puras Mezclas Elemento Compuesto Homogéneas Heterogéneas Disoluciones Coloides Suspensiones
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
CAPITULO 6 : Soluciones
 CAPITULO 6 : Soluciones Gran parte de los líquidos que conocemos o que manejamos habitualmente son soluciones o disoluciones. El agua de mar, la saliva, la orina, la lavandina, el vinagre y al agua que
CAPITULO 6 : Soluciones Gran parte de los líquidos que conocemos o que manejamos habitualmente son soluciones o disoluciones. El agua de mar, la saliva, la orina, la lavandina, el vinagre y al agua que
TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO
 TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO 1. Clasificaciones de los sistema materiales. Un sistema material es una porción de materia que se separa para facilitar su estudio experimental. Como existe
TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO 1. Clasificaciones de los sistema materiales. Un sistema material es una porción de materia que se separa para facilitar su estudio experimental. Como existe
Sustancias puras y mezclas: Qué es una sustancia? Qué es una sustancia pura?: Clasificación de las sustancias puras: elementos y compuestos;
 SEXTO Sustancias puras y mezclas: Qué es una sustancia?: Es cualquier variedad de materia que tiene composición definida y reconocible. Las sustancias se clasifican en sustancias puras y mezclas. Qué es
SEXTO Sustancias puras y mezclas: Qué es una sustancia?: Es cualquier variedad de materia que tiene composición definida y reconocible. Las sustancias se clasifican en sustancias puras y mezclas. Qué es
E.E.T. Nº9. Físico-Química de 2do año. Guía Nº3. Profesor: Alumno: Curso:
 E.E.T. Nº9 Físico-Química de 2do año Guía Nº3 Profesor: Alumno: Curso: Soluciones Una solución es un sistema homogéneo formado por dos o más componentes. En una solución formada por dos componentes se
E.E.T. Nº9 Físico-Química de 2do año Guía Nº3 Profesor: Alumno: Curso: Soluciones Una solución es un sistema homogéneo formado por dos o más componentes. En una solución formada por dos componentes se
I. TEORÍA ATÓMICO-MOLECULAR
 Índice 1. La materia 2. Clasificación de la materia 3. Leyes ponderales 4. Teoría atómica de Dalton 5. Leyes volumétricas 6. La unidad de cantidad de materia: el mol 2 1 La materia Materia es todo aquello
Índice 1. La materia 2. Clasificación de la materia 3. Leyes ponderales 4. Teoría atómica de Dalton 5. Leyes volumétricas 6. La unidad de cantidad de materia: el mol 2 1 La materia Materia es todo aquello
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración SGUICES010CB33-A16V1 Ítem Alternativa Habilidad 1 D Reconocimiento 2 A Reconocimiento 3 C
SOLUCIONARIO Guía Estándar Anual Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración SGUICES010CB33-A16V1 Ítem Alternativa Habilidad 1 D Reconocimiento 2 A Reconocimiento 3 C
ESTADOS DE AGREGACIÓN DE LA MATERIA
 LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
CURSO INTRODUCTORIO DE QUÍMICA
 CURSO INTRODUCTORIO DE QUÍMICA UNIDAD II. S MATERIALES INTRODUCCIÓN Se llama sistema material a una porción limitada de materia, dentro del universo, que se separa real o imaginariamente, para su estudio.
CURSO INTRODUCTORIO DE QUÍMICA UNIDAD II. S MATERIALES INTRODUCCIÓN Se llama sistema material a una porción limitada de materia, dentro del universo, que se separa real o imaginariamente, para su estudio.
PALACORRE. TEMA 2: Los cambios de aspecto de la materia I.E.S. LA CORREDORIA OVIEDO 1º ESO GRUPO: ALUMNO: DPTO. CIENCIAS NATURALES
 PALACORRE I.E.S. LA CORREDORIA OVIEDO DPTO. CIENCIAS NATURALES TEMA 2: Los cambios de aspecto de la materia 1º ESO ALUMNO: GRUPO: TEMA 2: LOS CAMBIOS DE ASPECTO DE LA MATERIA Nombre y apellidos: Fecha:
PALACORRE I.E.S. LA CORREDORIA OVIEDO DPTO. CIENCIAS NATURALES TEMA 2: Los cambios de aspecto de la materia 1º ESO ALUMNO: GRUPO: TEMA 2: LOS CAMBIOS DE ASPECTO DE LA MATERIA Nombre y apellidos: Fecha:
Para la solución de algunos de los ejercicios propuestos, se adjunta una parte del sistema periódico hasta el elemento Nº 20.
 Programa Estándar Anual Nº Guía práctica Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta
Programa Estándar Anual Nº Guía práctica Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta
1 Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es:
 IES Menéndez Tolosa 3º ESO (Física y Química) Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es: ( ) %peso = masade + masade 00 Completar las definiciones:
IES Menéndez Tolosa 3º ESO (Física y Química) Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es: ( ) %peso = masade + masade 00 Completar las definiciones:
Guía N 2 La materia y sus transformaciones
 Guía N 2 La materia y sus transformaciones Nombre: Curso: Fecha: Eje: La materia y sus transformaciones Objetivos: Describir algunas las propiedades de la materia Caracterizar los diferentes estados de
Guía N 2 La materia y sus transformaciones Nombre: Curso: Fecha: Eje: La materia y sus transformaciones Objetivos: Describir algunas las propiedades de la materia Caracterizar los diferentes estados de
FICHA 5: DISOLUCIONES %masa y % volumen
 FICHA 5: DISOLUCIONES %masa y % volumen 1. Calcula el % en masa de una disolución que contiene 30 g de soluto en 1 L de agua. Sol.: 2,9% 2. El vinagre es una disolución de ácido acético en agua al 3% en
FICHA 5: DISOLUCIONES %masa y % volumen 1. Calcula el % en masa de una disolución que contiene 30 g de soluto en 1 L de agua. Sol.: 2,9% 2. El vinagre es una disolución de ácido acético en agua al 3% en
DISOLUCIONES UNIDAD IV. Licda. Miriam Marroquín Leiva
 DISOLUCIONES UNIDAD IV 1 DISOLUCIÓN Es una mezcla homogénea de dos o más sustancias; el soluto y el disolvente. Es un término utilizado para describir un sistema en el cual una o más sustancias están mezcladas
DISOLUCIONES UNIDAD IV 1 DISOLUCIÓN Es una mezcla homogénea de dos o más sustancias; el soluto y el disolvente. Es un término utilizado para describir un sistema en el cual una o más sustancias están mezcladas
CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? 2. TÉCNICAS DE SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA.
 1. INTRODUCCIÓN. CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? Cuando una sustancia cualquiera contiene a otra distribuida en su seno como partículas muy pequeñas, se habla de un sistema disperso o de
1. INTRODUCCIÓN. CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? Cuando una sustancia cualquiera contiene a otra distribuida en su seno como partículas muy pequeñas, se habla de un sistema disperso o de
DISOLUCIONES. Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables.
 DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
MOL. Nº AVOGADRO DISOLUCIONES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
So S l o u l c u i c o i n o e n s e
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
1. Los estados de la materia
 1. Los estados de la materia Propiedades La materia que nos rodea aparece ante nosotros con muy diversos aspectos. Presenta distintas formas, colores, dureza, fluidez pero en general, consideramos que
1. Los estados de la materia Propiedades La materia que nos rodea aparece ante nosotros con muy diversos aspectos. Presenta distintas formas, colores, dureza, fluidez pero en general, consideramos que
LOS ESTADOS DE LA MATERIA
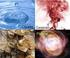 LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
PROPIEDADES DE LA MATERIA. Prof. Jackeline Ruttell torres Química Febrero 2017
 PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
LOS GASES Y LAS DISOLUCIONES. Departamento de Física y Química 3º ESO
 LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía.
 1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
INSTITUCIÒN EDUCATIVA JUAN MARIA CESPEDES. DOCENTE: Gissely A. Quintero S. ÁREA: Ciencias Naturales (Química) 11º
 INSTITUCIÒN EDUCATIVA Código: F-GA-024 EDUCACIÒN CON CALIDAD JUAN MARIA CESPEDES Versión: 02 Fecha: 2011-07-05 DOCENTE: Gissely A. Quintero S. ÁREA: Ciencias Naturales (Química) 11º PREGUNTAS DE SELECCIÓN
INSTITUCIÒN EDUCATIVA Código: F-GA-024 EDUCACIÒN CON CALIDAD JUAN MARIA CESPEDES Versión: 02 Fecha: 2011-07-05 DOCENTE: Gissely A. Quintero S. ÁREA: Ciencias Naturales (Química) 11º PREGUNTAS DE SELECCIÓN
El aire de la atmósfera (78% N 2 ; 21% O 2 ; 1% Ar, He, CO 2 y vapor de agua) y el agua del mar son ejemplos de soluciones.
 SOLUCIONES la materia se presenta, con mayor frecuencia, en forma de mezcla de sustancias puras. dentro de éstas mezclas hay que distinguir las: I) mezclas propiamente dichas II) y las soluciones. El aire
SOLUCIONES la materia se presenta, con mayor frecuencia, en forma de mezcla de sustancias puras. dentro de éstas mezclas hay que distinguir las: I) mezclas propiamente dichas II) y las soluciones. El aire
LA MATERIA: ESTADOS DE AGREGACIÓN
 LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
MOL. Nº AVOGADRO GASES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez DEYMER GÓMEZ CORREA:
 UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: SOLUCIONES 1 Fecha: 9/Marzo/2010 DEYMER GÓMEZ CORREA: 1 042 091 432 OBJETIVOS
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: SOLUCIONES 1 Fecha: 9/Marzo/2010 DEYMER GÓMEZ CORREA: 1 042 091 432 OBJETIVOS
DISOLUCIONES. Finalmente se incluye un cuestionario on line para que alumno pruebe sus conocimientos.
 Introducción general Objetivos y destinatarios DISOLUCIONES El material está destinado como complemento de estudio en lo concerniente al tema Soluciones para alumnos que cursen Química en la Carrera de
Introducción general Objetivos y destinatarios DISOLUCIONES El material está destinado como complemento de estudio en lo concerniente al tema Soluciones para alumnos que cursen Química en la Carrera de
Ejercicios. 1. Disolvemos 15 g de ClNa en 60 g de agua. Calcular la concentración en masa de la mezcla.
 TEMA 4: 4 : DISOLUCIONES MATERÍA HOMOGENEA Y HETEROGÉNEA Si la materia que examinamos es uniforme, es decir, sus propiedades y su composición son las mismas en todos los puntos de su masa, decimos que
TEMA 4: 4 : DISOLUCIONES MATERÍA HOMOGENEA Y HETEROGÉNEA Si la materia que examinamos es uniforme, es decir, sus propiedades y su composición son las mismas en todos los puntos de su masa, decimos que
ACTIVIDADES Actividad 1. Indica donde están las pelotas más concentradas: Actividad 2. a) Indica donde están las pelotas más concentradas:
 ACTIIDADES Actividad 1. Indica donde están las pelotas más concentradas: A B Actividad 2. a) Indica donde están las pelotas más concentradas: A b) Dónde hay más cantidad? B PORCENTAJE EN MASA Actividad
ACTIIDADES Actividad 1. Indica donde están las pelotas más concentradas: A B Actividad 2. a) Indica donde están las pelotas más concentradas: A b) Dónde hay más cantidad? B PORCENTAJE EN MASA Actividad
INSTITUCIÓN EDUCATIVA FE Y ALEGRÍA NUEVA GENERACIÓN
 INSTITUCIÓN EDUCATIVA FE Y ALEGRÍA NUEVA GENERACIÓN Formando para el amor y la vida - AREA CIENCIAS NATURALES: QUIMICA - FISICA Tema: La Materia, Energía y Sonido Tiempo: 2 periodos académicos Grado: Quinto
INSTITUCIÓN EDUCATIVA FE Y ALEGRÍA NUEVA GENERACIÓN Formando para el amor y la vida - AREA CIENCIAS NATURALES: QUIMICA - FISICA Tema: La Materia, Energía y Sonido Tiempo: 2 periodos académicos Grado: Quinto
La materia y sus propiedades
 La materia y sus propiedades Las sustancias puras simples: ELEMENTOS QUÍMICOS Los elementos químicos Algunos pueden encontrarse fácilmente en nuestro entorno Hierro (Fe) Cobre (Cu) ASPECTO HOMOGÉNEO Oxígeno
La materia y sus propiedades Las sustancias puras simples: ELEMENTOS QUÍMICOS Los elementos químicos Algunos pueden encontrarse fácilmente en nuestro entorno Hierro (Fe) Cobre (Cu) ASPECTO HOMOGÉNEO Oxígeno
Bioquímica Tema 2: Soluciones. Unidades Año: 2013
 TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
Materia: FÍSICA Y QUÍMICA 3º E.S.O Curso
 ACTIVIDADES FÍSICA Y QUÍMICA 3º ESO PROGRAMA DE REFUERZO. PRIMERA PARTE 1.-Calcular el tanto por ciento en peso y en volumen de una disolución que se prepara al disolver 40 ml de ácido nítrico cuya densidad
ACTIVIDADES FÍSICA Y QUÍMICA 3º ESO PROGRAMA DE REFUERZO. PRIMERA PARTE 1.-Calcular el tanto por ciento en peso y en volumen de una disolución que se prepara al disolver 40 ml de ácido nítrico cuya densidad
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA
 UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 2: SOLUCIONES. UNIDADES DE CONCENTRACIÓN. LEY DE RAOULT Y PROPIEDADES
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 2: SOLUCIONES. UNIDADES DE CONCENTRACIÓN. LEY DE RAOULT Y PROPIEDADES
M A T E R I A L E S SOLUCIONES
 M A T E R I A L E S SOLUCIONES I Componentes Mayor proporción solvente Menor proporción soluto Concentración: indica la cantidad de soluto presente en una dada cantidad de solvente o una dada cantidad
M A T E R I A L E S SOLUCIONES I Componentes Mayor proporción solvente Menor proporción soluto Concentración: indica la cantidad de soluto presente en una dada cantidad de solvente o una dada cantidad
UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE
 Química Analítica UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE 2015 Una solución es una mezcla homogénea de dos o
Química Analítica UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE 2015 Una solución es una mezcla homogénea de dos o
MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS
 MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS Concentración de una disolución 1º.- Calcula la masa de nitrato de hierro (II), Fe(NO 3 ) 2, existente en 100 ml de disolución acuosa al 6 % en masa. Dato:
MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS Concentración de una disolución 1º.- Calcula la masa de nitrato de hierro (II), Fe(NO 3 ) 2, existente en 100 ml de disolución acuosa al 6 % en masa. Dato:
FACULTAD DE INGENIERÍA QUÍMICA ESCUELA DE INGENIERÍA QUÍMICA VASQUEZ BRIONES VÍCTOR ZAVALETA GARCÍA LUIS RODRIGUEZ LÁZARO YOVANY RUIZ BARAHONA EDUARDO
 ACULTAD DE INGENIERÍA QUÍMICA ESCUELA DE INGENIERÍA QUÍMICA TEMA: CURSO: PROPIEDADES DE LA MATERIA QUÍMICA GENERAL INTEGRANTES: CICLO: I-C VASQUEZ BRIONES VÍCTOR ZAVALETA GARCÍA LUIS RODRIGUEZ LÁZARO YOVANY
ACULTAD DE INGENIERÍA QUÍMICA ESCUELA DE INGENIERÍA QUÍMICA TEMA: CURSO: PROPIEDADES DE LA MATERIA QUÍMICA GENERAL INTEGRANTES: CICLO: I-C VASQUEZ BRIONES VÍCTOR ZAVALETA GARCÍA LUIS RODRIGUEZ LÁZARO YOVANY
PREPARACIÓN DE SOLUCIONES
 PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
TEMA 13: LA MATERIA, BASE DEL UNIVERSO
 TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
