Santiago del Estero (S3000AOM) Santa Fe - República Argentina Tel.: +54 (342) Fax: +54 (342)
|
|
|
- María Teresa Ayala Miranda
- hace 6 años
- Vistas:
Transcripción
1 Expte. nº SANTA FE, 25 de Agosto de 2015 VISTAS estas actuaciones vinculadas con la planificación de la asignatura "Química Inorgánica" obligatoria para las carreras de Ingeniería Química e Ingeniería en Alimentos, Planes 1999, elevada por el Profesor Responsable del dictado de la misma, lng. Edgardo CAGNOLA, CONSIDERANDO: El aval de las direcciones de las carreras correspondientes, como así también lo aconsejado por la Comisión de Enseñanza, EL CONSEJO DIRECTIVO DE LA RESUELVE: ARTICULO 1.- Aprobar la planificación de la asignatura "Química Inorgánica" obligatoria para las carreras de Ingeniería Química e Ingeniería en Alimentos, Planes 1999, que como anexo forma parte integrante de la presente. ARTÍCULO 2.- Mantener como Profesor responsable del dictado de la asignatura mencionada en el artículo precedente, al lng. Edgardo CAGNOLA. ARTICULO 3.- Dejar sin efecto el artículo 2 de la resolución "CD" nº 353/1 O e, ntegrar la Comisión Examinadora de la asignatura mencionada, de la siguiente manera: Titulares: lng. Edgardo CAGNOLA, Tco. Domingo LIPRANDI y Dra. Mónica QUIROGA Suplentes: Dra. Verónica DIEZ, lng. Gabriel PAPA y Dra. Sonia BOCANEGRA ARTICULO 4.- Inscríbase, comuníquese, déjese constancia en el original de la resolución "CD" nº 353/1 O, hágase saber en copia a Secretaría Académica, Departamento Alumnado y Bedelía y archívese. RESOLUCION "CD" nº 394 jcm ~ STELLA MARIS PSENDA r. NRIQUE MAMMARELLA DECANO
2 -2- PROGRAMA ANALÍTICO Tema 1. Complejos de metales de transición: Características básicas. Formulación y nomenclatura sistemática. Configuración espacial; complejos tetra y hexacoordinados. Isomería. Teorías de Enlace para compuestos complejos; Teorías del Campo Cristalino y del Campo Ligando. Configuración electrónica. Propiedades magnéticas y espectrales. Equilibrios de coordinación. Tema 2. Estudio sistemático de no metales: No metales y metales, características generales y diferencias. Hidrógeno y oxígeno: Propiedades generales. Ozono. Hidruros, óxidos e hidróxidos. Agua oxigenada; oxoácidos y tenedencias de acidez Grupo 17: Propiedades generales de los Halógenos. Flúor; fluoruro de hidrógeno; fluoruros. Cloro, bromo y yodo: cloruro de hidrógeno y otros hidruros, óxidos, oxoácidos y oxoaniones. Grupo 16: Propiedades generales. Azufre. Octoazufre. Sulfuro de hidrógeno. Sulfuros metálicos. Haluros. Dióxido y trióxido de azufre. Hidrogenosulfitos y sulfitos. Ácido sulfúrico y sulfatos. Grupo 15: Propiedades generales. Nitrógeno; amoníaco y otros hidruros; monóxido de nitrógeno, dióxido de nitrógeno y otros óxidos; ácido nitroso y nitritos; ácido nítrico y nitratos; nitruros- Fósforo: alotropía; hidruros; óxidos; ácido fosfórico y fosfatos. Grupo 14: Propiedades generales. Carbono: alotropía, hidruros, monóxido de carbono y dióxido de carbono; hidrógenocarbonatos y carbonatos; carburos. Silicio: hidruros; dióxido de silicio; silicatos y aluminosilicatos. Grupo 13: Propiedades generales. Boro: deficiencia electrónica; hidruros, enlaces tricéntricos; haluros; ácido bórico y boratos. Tema 3. Estudio sistemático de metales: Grupo 13: Aluminio: propiedades como metal; haluros, particularidades estructurales; óxido; hidróxido, anfoterismo. Grupo 1: Propiedades generales de los metales alcalinos. Anomalías del Li. Óxidos, hidróxidos, carbonatos, hidrógeno carbonatos, haluros, nitratos y nitritos, sulfatos e hidrógeno sulfatos de Na y K. Grupo 2: Propiedades generales de los metales alcalino-térreos. Comparación con los metales alcalinos. Anomalías del Be. Óxidos, hidróxidos, hidruros, haluros. Carbonatos, hidrógeno carbonatos, nitratos y sulfatos de Mg y Ca. Dureza del agua. Metales de transición: Propiedades generales de la primera serie de transición. Cromo y manganeso; compuestos representativos. Hierro: obtención, óxidos e hidróxidos; fenómeno de corrosión. Cobalto y níquel: óxidos, hidróxidos y sales. Metales de post transición: Propiedades generales. Comparaciones con los Grupos 1 y 2. Cobre y zinc: óxidos, hidróxidos y sales.. En los temas 2 y 3 se desarrollarán los siguientes ítems, cuando sea pertinente: * Características generales del grupo considerado, similitudes y diferencias en relación a otros grupos. Principio.. de singularidad. * Abundancia, estado natural e isótopos del elemento más representativo. j * Para los átomos del elemento: estructura electrónica, tipos de enlace en que interviene, estados de oxidación, ~mp;edad., qu;m;,,,, l. 1
3 .. Ministerio de Educación -3- Expte. nº Resolución "CD" nº * Para la sustancia elemental: variedades alotrópicas, fundamento físico-químico de la obtención de laboratorio e industrial, estructura y enlaces, propiedades, usos, importancia ambiental. * Para los compuestos más representativos: fundamentos químicos de la obtención en laboratorio e industrial, características estructurales, propiedades y usos. * Fundamentos de predicción de la conducta química. * Asignación de propiedades ácido-base de Lewis, ácidos y bases de Lewis duros y blandos. Bibliografía Rodgers, G.E., Química Inorgánica. Introducción a la Química de Coordinación, del Estado Sólido y Descriptiva. Ed. McGraw-Hill, Cotton F. A. y Wilkinson G., Química Inorgánica básica, Editorial Limusa, Liptrot G. F., Química Inorgánica, 2da edición, 1980, Cía Editorial Continental S. A. Housecroft C. E., Sharpe A. G., Química Inorgánica, 2da edición, 2006, Editorial Pearson Prentice Hall. Beyer L., Fernández Herrero V., Química Inorgánica, 1era edición, 2000, Editorial Ariel Ciencia. Cotton, A.F., Química Inorgánica Avanzada, Editorial Limusa, Shriver, D.F., Atkins, P.W., Langford, C.H., lnorganic Chemistry (2 edición), Ed. Oxford Universtiy Press, Huheey, J.E., Química Inorgánica. Principios de estructura y reactividad (2 edición), STELLA MARIS PSENDA Tel.: +54 (342) Fax: +54 (342) fiq@fiq.unl.edu.ar
4 -3- RÉGIMEN DE CURSADO Tipos de clases y metodología Se distribuirá la carga horaria semanal en dos clases: Clase de Teoría y Clase de Prácticas. Se dispondrá, además, de horarios de consulta adecuadamente repartidos durante la semana. La carga horaria semanal asignada a la clase de Teoría es de 2 horas; en la misma no sólo se imparten los conocimientos teóricos sino que además se discuten pautas teórico-prácticas relacionadas con la clase de Prácticas. La clase de Prácticas tendrá una carga horaria semanal de 4 horas; según puede apreciarse en el cronograma anterior, tres de dichas clases serán sólo de Problemas y el resto involucrarán Trabajos Prácticos de Laboratorio y Problemas de un dado subtema. En la parte de Problemas se aplicarán los conceptos vistos a la resolución de situaciones problemáticas, poniendo especial énfasis en las metodologías y en el análisis de los resultados obtenidos. En la parte de Trabajos Prácticos se abordarán situaciones experimentales de laboratorio. El número de comisiones en las clases Prácticas dependerá del número de alumnos, el cual normalmente no excede de 24 por comisión. Semanalmente se establece un número no menor a cinco clases de consulta, que abarcan todos los temas de la asignatura, especificando los horarios, docentes y modalidad (teoría y/o práctica). RÉGIMEN DE REGULARIDAD Para ser considerados como REGULARES, los alumnos cursantes de la asignatura deberán cumplir los siguientes requisitos: a) Tener como mínimo el 80% de asistencia a las clases de Problemas y como mínimo el 80% de asistencia a las clases de Trabajos Prácticos; las clases de Teoría serán de asistencia libre. b) En las clases en que se realice Trabajo Práctico se evaluarán conocimientos mínimos acerca del mismo, incluyendo normas de seguridad pertinentes. El alumno deberá aprobar como mínimo dos tercios de estas evaluaciones. RÉGIMEN DE EVALUACIÓN Y PROMOCIÓN La asignatura podrá promocionarse por alguna de las siguientes formas: a) Mediante sistema de parciales (opcional) Los alumnos que estén en condición de regulares podrán rendir los siguientes parciales promocionales, en los cuales se evaluarán conocimientos relativos a la teoría, problemas y trabajos prácticos: Primer parcial: Se tomará a mediados del cursado, con un puntaje máximo de 100 puntos y una duración de 2,5 horas Segundo parcial: Se tomará en la semana siguiente a la finalización de las clases; será globalizador e incluirá como temario los conocimientos integrados de toda la asignatura; el puntaje máximo será 100 puntos y el tiempo asignado será de 2,5 horas. Para promocionar la asignatura mediante el sistema de parciales se deberá cumplir con los tres requisitos siguientes: 1) El puntaje obtenido en el primer parcial no deberá ser inferior a los 40 puntos. 2) El puntaje obtenido en el segundo parcial no deberá ser inferior a los 60 puntos. 3) La suma de los puntajes obtenidos en el 1 º y 2º parcial deberá dar 116 puntos como mínimo, o lo que es lo mismo, dar un promedio de 58 puntos como mínimo. b) Mediante examen final b-1) Los alumnos regulares podrán promocionar la asignatura en el examen final, en el cual se evaluarán conocimientos y procedimientos relativos a la teoría, problemas y trabajos prácticos; el tiempo asignado será de 3 oras.y se requerirá un 58% como mínimo para su aprobación, correspondiendo a la calificación 6.
5 -4- b-2) Los alumnos que deseen promocionar la asignatura en condición de libres, deberán rendir el mismo examen que los alumnos regulares mencionado en el punto anterior, y en caso de aprobar éste con un puntaje mínimo de 58 puntos, pasarán a una segunda instancia de examen, en el cual se abordarán aspectos de índole teórico-práctica, especialmente orientados al desempeño práctico y conceptual en el laboratorio. La nota final será un promedio de las notas obtenidas en ambas instancias, cada una de las cuales se aprueba con 58 puntos, lo que equivale a una calificación de 6. Modalidad de los exámenes: cada examen de los alumnos regulares es presencial, individual y escrito, mientras que los alumnos en condición de libres deben realizar un primer examen presencial individual, y escrito y una segunda parte oral. Correspondencia entre la calificación de exámenes y la escala de notas de acuerdo con Resolución CD Nº 611/09: PUNTAJE DE EXAMEN FINAL o PROMEDIO DE PARCIALES CALIFICACIÓN ASIGNADA 1-14 INSUFICIENTE INSUFICIENTE INSUFICIENTE INSUFICIENTE INSUFICIENTE APROBAD BUENO MUY BUENOS DISTINGUIDO SOBRESALIENTE10 RECURSOS MATERIALES Y HUMANOS Los Trabajos Prácticos de Laboratorio se llevarán a cabo en el laboratorio de la asignatura Química Inorgánica. Al dictado de la asignatura estará afectado el siguiente personal docente del Área de Química General e Inorgánica del Departamento de Química: Clases de Teoría: Edgardo A. Cagnola (Prof. Adjunto exclusiva) Clases de Problemas: Domingo A. Liprandi (JTP exclusiva) Mónica E. Quiroga (JTP exclusiva) Gabriel Papa (JTP semiexclusiva) Tel.: +54 (342) Fax: +54 (342) fiq@fiq.unl.edu.ar
6 -5- /// Clases de Trabajos Prácticos: Domingo A. Liprandi (JTP exclusiva) Mónica E. Quiroga (JTP exclusiva) Gabriel Papa (JTP semiexclusiva) José F. Paredes (Ayudante de 1" semiexclusiva) Colaboración: Lic. Zunilda Finelli (INCAPE) Clases de Consulta: Edgardo A. Cagnola (Prof. Adjunto exclusiva) Domingo A. Liprandi (JTP exclusiva) Mónica E. Quiroga (JTP exclusiva) Gabriel Papa (JTP semiexclusiva) Nota: parte de la dedicación de todos los docentes mencionados está normalm cuatrimestres, a otras asignaturas que se dictan en el área. f ctadr ~t en ambos. &2DA
7 -6- Cronograma SEMANA Clase de TEORÍA Clase de Prácticas: TRABAJOS PRÁCTICOS (TP) y PROBLEMAS (P) 1 Formulación y Nomenclatura Complejos (P) 2 Tema 1 Complejos y Teoría Campo Cristalino (TP) 3 Complejos y Teoría Campo Cristalino (P) 4 Hidrógeno y Oxígeno (TP y P) 5 Halógenos (TP y P) 6 Tema2 Azufre (TP y P) 7 Nitrógeno (TP y P) 8 Carbono (TP y P) 9 1er parcial Boro (TP y P) 10 Aluminio (TP y P) 11 Grupo 2 (trat. Agua) (TP y P) 12 Metales de Transición (P) Tema 3 13 Hierro (TP) - Metales de Transición (P) 14 Cobalto (TP) - Metales de Transición (P) 15 Níquel (TP) - Metales de Transición (P) 16 Consultas -- 2do Parcial S~DA r\ ) k 1 J ~~: Dr ~~R QUE MAMMARELLA DECANO
8 -7- a) Horas de Problemas y de Trabajos Prácticos: Tres de las clases prácticas son sólo de Problemas, con un total de 4 horas; de las doce clases restantes, una consiste totalmente en TP, y las otras once constan cada una de dos horas de Trabajos Prácticos de laboratorio y dos horas de Problemas, según consta en el siguiente detalle: Semana de cursado Clase de Prácticas: TRABAJOS PRÁCTICOS (TP) y PROBLEMAS (P) 1 Formulación y Nomenclatura Complejos (P - 4hs) 2 Complejos y Teoría Campo Cristalino (TP - 4 hs) 3 Complejos y Teoría Campo Cristalino (P - 4 hs) 4 Hidrógeno y Oxígeno (TP - 2 hs y P - 2hs) 5 Halógenos (TP - 2 hs y P - 2hs) 6 Azufre (TP - 2 hs y P - 2hs) 7 Nitrógeno (TP - 2 hs y P - 2hs) 8 Carbono (TP - 2 hs y P - 2hs) 9 Boro (TP - 2 hs y P - 2hs) 10 Aluminio (TP - 2 hs y P - 2hs) 11 Grupo 2 (trat. Agua) (TP - 2 hs y P - 2hs) 12 Metales de Transición (P) 13 Hierro (TP - 2hs) - Metales de Transición (P - 2hs) 14 Cobalto (TP - 2hs) - Metales de Transición (P - 2hs) 15 Níquel (TP - 2hs) - Metales de Transición (P - 2hs) b) Nómina de Trabajos Prácticos: 1) Complejos - Teoría de Campo Cristalino - Color de los complejos 2) Hidrógeno y Oxígeno - Obtención de dihidrógeno y dioxígeno y reacción entre ellos 3) Halógenos - Obtención y propiedades químicas de los dihalógenos y oxoaniones 4) Azufre - Estados de oxidación y reactividad de las especies correspondientes 5) Nitrógeno - Propiedades deamoníaco y oxoñácidos del N. 6 ro - Conducta química del elemento, perla de bórax y ácido bórico
9 .. Ministerio de Educación -8- /// 7) Aluminio - propiedades del aluminio elemental, carácter reductor, anfoterismo del hidróxido de aluminio 8) Tratamiento de Agua - dureza del agua, origen y.tratamientos 9) Hierro - estados de oxidación, conducta frente a ácidos, Fe(ll) y Fe(lll) 10) Cobalto - estados de oxidación, hidróxido de cobalto (11), oxidación 11) Niquel - estados de oxidación, jardín inorgánico. 12) Carbono protección superficial natural del aluminio, 5re~NDA RIQUE MAMMARELLA DECANO
QUÍMICA INORGÁNICA I - Licenciatura en Química QUÍMICA INORGÁNICA - Químico Analista y Profesorado en Química
 QUÍMICA INORGÁNICA I - Licenciatura en Química QUÍMICA INORGÁNICA - Químico Analista y Profesorado en Química Carácter: Obligatoria Carga horaria: 9 horas semanales, 135 horas totales (15 semanas de cursado)
QUÍMICA INORGÁNICA I - Licenciatura en Química QUÍMICA INORGÁNICA - Químico Analista y Profesorado en Química Carácter: Obligatoria Carga horaria: 9 horas semanales, 135 horas totales (15 semanas de cursado)
QUÍMICA INORGÁNICA (QI)
 GUIA DOCENTE DE LA ASIGNATURA Curso 2014-2015 QUÍMICA INORGÁNICA (QI) MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO Química Química Inorgánica 1º 2º 6 Básica PROFESORES: DIRECCIÓN COMPLETA DE CONTACTO PARA
GUIA DOCENTE DE LA ASIGNATURA Curso 2014-2015 QUÍMICA INORGÁNICA (QI) MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO Química Química Inorgánica 1º 2º 6 Básica PROFESORES: DIRECCIÓN COMPLETA DE CONTACTO PARA
DATOS BÁSICOS DE LA ASIGNATURA DATOS BÁSICOS DE LOS PROFESORES DATOS ESPECÍFICOS DE LA ASIGNATURA
 DATOS BÁSICOS DE LA ASIGNATURA #$%&'( )* +$(, $( -.$*/-#*0,1* $0( '2*,$0(,, /'1 3 ",0 " 1'0$( 1-,' %0,'( /$( DATOS BÁSICOS DE LOS PROFESORES #$%&'( #,'$4*-',-%#,$( 5'-( #**0-6$(!%- /( 1'/8&(,/27$#$(! DATOS
DATOS BÁSICOS DE LA ASIGNATURA #$%&'( )* +$(, $( -.$*/-#*0,1* $0( '2*,$0(,, /'1 3 ",0 " 1'0$( 1-,' %0,'( /$( DATOS BÁSICOS DE LOS PROFESORES #$%&'( #,'$4*-',-%#,$( 5'-( #**0-6$(!%- /( 1'/8&(,/27$#$(! DATOS
Grado en Química. Curso 2016/17
 GUÍA DOCENTE DE LA ASIGNATURA DATOS DE LA ASIGNATURA Asignatura: Química Inorgánica Descriptiva Código: 757509202 Módulo: Fundamental Materia: Química Curso: 2 Cuatrimestre: 2 Créditos ECTS 9 Teóricos:
GUÍA DOCENTE DE LA ASIGNATURA DATOS DE LA ASIGNATURA Asignatura: Química Inorgánica Descriptiva Código: 757509202 Módulo: Fundamental Materia: Química Curso: 2 Cuatrimestre: 2 Créditos ECTS 9 Teóricos:
ASIGNATURA: QUÍMICA INORGÁNICA
 Página 1 de 7 CARACTERÍSTICAS GENERALES* Tipo: Formación básica, Obligatoria, Optativa Trabajo de fin de grado, Prácticas externas Duración: Anual Semestre/s: 3 y 4 Número de créditos ECTS: 12 Idioma/s:
Página 1 de 7 CARACTERÍSTICAS GENERALES* Tipo: Formación básica, Obligatoria, Optativa Trabajo de fin de grado, Prácticas externas Duración: Anual Semestre/s: 3 y 4 Número de créditos ECTS: 12 Idioma/s:
TIPO: T CURSO: 2º SEMESTRE:1º y 2º CRÉDITOS (horas/semana): 9.0 CRÉDITOS ECTS: 7.5 PROFESOR: Dr. Jordi Abellà Iglesias IDIOMA: Castellano / Català
 22015 QUÍMICA INORGÁNICA Pág 1 de 7 ASIGNATURA: Química Inorgánica ESTUDIOS: INGENIERÍA QUÍMICA (1 er Ciclo) CÓDIGO: 22015 TIPO: T CURSO: 2º SEMESTRE:1º y 2º CRÉDITOS (horas/semana): 9.0 CRÉDITOS ECTS:
22015 QUÍMICA INORGÁNICA Pág 1 de 7 ASIGNATURA: Química Inorgánica ESTUDIOS: INGENIERÍA QUÍMICA (1 er Ciclo) CÓDIGO: 22015 TIPO: T CURSO: 2º SEMESTRE:1º y 2º CRÉDITOS (horas/semana): 9.0 CRÉDITOS ECTS:
U N I V E R S I D A D A L A S P E R U A N A S FACULTAD DE MEDICINA HUMANA
 1. DATOS INFORMATIVOS SILABO 1.1 Asignatura : QUIMICA INORGANICA 1.2 Código : 19-107 1.3 Área : Formativo 1.4 Escuela : Farmacia y Bioquímica 1.5 Ciclo : Segundo 1.6 Créditos : 04 1.7 Total de horas :
1. DATOS INFORMATIVOS SILABO 1.1 Asignatura : QUIMICA INORGANICA 1.2 Código : 19-107 1.3 Área : Formativo 1.4 Escuela : Farmacia y Bioquímica 1.5 Ciclo : Segundo 1.6 Créditos : 04 1.7 Total de horas :
Grado de Química Curso
 DATOS DE LA ASIGNATURA Asignatura: Química Inorgánica Descriptiva Código (uhu): 757509202 Módulo: Fundamental Materia: Química Créditos ECTS 9 Teóricos: 6 Prácticos: 3 Departamento/s: Química y CCMM Prof.
DATOS DE LA ASIGNATURA Asignatura: Química Inorgánica Descriptiva Código (uhu): 757509202 Módulo: Fundamental Materia: Química Créditos ECTS 9 Teóricos: 6 Prácticos: 3 Departamento/s: Química y CCMM Prof.
Pontificia Universidad Católica del Ecuador
 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: Química Inorgánica, T y L CÓDIGO: 13895 CARRERA: NIVEL: Licenciatura en Ciencias Químicas, con mención en Química Analítica Segundo Nivel No. CRÉDITOS: 7 CRÉDITOS
1. DATOS INFORMATIVOS: MATERIA O MÓDULO: Química Inorgánica, T y L CÓDIGO: 13895 CARRERA: NIVEL: Licenciatura en Ciencias Químicas, con mención en Química Analítica Segundo Nivel No. CRÉDITOS: 7 CRÉDITOS
Instancia curricular: Química III Química general e Inorgánica II
 Nivel: Terciario Carrera: Profesorado en Química Trayecto: Disciplinar Instancia curricular: Química III Química general e Inorgánica II Cursada: Anual Carga horaria: 6 horas Profesor: Alfredo Sanguinetti
Nivel: Terciario Carrera: Profesorado en Química Trayecto: Disciplinar Instancia curricular: Química III Química general e Inorgánica II Cursada: Anual Carga horaria: 6 horas Profesor: Alfredo Sanguinetti
Descriptores Creditos ECTS Carácter Curso Cuatrimestre. 9 OB 2 2c Castellano
 Guía Materia 2017 / 2018 DATOS IDENTIFICATIVOS Química inorgánica I Asignatura Código Titulacion Química inorgánica I V11G200V01404 Grado en Química Descriptores Creditos ECTS Carácter Curso Cuatrimestre
Guía Materia 2017 / 2018 DATOS IDENTIFICATIVOS Química inorgánica I Asignatura Código Titulacion Química inorgánica I V11G200V01404 Grado en Química Descriptores Creditos ECTS Carácter Curso Cuatrimestre
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS
 PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: MATERIA: Química Inorgánica, T y L CÓDIGO: 12799 CARRERA: Ciencias
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: MATERIA: Química Inorgánica, T y L CÓDIGO: 12799 CARRERA: Ciencias
DISTRIBUCIÓN HORARIA DE LA ASIGNATURA SEGÚN NORMATIVA
 GUÍA DOCENTE CURSO: 2016-17 DATOS BÁSICOS DE LA ASIGNATURA Asignatura: Química Inorgánica I Código de asignatura: 50902207 Plan: Grado en Química (Plan 2009) Año académico: 2016-17 Ciclo formativo: Grado
GUÍA DOCENTE CURSO: 2016-17 DATOS BÁSICOS DE LA ASIGNATURA Asignatura: Química Inorgánica I Código de asignatura: 50902207 Plan: Grado en Química (Plan 2009) Año académico: 2016-17 Ciclo formativo: Grado
TITULACIÓN: GRADO EN QUÍMICA CENTRO: FACULTAD DE CIENCIAS EXPERIMENTALES CURSO ACADÉMICO: GUÍA DOCENTE
 TITULACIÓN: GRADO EN QUÍMICA CENTRO: FACULTAD DE CIENCIAS EXPERIMENTALES CURSO ACADÉMICO: 2011-2012 GUÍA DOCENTE 1. DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: Química Inorgánica I CÓDIGO: 10312009 CURSO ACADÉMICO:
TITULACIÓN: GRADO EN QUÍMICA CENTRO: FACULTAD DE CIENCIAS EXPERIMENTALES CURSO ACADÉMICO: 2011-2012 GUÍA DOCENTE 1. DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: Química Inorgánica I CÓDIGO: 10312009 CURSO ACADÉMICO:
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS
 PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: Materia: Química Inorgánica Carrera: Química Analítica Nivel: Segundo
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: Materia: Química Inorgánica Carrera: Química Analítica Nivel: Segundo
Idioma en que se imparte: ECTS: Horas/ECTS: Volumen de trabajo del alumno: Castellano Inglés
 Guía Docente Asignatura: Química Inorgánica Módulo (según el plan de estudios): Materias específicas Titulación: Grado en Ingeniería Química Industrial Código: 509101008 Plan de Estudios: Plan 5091. Decreto
Guía Docente Asignatura: Química Inorgánica Módulo (según el plan de estudios): Materias específicas Titulación: Grado en Ingeniería Química Industrial Código: 509101008 Plan de Estudios: Plan 5091. Decreto
Química Inorgánica I
 GUÍA DOCENTE 2010-2011 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Código 2. Materia o módulo a la que pertenece la asignatura: Química Inorgánica 3. Departamento(s) responsable(s)
GUÍA DOCENTE 2010-2011 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Código 2. Materia o módulo a la que pertenece la asignatura: Química Inorgánica 3. Departamento(s) responsable(s)
QUÍMICA INORGÁNICA. Hoja 1 de 6. Programa de:
 Programa de: Hoja 1 de 6. UNIVERSIDAD NACIONAL DE CÓRDOBA FACULTAD DE CIENCIAS EXACTAS F. Y N. REPÚBLICA ARGENTINA QUÍMICA INORGÁNICA Código: Carrera: Ingeniería Química Plan:2004 V05 Puntos: 3 Escuela:
Programa de: Hoja 1 de 6. UNIVERSIDAD NACIONAL DE CÓRDOBA FACULTAD DE CIENCIAS EXACTAS F. Y N. REPÚBLICA ARGENTINA QUÍMICA INORGÁNICA Código: Carrera: Ingeniería Química Plan:2004 V05 Puntos: 3 Escuela:
Planificaciones Química Inorgánica. Docente responsable: JACOBO SILVIA ELENA. 1 de 5
 Planificaciones 6313 - Química Inorgánica Docente responsable: JACOBO SILVIA ELENA 1 de 5 OBJETIVOS Desarrollar en el alumno capacidad para: Interpretar las relaciones entre la estructura y las propiedades
Planificaciones 6313 - Química Inorgánica Docente responsable: JACOBO SILVIA ELENA 1 de 5 OBJETIVOS Desarrollar en el alumno capacidad para: Interpretar las relaciones entre la estructura y las propiedades
Guía Docente QUÍMICA INORGÁNICA 1ER CURSO 2º SEMESTRE GRADO EN FARMACIA Y BIOTECNOLOGÍA MODALIDAD: PRESENCIAL CURSO 2015/2016 FACULTAD DE FARMACIA
 Guía Docente QUÍMICA INORGÁNICA 1ER CURSO 2º SEMESTRE GRADO EN FARMACIA Y BIOTECNOLOGÍA MODALIDAD: PRESENCIAL CURSO 2015/2016 FACULTAD DE FARMACIA 1. IDENTIFICACIÓN DE LA ASIGNATURA 1.- ASIGNATURA: Nombre:
Guía Docente QUÍMICA INORGÁNICA 1ER CURSO 2º SEMESTRE GRADO EN FARMACIA Y BIOTECNOLOGÍA MODALIDAD: PRESENCIAL CURSO 2015/2016 FACULTAD DE FARMACIA 1. IDENTIFICACIÓN DE LA ASIGNATURA 1.- ASIGNATURA: Nombre:
QUIMICA APLICADA EN LA INGENIERIA GEOLOGICA
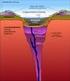 Ingeniería Geológica 1-5 CÓDIGO: B051/99/7491 CURSO: 2002-2003 Carga docente: 6 créditos (4,5 teóricos + 1,5 prácticos) Curso: 1º, Troncal Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es:
Ingeniería Geológica 1-5 CÓDIGO: B051/99/7491 CURSO: 2002-2003 Carga docente: 6 créditos (4,5 teóricos + 1,5 prácticos) Curso: 1º, Troncal Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es:
3ºESO-A PROFESORA LUCÍA ROMERO
 PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO-A PROFESORA LUCÍA ROMERO BIOLOGÍA Y GEOLOGÍA: Resumen de cada tema del libro y las siguientes actividades: PRIMER TRIMESTRE: - Tema 1: La salud
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO-A PROFESORA LUCÍA ROMERO BIOLOGÍA Y GEOLOGÍA: Resumen de cada tema del libro y las siguientes actividades: PRIMER TRIMESTRE: - Tema 1: La salud
U N I V E R S I D A D A L A S P E R U A N A S FACULTAD DE MEDICINA HUMANA y CIENCIAS DE LA SALUD Escuela Académico Profesional de Nutrición Humana
 1. DATOS INFORMATIVOS SILABO 1.1 Asignatura : QUIMICA INORGANICA 1.2 Código : 28-108 1.3 Area : Formativo 1.4 Facultad : Ciencias la Salud 1.5 Ciclo : Segundo 1.6 Créditos : 04 1.7 Total horas : 06 Teoría
1. DATOS INFORMATIVOS SILABO 1.1 Asignatura : QUIMICA INORGANICA 1.2 Código : 28-108 1.3 Area : Formativo 1.4 Facultad : Ciencias la Salud 1.5 Ciclo : Segundo 1.6 Créditos : 04 1.7 Total horas : 06 Teoría
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2
 FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
UNIVERSIDAD EMILIANO ZAPATA
 UNIVERSIDAD EMILIANO ZAPATA OBJETIVO DE LA MATERIA El estudiante describirá la importancia de la química en la ciencia y tecnología, a través del conocimiento de sus principios básicos, con el fin de explicar
UNIVERSIDAD EMILIANO ZAPATA OBJETIVO DE LA MATERIA El estudiante describirá la importancia de la química en la ciencia y tecnología, a través del conocimiento de sus principios básicos, con el fin de explicar
Programa de la asignatura Curso: 2007 / 2008 QUÍMICA INORGÁNICA (1229)
 Programa de la asignatura Curso: 2007 / 2008 QUÍMICA INORGÁNICA (1229) PROFESORADO Profesor/es: JOSE VICENTE CUEVAS VICARIO - correo-e: jvcv@ubu.es JAVIER GARCIA TOJAL - correo-e: qipgatoj@ubu.es FICHA
Programa de la asignatura Curso: 2007 / 2008 QUÍMICA INORGÁNICA (1229) PROFESORADO Profesor/es: JOSE VICENTE CUEVAS VICARIO - correo-e: jvcv@ubu.es JAVIER GARCIA TOJAL - correo-e: qipgatoj@ubu.es FICHA
Química General Básica. Nomenclatura de Compuestos Inorgánicos
 Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
TITULACIÓN: LICENCIATURA EN QUÍMICA CURSO ACADÉMICO: GUÍA DOCENTE de QUIMICA INORGÁNICA
 TITULACIÓN: LICENCIATURA EN QUÍMICA CURSO ACADÉMICO: 2011-2012 GUÍA DOCENTE de QUIMICA INORGÁNICA DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: QUÍMICA INORGÁNICA CÓDIGO: 3165 AÑO DE PLAN DE ESTUDIOS: 1995 adap.
TITULACIÓN: LICENCIATURA EN QUÍMICA CURSO ACADÉMICO: 2011-2012 GUÍA DOCENTE de QUIMICA INORGÁNICA DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: QUÍMICA INORGÁNICA CÓDIGO: 3165 AÑO DE PLAN DE ESTUDIOS: 1995 adap.
Universidad Nacional Mayor de San Marcos (Universidad del Perú, DECANA DE AMERICA)
 Universidad Nacional Mayor de San Marcos (Universidad del Perú, DECANA DE AMERICA) FACULTAD DE FARMACIA Y BIOQUIMICA ESCUELA ACADEMICO PROFESIONAL DE FARMACIA Y BIOQUIMICA DEPARTAMENTO ACADEMICO QUIMICA
Universidad Nacional Mayor de San Marcos (Universidad del Perú, DECANA DE AMERICA) FACULTAD DE FARMACIA Y BIOQUIMICA ESCUELA ACADEMICO PROFESIONAL DE FARMACIA Y BIOQUIMICA DEPARTAMENTO ACADEMICO QUIMICA
Antonio Rodríguez Diéguez
 GUIA DOCENTE DE LA ASIGNATURA QUÍMICA Curso 2016-2017 Actualizada en Consejo de Departamento 24/06/2016 MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO Física y Química Química 1º 1º 6 Básica PROFESOR(ES)
GUIA DOCENTE DE LA ASIGNATURA QUÍMICA Curso 2016-2017 Actualizada en Consejo de Departamento 24/06/2016 MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO Física y Química Química 1º 1º 6 Básica PROFESOR(ES)
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
Pontificia Universidad Católica del Ecuador
 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: GEOQUÍMICA CÓDIGO: CARRERA: Ingeniería en Ciencias Geográficas NIVEL: III No. CRÉDITOS: CRÉDITOS TEORÍA: 2 CRÉDITOS PRÁCTICA: 3 SEMESTRE / AÑO ACADÉMICO: 2011-2012
1. DATOS INFORMATIVOS: MATERIA O MÓDULO: GEOQUÍMICA CÓDIGO: CARRERA: Ingeniería en Ciencias Geográficas NIVEL: III No. CRÉDITOS: CRÉDITOS TEORÍA: 2 CRÉDITOS PRÁCTICA: 3 SEMESTRE / AÑO ACADÉMICO: 2011-2012
Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial
 Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial Programa de la asignatura: (QUI-012) Química Inorgánica I Total de Créditos:
Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial Programa de la asignatura: (QUI-012) Química Inorgánica I Total de Créditos:
Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Electromecánica
 Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Electromecánica Programa de la asignatura: (QUI-012) Química Inorgánica Total de Créditos:
Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Electromecánica Programa de la asignatura: (QUI-012) Química Inorgánica Total de Créditos:
5) Cuando un metal y un no metal reaccionan el tiende a perder electrones y el tiende a ganar electrones.
 Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
Características de electrones protones y neutrones
 Características de electrones protones y neutrones Carga eléctrica Masa Espín SI (C) Atómica SI(g) Atómica (uma) Protón +1,6021 10-19 +1 1,6725 10-24 1,0073 1/2 neutrón 0 0 1,6748 10-24 1,0087 1/2 electrón
Características de electrones protones y neutrones Carga eléctrica Masa Espín SI (C) Atómica SI(g) Atómica (uma) Protón +1,6021 10-19 +1 1,6725 10-24 1,0073 1/2 neutrón 0 0 1,6748 10-24 1,0087 1/2 electrón
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
1. Introducción 2. Configuración electrónica y clasificación periódica 3. Propiedades periódicas Cuestionario de orientación y problemas
 PRÓLOGO A LA PRIMERA EDICIÓN 13 PRÓLOGO A LA TERCERA EDICIÓN 15 CAPÍTULO 1 Estructura atómica 17 1. Introducción 2. Principales experimentos que contribuyeron al conocimiento de la estructura atómica 3.
PRÓLOGO A LA PRIMERA EDICIÓN 13 PRÓLOGO A LA TERCERA EDICIÓN 15 CAPÍTULO 1 Estructura atómica 17 1. Introducción 2. Principales experimentos que contribuyeron al conocimiento de la estructura atómica 3.
PROGRAMA QUÍMICA INORGÁNICA
 PROGRAMA QUÍMICA INORGÁNICA Objetivo de Estudio de la Disciplina El objetivo de la Química es el conocimiento de las especies químicas elementos y compuestos sus propiedades, reacciones químicas, los métodos
PROGRAMA QUÍMICA INORGÁNICA Objetivo de Estudio de la Disciplina El objetivo de la Química es el conocimiento de las especies químicas elementos y compuestos sus propiedades, reacciones químicas, los métodos
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos. 13 millones!!!
 La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
Universidad Central Del Este U C E Facultad de Ciencias de la Salud Escuela de Enfermería
 Universidad Central Del Este U C E Facultad de Ciencias de la Salud Escuela de Enfermería Programa de la asignatura: QUI-012 Química Inorgánica. Descripción General: Total de Créditos: 4 Teórico: 3 Práctico:
Universidad Central Del Este U C E Facultad de Ciencias de la Salud Escuela de Enfermería Programa de la asignatura: QUI-012 Química Inorgánica. Descripción General: Total de Créditos: 4 Teórico: 3 Práctico:
UD 2 ENLACE QUÍMICO Y FUERZAS INTERMOLECULARES FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
QUÍ MI CA I NORGANI CA. Dr. ADOLFO BOLLINI Profesor Titular. Avda 60 esq124 T el / Fax (0221) /
 QUÍ MI CA I NORGANI CA Dr. ADOLFO BOLLINI Profesor Titular Avda 60 esq124 T el / Fax (0221) 421 7578 / 482-4855 UNIVERSIDAD TECNOLÓGICA NACIONAL Facultad Regional La Plata CARRERA Ingeniería Química DISEÑO
QUÍ MI CA I NORGANI CA Dr. ADOLFO BOLLINI Profesor Titular Avda 60 esq124 T el / Fax (0221) 421 7578 / 482-4855 UNIVERSIDAD TECNOLÓGICA NACIONAL Facultad Regional La Plata CARRERA Ingeniería Química DISEÑO
LA QUÍMICA INORGÁNICA EN REACCIONES
 LA QUÍMICA INORGÁNICA EN REACCIONES PROYECTO EDITORIAL BIBLIOTECA DE QUÍMICAS Director: Carlos Seoane Prado Catedrático de Química Orgánica Universidad Complutense de Madrid Queda prohibida, salvo excepción
LA QUÍMICA INORGÁNICA EN REACCIONES PROYECTO EDITORIAL BIBLIOTECA DE QUÍMICAS Director: Carlos Seoane Prado Catedrático de Química Orgánica Universidad Complutense de Madrid Queda prohibida, salvo excepción
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
Nomenclatura de Compuestos Inorgánicos
 Repartido Nomenclatura Compuestos Inorgánicos Química 1 B.D. Prof. Javier Ponce Ecuaciones Químicas: Una ecuación química es la representación de una reacción química. En toda ecuación química se verifica
Repartido Nomenclatura Compuestos Inorgánicos Química 1 B.D. Prof. Javier Ponce Ecuaciones Químicas: Una ecuación química es la representación de una reacción química. En toda ecuación química se verifica
GUÍA DOCENTE Química Inorgánica I
 GUÍA DOCENTE 2015-2016 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Titulación Grado en Química Código 5273 2. Materia o módulo a la que pertenece la asignatura: Química
GUÍA DOCENTE 2015-2016 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Titulación Grado en Química Código 5273 2. Materia o módulo a la que pertenece la asignatura: Química
UNIVERSIDAD AUTÓNOMA DE SINALOA FACULTAD DE CIENCIAS QUIMICO BIOLÓGICAS PLANEACIÓN EN AULA LABORATORIO - EVALUACIÓN
 UNIVERSIDAD AUTÓNOMA DE SINALOA FACULTAD DE CIENCIAS QUIMICO BIOLÓGICAS PLANEACIÓN EN AULA LABORATORIO - EVALUACIÓN Periodo: Enero - Junio Ciclo: 2011-2012 I. TRONCO COMUN II. ASIGNATURA: QUIMICA INORGANICA
UNIVERSIDAD AUTÓNOMA DE SINALOA FACULTAD DE CIENCIAS QUIMICO BIOLÓGICAS PLANEACIÓN EN AULA LABORATORIO - EVALUACIÓN Periodo: Enero - Junio Ciclo: 2011-2012 I. TRONCO COMUN II. ASIGNATURA: QUIMICA INORGANICA
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
Plan Código Tipo Curso Créditos Periodos de (Teóricos+Prácticos) docencia Cuarto Cuarto 7,5(5,5T + 1,5P) 1C
 Asignatura: QUÍMICA INORGÁNICA AVANZADA Plan Código Tipo Curso Créditos Periodos de (Teóricos+Prácticos) docencia 6 57230 Cuarto Cuarto 7,5(5,5T + 1,5P) 1C Equipo docente Prof. Teoría: Antonio F. Antiñolo
Asignatura: QUÍMICA INORGÁNICA AVANZADA Plan Código Tipo Curso Créditos Periodos de (Teóricos+Prácticos) docencia 6 57230 Cuarto Cuarto 7,5(5,5T + 1,5P) 1C Equipo docente Prof. Teoría: Antonio F. Antiñolo
Universidad Técnica Nacional
 Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Número de oxidación. Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo
 FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
UNIDAD 1. La Química y su importancia. Materia y Substancia. Mezclas y compuestos. Clasificación de los fenómenos... 1
 ÍNDICE UNIDAD 1 La Química y su importancia. Materia y Substancia. Mezclas y compuestos. Clasificación de los fenómenos... 1 CAPÍTULO 1. La Química y su importancia... 1 Definiciones y subdivisiones de
ÍNDICE UNIDAD 1 La Química y su importancia. Materia y Substancia. Mezclas y compuestos. Clasificación de los fenómenos... 1 CAPÍTULO 1. La Química y su importancia... 1 Definiciones y subdivisiones de
EL CONSEJO DIRECTIVO RESUELVE:
 Expediente Nos. 500/9830CD Rosario, 23 de agosto de 2010 VISTO: que la Secretaria Académica, Lic. María de las Mercedes CAILA eleva, para su aprobación el Texto Ordenado del Reglamento de Cursado de Asignaturas;
Expediente Nos. 500/9830CD Rosario, 23 de agosto de 2010 VISTO: que la Secretaria Académica, Lic. María de las Mercedes CAILA eleva, para su aprobación el Texto Ordenado del Reglamento de Cursado de Asignaturas;
Formula y nombra los siguientes compuestos. Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O
 Co I3 Formula y nombra los siguientes compuestos Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O Cu2O Al2 O3 Na H Ca H2 Al H3 Au H Co H3 Fe H2 H F H Cl H2 S H2 Se Al2
Co I3 Formula y nombra los siguientes compuestos Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O Cu2O Al2 O3 Na H Ca H2 Al H3 Au H Co H3 Fe H2 H F H Cl H2 S H2 Se Al2
Guía docente de la asignatura
 Guía docente de la asignatura Asignatura Materia Química Inorgánica I Química Inorgánica Módulo Titulación Grado en Química Plan 472 Código 45948 Periodo de impartición 2º curso, Primer cuatrimestre Tipo/Carácter
Guía docente de la asignatura Asignatura Materia Química Inorgánica I Química Inorgánica Módulo Titulación Grado en Química Plan 472 Código 45948 Periodo de impartición 2º curso, Primer cuatrimestre Tipo/Carácter
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FUNDAMENTOS QUÍMICOS DE LA INGENIERÍA (I.ELÉCTRICA / I. ELECTRÓNICA)
 ASIGNATURA DE GRADO: FUNDAMENTOS QUÍMICOS DE LA INGENIERÍA (I.ELÉCTRICA / I. ELECTRÓNICA) Curso 2014/2015 (Código:68901111) 1.PRESENTACIÓN DE LA ASIGNATURA La asignatura Fundamentos Químicos de la Ingeniería
ASIGNATURA DE GRADO: FUNDAMENTOS QUÍMICOS DE LA INGENIERÍA (I.ELÉCTRICA / I. ELECTRÓNICA) Curso 2014/2015 (Código:68901111) 1.PRESENTACIÓN DE LA ASIGNATURA La asignatura Fundamentos Químicos de la Ingeniería
FORMULACIÓN Y NOMENCLATURA
 1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
Asignatura: Química 2. Curso: 3 ro. de Media. Proyecto Nº 3. Mes: Marzo-Abril. Año: Prof.: Lic. Manuel B. Noboa G.
 Asignatura: Química 2. Curso: 3 ro. de Media. Proyecto Nº 3. Mes: Marzo-Abril. Año: 2014-2015. Prof.: Lic. Manuel B. Noboa G. Unidad Nº 3: Elementos de los Bloques P y D. Propósito Nº 1: P. C.: 20 de marzo
Asignatura: Química 2. Curso: 3 ro. de Media. Proyecto Nº 3. Mes: Marzo-Abril. Año: 2014-2015. Prof.: Lic. Manuel B. Noboa G. Unidad Nº 3: Elementos de los Bloques P y D. Propósito Nº 1: P. C.: 20 de marzo
UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO FACULTAD DE AGRONOMÍA Y AGROINDUSTRIAS DEPARTAMENTO FÍSICO-MATEMÁTICO
 UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO FACULTAD DE AGRONOMÍA Y AGROINDUSTRIAS DEPARTAMENTO FÍSICO-MATEMÁTICO ASIGNATURA: QUIMICA PARA EL CURSO DE INGRESO 2010 CARRERAS: INGENIERÍA EN ALIMENTOS INGENIERÍA
UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO FACULTAD DE AGRONOMÍA Y AGROINDUSTRIAS DEPARTAMENTO FÍSICO-MATEMÁTICO ASIGNATURA: QUIMICA PARA EL CURSO DE INGRESO 2010 CARRERAS: INGENIERÍA EN ALIMENTOS INGENIERÍA
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
Formulación Inorgánica
 Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Pontificia Universidad Católica del Ecuador
 FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS BIOLOGICAS 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: Química General II (TEORIA Y LABORATORIO) CARRERA: Biología NIVEL: Segundo No. CREDITOS:
FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS BIOLOGICAS 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: Química General II (TEORIA Y LABORATORIO) CARRERA: Biología NIVEL: Segundo No. CREDITOS:
GUÍA DOCENTE Curso
 GUÍA DOCENTE Curso 2011-2012 Titulación: Grado en Química Código : 702G Centro: Facultad de Ciencias, Estudios Agroalimentarios e Informática Dirección: Edificio Científico Tecnológico-CCT C/ Madre de
GUÍA DOCENTE Curso 2011-2012 Titulación: Grado en Química Código : 702G Centro: Facultad de Ciencias, Estudios Agroalimentarios e Informática Dirección: Edificio Científico Tecnológico-CCT C/ Madre de
Santiago del Estero (S3000AOM) Santa Fe - República Argentina Tel.: +54 (342) Fax: +54 (342)
 SANTA FE, 23 de octubre de 2012 VISTAS estas actuaciones vinculadas con la elevación de la planificación de la asignatura Ingeniería Económica, obligatoria para las carreras de Ingeniería Química e Ingeniería
SANTA FE, 23 de octubre de 2012 VISTAS estas actuaciones vinculadas con la elevación de la planificación de la asignatura Ingeniería Económica, obligatoria para las carreras de Ingeniería Química e Ingeniería
CARACTERÍSTICAS DE LA ASIGNATURA
 Química General Química 1 CARACTERÍSTICAS DE LA ASIGNATURA ASIGNATURAS y CARRERAS: Química General : obligatoria para las carreras de Ingeniería Química - Plan 1999, Ingeniería en Alimentos - Plan 1999
Química General Química 1 CARACTERÍSTICAS DE LA ASIGNATURA ASIGNATURAS y CARRERAS: Química General : obligatoria para las carreras de Ingeniería Química - Plan 1999, Ingeniería en Alimentos - Plan 1999
CÁTEDRA DE QUÍMICA GENERAL E INORGÁNICA GUIA DE ESTUDIO Nº 3 ENLACE QUÍMICO
 GUIA DE ESTUDIO Nº 3 1. Define enlace químico. ENLACE QUÍMICO 2. Qué son los electrones de valencia? Cuántos electrones de valencia posee un átomo de nitrógeno? 3. Analiza la siguiente configuración electrónica
GUIA DE ESTUDIO Nº 3 1. Define enlace químico. ENLACE QUÍMICO 2. Qué son los electrones de valencia? Cuántos electrones de valencia posee un átomo de nitrógeno? 3. Analiza la siguiente configuración electrónica
UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIO DE LICENCIATURA PRAXIS MES XXI
 UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIO DE LICENCIATURA PRAXIS MES XXI NOMBRE DE LA ASIGNATURA: QUÍMICA FECHA DE ELABORACIÓN: ENERO 2005. ÁREA DEL PLAN DE ESTUDIOS: AS ( ) AC ( X ) APOBL (
UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIO DE LICENCIATURA PRAXIS MES XXI NOMBRE DE LA ASIGNATURA: QUÍMICA FECHA DE ELABORACIÓN: ENERO 2005. ÁREA DEL PLAN DE ESTUDIOS: AS ( ) AC ( X ) APOBL (
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
NOMENCLATURA DE ÁCIDOS Y BASES
 COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE CIENCIAS QUIMICAS
 PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE CIENCIAS QUIMICAS 1. DATOS INFORMATIVOS MATERIA Química General I CÓDIGO 12793 CARRERA Ciencias Químicas, Mención Química Analítica NIVEL I No. CREDITOS:
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE CIENCIAS QUIMICAS 1. DATOS INFORMATIVOS MATERIA Química General I CÓDIGO 12793 CARRERA Ciencias Químicas, Mención Química Analítica NIVEL I No. CREDITOS:
PROBABILIDAD Y ESTADÍSTICA. Programación Ciclo Lectivo 2013
 PROBABILIDAD Y ESTADÍSTICA Programación Ciclo Lectivo 2013 Objetivos de la primera clase 1 Presentarnos 2 3 Dar a conocer la programación del curso Presentar los medios y materiales del curso Nuestro equipo
PROBABILIDAD Y ESTADÍSTICA Programación Ciclo Lectivo 2013 Objetivos de la primera clase 1 Presentarnos 2 3 Dar a conocer la programación del curso Presentar los medios y materiales del curso Nuestro equipo
Química 2 Tercero de Media. Proyecto 3 Marzo/Abril Prof.: Lic. Manuel B. Noboa G. Unidad Nº 3: Elementos de los Bloques P y D.
 Química 2 Tercero de Media. Proyecto 3 Marzo/Abril 2016. Prof.: Lic. Manuel B. Noboa G. Unidad Nº 3: Elementos de los Bloques P y D. Cómo podemos relacionar el conocimiento químico de los metales y no
Química 2 Tercero de Media. Proyecto 3 Marzo/Abril 2016. Prof.: Lic. Manuel B. Noboa G. Unidad Nº 3: Elementos de los Bloques P y D. Cómo podemos relacionar el conocimiento químico de los metales y no
PROGRAMA DE ASIGNATURA
 REPÚBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD NACIONAL EXPERIMENTAL RAFAEL MARÍA BARALT PROGRAMA EDUCACIÓN PROYECTO BIOLOGIA Y QUIMICA PROGRAMA DE ASIGNATURA NOMBRE DE LA ASIGNATURA CODI G MENC SEMESTRE
REPÚBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD NACIONAL EXPERIMENTAL RAFAEL MARÍA BARALT PROGRAMA EDUCACIÓN PROYECTO BIOLOGIA Y QUIMICA PROGRAMA DE ASIGNATURA NOMBRE DE LA ASIGNATURA CODI G MENC SEMESTRE
Expte. Nº c/1 SANTA FE,
 Expte. Nº 37.548 c/1 SANTA FE, 16-12-2010 VISTO el nuevo Régimen de Enseñanza aprobado por Resolución C.D. Nº 955/2009 y las actuaciones por las cuales el Dr. Roberto Delfor MEYER, Profesor Titular de
Expte. Nº 37.548 c/1 SANTA FE, 16-12-2010 VISTO el nuevo Régimen de Enseñanza aprobado por Resolución C.D. Nº 955/2009 y las actuaciones por las cuales el Dr. Roberto Delfor MEYER, Profesor Titular de
1.- CONCEPTOS PREVIOS
 TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
ANEXO FORMATO DE PROGRAMA DE ENSEÑANZA. Comunicación Organizacional. 2. Modalidad de la asignatura: Materia Optativa
 ANEXO FORMATO DE PROGRAMA DE ENSEÑANZA Año: 2011 Comunicación Organizacional 1. Denominación completa de la asignatura. Comunicación organizacional 2. Modalidad de la asignatura: Materia Optativa 3. Carga
ANEXO FORMATO DE PROGRAMA DE ENSEÑANZA Año: 2011 Comunicación Organizacional 1. Denominación completa de la asignatura. Comunicación organizacional 2. Modalidad de la asignatura: Materia Optativa 3. Carga
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO METALES
 CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17
 FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
Asignatura: Química I Carrera: Ciclo Lectivo: Docente/s: Carga horaria semanal: Tipo de Asignatura: Fundamentación y Objetivos: Fundamentación
 Asignatura: Química II Carrera: Bioquímica Ciclo Lectivo: 2015 Docente/s: Coordinadora: Laura Villata, José Ruggera, Ana Valino, Ernesto Cristian Hainich, Laura Esteban, Daniela Lufrano, Julieta Bertana,
Asignatura: Química II Carrera: Bioquímica Ciclo Lectivo: 2015 Docente/s: Coordinadora: Laura Villata, José Ruggera, Ana Valino, Ernesto Cristian Hainich, Laura Esteban, Daniela Lufrano, Julieta Bertana,
Química 2 Tercero de Media. Proyecto 3 Marzo/Abril Prof.: Lic. Manuel B. Noboa G. Unidad Nº 3: Elementos de los Bloques P y D.
 Química 2 Tercero de Media. Proyecto 3 Marzo/Abril 2017. Prof.: Lic. Manuel B. Noboa G. Unidad Nº 3: Elementos de los Bloques P y D. Describir las propiedades químicas generales de los elementos del bloque
Química 2 Tercero de Media. Proyecto 3 Marzo/Abril 2017. Prof.: Lic. Manuel B. Noboa G. Unidad Nº 3: Elementos de los Bloques P y D. Describir las propiedades químicas generales de los elementos del bloque
Compuesto N. Stock N. tradicional N. sistemática. óxido de hierro (III) óxido férrico trióxido de dihierro
 Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
PROGRAMA DE ESTUDIO. Básico ( ) Profesional ( x ) Especializado ( ) Horas de Teórica ( ) Presencial ( x ) Teórica-práctica ( ) Híbrida ( )
 PROGRAMA DE ESTUDIO Nombre de la asignatura: LABORATORIO DE QUÍMICA INORGÁNICA 1 Clave: LQU02 Fecha de elaboración: marzo 2015 Horas Semestre Horas semana Horas de Ciclo Formativo: Básico ( ) Profesional
PROGRAMA DE ESTUDIO Nombre de la asignatura: LABORATORIO DE QUÍMICA INORGÁNICA 1 Clave: LQU02 Fecha de elaboración: marzo 2015 Horas Semestre Horas semana Horas de Ciclo Formativo: Básico ( ) Profesional
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
ASIGNATURA: LABORATORIO DE QUÍMICA E INGENIERÍA I
 Página 1 de 6 CARACTERÍSTICAS GENERALES Tipo: Formación básica, Obligatoria, Optativa Trabajo de fin de grado, Prácticas externas Duración: Semestral Semestre/s: 3 Número de créditos ECTS: 5 Idioma/s:
Página 1 de 6 CARACTERÍSTICAS GENERALES Tipo: Formación básica, Obligatoria, Optativa Trabajo de fin de grado, Prácticas externas Duración: Semestral Semestre/s: 3 Número de créditos ECTS: 5 Idioma/s:
Calcio(2+) Hierro(3+)
 CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO MATERIAS BÁSICAS QUÍMICA 1º 1º 6 BÁSICA
 GUIA DOCENTE DE LA ASIGNATURA QUÍMICA MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO MATERIAS BÁSICAS QUÍMICA 1º 1º 6 BÁSICA PROFESOR(ES) María Dolores Fernández Ramos (Grupo A) Salvador Casares Atienza (Grupo
GUIA DOCENTE DE LA ASIGNATURA QUÍMICA MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO MATERIAS BÁSICAS QUÍMICA 1º 1º 6 BÁSICA PROFESOR(ES) María Dolores Fernández Ramos (Grupo A) Salvador Casares Atienza (Grupo
Pontificia Universidad Católica del Ecuador
 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: QUIMICA ANALÍTICA I (T-L) CÓDIGO: 12810 CARRERA. CIENCIAS QUIMICAS, MENCIÓN QUÍMICA ANALÍTICA NIVEL: TERCERO No. CRÉDITOS: 5 CRÉDITOS TEORÍA: 3 SEMESTRE/AÑO ACADÉMICO:
1. DATOS INFORMATIVOS: MATERIA O MÓDULO: QUIMICA ANALÍTICA I (T-L) CÓDIGO: 12810 CARRERA. CIENCIAS QUIMICAS, MENCIÓN QUÍMICA ANALÍTICA NIVEL: TERCERO No. CRÉDITOS: 5 CRÉDITOS TEORÍA: 3 SEMESTRE/AÑO ACADÉMICO:
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
Pontificia Universidad Católica del Ecuador
 Pontificia Universidad Católica del Ecuador Escuela de Ciencias Químicas 1.- DATOS INFORMATIVOS: MATERIA: Química General I (Teoría y Laboratorio) CODIGO: 12793 CARRERA: Ciencias Químicas, mención Química
Pontificia Universidad Católica del Ecuador Escuela de Ciencias Químicas 1.- DATOS INFORMATIVOS: MATERIA: Química General I (Teoría y Laboratorio) CODIGO: 12793 CARRERA: Ciencias Químicas, mención Química
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
OBJETIVOS DE LA ASIGNATURA
 ASIGNATURA: QUÍMICA INORGÁNICA Y ORGÁNICA ESPECIALIDAD: INGENIERIA METALURGICA PLAN: 1995 ADECUADO (Ordenanza Nº 1058) NIVEL: 2º MODALIDAD: ANUAL DICTADO: ANUAL HORAS: 4 Hs semanales ÁREA: TECNOLOGÍAS
ASIGNATURA: QUÍMICA INORGÁNICA Y ORGÁNICA ESPECIALIDAD: INGENIERIA METALURGICA PLAN: 1995 ADECUADO (Ordenanza Nº 1058) NIVEL: 2º MODALIDAD: ANUAL DICTADO: ANUAL HORAS: 4 Hs semanales ÁREA: TECNOLOGÍAS
INTRODUCCIÓN A LA QUÍMICA
 INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
QI - Química Inorgánica
 Unidad responsable: 230 - ETSETB - Escuela Técnica Superior de Ingeniería de Telecomunicación de Barcelona Unidad que imparte: 713 - EQ - Departamento de Ingeniería Química Curso: Titulación: 2016 GRADO
Unidad responsable: 230 - ETSETB - Escuela Técnica Superior de Ingeniería de Telecomunicación de Barcelona Unidad que imparte: 713 - EQ - Departamento de Ingeniería Química Curso: Titulación: 2016 GRADO
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS.
 QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
QUÍMICA INORGÁNICA AVANZADA( )
 QUÍMICA INORGÁNICA AVANZADA ( 2010-11 ) Datos Generales Código 7443 Descripción Crdts. Teor. 7 SÓLIDOS INORGÁNICOS. COMPUESTOS DE COORDINACIÓN Y ORGANOMETÁLICOS. Crdts. Pract. 2 A efectos de intercambios
QUÍMICA INORGÁNICA AVANZADA ( 2010-11 ) Datos Generales Código 7443 Descripción Crdts. Teor. 7 SÓLIDOS INORGÁNICOS. COMPUESTOS DE COORDINACIÓN Y ORGANOMETÁLICOS. Crdts. Pract. 2 A efectos de intercambios
Compuestos Químicos. Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115
 Compuestos Químicos Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115 Tipos de enlaces Enlaces covalentes comparten electrones entre átomos y forman compuestos moleculares. Estos compuestos son representados
Compuestos Químicos Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115 Tipos de enlaces Enlaces covalentes comparten electrones entre átomos y forman compuestos moleculares. Estos compuestos son representados
