INFORME DE INTERVENCIONES NO FAVORABLES 2018 Condición de Salud: Cáncer de Ovario Epitelial Tecnología Sanitaria Evaluada: Trabectedina
|
|
|
- Carlos César Ríos Cabrera
- hace 5 años
- Vistas:
Transcripción
1 INFORME DE INTERVENCIONES NO FAVORABLES 2018 Condición de Salud: Cáncer de Ovario Epitelial Tecnología Sanitaria Evaluada: Trabectedina Sistema de Protección Financiera para Diagnósticos y Tratamientos de Alto Costo. Ley Nº Ley Ricarte Soto. Subsecretaría de Salud Pública División de Planificación Sanitaria Departamento Evaluación de Tecnologías Sanitarias y Salud Basada en Evidencia y Salud Basada en Evidencia
2 Ministerio de Salud. Informe de Intervenciones No favorables. Cáncer de ovario epitelial. Santiago, MINSAL Todos los derechos reservados. Este material puede ser reproducido total o parcialmente para fines de diseminación y capacitación. Prohibida su venta. Fecha 1ª Edición: 2017 Fecha 2ª Edición: Octubre
3 ÍNDICE 1. INTRODUCCIÓN SOLICITUDES EN EVALUACIÓN CONDICIÓN DE SALUD ANALIZADA TECNOLOGÍAS SANITARIAS ANALIZADAS RESUMEN EJECUTIVO... 4 Eficacia de los tratamientos... 5 Análisis Económico... 5 Implementación y efectos en las redes asistenciales DESCRIPCIÓN DE LA ENFERMEDAD... 6 Diagnóstico e identificación de subgrupos ALTERNATIVAS DISPONIBLES DESCRIPCIÓN DE LOS TRATAMIENTOS ANÁLISIS CRITERIOS DE INGRESO EFICACIA Y SEGURIDAD DE LOS TRATAMIENTOS a. Efectividad de los tratamientos b. Seguridad de los tratamientos ANÁLISIS ECONÓMICO IMPLEMENTACIÓN Y EFECTOS EN LAS REDES ASISTENCIALES REPERCUSIONES ÉTICAS, JURÍDICAS Y SOCIALES ALCANCE Y PLAZO DE LA EVALUACIÓN CONCLUSIÓN REFERENCIAS
4 CÁNCER DE OVARIO EPITELIAL 1. INTRODUCCIÓN Se considerarán para su evaluación aquellas solicitudes realizadas conforme al Reglamento que establece el proceso destinado a determinar los diagnósticos y tratamientos de alto costo con sistema de protección financiera, según lo establecido en los artículos 7 y 8 de la Ley N Estas solicitudes no son vinculantes para el Ministerio de Salud, debiendo, sin embargo, tomar especialmente en cuenta aquellas solicitudes y opiniones que hayan sido realizadas por sus comisiones técnicas asesoras y por las asociaciones de pacientes incluidas en el Registro de Asociaciones de Pacientes que crea la Ley De igual forma, para ser incorporadas en el proceso de evaluación científica de la evidencia, cada intervención debe cumplir con los criterios establecidos en el Artículo 6º del Reglamento mencionado, según lo indicado en el Numeral 9 del presente informe. 2. SOLICITUDES EN EVALUACIÓN Trabectedina para cáncer de ovario epitelial. 3. CONDICIÓN DE SALUD ANALIZADA Cáncer de ovario epitelial. 4. TECNOLOGÍAS SANITARIAS ANALIZADAS Trabectedina. 5. RESUMEN EJECUTIVO El cáncer epitelial de ovario es una alteración celular que se origina en el tejido proveniente del epitelio celómico de este órgano, representando al 85% de los tumores ováricos y su incidencia aumenta con la edad, ocurriendo la mitad de los casos en mujeres mayores de 65 años con un promedio de 55 años. Se clasifican en tumores potenciales benignos, de malignidad baja o borderline, y malignos. 4
5 Este informe evalúa trabectedina para cáncer de ovario epitelial recurrente sensible a platino (segunda línea). Eficacia de los tratamientos Se utilizaron 14 revisiones sistemáticas, las cuales incluyeron evidencia de efectividad de trabectedina (1 estudio primario), en pacientes con cáncer de ovario epitelial avanzado o recurrente. La terapia de trabectedina más doxorubicina tiene una certeza de la evidencia baja, comparado con la terapia de sólo doxorubicina, en pacientes con cáncer de ovario epitelial avanzado o recurrente. Por lo tanto, dado que el tamaño del efecto es muy pequeño para ser clínicamente relevante y, en conformidad con el Título III De las Evaluaciones Favorables de la Norma Técnica N 0192 del Ministerio de Salud, sobre el proceso de evaluación científica de la Evidencia establecido en el artículo 7 de la ley N , no se continúa con la evaluación en las otras etapas para trabectedina 2 da línea. Análisis Económico Trabectedina no fue evaluado esta dimensión, en conformidad con el Título III De las Evaluaciones Favorables de la Norma Técnica N 0192 del Ministerio de Salud, sobre el proceso de evaluación científica de la Evidencia establecido en el artículo 7 de la ley N , ya que la certeza de la evidencia de eficacia es baja en comparación a la alternativa de tratamiento. Implementación y efectos en las redes asistenciales Trabectedina no fue evaluado en esta dimensión, en conformidad con el Título III De las Evaluaciones Favorables de la Norma Técnica N 0192 del Ministerio de Salud, sobre el proceso de evaluación científica de la Evidencia establecido en el artículo 7 de la ley N , ya que la certeza de la evidencia de eficacia es baja en comparación a la alternativa de tratamiento. Cuadro resumen cumplimiento etapas de evaluación Problema de Salud Cáncer de Ovario epitelial Tratamiento solicitado Fue evaluado? Favorable / No favorable Etapa en que se excluye Observaciones Trabectedina Si No Favorable Eficacia Bajo tamaño del efecto. No es clínicamente relevante. 5
6 6. DESCRIPCIÓN DE LA ENFERMEDAD El cáncer epitelial de ovario es una alteración celular que se origina en el tejido proveniente del epitelio celómico de este órgano, representando al 85% de los tumores ováricos y su incidencia aumenta con la edad, ocurriendo la mitad de los casos en mujeres mayores de 65 años con un promedio de 55 años (1). Se clasifican en tumores potenciales benignos, de malignidad baja o borderline y malignos (2). Es el más frecuente de los cánceres ginecológicos, siendo la séptima causa de incidencia a nivel mundial con casos nuevos por año, así como la séptima causa de muertes en mujeres con casos (1). La incidencia esperada de cáncer epitelial de ovario en mujeres en Estados Unidos en el 2012 fue de aproximadamente ( muertes) y en Europa en 2008 se estimó en casos de pacientes ( muertes) (3). En el Reino Unido, según datos analizados por el National Institute for Health and Clinical Excellence (NICE), se reportan al 2008, mujeres portadoras de cáncer de ovario maligno o avanzado en etapas IIIB, IIIC y IV 1. En cuanto a la prevalencia del cáncer de ovario (todos sus tipos) en Chile al 2012, ésta corresponde a 28,6 casos por cada mujeres (incidencia acumulada a 5 años), equivalentes a 1995 casos de cáncer de ovario en alguno de sus tipos (4). En Chile, para el año 2010 el carcinoma epitelial de ovario constituyó la novena causa de muerte en la mujer, alcanzando el segundo lugar del total de tumores ginecológicos. Por otro lado, para el período , la tasa ajustada de incidencia de este cáncer en Chile fue de 6,4 por mujeres por año (1). Cuando el cáncer epitelial de ovario se detecta tempranamente, aproximadamente el 90% sobrevivirá más de cinco años. Sin embargo, su diagnóstico en un 70% se realiza en etapas avanzadas, III y IV, las que tienen mal pronóstico, con sobrevida a cinco años entre un 30 a 35% y 5 a 15%, para cada etapa respectivamente. Por el contrario, cuando es unilateral y localizado (etapa I) generalmente es curable (1,2). Diagnóstico e identificación de subgrupos Marcadores tumorales: El marcador tumoral CA-125 es el marcador sérico más utilizado para el tamizaje del cáncer de ovario, principalmente para el tipo epitelial (1,4). 1 National Institute for Health and Clinical Excellence (NICE). Ovarian Cancer: Recognition and Initial Management. 2011;(April):32; National Institute for Health and Clinical Excellence (NICE). Ovarian cancer : the recognition and initial management of ovarian cancer. 2011;(April):1 8 6
7 En este informe se considerarán pacientes con cáncer epitelial de ovario avanzado en etapas IIIB, IIIC y IV como tratamiento de primera línea, así como también en pacientes con cáncer recidivante, tanto sensibles como resistentes a platino (segunda línea). 7. ALTERNATIVAS DISPONIBLES Quimioterapia en 1a línea El tratamiento estándar es de la combinación de un agente platino y un taxano: carboplatino, cisplatino, paclitaxel, docetaxel. También existe la alternativa de doxorubicina liposomal. Para mantenimiento existe la opción de pazopanib o nintedanib (5). Terapia para pacientes con reincidencia, platino resistentes 1. Monoterapia con: paclitaxel, doxorubicina liposomal, gemcitabina, topotecan; etoposide, docetaxel, pemetrexed. 2. En combinación: paclitaxel con carboplatino, cisplatino y gemcitabina. 3. Terapia endocrina. 4. Terapia intraperitoneal hipertérmica (6). Terapia para pacientes con reincidencia, platino sensibles En primer lugar, se debe considerar terapia de cito reducción. Se recomienda el uso de un agente de platino, y se recomienda terapia en combinación en comparación con monoterapia ya que se asocia con mejor respuesta y progresión libre de enfermedad. Se recomienda, además, seguir terapia de mantenimiento. 1. En combinación: paclitaxel con carboplatino, carboplatino y gemcitabina, carboplatino y doxorubicina liposomal, cisplatino y gemcitabina. 2. Monoterapia: etoposide, topotecan, doxorubicina liposomal, gemcitabina, nabpaclitaxel. 3. Terapia de mantenimiento: cediranib, niraparib, olaparib, rucaparib (7). 7
8 8. DESCRIPCIÓN DE LOS TRATAMIENTOS TRABECTEDINA Registro e Indicación Trabectedina se encuentra registrado en el ISP con los números de registros y la condición evaluada, según se muestra en Tabla 1. Tabla 1. Registro en ISP para fulvestrant. Registro Nombre Fecha Registro Empresa F-17705/14 Yondelis Liofilizado para solución Johnson & Johnson S.A inyectable 1 mg Indicación En combinación con doxorubicina liposomal pegilada (PLD) está indicado en el tratamiento de pacientes con cáncer de ovario recidivante sensible al platino. Presentaciones Liofilizado para solución inyectable 1 mg. Laboratorio Yondelis de Johnson & Johnson S.A. Posología La dosis recomendada para el cáncer de ovario es de 1,1 mg/m 2 de superficie corporal, inmediatamente después de 30 mg/m 2 de PLD, cada 3 semanas, durante 6 ó más ciclos (se han utilizado hasta 38 ciclos en monoterapia y hasta 21 en terapia combinada). No se han observado toxicidades acumuladas en pacientes a los que se les administraron múltiples ciclos (8). 8
9 9. ANÁLISIS CRITERIOS DE INGRESO Las tecnologías evaluadas en el presente informe cumplen los criterios establecidos en el artículo Nº 6 del Reglamento que establece el proceso destinado a determinar los diagnósticos y tratamientos de alto costo con sistema de protección financiera, según lo establecido en los artículos 7 y 8 de la Ley N Éstos son: 1. Cobertura por la Ley : Las solicitudes de incorporación sólo pueden versar sobre diagnósticos o tratamientos basados ambos en exámenes diagnósticos y de seguimiento y, en el caso de tratamientos, además en medicamentos, elementos de uso médico o alimentos. 2. Pertinencia de la indicación: Los diagnósticos y tratamientos evaluados deberán, al momento de la solicitud, contar con registro o autorización con la indicación para la que ha sido propuesta la evaluación, en algún país que cuente con una autoridad regulatoria de alta vigilancia sanitaria (Instituto de Salud Pública, Agencia Europea de Medicamentos, FDA). Esta información fue extraída con fecha máxima el 29 de junio de 2018, del sitio electrónico del Instituto de Salud Pública. 3. Seguridad: Los diagnósticos y tratamientos evaluados no deberán tener reportes de reacciones adversas serias que hayan implicado una recomendación de restricción de uso en el grupo de pacientes a evaluar o hayan sido cancelados o suspendidos los permisos o registros por alguna autoridad regulatoria de referencia (Instituto de Salud Pública, Agencia Europea de Medicamentos, FDA). Esta información fue provista por el Instituto de Salud Pública mediante Ordinario Nº 591 del 05 de junio de Umbral: Sólo podrán ser objeto de evaluación aquellos diagnósticos y tratamientos cuyo costo sea igual o superior al umbral nacional al que se refiere el artículo 6º de la ley y que se encuentra fijado, a la fecha de elaboración de este informe, en $ , según consta en el Decreto Nº 80 del 23 de octubre de 2015, de los Ministerios de Salud y Hacienda. 5. Disponibilidad del Fondo: Los presupuestos estimados de diagnósticos y tratamiento evaluados no deben superar el 110% del fondo disponible que fija el Ministerio de Hacienda, previo al proceso de solicitud de información a proveedores. Para efectos de la determinación del cumplimiento de este criterio, se utilizó la disponibilidad presupuestaria preliminar informada por el Ministerio de Hacienda a través del Ordinario Nº 659 del 24 de abril de 2018, fijándose un gasto máximo de $5.905 Millones de pesos (110% del fondo disponible) para el año
10 10. EFICACIA Y SEGURIDAD DE LOS TRATAMIENTOS 10.a. Efectividad de los tratamientos Se evaluó la eficacia de trabectedina en mujeres con Cáncer de Ovario Epitelial avanzado o recurrente resistente o no a primera línea de tratamiento con platino. TRABECTEDINA Resultados de la búsqueda de evidencia Se encontró sólo 1 revisión sistemática, que evaluaba trabectedina (9), publicada el año Tabla 2. Características la evidencia para Trabectedina Cuál es la evidencia? Qué tipo de pacientes incluyeron los estudios? Qué tipo de intervenciones incluyeron los estudios? Qué tipo de desenlaces midieron? Para trabectedina, se extrajo la información de 1 revisión sistemática (9), la cual muestra los resultados de un artículo primario (10). Los pacientes incluidos en este reporte son mujeres con cáncer de ovario epitelial avanzado o recurrente, pudiendo haber sido resistentes o sensibles a terapias con platino. Intervención: consistió en trabectedina más doxorubicina comparada con doxorubicina sola. Los desenlaces medidos fueron progresión libre de enfermedad (PLE) y la sobrevida global (SG), ambos medidos en meses. PLE es el tiempo durante y después del tratamiento que un paciente vive con la enfermedad y ésta no empeora. SG equivale al periodo de tiempo, desde el diagnóstico o desde el comienzo del tratamiento, que los pacientes permanecen con vida. Fuente de financiamiento Genetech (10). 10
11 Resumen de resultados Tabla 3. Resumen de evidencia para trabectedina más doxorubicina vs doxorubicina, en pacientes con cáncer de ovario epitelial avanzado o recurrente. Trabectedina más doxorubicina vs doxorubicina, en pacientes con cáncer de ovario epitelial avanzado o recurrente. Pacientes Intervención Comparación Cáncer de ovario epitelial avanzado o recurrente. Trabectedina más doxorubicina. Doxorubicina. Desenlaces Mortalidad (corto plazo) 21 meses Progresión de enfermedad (corto plazo) 10 meses Efecto relativo (IC 95%) RR 0.97 (0,91 to 1,04) de participantes: 672 (1 ECA) RR 0.87 (0,79 to 0,96) de participantes: 417 (1 ECA) *Efectos absolutos anticipados (95% CI) Doxorubicina 85,7% Trabectedina + doxorubicina 587 Por 1000 Diferencia 2,6% menos (7,7 menos a 3,4 más) 85,1% 74,1% 11,1% menos (17,9 menos a 3,4 menos) Certeza de la evidencia (GRADE) MODERADO a BAJA a,b Mensajes claves en términos sencillos La terapia de trabectedina más doxorubicina probablemente reduce levemente la mortalidad comparado con la terapia de sólo doxorubicina en las pacientes con cáncer de ovario epitelial avanzado o recurrente. La terapia de trabectedina podría aumentar ligeramente la proporción de pacientes que logran disminuir la progresión de la enfermedad. * El riesgo en el grupo de intervención (y su intervalo de confianza del 95%) se basa en el riesgo asumido en el grupo de comparación y en el efecto relativo de la intervención (y su intervalo de confianza del 95%). Los riesgos SIN Intervención están basados en los riesgos del grupo control en los estudios. CI: Intervalo de confianza; RR: Razón de riesgo; MD: Diferencia media; ECA: Ensayo controlado aleatorizado; NA: No aplica a. Sin claridad en cómo se realizó la aleatorización de pacientes b. Intervalo de confianza ancho (imprecisión) 11
12 Consideraciones adicionales Los desenlaces que fueron incluidos en este resumen son aquellos considerados como críticos en la toma de decisión. Se puede observar que pese a que los desenlaces principales reportados por los estudios fueron sobrevida global y libre de progresión, estos datos fueron transformados para presentar mortalidad y progresión de la enfermedad, de manera de facilitar la comprensión de cada resultado. Por último, todos los estudios contemplados en esta síntesis son ECAs. No se encontraron estudios observacionales que fueran reportados en revisiones sistemáticas que abordaran la eficacia de trabectedina en cáncer de ovario. Trabectedina no continua el proceso de evaluación, dado que el tamaño del efecto es muy pequeño para ser clínicamente relevante y, en conformidad con el Título III De las Evaluaciones Favorables de la Norma Técnica N 0192 del Ministerio de Salud, sobre el proceso de evaluación científica de la Evidencia establecido en el artículo 7 de la ley N , no continua su evaluación. 10.b. Seguridad de los tratamientos En Tabla 4 se indican las reacciones adversas de trabectedina según lo notificado por la EMA. Tabla 4. Tabla de reacciones adversas para trabectedina 2 Sistema de clasificación de órganos Infecciones e infestaciones Trastornos de la sangre y del sistema linfático Trastornos del metabolismo y de la nutrición Trastornos psiquiátricos Reacciones adversas notificadas en 1 % de los pacientes con sarcoma de los tejidos blandos de los ensayos clínicos. Infección Muy frecuentes Neutropenia* (grado 3 = 26 %, grado 4 = 24 %), trombocitopenia* (grado 3 = 11 %, grado 4 = 2 %), anemia* (grado 3 = 10 %, grado 4 = 3 %), leucopenia* Neutropenia febril Muy frecuentes Anorexia (grado 3-4 < 1 %) Deshidratación, pérdida de apetito, hipopotasemia Insomnio 2 Tabla de reacciones adversas extraída de Anexo I Ficha Técnica de las Características del Producto trabectedina (Yondelis), de la Agencia de Medicamentos Europea EMA. 12
13 Trastornos del sistema nervioso Trastornos vasculares Trastornos respiratorios, torácicos y mediastínicos Trastornos gastrointestinales Trastornos hepatobiliares Trastornos de la piel y del tejido subcutáneo Trastornos musculoesqueléticos y del tejido conjuntivo Trastornos generales y alteraciones en el lugar de administración Exploraciones complementarias Muy frecuentes Dolor de cabeza Neuropatía sensorial periférica, disgeusia, mareos, parestesia Hipotensión, sofocos Poco frecuentes Síndrome de fuga capilar Disnea (grado 3-4 = 2 %), tos Muy frecuentes Vómitos (grado 3-4 = 6,5 %), náuseas (grado 3-4 = 6 %), estreñimiento (grado 3-4 < 1 %) Diarrea (grado 3-4 < 1 %), estomatitis (grado 3-4 < 1 %), dolor abdominal, dispepsia, dolor abdominal superior Muy frecuentes Hiperbilirrubinemia* (grado 3 = 1 %), incremento de alanina aminotransferasa* (grado 3 = 38 %, grado 4 = 3 %), incremento de aspartato aminotransferasa* (grado 3 = 44 %, grado 4 = 7 %), incremento de la fosfatasa alcalina en sangre*, incremento de la gammaglutamiltransferasa* Alopecia Mialgia, artralgia, dolor de espalda Muy frecuentes Cansancio (grado 3-4 = 9 %), astenia (grado 3-4 = 1 %) Pirexia, edema, edema periférico, reacción en el lugar de inyección Muy frecuentes Incremento de la creatina fosfoquinasa en sangre* (grado 3-4 = 4 %), incremento de la creatinina en sangre*, disminución de la albúmina en sangre* Pérdida de peso Las reacciones adversas que se indican a continuación se clasifican como muy frecuentes ( 1/10), frecuentes ( 1/100 a < 1/10) y poco frecuentes ( 1/1000 a < 1/100). El ISP no reporta reacciones adversas medicamentosas a trabectedina en periodo 2015 a junio
14 11. ANÁLISIS ECONÓMICO Trabectedina no fue evaluado esta dimensión, en conformidad con el Título III De las Evaluaciones Favorables de la Norma Técnica N 0192 del Ministerio de Salud, sobre el proceso de evaluación científica de la Evidencia establecido en el artículo 7 de la ley N , ya que la certeza de la evidencia de eficacia es baja en comparación a la alternativa de tratamiento. 12. IMPLEMENTACIÓN Y EFECTOS EN LAS REDES ASISTENCIALES Trabectedina no fue evaluado esta dimensión, en conformidad con el Título III De las Evaluaciones Favorables de la Norma Técnica N 0192 del Ministerio de Salud, sobre el proceso de evaluación científica de la Evidencia establecido en el artículo 7 de la ley N , ya que la certeza de la evidencia de eficacia es baja en comparación a la alternativa de tratamiento. 13. REPERCUSIONES ÉTICAS, JURÍDICAS Y SOCIALES Trabectedina no fue evaluado esta dimensión, en conformidad con el Título III De las Evaluaciones Favorables de la Norma Técnica N 0192 del Ministerio de Salud, sobre el proceso de evaluación científica de la Evidencia establecido en el artículo 7 de la ley N , ya que la certeza de la evidencia de eficacia es baja en comparación a la alternativa de tratamiento. 14. ALCANCE Y PLAZO DE LA EVALUACIÓN La presente evaluación será actualizada en un plazo máximo de hasta 5 años o al presentarse alguna de las condiciones establecidas en el subtítulo II.ii Alcance y plazo de revisión de la evaluación, de la Norma Técnica N 0192 del Ministerio de Salud, sobre el proceso de evaluación científica de la Evidencia establecido en el artículo 7 de la ley N CONCLUSIÓN Para dar cumplimiento al artículo 28 del Reglamento que establece el proceso destinado a determinar los diagnósticos y tratamientos de alto costo con Sistema de Protección Financiera, según lo establecido en los artículos 7 y 8 de la ley N , aprobado por el decreto N 13 del Ministerio de Salud, se concluye que el presente informe de evaluación se considera no favorable, de acuerdo a lo establecido en el Título III. de las Evaluaciones Favorables de la Norma Técnica N 0192 de este mismo ministerio. 14
15 16. REFERENCIAS 1. Ministerio de Salud Chile. Guía Clínica AUGE Cáncer de Ovario Epitelial Jessmon P, Boulanger T, Zhou W, Patwardhan P. Epidemiology and treatment patterns of epithelial ovarian cancer. Expert Rev Anticancer Ther [Internet]. 2017;0(0): Available from: 3. Aghajanian C, Blank S V, Goff BA, Judson PL, Teneriello MG, Husain A, et al. OCEANS: A Randomized, Double-Blind, Placebo-Controlled Phase III Trial of Chemotherapy With or Without Bevacizumab in Patients With Platinum-Sensitive Recurrent Epithelial Ovarian, Primary Peritoneal, or Fallopian Tube Cancer. J Clin Oncol [Internet] Jun 10;30(17): Available from: 4. Ferlay J, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, et al. Cancer incidence and mortality worldwide. IARC CancerBase No. 11GLOBOCAN Coleman RL, Brady MF, Herzog TJ, Sabbatini P, Armstrong DK, Walker JL, et al. A phase III randomized controlled clinical trial of carboplatin and paclitaxel alone or in combination with bevacizumab followed by bevacizumab and secondary cytoreductive surgery in platinum-sensitive, recurrent ovarian, peritoneal primary and fallopian. Gynecol Oncol [Internet]. 2015;137(2015):3 4. Available from: 6. Birrer M, Fujiwara K. Medical treatment for relapsed epithelial ovarian, fallopian tubal, or peritoneal cancer: Platinum-resistant disease - UpToDate [Internet]. [cited 2018 Sep 28]. Available from: arian,%2520fallopian%2520tubal,%2520or%2520peritoneal%25 7. Coleman R, Sabbatini P. Medical treatment for relapsed epithelial ovarian, fallopian tubal, or peritoneal cancer: Platinum-sensitive disease - UpToDate [Internet]. [cited 2018 Sep 28]. Available from: 8. European Medicines Agency (EMA). Yondelis trabectedina Edwards SJ, Barton S, Thurgar E, Trevor N. Topotecan, pegylated liposomal doxorubicin hydrochloride, paclitaxel, trabectedin and gemcitabine for advanced recurrent or refractory ovarian cancer: A systematic review and economic evaluation. Health Technol Assess (Rockv). 2015;19(7): Monk BJ, Herzog TJ, Kaye SB, Krasner CN, Vermorken JB, Muggia FM, et al. Trabectedin Plus Pegylated Liposomal Doxorubicin in Recurrent Ovarian Cancer. J Clin Oncol [Internet] Jul 1 [cited 2017 Sep 11];28(19): Available from: 15
Sistema de Protección Financiera para Diagnósticos y Tratamientos de Alto Costo. Ley Nº Ley Ricarte Soto.
 INFORME DE EVALUACIÓN CIENTÍFICA BASADA EN LA EVIDENCIA DISPONIBLE Condición de Salud: Cáncer de Ovario Epitelial Tecnología Sanitaria Evaluada: Bevacizumab y Trabectedina. Subsecretaría de Salud Pública
INFORME DE EVALUACIÓN CIENTÍFICA BASADA EN LA EVIDENCIA DISPONIBLE Condición de Salud: Cáncer de Ovario Epitelial Tecnología Sanitaria Evaluada: Bevacizumab y Trabectedina. Subsecretaría de Salud Pública
Tratamiento de segunda línea en tumores con sensibilidad a platino.
 Cáncer de ovario Tratamiento de segunda línea en tumores con sensibilidad a platino. Sara Pérez Ramírez MIR IV Oncología Médica Hospital Gregorio Marañón Madrid, 27 Mayo 2014 Introducción Entre el 70-80%
Cáncer de ovario Tratamiento de segunda línea en tumores con sensibilidad a platino. Sara Pérez Ramírez MIR IV Oncología Médica Hospital Gregorio Marañón Madrid, 27 Mayo 2014 Introducción Entre el 70-80%
: Topotecan 4mg inyectable
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE RESULTADOS DE CRIZOTINIB EN CÁNCER DE PULMÓN NO MICROCÍTICO. Mª José Moreno Fernández
 EVALUACIÓN DE RESULTADOS DE CRIZOTINIB EN CÁNCER DE PULMÓN NO MICROCÍTICO Mª José Moreno Fernández Introducción. Situación actual de Crizotinib. Objetivos. Material y métodos. Resultados. Limitaciones
EVALUACIÓN DE RESULTADOS DE CRIZOTINIB EN CÁNCER DE PULMÓN NO MICROCÍTICO Mª José Moreno Fernández Introducción. Situación actual de Crizotinib. Objetivos. Material y métodos. Resultados. Limitaciones
Tratamiento de la recai da del ca ncer de ovario en pacientes no candidatas a platino
 Tratamiento de la recai da del ca ncer de ovario en pacientes no candidatas a platino Ana Santaballa Bertrán, MD, PhD Servicio Oncologi a Me dica, Hospital Universitario y Polite cnico la Fe, Valencia
Tratamiento de la recai da del ca ncer de ovario en pacientes no candidatas a platino Ana Santaballa Bertrán, MD, PhD Servicio Oncologi a Me dica, Hospital Universitario y Polite cnico la Fe, Valencia
REUNION BIBLOGRAFICA M
 REUNION BIBLOGRAFICA Ma. Florencia Leguizamón INTRODUCCIÓN Los pacientes con cáncer de pulmón avanzado no células pequeñas con mutación del EGFR pueden experimentar una importante reducción del tumor
REUNION BIBLOGRAFICA Ma. Florencia Leguizamón INTRODUCCIÓN Los pacientes con cáncer de pulmón avanzado no células pequeñas con mutación del EGFR pueden experimentar una importante reducción del tumor
Cáncer de ovario: estado del Arte y nuevas alternativas terapeúticas. Mª Jesús Rubio Pérez H.U.Reina Sofía. Córdoba
 Cáncer de ovario: estado del Arte y nuevas alternativas terapeúticas Mª Jesús Rubio Pérez H.U.Reina Sofía. Córdoba Introducción La secuencia estándar del tratamiento consiste en: Realización de una cirugía
Cáncer de ovario: estado del Arte y nuevas alternativas terapeúticas Mª Jesús Rubio Pérez H.U.Reina Sofía. Córdoba Introducción La secuencia estándar del tratamiento consiste en: Realización de una cirugía
Comisión Nacional del Mercado de Valores Att. Director del Área de Mercados C/ Miguel Ángel 11, 1º Madrid
 Comisión Nacional del Mercado de Valores Att. Director del Área de Mercados C/ Miguel Ángel 11, 1º 28010 Madrid Madrid, a 1 de octubre de 2012 De conformidad con lo previsto en el artículo 82 de la Ley
Comisión Nacional del Mercado de Valores Att. Director del Área de Mercados C/ Miguel Ángel 11, 1º 28010 Madrid Madrid, a 1 de octubre de 2012 De conformidad con lo previsto en el artículo 82 de la Ley
Indicaciones clínicas formalmente aprobadas y fecha de aprobación:
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
Cáncer de Ovario Platino-Resistente. Tatiana Hernández Guerrero Médico Residente 4º año Servicio de Oncología Médica. Fundación Jiménez Díaz Madrid
 Cáncer de Ovario Platino-Resistente. Tatiana Hernández Guerrero Médico Residente 4º año Servicio de Oncología Médica. Fundación Jiménez Díaz Madrid Enfermedad platino-resistente. Definición La respuesta
Cáncer de Ovario Platino-Resistente. Tatiana Hernández Guerrero Médico Residente 4º año Servicio de Oncología Médica. Fundación Jiménez Díaz Madrid Enfermedad platino-resistente. Definición La respuesta
Cáncer de Ovario. Tratamiento sistémico de primera línea
 Cáncer de Ovario. Tratamiento sistémico de primera línea Mauro Antonio Valles Cancela MIR IV Oncología Médica Hospital Clínico Lozano Blesa. Zaragoza Un Poco de historia Alquilantes 80s CFM +ADR Standard
Cáncer de Ovario. Tratamiento sistémico de primera línea Mauro Antonio Valles Cancela MIR IV Oncología Médica Hospital Clínico Lozano Blesa. Zaragoza Un Poco de historia Alquilantes 80s CFM +ADR Standard
CUESTIONES RESUELTAS Y EVIDENCIA QUE LAS APOYA
 CUESTIONES RESUELTAS Y EVIDENCIA QUE LAS APOYA PEDRO ANTONIO CASCALES CAMPOS UNIDAD DE CIRUGÍA ONCOLÓGICA PERITONEAL HOSPITAL CLÍNICO UNIVERSITARIO VIRGEN DE LA ARRIXACA-IMIB ARRIXACA UNIVERSIDAD DE MURCIA
CUESTIONES RESUELTAS Y EVIDENCIA QUE LAS APOYA PEDRO ANTONIO CASCALES CAMPOS UNIDAD DE CIRUGÍA ONCOLÓGICA PERITONEAL HOSPITAL CLÍNICO UNIVERSITARIO VIRGEN DE LA ARRIXACA-IMIB ARRIXACA UNIVERSIDAD DE MURCIA
RESUMEN EJECUTIVO Guía de Práctica Clínica Retinopatía Diabética 2017
 Subsecretaría de Salud Pública División de Prevención y Control de Enfermedades, DIPRECE División de Planificación Sanitaria, DIPLAS RESUMEN EJECUTIVO Guía de Práctica Clínica Retinopatía Diabética 2017
Subsecretaría de Salud Pública División de Prevención y Control de Enfermedades, DIPRECE División de Planificación Sanitaria, DIPLAS RESUMEN EJECUTIVO Guía de Práctica Clínica Retinopatía Diabética 2017
VINORELBINA ORAL. Evaluación para la Guía Farmacoterapéutica de Hospitales del Sistema Sanitario Público de Andalucía, Según el método GINF.
 VINORELBINA ORAL Evaluación para la Guía Farmacoterapéutica de Hospitales del Sistema Sanitario Público de Andalucía, Según el método GINF. Autores: Carmen Martínez Díaz, Jorge Díaz Navarro. Hospital Universitario
VINORELBINA ORAL Evaluación para la Guía Farmacoterapéutica de Hospitales del Sistema Sanitario Público de Andalucía, Según el método GINF. Autores: Carmen Martínez Díaz, Jorge Díaz Navarro. Hospital Universitario
Ponente: Héctor Randhall Callata Carhuapoma MIR Oncología Médica 5º año Hospital Clínico San Carlos
 REINTRODUCCIÓN DE AGENTES PLATINO TRAS TRATAMIENTO CON TRABECTEDINA EN PACIENTES CON CÁNCER DE OVARIO RECURRENTE (COR) RESISTENTE/REFRACTARIO (RR) Y PARCIALMENTE SENSIBLE A PLATINO (PSP) Héctor R. Callata
REINTRODUCCIÓN DE AGENTES PLATINO TRAS TRATAMIENTO CON TRABECTEDINA EN PACIENTES CON CÁNCER DE OVARIO RECURRENTE (COR) RESISTENTE/REFRACTARIO (RR) Y PARCIALMENTE SENSIBLE A PLATINO (PSP) Héctor R. Callata
BIBLIOGRAFICO ONCOLOGIA ESTUDIO: AVAPERL. Dra. Evelyn S Colombo
 BIBLIOGRAFICO ONCOLOGIA 03.09.13 ESTUDIO: AVAPERL Dra. Evelyn S Colombo Para los pacientes con NSCLC avanzado o metastásico, el pronóstico es pobre, y las tasas de supervivencia a 1 año es de 30 % a 40
BIBLIOGRAFICO ONCOLOGIA 03.09.13 ESTUDIO: AVAPERL Dra. Evelyn S Colombo Para los pacientes con NSCLC avanzado o metastásico, el pronóstico es pobre, y las tasas de supervivencia a 1 año es de 30 % a 40
1. DENOMINACIÓN DEL ESQUEMA: DOXORUBICINA LIPOSOMAL. Cáncer de ovario avanzado en mujeres en las que ha fallado un régimen de primera
 1. DENOMINACIÓN DEL ESQUEMA: DOXORUBICINA LIPOSOMAL 2. USO TERAPÉUTICO Cáncer de ovario avanzado en mujeres en las que ha fallado un régimen de primera línea conteniendo platino. 3. ESQUEMA (1) Medicamento
1. DENOMINACIÓN DEL ESQUEMA: DOXORUBICINA LIPOSOMAL 2. USO TERAPÉUTICO Cáncer de ovario avanzado en mujeres en las que ha fallado un régimen de primera línea conteniendo platino. 3. ESQUEMA (1) Medicamento
Comisión Nacional del Mercado de Valores Att. Director del Área de Mercados C/ Miguel Ángel 11, 1º Madrid
 Comisión Nacional del Mercado de Valores Att. Director del Área de Mercados C/ Miguel Ángel 11, 1º 28010 Madrid Madrid, a 7 de junio de 2011 De conformidad con lo previsto en el artículo 82 de la Ley del
Comisión Nacional del Mercado de Valores Att. Director del Área de Mercados C/ Miguel Ángel 11, 1º 28010 Madrid Madrid, a 7 de junio de 2011 De conformidad con lo previsto en el artículo 82 de la Ley del
RESUMEN EJECUTIVO Guía de Práctica Clínica Vicios de Refracción en Personas de 65 años y más 2017
 Subsecretaría de Salud Pública División de Prevención y Control de Enfermedades, DIPRECE División de Planificación Sanitaria, DIPLAS RESUMEN EJECUTIVO Guía de Práctica Clínica Vicios de Refracción en Personas
Subsecretaría de Salud Pública División de Prevención y Control de Enfermedades, DIPRECE División de Planificación Sanitaria, DIPLAS RESUMEN EJECUTIVO Guía de Práctica Clínica Vicios de Refracción en Personas
MIELOMA MÚLTIPLE: Bortezomib 1/6
 MIELOMA MÚLTIPLE: Bortezomib 1/6 1. DENOMINACIÓN DEL ESQUEMA: BORTEZOMIB 2. USO TERAPÉUTICO (1) : Tratamiento de pacientes con mieloma múltiple que han recibido al menos dos tratamientos previos y que
MIELOMA MÚLTIPLE: Bortezomib 1/6 1. DENOMINACIÓN DEL ESQUEMA: BORTEZOMIB 2. USO TERAPÉUTICO (1) : Tratamiento de pacientes con mieloma múltiple que han recibido al menos dos tratamientos previos y que
CÁNCER DE VEJIGA. Novedades: Terapia de mantenimiento. Begoña Pérez-Valderrama. HH.UU. Virgen del Rocío. Sevilla.
 CÁNCER DE VEJIGA. Novedades: Terapia de mantenimiento. Begoña Pérez-Valderrama. HH.UU. Virgen del Rocío. Sevilla. INTRODUCCIÓN CARCINOMA UROTELIAL. Europa 90% -> vejiga urinaria 8 % -> pelvis renal 151.297
CÁNCER DE VEJIGA. Novedades: Terapia de mantenimiento. Begoña Pérez-Valderrama. HH.UU. Virgen del Rocío. Sevilla. INTRODUCCIÓN CARCINOMA UROTELIAL. Europa 90% -> vejiga urinaria 8 % -> pelvis renal 151.297
Vitamina K para evitar la anticoagulación en recién nacidos
 Vitamina K para evitar la anticoagulación en recién nacidos PREGUNTA Es necesaria la administración de para evitar problemas de anticoagulación en recién nacidos? CONTEXTO Anticoagulación en recién nacidos
Vitamina K para evitar la anticoagulación en recién nacidos PREGUNTA Es necesaria la administración de para evitar problemas de anticoagulación en recién nacidos? CONTEXTO Anticoagulación en recién nacidos
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. DENOMINACIÓN DEL MEDICAMENTO Docetaxel Winthrop 20 mg concentrado y disolvente para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. DENOMINACIÓN DEL MEDICAMENTO Docetaxel Winthrop 20 mg concentrado y disolvente para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Bortezomib. Informe preliminar del Servicio de Farmacia
 Servicio Andaluz de Salud CONSEJERÍA DE SALUD Hospital Universitario Reina Sofía Bortezomib Informe preliminar del Servicio de Farmacia 1.- Identificación del fármaco: Nombre Comercial: Velcade 3.5mg Presentaciones:
Servicio Andaluz de Salud CONSEJERÍA DE SALUD Hospital Universitario Reina Sofía Bortezomib Informe preliminar del Servicio de Farmacia 1.- Identificación del fármaco: Nombre Comercial: Velcade 3.5mg Presentaciones:
A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN
 6 CARMUSTINA EN IMPLANTES A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. CARMUSTINA
6 CARMUSTINA EN IMPLANTES A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. CARMUSTINA
Prevención de la hemorragia posparto (misoprostol)
 posparto (misoprostol) PREGUNTA Cuál es el papel de misoprostol en la prevención de la posparto? CONTEXTO Hemorragia posparto La posparto se define como una pérdida sanguínea vaginal de más de 500 ml.
posparto (misoprostol) PREGUNTA Cuál es el papel de misoprostol en la prevención de la posparto? CONTEXTO Hemorragia posparto La posparto se define como una pérdida sanguínea vaginal de más de 500 ml.
Medicamento Dosis Días Administración Vinorelbina mg/m 2 (2,3) 1 Infusión de 50 ml SF administrado en min* (4,5)
 1. DENOMINACIÓN DEL ESQUEMA: VINORELBINA 2. INDICACIÓN Carcinoma de mama avanzado (1) 3. ESQUEMA Medicamento Dosis Días Administración Vinorelbina 25 30 mg/m 2 (2,3) 1 Infusión de 50 ml SF administrado
1. DENOMINACIÓN DEL ESQUEMA: VINORELBINA 2. INDICACIÓN Carcinoma de mama avanzado (1) 3. ESQUEMA Medicamento Dosis Días Administración Vinorelbina 25 30 mg/m 2 (2,3) 1 Infusión de 50 ml SF administrado
RESUMEN EJECUTIVO Guía de Práctica Clínica Displasia Broncopulmonar del Prematuro 2017
 Subsecretaría de Salud Pública División de Prevención y Control de Enfermedades, DIPRECE División de Planificación Sanitaria, DIPLAS RESUMEN EJECUTIVO Guía de Práctica Clínica Displasia Broncopulmonar
Subsecretaría de Salud Pública División de Prevención y Control de Enfermedades, DIPRECE División de Planificación Sanitaria, DIPLAS RESUMEN EJECUTIVO Guía de Práctica Clínica Displasia Broncopulmonar
Impacto de los nuevos tratamientos. Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena
 Impacto de los nuevos tratamientos Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena Indicaciones. Ipilimumab (Yervoy): EMA: tratamiento del melanoma avanzado (irresecable o metastásico) en adultos
Impacto de los nuevos tratamientos Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena Indicaciones. Ipilimumab (Yervoy): EMA: tratamiento del melanoma avanzado (irresecable o metastásico) en adultos
PAPEL DE CETUXIMAB EN EL TRATAMIENTO DE 1ª LÍNEA DE CECC RECURRENTE Y METASTÁSICO. Pedro Pérez Segura Oncología Médica - HCSC
 PAPEL DE CETUXIMAB EN EL TRATAMIENTO DE 1ª LÍNEA DE CECC RECURRENTE Y METASTÁSICO Pedro Pérez Segura Oncología Médica - HCSC TRAYECTORIA DE CETUXIMAB Aprob CTX 1ªL ESMO/ASCO 1977 1985 2005 2008 2009 2010
PAPEL DE CETUXIMAB EN EL TRATAMIENTO DE 1ª LÍNEA DE CECC RECURRENTE Y METASTÁSICO Pedro Pérez Segura Oncología Médica - HCSC TRAYECTORIA DE CETUXIMAB Aprob CTX 1ªL ESMO/ASCO 1977 1985 2005 2008 2009 2010
REUNION BIBLIOGRAFICA Martes 26 de Noviembre de 2013
 REUNION BIBLIOGRAFICA Martes 26 de Noviembre de 2013 CENTRO: HOSPITAL NACIONAL DE CLINICAS Mendez Norberto, Médico. PUNTOS CLAVE CANCER GASTRICO La incidencia de cáncer gástrico (CG)se correlaciona con
REUNION BIBLIOGRAFICA Martes 26 de Noviembre de 2013 CENTRO: HOSPITAL NACIONAL DE CLINICAS Mendez Norberto, Médico. PUNTOS CLAVE CANCER GASTRICO La incidencia de cáncer gástrico (CG)se correlaciona con
Alrededor del 80% de las mujeres con cáncer de ovario recaerán en los 2 primeros años
 Alrededor del 80% de las mujeres con cáncer de ovario recaerán en los 2 primeros años PharmaMar organiza el VII Foro Cáncer de Ovario con oncólogos líderes para debatir sobre las principales novedades
Alrededor del 80% de las mujeres con cáncer de ovario recaerán en los 2 primeros años PharmaMar organiza el VII Foro Cáncer de Ovario con oncólogos líderes para debatir sobre las principales novedades
Experiencia de enfermería oncológica en la elaboración de una guía de administración de quimioterapia antineoplásica. Marta González Fernández-Conde
 Experiencia de enfermería oncológica en la elaboración de una guía de administración de quimioterapia antineoplásica Marta González Fernández-Conde Introducción El aumento de casos cáncer ha supuesto un
Experiencia de enfermería oncológica en la elaboración de una guía de administración de quimioterapia antineoplásica Marta González Fernández-Conde Introducción El aumento de casos cáncer ha supuesto un
EN CONTRA QUIMIOTERAPIA INTRAPERITONEAL. Dra María Quindós Varela. CHU de A Coruña
 EN CONTRA QUIMIOTERAPIA INTRAPERITONEAL Dra María Quindós Varela. CHU de A Coruña Coordinador Científico: Dr. Fernando Rivera Hospital Universitario Marqués de Valdecilla, Santander Organizado por: Fundación
EN CONTRA QUIMIOTERAPIA INTRAPERITONEAL Dra María Quindós Varela. CHU de A Coruña Coordinador Científico: Dr. Fernando Rivera Hospital Universitario Marqués de Valdecilla, Santander Organizado por: Fundación
FOLLETO DE INFORMACION AL PACIENTE. ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg
 FOLLETO INFORMACION AL PACIENTE ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg NANOPARTICULAS DE PACLITAXEL LIGADO A ALBÚMINA Leer esta Información para el paciente antes de empezar a recibir ABRAXANE
FOLLETO INFORMACION AL PACIENTE ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg NANOPARTICULAS DE PACLITAXEL LIGADO A ALBÚMINA Leer esta Información para el paciente antes de empezar a recibir ABRAXANE
FORMAS FARMACÉUTICAS Y CONCENTRACIONES
 NOMBRE DEL PRODUCTO YONDELIS Trabectedina para inyección (1 mg) FORMAS FARMACÉUTICAS Y CONCENTRACIONES Polvo para concentrado de solución para infusión. El producto farmacéutico YONDELIS se comercializa
NOMBRE DEL PRODUCTO YONDELIS Trabectedina para inyección (1 mg) FORMAS FARMACÉUTICAS Y CONCENTRACIONES Polvo para concentrado de solución para infusión. El producto farmacéutico YONDELIS se comercializa
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Yondelis 0,25 mg polvo para concentrado para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Yondelis 0,25 mg polvo para concentrado para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cáncer de pulmón de células no pequeñas no escamoso, avanzado o recurrente, primera línea de terapia en combinación con cisplatino y gemcitabina:
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
Prevención de la hemorragia posparto (misoprostol frente oxitocina)
 posparto (misoprostol frente oxitocina) PREGUNTA Es equivalente en eficacia y seguridad la utilización de misoprostol frente a la oxitocina para la prevención de la posparto? CONTEXTO Hemorragia posparto
posparto (misoprostol frente oxitocina) PREGUNTA Es equivalente en eficacia y seguridad la utilización de misoprostol frente a la oxitocina para la prevención de la posparto? CONTEXTO Hemorragia posparto
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva 20 mg/0,5 ml concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva 20 mg/0,5 ml concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
Niraparib en el tratamiento del cáncer de ovario Eficacia y seguridad relativas de niraparib y olaparib: comparaciones indirectas.
 Abril 2018 Niraparib en el tratamiento del cáncer de ovario Eficacia y seguridad relativas de niraparib y olaparib: comparaciones indirectas. Niraparib en el tratamiento del cáncer de ovario Eficacia y
Abril 2018 Niraparib en el tratamiento del cáncer de ovario Eficacia y seguridad relativas de niraparib y olaparib: comparaciones indirectas. Niraparib en el tratamiento del cáncer de ovario Eficacia y
Protocolo de uso Fuera de Ficha Técnica de ERBITAX (cetuximab + paclitaxel) en tumores de cabeza y cuello
 Protocolo de uso Fuera de Ficha Técnica de ERBITAX (cetuximab + paclitaxel) en tumores de cabeza y cuello Elaborado por: Servicios de Oncología Médica y Farmacia del Hospital Clínico Universitario Virgen
Protocolo de uso Fuera de Ficha Técnica de ERBITAX (cetuximab + paclitaxel) en tumores de cabeza y cuello Elaborado por: Servicios de Oncología Médica y Farmacia del Hospital Clínico Universitario Virgen
Effectiveness and safety of atomoxetine for ADHD in population between 6 and 19 years: a systematic review
 Anexo 4 Resultados de los estudios ATX versus placebo Revisiones sistemáticas: Estudio Características Nº y tipos de estudios Calidad metodológica de estudios Variable de resultado Síntesis de resultados
Anexo 4 Resultados de los estudios ATX versus placebo Revisiones sistemáticas: Estudio Características Nº y tipos de estudios Calidad metodológica de estudios Variable de resultado Síntesis de resultados
Precio adquisición: PVL+ IVA: 477,78 y 1797,96 Grupo Terapéutico: L01AX: Otros alcaloides de plantas y productos naturales
 TRABEDECTINA EN CÁNCER DE OVARIO Informe de la CFT, basado en el informe para la Guía Farmacoterapéutica de Hospitales de Andalucía HOSPITAL REINA SOFÍA 1.- Identificación del fármaco: Nombre Comercial:
TRABEDECTINA EN CÁNCER DE OVARIO Informe de la CFT, basado en el informe para la Guía Farmacoterapéutica de Hospitales de Andalucía HOSPITAL REINA SOFÍA 1.- Identificación del fármaco: Nombre Comercial:
DIRECCION DE ATENCIÓN Y EVALUACIÓN COMISIÓN DE EVALUACIÓN DE MEDICAMENTOS DE ALTO IMPACTO (CEMAI)
 Página 1 de 5 Introducción El mieloma múltiple (MM) es un tipo de cáncer que se produce por una degeneración maligna de las células plasmáticas, que se encuentran normalmente en la médula ósea. Representa
Página 1 de 5 Introducción El mieloma múltiple (MM) es un tipo de cáncer que se produce por una degeneración maligna de las células plasmáticas, que se encuentran normalmente en la médula ósea. Representa
TECNOLOGÍA EN SALUD DE INTERÉS Oxcarbazepina, lacosamida, vigabatrina, topiramato y levetiracetam 1. RESUMEN
 TECNOLOGÍA EN SALUD DE INTERÉS Oxcarbazepina, lacosamida, vigabatrina, topiramato y levetiracetam 1. RESUMEN Título del reporte: Efectividad y seguridad de oxcarbazepina, lacosamida, vigabatrina, topiramato
TECNOLOGÍA EN SALUD DE INTERÉS Oxcarbazepina, lacosamida, vigabatrina, topiramato y levetiracetam 1. RESUMEN Título del reporte: Efectividad y seguridad de oxcarbazepina, lacosamida, vigabatrina, topiramato
NOMBRE DEL MEDICAMENTO YONDELIS Trabectedina para inyección (1 mg)
 NOMBRE DEL MEDICAMENTO YONDELIS Trabectedina para inyección (1 mg) COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene 1 mg de trabectedina. 1 ml de solución reconstituida contiene 0,05 mg de trabectedina
NOMBRE DEL MEDICAMENTO YONDELIS Trabectedina para inyección (1 mg) COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene 1 mg de trabectedina. 1 ml de solución reconstituida contiene 0,05 mg de trabectedina
Un análisis bibliográfico (y pragmático) JM. López Vega Universidad de Cantabria
 Un análisis bibliográfico (y pragmático) del ensayo VELVET JM. López Vega Universidad de Cantabria Fundamentos del ensayo VELVET Ensayo HERNATA Andersson, J Clin Oncol 2011 TAXOTERE N = 143 VINORELBINA
Un análisis bibliográfico (y pragmático) del ensayo VELVET JM. López Vega Universidad de Cantabria Fundamentos del ensayo VELVET Ensayo HERNATA Andersson, J Clin Oncol 2011 TAXOTERE N = 143 VINORELBINA
PharmaMar anuncia la presentación de 15 estudios con Yondelis y Aplidin en el 46 encuentro anual de la Sociedad Americana de Oncología Clínica (ASCO)
 PharmaMar anuncia la presentación de 15 estudios con Yondelis y Aplidin en el 46 encuentro anual de la Sociedad Americana de Oncología Clínica (ASCO) Madrid, 9 de junio de 2010: PharmaMar SA (Grupo Zeltia,
PharmaMar anuncia la presentación de 15 estudios con Yondelis y Aplidin en el 46 encuentro anual de la Sociedad Americana de Oncología Clínica (ASCO) Madrid, 9 de junio de 2010: PharmaMar SA (Grupo Zeltia,
TECNOLOGÍA EN SALUD DE INTERÉS. Oxcarbazepina, lacosamida, vigabatrina, topiramato o levetiracetam. 1. RESUMEN
 TECNOLOGÍA EN SALUD DE INTERÉS Oxcarbazepina, lacosamida, vigabatrina, topiramato y levetiracetam 1. RESUMEN Título del reporte: Efectividad y seguridad de oxcarbazepina, lacosamida, vigabatrina, topiramato
TECNOLOGÍA EN SALUD DE INTERÉS Oxcarbazepina, lacosamida, vigabatrina, topiramato y levetiracetam 1. RESUMEN Título del reporte: Efectividad y seguridad de oxcarbazepina, lacosamida, vigabatrina, topiramato
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO DOCETAXEL KABI 80 mg/4 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO DOCETAXEL KABI 80 mg/4 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
EVALUACION Y ANALISIS DEL COMITÉ FARMACOTERAPÈUTICO PARA INCLUSION DE MEDICAMENTOS Al LISTADO OFICIAL
 MINISTERIO DE SALUD Anexo No.2 EVALUACION Y ANALISIS DEL COMITÉ FARMACOTERAPÈUTICO PARA INCLUSION DE MEDICAMENTOS Al LISTADO OFICIAL A. IDENTIFICACIÓN DEL FÁRMACO Denominación común internacional (DCI)
MINISTERIO DE SALUD Anexo No.2 EVALUACION Y ANALISIS DEL COMITÉ FARMACOTERAPÈUTICO PARA INCLUSION DE MEDICAMENTOS Al LISTADO OFICIAL A. IDENTIFICACIÓN DEL FÁRMACO Denominación común internacional (DCI)
Tratamiento antimicrobiano de la bacteriuria en mujeres embarazadas
 antimicrobiano de la bacteriuria en mujeres embarazadas PREGUNTA Se requiere antimicrobiano de la bacteriuria asintomática en mujeres embarazadas? CONTEXTO asintomática en mujeres embarazadas La bacteriuria
antimicrobiano de la bacteriuria en mujeres embarazadas PREGUNTA Se requiere antimicrobiano de la bacteriuria asintomática en mujeres embarazadas? CONTEXTO asintomática en mujeres embarazadas La bacteriuria
Revista Cubana de Hematología, Inmunología y Hemoterapia. 2017; 36 (Suplemento).
 Seguridad clínica del anticuerpo monoclonal CIMABIOR en pacientes con linfoma no hodgkiniano: revisión integrada de datos 1 García-Vega Y 1, Hernández-Casaña P 1, Saumell-Nápoles Y 1, Fernández-Águila
Seguridad clínica del anticuerpo monoclonal CIMABIOR en pacientes con linfoma no hodgkiniano: revisión integrada de datos 1 García-Vega Y 1, Hernández-Casaña P 1, Saumell-Nápoles Y 1, Fernández-Águila
Prospecto: información para el usuario. PARAPLATIN 450 mg/ 45 ml solución para perfusión Carboplatino
 Prospecto: información para el usuario PARAPLATIN 450 mg/ 45 ml solución para perfusión Carboplatino Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. Conserve este prospecto,
Prospecto: información para el usuario PARAPLATIN 450 mg/ 45 ml solución para perfusión Carboplatino Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. Conserve este prospecto,
Cada CÁPSULA contiene: Temozolomida 5 mg Excipiente c.b.p. 1 cápsula. Temozolomida 20 mg Excipiente c.b.p. 1 cápsula.
 Marca TEMODAL Forma Famacéutica y Formulación Presentación PRESENTACIONES: Cajas de cartón con un frasco de vidrio ámbar con 5, 10 o 20cápsulas de 5, 20, 100, 140, 180 o 250 mg. COMPOSICIÓN FORMA FARMACÉUTICA
Marca TEMODAL Forma Famacéutica y Formulación Presentación PRESENTACIONES: Cajas de cartón con un frasco de vidrio ámbar con 5, 10 o 20cápsulas de 5, 20, 100, 140, 180 o 250 mg. COMPOSICIÓN FORMA FARMACÉUTICA
La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos.
 Pág. 1 de 5 La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos. El objetivo es difundir información sobre la seguridad y eficacia de los medicamentos basados
Pág. 1 de 5 La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos. El objetivo es difundir información sobre la seguridad y eficacia de los medicamentos basados
CA TESTICULO SEMINOMA DR. JUAN CARLOS PERALTA
 CA TESTICULO SEMINOMA DR. JUAN CARLOS PERALTA El Cáncer de Testículo representa 1,5% de las neoplasias masculinas, 5% de los tumores urológicos FACTORES DE RIESGO: Criptorquidia. Síndrome de Klinefelter.
CA TESTICULO SEMINOMA DR. JUAN CARLOS PERALTA El Cáncer de Testículo representa 1,5% de las neoplasias masculinas, 5% de los tumores urológicos FACTORES DE RIESGO: Criptorquidia. Síndrome de Klinefelter.
TRABECTEDINA en cáncer de ovario Informe para la Guía Farmacoterapéutica de Hospitales de Andalucía Junio de 2010
 TRABECTEDINA en cáncer de ovario Informe para la Guía Farmacoterapéutica de Hospitales de Andalucía Junio de 2010 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Trabectedina Indicación clínica
TRABECTEDINA en cáncer de ovario Informe para la Guía Farmacoterapéutica de Hospitales de Andalucía Junio de 2010 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Trabectedina Indicación clínica
Recomendaciones del Estudio Genético de BRCA1 y BRCA2 en Cáncer de Ovario
 Recomendaciones del Estudio Genético de BRCA1 y BRCA2 en Cáncer de Ovario Consenso del Grupo Español de Investigación en Cáncer de Ovario (GEICO) y de la Sociedad Española de Oncología Médica (SEOM) Los
Recomendaciones del Estudio Genético de BRCA1 y BRCA2 en Cáncer de Ovario Consenso del Grupo Español de Investigación en Cáncer de Ovario (GEICO) y de la Sociedad Española de Oncología Médica (SEOM) Los
Indicaciones clínicas formalmente aprobadas y fecha de aprobación:
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
1. DENOMINACIÓN DEL ESQUEMA : CAPECITABINA IRINOTECAN. Carcinoma colorectal avanzado / metastásico (Ensayos clínicos en fase II.
 1. DENOMINACIÓN DEL ESQUEMA : CAPECITABINA IRINOTECAN 2. USO TERAPÉUTICO (1,2) Carcinoma colorectal avanzado / metastásico (Ensayos clínicos en fase II. 3. ESQUEMA (1,2) Dos esquemas : Esquema Medicamento
1. DENOMINACIÓN DEL ESQUEMA : CAPECITABINA IRINOTECAN 2. USO TERAPÉUTICO (1,2) Carcinoma colorectal avanzado / metastásico (Ensayos clínicos en fase II. 3. ESQUEMA (1,2) Dos esquemas : Esquema Medicamento
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Yondelis 0,25 mg polvo para concentrado para solución para perfusión. Yondelis 1 mg polvo para concentrado
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Yondelis 0,25 mg polvo para concentrado para solución para perfusión. Yondelis 1 mg polvo para concentrado
Medicamento con autorización anulada
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva Pharma 20 mg concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva Pharma 20 mg concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
Prepara el útero para el embarazo al promover cambios secretores en el endometrio.
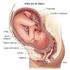 Fisiología Producen los estrógenos, promueven el crecimiento y la maduración de los órganos sexuales interno y externos, que producen los caracteres sexuales femeninos. Prepara el útero para el embarazo
Fisiología Producen los estrógenos, promueven el crecimiento y la maduración de los órganos sexuales interno y externos, que producen los caracteres sexuales femeninos. Prepara el útero para el embarazo
13º Congreso Argentino de Pediatría Social y Derechos del Niño y 8º Congreso Argentino de Lactancia Materna. Lactancia
 13º Congreso Argentino de Pediatría Social y Derechos del Niño y 8º Congreso Argentino de Lactancia Materna Cáncer de mama y Lactancia Cáncer de Mama Características Anatomopatológicas en Argentina 1 de
13º Congreso Argentino de Pediatría Social y Derechos del Niño y 8º Congreso Argentino de Lactancia Materna Cáncer de mama y Lactancia Cáncer de Mama Características Anatomopatológicas en Argentina 1 de
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva 20 mg /0,72 ml concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva 20 mg /0,72 ml concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
Comunicación Dirigida a Profesionales Sanitarios. Madrid, 13 de Mayo 2013
 Madrid, 13 de Mayo 2013 Comunicación Dirigida a Profesionales Sanitarios Información importante respecto a las restricciones de utilización de ranelato de estroncio (Protelos /Osseor ) tras el análisis
Madrid, 13 de Mayo 2013 Comunicación Dirigida a Profesionales Sanitarios Información importante respecto a las restricciones de utilización de ranelato de estroncio (Protelos /Osseor ) tras el análisis
Olaparib en cáncer de ovario. Andrés Redondo Hospital Universitario La Paz
 Olaparib en cáncer de ovario Andrés Redondo Hospital Universitario La Paz Olaparib en cáncer de ovario Agenda Introducción Olaparib en pacientes con mutación en BRCA Agente único en politratadas Mantenimiento
Olaparib en cáncer de ovario Andrés Redondo Hospital Universitario La Paz Olaparib en cáncer de ovario Agenda Introducción Olaparib en pacientes con mutación en BRCA Agente único en politratadas Mantenimiento
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO TAXOTERE 20 mg/0,5 ml concentrado y disolvente para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO TAXOTERE 20 mg/0,5 ml concentrado y disolvente para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y
ANÁLISIS IMPACTO SISTEMA NACIONAL DE SALUD
 ANÁLISIS IMPACTO PRESUPUESTARIO PARA EL SISTEMA NACIONAL DE SALUD Trabectedina (Yondelis ) en combinación con DLP en el tratamiento del cáncer de ovario recurrente semi-sensible a platino 1 QUÉ ES? Estudio
ANÁLISIS IMPACTO PRESUPUESTARIO PARA EL SISTEMA NACIONAL DE SALUD Trabectedina (Yondelis ) en combinación con DLP en el tratamiento del cáncer de ovario recurrente semi-sensible a platino 1 QUÉ ES? Estudio
Cada ml de concentrado contiene 20 mg de docetaxel (como trihidrato).
 1. NOMBRE DEL MEDICAMENTO TAXOTERE 80 mg/4 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de concentrado contiene 20 mg de docetaxel (como trihidrato). Un
1. NOMBRE DEL MEDICAMENTO TAXOTERE 80 mg/4 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de concentrado contiene 20 mg de docetaxel (como trihidrato). Un
Pacientes con cáncer de mama metastásico cuyos tumores sobreexpresen HER2
 1. DENOMINACIÓN DEL ESQUEMA: TRASTUZUMAB 2. INDICACIÓN Pacientes con cáncer de mama metastásico cuyos tumores sobreexpresen HER2 con 3 cruces (determinado por inmunohistoquímica) y que hayan recibido al
1. DENOMINACIÓN DEL ESQUEMA: TRASTUZUMAB 2. INDICACIÓN Pacientes con cáncer de mama metastásico cuyos tumores sobreexpresen HER2 con 3 cruces (determinado por inmunohistoquímica) y que hayan recibido al
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Winthrop20 mg/1 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Winthrop20 mg/1 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Fecha: 9 de abril de 2018 NOTA DE PRENSA
 www.lilly.com Fecha: 9 de abril de 2018 Eli Lilly and Company Lilly Corporate Center Indianapolis, Indiana 46285 U.S.A. NOTA DE PRENSA El ensayo en fase 3 REACH 2 con ramucirumab (Cyramza ) logra el objetivo
www.lilly.com Fecha: 9 de abril de 2018 Eli Lilly and Company Lilly Corporate Center Indianapolis, Indiana 46285 U.S.A. NOTA DE PRENSA El ensayo en fase 3 REACH 2 con ramucirumab (Cyramza ) logra el objetivo
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Winthrop20 mg/1 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Winthrop20 mg/1 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox
 TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
INFORME PARA LA CURMP SOBRE POSICIONAMIENTO TERAPÉUTICO DE NIVOLUMAB EN CÁNCER DE PULMÓN NO MICROCÍTICO METASTÁSICO EN SEGUNDA LÍNEA DE TRATAMIENTO
 Página 1 de 5 Introducción El Cáncer de Pulmón (CP) es el tumor que más muertes causa en los países desarrollados, representando un problema sanitario de primera magnitud. Globalmente, el CP representa
Página 1 de 5 Introducción El Cáncer de Pulmón (CP) es el tumor que más muertes causa en los países desarrollados, representando un problema sanitario de primera magnitud. Globalmente, el CP representa
DOCETAXEL KABI 120 mg/6 ml concentrado para solución para perfusión EFG
 1. NOMBRE DEL MEDICAMENTO DOCETAXEL KABI 120 mg/6 ml concentrado para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de concentrado contiene 20 mg de docetaxel anhidro. Un
1. NOMBRE DEL MEDICAMENTO DOCETAXEL KABI 120 mg/6 ml concentrado para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de concentrado contiene 20 mg de docetaxel anhidro. Un
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva 20 mg /0,72 ml concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva 20 mg /0,72 ml concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Accord 20 mg/1 ml concentrado para solución para perfusión EFG Docetaxel Accord 80 mg/4 ml concentrado
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Accord 20 mg/1 ml concentrado para solución para perfusión EFG Docetaxel Accord 80 mg/4 ml concentrado
Sistema de Protección Financiera para Diagnósticos y Tratamientos de Alto Costo. Ley Nº Ley Ricarte Soto.
 Subsecretaría de Salud Pública División de Planificación Sanitaria Departamento Evaluación de Tecnologías Sanitarias y Salud Basada en Evidencia INFORME DE EVALUACIÓN CIENTÍFICA BASADA EN LA EVIDENCIA
Subsecretaría de Salud Pública División de Planificación Sanitaria Departamento Evaluación de Tecnologías Sanitarias y Salud Basada en Evidencia INFORME DE EVALUACIÓN CIENTÍFICA BASADA EN LA EVIDENCIA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Hospira UK Limited 20 mg/1 ml concentrado para solución para perfusión Docetaxel Hospira UK Limited
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Hospira UK Limited 20 mg/1 ml concentrado para solución para perfusión Docetaxel Hospira UK Limited
YONDELIS TRABECTEDINA
 PROSPECTO YONDELIS TRABECTEDINA Polvo liofilizado para inyectables Industria Alemana Venta Bajo Receta Archivada Para infusión intravenosa COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene: Trabectedina
PROSPECTO YONDELIS TRABECTEDINA Polvo liofilizado para inyectables Industria Alemana Venta Bajo Receta Archivada Para infusión intravenosa COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene: Trabectedina
Prospecto: información para el paciente. Carnicor 200 mg/ml solución inyectable L-carnitina
 Prospecto: información para el paciente Carnicor 200 mg/ml solución inyectable L-carnitina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
Prospecto: información para el paciente Carnicor 200 mg/ml solución inyectable L-carnitina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
El CHIP recomienda la aprobación en la UE de Avastin, de Roche, contra el cáncer de ovario recidivante resistente al platino
 Comunicado de prensa Basilea, 27 de junio de 2014 El CHIP recomienda la aprobación en la UE de Avastin, de Roche, contra el cáncer de ovario recidivante resistente al platino Avastin es el primer biomedicamento
Comunicado de prensa Basilea, 27 de junio de 2014 El CHIP recomienda la aprobación en la UE de Avastin, de Roche, contra el cáncer de ovario recidivante resistente al platino Avastin es el primer biomedicamento
CARCINOMA DE OVARIO. ALERGIA A SALES DE PLATINO
 CARCINOMA DE OVARIO. ALERGIA A SALES DE PLATINO AUTOR PRINCIPAL MARÍA PILAR FELICES LOBERA HOSPITAL UNIVERSITARIO MIGUEL SERVET. ZARAGOZA SUPERVISIÓN ANA HERRERO CASO CLÍNICO Diagnóstico clínico Se trata
CARCINOMA DE OVARIO. ALERGIA A SALES DE PLATINO AUTOR PRINCIPAL MARÍA PILAR FELICES LOBERA HOSPITAL UNIVERSITARIO MIGUEL SERVET. ZARAGOZA SUPERVISIÓN ANA HERRERO CASO CLÍNICO Diagnóstico clínico Se trata
Análisis de impacto presupuestal de docetaxel para cáncer de próstata
 Análisis de impacto presupuestal de docetaxel para cáncer de próstata Grupo desarrollador Grupo de Investigación en Economía de la Salud, Universidad de Cartagena Fundación Salutia Autores Martín Romero
Análisis de impacto presupuestal de docetaxel para cáncer de próstata Grupo desarrollador Grupo de Investigación en Economía de la Salud, Universidad de Cartagena Fundación Salutia Autores Martín Romero
JAMA Abril-Mayo 2012
 JAMA Abril-Mayo 2012 Ting-I Wu Lai MIR Geriatría JAMA 11 deabril JAMA 11 de Abril La AHA avisa sobre la poca concienciación sobre la enfermedad arterial periférica, tanto por parte de la sociedad como
JAMA Abril-Mayo 2012 Ting-I Wu Lai MIR Geriatría JAMA 11 deabril JAMA 11 de Abril La AHA avisa sobre la poca concienciación sobre la enfermedad arterial periférica, tanto por parte de la sociedad como
