SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR Problemas a resolver con el programa FLASH
|
|
|
- Milagros Villanueva Caballero
- hace 8 años
- Vistas:
Transcripción
1 SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR Problemas a resolver con el programa FLASH 1. Resuelve los siguientes cálculos de equilibrio. En todos los casos se debe determinar la temperatura, presión y composición y proporción de las fases en equilibrio. FL1. Punto de rocío a 110ºC de una mezcla que contiene un 67.4% en moles de n-heptano y 32.6% de n-octano. FL2. Punto de rocío a 95ºC, de una mezcla que contiene un 78.9% en moles de benceno, un 15.6% de tolueno y un 5.5% de xileno. FL3. Punto de burbuja a 1 atm de una mezcla que contiene un 50% en moles de benceno, un 25% de tolueno y un 25% de xileno. FL4. Punto de de burbuja a 110ºC de una mezcla que contiene un 48.7% en moles de n-heptano y 51.3% de n-octano. FL5. Fases en equilibrio a partir de un líquido subenfriado que contiene 50% en moles de benceno, 25% en moles de tolueno y 25% en moles de o- xileno a 1 atm y 100ºC. Compara los resultados con los que se obtienen partiendo de un liquido saturado, de un vapor saturado y de un vapor sobrecalentado. FL6. Fases en equilibrio obtenidas a partir de un líquido subenfriado que contiene 50% benceno, 25% tolueno y 25% o-xileno (en moles) que se somete a destilación flash con vaporización del 32.5% en moles de la carga a 1 atm de presión. FL7. Composición del vapor en equilibrio a 1.2 atm con un líquido con la siguiente composición en moles: 95.2% de benceno, 0.7% de ciclohexano y 4.10% de tolueno. FL8. Composición del líquido en equilibrio a 1.5 atm con un vapor con la siguiente composición en moles: 48.9% de benceno, 32.1% de ciclohexano y 19% de acetato de etilo. 2. Obtén los datos de equilibrio líquido-vapor a 1 atm para los siguientes sistemas: - benceno-tolueno - benceno-ciclohexano - benceno-cloroformo - metanol-etanol - agua-etanol - agua-ciclohexano - agua-cloroformo
2 3. (FL9). Una mezcla equimolar de benceno y tolueno se evapora totalmente a una temperatura constante de 90ºC. Cuáles son las presiones de comienzo y finalización del proceso de vaporización? 4 (FL10). En el esquema que sigue, 150 kmol/h de un líquido saturado, L 1 a 758 kpa y cuya composición molar es : propano 10%, n-butano 40% y n-pentano 50%, entra en el ebullidor procedente de la etapa 1. Cuáles son las composiciones y cantidades de V B y B?. Cuál es la capacidad Q R del ebullidor?. B = 50 kmol/h 5 (FL11). Ha de separarse propileno de 1-buteno por destilación, con el fin de obtener un vapor destilado que contenga 90% en moles de propileno. Calcula la presión de operación de la columna, suponiendo que la temperatura de salida del condensador parcial es de 100ºF (la mínima alcanzable con el agua de refrigeración). Determina la composición del líquido de reflujo. 6 (FL12). Las corrientes que entran en la etapa F de una columna de destilación son las que se indican a continuación. Cuál es la temperatura de la etapa y las cantidades de las corrientes V F y L F si la presión de todas las corrientes es de 758 kpa?. L F-1 =100 kmol/h; V F+1 =196 kmol/h Fracciones molares Alimento V F+1 L F-1 Propano n-butano n-pentano (ELL1). Calcula la composición de las fases en equilibrio resultantes al poner en contacto las siguientes mezclas líquidas a 25ºC y 1 atm de presión: F : 25 kg de agua, 20 kg de acetona y 55 kg de ácido acético E2: kg de agua, kg de acetona, 9.52kg de ácido acético y kg de cloroformo.
3 8 (ELL2). Calcula la composición de las fases en equilibrio resultantes al poner en contacto las siguientes mezclas líquidas a 25ºC y 1 atm de presión: R1: fracciones molares: de ciclohexano, de benceno, de isooctano y de furfural. Caudal: 64.6 kmol/h. E3: de ciclohexano, de benceno, de isooctano y de furfural. Caudal kmol/h. 9 (ELL3). Calcula las composiciones de las dos fases en equilibrio que resultan al preparar una mezcla líquida a 25ºC y 1 atm que contiene 4.18% de ácido acético, 46.4% de agua y 49.42% de isopropil éter (los porcentajes son en peso). 10. (ELL4). El sistema agua-etanol-benceno presenta, a 1 atm, un azeótropo heterogéneo con la siguiente composición: agua, 7.4% en peso; etanol, 18.5%; benceno, 74.1% en peso. Para la citada mezcla, calcula la temperatura de burbuja y la temperatura de rocío. Comenta los valores obtenidos. 11. Obtén la curva binodal correspondiente a los siguientes sistemas a 25ºC y 1 atm: - ácido acético-agua-isopropil éter - agua-cloformo-acetona - agua-etanol-benceno 12. Calcula las temperaturas de burbuja y de rocío y determina, si existen, los azeótropos de los siguientes sistemas: - ácido acético-agua-isopropil éter - agua-cloformo-acetona - agua-etanol-benceno - etanol-1-propanol-2-propanol 13 (FL13). En el sistema de cabeza de una columna de destilación se obtiene un vapor, procedente del primer piso de la columna, con la siguiente composición (fracción molar): 0.10 de etano, 0.20 de propano y 0.70 de butano y se retira un 10% del mismo como destilado en fase vapor a 100ºC. Cuál es la presión en el tanque de reflujo? 14. (FL14). Un líquido en equilibrio procedente de una cámara de flash a 100ºF y 485 psia, con la siguiente composición (fracciones molares): H 2 = , CH 4 = , benceno= y tolueno=0.2276, entra como alimentación en un estabilizador para separar el H2 y el CH4 que quedan. La presión en el plato de alimentación del estabilizador es de 165 psia. Calcula el porcentaje de vaporización de la alimentación si la presión disminuye adiabáticamente desde 485 hasta 165 psia debido a la caída de presión en la válvula y en la conducción.
4 SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR Problemas a resolver con el programa EXTRACTOR 1 (EX1). Simula un extractor de 3 etapas en el que se separa una mezcla de agua (W), acetona (A), ácido acético (AC) y cloroformo (C) y en el que se introduce el disolvente C por la 1ª etapa, y por la última un alimento con la siguiente composición (fracción másica): X W = 0.25, X A = 0.20, X AC = 0.55, X C = 0. El caudal de alimento es de 100 kg/h y el de disolvente de 350 kg/h. Parámetros binarios para el modelo UNIQUAC (K) W A AH C W A AH C (EX3). La separación de benceno (B) de n-hexano (H) por destilación ordinaria presenta cierta dificultad. A presión atmosférica los puntos de ebullición se diferencian en 18.3ºC. Sin embargo, habida cuenta de la no idealidad de la fase líquida, la volatilidad relativa disminuye a un valor inferior a 1.15 para elevadas concentraciones de benceno. Un método alternativo de separación es la extracción líquido-líquido con una mezcla de dimetilformamida (DMF) y agua. El disolvente, a 20ºC, es mucho más selectivo para el benceno que para el n- hexano. Calcula, para dos composiciones del disolvente, las composiciones y flujos de las corrientes interetapas para una cascada de extracción líquidolíquido de cinco etapas de equilibrio, con T = 20ºC y P = 20 psia en todo el sistema, y con los siguientes caudales y composiciones: Alimento (20ºC, 20 psia): 300 lb-mol/ de H y 100 lb-mol/h de benceno Disolvente (20ºC, 20 psia): CASO A: 750 lb-mol/h de DMF y 250 lb-mol/h de agua; CASO B: 500 lb-mol/h de DMF y 500 lb-mol/h de agua Los datos experimentales del equilibrio entre fases para el sistema cuaternario fueron ajustados por la ecuación NRTL por Cohen y Renon (Can. J. Chem. Eng., 48, , 1970). Las constantes de los pares binarios resultantes son: Par binario, i, j τ ij = (g ij g jj )/(RT) τ ji = (g ji g ii )/(RT) α ji DMF, H Agua, H B, H Agua, DMF B, DMF B, agua (EX4). Se desea separar una mezcla de ciclohexano y ciclopentano por extracción líquido-líquido a 25ºC con metanol. Calcula las composiciones y los
5 flujos tanto de productos como de corrientes interetapas para las siguientes condiciones: Alimento: 700 lb-mol/h de ciclohexano y 300 lb-mol/h de ciclopentano Disolvente: 1000 lb-mol/h de metanol a) 1 etapa de equilibrio b) 2 etapas de equilibrio c) 5 etapas de equilibrio d) 10 etapas de equilibrio 4 (EX5). Se desea extraer la acetona de una mezcla que contiene 30% en peso de acetona y 70% en peso de acetato de etilo a 30ºC, usando agua pura como disolvente. El refinado final ha de contener 5% de acetona, en base libre de agua. Determina las relaciones mínima y máxima de caudales de disolvente y alimento y obtén el número de etapas de equilibrio necesarias para dos valores intermedios de dicha relación. Sugerencias: se puede utilizar el análisis de sensibilidad para determinar los caudales máximo y mínimo de disolvente. 5 (EX6). 100 kg/h de una mezcla ácido acético-cloroformo de composición 35% de ácido acético, se extraen con agua en una columna de extracción en contracorriente a 18ºC, para obtener un refinado que contenga menos del 3% en peso de ácido acético. Calcula el número de etapas necesarias si la cantidad de agua a emplear es de 25 kg/h. 6 (EX7). 200 kg/h de una mezcla ácido acético-cloroformo de composición 28% en peso de ácido acético se extraen con agua operando en una columna de extracción que consta de tres etapas de equilibrio. Determina la cantidad de agua a emplear como disolvente si se desea obtener un refinado que contenga un 10% de ácido acético. 7. (EX8). Se dispone de 1000 kg/h de una disolución acuosa de ácido benzoico de composición 30% en peso de ácido. Para separar el ácido benzoico se somete la mezcla a un proceso de extracción a 20ºC, empleando 1800 kg/h de benceno como disolvente. Si el sistema consta de 2 etapas de equilibrio, cuál es el porcentaje de ácido benzoico que ha pasado al refinado final? 8 (EX9). Se dispone de 1500 kg/h de una disolución acuosa de piridina de composición 50% en peso. Se pretende reducir su concentración por debajo del 3% en un proceso de extracción en contracorriente empleando clorobenceno como agente extractor. Calcula: a) La cantidad mínima de clorobenceno a emplear. b) El número de etapas teóricas si se emplean 1500 kg/h de clorobenceno c) La cantidad y composición del refinado y extracto que salen del sistema.
6 SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR Problemas a resolver con el programa de columnas 1 (COL1). Se desea diseñar una columna de destilación para separar la mezcla cuya composición se muestra en la tabla adjunta. La presión de operación es de 315 psia. El alimento entra a la columna vaporizado en un 66 % y la columna va equipada con un condensador parcial. Se desea conseguir el 98.4% del propano alimentado en el destilado, y el 98.2% del n-butano en el residuo. Calcula: a) El número de pisos teóricos necesarios para una columna trabajando a un reflujo 1.5 veces superior al mínimo b) El número mínimo de pisos c) La posición óptima del piso de alimentación d) La razón de reflujo mínima MOLES Metano 26 Etano 9 Propano 25 n-butano 17 n-pentano 11 n-hexano 12 2 (COL2). Para la columna del problema COL1, obtén los caudales y las composiciones de las corrientes que salen de cada piso. Comprueba el efecto sobre la composición y el caudal de los productos de una modificación de: a) el número de pisos b) la razón de reflujo c) la condición térmica del alimento Simula la columna especificando en reflujo inferior al mínimo y un número de pisos inferior al mínimo. Qué ocurre? 3 (COL3). Se dispone de 100 kmol/h de un alimento que contiene 45% en moles de CS 2 y 55% en moles de CI 4 C. Se desea obtener más del 95% de CS 2 en el destilado y más del 97% de CI 4 C en el residuo. Diseña la columna de destilación capaz de realizar dicha separación y obtén los perfiles de vapor, líquido y componente a lo largo de la columna. La presión de operación es 1 atm. El alimento se introduce en la columna como líquido saturado. 4 (COL4). Determina la separación que se puede alcanzar para la operación de absorción indicada más adelante, para las siguientes combinaciones de condiciones:
7 a) seis etapas de equilibrio y una presión de operación de 75 psia b) tres etapas de equilibrio y una presión de operación de 150 psia c) seis etapas de equilibrio y una presión de operación de 150 psia 5 (COL5). Para la operación de flash y stripping que se indica más abajo, determina los kg-mol/h de vapor de agua, si el sistema de stripping tiene diez etapas teóricas y opera a 2 atm. El alimento entra a 30ºF.
8 6 (COL6). Calcula las composiciones de los productos, las temperaturas de las etapas, los flujos y composiciones interetapas, el servicio del ebullidor y el del condensador para las siguientes especificaciones de destilación: Columna provista de 9 platos, caldera y condensador parcial. Alimento líquido en el punto de burbuja a 120 psia. Se introduce en el 5 0 piso (comenzando a contar desde el plato de cabeza). lb-mol/h C3 5 ic4 15 nc4 25 ic5 20 nc5 35 Destilado vapor lb-mol/h Reflujo: lb-mol/h P = 120 psia en toda la columna 7 (COL7). Calcula la composición de los productos, temperatura de las etapas, flujos y composiciones interetapas, servicio del ebullidor y servicio del condensador para las siguientes especificaciones de destilación, que representan un intento para la obtención de cuatro productos casi puros en una operación de destilación simple. El reflujo es un líquido saturado. La columna está provista de 28 platos, caldera y condensador total. Alimento: 25 psia, F. Se introduce en el piso 14 (comenzando a contar desde el plato de cabeza). lb-mol/h nc nc nc nc Destilado: lb-mol/h Razón de reflujo: 20 Extracción de producto en el piso 10 (comenzando a contar desde el plato de cabeza) lb-mol/h Extracción de producto en el piso 24 (comenzando a contar desde el plato de cabeza): lb-mol/h P en el condensador= 20 psia P en la caldera = 25 psia 8 (COL8). Calcula la composición de los productos, temperatura de las etapas, flujos y composiciones interetapas y servicio del ebullidor para el absorbedor con ebullición que se describe a continuación. La columna está provista de 25 platos y caldera.
9 Aceite absorbente: 6OºF, 230 psia, 40 lb-mol de nc9 Alimento. 230 psia, F. Se introduce en el piso 9 (comenzando a contar desde el plato de cabeza): lb-mol/h C1 46 C2 42 C3 66 ic4 13 nc4 49 ic5 11 nc5 20 nc6 24 nc9 148 Producto de cabeza: 103 lb-mol/h Ebullidor interetapas: piso 13 (comenzando a contar desde el plato de cabeza): 10 6 Btu/h P = 230 psia en toda la torre 9 (COL9). Para reducir el contenido en dióxido de azufre de una corriente gaseosa se utiliza un absorbedor con 4 etapas. El gas a limpiar entra al fondo del absorbedor a 40 C y 1 bar con un caudal de kmol/h y composición expresada como porcentaje en volumen de 6.6% en C0 2, 0.045% en S0 2 y el resto nitrógeno. El líquido absorbente está formado por una suspensión de carbonato cálcico en agua (19 g de carbonato por kg de agua) a 20 C que se introducirá por la parte superior del absorbedor. Determina el caudal de suspensión de carbonato necesaria para que la concentración de S0 2 en el gas limpio de salida expresada como porcentaje en volumen sea inferior a %. 10 (COL10). Se desea eliminar el contenido en cloruro de hidrógeno de una corriente de aire que contiene 36.3 kmol/h de nitrógeno, 9.1 de oxígeno y 13.6 de cloruro de hidrógeno a 38 C y 3.45 bar. Para ello se dispone de una columna de absorción de 20 etapas que opera a 3.45 bar. El absorbente utilizado es una corriente de agua de kmol/h a 38 C (algo impurificada con 0.45 kmol/h de HCI) que entra a la parte superior de la columna. Obtén la composición y caudal de las corrientes obtenidas. 11 (COL11). Se dispone de una corriente líquida a 60 C y 4 bares compuesta por 1743 kmol/h de agua que lleva en disolución 2 kmol/h de sulfuro de hidrógeno y 3.26 kmol/h de amoniaco. Para separar el sulfuro de hidrogeno y el amoníaco de dicha corriente se lleva a una torre de destilación de 20 etapas. El alimento entra a la torre en la etapa 4. La presión en lo alto de la columna es de 1 bar y la caída de presión a lo largo de la columna es de 0.17 bares.
10 Para mejorar la eficacia de la columna se extrae una corriente lateral líquida de la etapa justo superior a la entrada de alimento (etapa 3), se enfría y se lleva a lo alto de la torre. Esto conduce a que la salida de gas por lo alto de la columna sea de 7 kmol/h. Determina la composición de esta corriente gaseosa si al calderín de la columna de rectificación se está aportando un caudal de energía de MJ/h. COL12. Para llevar a cabo la obtención de acetato de etilo por esterificación de etanol y ácido acético se dispone de una columna de rectificación de 20 etapas donde se va a llevar a cabo la reacción y separación de componentes. La columna operará con una razón de reflujo (reciclado/destilado) de 4 y el calderín aportará 8000 MJ/h de energía. Las eficiencias de las etapas superior e inferior son de 0.6. La columna opera a una presión de bares y la caída de presión a lo largo de la columna es despreciable. El etanol a una temperatura de 70 C y 1.2 bar con un caudal de 50 kmol/h (de los que solo 43 son de etanol y los otro 7 de agua) entra a la columna en la etapa 13. El acético, a 70 C y 1.2 bar con un caudal de 25 kmol/h lo hace en la etapa 6. Supón que la reacción se lleva a cabo entre las etapas 4 y 18 y que el volumen de reacción de líquido retenido en los platos de la columna es de 20 litros. La cinética de la velocidad de esterificación viene dada por una reacción de orden cero en el que el factor de frecuencia A es de 2.9E+4 mol/(min L) y la energía de activación E es 7150 cal/mol. Para la velocidad de saponificación (de sentido inverso y que se da simultáneamente) A vale 7.38e+3 y E 7150 Determina la composición y caudal de las corrientes de salida de la columna. 13 (COL 13). Simula la siguiente columna de rectificación. 16 etapas, condensador mixto (etapa 1) y caldera (etapa 16) Presión en el condensador = 238 psia; presión en la caldera = 243 psia Alimento en el piso 6: 170 F, 300 psia, Composición (lbmol/h): etano = 2.5, propano = 14.0, n-butano = 19.0, n-pentano = 5.0, n-hexano = 0.5. Alimento en el piso 9: 230 F, 275 psia, Composición (lbmol/h): etano = 0.5, propano = 6.0, n-butano = 18.0, n-pentano = 30.0, n-hexano = 4.5. Condensador mixto: 15 lbmol/h de destilado vapor y 5 lbmol/h de destilado liquido. Enfriador interetapas en la etapa 3. Se eliminan Btu/h Extracción de corriente liquida lateral en el piso 3 de 3 lbmol/h Extracción de corriente vapor lateral en el piso 13 de 37 lbmol/h
11 SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR Problemas a resolver con la base de datos de Chemcad 1. Selecciona un compuesto cualquiera de la base de batos de ChemCAD y visualiza sus propiedades mediante los siguientes comandos: Comp/Databank/View-Edit Comp/Databank/BIPs Comp/Databank/UNIFAC BIPs Reports Plot Properties 2. Introduce un componente nuevo mediante el comando Comp/Databank/New comp. Cambia e introduce datos para dicho componente. Elimínalo de la lista de componentes. 3. Modifica los datos existentes para un componente de la base de datos, mediante las opciones de: 1. Copiarlo 2. Cambiar los datos 3. Salir y editarlo 4. borrarlo 4. Obtén los parámetros binarios del modelo UNIQUAC para el cálculo del equilibrio líquido-líquido de un sistema ternario o cuaternario por regresión de los datos experimentales de equilibrio. 5. Obtén los parámetros binarios del modelo NRTL para el cálculo del equilibrio líquido-vapor de un sistema binario por regresión de los datos experimentales de equilibrio. 6 (DAT4). Propón una configuración para una columna de rectificación capaz de separar la siguiente mezcla, cuya composición se da en forma de curva de destilación. Se desea obtener como destilado una fracción de punto de ebullición inferior a 180ºF. Como agente de calefacción se utiliza vapor directo. La columna ha de operar a 5 atm. Componente % volumen Agua Metano 0.1 Etano 0.15 Propano 0.9 Iso-butano 0.4 n-butano 1.6 iso-pentano 1.2 n-pentano 1.7 resto: representado por su curva de destilación
12 Densidad específica (grados Api): 31.4 % destilado T(ºF) % volumen densidad específica (grados Api) Los pseudocomponentes a definir en cada fracción son: Intervalo de T Nº de pseudocomponentes ºF ºF ºF ºF 5 Como vapor de calefacción se utiliza vapor saturado a la presión de operación de la columna.
13 SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR Problemas correspondientes a procesos industriales ABS1. PROCESO DE ABSORCIÓN-DESORCIÓN DE H 2 S (AGENTE DE ABSORCIÓN: AGUA) Se dispone de una corriente de aire que contiene un 5% en peso de H 2 S, a 150ºC y 1 atm, y se desea separar, por absorción con agua, en una corriente de aire, prácticamente exento de H 2 S, y en otra de H 2 S, con menos del 2% de agua. Para ello se utilizarán dos torres de absorción, con 10 pisos cada una: en la primera columna, el H 2 S es eliminado por absorción con agua, y en la segunda se desorbe. La corriente de agua fría procedente de la primera columna, antes de ser introducida en la segunda columna, intercambia calor con el agua caliente procedente de la segunda columna, que, a su vez, se retorna a la primera para ser utilizada como absorbente. Calcula los caudales y las condiciones de operación para tratar 100 kg/h de alimento. ABS2. PROCESO DE ABSORCIÓN-DESORCIÓN DE H 2 S (AGENTE DE ABSORCIÓN: MONOETANOLAMINA) Se dispone de una corriente de aire que contiene un 5% en peso de H 2 S, a 150ºC y 1 atm, y se desea separar, por absorción con monoetanolamina (MEA), en una corriente de aire, prácticamente exento de H 2 S, y en otra de H 2 S, con menos del 2% de MEA. Para ello se utilizarán dos torres de absorción, con 10 pisos cada una: en la primera columna, el H 2 S es eliminado por absorción con MEA y en la segunda se desorbe. La corriente de MEA fría procedente de la primera columna, antes de ser introducida en la segunda columna, intercambia calor con la MEA caliente procedente de la segunda columna, que, a su vez, se retorna a la primera para ser utilizada como absorbente. Calcula los caudales y las condiciones de operación para tratar 100 kg/h de alimento.
14 EST PLANTA ESTABILIZADORA DE CONDENSADO Simula la siguiente operación para la estabilización de una corriente de condensado (1) procedente de otra sección de la planta: La corriente 1 se encuentra a 75ºF y 200 psia y su composición es la siguiente: Componente Caudal (lbmol/h) N CH C 2 H C 3 H i-c 4 H n-c 4 H i-c 5 H n-c 5 H n-c 6 H Dicha corriente 1 se enfría en el intercambiador de calor 1, y en el intercambiador de calor 2 se enfría todavía más, hasta conseguir una temperatura tal que se obtenga una mezcla parcialmente vaporizada apropiada para el funcionamiento de la planta. Se estima que la pérdida de presión en cada intercambiador es de 5 psia. La condición térmica de la corriente 3 debe ser tal que en el separador de fases 3 se genere un vapor cuya temperatura de rocío a cualquier presión sea igual o menor que 25ºF, ya que va a actuar como fluido de refrigeración en el intercambiador 1, dando como producto la corriente 5. El líquido procedente de la cámara flash (corriente 6) se expande hasta 125 psia en la válvula 4, para dar la corriente 7, que se alimenta a una columna de
15 destilación, de la que se desea extraer un producto de cola, que es el condensado estabilizado deseado, que no debe contener más de un 1% de propano. Otros datos de interés: El intercambiador de calor 2 funciona con propano como refrigerante, que proporciona un enfriamiento isotermo a -20ºC. Se dispone de vapor a 150 psia. El estabilizador usa pisos de válvulas. La presión de salida de la válvula 4 es de 125 psia. En la columna 5: - Presión de cabeza= 125 psia - Pérdida de presión en la columna = 5 psia - Número de pisos = 12 - No hay condensador - Se desea 30 lbmol/h de producto de colas - El residuo ha de contener menos de 1% de propano.
16 ETANOL. OBTENCIÓN DE ETANOL PURO POR DESTILACIÓN AZEOTRÓPICA HETEROGÉNEA El agua y el etanol forman un azeótropo binario mínimo que contiene 95.6% en peso de alcohol, y que hierve a 78.17ºC (a 101 kpa). Por consiguiente, es imposible obtener etanol absoluto (T eb = 78.40ºC) por destilación ordinaria. La adición de ciertos disolventes, como el benceno, a la mezcla alcohol-agua, da lugar a un heteroazeótropo ternario que tiene temperatura de ebullición mínima, cuyas composiciones en peso son 18.5% de alcohol, 74.1% de benceno y 7.4% de agua. Al condensar, el heteroazeótropo ternario se separa en dos fases líquidas: una capa inferior de 14.5% de alcohol, 84.5% de benceno y 1% de agua, y una capa superior de 53% de alcohol, 11% de benceno y 36% de agua, estando todas las composiciones expresadas en peso. En una operación de destilación azeotrópica heterogénea de etanol, la capa rica en benceno se devuelve a la columna de destilación como reflujo. La otra capa se trata posteriormente por destilación para recuperar y recircular el alcohol y el benceno. El alcohol absoluto, que tiene una temperatura de ebullición superior a la del azeótropo, se separa por el fondo de la columna. En la siguiente figura se representa esquemáticamente el proceso descrito: Calcula los caudales y las condiciones de operación para tratar 100 kg/h de alimento.
17 ConcAcH COMPARACIÓN DE TRES PROCESOS PARA CONCENTRAR ÁCIDO ACÉTICO Se desea comparar la eficacia de tres procesos para concentrar una disolución acuosa de ácido acético, a 20ºC, desde un 25.6% hasta un 99.5%. Las tres alternativas son: a) destilación azeotrópica con acetato de isopropilo. El vapor de cabeza de esta columna se ha de condensar y se recircula, al primer piso de la columna, la fase orgánica obtenida. El ácido acético se obtiene como residuo de esta columna. b) extracción continua en contracorriente con metilisobutilcetona, seguida de destilación del extracto a presión atmosférica (el disolvente recuperado ha de tener un máximo del 0.001% de ácido). El refinado obtenido ha de estar prácticamente exento de ácido acético. En la columna de rectificación se obtiene como destilado el disolvente recuperado, que se recircula a la columna de extracción y como residuo el ácido acético concentrado. c) Mismo proceso que b), pero con isopropil éter como disolvente. La columna de destilación disponible está provista de 35 pisos (34 más la caldera). La columna de extracción está provista de un relleno cuya altura total puede considerarse equivalente a 15 etapas teóricas.
Curso 2008/09 SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR. Problemas a resolver con el programa FLASH
 Curso 2008/09 SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR Problemas a resolver con el programa FLASH 1. Resuelve los siguientes cálculos de equilibrio. En todos los casos se debe determinar
Curso 2008/09 SIMULACIÓN Y DISEÑO DE PROCESOS INDUSTRIALES POR ORDENADOR Problemas a resolver con el programa FLASH 1. Resuelve los siguientes cálculos de equilibrio. En todos los casos se debe determinar
Destilación. Producto 1 más volátil que Producto 2 (P 0 1 > P0 2 ) Figura 1
 Destilación La destilación es una técnica que nos permite separar mezclas, comúnmente líquidas, de sustancias que tienen distintos puntos de ebullición. Cuanto mayor sea la diferencia entre los puntos
Destilación La destilación es una técnica que nos permite separar mezclas, comúnmente líquidas, de sustancias que tienen distintos puntos de ebullición. Cuanto mayor sea la diferencia entre los puntos
Deshidratación de gas natural con glicoles. Prof. Alexis Bouza Enero-Marzo 2009
 Deshidratación de gas natural con glicoles El gas natural es secado por lavado en contracorriente t con un solvente que tiene una fuerte afinidad por el agua. El solvente es usualmente un glicol. l El
Deshidratación de gas natural con glicoles El gas natural es secado por lavado en contracorriente t con un solvente que tiene una fuerte afinidad por el agua. El solvente es usualmente un glicol. l El
LÍNEAS DEL DIAGRAMA DE MOLLIER
 DIAGRAMA DE MOLLIER El refrigerante cambia de estado a lo largo del ciclo frigorífico como hemos visto en el capítulo anterior. Representaremos sobre el diagrama de p-h las distintas transformaciones que
DIAGRAMA DE MOLLIER El refrigerante cambia de estado a lo largo del ciclo frigorífico como hemos visto en el capítulo anterior. Representaremos sobre el diagrama de p-h las distintas transformaciones que
RECTIFICACIÓN DE MEZCLAS BINARIAS EN COLUMNAS DE PLATOS
 Prácticas docentes en la COD: 10-71 RECTIFICACIÓN DE MEZCLAS BINARIAS EN COLUMNAS DE PLATOS INTRODUCCIÓN Las operaciones básicas que se llevan a cabo en la industria química, implican en la mayoría de
Prácticas docentes en la COD: 10-71 RECTIFICACIÓN DE MEZCLAS BINARIAS EN COLUMNAS DE PLATOS INTRODUCCIÓN Las operaciones básicas que se llevan a cabo en la industria química, implican en la mayoría de
Capítulo I Fundamentos de procesos de destilación
 1.1.Introducción Capítulo I Fundamentos de procesos de destilación La destilación es el método de separación de sustancias químicas puras, más antiguo e importante que se conoce. La época más activa de
1.1.Introducción Capítulo I Fundamentos de procesos de destilación La destilación es el método de separación de sustancias químicas puras, más antiguo e importante que se conoce. La época más activa de
DESTILACIÓN DE UNA MEZCLA DE ETANOL-AGUA
 UNIVERSIDAD AUTÓNOMA DE CHIHUAHUA Facultad de Ciencias Químicas Operaciones Unitarias II Práctica de Laboratorio DESTILACIÓN DE UNA MEZCLA DE ETANOL-AGUA Profesor.- Dr. Iván Salmerón Integrantes: Samantha
UNIVERSIDAD AUTÓNOMA DE CHIHUAHUA Facultad de Ciencias Químicas Operaciones Unitarias II Práctica de Laboratorio DESTILACIÓN DE UNA MEZCLA DE ETANOL-AGUA Profesor.- Dr. Iván Salmerón Integrantes: Samantha
CALCULOS EN DESTILACION CONTINUA PARA SISTEMAS BINARIOS UTILIZANDO HOJA DE CALCULO EXCEL
 CALCULOS EN DESTILACION CONTINUA PARA SISTEMAS BINARIOS UTILIZANDO HOJA DE CALCULO EXCEL M. Otiniano. Departamento de Operaciones Unitarias. Facultad de Química e Ingeniería Química. Universidad Nacional
CALCULOS EN DESTILACION CONTINUA PARA SISTEMAS BINARIOS UTILIZANDO HOJA DE CALCULO EXCEL M. Otiniano. Departamento de Operaciones Unitarias. Facultad de Química e Ingeniería Química. Universidad Nacional
LABORATORIO DE QUÍMICA ANALÍTICA E INSTRUMENTAL 502503. GUÍA No 2.3- METODOS DE SEPARACIÓN POR DESTILACIÓN
 LABORATORIO DE QUÍMICA ANALÍTICA E INSTRUMENTAL 502503 GUÍA No 2.3- METODOS DE SEPARACIÓN POR DESTILACIÓN I. EL PROBLEMA Dos líquidos completamente miscibles se pueden separar por métodos físicos llamados
LABORATORIO DE QUÍMICA ANALÍTICA E INSTRUMENTAL 502503 GUÍA No 2.3- METODOS DE SEPARACIÓN POR DESTILACIÓN I. EL PROBLEMA Dos líquidos completamente miscibles se pueden separar por métodos físicos llamados
Procesos industriales
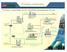 Procesos industriales en los complejos procesadores de gas Gas ácido Azufre Plantas de azufre proceso Claus y Superclaus Gas seco Gas seco libre de Nitrógeno Gas amargo de PEP Endulzadoras de gas Eliminación
Procesos industriales en los complejos procesadores de gas Gas ácido Azufre Plantas de azufre proceso Claus y Superclaus Gas seco Gas seco libre de Nitrógeno Gas amargo de PEP Endulzadoras de gas Eliminación
ANÁLISIS DE EXERGÍA EN PROCESOS DE LICUEFACCIÓN DE GAS NATURAL PARA POTENCIALES DESARROLLOS EN VENEZUELA
 PDV Caribe ANÁLISIS DE EXERGÍA EN PROCESOS DE LICUEFACCIÓN DE GAS NATURAL PARA POTENCIALES DESARROLLOS EN VENEZUELA Ramiro Guerrero Navia*, Marco González De León PDV Caribe*, Universidad Simón Bolívar
PDV Caribe ANÁLISIS DE EXERGÍA EN PROCESOS DE LICUEFACCIÓN DE GAS NATURAL PARA POTENCIALES DESARROLLOS EN VENEZUELA Ramiro Guerrero Navia*, Marco González De León PDV Caribe*, Universidad Simón Bolívar
4. METODOLOGÍA. 4.1 Selección de la mezcla
 4. METODOLOGÍA 4.1 Selección de la mezcla Para iniciar con las simulaciones, primero se tuvo que seleccionar la mezcla binaria a utilizar. Se hicieron pruebas con los siete primeros hidrocarburos (metano-heptano)
4. METODOLOGÍA 4.1 Selección de la mezcla Para iniciar con las simulaciones, primero se tuvo que seleccionar la mezcla binaria a utilizar. Se hicieron pruebas con los siete primeros hidrocarburos (metano-heptano)
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA
 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA PROGRAMA DE INGENIERIA DE ALIMENTOS 211612 TRANSFERENCIA DE MASA ACTIVIDAD 11 RECONOCIMIENTO UNIDAD 3 BOGOTA D.C. Extracción líquido - líquido La extracción líquido-líquido,
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA PROGRAMA DE INGENIERIA DE ALIMENTOS 211612 TRANSFERENCIA DE MASA ACTIVIDAD 11 RECONOCIMIENTO UNIDAD 3 BOGOTA D.C. Extracción líquido - líquido La extracción líquido-líquido,
0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 Entropía s [KJ/Kg.ºK]
![0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 Entropía s [KJ/Kg.ºK] 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 Entropía s [KJ/Kg.ºK]](/thumbs/25/5925823.jpg) UNIVERSIDAD NACIONAL DE TUCUMÁN Facultad de Ciencias Exactas y Tecnología CENTRALES ELÉCTRICAS TRABAJO PRÁCTICO Nº 3 CENTRALES TÉRMICAS DE VAPOR CICLO DE RANKINE ALUMNO: AÑO 2015 INTRODUCCIÓN El Ciclo
UNIVERSIDAD NACIONAL DE TUCUMÁN Facultad de Ciencias Exactas y Tecnología CENTRALES ELÉCTRICAS TRABAJO PRÁCTICO Nº 3 CENTRALES TÉRMICAS DE VAPOR CICLO DE RANKINE ALUMNO: AÑO 2015 INTRODUCCIÓN El Ciclo
ESTUDIO DEL CICLO DE RANKINE
 ESTUDIO DEL CICLO DE RANKINE 1. INTRODUCCIÓN El ciclo de Rankine es el ciclo ideal que sirve de base al funcionamiento de las centrales térmicas con turbinas de vapor, las cuales producen actualmente la
ESTUDIO DEL CICLO DE RANKINE 1. INTRODUCCIÓN El ciclo de Rankine es el ciclo ideal que sirve de base al funcionamiento de las centrales térmicas con turbinas de vapor, las cuales producen actualmente la
Condensación y ebullición ING Roxsana Romero Ariza Junio 2013
 Condensación y ebullición ING Roxsana Romero Ariza Junio 2013 EBULLICIÓN La transferencia de calor a un líquido en ebullición es muy importante en la evaporación y destilación, así como en otros tipos
Condensación y ebullición ING Roxsana Romero Ariza Junio 2013 EBULLICIÓN La transferencia de calor a un líquido en ebullición es muy importante en la evaporación y destilación, así como en otros tipos
21. PLANTA DE ENFRIAMIENTO DE UN GAS
 21. PLANTA DE ENFRIAMIENTO DE UN GAS 1. OBJETIVOS 1.1. Simular, en estado estacionario, una versión simplificada de una planta de enfriamiento de un mezcla de hidrocarburos gaseosa 1.2. Ajustar la temperatura
21. PLANTA DE ENFRIAMIENTO DE UN GAS 1. OBJETIVOS 1.1. Simular, en estado estacionario, una versión simplificada de una planta de enfriamiento de un mezcla de hidrocarburos gaseosa 1.2. Ajustar la temperatura
PROBLEMAS. Segundo Principio. Problema 1
 PROBLEMAS Segundo Principio Problema 1 La figura muestra un sistema que capta radiación solar y la utiliza para producir electricidad mediante un ciclo de potencia. El colector solar recibe 0,315 kw de
PROBLEMAS Segundo Principio Problema 1 La figura muestra un sistema que capta radiación solar y la utiliza para producir electricidad mediante un ciclo de potencia. El colector solar recibe 0,315 kw de
PRÁCTICA DE LABORATORIO DE QUÍMICA DESTILACIÓN ALCOHÓLICA DE UNA BEBIDA COMERCIAL
 PRÁCTICA DE LABORATORIO DE QUÍMICA DESTILACIÓN ALCOHÓLICA DE UNA BEBIDA COMERCIAL 1. OBJETIVOS. Determinar el contenido alcohólico en una bebida comercial. Determinar la temperatura a la cual se separa
PRÁCTICA DE LABORATORIO DE QUÍMICA DESTILACIÓN ALCOHÓLICA DE UNA BEBIDA COMERCIAL 1. OBJETIVOS. Determinar el contenido alcohólico en una bebida comercial. Determinar la temperatura a la cual se separa
SECADO DE EMBUTIDOS. es una fuente propicia para el desarrollo de bacterias y mohos.
 SECADO DE EMBUTIDOS Imtech DryGenic ayuda a los fabricantes con procesos de secado de embutidos a obtener embutidos de mayor calidad, en un entorno libre de bacterias, limpio y a una temperatura y humedad
SECADO DE EMBUTIDOS Imtech DryGenic ayuda a los fabricantes con procesos de secado de embutidos a obtener embutidos de mayor calidad, en un entorno libre de bacterias, limpio y a una temperatura y humedad
D E S C R I P C I O N
 SISTEMA DE REFRIGERACIÓN CON CO 2 COMO FLUIDO SECUNDARIO D E S C R I P C I O N OBJETO DE LA INVENCIÓN La presente invención se refiere a un sistema de refrigeración con CO 2 como fluido secundario que
SISTEMA DE REFRIGERACIÓN CON CO 2 COMO FLUIDO SECUNDARIO D E S C R I P C I O N OBJETO DE LA INVENCIÓN La presente invención se refiere a un sistema de refrigeración con CO 2 como fluido secundario que
Extracción sólido-líquido
 Extracción sólido-líquido Objetivos de la práctica! Determinar la concentración de saturación del soluto en el disolvente en un sistema ternario arena-azúcar-agua, estableciendo la zona operativa del diagrama
Extracción sólido-líquido Objetivos de la práctica! Determinar la concentración de saturación del soluto en el disolvente en un sistema ternario arena-azúcar-agua, estableciendo la zona operativa del diagrama
Los gases combustibles pueden servir para accionar motores diesel, para producir electricidad, o para mover vehículos.
 PIRÓLISIS 1. Definición La pirólisis se define como un proceso termoquímico mediante el cual el material orgánico de los subproductos sólidos se descompone por la acción del calor, en una atmósfera deficiente
PIRÓLISIS 1. Definición La pirólisis se define como un proceso termoquímico mediante el cual el material orgánico de los subproductos sólidos se descompone por la acción del calor, en una atmósfera deficiente
REFRIGERACIÓN POR ABSORCIÓN
 REFRIGERACIÓN POR ABSORCIÓN Estos equipos utilizan como base el principio de higroscópico de algunas sales como el Bromuro de litio para generar un vacío en una cavidad que ocasiona una disminución brusca
REFRIGERACIÓN POR ABSORCIÓN Estos equipos utilizan como base el principio de higroscópico de algunas sales como el Bromuro de litio para generar un vacío en una cavidad que ocasiona una disminución brusca
ESTEQUIOMETRÍA DE REACCIONES QUÍMICAS
 ESTEQUIOMETRÍA DE REACCIONES QUÍMICAS La ecuación estequimétrica de una reacción química impone restricciones en las cantidades relativas de reactivos y productos en las corrientes de entrada y salida
ESTEQUIOMETRÍA DE REACCIONES QUÍMICAS La ecuación estequimétrica de una reacción química impone restricciones en las cantidades relativas de reactivos y productos en las corrientes de entrada y salida
QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO
 QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
DESTILACION CONTINUA
 9/0/200 Universidad de Los Andes acultad de Ingeniería Escuela de Ingeniería Química Dpto. de Operaciones Unitarias Proectos DESTILACION CONTINUA Prof. Yoana Castillo oanacastillo@ula.ve Web:http://webdelprofesor.ula.ve/ingenieria/oanacastillo/
9/0/200 Universidad de Los Andes acultad de Ingeniería Escuela de Ingeniería Química Dpto. de Operaciones Unitarias Proectos DESTILACION CONTINUA Prof. Yoana Castillo oanacastillo@ula.ve Web:http://webdelprofesor.ula.ve/ingenieria/oanacastillo/
UNIVERSIDAD AUTONOMA DE CHIHUAHUA
 UNIVERSIDAD AUTONOMA DE CHIHUAHUA FACULTAD DE CIENCIAS QUIMICAS OPERACIONES UNITARIAS ll Ensayo Integrantes: Areli Prieto Velo 232644 Juan Carlos Calderón Villa 232654 Víctor Gutiérrez 245369 Fernando
UNIVERSIDAD AUTONOMA DE CHIHUAHUA FACULTAD DE CIENCIAS QUIMICAS OPERACIONES UNITARIAS ll Ensayo Integrantes: Areli Prieto Velo 232644 Juan Carlos Calderón Villa 232654 Víctor Gutiérrez 245369 Fernando
INGENIERÍA QUÍMICA Problemas propuestos Pág. 1 BALANCES DE ENERGÍA
 Problemas propuestos Pág. 1 BALANCES DE ENERGÍA Problema nº 31) [04-03] Considérese una turbina de vapor que funciona con vapor de agua que incide sobre la misma con una velocidad de 60 m/s, a una presión
Problemas propuestos Pág. 1 BALANCES DE ENERGÍA Problema nº 31) [04-03] Considérese una turbina de vapor que funciona con vapor de agua que incide sobre la misma con una velocidad de 60 m/s, a una presión
CALENTAMIENTO DE AGUA CALIENTE SANITARIA
 CALENTAMIENTO DE AGUA CALIENTE SANITARIA De todas las formas de captación térmica de la energía solar, las que han adquirido un desarrollo comercial en España han sido los sistemas para su utilización
CALENTAMIENTO DE AGUA CALIENTE SANITARIA De todas las formas de captación térmica de la energía solar, las que han adquirido un desarrollo comercial en España han sido los sistemas para su utilización
FÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación GAS LÍQUIDO SÓLIDO
 Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
ESTADOS DE AGREGACIÓN DE LA MATERIA
 ESADOS DE AGREGACIÓN DE LA MAERIA. Propiedades generales de la materia La materia es todo aquello que tiene masa y volumen. La masa se define como la cantidad de materia de un cuerpo. Se mide en kg. El
ESADOS DE AGREGACIÓN DE LA MAERIA. Propiedades generales de la materia La materia es todo aquello que tiene masa y volumen. La masa se define como la cantidad de materia de un cuerpo. Se mide en kg. El
Procesos industriales
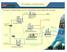 Procesos industriales en los complejos procesadores de gas Azufre Plantas de azufre proceso Claus y Superclaus Gas seco Gas amargo de PEP Endulzadoras de gas Líquidos del gas Etano Gas dulce terciario
Procesos industriales en los complejos procesadores de gas Azufre Plantas de azufre proceso Claus y Superclaus Gas seco Gas amargo de PEP Endulzadoras de gas Líquidos del gas Etano Gas dulce terciario
FACULTAD DE CIENCIAS QUIMICAS
 UNIVERSIDAD AUTONOMA DE CHIHUAHUA FACULTAD DE CIENCIAS QUIMICAS OPERACIONES UNITARIAS II Dr. Iván Salmerón Ochoa REPORTE DE LABORATORIO: DESTILACIÓN FRACCIONADA AGUIRRE OLVERA OSCAR OSWALDO 232619 ARZATE
UNIVERSIDAD AUTONOMA DE CHIHUAHUA FACULTAD DE CIENCIAS QUIMICAS OPERACIONES UNITARIAS II Dr. Iván Salmerón Ochoa REPORTE DE LABORATORIO: DESTILACIÓN FRACCIONADA AGUIRRE OLVERA OSCAR OSWALDO 232619 ARZATE
PROBLEMAS DE BALANCES DE MATERIA
 PROBLEMAS DE BALANCES DE MATERIA José Abril Requena 2013 2013 José Abril Requena INDICE Un poco de teoría... 3 Problemas resueltos... 8 Problema 1... 8 Problema 2... 8 Problema 3... 9 Problema 4... 10
PROBLEMAS DE BALANCES DE MATERIA José Abril Requena 2013 2013 José Abril Requena INDICE Un poco de teoría... 3 Problemas resueltos... 8 Problema 1... 8 Problema 2... 8 Problema 3... 9 Problema 4... 10
Facultad de Ciencias Experimentales Departamento de Ingeniería Química, Ambiental y de los Materiales. Cuaderno de prácticas de la asignatura
 UNIVERSIDAD DE JAÉN Facultad de Ciencias Experimentales Departamento de Ingeniería Química, Ambiental y de los Materiales Cuaderno de prácticas de la asignatura BASES DE LA INGENIERÍA AMBIENTAL Licenciatura
UNIVERSIDAD DE JAÉN Facultad de Ciencias Experimentales Departamento de Ingeniería Química, Ambiental y de los Materiales Cuaderno de prácticas de la asignatura BASES DE LA INGENIERÍA AMBIENTAL Licenciatura
LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA CRISTALIZACIÓN.
 CRISTALIZACIÓN. Un compuesto orgánico cristalino está constituido por un empaquetamiento tridimensional de moléculas unidas principalmente por fuerzas de Van der Waals, que originan atracciones intermoleculares
CRISTALIZACIÓN. Un compuesto orgánico cristalino está constituido por un empaquetamiento tridimensional de moléculas unidas principalmente por fuerzas de Van der Waals, que originan atracciones intermoleculares
LABORATORIO DE QUÍMIA FACULTAD DE FARMACIA DESTILACIÓN
 LABORATORIO DE QUÍMIA FACULTAD DE FARMACIA DESTILACIÓN 1. Introducción La destilación es un proceso mediante el cual un líquido se calienta hasta hacerlo pasar a estado gaseoso. A continuación, los vapores
LABORATORIO DE QUÍMIA FACULTAD DE FARMACIA DESTILACIÓN 1. Introducción La destilación es un proceso mediante el cual un líquido se calienta hasta hacerlo pasar a estado gaseoso. A continuación, los vapores
CAPITULO 5. PROCESO DE SECADO. El secado se describe como un proceso de eliminación de substancias volátiles (humedad)
 CAPITULO 5. PROCESO DE SECADO. 5.1 Descripción general del proceso de secado. El secado se describe como un proceso de eliminación de substancias volátiles (humedad) para producir un producto sólido y
CAPITULO 5. PROCESO DE SECADO. 5.1 Descripción general del proceso de secado. El secado se describe como un proceso de eliminación de substancias volátiles (humedad) para producir un producto sólido y
Planta Deshidratadora/Regeneradora de TEG
 UNIVERSIDAD TECNOLÓGICA NACIONAL - FACULTAD REGIONAL ROSARIO Departamento de Ingeniería Química INTEGRACIÓN IV Año 2001 Trabajo Práctico Regularizador Nº 1 Planta Deshidratadora/Regeneradora de TEG La
UNIVERSIDAD TECNOLÓGICA NACIONAL - FACULTAD REGIONAL ROSARIO Departamento de Ingeniería Química INTEGRACIÓN IV Año 2001 Trabajo Práctico Regularizador Nº 1 Planta Deshidratadora/Regeneradora de TEG La
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire.
 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire. El proceso de secado es una de las operaciones más importantes en la industria
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire. El proceso de secado es una de las operaciones más importantes en la industria
ANEJO 5: INSTALACIÓN DE VAPOR
 ANEJO 5: INSTALACIÓN DE VAPOR ANEJO 5: INSTALACIÓN DE VAPOR. 1. Consumo de vapor. 2. Caldera de vapor. 2.1. Instalación de agua para la caldera. 2.2. Instalación de fuel-oil. 1.-. Para la instalación de
ANEJO 5: INSTALACIÓN DE VAPOR ANEJO 5: INSTALACIÓN DE VAPOR. 1. Consumo de vapor. 2. Caldera de vapor. 2.1. Instalación de agua para la caldera. 2.2. Instalación de fuel-oil. 1.-. Para la instalación de
el calor cedido al medio disipante (generalmente el aire ambiente o agua) i W el trabajo necesario para que funcione el sistema.
 Capítulo 1 Métodos frigoríficos 1. Introducción La refrigeración consiste en la extracción de calor de una sustancia que deseamos mantener a una temperatura inferior a la del medio ambiente. Para ello
Capítulo 1 Métodos frigoríficos 1. Introducción La refrigeración consiste en la extracción de calor de una sustancia que deseamos mantener a una temperatura inferior a la del medio ambiente. Para ello
En la segunda manera, se crea un vacío suficientemente elevado y se observa si el manómetro mantiene constante el valor de vacío alcanzado.
 PROCEDIMIENTO PARA CARGAR CON GAS UNA INSTALACiÓN FRIGORíFICA Y PONERLA EN MARCHA. CONTROL DE LA ESTANQUIDAD DE LA INSTALACiÓN. La primera operación que deberá realizarse es la verificación de la estanquidad
PROCEDIMIENTO PARA CARGAR CON GAS UNA INSTALACiÓN FRIGORíFICA Y PONERLA EN MARCHA. CONTROL DE LA ESTANQUIDAD DE LA INSTALACiÓN. La primera operación que deberá realizarse es la verificación de la estanquidad
TEMA 1 Conceptos básicos de la termodinámica
 Bases Físicas y Químicas del Medio Ambiente TEMA 1 Conceptos básicos de la termodinámica La termodinámica es el estudio de la transformación de una forma de energía en otra y del intercambio de energía
Bases Físicas y Químicas del Medio Ambiente TEMA 1 Conceptos básicos de la termodinámica La termodinámica es el estudio de la transformación de una forma de energía en otra y del intercambio de energía
Estudio de la evaporación
 Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
Destilación - Método del polo de operación II. Problemas. Problemas de Operaciones Unitarias II Ingeniería Química 1
 Destilación - Método del polo de operación II Problemas PROBLEMA 1. A una columna de agotamiento como la indicada en la figura, ingresa una mezcla etanol/agua en su punto de burbuja, de composición 50
Destilación - Método del polo de operación II Problemas PROBLEMA 1. A una columna de agotamiento como la indicada en la figura, ingresa una mezcla etanol/agua en su punto de burbuja, de composición 50
Diagrama de Fases Temperatura de Ebullición-Composición de una Mezcla
 Diagrama de Fases Temperatura de Ebullición-Composición de una Mezcla Líquida Binaria. Fundamentos teóricos. 1.- Equilibrios líquido-vapor en sistemas binarios: Disoluciones ideales. 2.- Diagramas de fase
Diagrama de Fases Temperatura de Ebullición-Composición de una Mezcla Líquida Binaria. Fundamentos teóricos. 1.- Equilibrios líquido-vapor en sistemas binarios: Disoluciones ideales. 2.- Diagramas de fase
La inertización de procesos industriales con recuperación de volátiles. Franz Bechtold Abelló Linde, S.A. Expoquimia 16 de noviembre de 2011
 La inertización de procesos industriales con recuperación de volátiles Franz Bechtold Abelló Linde, S.A. Expoquimia 16 de noviembre de 2011 Inertización de procesos La necesidad del uso de atmósferas inertes,
La inertización de procesos industriales con recuperación de volátiles Franz Bechtold Abelló Linde, S.A. Expoquimia 16 de noviembre de 2011 Inertización de procesos La necesidad del uso de atmósferas inertes,
ENERGÍA ELÉCTRICA. Central térmica
 ENERGÍA ELÉCTRICA. Central térmica La central térmica de Castellón (Iberdrola) consta de dos bloques de y 5 MW de energía eléctrica, y utiliza como combustible gas natural, procedente de Argelia. Sabiendo
ENERGÍA ELÉCTRICA. Central térmica La central térmica de Castellón (Iberdrola) consta de dos bloques de y 5 MW de energía eléctrica, y utiliza como combustible gas natural, procedente de Argelia. Sabiendo
TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones.
 Esquema: TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones. TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones....1 1.- Introducción...1 2.- Máquina frigorífica...1
Esquema: TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones. TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones....1 1.- Introducción...1 2.- Máquina frigorífica...1
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRIMERA PARTE
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A ESTUDIOS UNIVERSITARIOS (LOGSE) Curso 2006-2007 MATERIA: QUÍMICA INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consta de dos partes.
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A ESTUDIOS UNIVERSITARIOS (LOGSE) Curso 2006-2007 MATERIA: QUÍMICA INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consta de dos partes.
Problemas de Fundamentos de Química (1º Grado en Física) Tema 2. FUERZAS INTERMOLECULARES
 Problemas de Fundamentos de Química (1º Grado en Física) Tema 2. FUERZAS INTERMOLECULARES 2.1. Calcula la presión que ejerce 1 mol de Cl 2 (g), de CO 2 (g) y de CO (g) cuando se encuentra ocupando un volumen
Problemas de Fundamentos de Química (1º Grado en Física) Tema 2. FUERZAS INTERMOLECULARES 2.1. Calcula la presión que ejerce 1 mol de Cl 2 (g), de CO 2 (g) y de CO (g) cuando se encuentra ocupando un volumen
REACTORES QUÍMICOS - PROBLEMAS RCTA 36-46
 REACTORES QUÍMICOS - PROBLEMAS RCTA 6-46 Curso 011-01 6.- Para llevar a cabo la descomposición del acetaldehído en fase gas, una reacción irreversible y de segundo orden respecto a este compuesto, se emplea
REACTORES QUÍMICOS - PROBLEMAS RCTA 6-46 Curso 011-01 6.- Para llevar a cabo la descomposición del acetaldehído en fase gas, una reacción irreversible y de segundo orden respecto a este compuesto, se emplea
CAMBIO DE FASE : VAPORIZACIÓN
 CAMBIO DE FASE : VAPORIZACIÓN Un líquido no tiene que ser calentado a su punto de ebullición antes de que pueda convertirse en un gas. El agua, por ejemplo, se evapora de un envase abierto en la temperatura
CAMBIO DE FASE : VAPORIZACIÓN Un líquido no tiene que ser calentado a su punto de ebullición antes de que pueda convertirse en un gas. El agua, por ejemplo, se evapora de un envase abierto en la temperatura
INDICE 3. CALCULO Y DISEÑO DE LAS LINEAS DE REFRIGERANTE 3.1.1. PERDIDA DE PRESION 3.1.2. RETORNO DEL ACEITE AL COMPRESOR 3.1.3.
 Cálculo y Diseño de Líneas de Refrigerante INDICE 0. INTRODUCCION 1. PRINCIPIOS BASICOS 2. MATERIAL 3. CALCULO Y DISEÑO DE LAS LINEAS DE REFRIGERANTE 3.1. LINEA DE ASPIRACION 3.1.1. PERDIDA DE PRESION
Cálculo y Diseño de Líneas de Refrigerante INDICE 0. INTRODUCCION 1. PRINCIPIOS BASICOS 2. MATERIAL 3. CALCULO Y DISEÑO DE LAS LINEAS DE REFRIGERANTE 3.1. LINEA DE ASPIRACION 3.1.1. PERDIDA DE PRESION
EXPERIMENTO 2: SEPARACIÓN DE HEXANO Y CICLOHEXANO UTILIZANDO UNA COLUMNA DE RECTIFICACIÓN OBJETIVO:
 EXPERIMENTO 2: SEPARACIÓN DE HEXANO Y CICLOHEXANO UTILIZANDO UNA COLUMNA DE RECTIFICACIÓN OBJETIVO: El objetivo de la práctica es el manejo de una columna de rectificación de relleno, estudiando la separación
EXPERIMENTO 2: SEPARACIÓN DE HEXANO Y CICLOHEXANO UTILIZANDO UNA COLUMNA DE RECTIFICACIÓN OBJETIVO: El objetivo de la práctica es el manejo de una columna de rectificación de relleno, estudiando la separación
AUDITORÍAS ENERGÉTICAS
 MÁSTER DE ENERGÍA: GENERACIÓN, GESTIÓN Y USO EFICIENTE Asignatura: GESTIÓN ENERGÉTICA AUDITORÍAS ENERGÉTICAS E.T.S. Ingenieros Industriales Dr. Eloy Velasco Gómez Profesor Titular de Universidad Dpto.
MÁSTER DE ENERGÍA: GENERACIÓN, GESTIÓN Y USO EFICIENTE Asignatura: GESTIÓN ENERGÉTICA AUDITORÍAS ENERGÉTICAS E.T.S. Ingenieros Industriales Dr. Eloy Velasco Gómez Profesor Titular de Universidad Dpto.
ELIMINACION DE GASES DISUELTOS DESAIREADORES
 Departamento de Tecnología y ELIMINACION DE GASES DISUELTOS DESAIREADORES Eduardo Barreiro Daniel Ghislieri ELIMINACION DE GASES DISUELTOS D E S A I R E A D O R E S Una vez eliminados los sólidos en suspensión,
Departamento de Tecnología y ELIMINACION DE GASES DISUELTOS DESAIREADORES Eduardo Barreiro Daniel Ghislieri ELIMINACION DE GASES DISUELTOS D E S A I R E A D O R E S Una vez eliminados los sólidos en suspensión,
Figura 11. Diagrama de la jerarquía de un proceso
 Capítulo 4. Metodología 4.1 Síntesis del diagrama de flujo para el proceso de producción de dimetil éter La representación de un proceso químico está dada por un diagrama de flujo. Para que esta representación
Capítulo 4. Metodología 4.1 Síntesis del diagrama de flujo para el proceso de producción de dimetil éter La representación de un proceso químico está dada por un diagrama de flujo. Para que esta representación
Fig. 11.1: Caldera humotubular de un paso (Shield).
 UNIDAD 11 Generadores de Vapor 1. General La generación de vapor para el accionamiento de las turbinas se realiza en instalaciones generadoras comúnmente denominadas calderas. La instalación comprende
UNIDAD 11 Generadores de Vapor 1. General La generación de vapor para el accionamiento de las turbinas se realiza en instalaciones generadoras comúnmente denominadas calderas. La instalación comprende
El balance de energía. Aplicaciones de la primera ley de la termodinámica. Ejercicios.
 TERMODINÁMICA (0068) PROFR. RIGEL GÁMEZ LEAL El balance de energía. Aplicaciones de la primera ley de la termodinámica. Ejercicios. 1. Suponga una máquina térmica que opera con el ciclo reversible de Carnot
TERMODINÁMICA (0068) PROFR. RIGEL GÁMEZ LEAL El balance de energía. Aplicaciones de la primera ley de la termodinámica. Ejercicios. 1. Suponga una máquina térmica que opera con el ciclo reversible de Carnot
Datos ELV, Fracciones molares de n-c 6 H 14, 1 atm x (líquido) 0,0 0,1 0,3 0,5 0,55 0,7 1,0 y (vapor) 0,0 0,36 0,70 0,85 0,90 0,95 1,0 Sigue
 Método del polo de operación (I) - Destilación Problemas PROBLEMA 1*. Cierta cantidad de una mezcla de vapor de alcohol etílico y agua, 50 % molar, a una temperatura de 190 ºF, se enfría hasta su punto
Método del polo de operación (I) - Destilación Problemas PROBLEMA 1*. Cierta cantidad de una mezcla de vapor de alcohol etílico y agua, 50 % molar, a una temperatura de 190 ºF, se enfría hasta su punto
UNEFM TERMODINAMICA APLICADA ING. ANA PEÑA GUIA DE PSICOMETRIA
 MEZCLA DE GAS VAPOR UNEFM TERMODINAMICA APLICADA ING. ANA PEÑA GUIA DE PSICOMETRIA AIRE SECO Y ATMOSFÉRICO: El aire es una mezcla de Nitrógeno, Oxígeno y pequeñas cantidades de otros gases. Aire Atmosférico:
MEZCLA DE GAS VAPOR UNEFM TERMODINAMICA APLICADA ING. ANA PEÑA GUIA DE PSICOMETRIA AIRE SECO Y ATMOSFÉRICO: El aire es una mezcla de Nitrógeno, Oxígeno y pequeñas cantidades de otros gases. Aire Atmosférico:
COGENERACIÓN. Santiago Quinchiguango
 COGENERACIÓN Santiago Quinchiguango Noviembre de 2014 8.3 Selección del motor térmico. 8.3 Selección del motor térmico. MOTORES TÉRMICOS INTRODUCCIÓN Los motores térmicos son dispositivos que transforman
COGENERACIÓN Santiago Quinchiguango Noviembre de 2014 8.3 Selección del motor térmico. 8.3 Selección del motor térmico. MOTORES TÉRMICOS INTRODUCCIÓN Los motores térmicos son dispositivos que transforman
JULIO 2012. FASE ESPECÍFICA. QUÍMICA.
 JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
TEMA 11. MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN
 TEMA 11. MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN 1. Destilación 2. Extracción 3. Sublimación 4. Cristalización 5. Cromatografía 6. Fórmulas empíricas y moleculares 2 Tema 11 TEMA 11. Métodos físicos
TEMA 11. MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN 1. Destilación 2. Extracción 3. Sublimación 4. Cristalización 5. Cromatografía 6. Fórmulas empíricas y moleculares 2 Tema 11 TEMA 11. Métodos físicos
TECNOLOGÍA JAPONESA AL SERVICIO DE LA REFRIGERACIÓN INDUSTRIAL MAYEKAWA CHILE S.A.C. E I.
 TECNOLOGÍA JAPONESA AL SERVICIO DE LA REFRIGERACIÓN INDUSTRIAL MAYEKAWA CHILE S.A.C. E I. REFRIGERACIÓN Ahorro de energía Este concepto ya esta en la mente de cada empresa y persona. Actualmente, es parte
TECNOLOGÍA JAPONESA AL SERVICIO DE LA REFRIGERACIÓN INDUSTRIAL MAYEKAWA CHILE S.A.C. E I. REFRIGERACIÓN Ahorro de energía Este concepto ya esta en la mente de cada empresa y persona. Actualmente, es parte
APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN
 259 APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN La desecación se emplea para extraer la humedad de los líquidos, soluciones y sustancias sólidas. El grado de desecación de una sustancia depende
259 APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN La desecación se emplea para extraer la humedad de los líquidos, soluciones y sustancias sólidas. El grado de desecación de una sustancia depende
Equilibrio de fases en sistemas binarios y ternarios
 Equilibrio de fases en sistemas binarios y ternarios. Equilibrio líquido-vapor Desviaciones positivas y negativas de la ley de Raoult. Las desviaciones son debidas a factores de origen molecular. Recordemos
Equilibrio de fases en sistemas binarios y ternarios. Equilibrio líquido-vapor Desviaciones positivas y negativas de la ley de Raoult. Las desviaciones son debidas a factores de origen molecular. Recordemos
[1] Si se analiza en un perfil del suelo la distribución vertical del agua en profundidad
![[1] Si se analiza en un perfil del suelo la distribución vertical del agua en profundidad [1] Si se analiza en un perfil del suelo la distribución vertical del agua en profundidad](/thumbs/25/5767219.jpg) 1. INTRODUCCIÓN 1.1. MARCO TEÓRICO Distribución vertical del agua en el suelo [1] Si se analiza en un perfil del suelo la distribución vertical del agua en profundidad Figura 1 se pueden distinguir la
1. INTRODUCCIÓN 1.1. MARCO TEÓRICO Distribución vertical del agua en el suelo [1] Si se analiza en un perfil del suelo la distribución vertical del agua en profundidad Figura 1 se pueden distinguir la
Una caldera de vapor para cada necesidad Generador de vapor rápido o caldera pirotubular
 Una caldera de vapor para cada necesidad Generador de vapor rápido o caldera pirotubular Al adquirir calderas de vapor nos preguntamos a qué principio constructivo debemos dar la preferencia. En este artículo
Una caldera de vapor para cada necesidad Generador de vapor rápido o caldera pirotubular Al adquirir calderas de vapor nos preguntamos a qué principio constructivo debemos dar la preferencia. En este artículo
Física y Tecnología Energética. 9 - Máquinas Térmicas. Motor de vapor. Turbinas.
 Física y Tecnología Energética 9 - Máquinas Térmicas. Motor de vapor. Turbinas. Máquina de vapor de Newcomen (1712) Cuando se hierve agua su volumen se expande 1000 veces y puede empujar un pistón Es necesario
Física y Tecnología Energética 9 - Máquinas Térmicas. Motor de vapor. Turbinas. Máquina de vapor de Newcomen (1712) Cuando se hierve agua su volumen se expande 1000 veces y puede empujar un pistón Es necesario
CAPÍTULO 1. INTRODUCCIÓN
 CAPÍTULO 1. INTRODUCCIÓN Constantemente, la ingeniería ha buscado diferentes caminos para desarrollar proyectos que presenten alta eficiencia con el menor daño producido al medio ambiente y hagan de nuestro
CAPÍTULO 1. INTRODUCCIÓN Constantemente, la ingeniería ha buscado diferentes caminos para desarrollar proyectos que presenten alta eficiencia con el menor daño producido al medio ambiente y hagan de nuestro
Examen de TERMODINÁMICA II Curso 1997-98
 ESCUELA SUPERIOR DE INGENIEROS INDUSTRIALES Universidad de Navarra Examen de TERMODINÁMICA II Curso 997-98 Obligatoria centro - créditos de agosto de 998 Instrucciones para el examen de TEST: Cada pregunta
ESCUELA SUPERIOR DE INGENIEROS INDUSTRIALES Universidad de Navarra Examen de TERMODINÁMICA II Curso 997-98 Obligatoria centro - créditos de agosto de 998 Instrucciones para el examen de TEST: Cada pregunta
La finalidad del mismo fue conseguir separar las sales presentes en la salmuera con varios objetivos;
 LÍNEA DE INVESTIGACIÓN 1. Investigación a nivel piloto de la tecnología de recuperación de sales divalentes procedentes de salmueras. Caracterización y posibles usos de alternativas de las salmueras para
LÍNEA DE INVESTIGACIÓN 1. Investigación a nivel piloto de la tecnología de recuperación de sales divalentes procedentes de salmueras. Caracterización y posibles usos de alternativas de las salmueras para
Aire Acondicionado (I.I.)
 Aire Acondicionado (I.I.) T15.- Otros Recuperadores de Calor Las trasparencias son el material de apoyo del profesor para impartir la clase. No son apuntes de la asignatura. Al alumno le pueden servir
Aire Acondicionado (I.I.) T15.- Otros Recuperadores de Calor Las trasparencias son el material de apoyo del profesor para impartir la clase. No son apuntes de la asignatura. Al alumno le pueden servir
Absorción (desorción) de Gases. Transferencia de Materia 2 Semestre 2010 Alonso Jaques
 Absorción (desorción) de Gases Transferencia de Materia 2 Semestre 2010 Alonso Jaques Laboratorio: Ver aviso. Quiz Lab. 3. Zwietering correlation: n JS = Sν 0.1 g ρ S ρ L /ρ L 0.45 X 0.13 d P 0.2 D 0.85
Absorción (desorción) de Gases Transferencia de Materia 2 Semestre 2010 Alonso Jaques Laboratorio: Ver aviso. Quiz Lab. 3. Zwietering correlation: n JS = Sν 0.1 g ρ S ρ L /ρ L 0.45 X 0.13 d P 0.2 D 0.85
Las sustancias puras son los elementos y los compuestos.
 Las sustancias puras son los elementos y los compuestos. Un elemento es una sustancia pura porque todas las partículas que lo forman son iguales y tiene unas propiedades características. Ejemplo: el oxígeno,
Las sustancias puras son los elementos y los compuestos. Un elemento es una sustancia pura porque todas las partículas que lo forman son iguales y tiene unas propiedades características. Ejemplo: el oxígeno,
Cantidad en el sistema en el tiempo 1 (t 1 )
 I. BALANCES DE MATERIA SIN REACCIÓN QUÍMICA EN FLUJO CONTINUO. Tema 2. Balance de masa sin reacción química en flujo continúo I.2 Objetivo de aprendizaje: SABER: Deducir la ecuación de balance de masa.
I. BALANCES DE MATERIA SIN REACCIÓN QUÍMICA EN FLUJO CONTINUO. Tema 2. Balance de masa sin reacción química en flujo continúo I.2 Objetivo de aprendizaje: SABER: Deducir la ecuación de balance de masa.
Cómo llevar a cabo una reacción química desde el punto de vista experimental
 Cómo llevar a cabo una reacción química desde el punto de vista experimental Para obtener un compuesto se pueden utilizar varias técnicas, que incluyen el aislamiento y la purificación del mismo. Pero
Cómo llevar a cabo una reacción química desde el punto de vista experimental Para obtener un compuesto se pueden utilizar varias técnicas, que incluyen el aislamiento y la purificación del mismo. Pero
Ciclos de Potencia Curso 2007. Ejercicios
 Ejercicios Cuando no se indica otra cosa, los dispositivos y ciclos se asumen ideales. En todos los casos, bosqueje los ciclos y realice los diagramas apropiados. Se indican las respuestas para que controle
Ejercicios Cuando no se indica otra cosa, los dispositivos y ciclos se asumen ideales. En todos los casos, bosqueje los ciclos y realice los diagramas apropiados. Se indican las respuestas para que controle
Determinación del calor latente de fusión del hielo
 Determinación del calor latente de usión del hielo Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica
Determinación del calor latente de usión del hielo Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica
DESTILACIÓN. DETERMINACIÓN DEL GRADO ALCOHÓLICO DEL VINO
 1. INTRODUCCION La destilación es un proceso que consiste en calentar un líquido hasta que sus componentes más volátiles pasan a la fase de vapor y, a continuación, enfriar el vapor para recuperar dichos
1. INTRODUCCION La destilación es un proceso que consiste en calentar un líquido hasta que sus componentes más volátiles pasan a la fase de vapor y, a continuación, enfriar el vapor para recuperar dichos
Transferencia de calor Intercambiadores de calor
 Transferencia de calor Intercambiadores de calor Construcción de los intercambiadores de calor La construcción general de los intercambiadores de carcasa y tubos consiste en un haz de tubos paralelos dentro
Transferencia de calor Intercambiadores de calor Construcción de los intercambiadores de calor La construcción general de los intercambiadores de carcasa y tubos consiste en un haz de tubos paralelos dentro
UTN FRR CATEDRA DE INTEGRACIÓN III PAG. 1
 UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAENTO DE INGENIERIA QUIICA CATEDRA DE INTEGRACIÓN III DIAGRAAS DE ENTALPIA COPOSICION UTN FRR CATEDRA DE INTEGRACIÓN III PAG. DIAGRAAS DE
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAENTO DE INGENIERIA QUIICA CATEDRA DE INTEGRACIÓN III DIAGRAAS DE ENTALPIA COPOSICION UTN FRR CATEDRA DE INTEGRACIÓN III PAG. DIAGRAAS DE
Materiales recopilados por la Ponencia Provincial de Química para Selectividad TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la
![CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la](/thumbs/26/7800050.jpg) 34 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO 4.1 Lecho fluidizado con vapor sobrecalentado Potter [10], ha demostrado en una planta piloto que materiales sensibles a la temperatura pueden
34 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO 4.1 Lecho fluidizado con vapor sobrecalentado Potter [10], ha demostrado en una planta piloto que materiales sensibles a la temperatura pueden
TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. Calcule: a) Los moles de metano que quedan. b) Las moléculas
TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. Calcule: a) Los moles de metano que quedan. b) Las moléculas
4027 Síntesis de 11-cloroundec-1-eno a partir de 10-undecen-1- ol
 4027 Síntesis de 11-cloroundec-1-eno a partir de 10-undecen-1- ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Clasificación Tipos de reacción y clases de productos
4027 Síntesis de 11-cloroundec-1-eno a partir de 10-undecen-1- ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Clasificación Tipos de reacción y clases de productos
Instalaciones de tratamiento de agua de alimentación de caldera
 Instalaciones de tratamiento de agua de alimentación de caldera Introducción La calidad del agua de alimentación a la caldera repercute directamente sobre el buen funcionamiento de la misma así como sobre
Instalaciones de tratamiento de agua de alimentación de caldera Introducción La calidad del agua de alimentación a la caldera repercute directamente sobre el buen funcionamiento de la misma así como sobre
C()n()cer- el C()WP()rtamient() del air-e pe..-mite aplicar- cñteñ()s C()r-r-ect()s de manej() en el ac()ndici()namient() y almacenaie..
 C()n()cer- el C()WP()rtamient() del air-e pe..-mite aplicar- cñteñ()s C()r-r-ect()s de manej() en el ac()ndici()namient() y almacenaie.. Ricardo Muñoz C. Ingeniero Agrónomo M.S. Sicrometría, en términos
C()n()cer- el C()WP()rtamient() del air-e pe..-mite aplicar- cñteñ()s C()r-r-ect()s de manej() en el ac()ndici()namient() y almacenaie.. Ricardo Muñoz C. Ingeniero Agrónomo M.S. Sicrometría, en términos
2.3 SISTEMAS HOMOGÉNEOS.
 2.3 SISTEMAS HOMOGÉNEOS. 2.3.1 DISOLUCIONES. Vemos que muchos cuerpos y sistemas materiales son heterogéneos y podemos observar que están formados por varias sustancias. En otros no podemos ver que haya
2.3 SISTEMAS HOMOGÉNEOS. 2.3.1 DISOLUCIONES. Vemos que muchos cuerpos y sistemas materiales son heterogéneos y podemos observar que están formados por varias sustancias. En otros no podemos ver que haya
SISTEMA DE CONTROL DE LAS VARIABLES OPERACIONALES EN LA POLIMERIZACIÓN DE PROPILENO A ESCALA PILOTO
 SISTEMA DE CONTROL DE LAS VARIABLES OPERACIONALES EN LA POLIMERIZACIÓN DE PROPILENO A ESCALA PILOTO Jenny C. Campos 1*, Carlos E. Ortega 1, Nicolino Bracho 2, Charles Gutiérrez 3, Haydee Oliva 4 1) Escuela
SISTEMA DE CONTROL DE LAS VARIABLES OPERACIONALES EN LA POLIMERIZACIÓN DE PROPILENO A ESCALA PILOTO Jenny C. Campos 1*, Carlos E. Ortega 1, Nicolino Bracho 2, Charles Gutiérrez 3, Haydee Oliva 4 1) Escuela
Turbinas de vapor. Introducción
 Turbinas de vapor Introducción La turbina de vapor es una máquina de fluido en la que la energía de éste pasa al eje de la máquina saliendo el fluido de ésta con menor cantidad de energía. La energía mecánica
Turbinas de vapor Introducción La turbina de vapor es una máquina de fluido en la que la energía de éste pasa al eje de la máquina saliendo el fluido de ésta con menor cantidad de energía. La energía mecánica
TRABAJO DE RECUPERACIÓN DEL PRIMER PARCIAL 2012-2013
 TRABAJO DE RECUPERACIÓN DEL PRIMER PARCIAL 2012-2013 ÁREA: QUÍMICA CURSO: SEGUNDO DE BACHILLERATO NOMBRE: FECHA DE ENTREGA: Jueves, 22-11-2012 INDICACIONES GENERALES: El trabajo deberá ser entregado a
TRABAJO DE RECUPERACIÓN DEL PRIMER PARCIAL 2012-2013 ÁREA: QUÍMICA CURSO: SEGUNDO DE BACHILLERATO NOMBRE: FECHA DE ENTREGA: Jueves, 22-11-2012 INDICACIONES GENERALES: El trabajo deberá ser entregado a
FLUJOGRAMA DE PROCESOS. SELECCIÓN
 FLUJOGRAMA DE PROCESOS. SELECCIÓN DE UN PROCESO AGROINDUSTRIAL. PROCESOS INTEGRADOS. EXPERIMENTACIÓN EN PLANTA PILOTO. ING. WILLIAMS CASTILLO MARTINEZ SISTEMA GLOBAL DE UN PROCESO Materias Primas Insumos
FLUJOGRAMA DE PROCESOS. SELECCIÓN DE UN PROCESO AGROINDUSTRIAL. PROCESOS INTEGRADOS. EXPERIMENTACIÓN EN PLANTA PILOTO. ING. WILLIAMS CASTILLO MARTINEZ SISTEMA GLOBAL DE UN PROCESO Materias Primas Insumos
INTERCAMBIADORES DE CALOR. Mg. Amancio R. Rojas Flores
 INTERCAMBIADORES DE CALOR Mg. Amancio R. Rojas Flores INTRODUCCIÓN Los intercambiadores de calor son aparatos que facilitan el intercambio de calor entre dos fluidos que se encuentran a temperaturas diferentes
INTERCAMBIADORES DE CALOR Mg. Amancio R. Rojas Flores INTRODUCCIÓN Los intercambiadores de calor son aparatos que facilitan el intercambio de calor entre dos fluidos que se encuentran a temperaturas diferentes
Calentadores Solares
 Calentadores Solares Modelos Usted ha adquirido un Calentador Solar A partir de hoy empezará a ahorrar dinero y apoyará a la conservación del medio ambiente. Nuestro calentador funciona con los rayos del
Calentadores Solares Modelos Usted ha adquirido un Calentador Solar A partir de hoy empezará a ahorrar dinero y apoyará a la conservación del medio ambiente. Nuestro calentador funciona con los rayos del
Calentadores y Sistemas de Fluido Térmico.
 Calentadores y Sistemas de Fluido Térmico. El objetivo del presente artículo es entregar información técnica para diseñar, especificar y operar sistemas de fluido térmico. Introducción Agua y vapor son
Calentadores y Sistemas de Fluido Térmico. El objetivo del presente artículo es entregar información técnica para diseñar, especificar y operar sistemas de fluido térmico. Introducción Agua y vapor son
