Física de Sistemas Fuera del Equilibrio Gas de Knudsen
|
|
|
- María Antonia Rubio Toro
- hace 8 años
- Vistas:
Transcripción
1 Física de Sistemas Fuera del Equilibrio Gas de Knudsen Iñigo Romero Arandia 9 de mayo de. Ejercicio 6: Efusión en el gas de Knudsen El gas de Knudsen es una configuración experimental en la que dos gases en contacto con fuentes a temperaturas diferentes se ponen en contacto a través de una superficie porosa. Las dimensiones del poro en la superficie son muy pequenãs y comparables al recorrido libre medio de los gases. Aunque cada uno de los dos volúmenes está en equilibrio local en contacto con las respectivas fuentes, el conjunto total formado por los dos sistemas se puede mantener en un estado estacionario fuera del equilibrio. En esta situación aparece un flujo de energía entre los dos sistemas... Relación -P Considerar un gas de Knudsen formado por dos sistemas cerrados en formados por dos gases ideales idénticos que ocupan iguales volúmenes, V V V. Los gases están a temperaturas diferentes, y, y se encuentran conectados a través de una abertura de diámetro d l, donde l es el recorrido libre medio de los gases. Utilizando la distribución de Maxwell demostrar que el flujo de moléculas a través del orificio es: KB J n n πm En este caso m es la masa de las moléculas, y n la densidad molecular. ( El flujo de moléculas a través de la abertura dependerá de la cantidad de moléculas que tengan velocidad en la dirección z. Las moléculas que cruzarán del volumen inferior al superior serán las que tengan velocidad positiva, entre e infinito: Distribución de Maxwell-Boltzmann: J n f(u i nu z f(ud 3 u ( ( / λ e λu i (3 π Con i x, y, z. La distribución de Maxwell cumple la condición de normalización siguiente: f(u i du i (4
2 Se ha utilizado el siguiente cambio de variable: λ m k b (5 Sustituyendo en la ecuación ( las definiciones superiores ( 3, ( 4 : J n Calculando la integral a parte: nu z f(u z du z f(u y du y f(u x du x n u i f(u i du i ( [ ] / λ e λu i π λ Con este resultado, y sustituyendo el valor de λ, ( 5 el flujo queda: ( / λ π u z f(u z du z λ (6 πλ J n n n πλ πm k B KB n πm (7 Demostrar que en el estado estacionario: P P (8 En el estado estacionario el flujo de moléculas a través de la abertura debe ser nulo. Esto es debido a que los sistemas son cerrados, por lo que no intercambian materia con las fuentes. Al no haber ninguna fuente de materia, si hubiera un flujo de moléculas neto de un volumen a otro, en algún momento las moléculas en uno de los recipientes se terminarían, y por tanto no sería una situción estacionaria. Usando la condición de que el flujo neto de moléculas es nulo y haciendo el cambio u z u z teniendo en cuenta que la función de Maxwell sólo depende del módulo de la velocidad: Jn total Jn + Jn n u z f(u z du z + n u z f(u z du z n u z f(u z du z + n ( u z f(u z ( du z n u z f(u z du z n u z f(u z du z Utilizando el resultado demostrado en el apartado anterior, (, y teniendo en cuenta que los dos gases son idénticos, m m m: Jn total kb n πm n kb πm (9 Al tratarse de gases ideales se cumplirá la ecuación de estado: P V Nk B n i N i V P i k B i ( Aquí N es la cantidad de moléculas, y n la densidad molecular. Se ha utilizado V V V. Sustituyendo este resultado: n n P P P P ( k B k B
3 .. Conductividad térmica J q transferencia de energía cinética e energía de intercambio entre los dos sistemas por cada molécula que atraviesa el poro. Demostrar que la energía de intercambio vale: e k B ( Una forma de realizar este cálculo es mediante el flujo de energía cinética, que se puede calcular de manera análoga al caso del flujo de partículas, ecuación (, poniendo la energía cinética: J q n mu u z f(ud 3 u (3 Utilizando las ecuaciones ( 3, ( 4, y ( 5, y teniendo en cuenta que las integrales en las direcciones x e y van desde hasta y son equivalentes: J q n m ( du x du y du z u x + u y + u z uz f(u z f(u x f(u y n m du x du y du z u xu z f(u z f(u x f(u y + + n m du x du y du z u 3 zf(u z f(u x f(u y Cálculo de las integrales por partes, utilizando el resultado de la integral 6: ( [ ] / λ u e i f(u i du i (u λu i e λu i i π λ λ u 3 i f(u i du i ( [ [ ] / λ u e λu i e λu i i u i π λ λ ] ( / λ π π λ λ λ ( / λ π λ λ (4 ( / λ π λ (5 Introduciendo estos resultados en el flujo de energía: J q ( [ ( ( / λ nm λ π λ + ( ( ] / λ π λ (6 eniendo en cuenta el valor de J n (, y sustituyendo el valor de λ ( 5 : ( ] J q J n [ k B + (k B J n k B (7 Una vez calculada esta integral la energía de intercambio por molécula es inmediata: e Jq J n resultado esperado, ecuación (. k B, que es el Evaluar la conductividad térmica, κ definida por: donde, con >, y / i para i,. J q κ (8 3
4 El flujo total de energía cinética será la suma del flujo del primer recipiente al segundo más el del segundo al primero: [ ] Jq total Jq + Jq k B Jn + k B Jn KB k B n πm KB n πm [ ] P KB k B k B πm P KB kb ] [P P k B πm πm [ ] kb kb P P P ( πm πm kb πm P Se ha utilizado que n i N i /V Pi k B i y la relación entre las presiones y las temperaturas del estado estacionario, ecuación 8. De esta expresión se puede conseguir de manera inmediata el valor de la conductividad térmica, κ, en función de la temperatura y la presión de uno de los recipientes, y de la masa de las partículas: κ J q P kb (9 πm.3. Calor de intercambio El calor de intercambio se define como el calor intercambiado entre los dos sistemas por que cada mol que atraviesa la abertura en una dirección dada. Demostrar que este calor de intercambio por mol viene dado por: q R Qué significa que antes e fuera positiva y ahora q negativa? Qué interpretación física tiene? ( Esta energía de intercambio se puede interpretar como la suma de las energías cinéticas medias en las direcciones x e y, que según el principio de equipartición valen: < mu x >< mu y > k B más otro k B que aporta la dirección z. Estos dos términos se pueden identificar en las integrales para el cálculo del flujo, y en la ecuación 7. Esto quiere decir que una molécula que esté en uno de los recipientes con una energía 3 k B, por cada grado de libertad, al entrar en la abertura adquiere un k B extra. Al llegar al otro recipiente la molécula vuelve a recuperar la energía del gas ideal, 3 k B, alcanzando una situación de equilibrio con su alrededor y por tanto pierde en este volumen el k B extra que había cogido del primer volumen al entrar en el poro. Este k B se puede interpretar como la transferencia de calor de un sistema al otro. Como este calor sale del recipiente de origen de la partícula hacia el otro, supone una pérdida de energía y tendrá signo negativo. eniendo esto en cuenta el calor de intercambio por mol será q R. Otra forma de verlo puede ser que las moléculas de un sistema en equilibrio térmico con la fuente tienen una energía promedio de 3 k B, pero todas las moléculas individuales no tendrán esta energía, algunas tendrán una energía mayor, y otras menor. Como la energía de intercambio es k B se puede interpretar como que las partículas que tienen mayor energía, o lo que es lo mismo, mayor velocidad, tienen una probabilidad mayor de cruzar al otro sistema. Si no hubiera fuente, el paso de las moléculas con mayor energía al otro volumen provocaría un enfriamiento del recipiente, ya que al faltar las partículas más energéticas el valor medio de la energía también disminuiría. Esto vuelve a demuestra que las fuentes son imprescindibles para alcanzar un estado estacionario de no equilibrio. 4
5 .4. Límite en que d l Explicar que pasaría si se aumentase el diámetro de la abertura hasta hacerla comparable al recorrido libre medio. Cuánto valen e y q en el límite d l? Se mantienen válidas las relaciones 8,, y? Cómo cambian? Al aumentar las dimensiones de la abertura y hacerla mayor que el recorrido libre medio, las partículas empezarán a colisionar con otras partículas al pasar de un sistema a otro. En el caso anterior como d l la partícula que estaba cruzando colisionaba antes con las paredes de la abertura que con otras moléculas, y como los choques con las paredes se desprecian al considerar el gas ideal no había perdida de energía. Sin embargo, al empezar a colisionar con otras partículas, se realizará un trabajo, que se equivalente a pv R (por mol. Las moléculas alcanzarán un equilibrio local con las de los alrededores dentro de la abertura, termalizarán, y eso llevará a la difusión habitual que explica la ley de Fick. La energía intercambiada se puede dividir en dos aportaciones: por un lado la entalpía, que es la energía intercambiada a presión constante, y por otro lado la energía intercambiada por la diferencia de presiones: e q + h ( En el caso del gas ideal la entalpía por mol es h GI 5 R. Según esto, cuando d l se obtiene que q e h R 5 R R, que es el resultado deducido antes. Cuando d l habrá que añadirle el término debido al trabajo a la energía intercambiada, que ser la que tenía la molécula según el principio de equipartición más el trabajo realizado al cruzar el poro: e 3 k B + pv 5 k B. En consecuencia, el calor intercambio desaparece, ya que e R + R 5 R h (por mol y por tanto q e h. Interpretando este calor como la energia de intercambio debido a la diferencia de presión tiene sentido que éste se anule porque las moléculas al colisionar con las otras partículas a su alrededor alcanzan un equilibrio local, anulando la diferencia de presiones..5. Evolución hacia el estado estacionario Ahora inicialmente los dos sistemas contienen el mismo número de moles (ocupan volúmenes idénticos, y se ponen en contacto con una abertura de diámetro d l. La efusión del gas hace evolucionar al sistema desde un estado inicial no estacionario hacia un estado final estacionario descrito por la ecuación 8. Asumiendo equilibio local para cada sistema, con la ley de los gases perfectos y tomando, + con evaluar la variación de la entropía total del sistema S S f S i y la variación de la energía libre de Helmholtz F F f F i, donde los superíndices f e i indican el estado final e inicial respectivamente. Comentar los resultados. En particular discutir el signo de las variaciones de entropía y energía libre. Están de acuerdo con la segunda ley de la termodinámica? La entropía del gas ideal viene dada por la ecuación de Sakur-etrode: [ S GI Nk B ln V N + 3 ( ln πmk B h Nk B ( ln V ln N ln a ] ( (3 Donde a es a πmk B h. En el estado inicial la entropía de los dos sistemas será: S i Nk B (ln V ln N ln a (4 5
6 S i Nk B (ln V ln N ln a( + Nk B (ln V ln N ln a + 3 ( ln + (5 Para calcular la entropía en el estado final estacionario es conveniente conocer el numero de partículas en función de la temperatura. Para lograr esto se utilizarán las siguientes condiciones:. N + N N Condición de sistema cerrado, sin intercambio de materia con fuentes. N i PiV k B i 3. P P Ecuación de estado del gas ideal Relación impuesta por situación estacionaria. Haciendo el cambio de variable x, y teniendo en cuenta que aylor alrededor del punto x. Los desarrollos de aylor que se utilizaran, hasta segundo orden, serán los siguientes: a ( + x + x 8 x + (x 3 b ( + x x x + (x 3 c ( + x x + x + (x 3 d ln ( + x x x + (x 3 Sustituyendo la condición en la 3: N k B V V N N N k B se pueden hacer desarrollos de Empleando ahora la condición, N N N : N N N ( + N N N N N + + Haciendo expansiones de aylor para x hasta segundo orden: N N N + ( + x + ( x x N x x N [ ( x ] x + x 6 Finalmente se obtiene: N N [ + 4 x 8 x ] (6 Utilizando la condición se consigue la correspondiente expresión para N : N N [ 4 x + 8 ] x (7 6
7 .5.. Entropía Sustituyendo estas dos expresiones en la ecuación de la entropía se obtiene el valor de ésta en el estado estacionario: S f Nk B [ + 4 x 8 ] (ln x V ln N ( + 4 x 8 x ln a Nk B [ + 4 x 8 ] (ln x V ln N ln ( + 4 x 8 x ln a Nk B [ + 4 x 8 ] (ln x V ln N [ ln a ( 4 x 8 x ] 6 x Nk B [ + 4 x 8 ] ( x A ( 4 x 5 3 x Nk B [( + 4 x 8 x A 4 x + 3 ] 3 x Se ha hecho el cambio A ln V ln N ln a. Para el otro recipiente sale: S f Nk B [ 4 x + 8 ] (ln x V ln N ( 4 x + 8 x ln a( + Nk B [ 4 x + 8 ] (ln x V ln N ln ( 4 x + 8 x ln a ( + x Nk B [ 4 x + 8 ] (A x + 3 [ ln ( + x ( 4 x + 8 x ] 6 x Nk B [ + 4 x 8 ] ( x A + 3 ln ( + x ( 4 x x Nk B [( + 4 x 8 (A x + 3 ln ( + x + 4 x 5 ] 3 x Nk B [( + 4 x 8 (A x + 3 ln ( + x + 4 x 53 ] x Nk B [( 4 x + 8 (A x + 3 ln ( + x + 4 x 53 ] x (8 (9 Realizando la diferencia en los dos casos se obtiene: S S f Si [( Nk B 4 x 8 x A 4 x + 3 ] 3 x S S f Si Nk B [( 4 x + 8 (A x + Nk B [( 4 x + 8 x A + 4 x 7 ] 3 x 3 x (x + 4 x 53 ] x Sumando esta dos diferencias se consigue la variación de entropía del sistema completo. S S + S ( Nk B 7 x 7 ( ( ( Nk B + (3 (3 (3 7
8 El resultado obtenido puede parecer sorprendente, porque parece que viola el segundo principio de la termodinámica, ya que ha salido S <. Sin embargo, hay que tener en cuenta que el segundo principio establece que la entropía total, la del universo, es la que debe aumentar siempre. En este caso la entropía del sistema es negativa, pero esto es compesado por las fuentes, que al aportar calor producen entropía, de manera que: S universo S sistema + S fuentes > (33 Esto explica la necesidad de fuentes para alcanzar un estado estacionario..5.. Energía Libre de Helmholtz Para conseguir el cambio en la energía libre de Helmholtz utilizaré la variación de energía interna y de la entropía: F U S F U S Para esto hace falta calcular el cambio de la energía interna, que según el principio de equipartición es U 3 Nk B, entre el estado inicial y el estacionario : Restando los dos términos: Haciendo lo mismo para el volumen : U i 3 N U f 3 N k B 3 N U i 3 N U f 3 N k B ( + 3 N k B Haciendo la diferencia: U 3 4 Nk B k B ( + 4 x 8 x k B ( 4 x 8 x k B( + 3 N k B ( + x ( 4 x + 8 x ( + x 3 4 Nk B U 3 4 Nk B ( 4 x 8 x Una vez calculada la energía interna se puede calcular la F de cada recipiente: ( + 34 x 8 x F U S 3 ( 4 Nk B 4 x 8 x [( Nk B 4 x 8 x A 4 x + 33 ] x ( 5 Nk B 8 x 9 3 x ( 4 x 8 x A En el caso del segundo recipiente hay que tener en cuenta que su temperatura es diferente, ( + ( + + x, por lo que tendrá unos términos diferentes que no se anularán al sumar para los dos sistemas: F 3 4 Nk B ( 4 x 8 x ( + x Nk B [( 4 x + 8 x A + 4 x 7 ] 3 x 3 4 Nk B ( 4 x 8 x Nk B [( 4 x + 8 x A + 4 x 7 ] ( 3 x x 4 x 4 xa + (x 3 [ Nk B 5 8 x x ( 4 x + 8 x A + 4 ] Ax (37 8 (34 (35 (36
9 Sumando para los dos volúmenes se consigue: F F + F Nk B ( A x ( 8 Nk B ln V ln N ln πmk ( B h ( 7 8 Nk B 4 + ln V N + 3 ln πmk B h ( ( ( 3 + ( ( 3 + (38 Evaluando el resultado obtenido que claro que F >, ya que aunque aparezcan logaritmos es fácil ver que son mayores que cero. La constante h al cuadrado es mucho menor a k B m, y por ello el tercer término es positivo. Además en el límite termodinámico el segundo término tambi n será positivo, porque V y N son del mismo orden. En un sistema en equilibrio la energía libre tiende al valor mínimo, igual que la entropía se maximiza. Si el sistema estuviera en equilibrio se esperaría que F <, pero como el sistema alcanza un estado estacionario esto no ocurre. Es lo mismo que ocurre con la entropía, que si el estado final fuera el de equilibrio la entropía sería máxima, por tanto S >, pero al ser un estado estacionario se consigue S sist <.. Ejercicio 7: Efecto termomolecular en el gas de Knudsen Se consideran dos recipientes llenos de un gas a temperaturas y concentraciones diferentes, puestos en contacto mediante una abertura de diámetro comparable o menor que el recorrido libre medio. Ésto puede representar una membrana o una superficie porosa. Los dos sistemas están en contacto en presencia de un gradiente de temperatura y concentración (potencial químico. El objetivo del ejercicio es evaluar el calor de transferencia usando la teoría de Onsager. Demostrar que para un sistema multicomponente en presencia de un gradiente de concentración y temperaturas existe una descomposición alternativa de la producción de entropia en términos de flujos y fuerzas o afinidades: Siendo los nuevos flujos y fuerzas: σ J q i J i ( µ i (39 J q J q i h i Ji ; X q X q (4 J i J i ; X i ( µ i Las J y X sin primas son los flujos y fuerzas habituales y las h i son las entalpías parciales, ( ( µi h i ( y el término µi viene definido por: P,n s ( µi h i + ( µ i (4 (4 (43 9
10 La producción de entropia con las fuerzas y flujos habituales se escribe como: σ J q i ( J i µi (44 Dividiendo ( µ i y utilizando las definiciones superiores: σ J q J q ( i i J q i ( J i µi (45 J i ( h i + ( µ i h i Ji i J i ( µ i (46 (47 J q i J i ( µ i (48 Este cambio permite separar el flujo de energia total debido al gradiente de temperatura, que es el flujo de calor entre las fuentes y el flujo de moléculas a través de la abertura. El flujo de energia anterior tenía en cuenta la energia intercambiada al pasar una molécula de un recipiente a otro, y con este cambio se ha conseguido separar completamente los flujos de energia y materia. Para el caso del gas de Knudsen comentado al inicio del ejercicio, demostrar que: σ J q J v m p (49 donde ahora J q, J m son los nuevos flujos de energia y masa por mol del apartado anterior (los primados, v es el volumen molar, y, p son las diferencias de temperatura y presión de los dos sistemas, que suponemos pequeñas comparadas con, p. Comprobar que el flujo de de energia total entre los dos sistemas se puede escribir como: J q de hdn donde de es la transferencia de energia por unidad de tiempo transportada por cada mol que cruza la abertura. Interpretar el significado físico de J q. Que diferencia física hay entre J q y de? Relacionar estos términos con la energia y el calor de transferencia definidos en el ejercicio anterior: e, q. El potencial de químico de un gas ideal se puede escribir de la siguiente manera: (5 µ µ + R ln c µ + R ln n V µ + R ln P R (5 Donde c es la concentración, y se ha utilizando la ecuación de estado del gas ideal. De esta expresión se puede obtener el gradiente a constante: Sustituyendo este resultado: ( µ R p p V p v p (5 n σ J q J q J ( µ i i i J v m p (53
11 Para demostrar 5 se puede calcular explícitamente la producción de entropia e identificar los diferentes términos con los flujos. Considerando ahora un sistema cerrado compuesto por dos recipientes que pueden intercambiar materia y energia (los recipientes serán sistemas abiertos la diferencial de energia se puede escribir como: de dφ pdv (54 Sustituyendo ahora la diferencial de energia interna: de ds pdv + µdn dφ pdv ds dφ µ dn (55 El término dφ se puede dividir en dos contribuciones: el calor que viene del exterior (en esta caso la fuente, y la energia que viene del otro recipiente: dφ dq ext + dφ (56 Con esto y sumando la variación de entropia de los sistemas se pueden identificar los términos que provocan los flujos. eniendo en cuenta que dφ dφ y dn dn dn, es decir, que sin considerar el calor que se intercambia con las fuentes, las partículas y el calor que salgan del primer sistema irán al segundo y viceversa, se consigue: ds dφ µ dn + dφ µ dn (57 dqext + dqext + dφ ds ext + dφ ( + dφ µ dn µ dn (58 ( µ µ dn (59 ds ext dφ ( µ dn (6 Desde esta expresión se pueden identificar los flujos y fuerzas que dan lugar a la producción de entropia para los dos recipientes comparando con la ecuación con los flujos iniciales, antes de realizar el cambio. Sin tener en cuenta el intercambio con el exterior se obtiene para producción de entropia: σ ds i Identificando se consiguen los flujos iniciales: dφ J q J q dφ ( µ J ( m µ dn (6 J m dn (64 Por otro lado, de la ecuación 54 se puede ver que el primer flujo J q es debido a la variación de energia, ya que el volumen del sistema no varía. Identificando dφ con de y separando el calor del exterior del intercambio entre los recipientes la variación de energia es : de dq ext + dφ p dv dq ext + de dq ext (6 (63 + J q (65
12 Separando de nuevo ( µ se podrán conseguir los flujos nuevos, los primados: σ ds i dφ ( µ dn (66 ( dφ h + ( µ dn (67 ( dφ h dn dn ( µ (68 Comparando ahora con la producción de entropia en función de los flujos nuevos (primados: Se identifican: ( dφ σ h dn J q J m ( µ J q dφ J m dn Con el resultado obtenido en la ecuación 65 se consigue: h dn dn ( µ (69 (7 (7 (7 J q dφ h dn de hdn (73 EL J q, que es el J q nuevo, es el intercambio de calor, la energia transferida sin tener en cuenta la debida al cambio de recipiente de la materia. Esta energia es la intercambiada entre las fuentes sin considerar el movimiento de las partículas. Mientras, el viejo era el intercambio de energia, de, que incluye el intercambio de calor y el intercambio de energia debido a la transferencia de materia. En consecuencia, el término J q sería el equivalente a q, es decir: J q q dn (74 y el de está relacionado con e : J q de De estas relaciones se puede deducir directamente: e dn (75 J q q dn de hdn dn e hdn q e h (76 Utilizando la teoría de Onsager expresar los flujos en función de las fuerzas introduciendo coeficientes de Onsager: L qq, L mm, L qm, L mq. J q L qq J m L mq L v qm p (77 L v mm p (78
13 Demostrar que se satisface la relación: ( p J m ( Jq v J m (79 donde los subíndices J m y indican estados estacionarios diferentes. En el primer caso el flujo neto de materia se anula manteniendo diferentes temperaturas, y en el segundo hay un flujo de materia a manteniendo los dos sistemas a la misma temperatura. Si J m, anulando la ecuación 78: L mq L mm v ( p J m Por otro lado, si, dividiendo las expresiones 78 y 77: ( L qm Jq q (8 L mm J m Este cociente representa el flujo de energia por unidad de flujo de masa, y se le suele llamar calor de intercambio. Como los coeficientes de Onsager son simétricos L qm L mq se pueden igualar estas dos expresiones y se consigue demostrar la igualdad 79: v ( p J m ( Jq J m ( p ( Jq J m v J m Utilizando el resultado 8 demostrar que el calor de tranferencia q (calor transferido por unidad de masa por unidad de tiempo es igual a: q R (8 de acuerdo con el resultado. Probar que e q + h para obtener el resultado. Por último evaluar q en el límite donde la abertura es mucho mayor que el recorrido libre medio. La ecuación 8 se puede escribir como: (8 P (83 P omando logaritmos en los dos lados, derivando y sustituyendo la ecuación de estado del gas ideal por mol (piden el calor de intercambio por mol, P V R : ln P ln P ln P ln P (ln ln ln P ln P P P P P R v (84 3
14 La ecuación 8 es válida para el caso estacionario en que el flujo de materia neto es nulo. Por tanto, se puede sustituir este último resultado en la ecuación 8, que debido a la simetría de los coeficientes de Onsager es igual al calor de intercambio por mol: q L qm L ( mq p v v R L mm L mm J m v R (85 Utilizando este resultado, y la entalpía del gas ideal se consigue la transferencia de energia por mol: e q + h R + 5R R (86 Este resultado es equivalente al conseguido en el apartado anterior por cada molécula,, ya que k B N A R. Cuando la abertura es mayor que el recorrido libre medio, d l, tal y como se ha comentado en el ejercicio anterior, el calor de intercambio se anula, porque al cruzar la abertura se realiza un trabajo al chocar antes contra otras partículas que contra las paredes. Debido a esto la energia intercambiada aumenta, y se deja de transferir calor: e R + R 5 R h, y q e h. 3. Aplicaciones Aunque parezca un modelo teórico, el sistema del gas de Knudsen tiene aplicaciones prácticas. El fundamento físico explica se usa en la separación de isótopos, como en el caso de enriquecimiento del Uranio, porque el flujo de moléculas depende de la masa. Recordando la expresión obtenida en el primer K apartado (ecuación : J n n B πm se ve que el flujo depende de la masa. Este hecho provocará una distribución diferente entre los dos recipientes si se colocan dos tipos de elementos diferentes, quedando el más ligero en el sistema más caliente. El mismo principio se utiliza en el proceso de obtención del hidrógeno, para separarlo de la mezcla de gases que se obtiene tras calentarlo. En estos casos se utilizan membranas porosas en lugar de una sola abertura, para poder realizar el proceso con mayor rapidez. Referencias [] Ilya Prigogine: ermodinámica de procesos fuera del equilibrio 4
TEMA 1 Conceptos básicos de la termodinámica
 Bases Físicas y Químicas del Medio Ambiente TEMA 1 Conceptos básicos de la termodinámica La termodinámica es el estudio de la transformación de una forma de energía en otra y del intercambio de energía
Bases Físicas y Químicas del Medio Ambiente TEMA 1 Conceptos básicos de la termodinámica La termodinámica es el estudio de la transformación de una forma de energía en otra y del intercambio de energía
ESTADOS DE AGREGACIÓN DE LA MATERIA
 ESADOS DE AGREGACIÓN DE LA MAERIA. Propiedades generales de la materia La materia es todo aquello que tiene masa y volumen. La masa se define como la cantidad de materia de un cuerpo. Se mide en kg. El
ESADOS DE AGREGACIÓN DE LA MAERIA. Propiedades generales de la materia La materia es todo aquello que tiene masa y volumen. La masa se define como la cantidad de materia de un cuerpo. Se mide en kg. El
Termodinámica y Ondas
 Termodinámica y Ondas Prueba #1 Prof. Andrés Gomberoff Segundo semestre 2015 Ayudante: Constanza Farías 1. Para cierto sistema gaseoso se ha determinado que, para presiones suficientemente grandes (mayores
Termodinámica y Ondas Prueba #1 Prof. Andrés Gomberoff Segundo semestre 2015 Ayudante: Constanza Farías 1. Para cierto sistema gaseoso se ha determinado que, para presiones suficientemente grandes (mayores
ENERGÍA INTERNA PARA GASES NO IDEALES.
 DEPARTAMENTO DE FISICA UNIERSIDAD DE SANTIAGO DE CHILE ENERGÍA INTERNA PARA GASES NO IDEALES. En el caso de los gases ideales o cualquier cuerpo en fase no gaseosa la energía interna es función de la temperatura
DEPARTAMENTO DE FISICA UNIERSIDAD DE SANTIAGO DE CHILE ENERGÍA INTERNA PARA GASES NO IDEALES. En el caso de los gases ideales o cualquier cuerpo en fase no gaseosa la energía interna es función de la temperatura
35 Facultad de Ciencias Universidad de Los Andes Mérida-Venezuela. Potencial Eléctrico
 q 1 q 2 Prof. Félix Aguirre 35 Energía Electrostática Potencial Eléctrico La interacción electrostática es representada muy bien a través de la ley de Coulomb, esto es: mediante fuerzas. Existen, sin embargo,
q 1 q 2 Prof. Félix Aguirre 35 Energía Electrostática Potencial Eléctrico La interacción electrostática es representada muy bien a través de la ley de Coulomb, esto es: mediante fuerzas. Existen, sin embargo,
Ayudantía 6 - Soluciones 2da Ley de la Termodinámica y Condiciones de Equilibrio
 Ponticia Universidad Católica de Chile Facultad de Física Termodinámica y Teoría Cinética: Fiz 02 Ayudantía 6 - Soluciones 2da Ley de la Termodinámica y Condiciones de Equilibrio Profesor: Miguel Kiwi
Ponticia Universidad Católica de Chile Facultad de Física Termodinámica y Teoría Cinética: Fiz 02 Ayudantía 6 - Soluciones 2da Ley de la Termodinámica y Condiciones de Equilibrio Profesor: Miguel Kiwi
Unidad IV: Cinética química
 63 Unidad IV: Cinética química El objetivo de la cinética química es el estudio de las velocidades de las reacciones químicas y de los factores de los que dependen dichas velocidades. De estos factores,
63 Unidad IV: Cinética química El objetivo de la cinética química es el estudio de las velocidades de las reacciones químicas y de los factores de los que dependen dichas velocidades. De estos factores,
INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA. La mecánica cuántica estudia la estructura atómica, los enlaces en moléculas y la espectroscopia.
 INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA 1. Qué es la Química Física? "La química física estudia los principios que gobiernan las propiedades el comportamiento de los sistemas químicos" El estudio de los
INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA 1. Qué es la Química Física? "La química física estudia los principios que gobiernan las propiedades el comportamiento de los sistemas químicos" El estudio de los
Solubilidad. y se representa por.
 Solubilidad Solubilidad. La solubilidad mide la cantidad máxima de soluto capaz de disolverse en una cantidad definida de disolvente, a una temperatura determinada, y formar un sistema estable que se denomina
Solubilidad Solubilidad. La solubilidad mide la cantidad máxima de soluto capaz de disolverse en una cantidad definida de disolvente, a una temperatura determinada, y formar un sistema estable que se denomina
LEYES DE CONSERVACIÓN: ENERGÍA Y MOMENTO
 LEYES DE CONSERVACIÓN: ENERGÍA Y MOMENTO 1. Trabajo mecánico y energía. El trabajo, tal y como se define físicamente, es una magnitud diferente de lo que se entiende sensorialmente por trabajo. Trabajo
LEYES DE CONSERVACIÓN: ENERGÍA Y MOMENTO 1. Trabajo mecánico y energía. El trabajo, tal y como se define físicamente, es una magnitud diferente de lo que se entiende sensorialmente por trabajo. Trabajo
DRAFT. Trabajo, Calor y Primer Principio de la Termodinámica.
 DRAFT Trabajo, Calor y Primer Principio de la Termodinámica. J.V. Alvarez Departmento de Fisica de la Materia Condensada, Universidad Autonoma de Madrid. 28049 Madrid, Spain. (Dated: October 10, 2007)
DRAFT Trabajo, Calor y Primer Principio de la Termodinámica. J.V. Alvarez Departmento de Fisica de la Materia Condensada, Universidad Autonoma de Madrid. 28049 Madrid, Spain. (Dated: October 10, 2007)
Funciones de varias variables
 Funciones de varias variables Derivadas parciales. El concepto de función derivable no se puede extender de una forma sencilla para funciones de varias variables. Aquí se emplea el concepto de diferencial
Funciones de varias variables Derivadas parciales. El concepto de función derivable no se puede extender de una forma sencilla para funciones de varias variables. Aquí se emplea el concepto de diferencial
Física Estadística. Tarea 8. A entregar: Miércoles 29 de abril de 2015.
 Física Estadística Tarea 8 A entregar: Miércoles 29 de abril de 2015. Una manera alternativa de deducir las distribuciones de Bose- Einstein y Fermi-Dirac... y Maxwell-Boltzmann. En algunos textos todavía
Física Estadística Tarea 8 A entregar: Miércoles 29 de abril de 2015. Una manera alternativa de deducir las distribuciones de Bose- Einstein y Fermi-Dirac... y Maxwell-Boltzmann. En algunos textos todavía
Ecuaciones de primer grado con dos incógnitas
 Ecuaciones de primer grado con dos incógnitas Si decimos: "las edades de mis padres suman 120 años", podemos expresar esta frase algebraicamente de la siguiente forma: Entonces, Denominamos x a la edad
Ecuaciones de primer grado con dos incógnitas Si decimos: "las edades de mis padres suman 120 años", podemos expresar esta frase algebraicamente de la siguiente forma: Entonces, Denominamos x a la edad
CESMA BUSINESS SCHOOL MATEMÁTICAS FINANCIERAS. TEMA 3 CAPITALIZACIÓN COMPUESTA
 CESMA BUSINESS SCHOOL MATEMÁTICAS FINANCIERAS. TEMA 3 CAPITALIZACIÓN COMPUESTA Javier Bilbao García 1 1.- Capitalización Compuesta Definición: Operación financiera que persigue sustituir un capital por
CESMA BUSINESS SCHOOL MATEMÁTICAS FINANCIERAS. TEMA 3 CAPITALIZACIÓN COMPUESTA Javier Bilbao García 1 1.- Capitalización Compuesta Definición: Operación financiera que persigue sustituir un capital por
Problemas de Física 1 o Bachillerato
 Problemas de Física o Bachillerato Principio de conservación de la energía mecánica. Desde una altura h dejamos caer un cuerpo. Hallar en qué punto de su recorrido se cumple E c = 4 E p 2. Desde la parte
Problemas de Física o Bachillerato Principio de conservación de la energía mecánica. Desde una altura h dejamos caer un cuerpo. Hallar en qué punto de su recorrido se cumple E c = 4 E p 2. Desde la parte
Bases Físicas del Medio Ambiente. Sistemas Termodinámicos
 Bases Físicas del Medio Ambiente Sistemas Termodinámicos Programa VII. SISTEMAS TERMODINÁMICOS. (1h) Introducción. Sistema termodinámico. Estados de equilibrio. Procesos termodinámicos. Equilibrio termodinámico.
Bases Físicas del Medio Ambiente Sistemas Termodinámicos Programa VII. SISTEMAS TERMODINÁMICOS. (1h) Introducción. Sistema termodinámico. Estados de equilibrio. Procesos termodinámicos. Equilibrio termodinámico.
Apuntes de Matemática Discreta 9. Funciones
 Apuntes de Matemática Discreta 9. Funciones Francisco José González Gutiérrez Cádiz, Octubre de 004 Universidad de Cádiz Departamento de Matemáticas ii Lección 9 Funciones Contenido 9.1 Definiciones y
Apuntes de Matemática Discreta 9. Funciones Francisco José González Gutiérrez Cádiz, Octubre de 004 Universidad de Cádiz Departamento de Matemáticas ii Lección 9 Funciones Contenido 9.1 Definiciones y
TIPO DE CAMBIO, TIPOS DE INTERES Y MOVIMIENTOS DE CAPITAL
 TIPO DE CAMBIO, TIPOS DE INTERES Y MOVIMIENTOS DE CAPITAL En esta breve nota se intentan analizar las relaciones existentes en el sector español entre tipo de cambio, tasa de inflación y tipos de interés,
TIPO DE CAMBIO, TIPOS DE INTERES Y MOVIMIENTOS DE CAPITAL En esta breve nota se intentan analizar las relaciones existentes en el sector español entre tipo de cambio, tasa de inflación y tipos de interés,
Turbinas de vapor. Introducción
 Turbinas de vapor Introducción La turbina de vapor es una máquina de fluido en la que la energía de éste pasa al eje de la máquina saliendo el fluido de ésta con menor cantidad de energía. La energía mecánica
Turbinas de vapor Introducción La turbina de vapor es una máquina de fluido en la que la energía de éste pasa al eje de la máquina saliendo el fluido de ésta con menor cantidad de energía. La energía mecánica
4 Pruebas y análisis del software
 4 Pruebas y análisis del software En este capítulo se presentan una serie de simulaciones donde se analiza el desempeño de ambos sistemas programados en cuanto a exactitud con otros softwares que se encuentran
4 Pruebas y análisis del software En este capítulo se presentan una serie de simulaciones donde se analiza el desempeño de ambos sistemas programados en cuanto a exactitud con otros softwares que se encuentran
Transformación de trabajo en calor y calor en trabajo. Motores y Frigoríficos.
 Transformación de trabajo en calor y calor en trabajo Motores y Frigoríficos. De lo expuesto, se debe concluir que cualquier sistema que este expuesto al intercambio de trabajo y calor con el exterior
Transformación de trabajo en calor y calor en trabajo Motores y Frigoríficos. De lo expuesto, se debe concluir que cualquier sistema que este expuesto al intercambio de trabajo y calor con el exterior
Determinación del calor latente de fusión del hielo
 Determinación del calor latente de usión del hielo Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica
Determinación del calor latente de usión del hielo Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica
Función exponencial y Logaritmos
 Eje temático: Álgebra y funciones Contenidos: Función exponencial y Logaritmos Nivel: 4 Medio Función exponencial y Logaritmos 1. Funciones exponenciales Existen numerosos fenómenos que se rigen por leyes
Eje temático: Álgebra y funciones Contenidos: Función exponencial y Logaritmos Nivel: 4 Medio Función exponencial y Logaritmos 1. Funciones exponenciales Existen numerosos fenómenos que se rigen por leyes
Tema 2. Espacios Vectoriales. 2.1. Introducción
 Tema 2 Espacios Vectoriales 2.1. Introducción Estamos habituados en diferentes cursos a trabajar con el concepto de vector. Concretamente sabemos que un vector es un segmento orientado caracterizado por
Tema 2 Espacios Vectoriales 2.1. Introducción Estamos habituados en diferentes cursos a trabajar con el concepto de vector. Concretamente sabemos que un vector es un segmento orientado caracterizado por
A continuación voy a colocar las fuerzas que intervienen en nuestro problema.
 ísica EL PLANO INCLINADO Supongamos que tenemos un plano inclinado. Sobre él colocamos un cubo, de manera que se deslice sobre la superficie hasta llegar al plano horizontal. Vamos a suponer que tenemos
ísica EL PLANO INCLINADO Supongamos que tenemos un plano inclinado. Sobre él colocamos un cubo, de manera que se deslice sobre la superficie hasta llegar al plano horizontal. Vamos a suponer que tenemos
f( x) = ( x)2 + 11 x + 5 = 0 = x2 + 11 = 0 = No hay solución y = 0 + 11 0 + 5 = 11
 1. y = x + 11 x + 5 a) ESTUDIO DE f: 1) Dominio: Como es un cociente del dominio habrá que excluir los valores que anulen el denominador. Por tanto: x + 5 = 0 x = 5 ) Simetría: A simple vista, como el
1. y = x + 11 x + 5 a) ESTUDIO DE f: 1) Dominio: Como es un cociente del dominio habrá que excluir los valores que anulen el denominador. Por tanto: x + 5 = 0 x = 5 ) Simetría: A simple vista, como el
Profr. Efraín Soto Apolinar. La función lineal. y = a 0 + a 1 x. y = m x + b
 La función lineal Una función polinomial de grado uno tiene la forma: y = a 0 + a 1 x El semestre pasado estudiamos la ecuación de la recta. y = m x + b En la notación de funciones polinomiales, el coeficiente
La función lineal Una función polinomial de grado uno tiene la forma: y = a 0 + a 1 x El semestre pasado estudiamos la ecuación de la recta. y = m x + b En la notación de funciones polinomiales, el coeficiente
Potencial eléctrico. du = - F dl
 Introducción Como la fuerza gravitatoria, la fuerza eléctrica es conservativa. Existe una función energía potencial asociada con la fuerza eléctrica. Como veremos, la energía potencial asociada a una partícula
Introducción Como la fuerza gravitatoria, la fuerza eléctrica es conservativa. Existe una función energía potencial asociada con la fuerza eléctrica. Como veremos, la energía potencial asociada a una partícula
ACCIONES Y OTROS TÍTULOS DE INVERSIÓN
 ACCIONES Y OTROS TÍTULOS DE INVERSIÓN TASAS EFECTIVAS DE RENDIMIENTO ANUAL Y MENSUAL: Es aquélla que se emplea en la compraventa de algunos valores en el Mercado Bursátil o Bolsa de Valores. Estas tasas
ACCIONES Y OTROS TÍTULOS DE INVERSIÓN TASAS EFECTIVAS DE RENDIMIENTO ANUAL Y MENSUAL: Es aquélla que se emplea en la compraventa de algunos valores en el Mercado Bursátil o Bolsa de Valores. Estas tasas
Aproximación local. Plano tangente. Derivadas parciales.
 Univ. de Alcalá de Henares Ingeniería de Telecomunicación Cálculo. Segundo parcial. Curso 004-005 Aproximación local. Plano tangente. Derivadas parciales. 1. Plano tangente 1.1. El problema de la aproximación
Univ. de Alcalá de Henares Ingeniería de Telecomunicación Cálculo. Segundo parcial. Curso 004-005 Aproximación local. Plano tangente. Derivadas parciales. 1. Plano tangente 1.1. El problema de la aproximación
MEDIDA DE LA VELOCIDAD DEL SONIDO. TUBO DE RESONANCIA
 eman ta zabal zazu Departamento de Física de la Materia Condensada universidad del país vasco euskal herriko unibertsitatea FACULTAD DE CIENCIA Y TECNOLOGÍA UNIVERSIDAD DEL PAÍS VASCO DEPARTAMENTO de FÍSICA
eman ta zabal zazu Departamento de Física de la Materia Condensada universidad del país vasco euskal herriko unibertsitatea FACULTAD DE CIENCIA Y TECNOLOGÍA UNIVERSIDAD DEL PAÍS VASCO DEPARTAMENTO de FÍSICA
Análisis de los datos
 Universidad Complutense de Madrid CURSOS DE FORMACIÓN EN INFORMÁTICA Análisis de los datos Hojas de cálculo Tema 6 Análisis de los datos Una de las capacidades más interesantes de Excel es la actualización
Universidad Complutense de Madrid CURSOS DE FORMACIÓN EN INFORMÁTICA Análisis de los datos Hojas de cálculo Tema 6 Análisis de los datos Una de las capacidades más interesantes de Excel es la actualización
ORGANIZACIÓN INDUSTRIAL (16691-ECO) PARTE II: MODELOS DE COMPETENCIA IMPERFECTA TEMA 2: EL MONOPOLIO SOLUCIÓN A LOS PROBLEMAS PROPUESTOS
 ORGANIZACIÓN INDUSTRIAL (16691-ECO) PARTE II: MODELOS DE COMPETENCIA IMPERFECTA TEMA 2: EL MONOPOLIO 2.1 ANÁLISIS DE EQUILIBRIO 2.2. DISCRIMINACIÓN DE PRECIOS Y REGULACIÓN SOLUCIÓN A LOS PROBLEMAS PROPUESTOS
ORGANIZACIÓN INDUSTRIAL (16691-ECO) PARTE II: MODELOS DE COMPETENCIA IMPERFECTA TEMA 2: EL MONOPOLIO 2.1 ANÁLISIS DE EQUILIBRIO 2.2. DISCRIMINACIÓN DE PRECIOS Y REGULACIÓN SOLUCIÓN A LOS PROBLEMAS PROPUESTOS
EFECTO JOULE-THOMSON
 PRACTICA nº 4 EFECTO JOULE-THOMSON Fundamentos teóricos El proceso de Joule-Thomson consiste en el paso de un gas desde un contenedor a presión constante a otro a presión también constante y menor (Pf
PRACTICA nº 4 EFECTO JOULE-THOMSON Fundamentos teóricos El proceso de Joule-Thomson consiste en el paso de un gas desde un contenedor a presión constante a otro a presión también constante y menor (Pf
UNIDAD 1. LOS NÚMEROS ENTEROS.
 UNIDAD 1. LOS NÚMEROS ENTEROS. Al final deberás haber aprendido... Interpretar y expresar números enteros. Representar números enteros en la recta numérica. Comparar y ordenar números enteros. Realizar
UNIDAD 1. LOS NÚMEROS ENTEROS. Al final deberás haber aprendido... Interpretar y expresar números enteros. Representar números enteros en la recta numérica. Comparar y ordenar números enteros. Realizar
La derivada de y respecto a x es lo que varía y por cada unidad que varía x. Ese valor se designa por dy dx.
 Conceptos de derivada y de diferencial Roberto C. Redondo Melchor, Norberto Redondo Melchor, Félix Redondo Quintela 1 Universidad de Salamanca 18 de agosto de 2012 v1.3: 17 de septiembre de 2012 Aunque
Conceptos de derivada y de diferencial Roberto C. Redondo Melchor, Norberto Redondo Melchor, Félix Redondo Quintela 1 Universidad de Salamanca 18 de agosto de 2012 v1.3: 17 de septiembre de 2012 Aunque
EJERCICIOS DE MATEMÁTICAS I HOJA 4. Ejercicio 1. Se consideran los vectores
 EJERCICIOS DE MATEMÁTICAS I HOJA 4 Ejercicio 1. Se consideran los vectores u 1 = (1, 1, 0, 1), u 2 = (0, 2, 1, 0), u 3 = ( 1, 1, 1, 1), u 4 = (2, 2, 1, 0) de R 4. Expresa, si es posible, los vectores u
EJERCICIOS DE MATEMÁTICAS I HOJA 4 Ejercicio 1. Se consideran los vectores u 1 = (1, 1, 0, 1), u 2 = (0, 2, 1, 0), u 3 = ( 1, 1, 1, 1), u 4 = (2, 2, 1, 0) de R 4. Expresa, si es posible, los vectores u
Características de funciones que son inversas de otras
 Características de funciones que son inversas de otras Si f es una función inyectiva, llamamos función inversa de f y se representa por f 1 al conjunto. f 1 = a, b b, a f} Es decir, f 1 (x, y) = { x =
Características de funciones que son inversas de otras Si f es una función inyectiva, llamamos función inversa de f y se representa por f 1 al conjunto. f 1 = a, b b, a f} Es decir, f 1 (x, y) = { x =
RESPUESTAS A LAS PREGUNTAS DEL TEMA 3
 RESPUESTAS A LAS PREGUNTAS DEL TEMA 3 Las respuestas en algún caso (primera pregunta) son más largas de lo requerido para que sirva de explicación 1. Explica brevemente qué significan cada una de las curvas
RESPUESTAS A LAS PREGUNTAS DEL TEMA 3 Las respuestas en algún caso (primera pregunta) son más largas de lo requerido para que sirva de explicación 1. Explica brevemente qué significan cada una de las curvas
Datos del autor. Nombres y apellido: Germán Andrés Paz. Lugar de nacimiento: Rosario (Código Postal 2000), Santa Fe, Argentina
 Datos del autor Nombres y apellido: Germán Andrés Paz Lugar de nacimiento: Rosario (Código Postal 2000), Santa Fe, Argentina Correo electrónico: germanpaz_ar@hotmail.com =========0========= Introducción
Datos del autor Nombres y apellido: Germán Andrés Paz Lugar de nacimiento: Rosario (Código Postal 2000), Santa Fe, Argentina Correo electrónico: germanpaz_ar@hotmail.com =========0========= Introducción
1. Números Reales 1.1 Clasificación y propiedades
 1. Números Reales 1.1 Clasificación y propiedades 1.1.1 Definición Número real, cualquier número racional o irracional. Los números reales pueden expresarse en forma decimal mediante un número entero,
1. Números Reales 1.1 Clasificación y propiedades 1.1.1 Definición Número real, cualquier número racional o irracional. Los números reales pueden expresarse en forma decimal mediante un número entero,
ENERGÍA INTERNA DE UN SISTEMA
 ENERGÍA INTERNA DE UN SISTEMA Definimos energía interna U de un sistema la suma de las energías cinéticas de todas sus partículas constituyentes, más la suma de todas las energías de interacción entre
ENERGÍA INTERNA DE UN SISTEMA Definimos energía interna U de un sistema la suma de las energías cinéticas de todas sus partículas constituyentes, más la suma de todas las energías de interacción entre
MATEMÁTICAS para estudiantes de primer curso de facultades y escuelas técnicas
 Universidad de Cádiz Departamento de Matemáticas MATEMÁTICAS para estudiantes de primer curso de facultades y escuelas técnicas Tema Representación gráfica de funciones reales de una variable real Elaborado
Universidad de Cádiz Departamento de Matemáticas MATEMÁTICAS para estudiantes de primer curso de facultades y escuelas técnicas Tema Representación gráfica de funciones reales de una variable real Elaborado
Problemas de Complementos de Matemáticas. Curso 01/02
 Problemas de Complementos de Matemáticas. Curso /2.- Resolver las E.D.O. lineales de primer orden siguientes y los problemas de condiciones x + 3x/t = 6t 2 x + 3x = 3t 2 e 3t t 4 x + 2t 3 x = tx + (tx
Problemas de Complementos de Matemáticas. Curso /2.- Resolver las E.D.O. lineales de primer orden siguientes y los problemas de condiciones x + 3x/t = 6t 2 x + 3x = 3t 2 e 3t t 4 x + 2t 3 x = tx + (tx
TEMA II.6. Variación de la Presión con la Elevación. Dr. Juan Pablo Torres-Papaqui
 TEMA II.6 Variación de la Presión con la Elevación Dr. Juan Pablo Torres-Papaqui Departamento de Astronomía Universidad de Guanajuato DA-UG (México) papaqui@astro.ugto.mx División de Ciencias Naturales
TEMA II.6 Variación de la Presión con la Elevación Dr. Juan Pablo Torres-Papaqui Departamento de Astronomía Universidad de Guanajuato DA-UG (México) papaqui@astro.ugto.mx División de Ciencias Naturales
La crisis de la Energía
 La crisis de la Energía Por Renato IRALDI Modelos de consumo energético bpe = bep= Barriles de petróleo equivalente = Energia producida por un barril de petróleo Suposiciones: Suponemos que los combustibles
La crisis de la Energía Por Renato IRALDI Modelos de consumo energético bpe = bep= Barriles de petróleo equivalente = Energia producida por un barril de petróleo Suposiciones: Suponemos que los combustibles
Fundamentos de la Mecánica Estadística (la explicación microscópica de la Termodinámica)
 Fundamentos de la Mecánica Estadística (la explicación microscópica de la Termodinámica) C. Dib Depto de Física, Universidad Técnica Federico Santa María, Valparaíso, Chile (Dated: June 16, 21) La Termodinámica
Fundamentos de la Mecánica Estadística (la explicación microscópica de la Termodinámica) C. Dib Depto de Física, Universidad Técnica Federico Santa María, Valparaíso, Chile (Dated: June 16, 21) La Termodinámica
ANÁLISIS ECONÓMICO DE INVERSIONES.
 ANÁLISIS ECONÓMICO DE INVERSIONES. José Ignacio González Soriano Agosto 2013 INDICE 1. FORMULAS FINANCIERAS.... 2 1.1.- VALOR ACTUAL NETO.... 3 1.1.1.- DEFINICIÓN... 3 1.1.2.- CASO GENERAL... 3 1.1.3.-
ANÁLISIS ECONÓMICO DE INVERSIONES. José Ignacio González Soriano Agosto 2013 INDICE 1. FORMULAS FINANCIERAS.... 2 1.1.- VALOR ACTUAL NETO.... 3 1.1.1.- DEFINICIÓN... 3 1.1.2.- CASO GENERAL... 3 1.1.3.-
CASO PRÁCTICO. ANÁLISIS DE DATOS EN TABLAS DINÁMICAS
 CASO PRÁCTICO. ANÁLISIS DE DATOS EN TABLAS DINÁMICAS Nuestra empresa es una pequeña editorial que maneja habitualmente su lista de ventas en una hoja de cálculo y desea poder realizar un análisis de sus
CASO PRÁCTICO. ANÁLISIS DE DATOS EN TABLAS DINÁMICAS Nuestra empresa es una pequeña editorial que maneja habitualmente su lista de ventas en una hoja de cálculo y desea poder realizar un análisis de sus
EL FONDO DE MANIOBRA Y LAS NECESIDADES OPERATIVAS DE FONDOS
 2 EL FONDO DE MANIOBRA Y LAS NECESIDADES OPERATIVAS DE FONDOS Las inversiones de una empresa están reflejadas en su activo. Una forma de clasificación de las diferentes inversiones es en función del plazo
2 EL FONDO DE MANIOBRA Y LAS NECESIDADES OPERATIVAS DE FONDOS Las inversiones de una empresa están reflejadas en su activo. Una forma de clasificación de las diferentes inversiones es en función del plazo
4º ESO 1. ECUAC. 2º GRADO Y UNA INCÓGNITA
 4º ESO 1. ECUAC. 2º GRADO Y UNA INCÓGNITA Una ecuación con una incógnita es de segundo grado si el exponente de la incógnita es dos. Ecuaciones de segundo grado con una incógnita son: Esta última ecuación
4º ESO 1. ECUAC. 2º GRADO Y UNA INCÓGNITA Una ecuación con una incógnita es de segundo grado si el exponente de la incógnita es dos. Ecuaciones de segundo grado con una incógnita son: Esta última ecuación
TRABAJO. ENERGÍA. PRINCIPIO DE CONSERVACIÓN
 TRABAJO. ENERGÍA. PRINCIPIO DE CONSERVACIÓN Un coche de 50 kg (con el conductor incluido) que funciona con gasolina está situado en una carretera horizontal, arranca y acelerando uniformemente, alcanza
TRABAJO. ENERGÍA. PRINCIPIO DE CONSERVACIÓN Un coche de 50 kg (con el conductor incluido) que funciona con gasolina está situado en una carretera horizontal, arranca y acelerando uniformemente, alcanza
CURSO BÁSICO DE MATEMÁTICAS PARA ESTUDIANTES DE ECONÓMICAS Y EMPRESARIALES
 INECUACIONES NOTA IMPORTANTE: El signo de desigualdad de una inecuación puede ser,, < o >. Para las cuestiones teóricas que se desarrollan en esta unidad únicamente se utilizará la desigualdad >, siendo
INECUACIONES NOTA IMPORTANTE: El signo de desigualdad de una inecuación puede ser,, < o >. Para las cuestiones teóricas que se desarrollan en esta unidad únicamente se utilizará la desigualdad >, siendo
Introdución a la capa límite laminar bidimensional y estacionaria
 Introdución a la capa límite laminar bidimensional y estacionaria M. Rodríguez 1 Introducción En los movimientos a altos números de Reynolds (basado en la longitud característica del movimiento), los efectos
Introdución a la capa límite laminar bidimensional y estacionaria M. Rodríguez 1 Introducción En los movimientos a altos números de Reynolds (basado en la longitud característica del movimiento), los efectos
Qué son los monomios?
 Qué son los monomios? Recordemos qué es una expresión algebraica. Definición Una expresión algebraica es aquella en la que se utilizan letras, números y signos de operaciones. Si se observan las siguientes
Qué son los monomios? Recordemos qué es una expresión algebraica. Definición Una expresión algebraica es aquella en la que se utilizan letras, números y signos de operaciones. Si se observan las siguientes
ANÁLISIS DE DATOS NO NUMERICOS
 ANÁLISIS DE DATOS NO NUMERICOS ESCALAS DE MEDIDA CATEGORICAS Jorge Galbiati Riesco Los datos categóricos son datos que provienen de resultados de experimentos en que sus resultados se miden en escalas
ANÁLISIS DE DATOS NO NUMERICOS ESCALAS DE MEDIDA CATEGORICAS Jorge Galbiati Riesco Los datos categóricos son datos que provienen de resultados de experimentos en que sus resultados se miden en escalas
Master de Negocios y Alta Dirección 2008
 Master de Negocios y Alta Dirección 2008 RATIOS DE EJEMPLO:. 1.- Ratios de Actividad. a) Crecimiento de la cifra de ventas. b) Rotación de los activos. c) Rotación de Activos fijos. d) Crecimiento del
Master de Negocios y Alta Dirección 2008 RATIOS DE EJEMPLO:. 1.- Ratios de Actividad. a) Crecimiento de la cifra de ventas. b) Rotación de los activos. c) Rotación de Activos fijos. d) Crecimiento del
a < b y se lee "a es menor que b" (desigualdad estricta) a > b y se lee "a es mayor que b" (desigualdad estricta)
 Desigualdades Dadas dos rectas que se cortan, llamadas ejes (rectangulares si son perpendiculares, y oblicuos en caso contrario), un punto puede situarse conociendo las distancias del mismo a los ejes,
Desigualdades Dadas dos rectas que se cortan, llamadas ejes (rectangulares si son perpendiculares, y oblicuos en caso contrario), un punto puede situarse conociendo las distancias del mismo a los ejes,
Problema 1: Cinemática
 7 ma OMF 0 de septiembre de 203 Problema : Cinemática Pregunta : La velocidad de A al chocar con B podemos calcularla mediante conservación de la energía. Como toda la energía potencial se transforma en
7 ma OMF 0 de septiembre de 203 Problema : Cinemática Pregunta : La velocidad de A al chocar con B podemos calcularla mediante conservación de la energía. Como toda la energía potencial se transforma en
Definición de vectores
 Definición de vectores Un vector es todo segmento de recta dirigido en el espacio. Cada vector posee unas características que son: Origen: O también denominado Punto de aplicación. Es el punto exacto sobre
Definición de vectores Un vector es todo segmento de recta dirigido en el espacio. Cada vector posee unas características que son: Origen: O también denominado Punto de aplicación. Es el punto exacto sobre
Apunte LTspice: Acoplamiento magnético y transformadores
 Apunte LTspice: Acoplamiento magnético y transformadores Ayudante: Marco Guerrero Ilufi - Felipe Vega Prado Contacto: m.guerrero144@gmail.com - felipe.vegapr@gmail.com 2 de junio de 2011 Introducción En
Apunte LTspice: Acoplamiento magnético y transformadores Ayudante: Marco Guerrero Ilufi - Felipe Vega Prado Contacto: m.guerrero144@gmail.com - felipe.vegapr@gmail.com 2 de junio de 2011 Introducción En
EJEMPLO 2: Ing. Mario René De León García. 1. FUNCIÓN EXPONENCIAL EJEMPLO 1:
 FUNCIONES EXPONENCIAL Y LOGARÍTMICA Por: Ing. Mario René De León García.. FUNCIÓN EXPONENCIAL Una función eponencial tiene la forma, donde a es la base de la potencia la variable es el eponente. Esta función
FUNCIONES EXPONENCIAL Y LOGARÍTMICA Por: Ing. Mario René De León García.. FUNCIÓN EXPONENCIAL Una función eponencial tiene la forma, donde a es la base de la potencia la variable es el eponente. Esta función
CHOQUE.(CANTIDAD DE MOVIMIENTO )
 APUNTES Materia: Tema: Curso: Física y Química Momento Lineal 4º ESO CHOQUE.(CANTIDAD DE MOVIMIENTO ) CANTIDAD DE MOVIMIENTO Si un cuerpo de masa m se está moviendo con velocidad v, la cantidad de movimiento
APUNTES Materia: Tema: Curso: Física y Química Momento Lineal 4º ESO CHOQUE.(CANTIDAD DE MOVIMIENTO ) CANTIDAD DE MOVIMIENTO Si un cuerpo de masa m se está moviendo con velocidad v, la cantidad de movimiento
Covarianza y coeficiente de correlación
 Covarianza y coeficiente de correlación Cuando analizábamos las variables unidimensionales considerábamos, entre otras medidas importantes, la media y la varianza. Ahora hemos visto que estas medidas también
Covarianza y coeficiente de correlación Cuando analizábamos las variables unidimensionales considerábamos, entre otras medidas importantes, la media y la varianza. Ahora hemos visto que estas medidas también
MACROECONOMÍA. Tema 6 El comercio internacional. - MACROECONOMÍA -
 MACROECONOMÍA Tema 6 El comercio internacional. Introducción. En este tema vamos tratar de responder a las siguientes cuestiones: por qué los países comercian entre sí? quién gana y quién pierde con el
MACROECONOMÍA Tema 6 El comercio internacional. Introducción. En este tema vamos tratar de responder a las siguientes cuestiones: por qué los países comercian entre sí? quién gana y quién pierde con el
XVI Olimpíada Iberoamericana de Física ECUADOR 2011 Prueba Teórica 1 26 septiembre 2011 01 de Octubre 2011. Energía de las Olas
 Prueba Teórica 1 Energía de las Olas Durante muchos años investigadores han intentado desarrollar un aparato para extraer la energía de las olas del mar. De los métodos usados el más simple consiste en
Prueba Teórica 1 Energía de las Olas Durante muchos años investigadores han intentado desarrollar un aparato para extraer la energía de las olas del mar. De los métodos usados el más simple consiste en
Un problema sobre repetidas apuestas al azar
 Un problema sobre repetidas apuestas al azar Eleonora Catsigeras 1 10 de marzo de 2003. Resumen En estas notas se da el enunciado y una demostración de un conocido resultado sobre la probabilidad de éxito
Un problema sobre repetidas apuestas al azar Eleonora Catsigeras 1 10 de marzo de 2003. Resumen En estas notas se da el enunciado y una demostración de un conocido resultado sobre la probabilidad de éxito
MANUAL DE PROCEDIMIENTO PARA LA INSTALACION Y CONTROL DE ECO-CAR
 MANUAL DE PROCEDIMIENTO PARA LA INSTALACION Y CONTROL DE ECO-CAR A/ INSTALACION. Para una óptima instalación del dispositivo Eco-car se deben observar las siguientes pautas: 1.- El dispositivo debe estar
MANUAL DE PROCEDIMIENTO PARA LA INSTALACION Y CONTROL DE ECO-CAR A/ INSTALACION. Para una óptima instalación del dispositivo Eco-car se deben observar las siguientes pautas: 1.- El dispositivo debe estar
Laboratorio 4. Cocientes de capacidades de calor de gases
 Laboratorio 4. Cocientes de capacidades de calor de gases Objetivo Determinar el cociente de capacidades de calor () para gases como dióxido de carbono (CO ) y nitrógeno (N ) utilizando la expansión adiabática.
Laboratorio 4. Cocientes de capacidades de calor de gases Objetivo Determinar el cociente de capacidades de calor () para gases como dióxido de carbono (CO ) y nitrógeno (N ) utilizando la expansión adiabática.
1. INTRODUCCIÓN 1.1 INGENIERÍA
 1. INTRODUCCIÓN 1.1 INGENIERÍA Es difícil dar una explicación de ingeniería en pocas palabras, pues se puede decir que la ingeniería comenzó con el hombre mismo, pero se puede intentar dar un bosquejo
1. INTRODUCCIÓN 1.1 INGENIERÍA Es difícil dar una explicación de ingeniería en pocas palabras, pues se puede decir que la ingeniería comenzó con el hombre mismo, pero se puede intentar dar un bosquejo
EL ESTADO DE ORIGEN Y APLICACION DE FONDOS
 El estado de origen y aplicación de fondos EL ESTADO DE ORIGEN Y APLICACION DE FONDOS 1.- Introducción.- Como se indicó al tratar la cuenta de resultados, la misma es la expresión contable del movimiento
El estado de origen y aplicación de fondos EL ESTADO DE ORIGEN Y APLICACION DE FONDOS 1.- Introducción.- Como se indicó al tratar la cuenta de resultados, la misma es la expresión contable del movimiento
UNIDAD 1 LAS LEYES FINANCIERAS DE CAPITALIZACIÓN DESCUENTO
 - 1 - UNIDAD 1 LAS LEYES FINANCIERAS DE CAPITALIZACIÓN Y DESCUENTO Tema 1: Operaciones financieras: elementos Tema 2: Capitalización y descuento simple Tema 3: Capitalización y descuento compuesto Tema
- 1 - UNIDAD 1 LAS LEYES FINANCIERAS DE CAPITALIZACIÓN Y DESCUENTO Tema 1: Operaciones financieras: elementos Tema 2: Capitalización y descuento simple Tema 3: Capitalización y descuento compuesto Tema
EJERCICIOS SOBRE : NÚMEROS ENTEROS
 1.- Magnitudes Absolutas y Relativas: Se denomina magnitud a todo lo que se puede medir cuantitativamente. Ejemplo: peso de un cuerpo, longitud de una cuerda, capacidad de un recipiente, el tiempo que
1.- Magnitudes Absolutas y Relativas: Se denomina magnitud a todo lo que se puede medir cuantitativamente. Ejemplo: peso de un cuerpo, longitud de una cuerda, capacidad de un recipiente, el tiempo que
0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 Entropía s [KJ/Kg.ºK]
![0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 Entropía s [KJ/Kg.ºK] 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 Entropía s [KJ/Kg.ºK]](/thumbs/25/5925823.jpg) UNIVERSIDAD NACIONAL DE TUCUMÁN Facultad de Ciencias Exactas y Tecnología CENTRALES ELÉCTRICAS TRABAJO PRÁCTICO Nº 3 CENTRALES TÉRMICAS DE VAPOR CICLO DE RANKINE ALUMNO: AÑO 2015 INTRODUCCIÓN El Ciclo
UNIVERSIDAD NACIONAL DE TUCUMÁN Facultad de Ciencias Exactas y Tecnología CENTRALES ELÉCTRICAS TRABAJO PRÁCTICO Nº 3 CENTRALES TÉRMICAS DE VAPOR CICLO DE RANKINE ALUMNO: AÑO 2015 INTRODUCCIÓN El Ciclo
CAPÍTULO III. FUNCIONES
 CAPÍTULO III LÍMITES DE FUNCIONES SECCIONES A Definición de límite y propiedades básicas B Infinitésimos Infinitésimos equivalentes C Límites infinitos Asíntotas D Ejercicios propuestos 85 A DEFINICIÓN
CAPÍTULO III LÍMITES DE FUNCIONES SECCIONES A Definición de límite y propiedades básicas B Infinitésimos Infinitésimos equivalentes C Límites infinitos Asíntotas D Ejercicios propuestos 85 A DEFINICIÓN
Tema 3. Medidas de tendencia central. 3.1. Introducción. Contenido
 Tema 3 Medidas de tendencia central Contenido 31 Introducción 1 32 Media aritmética 2 33 Media ponderada 3 34 Media geométrica 4 35 Mediana 5 351 Cálculo de la mediana para datos agrupados 5 36 Moda 6
Tema 3 Medidas de tendencia central Contenido 31 Introducción 1 32 Media aritmética 2 33 Media ponderada 3 34 Media geométrica 4 35 Mediana 5 351 Cálculo de la mediana para datos agrupados 5 36 Moda 6
Módulo 9 Sistema matemático y operaciones binarias
 Módulo 9 Sistema matemático y operaciones binarias OBJETIVO: Identificar los conjuntos de números naturales, enteros, racionales e irracionales; resolver una operación binaria, representar un número racional
Módulo 9 Sistema matemático y operaciones binarias OBJETIVO: Identificar los conjuntos de números naturales, enteros, racionales e irracionales; resolver una operación binaria, representar un número racional
3 Aplicaciones de primer orden
 CAPÍTULO 3 Aplicaciones de primer orden 3.4 Ley de Enfriamiento de Newton Si un cuerpo u objeto que tiene una temperatura T 0 es depositado en un medio ambiente que se mantiene a una temperatura T a constante,
CAPÍTULO 3 Aplicaciones de primer orden 3.4 Ley de Enfriamiento de Newton Si un cuerpo u objeto que tiene una temperatura T 0 es depositado en un medio ambiente que se mantiene a una temperatura T a constante,
Definición 1.1.1. Dados dos números naturales m y n, una matriz de orden o dimensión m n es una tabla numérica rectangular con m filas y n columnas.
 Tema 1 Matrices Estructura del tema. Conceptos básicos y ejemplos Operaciones básicas con matrices Método de Gauss Rango de una matriz Concepto de matriz regular y propiedades Determinante asociado a una
Tema 1 Matrices Estructura del tema. Conceptos básicos y ejemplos Operaciones básicas con matrices Método de Gauss Rango de una matriz Concepto de matriz regular y propiedades Determinante asociado a una
Cap. 24 La Ley de Gauss
 Cap. 24 La Ley de Gauss Una misma ley física enunciada desde diferentes puntos de vista Coulomb Gauss Son equivalentes Pero ambas tienen situaciones para las cuales son superiores que la otra Aquí hay
Cap. 24 La Ley de Gauss Una misma ley física enunciada desde diferentes puntos de vista Coulomb Gauss Son equivalentes Pero ambas tienen situaciones para las cuales son superiores que la otra Aquí hay
(b) v constante, por lo que la bola posee una aceleración normal hacia el centro de curvatura.
 Cuestiones 1. Una bola pequeña rueda en el interior de un recipiente cónico de eje vertical y semiángulo α en el vértice A qué altura h sobre el vértice se encontrará la bolita en órbita estable con una
Cuestiones 1. Una bola pequeña rueda en el interior de un recipiente cónico de eje vertical y semiángulo α en el vértice A qué altura h sobre el vértice se encontrará la bolita en órbita estable con una
Las ecuaciones que nos dan la posición (x) de la partícula en función del tiempo son las siguientes: ( )
 DESARROLLO DE LA PARTE TEÓRICA DE LA UNIDAD DIDÁCTICA. 1. Cinemática del movimiento armónico simple. Dinámica del movimiento armónico simple 3. Energía del movimiento armónico simple 4. Aplicaciones: resorte
DESARROLLO DE LA PARTE TEÓRICA DE LA UNIDAD DIDÁCTICA. 1. Cinemática del movimiento armónico simple. Dinámica del movimiento armónico simple 3. Energía del movimiento armónico simple 4. Aplicaciones: resorte
SESION 4. 1. El comando Integrate 2. Aproximación de integrales definidas 3. Integración de funciones racionales
 SESION. El comando Integrate. Aproimación de integrales definidas. Integración de funciones racionales . El comando Integrate El cálculo de integrales definidas e indefinidas en MATHEMATICA es sencillo
SESION. El comando Integrate. Aproimación de integrales definidas. Integración de funciones racionales . El comando Integrate El cálculo de integrales definidas e indefinidas en MATHEMATICA es sencillo
Las Relaciones Públicas en el Marketing social
 Las Relaciones Públicas en el Marketing social El marketing social es el marketing que busca cambiar una idea, actitud o práctica en la sociedad en la que se encuentra, y que intenta satisfacer una necesidad
Las Relaciones Públicas en el Marketing social El marketing social es el marketing que busca cambiar una idea, actitud o práctica en la sociedad en la que se encuentra, y que intenta satisfacer una necesidad
, o más abreviadamente: f ( x)
 TEMA 5: 1. CONCEPTO DE FUNCIÓN Observa los siguientes ejemplos: El precio de una llamada telefónica depende de su duración. El consumo de gasolina de un coche depende de la velocidad del mismo. La factura
TEMA 5: 1. CONCEPTO DE FUNCIÓN Observa los siguientes ejemplos: El precio de una llamada telefónica depende de su duración. El consumo de gasolina de un coche depende de la velocidad del mismo. La factura
5. Diseño e Implementación del sistema (software)
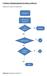 5. Diseño e Implementación del sistema (software) Diagrama de flujo de la aplicación: Aplicación Seleccionar Registros Ir a Archivo? Si Archivo No Sincronizar? Si α No Validar Usuario? Si β No Salir Diagrama:
5. Diseño e Implementación del sistema (software) Diagrama de flujo de la aplicación: Aplicación Seleccionar Registros Ir a Archivo? Si Archivo No Sincronizar? Si α No Validar Usuario? Si β No Salir Diagrama:
Divisibilidad y números primos
 Divisibilidad y números primos Divisibilidad En muchos problemas es necesario saber si el reparto de varios elementos en diferentes grupos se puede hacer equitativamente, es decir, si el número de elementos
Divisibilidad y números primos Divisibilidad En muchos problemas es necesario saber si el reparto de varios elementos en diferentes grupos se puede hacer equitativamente, es decir, si el número de elementos
Mecánica Estadística. Ayudantía 5
 Mecánica Estadística. Ayudantía 5 César Augusto Hidalgo Ramaciotti. Licenciado en Física. Facultad de Física. Pontifícia Universidad Católica de Chile. Ejercicio 1.- A lo largo de dos barras paralelas
Mecánica Estadística. Ayudantía 5 César Augusto Hidalgo Ramaciotti. Licenciado en Física. Facultad de Física. Pontifícia Universidad Católica de Chile. Ejercicio 1.- A lo largo de dos barras paralelas
Diagonalización de matrices
 diagonalizacion.nb Diagonalización de matrices Práctica de Álgebra Lineal, E.U.A.T., Grupos ºA y ºB, 2005 Algo de teoría Qué es diagonalizar una matriz? Para estudiar una matriz suele ser conveniente expresarla
diagonalizacion.nb Diagonalización de matrices Práctica de Álgebra Lineal, E.U.A.T., Grupos ºA y ºB, 2005 Algo de teoría Qué es diagonalizar una matriz? Para estudiar una matriz suele ser conveniente expresarla
OPCIÓN A. moléculas 1 mol. moléculas 2 átomos. moléculas. = 0,166 10 22 moles.
 OPCIÓN A CUESTIÓN 4.- Se tienen tres depósitos cerrados A, B y C de igual olumen y que se encuentran a la misma temperatura. En ellos se introducen, respectiamente, 0 g de H (g), 7 moles de O (g) y 0 3
OPCIÓN A CUESTIÓN 4.- Se tienen tres depósitos cerrados A, B y C de igual olumen y que se encuentran a la misma temperatura. En ellos se introducen, respectiamente, 0 g de H (g), 7 moles de O (g) y 0 3
Tema 1: Fundamentos de lógica, teoría de conjuntos y estructuras algebraicas: Apéndice
 Tema 1: Fundamentos de lógica, teoría de conjuntos y estructuras algebraicas: Apéndice 1 Polinomios Dedicaremos este apartado al repaso de los polinomios. Se define R[x] ={a 0 + a 1 x + a 2 x 2 +... +
Tema 1: Fundamentos de lógica, teoría de conjuntos y estructuras algebraicas: Apéndice 1 Polinomios Dedicaremos este apartado al repaso de los polinomios. Se define R[x] ={a 0 + a 1 x + a 2 x 2 +... +
- MANUAL DE USUARIO -
 - MANUAL DE USUARIO - Aplicación: Kz Precio Hora Instagi Instagi Teléfono: 943424465-943466874 Email: instagi@instagi.com GUIA PROGRAMA CALCULO PRECIO HORA 1. Introducción 2. Datos de la empresa 2.1.Gastos
- MANUAL DE USUARIO - Aplicación: Kz Precio Hora Instagi Instagi Teléfono: 943424465-943466874 Email: instagi@instagi.com GUIA PROGRAMA CALCULO PRECIO HORA 1. Introducción 2. Datos de la empresa 2.1.Gastos
2) Se ha considerado únicamente la mano de obra, teniéndose en cuenta las horas utilizadas en cada actividad por unidad de página.
 APLICACIÓN AL PROCESO PRODUCTIVO DE LA EMPRESA "F. G. / DISEÑO GRÁFICO". AÑO 2004 Rescala, Carmen Según lo explicado en el Informe del presente trabajo, la variación en la producción de páginas web de
APLICACIÓN AL PROCESO PRODUCTIVO DE LA EMPRESA "F. G. / DISEÑO GRÁFICO". AÑO 2004 Rescala, Carmen Según lo explicado en el Informe del presente trabajo, la variación en la producción de páginas web de
Comente: Los bancos siempre deberían dar crédito a los proyectos rentables. Falso, hay que evaluar la capacidad de pago.
 Explique Brevemente en que consiste el leasing y nombre los diferentes tipos existentes. Es un mecanismo de financiamiento de Activos el cual permite el uso del activo por un periodo determinado a cambio
Explique Brevemente en que consiste el leasing y nombre los diferentes tipos existentes. Es un mecanismo de financiamiento de Activos el cual permite el uso del activo por un periodo determinado a cambio
FUNCIONES CUADRÁTICAS Y RACIONALES
 www.matesronda.net José A. Jiménez Nieto FUNCIONES CUADRÁTICAS Y RACIONALES 1. FUNCIONES CUADRÁTICAS. Representemos, en función de la longitud de la base (), el área (y) de todos los rectángulos de perímetro
www.matesronda.net José A. Jiménez Nieto FUNCIONES CUADRÁTICAS Y RACIONALES 1. FUNCIONES CUADRÁTICAS. Representemos, en función de la longitud de la base (), el área (y) de todos los rectángulos de perímetro
PRUEBA ESPECÍFICA PRUEBA 201
 PRUEBA DE ACCES A LA UNIVERSIDAD MAYRES DE 5 AÑS PRUEBA ESPECÍFICA PRUEBA 01 PRUEBA SLUCINARI HAUTAPRBAK 5 URTETIK 014ko MAIATZA DE 5 AÑS MAY 014 Aclaraciones previas Tiempo de duración de la prueba: 1
PRUEBA DE ACCES A LA UNIVERSIDAD MAYRES DE 5 AÑS PRUEBA ESPECÍFICA PRUEBA 01 PRUEBA SLUCINARI HAUTAPRBAK 5 URTETIK 014ko MAIATZA DE 5 AÑS MAY 014 Aclaraciones previas Tiempo de duración de la prueba: 1
