Las 2 fuentes de colesterol: comida y herencia familiar.
|
|
|
- Arturo Piñeiro Torregrosa
- hace 8 años
- Vistas:
Transcripción
1 Las 2 fuentes de colesterol: comida y herencia familiar.
2 Hable con su médico para saber si VYTORIN es adecuado para usted.
3 Su colesterol. Viene del pernil y de sus padres. Usted lo ha escuchado, y quizá hasta lo ha dicho: el colesterol sólo viene de la comida. Lo que quizá no ha escuchado es que el colesterol en realidad tiene mucho que ver con la herencia familiar. Eso podría explicar por qué sus cifras de colesterol LDL (malo) podrían seguir siendo altas, incluso si realmente ha tratado de bajarlas con dieta y ejercicio. La dieta y el ejercicio son elementos importantes para bajar el colesterol. Obtenga consejos útiles para ambos en la página 10. Además del colesterol que viene de las comidas que usted come, su cuerpo produce colesterol según su herencia familiar, lo que significa que su mamá, su papá y hasta sus abuelos pueden tener influencia en su colesterol. Entonces, si tiene problemas para bajar su colesterol a pesar de hacer dieta y ejercicio, no se culpe. El colesterol de todas las personas viene de 2 fuentes. Hacer frente a ambas es una forma eficaz de bajarlo. La buena noticia es que ahora puede concentrarse en las dos fuentes con un producto que ayuda a bloquear la absorción del colesterol que viene de la comida y reduce el colesterol que el cuerpo produce según su herencia familiar. 1
4 Las 2 fuentes de colesterol. La primera es la comida. La segunda es su cuerpo. Al haber 2 fuentes de colesterol a las que hacer frente, no resulta extraño que tantos adultos tengan colesterol alto. La mayoría de las personas ni siquiera están seguras de dónde viene el colesterol. El colesterol de las comidas que usted come. Es difícil deshacerse del colesterol de las comidas, aunque usted esté atento a su dieta. Todas las comidas de origen animal contienen colesterol, incluyendo los huevos, la carne roja y los camarones. En general, los alimentos con alto nivel de grasas saturadas o grasas trans también deberían limitarse. Entre ellos se incluyen alimentos en los que usted quizá no haya pensado, como: Sándwich tostado de queso Plátano frito Margarina Hamburguesas Al comer, el colesterol de las comidas se absorbe por el tubo digestivo. Luego avanza hacia su hígado, y puede circular por todo su cuerpo valiéndose de la sangre para ello. Ésa es una de las fuentes. Además, hay una segunda fuente de colesterol no muy conocida: su propio cuerpo. El colesterol producido por su cuerpo, según la herencia familiar. Como mucha gente, tal vez usted no sepa que su cuerpo produce colesterol en forma natural, según la herencia familiar, a pesar de ser de donde proviene la Hígado y otras células de su cuerpo Colesterol producido por su cuerpo Colesterol de los alimentos que come El colesterol de ambas fuentes puede acumularse en su sangre. Tracto digestivo Entender el colesterol mayoría de su colesterol total. Su hígado produce colesterol, así como también lo hacen otras células específicas en todo su cuerpo. Una vez que se produce el colesterol, éste puede pasar a la sangre. Qué significa este proceso para usted? Tome el colesterol que produce su cuerpo y súmelo al colesterol que obtiene de las comidas. Ahora puede apreciar con qué facilidad se puede acumular el colesterol en su sangre y cómo puede aumentar su nivel de colesterol total. La buena noticia es que tratar las dos fuentes puede reducir significativamente su colesterol. Cuando la dieta y el ejercicio no son suficiente, tomar VYTORIN (ezetimibe/) puede ayudar. 2 3
5 VYTORIN (ezetimibe/) El único producto que: Ayuda a bloquear la absorción del colesterol que viene de la comida, y Reduce el colesterol que el cuerpo produce según su herencia familiar VYTORIN contiene dos medicamentos para el colesterol en una sola pastilla: Zetia (ezetimibe) y Zocor (). No se ha comprobado que VYTORIN reduzca los ataques al corazón o los derrames cerebrales más que Zocor solo. VYTORIN puede: Bajar su nivel de colesterol LDL (malo). Bajar el nivel total de su colesterol. Bajar el nivel de sus triglicéridos (un tipo especial de grasa en su sangre). Aumentar el colesterol HDL (bueno). Sólo una pastilla al día. Su médico puede decidir que, junto con una dieta saludable y ejercicio, VYTORIN es apropiado para usted. Si éste es el caso, recuerde tomar una pastilla al día por la noche, o como su médico se lo indique. Tome VYTORIN con o sin comida: la decisión es suya. VYTORIN y ZETIA son marcas comerciales de MSP Singapore Company, LLC. Otras marcas enumeradas son marcas comerciales de sus respectivos propietarios y no son marcas comerciales de MSP Singapore Company, LLC. VYTORIN redujo el colesterol malo más que Lipitor o Zocor. VYTORIN contiene dos medicamentos para el colesterol en una sola pastilla: Zetia (ezetimibe) y Zocor (). No se ha comprobado que VYTORIN reduzca los ataques al corazón o los derrames cerebrales más que Zocor solo. Estudios médicos han comprobado que VYTORIN redujo el colesterol malo más que Lipitor o Zocor por sí solos. Se ha comprobado que VYTORIN reduce el colesterol malo entre un 45% y un 60% (El efecto promedio depende de la dosis; 52% a la dosis inicial usual.) Información Importante Sobre los Riesgos de VYTORIN: VYTORIN es una pastilla recetada y no es para todos, incluyendo mujeres lactantes, embarazadas o que pueden quedar embarazadas, y también personas con problemas del hígado. Dolor o debilidad muscular inexplicables podrían ser síntomas de un raro pero serio efecto secundario, por lo cual debe ser reportado a su médico de inmediato. VYTORIN puede interactuar con otros medicamentos o ciertas comidas, aumentando el riesgo de experimentar este serio efecto secundario. Así que dígale a su médico acerca de cualquier otro medicamento que esté tomando. Su médico puede hacerle unos sencillos exámenes de sangre antes y mientras esté con el tratamiento de VYTORIN para determinar si tiene problemas del hígado. 4 5
6 Tiene preguntas? Nosotros tenemos respuestas. Ahora que sabe que el colesterol viene de 2 fuentes (la comida y la herencia familiar), quizá aún tenga algunas preguntas. No se preocupe. Aquí hay respuestas a algunas preguntas usuales sobre el colesterol. P. Qué podría pasar si tuviera colesterol alto? R. Tener el colesterol LDL (malo) alto puede ponerlo en situación de riesgo de una enfermedad cardíaca, ataque al corazón o derrame cerebral, especialmente si usted tiene cualquiera de estos factores adicionales de riesgo: Tiene el colesterol HDL bajo Tiene diabetes Fuma Es obeso(a) Tiene presión arterial alta No hace actividad física Tiene herencia familiar de enfermedad cardíaca Tiene una dieta alta en grasas o alta en colesterol Es un hombre de 45 años o más Es una mujer de 55 años o más P. Qué es el colesterol? R. El colesterol es una sustancia suave y cerosa que se encuentra en la sangre. Aunque su cuerpo necesita colesterol para la creación y el mantenimiento de las células, si hay demasiado puede acumularse en las paredes de las arterias. P. Qué son el colesterol LDL y el colesterol HDL? R. El colesterol LDL (lipoproteína de baja densidad) es llamado colesterol malo porque puede acumularse en las paredes de las arterias y formar una 6 placa dura y gruesa que obstruye las arterias y bloquea el paso de la sangre al corazón y el cerebro. HDL se refiere a la lipoproteína de alta densidad, también llamado colesterol bueno porque ayuda a eliminar el colesterol malo del cuerpo. 7
7 P. Qué debería hacer? R. Lo primero que debería hacer sería hacerse una simple prueba de sangre para conocer su nivel de colesterol y consultar a su médico para saber cuál debería ser su meta en cuanto al colesterol LDL (malo). Cuidar su dieta y hacer ejercicio pueden ser de ayuda, pero si su colesterol no baja lo suficiente, su médico podría sugerirle que comience a tomar medicina. 8 P. Puede VYTORIN (ezetimibe/) ayudarme a reducir mi colesterol malo? R. Sí. Estudios medicos han comprobado que VYTORIN reduce el colesterol malo entre un 45% y 60% (el efecto promedio depende de la dosis; 52% a la dosis inicial usual) cuando la dieta y el ejercicio no son suficiente. VYTORIN ayuda a bloquear la absorción del colesterol que viene de la comida y reduce el colesterol que su cuerpo produce segun su herencia familiar. De todas formas, deberá seguir haciendo ejercicio y vigilando su dieta mientras tome VYTORIN. Información Importante Sobre los Riesgos de VYTORIN: Entre los efectos secundarios se incluyeron dolor de cabeza, dolores musculares y diarrea. 9
8 Una dieta saludable: buen sabor y bueno para usted. Comer saludablemente es un elemento vital para bajar su colesterol. Para facilitarlo, comience de a poco haciendo pequeñas sustituciones en su dieta. Reemplace bistecs, hamburguesas y comidas fritas por pescado, pollo y pavo horneados o a la parrilla. Ejercicio: un poco sirve para mucho. Hacer ejercicio en forma regular no significa necesariamente imponerse uno mismo algo que se parezca a un entrenamiento militar. Las pequeñas cosas pueden ser más útiles de lo que a usted quizá le parecen. Simplemente dar caminatas o ir por las escaleras en vez de tomar un ascensor puede ser importante y contribuir a bajar su nivel de colesterol. Si se siente ambicioso, vaya a un gimnasio o pruebe nuevos deportes, como voleibol, softball o tenis. Haga cosas que le gusten, y diviértase. La mejor manera de asegurarse de que se mantendrá fiel al programa de ejercicios es comprobando que se está divirtiendo. Mejor aun, consiga a un amigo para que se le una. Por supuesto que debe hablar con su médico antes de empezar cualquier régimen de ejercicios. VYTORIN trata las 2 fuentes de colesterol. Medicamentos: pueden ayudar a reducir aún más su colesterol. Con 2 fuentes de colesterol con los que luchar, bajar el colesterol LDL (malo) puede ser complejo. Así que, cuando la dieta y el ejercicio no son suficiente, su médico puede recetar VYTORIN. Cuando tome cualquier medicamento, asegúrese de seguir las recomendaciones de su médico y de continuar tomando sus medicamentos como se le indicó. Siga estos pasos para una vida más sana. 1. Lea en nuestros 9 formas inteligentes de mantenerse activo y Enfóquese en alimentos más sanos que se encuentran en el bolsillo de este folleto consejos útiles sobre dieta y ejercicio que podrá usar todos los días. 2. Lleve las Preguntas para la cita con su médico y use la Ficha de meta y resultados para anotar sus cifras de colesterol después de cada visita
9 Hable con su médico para saber si VYTORIN es adecuado para usted. Desea más información? Estos recursos pueden ser de ayuda. Centro Nacional de la American Heart Association 7272 Greenville Avenue Dallas, TX AHA-USA-1 ( ) Institutos Nacionales de Salud 9000 Rockville Pike Bethesda, MD (sólo en inglés) Programa Nacional de Educación sobre el Colesterol Centro de Información de NHLBI PO Box Bethesda, MD Para más información, visite vytorin.com/espanol Lea la Información para el Paciente sobre el Producto y hable de ella con su médico. Se ofrece también la Información de Prescripción para el médico. 12
10 Una dieta saludable es importante, pero cuando no es suficiente, tomar VYTORIN puede ayudar. VYTORIN contiene dos medicamentos para el colesterol en una sola pastilla: Zetia (ezetimibe) y Zocor (). No se ha comprobado que VYTORIN reduzca los ataques al corazón o los derrames cerebrales más que Zocor solo. Información Importante Sobre los Riesgos de VYTORIN: VYTORIN es una pastilla recetada y no es para todos, incluyendo mujeres lactantes, embarazadas o que pueden quedar embarazadas, y también personas con problemas del hígado.
11 VYTORIN trata las 2.
12 VYTORIN (ezetimibe/) Tabletas ASPECTOS DESTACADOS DE LA INFORMACIÓN SOBRE PRESCRIPCIÓN Estos aspectos destacados no incluyen toda la información necesaria para usar VYTORIN de manera segura y eficaz. Consultar la información completa sobre prescripción de VYTORIN. VYTORIN (ezetimibe/) Tabletas Aprobación inicial en Estados Unidos: INDICACIONES Y USO VYTORIN, que contiene un inhibidor de la absorción del colesterol y un inhibidor de la HMG-CoA reductasa (estatina), está indicado como tratamiento adyuvante de la dieta para lograr los siguientes objetivos: reducir niveles elevados de C-total, C-LDL, Apo B, TG y C-no HDL, y aumentar el nivel de C-HDL en pacientes afectados de hiperlipidemia primaria (familiar heterocigótica y no familiar) o hiperlipidemia mixta. (1.1) reducir niveles elevados de C-total y C-LDL en pacientes afectados de hipercolesterolemia familiar homocigótica (HFHo), como adyuvante de otros tratamientos hipolipemiantes. (1.2) Limitaciones de Uso (1.3) No se ha establecido ningún beneficio adicional de VYTORIN en la morbilidad y mortalidad cardiovasculares superior al demostrado para la. VYTORIN no ha sido estudiado en dislipidemias tipo I, III, IV y V de Fredrickson POSOLOGÍA Y ADMINISTRACIÓN El intervalo de dosis es de 10/10 mg/día hasta 10/80 mg/día. (2.1) La dosis inicial recomendada habitualmente es de 10/20 mg/día. (2.1) VYTORIN debe administrarse 2 horas antes o bien 4 horas después de la administración de un quelante de ácidos biliares. (2.6, 7.4) FORMAS FARMACÉUTICAS Y CONCENTRACIONES Tabletas (mg de ezetimibe/mg de ): 10/10, 10/20, 10/40, 10/80 (3) CONTRAINDICACIONES Hipersensibilidad a cualquier componente de este medicamento (4, 6.2) Enfermedad hepática activa o elevaciones persistentes y de origen desconocido de los niveles de transaminasas hepáticas (4, 5.2) Mujeres embarazadas o con potencial de embarazo (4, 8.1) Madres lactantes (4, 8.3) ADVERTENCIAS Y PRECAUCIONES Debe advertirse a los pacientes que notifiquen sin demora cualquier síntoma de miopatía. Debe interrumpirse inmediatamente la administración de VYTORIN si se diagnostica o se sospecha miopatía. (5.1) Efectos en el músculo esquelético (p. ej., miopatía y rabdomiólisis): Los riesgos aumentan en presencia de dosis más elevadas y ante la administración concomitante de ciertos inhibidores de CYP3A4, gemfibrozil, ciclosporina, danazol, amiodarona y INFORMACIÓN COMPLETA SOBRE PRESCRIPCIÓN: CONTENIDO* 1 INDICACIONES Y USO 1.1 Hiperlipidemia Primaria 1.2 Hipercolesterolemia Familiar Homocigótica (HFHo) 1.3 Limitaciones de Uso 2 POSOLOGÍA Y ADMINISTRACIÓN 2.1 Dosis Recomendadas 2.2 Pacientes con Hipercolesterolemia Familiar Homocigótica 2.3 Pacientes con Disfunción Hepática 2.4 Pacientes con Disfunción Renal 2.5 Pacientes Geriátricos 2.6 Coadministración con Otros Fármacos 3 FORMAS FARMACÉUTICAS Y CONCENTRACIONES 4 CONTRAINDICACIONES 5 ADVERTENCIAS Y PRECAUCIONES 5.1 Miopatía/Rabdomiólisis 5.2 Enzimas Hepáticas 5.3 Disfunción hepática 6 REACCIONES ADVERSAS 6.1 Experiencia en Ensayos Clínicos 6.2 Experiencia Posmercadeo 7 INTERACCIONES DE FÁRMACOS 7.1 Interacciones con el CYP3A4 7.2 Hipolipemiantes que Pueden Causar Miopatía Cuando Se Administran por Sí Solos 7.3 Amiodarona o Verapamil 7.4 Colestiramina 7.5 Ciclosporina o Danazol 7.6 Digoxina 7.7 Fibratos verapamil. Entre los factores predisponentes se encuentran: edad avanzada ( 65 años), hipotiroidismo incontrolado y disfunción renal. (5.1, 8.5, 8.6) Anomalías y monitoreo de enzimas hepáticas: Pueden producirse elevaciones persistentes de transaminasas hepáticas. Monitorear las enzimas hepáticas antes y durante el tratamiento. Los pacientes cuyas dosis se hayan ajustado a 10/80 mg deben someterse a pruebas adicionales de la función hepática. (5.2) No se recomienda VYTORIN a pacientes afectados de disfunción hepática moderada o grave. (5.3, 12.3) REACCIONES ADVERSAS Reacciones adversas frecuentes (incidencia 2% y mayor que con el placebo) en ensayos clínicos: cefalea, aumento de ALT, mialgia, infección de las vías respiratorias superiores y diarrea. (6.1) Para notificar SOSPECHAS DE REACCIONES ADVERSAS, llamar a Merck/Schering- Plough Pharmaceuticals al , o comunicarse con la FDA al FDA-1088 o en INTERACCIONES DE FÁRMACOS Interacciones de Fármacos Asociadas a un Mayor Riesgo de Miopatía/Rabdomiólisis (2.6, 5.1, 7.1, 7.2, 7.3, 7.5, 7.7) Fármacos Interactuantes Recomendaciones de Prescripción Itraconazol, ketoconazol, eritromicina, Evitar VYTORIN claritromicina, telitromicina, inhibidores de la proteasa del VIH, nefazodona, fibratos Ciclosporina, danazol Amiodarona, verapamil Jugo de toronja No superar los 10/10 mg de VYTORIN al día No superar los 10/20 mg de VYTORIN al día Evitar grandes cantidades de jugo de toronja (>1 cuarto de galón al día) Ciclosporina: la coadministración aumenta la exposición a VYTORIN y la ciclosporina. Se deben vigilar las concentraciones de ciclosporina. (7.5, 12.3) Anticoagulantes cumarínicos: la prolonga el IIN. Se debe lograr un IIN estable antes de iniciar el tratamiento con VYTORIN. Cuando se inicie o modifique el tratamiento con VYTORIN, monitorear el IIN con frecuencia hasta que haya alcanzado la estabilidad. (7.8) Colestiramina: la coadministración disminuye la exposición al ezetimibe. (2.6, 7.4) USO EN POBLACIONES ESPECÍFICAS Disfunción renal grave: Debe procederse con cautela y vigilarse estrechamente al paciente. (2.4, 8.6) Consultar la sección 17 para obtener INFORMACIÓN SOBRE ASESORAMIENTO DE LOS PACIENTES y el prospecto para los pacientes autorizado por la FDA. Modificado: 07/ Anticoagulantes Cumarínicos 8 USO EN POBLACIONES ESPECÍFICAS 8.1 Embarazo 8.3 Madres Lactantes 8.4 Uso Pediátrico 8.5 Uso Geriátrico 8.6 Disfunción Renal 8.7 Disfunción Hepática 10 SOBREDOSIS 11 DESCRIPCIÓN 12 FARMACOLOGÍA CLÍNICA 12.1 Mecanismo de Acción 12.2 Farmacodinamia 12.3 Farmacocinética 13 TOXICOLOGÍA NO CLÍNICA 13.1 Carcinogénesis, Mutagénesis, Deterioro de la Fertilidad 13.2 Toxicología y/o Farmacología Animal 14 ESTUDIOS CLÍNICOS 14.1 Hiperlipidemia Primaria 14.2 Hipercolesterolemia Familiar Homocigótica (HFHo) 16 PRESENTACIÓN/CONSERVACIÓN Y MANEJO 17 INFORMACIÓN SOBRE ASESORAMIENTO DE LOS PACIENTES 17.1 Dolor Muscular 17.2 Enzimas Hepáticas 17.3 Embarazo 17.4 Lactancia 17.5 Prospecto para los Pacientes Autorizado por la FDA *No se mencionan las secciones o subsecciones omitidas de la información completa sobre prescripción.
13 VYTORIN (ezetimibe/) Tabletas FULL INFORMACIÓN PRESCRIBING COMPLETA INFORMATION SOBRE PRESCRIPCIÓN 1 INDICACIONES Y USO El tratamiento con modificadores del perfil lipídico debe ser sólo un componente de la intervención sobre múltiples factores de riesgo en los pacientes con riesgo significativamente mayor de trastornos vasculares ateroscleróticos por hipercolesterolemia. La farmacoterapia está indicada como adyuvante de la dieta cuando la respuesta a una dieta restrictiva en grasas saturadas y colesterol, junto con otras medidas no farmacológicas, no ha resultado suficiente. 1.1 Hiperlipidemia Primaria VYTORIN está indicado para reducir niveles elevados de colesterol total (C total), colesterol asociado a lipoproteínas de baja densidad (C-LDL), apolipoproteína B (Apo B), triglicéridos (TG) y colesterol no asociado a proteínas de alta densidad (C-no HDL), así como para aumentar los niveles de colesterol asociado a lipoproteínas de alta densidad (C-HDL), en pacientes afectados de hiperlipidemia primaria (familiar heterocigótica y no familiar) o hiperlipidemia mixta. 1.2 Hipercolesterolemia Familiar Homocigótica (HFHo) VYTORIN está indicado para la reducción de valores elevados de C-total y C-LDL en pacientes con hipercolesterolemia familiar homocigótica como adyuvante de otros tratamientos hipolipemiantes (p. ej. aféresis de las LDL) o si no están disponibles tales tratamientos. 1.3 Limitaciones de Uso No se ha establecido ningún beneficio adicional de VYTORIN en la morbilidad y mortalidad cardiovasculares superior al demostrado para la. VYTORIN no ha sido estudiado en dislipidemias tipo I, III, IV y V de Fredrickson. 2 POSOLOGÍA Y ADMINISTRACIÓN 2.1 Dosis Recomendadas El intervalo de dosis es de 10/10 mg/día hasta 10/80 mg/día. La dosis inicial recomendada habitualmente es de 10/20 mg/día. VYTORIN debe tomarse como una sola dosis diaria, por la noche, con o sin alimentos. Puede considerarse iniciar el tratamiento con 10/10 mg/día para los pacientes que necesiten reducciones menos drásticas del C- LDL. Los pacientes que necesiten una reducción superior en el nivel de C-LDL (mayor del 55%) pueden ser iniciados con 10/40 mg/día. Tras el inicio de VYTORIN o el ajuste de la dosis, pueden analizarse las concentraciones de lípidos 2 o más semanas después y ajustarse la posología, si es necesario. 2.2 Pacientes con Hipercolesterolemia Familiar Homocigótica La dosis recomendada para pacientes con hipercolesterolemia familiar homocigótica es VYTORIN 10/40 mg/día o 10/80 mg/día por la noche. VYTORIN debe usarse como adyuvante de otros tratamientos hipolipemiantes (p. ej., aféresis de las LDL) en estos pacientes o si tales tratamientos no están disponibles. 2.3 Pacientes con Disfunción Hepática No es necesario ajustar la dosis en los pacientes que tengan disfunción hepática leve [véase Advertencias y Precauciones (5.3)]. 2.4 Pacientes con Disfunción Renal No es necesario ajustar la dosis en los pacientes que tengan disfunción renal leve o moderada. Sin embargo, para los pacientes afectados de insuficiencia renal grave, no debe instaurarse VYTORIN a menos que el paciente ya haya tolerado el tratamiento con a una dosis de 5 mg o mayor. Se debe proceder con cautela cuando se administre VYTORIN a estos pacientes, quienes deberán ser objeto de vigilancia estricta [véanse Advertencias y Precauciones (5.1); Farmacología Clínica (12.3)]. 2.5 Pacientes Geriátricos No es necesario ajustar la dosis en los pacientes geriátricos [véase Farmacología Clínica (12.3)]. 2.6 Coadministración con Otros Fármacos [Véanse Advertencias y Precauciones (5.1) e Interacciones de Fármacos (7).] Quelantes de los Ácidos Biliares VYTORIN debe administrarse 2 horas antes o bien 4 horas después de la administración de un quelante de ácidos biliares [véase Interacciones de Fármacos (7.4)]. Ciclosporina o Danazol Se debe actuar con cautela cuando se instaure VYTORIN en presencia de ciclosporina. En pacientes que toman ciclosporina o danazol, no debe iniciarse VYTORIN a menos que el paciente ya haya tolerado el tratamiento con a una dosis de 5 mg o mayor. La dosis de VYTORIN no debe superar los 10/10 mg/día [véase Interacciones de Fármacos (7.5)]. Amiodarona o Verapamil En pacientes que tomen amiodarona o verapamil concomitantemente con VYTORIN, la dosis no debe superar los 10/20 mg/día [véanse Advertencias y Precauciones (5.1) e Interacciones de Fármacos (7.3)]. VYTORIN (ezetimibe/) Tabletas Otros Tratamientos Hipolipemiantes Concomitantes No se ha establecido la seguridad ni la eficacia de VYTORIN administrado con fibratos. Por lo tanto, se debe evitar la coadministración de VYTORIN y fibratos [véanse Advertencias y Precauciones (5.1) e Interacciones de Fármacos (7.2 y 7.7)]. Existe un mayor riesgo de miopatía cuando la se administra concomitantemente con fibratos (especialmente con gemfibrozil). Se debe evitar la coadministración de gemfibrozil porque la exposición a la aumenta ante la politerapia. [Véanse Advertencias y Precauciones (5.1) e Interacciones de Fármacos (7.2 y 7.7).] 3 FORMAS FARMACÉUTICAS Y CONCENTRACIONES VYTORIN 10/10 (tabletas de ezetimibe 10 mg/ 10 mg) son tabletas blancas a blanquecinas en forma de cápsula, y llevan el código 311 en una cara. VYTORIN 10/20 (tabletas de ezetimibe 10 mg/ 20 mg) son tabletas blancas a blanquecinas en forma de cápsula, y llevan el código 312 en una cara. VYTORIN 10/40 (tabletas de ezetimibe 10 mg/ 40 mg) son tabletas blancas a blanquecinas en forma de cápsula, y llevan el código 313 en una cara. VYTORIN 10/80 (tabletas de ezetimibe 10 mg/ 80 mg) son tabletas blancas a blanquecinas en forma de cápsula, y llevan el código 315 en una cara. 4 CONTRAINDICACIONES Hipersensibilidad a cualquier componente de este medicamento [véase Reacciones Adversas (6.2)]. Enfermedad hepática activa o elevaciones persistentes y de origen desconocido de los niveles de transaminasas hepáticas [véase Advertencias y Precauciones (5.2)]. Mujeres embarazadas o con potencial de embarazo. Los niveles de colesterol y triglicéridos en suero aumentan durante el embarazo normal, y el colesterol o sus derivados son esenciales para el desarrollo fetal. Ya que los inhibidores de la HMG-CoA reductasa (estatinas) tales como la disminuyen la síntesis del colesterol y, posiblemente, la síntesis de otras sustancias con actividad biológica derivadas del colesterol, VYTORIN podría perjudicar al feto si se lo administra a una mujer embarazada. La ateroesclerosis es un proceso crónico y la suspensión de los hipolipemiantes durante el embarazo debería tener un efecto leve en los resultados del tratamiento a largo plazo de la hipercolesterolemia primaria. No se han realizado estudios adecuados y bien controlados de la administración de VYTORIN durante el embarazo; sin embargo, en escasos informes se observaron anomalías congénitas tras la exposición intrauterina a las estatinas. En estudios sobre reproducción animal en ratas y conejos, la no reveló ningún potencial teratogénico. VYTORIN debe administrarse a mujeres en edad fértil sólo si es muy poco probable que estas pacientes queden embarazadas. Si una mujer queda embarazada mientras toma este medicamento, se debe suspender VYTORIN inmediatamente e informar a la paciente del riesgo potencial al feto [véase Uso en Poblaciones Específicas (8.1)]. Madres lactantes. No se sabe si la se excreta en la leche humana; sin embargo, una pequeña cantidad de otro fármaco de esta clase sí pasa a la leche materna. Dado que las estatinas tienen el potencial de provocar reacciones adversas graves en bebés lactantes, las mujeres que precisan tratamiento con VYTORIN no deben amamantar a sus bebés [véase Uso en Poblaciones Específicas (8.3)]. 5 ADVERTENCIAS Y PRECAUCIONES 5.1 Miopatía/Rabdomiólisis En los estudios clínicos no hubo un exceso de casos de miopatía o rabdomiólisis asociados al ezetimibe en comparación con el grupo control pertinente (placebo o estatina por sí sola). Sin embargo, se sabe que la miopatía y la rabdomiólisis son reacciones adversas a las estatinas y a otros hipolipemiantes. En ensayos clínicos, la incidencia de concentraciones de CK >10 veces el límite superior de la normalidad (LSN) fue de 0.2% para VYTORIN, 0.6% para el placebo, 0.0% para el ezetimibe y 0.3% para todas las dosis de. Como es el caso de otras estatinas, en ocasiones la causa miopatías manifestadas como dolor muscular, sensibilidad al tacto o debilidad y concentraciones de creatina cinasa superiores a 10 veces el LSN. A veces la miopatía toma la forma de rabdomiólisis con o sin insuficiencia renal aguda secundaria a la mioglobinuria y, en raros casos, ha habido muertes. El riesgo de miopatía aumenta en presencia de altos niveles de actividad de estatinas en plasma. Entre los factores predisponentes de miopatía se encuentran: edad avanzada ( 65 años), hipotiroidismo incontrolado y disfunción renal. Al igual que sucede con otras estatinas, el riesgo de miopatía/ rabdomiólisis depende de la dosis. En una base de datos de ensayos clínicos en la que 2
14 VYTORIN (ezetimibe/) Tabletas se trató a 41,050 pacientes con, de los cuales 24,747 (aproximadamente el 60%) fueron tratados durante al menos 4 años, la incidencia de miopatía fue de aproximadamente un 0.02%, 0.08% y 0.53% con 20, 40 y 80 mg/día, respectivamente. En estos ensayos se vigiló estrictamente a los pacientes y se excluyeron algunos productos medicinales interactuantes. En la experiencia posmercadeo con el ezetimibe, se han notificado casos de miopatía y rabdomiólisis. La mayoría de los pacientes que presentaron rabdomiólisis ya estaban tomando una estatina antes de iniciar el tratamiento con ezetimibe. Sin embargo, se han notificado casos de rabdomiólisis con muy poca frecuencia en la monoterapia con ezetimibe, y con muy poca frecuencia en la adición de ezetimibe a fármacos asociados a un aumento del riesgo de rabdomiólisis, como los fibratos. Todos los pacientes que inicien un tratamiento con VYTORIN, o cuya dosis de VYTORIN se esté aumentando, deben ser advertidos del riesgo de miopatía y recibir instrucciones de informar sin demora cualquier dolor muscular, sensibilidad al tacto o debilidad muscular de origen desconocido. El tratamiento con VYTORIN debe suspenderse inmediatamente si se diagnostica o se sospecha una miopatía. En la mayoría de los casos, los síntomas musculares y los aumentos en la CK se resolvieron cuando se suspendió rápidamente el tratamiento con. Podría considerarse la posibilidad de realizar determinaciones periódicas de la CK en pacientes que empiecen el tratamiento con o cuya dosis se esté aumentando, pero no hay garantías de que tal vigilancia vaya a evitar una miopatía. Muchos de los pacientes que han presentado rabdomiólisis durante el tratamiento con han tenido antecedentes médicos complicados, como insuficiencia renal por lo general a consecuencia de diabetes mellitus prolongada. Estos pacientes que tomen VYTORIN requieren una vigilancia más estrecha. El tratamiento con VYTORIN deberá suspenderse temporalmente unos días antes de una cirugía mayor electiva y cuando sobrevenga algún trastorno médico o quirúrgico importante. Interacciones de Fármacos El riesgo de miopatía y rabdomiólisis aumenta en presencia de altos niveles de actividad de estatinas en plasma. La es metabolizada por la isoforma 3A4 del citocromo P450. Ciertos fármacos que inhiben esta vía metabólica pueden elevar las concentraciones de en plasma y aumentar el riesgo de miopatía. Entre éstos se encuentran: itraconazol, ketoconazol y otros azoles antifúngicos; los antibióticos macrólidos eritromicina y claritromicina y el antibiótico ketólido telitromicina; inhibidores de la proteasa del VIH; el antidepresivo nefazodona, o grandes cantidad de jugo de toronja (>1 cuarto de galón al día). Debe evitarse la administración concomitante de VYTORIN y estos inhibidores del CYP3A4. Si no se puede evitar el tratamiento con itraconazol, ketoconazol, eritromicina, claritromicina o telitromicina, se debe suspender la administración de VYTORIN en el transcurso del tratamiento. [Véase Interacciones de Fármacos (7).] Deben sopesarse cuidadosamente los beneficios de la coadministración de VYTORIN con los siguientes fármacos, frente a los riesgos potenciales de estas politerapias: gemfibrozil, otros hipolipemiantes (otros fibratos o 1 g/día de niacina), ciclosporina, danazol, amiodarona o verapamil. Se debe actuar con cautela al prescribir otros fibratos o dosis hipolipemiantes ( 1 g/día) de niacina con VYTORIN, ya que estos fármacos pueden producir miopatía si son administrados por sí solos. Las recomendaciones de prescripción para fármacos interactuantes se resumen en el Cuadro 1 [véanse también Posología y Administración (2.6), Interacciones de Fármacos (7) y Farmacología Clínica (12.3)]. Cuadro 1 Interacciones Farmacológicas Asociadas a un Mayor Riesgo de Miopatía/Rabdomiólisis Fármacos Interactuantes Recomendaciones de Prescripción Itraconazol Evitar VYTORIN Ketoconazol Eritromicina Claritromicina Telitromicina Inhibidores de la proteasa del VIH Nefazodona Fibratos* Ciclosporina No superar los 10/10 mg de VYTORIN al día Danazol Amiodarona No superar los 10/20 mg de VYTORIN al día Verapamil Jugo de toronja Evitar grandes cantidades de jugo de toronja (>1 cuarto de galón al día) VYTORIN (ezetimibe/) Tabletas 5.2 Enzimas Hepáticas En tres ensayos controlados con placebo, de 12 semanas de duración, la incidencia de elevaciones consecutivas ( 3 veces el LSN) en las transaminasas séricas fue del 1.7% en total en los pacientes tratados con VYTORIN y aparentemente estuvo relacionada con la dosis; la incidencia fue del 2.6% en los pacientes tratados con VYTORIN 10/80. En extensiones controladas a largo plazo (48 semanas) que incluyeron tanto a pacientes nuevos como a pacientes tratados anteriormente, la incidencia de elevaciones consecutivas ( 3 veces el LSN) de transaminasas séricas fue del 1.8% en general y del 3.6% en los pacientes tratados con VYTORIN 10/80. Estas elevaciones de las transaminasas generalmente fueron asintomáticas, no se asociaron a colestasia y volvieron a los valores basales después de suspendido el tratamiento o con un tratamiento continuo. Se recomienda realizar pruebas de función hepática antes del inicio del tratamiento con VYTORIN, y de allí en adelante cuando esté clínicamente indicado. A los pacientes en quienes se ajustó la dosis hasta 10/80 mg se debe realizar una prueba adicional antes del ajuste, 3 meses después del ajuste a la dosis de 10/80 mg y periódicamente de allí en adelante (p. ej., semianualmente) durante el primer año de tratamiento. Se debe hacer un seguimiento de los pacientes que presenten un aumento en los niveles de las transaminasas con una segunda evaluación de función hepática para confirmar el hallazgo y, de allí en adelante, realizar pruebas de función hepática frecuentes hasta que las anomalías vuelvan a la normalidad. Si persisten aumentos en las AST o ALT de 3 veces el LSN o más, se recomienda suspender el tratamiento con VYTORIN. VYTORIN debe ser administrado con cautela en pacientes que consumen cantidades considerables de alcohol y/o que tienen antecedentes de enfermedad hepática. Las enfermedades hepáticas activas o las elevaciones persistentes y de origen desconocido de transaminasas son contraindicaciones para el uso de VYTORIN. 5.3 Disfunción Hepática Debido a los efectos desconocidos de la mayor exposición al ezetimibe en los pacientes con disfunción hepática de moderada a grave, no se recomienda administrar VYTORIN a estos pacientes. [Véase Farmacología Clínica (12.3).] 6 REACCIONES ADVERSAS Las siguientes reacciones adversas graves se explican más detalladamente en otras secciones del prospecto: Rabdomiólisis y miopatía [véase Advertencias y Precauciones (5.1)] Anomalías de las enzimas hepáticas [véase Advertencias y Precauciones (5.2)] 6.1 Experiencia en Ensayos Clínicos VYTORIN Dado que los estudios clínicos se llevan a cabo en condiciones enormemente diversas, los índices de reacciones adversas observadas en los estudios clínicos de un fármaco no se pueden comparar directamente con los índices observados en los estudios clínicos de otros fármacos, y podrían no representar los índices observados en la práctica. En la base de datos de ensayos clínicos controlados con placebo de VYTORIN (ezetimibe/) de 1420 pacientes (intervalo de edades: años, 52% mujeres, 87% de raza blanca, 3% de raza negra, 5% hispanos, 3% asiáticos) con una mediana de duración del tratamiento de 27 semanas, 5% de los pacientes que tomaban VYTORIN y 2.2% de los pacientes que tomaban placebo suspendieron el tratamiento a causa de reacciones adversas. Las reacciones adversas más frecuentes observadas en el grupo tratado con VYTORIN que condujeron al abandono del tratamiento y que se produjeron a una mayor frecuencia que con el placebo fueron: Aumento de la ALT (0.9%) Mialgia (0.6%) Aumento de la AST (0.4%) Dolor de espalda (0.4%) En ensayos clínicos controlados, las reacciones adversas comunicadas con mayor frecuencia (incidencia >2% y mayor que con el placebo) fueron: cefalea (5.8%), aumento de ALT (3.7%), mialgia (3.6%), infección de las vías respiratorias superiores (3.6%) y diarrea (2.8%). Se ha evaluado la seguridad de VYTORIN en más de 10,189 pacientes en ensayos clínicos. En el Cuadro 2 se resume la frecuencia de reacciones clínicas adversas notificadas en >2% de los pacientes tratados con VYTORIN (n=1420) y con una incidencia mayor que con el placebo, independientemente de la evaluación de causalidad, observadas en cuatro estudios controlados con placebo. *Debe evitarse la politerapia con fibratos; sin embargo, aunque no se recomienda, si VYTORIN se va a tomar en politerapia con gemfibrozil, la dosis no debe superar los 10/10 mg al día. Se deben sopesar cuidadosamente los beneficios del uso de VYTORIN en pacientes que reciben ciclosporina o danazol frente a los riesgos de estas politerapias. Debe evitarse la administración conjunta de VYTORIN en dosis mayores de 10/20 mg al día con amiodarona o verapamil, a menos que sea probable que el beneficio clínico supere el mayor riesgo de miopatía. 3
15 VYTORIN (ezetimibe/) Tabletas Cuadro 2* Reacciones Clínicas Adversas Notificadas en >2% de los Pacientes Tratados con VYTORIN con una Incidencia Mayor que con el Placebo, Independientemente de la Causalidad Placebo 10 mg ** VYTORIN** Sistema Corporal/Clase de Órganos (%) (%) (%) (%) Acontecimiento Adverso n=371 n=302 n=1234 n=1420 Cuerpo completo, trastornos generales Dolor de cabeza Trastornos del sistema digestivo Diarrea Infección e infestaciones Influenza Infección de las vías respiratorias superiores Trastornos musculoesqueléticos y del tejido conectivo Mialgia Dolor en las extremidades * Incluye dos estudios combinados controlados con placebo en los que se coadministraron los ingredientes activos equivalentes a VYTORIN, y dos estudios controlados con placebo en los que se administró VYTORIN. ** Todas las dosis. Otras reacciones adversas comunicadas con ezetimibe en estudios controlados con placebo, independientemente de la evaluación de causalidad: Trastornos del sistema musculoesquelético: artralgia; Infecciones e infestaciones: sinusitis; Cuerpo completo, trastornos generales: fatiga. Otras reacciones adversas comunicadas con en estudios clínicos controlados con placebo, independientemente de la evaluación de causalidad: Trastornos cardíacos: fibrilación auricular; Trastornos auditivos y del laberinto: vértigo; Trastornos del sistema digestivo: dolor abdominal, estreñimiento, dispepsia, flatulencia, gastritis; Trastornos de la piel y tejido subcutáneo: eczema, sarpullido; Trastornos endocrinos: diabetes mellitus; Infecciones e infestaciones: bronquitis, sinusitis, infecciones de las vías urinarias; Cuerpo completo, trastornos generales: astenia, edema/hinchazón; Trastornos psiquiátricos: insomnio. Análisis de Laboratorio Se han observado aumentos notables persistentes de las transaminasas hepáticas en suero [véase Advertencias y Precauciones (5.2)]. Se han notificado casos de elevaciones de la fosfatasa alcalina y la γ-glutamil transpeptidasa. Cerca de un 5% de los pacientes que tomaban mostraron elevaciones en los niveles de CK 3 o más veces el valor normal en una o más ocasiones. Estas elevaciones se atribuyeron a la fracción no cardíaca de la CK [véase Advertencias y Precauciones (5.1)]. 6.2 Experiencia Posmercadeo Dado que las reacciones indicadas más abajo se comunican voluntariamente de una población de tamaño incierto, generalmente no es posible calcular de manera fiable su frecuencia ni establecer una relación causal con la exposición al fármaco. En experiencias posmercadeo con VYTORIN, ezetimibe o se han notificado las siguientes reacciones adversas: prurito; alopecia; una diversidad de alteraciones cutáneas (p. ej., nódulos, pigmentación, sequedad de la piel o las membranas mucosas, alteraciones del pelo o las uñas); mareos; calambres musculares; mialgia; artralgia; pancreatitis; deterioro de la memoria; parestesia; neuropatía periférica; vómitos; náuseas; anemia; miopatía/rabdomiólisis [véase Advertencias y Precauciones (5.1)]; hepatitis/ictericia; insuficiencia hepática; depresión; colelitiasis; colecistitis; trombocitopenia; elevaciones de las transaminasas hepáticas; elevación de la creatina fosfocinasa. Se han notificado reacciones de hipersensibilidad, incluida anafilaxia, angioedema, sarpullido y urticaria. Además, rara vez se ha notificado un síndrome de hipersensibilidad aparente, caracterizado por uno o más de los siguientes síntomas/afecciones: anafilaxia, angioedema, síndrome de tipo lupus eritematoso, polimialgia reumática, dermatomiositis, vasculitis, púrpura, trombocitopenia, leucopenia, anemia hemolítica, ANA positivo, aumento de la velocidad de eritrosedimentación, eosinofilia, artritis, artralgia, urticaria, astenia, fotosensibilidad, fiebre, escalofríos, rubor, malestar general, disnea, necrólisis epidérmica tóxica, eritema multiforme, incluido el síndrome de Stevens-Johnson. VYTORIN (ezetimibe/) Tabletas 7 INTERACCIONES DE FÁRMACOS [Véase Farmacología Clínica (12.3).] VYTORIN 7.1 Interacciones con el CYP3A4 El riesgo de miopatía aumenta si se reduce la eliminación del componente de de VYTORIN. Por lo tanto, cuando se administra VYTORIN con un inhibidor del CYP3A4 (como los que se indican a continuación), los niveles plasmáticos elevados de actividad inhibitoria de la HMG-CoA reductasa pueden aumentar el riesgo de miopatía y rabdomiólisis, especialmente en presencia de dosis más altas de VYTORIN. [Véanse Advertencias y Precauciones (5.1) y Farmacología Clínica (12.3).] Itraconazol, ketoconazol y otros azoles antifúngicos Los antibióticos macrólidos eritromicina y claritromicina, y el antibiótico ketólido telitromicina Inhibidores de la proteasa del VIH El antidepresivo nefazodona Jugo de toronja en grandes cantidades (>1 cuarto de galón al día) Se debe evitar la administración concomitante de estos fármacos, sustancias y otros medicamentos cuya etiqueta indique que tienen un efecto inhibitorio potente sobre el CYP3A4, a menos que los beneficios de la politerapia superen el aumento en el riesgo. Si no se puede evitar el tratamiento con itraconazol, ketoconazol, eritromicina, claritromicina o telitromicina, se debe suspender la administración de VYTORIN en el transcurso del tratamiento. 7.2 Hipolipemiantes que Pueden Causar Miopatía Cuando Se Administran por Sí Solos El riesgo de miopatía aumenta con el gemfibrozil y, en menor medida, con otros fibratos y la niacina (ácido nicotínico) ( 1 g/día) [véase Advertencias y Precauciones (5.1)]. 7.3 Amiodarona o Verapamil El riesgo de miopatía/rabdomiólisis aumenta ante la administración concomitante de amiodarona o verapamil y dosis más elevadas de VYTORIN [véase Advertencias y Precauciones (5.1)]. 7.4 Colestiramina La administración concomitante de colestiramina redujo el AUC media del ezetimibe total aproximadamente en un 55%. La reducción en incrementos del C-LDL obtenida al añadir VYTORIN al tratamiento con colestiramina puede verse mermada por esta interacción. 7.5 Ciclosporina o Danazol El riesgo de miopatía/rabdomiólisis aumenta con la administración concomitante de ciclosporina o danazol, especialmente en presencia de dosis más altas de VYTORIN [véanse Advertencias y Precauciones (5.1) y Farmacología Clínica (12.3)]. Se debe proceder con cautela al administrar VYTORIN y ciclosporina concomitantemente, porque esta asociación aumenta la exposición al ezetimibe y la ciclosporina [véase Posología y Administración (2.6)]. En pacientes que reciben VYTORIN y ciclosporina se deben monitorear las concentraciones de ésta [véase Farmacología Clínica (12.3)]. El grado de aumento en la exposición al ezetimibe puede ser mayor en pacientes con disfunción renal grave. En los pacientes tratados con ciclosporina deben sopesarse detenidamente los posibles efectos de una mayor exposición al ezetimibe a causa del uso concomitante de ambos fármacos frente a la mejoría en las cifras de lípidos que ofrece el ezetimibe. [Véanse Advertencias y Precauciones (5.1) y Farmacología Clínica (12.3).] 7.6 Digoxina En un estudio, la administración concomitante de digoxina con ocasionó una ligera elevación de las concentraciones de digoxina en plasma. Se debe hacer un seguimiento apropiado de los pacientes que toman digoxina cuando se instaura VYTORIN. 7.7 Fibratos No se ha establecido la seguridad ni la eficacia de VYTORIN administrado con fibratos. Los fibratos pueden aumentar la excreción de colesterol a la bilis y causar colelitiasis. En un estudio preclínico en perros, el ezetimibe elevó el colesterol de la bilis de la vesícula biliar [véase Toxicología y/o Farmacología Animal (13.2)]. No se recomienda la coadministración de VYTORIN con fibratos hasta tanto no se haya estudiado su uso en pacientes. [Véase Advertencias y Precauciones (5.1).] 7.8 Anticoagulantes Cumarínicos La, mg/día, potenció moderadamente el efecto de los anticoagulantes cumarínicos: el tiempo de protrombina, informado como Índice Internacional Normalizado (IIN), aumentó de un valor basal de 1.7 a 1.8 y de 2.6 a 3.4 en los estudios en voluntarios sanos y de pacientes hipercolesterolémicos, respectivamente. Con otras estatinas, se ha notificado sangrado clínicamente evidente y/o aumento en el tiempo de protrombina en algunos pacientes que tomaban anticoagulantes cumarínicos concomitantemente. En dichos pacientes, se debe determinar el tiempo de protrombina 4
16 VYTORIN (ezetimibe/) Tabletas VYTORIN (ezetimibe/) Tabletas antes de iniciar VYTORIN y con la frecuencia suficiente durante el inicio del tratamiento para garantizar que no haya alteración significativa del tiempo de protrombina. Una vez que se haya documentado un tiempo estable de protrombina, se pueden vigilar los tiempos de protrombina a los intervalos recomendados, por lo general, para pacientes que reciben anticoagulantes cumarínicos. Se debe repetir el mismo procedimiento si se suspende o se cambia la dosis de VYTORIN. No se ha asociado el tratamiento con a sangrado ni a cambios en el tiempo de protrombina en pacientes que no toman anticoagulantes. En un estudio con doce hombres adultos sanos, la administración concomitante de ezetimibe (10 mg una vez al día) no afectó significativamente ni a la biodisponibilidad de la warfarina ni al tiempo de protrombina. Ha habido informes posmercadeo de aumentos en el IIN en pacientes a quienes se les ha añadido ezetimibe a la warfarina. La mayoría de estos pacientes tomaban también otros medicamentos. No se ha estudiado el efecto de VYTORIN sobre el tiempo de protrombina. 8 USO EN POBLACIONES ESPECÍFICAS 8.1 Embarazo Categoría X de embarazo. [Véase Contraindicaciones (4).] VYTORIN VYTORIN está contraindicado en mujeres embarazadas o con potencial de embarazo. Los hipolipemiantes no ofrecen ningún beneficio durante el embarazo, porque el colesterol y sus derivados son necesarios para el desarrollo normal del feto. Los niveles de colesterol y triglicéridos en suero aumentan durante el embarazo normal. La ateroesclerosis es un proceso crónico, y la suspensión de los medicamentos hipolipemiantes durante el embarazo debería tener un efecto leve en los resultados del tratamiento a largo plazo de la hipercolesterolemia primaria. No hay estudios adecuados y bien controlados sobre la administración de VYTORIN durante el embarazo; sin embargo, hay escasos informes de anomalías congénitas en lactantes que fueron expuestos a las estatinas in utero. Los estudios sobre reproducción en animales de la en ratas y conejos no mostraron ningún indicio de teratogenicidad. Los niveles séricos de colesterol y triglicéridos aumentan durante el embarazo normal, y el colesterol o sus derivados son esenciales para el desarrollo fetal. Ya que las estatinas, como la, disminuyen la síntesis del colesterol y, posiblemente, la síntesis de otras sustancias con actividad biológica derivadas del colesterol, VYTORIN podría perjudicar al feto si se lo administra a una mujer embarazada. Si se administra VYTORIN a una mujer embarazada, o que quede embarazada mientras toma este fármaco, debe informarse a la paciente de los posibles peligros a los que puede exponerse el feto. Debe instarse a las mujeres con potencial de embarazo que requieran tomar VYTORIN como tratamiento de un trastorno de los lípidos a que practiquen un método anticonceptivo eficaz. Las mujeres que estén buscando un embarazo deben considerar la posibilidad de suspender el tratamiento con VYTORIN. Si se produce el embarazo, debe suspenderse inmediatamente el tratamiento con VYTORIN. En estudios sobre el desarrollo embriofetal basados en la administración por sonda oral a ratas y conejos durante la organogénesis, no se observaron indicios de efectos embrioletales con las dosis estudiadas (250, 500, 1000 mg/kg/día). En ratas se observó una mayor incidencia de alteraciones óseas fetales frecuentes (par de costillas torácicas supernumerarias, centro de vértebras cervicales sin osificar, costillas acortadas) con dosis de 1000 mg/kg/día (~10 veces la exposición humana con 10 mg diarios según el AUC 0-24h del ezetimibe total). En conejos tratados con ezetimibe se observó una mayor incidencia de costillas torácicas supernumerarias con 1000 mg/kg/día (150 veces la exposición humana con 10 mg diarios según el AUC 0-24h del ezetimibe total). El ezetimibe atraviesa la placenta cuando se administran múltiples dosis orales a ratas y conejas preñadas. En los estudios en los que se coadministraron dosis múltiples de ezetimibe con estatinas a ratas y conejos durante la organogénesis, se constató una mayor exposición al ezetimibe y la estatina. Las alteraciones reproductivas aparecen con dosis más bajas en la politerapia que en la monoterapia. La no fue teratogénica en ratas o conejos que recibieron dosis (25, 10 mg/kg/día, respectivamente) equivalentes a 3 veces la exposición humana sobre la base del área de superficie, mg/m 2. Sin embargo, en estudios con otra estatina que guardaba relación estructural, se observaron malformaciones esqueléticas en ratas y ratones. Hay escasos informes de anomalías congénitas tras la exposición intrauterina a las estatinas. En un análisis 1 de aproximadamente 100 embarazos seguidos prospectivamente en mujeres expuestas a la o a otra estatina que guardaba relación estructural, las incidencias de anomalías congénitas, abortos espontáneos y muertes fetales/mortinatos no sobrepasaron lo que se esperaría en la población general. El número de casos es adecuado sólo para excluir un aumento de 3 a 4 veces de las anomalías congénitas respecto a la incidencia de fondo. En un 89% de los embarazos seguidos prospectivamente, el tratamiento con el fármaco se inició antes del embarazo y se descontinuó en algún momento durante el primer trimestre cuando se identificó el embarazo. 8.3 Madres Lactantes No se sabe si la se excreta en la leche humana. Debido a que una pequeña cantidad de otro fármaco de esta misma clase se excreta en la leche humana, y al potencial de reacciones adversas graves en los bebés lactantes, las mujeres que toman no deben amamantar a sus bebés. Se debe decidir si se suspende la lactancia o se deja de administrar el fármaco, teniendo en cuenta la importancia del tratamiento para la madre [véase Contraindicaciones (4)]. En estudios en ratas, la exposición al ezetimibe total en las crías amamantadas llegó hasta la mitad de la observada en el plasma materno. No se sabe si el ezetimibe o la se excretan en la leche materna en el ser humano. Debido a que una pequeña cantidad de otro fármaco de la misma clase que la se excreta en la leche humana, y al potencial de reacciones adversas graves en los bebés lactantes, las mujeres que amamantan no deben tomar VYTORIN [véase Contraindicaciones (4)]. 8.4 Uso Pediátrico Se han evaluado los efectos de la coadministración de ezetimibe y (n=126) en comparación con en monoterapia (n=122) en adolescentes de ambos sexos afectados de hipercolesterolemia familiar heterocigótica (HFHe). En un estudio multicéntrico controlado y con doble enmascaramiento, seguido de una fase abierta, se asignó aleatoriamente a 142 niños y 106 niñas posmenárquicas de 10 a 17 años de edad (media de edad: 14.2 años; 43% niñas, 82% de raza blanca, 4% asiáticos, 2% de raza negra, 13% de raza mixta) afectados de HFHe a recibir ya sea ezetimibe coadministrado con o en monoterapia. La inclusión en el estudio exigió 1) un nivel basal de C-LDL entre 160 y 400 mg/dl y 2) antecedentes médicos y una presentación clínica indicativos de HFHe. La media del valor basal de C-LDL fue 225 mg/dl (intervalo: mg/dl) en el grupo de ezetimibe coadministrado con, en comparación con 219 mg/dl (intervalo: mg/dl) en el grupo de en monoterapia. Los pacientes recibieron ezetimibe y coadministrados (10 mg, 20 mg o 40 mg) o en monoterapia (10 mg, 20 mg o 40 mg) durante 6 semanas; ezetimibe coadministrado con 40 mg de o 40 mg de en monoterapia durante las siguientes 27 semanas, y ezetimibe y coadministrados y sin enmascaramiento (10 mg, 20 mg o 40 mg) durante 20 semanas de allí en adelante. En el Cuadro 3 se resumen los resultados del estudio obtenidos en la Semana 6. Los resultados obtenidos en la Semana 33 concordaron con los de la Semana 6. Cuadro 3 Media de la Diferencia Porcentual en la Semana 6 entre el Grupo Conjunto de Coadministrado con y el Grupo Conjunto de en Monoterapia en Pacientes Adolescentes Afectados de Hipercolesterolemia Familiar Heterocigótica C-Total C-LDL Apo B C-no HDL TG a C-HDL Media de la diferencia porcentual entre -12% -15% -12% -14% -2% +0.1% grupos de tratamiento Intervalo de (-15%, -9%) (-18%, -12%) (-15%, -9%) (-17%, -11%) (-9, +4) (-3, +3) Confianza del 95% a Para los triglicéridos, mediana de la variación porcentual respecto al valor basal Entre el inicio del ensayo y el final de la Semana 33, 7 (6%) de los pacientes del grupo de ezetimibe coadministrado con y 2 (2%) de los pacientes del grupo de en monoterapia abandonaron el estudio a causa de una reacción adversa. Durante el ensayo, se observaron elevaciones de las transaminasas hepáticas (dos determinaciones consecutivas de ALT y/o AST 3 veces el LSN) en cuatro (3%) pacientes del grupo de ezetimibe coadministrado con y en dos (2%) pacientes del grupo de en monoterapia. Se produjeron elevaciones de CPK ( 10 veces el LSN) en dos (2%) pacientes del grupo de ezetimibe coadministrado con y en ninguno de los pacientes del grupo de en monoterapia. En este estudio controlado limitado no se detectó ningún efecto significativo sobre el crecimiento ni la maduración sexual de los adolescentes de ambos sexos, ni tampoco sobre la duración del ciclo menstrual en las niñas. No se ha estudiado en adolescentes la coadministración de ezetimibe con en dosis superiores a los 40 mg/día. Además, no se ha estudiado VYTORIN en pacientes menores de 10 años de edad ni en niñas premenárquicas. Según las concentraciones de ezetimibe total (ezetimibe + ezetimibe-glucurónido), no existen diferencias farmacocinéticas entre los adolescentes y los adultos. No se dispone de datos farmacocinéticos en la población pediátrica menor de 10 años de edad. 1 Manson, J.M., Freyssinges, C., Ducrocq, M.B., Stephenson, W.P., Postmarketing Surveillance of Lovastatin and Simvastatin Exposure During Pregnancy [Farmacovigilancia de la exposición a lovastatina y durante el embarazo], Reproductive Toxicology, 10(6): ,
17 VYTORIN (ezetimibe/) Tabletas VYTORIN (ezetimibe/) Tabletas No se ha estudiado la farmacocinética de la en la población pediátrica. 8.5 Uso Geriátrico Entre los 10,189 pacientes que recibieron VYTORIN en los estudios clínicos, 3242 (32%) tenían 65 años de edad o más (esto incluyó a 844 [8%] mayores de 75 años de edad). No se observaron diferencias generales en la seguridad y eficacia en estos sujetos en comparación con sujetos más jóvenes, y otras experiencias clínicas comunicadas no han identificado diferencias en las respuestas entre los pacientes ancianos y más jóvenes; sin embargo, no se puede descartar la posibilidad de que algunas personas de edad más avanzada presenten una mayor sensibilidad. Ya que la edad avanzada ( 65 años) es un factor predisponente de miopatía, VYTORIN debe recetarse con cautela a la población geriátrica. [Véase Farmacología Clínica (12.3).] 8.6 Disfunción Renal Se debe proceder con cautela al administrar VYTORIN a pacientes con disfunción renal grave. [Véase Posología y Administración (2.4).] 8.7 Disfunción Hepática Está contraindicado VYTORIN en pacientes afectados de enfermedad hepática activa o elevaciones persistentes y de origen desconocido de transaminasas hepáticas. No se recomienda VYTORIN a pacientes con disfunción hepática moderada o grave. [Véanse Contraindicaciones (4) y Advertencias y Precauciones (5.2).] 10 SOBREDOSIS VYTORIN No se puede recomendar un tratamiento específico para la sobredosis de VYTORIN. En caso de sobredosis deben instaurarse medidas sintomáticas y de soporte. En estudios clínicos, la administración de 50 mg/día de ezetimibe a 15 sujetos sanos durante un máximo de 14 días o de 40 mg/día a 18 pacientes con hiperlipidemia primaria durante un máximo de 56 días se toleró bien en general. Se han notificado algunos casos de sobredosis; la mayoría no se han asociado a experiencias adversas. Las experiencias adversas notificadas no han sido graves. Se observó letalidad significativa en ratones tras la administración oral de una única dosis de 9 g/m 2. No se observaron indicios de letalidad en ratas o perros tratados con dosis de 30 y 100 g/m 2, respectivamente. No se observaron signos diagnósticos específicos en roedores. A estas dosis, los únicos signos observados en perros fueron emesis y heces mucosas. Se ha informado de unos cuantos casos de sobredosis de ; la dosis máxima ingerida fue de 3.6 g. Todos los pacientes se recuperaron sin secuelas. Al presente no se sabe si la y sus metabolitos son dializables en el ser humano. 11 DESCRIPCIÓN VYTORIN contiene ezetimibe, un inhibidor selectivo de la absorción intestinal de colesterol y los fitoesteroles afines, y, un inhibidor de la HMG-CoA reductasa. El nombre químico del ezetimibe es 1-(4-fluorofenil)-3(R)-[3-(4-fluorofenil)-3(S)- hidroxipropil]-4(s)-(4-hidroxifenil)-2-azetidinona. La fórmula empírica es C 24 H 21 F 2 NO 3 y su peso molecular es El ezetimibe es un polvo blanco y cristalino, fácilmente soluble a muy soluble en etanol, metanol y acetona, y prácticamente insoluble en agua. Su fórmula estructural es: La, una lactona inactiva, se hidroliza a la correspondiente forma β-hidroxiácido, que es un inhibidor de la HMG-CoA reductasa. La es ácido butanoico, 2,2-dimetil-,1,2,3,7,8,8a-hexahidro-3,7-dimetil-8-[2-(tetrahidro-4-hidroxi-6-oxo- 2H-piran-2-il)-etil]-1-naftalenil éster, [1S-[1α,3α,7β,8β(2S*,4S*),-8aβ]]. La fórmula empírica de la es C25H38O5 y su peso molecular es La es un polvo cristalino, no higroscópico, de blanco a blanquecino, prácticamente insoluble en agua y fácilmente soluble en cloroformo, metanol y etanol. Su fórmula estructural es: VYTORIN está disponible para administración oral en forma de tabletas que contienen 10 mg de ezetimibe y 10 mg de (VYTORIN 10/10), 20 mg de (VYTORIN 10/20), 40 mg de (VYTORIN 10/40) u 80 mg de (VYTORIN 10/80). Cada tableta contiene los siguientes ingredientes inactivos: butilhidroxianisol NF, ácido cítrico monohidratado USP, croscarmelosa sódica NF, hipromelosa USP, lactosa monohidratada NF, estearato de magnesio NF, celulosa microcristalina NF y galato de propilo NF. 12 FARMACOLOGÍA CLÍNICA 12.1 Mecanismo de Acción VYTORIN El colesterol plasmático proviene de la absorción intestinal y de la síntesis endógena. VYTORIN contiene ezetimibe y, dos compuestos hipolipemiantes que tienen mecanismos de acción complementarios. VYTORIN reduce las concentraciones elevadas de C-total, C-LDL, Apo B, TG y C-no HDL y aumenta las de C-HDL mediante la doble inhibición de la absorción y la síntesis del colesterol. El ezetimibe reduce la colesterolemia inhibiendo la absorción de colesterol en el intestino delgado. Se ha demostrado que el objetivo molecular de ezetimibe es el transportador de esteroles Niemann-Pick C1-Like 1 (NPC1L1), el cual interviene en la absorción del colesterol y los fitoesteroles en el intestino. En un estudio clínico de 2 semanas con 18 pacientes hipercolesterolémicos, el ezetimibe inhibió la absorción intestinal del colesterol en un 54%, en comparación con el placebo. El ezetimibe no mostró efectos clínicamente significativos sobre las concentraciones plasmáticas de las vitaminas liposolubles A, D y E, y no afectó a la producción suprarrenal de hormonas esteroides. El ezetimibe se localiza en el borde en cepillo del intestino delgado e inhibe la absorción de colesterol, lo que conduce a un menor aporte de colesterol intestinal al hígado. Ello provoca una disminución de las reservas hepáticas de colesterol y un aumento del aclaramiento de colesterol de la sangre; este mecanismo particular es complementario al de las estatinas [véase Estudios Clínicos (14)]. La es un profármaco que, tras ser administrado, se hidroliza al β- hidroxiácido (o ácida), que es su forma activa. La es un inhibidor específico de la 3-hidroxi-3-metilglutaril-coenzima A (HMG-CoA) reductasa, que es la enzima que cataliza la conversión de la HMG-CoA a mevalonato, un paso temprano y determinante de la velocidad en la vía biosintética del colesterol. Además, la reduce las lipoproteínas de muy baja densidad (VLDL) y los TG, y aumenta el C-HDL Farmacodinamia Los estudios clínicos han demostrado que la presencia de niveles elevados de C- total, C-LDL y Apo B (principal proteína constituyente del LDL) favorece la aterosclerosis en seres humanos. Además, las concentraciones bajas de C-HDL están asociadas a la aparición de aterosclerosis. En estudios epidemiológicos se ha establecido que la morbilidad y la mortalidad cardiovasculares varían en relación directa con la concentración de C-total y C-LDL e inversa con la concentración de C-HDL. Al igual que las LDL, las lipoproteínas ricas en triglicéridos y enriquecidas en colesterol, como las VLDL, las lipoproteínas de densidad intermedia (IDL) y los remanentes también pueden favorecer la aterosclerosis. No se ha determinado el efecto independiente de elevar el C-HDL o reducir los TG sobre el riesgo de morbilidad y mortalidad coronaria y cardiovascular Farmacocinética Los resultados de un estudio de bioequivalencia en sujetos sanos demostraron que las tabletas combinadas de VYTORIN (ezetimibe/) 10 mg/10 mg a 10 mg/80 mg tienen la misma bioequivalencia que la coadministración de las correspondientes dosis de ezetimibe (ZETIA ) y (ZOCOR ) en forma de tabletas individuales. 6
18 VYTORIN (ezetimibe/) Tabletas Absorción Tras la administración oral, el ezetimibe se absorbe y se conjuga en gran proporción con un glucurónido fenólico farmacológicamente activo (ezetimibe-glucurónido). Se encontró que la disponibilidad del β-hidroxiácido en la circulación sistémica tras la administración de una dosis oral de fue menor del 5% de la dosis, lo que concuerda con la alta fracción de extracción de las estatinas en el primer paso hepático. Efecto de los Alimentos en la Absorción Oral La administración concomitante de alimentos (comidas ricas en grasas o sin grasas) no influyó en el grado de absorción del ezetimibe cuando éste se administró como tabletas de 10 mg. La C máx del ezetimibe aumentó en un 38% con la ingestión de comidas ricas en grasas. En comparación con el estado de ayuno, los perfiles plasmáticos de los inhibidores activos y los inhibidores totales de la HMG-CoA reductasa no se vieron afectados cuando la se administró inmediatamente antes de una comida baja en grasa como la que recomienda la Asociación Estadounidense del Corazón. Distribución El ezetimibe y el ezetimibe-glucurónido se unen en gran proporción (>90%) a las proteínas del plasma humano. Tanto la como su metabolito β-hidroxiácido se unen en gran proporción (aproximadamente 95%) a las proteínas plasmáticas humanas. Cuando se administró radiomarcada a ratas, la radiactividad procedente de la cruzó la barrera hematoencefálica. Metabolismo y Excreción El ezetimibe se metaboliza fundamentalmente en el intestino delgado y el hígado mediante la conjugación con glucurónidos y se elimina luego por vía biliar y renal. En todas las especies evaluadas se ha observado un metabolismo oxidativo mínimo. En el ser humano el ezetimibe se metaboliza rápidamente a ezetimibe-glucurónido. El ezetimibe y el ezetimibe-glucurónido son los principales compuestos derivados del fármaco detectados en el plasma y constituyen del 10 al 20% y del 80 al 90%, respectivamente, de la concentración plasmática total de fármaco. Tanto el ezetimibe como el ezetimibe-glucurónido se eliminan del plasma, con una semivida en ambos casos de 22 horas aproximadamente. Los perfiles de la concentración plasmática a lo largo del tiempo muestran múltiples picos, lo que indica un reciclado enterohepático. Tras la administración oral de 14 C-ezetimibe (20 mg) a sujetos humanos, el ezetimibe total (ezetimibe + ezetimibe-glucurónido) representó aproximadamente el 93% de la radiactividad total en plasma. Al cabo de 48 horas no había niveles de radiactividad detectables en plasma. A lo largo de un periodo de recolección de 10 días se recuperó en heces y orina aproximadamente el 78% y el 11%, respectivamente, de la radiactividad administrada. En las heces, el principal componente fue el ezetimibe, que representó el 69% de la dosis administrada; en la orina predominó el ezetimibe-glucurónido, que representó el 9% de la dosis administrada. La es una lactona que se hidroliza fácilmente in vivo al correspondiente β-hidroxiácido, un inhibidor potente de la HMG-CoA reductasa. La inhibición de la HMG-CoA reductasa es la base para un ensayo en estudios farmacocinéticos de los metabolitos del β-hidroxiácido (inhibidores activos) y, después de la hidrólisis básica, de los inhibidores activos más los latentes (los inhibidores totales) en el plasma después de la administración de la. Los metabolitos activos principales de la presentes en el plasma humano son el β-hidroxiácido de la y sus derivados 6 -hidroxi, 6 -hidroximetilo y 6 -exometileno. Después de una dosis oral de marcada con 14 C en humanos, el 13% de la dosis se eliminó en la orina y el 60%, en las heces. Las concentraciones plasmáticas de radiactividad total ( más los metabolitos de 14 C) llegaron a su punto máximo a las 4 horas y disminuyeron rápidamente a cerca de un 10% del punto máximo a las 12 horas posdosis. VYTORIN (ezetimibe/) Tabletas Poblaciones Específicas Pacientes Geriátricos En un estudio de dosis múltiples en el que se administraron 10 mg de ezetimibe una vez al día durante 10 días, las concentraciones plasmáticas de ezetimibe total fueron unas 2 veces superiores en los pacientes ancianos (>65 años) sanos que en los más jóvenes. En un estudio de 16 pacientes ancianos de 70 a 78 años de edad que recibieron en dosis de 40 mg/día, el nivel plasmático medio de la actividad inhibitoria de la HMG-CoA reductasa fue aproximadamente un 45% mayor que el observado en 18 pacientes de años de edad. Pacientes Pediátricos: [Véase Uso Pediátrico (8.4).] Sexo En un estudio de dosis múltiples en el que se administraron 10 mg de ezetimibe una vez al día durante 10 días, las concentraciones plasmáticas de ezetimibe total fueron ligeramente superiores (<20%) en las mujeres que en los hombres. Raza Según un metanálisis de los estudios farmacocinéticos con dosis múltiples, no hubo diferencias farmacocinéticas entre los sujetos negros y los caucásicos. Los estudios con sujetos asiáticos indicaron que la farmacocinética del ezetimibe fue similar a la observada en sujetos de raza blanca. Disfunción Hepática Después de una dosis única de 10 mg de ezetimibe, la exposición media (según el área bajo la curva [AUC]) del ezetimibe total fue aproximadamente 1.7 veces mayor en los pacientes con disfunción hepática leve (puntuación de Child-Pugh entre 5 y 6) que en los sujetos sanos. El AUC media del ezetimibe total y el ezetimibe aumentó unas 3 a 4 veces y 5 a 6 veces, respectivamente, en los pacientes con disfunción hepática moderada (puntuación de Child-Pugh entre 7 y 9) o grave (puntuación de Child-Pugh entre 10 y 15). En un estudio de dosis múltiples de 14 días de duración (10 mg diarios), el AUC media del ezetimibe total y el ezetimibe fue aproximadamente 4 veces mayor en los pacientes con disfunción hepática moderada que en los sujetos sanos. Disfunción Renal Tras la administración de una dosis única de 10 mg de ezetimibe a pacientes con enfermedad renal grave (n=8; CrCl media 30 ml/min/1.73 m 2 ), los valores medios del AUC del ezetimibe total y el ezetimibe fueron aproximadamente 1.5 veces mayores que los observados en sujetos sanos (n=9). En estudios farmacocinéticos realizados con otra estatina cuya ruta principal de eliminación es similar a la de la se ha sugerido que, para un nivel dado de dosis, se puede lograr una mayor exposición sistémica en pacientes con disfunción renal grave (determinada según el aclaramiento de creatinina). Interacciones de Fármacos [Véase también Interacciones de Fármacos (7).] No se observó ninguna interacción farmacocinética clínicamente significativa cuando se coadministró ezetimibe con. No se han realizado estudios específicos de interacciones farmacocinéticas de medicamentos con VYTORIN. Citocromo P450: En un estudio basado en la administración simultánea de varios fármacos combinados (cocktail study) a doce hombres adultos sanos, el ezetimibe no tuvo efectos significativos sobre una serie de fármacos de sondeo (cafeína, dextrometorfano, tolbutamida y midazolam IV) que han demostrado ser metabolizados por el citocromo P450 (1A2, 2D6, 2C8/9 y 3A4). Esto indica que el ezetimibe no inhibe ni induce estas isoenzimas del citocromo P450, por lo que es improbable que afecte al metabolismo de los fármacos metabolizados por dichas enzimas. En un estudio de 12 voluntarios sanos, la en dosis de 80 mg no tuvo ningún efecto en el metabolismo de los sustratos de sondeo de la isoforma 3A4 del citocromo P450 (CYP3A4) midazolam y eritromicina. Esto indica que la no es un inhibidor del CYP3A4 y, por lo tanto, no se espera que afecte a los niveles plasmáticos de otros fármacos metabolizados por el CYP3A4. Aunque el mecanismo no se comprende totalmente, la ciclosporina ha demostrado aumentar el AUC de la estatinas. El aumento en el AUC de la ácida presumiblemente se debe, en parte, a la inhibición del CYP3A4. La es un sustrato para el CYP3A4. Los inhibidores del CYP3A4 pueden elevar las concentraciones plasmáticas de la actividad inhibitoria de la HMG-CoA reductasa y aumentar el riesgo de miopatía. [Véanse Advertencias y Precauciones (5.1); Interacciones de Fármacos (7.1).] 7
19 VYTORIN (ezetimibe/) Tabletas VYTORIN (ezetimibe/) Tabletas Cuadro 4 Efecto de Fármacos Coadministrados en el Total Fármaco Coadministrado y Total * Esquema Posológico Variación del AUC Variación de la C máx Ciclosporina: requiere dosis estable ( mg dos veces al día),** 240% 290% Fenofibrato, 200 mg una vez al día, 14 días 48% 64% Gemfibrozil, 600 mg dos veces al día, 7 días 64% 91% Colestiramina, 4 g dos veces al día, 14 días 55% 4% Antiácido con hidróxidos de aluminio y de 4% 30% magnesio, dosis única Cimetidina, 400 mg dos veces al día, 7 días 6% 22% Glipizida, 10 mg, dosis única 4% 8% Estatinas Lovastatina 20 mg una vez al día, 7 días 9% 3% Provastatina 20 mg una vez al día, 14 días 7% 23% Atorvastatina 10 mg una vez al día, 14 días 2% 12% Rosuvastatina 10 mg una vez al día, 14 días 13% 18% Fluvastatina 20 mg una vez al día, 14 días 19% 7% * Sobre la base de una dosis de 10 mg de ezetimibe **Pacientes postrasplante de riñón con función renal normal o leve disfunción renal. En otro estudio, un paciente receptor de trasplante renal con insuficiencia renal grave (aclaramiento de creatinina 13.2 ml/min/1.73 m 2 ) que estaba recibiendo numerosos medicamentos, incluida la ciclosporina, presentó una exposición 12 veces mayor al ezetimibe total que los sujetos sanos. Véase 7. Interacciones de Fármacos Supralox, 20 ml Cuadro 5 Efecto de la Coadministración de en la Exposición Sistémica a Otros Fármacos Fármaco Coadministrado y Esquema Posológico Variación del AUC Variación de la C máx Esquema Posológico de del Fármaco del Fármaco Coadministrado Warfarina, 25 mg, dosis 10 mg una vez 2% (R-warfarina) 3% (R-warfarina) única el Día 7 al día, 11 días 4% (S-warfarina) 1% (S-warfarina) Digoxina, 0.5 mg, 10 mg una vez al día, 2% 7% dosis única 8 días Gemfibrozil, 600 mg dos 10 mg una vez al día, 1% 11% veces al día, 7 días 7 días Etinil estradiol y 10 mg una vez al día, Etinil estradiol Etinil estradiol Levonorgestrel, una vez Días 8-14 del ciclo 0% 9% al día, 21 días de 21 días de Levonorgestrel Levonorgestrel anticonceptivos orales 0% 5% Glipizida, 10 mg los 10 mg una vez al día, Días 2-9 3% 5% Días 1 y 9 Fenofibrato, 200 mg una 10 mg una vez al día, 14 días 11% 7% vez al día, 14 días Ciclosporina, 100 mg, 20 mg una vez al día, 8 días 15% 10% dosis única el Día 7 Estatinas Lovastatina 20 mg una vez 10 mg una vez al día, 7 días 19% 3% al día, 7 días Provastatina 20 mg una vez 10 mg una vez al día, 14 días 20% 24% al día, 14 días Atorvastatina 10 mg una vez 10 mg una vez al día, 14 días 4% 7% al día, 14 días Rosuvastatina 10 mg una vez 10 mg una vez al día, 14 días 19% 17% al día, 14 días Fluvastatina 20 mg una vez 10 mg una vez al día, 14 días 39% 27% al día, 14 días Véase 7. Interacciones de Fármacos Cuadro 6 Efecto de la Coadministración de Fármacos o Jugo de Toronja en la Exposición Sistémica a la Fármaco Coadministrado o Jugo de Toronja Dosis Coadministrada de Fármaco o Jugo de Toronja Dosis de Cociente de las Medias Geométricas (Cociente* con / sin fármaco coadministrado) Sin Efecto = 1.00 AUC Evítese tomar con VYTORIN [véase Advertencias y Precauciones (5.1)] Telitromicina 200 mg una vez al día por 4 días Nelfinavir Itraconazol 1250 mg dos veces al día por 14 días 200 mg una vez al día por 4 días 80 mg ácida 20 mg una vez al día por 28 días * Resultados basados en análisis químicos salvo en el caso del propranolol, según se indica. Los resultados podrían ser representativos de los siguientes inhibidores de CYP3A4: ketoconazol, eritromicina, claritromicina, inhibidores de la proteasa del VIH y nefazodona. ácida hace referencia al β-hidroxiácido de la. No se ha estudiado el efecto de cantidades de jugo de toronja intermedias entre las utilizadas en estos dos estudios farmacocinéticos de. Doblemente concentrado: una lata de concentrado congelado diluido con una lata de agua. Se administró el jugo de toronja tres veces al día por 2 días, y 200 ml junto con una dosis única de y 30 y 90 minutos después de una única dosis de el Día 3. # Concentración normal: una lata de concentrado congelado diluido con 3 latas de agua. Se administró el jugo de toronja con el desayuno durante 3 días, y la se administró la noche del Día TOXICOLOGÍA NO CLÍNICA 13.1 Carcinogénesis, Mutagénesis, Deterioro de la Fertilidad VYTORIN No se han realizado estudios de carcinogenicidad ni de fertilidad en animales con la combinación de ezetimibe y. La combinación de ezetimibe con C máx ácida mg ácida Evítese tomar >1 cuarto de galón de jugo de toronja con VYTORIN [véase Advertencias y Precauciones (5.1)] Jugo de Toronja (dosis alta) 200 ml, jugo doblemente concentrado, tres 60 mg, dosis única ácida 7 16 veces al día Jugo de Toronja (dosis baja) 8 onzas (cerca de 237 ml), concentración 20 mg, dosis única ácida normal # Evítese tomar con VYTORIN. Si VYTORIN se coadministra con gemfibrozil, la dosis no debe superar los 10/10 mg al día, sobre la base de experiencias clínicas y/o posmercadeo con [véase Advertencias y Precauciones (5.1)] Gemfibrozil 600 mg dos veces al día por 3 días 40 mg ácida Evítese tomar con >10/20 mg de VYTORIN, sobre la base de experiencias clínicas y/o posmercadeo con [véase Advertencias y Precauciones (5.1)] Verapamil SR 240 mg una vez al 80 mg el Día 10 día los Días 1-7, luego ácida mg dos veces al día los Días 8-10 No se requiere efectuar ningún ajuste de dosis para los siguientes fármacos: Fenofibrato Niacina de liberación prolongada Diltiazem Amlodipina Propranolol 160 mg una vez al día x 14 días 80 mg una vez al día los Días g, dosis única 20 mg, dosis única 120 mg dos veces al día por 10 días 10 mg una vez al día x 10 días 80 mg, dosis única ácida ácida 80 mg el Día 10 ácida 80 mg el Día 10 ácida 80 mg, dosis inhibidor total única inhibidor activo de 33.6 a 21.1 ng eq/ml de 7.0 a 4.7 ng eq/ml 8
20 VYTORIN (ezetimibe/) Tabletas VYTORIN (ezetimibe/) Tabletas no mostró indicios de mutagenicidad in vitro en una prueba microbiana de mutagenicidad (Ames) que empleó Salmonella typhimurium y Escherichia coli con o sin activación metabólica. No se observaron indicios de clastogenicidad in vitro en una prueba de aberraciones cromosómicas en linfocitos humanos de sangre periférica con ezetimibe y con o sin activación metabólica. No hubo indicios de genotoxicidad a dosis de hasta 600 mg/kg con la combinación de ezetimibe y (1:1) en la prueba in vivo de micronúcleo de ratón. Se realizó un estudio de carcinogénesis de 104 semanas en ratas que recibieron ezetimibe en la dieta en dosis de hasta 1500 mg/kg/día (machos) y 500 mg/kg/día (hembras) (~20 veces la exposición humana con 10 mg diarios según el AUC 0-24h del ezetimibe total). También se realizó un estudio de carcinogénesis de 104 semanas en ratones que recibieron ezetimibe en la dieta en dosis de hasta 500 mg/kg/día (>150 veces la exposición humana con 10 mg diarios según el AUC 0-24h del ezetimibe total). No se observaron aumentos estadísticamente significativos de la incidencia de tumores en las ratas y los ratones tratados con el fármaco. No se observaron signos de mutagénesis in vitro en un ensayo de mutagénesis microbiana (Ames) con Salmonella typhimurium y Escherichia coli con o sin activación metabólica. No se observaron signos de clastogénesis en un ensayo in vitro de aberraciones cromosómicas en linfocitos de sangre periférica humana con o sin activación metabólica. Tampoco se observaron signos de genotoxicidad en el ensayo in vivo de micronúcleos de ratón. En estudios de fertilidad basados en la administración de ezetimibe por sonda oral a ratas, no se observaron signos de toxicidad de reproducción en machos ni en hembras con dosis de hasta 1000 mg/kg/día (~7 veces la exposición humana con 10 mg diarios según el AUC 0-24h del ezetimibe total). En un estudio de carcinogenicidad de 72 semanas, se administraron dosis diarias de 25, 100 y 400 mg/kg de peso corporal de a ratones, lo que dio como resultado niveles plasmáticos medios del fármaco aproximadamente 1, 4 y 8 veces más altos que el nivel plasmático medio del fármaco en humanos, respectivamente (como actividad inhibitoria total a partir del AUC) después de una dosis oral de 80 mg. Los carcinomas hepáticos aumentaron significativamente en las hembras que recibieron dosis altas y en los machos que recibieron dosis medianas y altas, observándose una incidencia máxima del 90% en los machos. La incidencia de adenomas hepáticos aumentó significativamente en las hembras que recibían dosis medianas y altas. El tratamiento con el fármaco también aumentó significativamente la incidencia de adenomas del pulmón en los machos y hembras que recibían dosis medianas y altas. Los adenomas de la glándula harderiana (una glándula del ojo de los roedores) fueron significativamente mayores en los ratones que recibían dosis altas que en los controles. No se observó ningún indicio de un efecto tumorígeno con 25 mg/kg/día. En un estudio aparte de carcinogenicidad de 92 semanas en ratones, con dosis de hasta 25 mg/kg/día, no se observó ningún indicio de efecto tumorígeno (los niveles plasmáticos medios del fármaco fueron 1 vez más altos que en los humanos que recibieron 80 mg de según lo determinado por el AUC). En un estudio de dos años en ratas a 25 mg/kg/día, hubo un aumento estadísticamente significativo en la incidencia de adenomas foliculares de la glándula tiroides en ratas hembras expuestas a niveles de aproximadamente 11 veces más altos que en humanos que recibieron 80 mg de (según lo determinado por el AUC). Un segundo estudio de dos años sobre carcinogenicidad en ratas con dosis de 50 y 100 mg/kg/día produjo adenomas y carcinomas hepatocelulares (en ratas hembras con ambas dosis y en ratas machos con 100 mg/kg/día). Los adenomas de las células foliculares de la glándula tiroides aumentaron en los machos y en las hembras con ambas dosis; los carcinomas de las células foliculares de la glándula tiroides aumentaron en las hembras con 100 mg/kg/día. El aumento en la incidencia de neoplasmas de tiroides parece concordar con los hallazgos de otras estatinas. Estos niveles de tratamiento representaron niveles plasmáticos del fármaco (AUC) aproximadamente 7 y 15 veces (machos) y 22 y 25 veces (hembras) mayores que la exposición plasmática media del fármaco en seres humanos después de una dosis diaria de 80 mg. No se observó ningún indicio de mutagenicidad en una prueba de mutagenicidad microbiana (Ames) con o sin activación metabólica del hígado en ratas o en ratones. Tampoco se observaron indicios de daños al material genético en un ensayo de elución alcalina in vitro en el que se utilizaron hepatocitos de rata, ni en un estudio sobre mutaciones directas de células V-79 de mamífero, ni en un estudio in vitro sobre aberraciones cromosómicas de las células CHO, ni en un ensayo in vivo sobre aberraciones cromosómicas en la médula ósea de ratones. Hubo una disminución de la fertilidad en las ratas machos tratadas con durante 34 semanas con 25 mg/kg de peso corporal (4 veces el nivel máximo de exposición humana, a partir del AUC, en pacientes que toman 80 mg/día); sin embargo, no se observó este efecto durante un estudio de fertilidad subsiguiente en el que se administró la a este mismo nivel de dosis en ratas machos durante 11 semanas (el ciclo completo de espermatogénesis incluyendo la maduración del epidídimo). No se observaron cambios microscópicos en los testículos de las ratas en ninguno de los dos estudios. Con 180 mg/kg/día (lo que produce niveles de exposición 9 22 veces más altos que los niveles en seres humanos que toman 80 mg/día, a partir del área de superficie, mg/m 2 ), se observó degeneración de los túbulos seminíferos (necrosis y pérdida del epitelio espermatogénico). En perros, hubo atrofia testicular relacionada con el fármaco, disminución de la espermatogénesis, degeneración espermatocítica y formación de células gigantes con dosis de 10 mg/kg/día (aproximadamente 2 veces la exposición humana, a partir del AUC, a 80 mg/día). No está clara la importancia clínica de estos hallazgos Toxicología y/o Farmacología Animal Toxicidad del SNC Se observó degeneración del nervio óptico en perros clínicamente normales tratados con durante 14 semanas con 180 mg/kg/día, una dosis que produjo niveles plasmáticos medios del fármaco alrededor de 12 veces mayores que el nivel plasmático medio del fármaco en seres humanos que toman 80 mg/día. Un fármaco químicamente similar en esta clase también produjo degeneración del nervio óptico (degeneración walleriana de las fibras retinogeniculadas) en perros clínicamente normales, de manera dependiente de la dosis, comenzando a 60 mg/kg/día, una dosis que produjo niveles plasmáticos medios del fármaco alrededor de 30 veces mayores que el nivel plasmático medio del fármaco en seres humanos que toman la dosis recomendada más alta (medido según la actividad inhibitoria enzimática total). Este mismo fármaco también produjo degeneración vestibulococlear tipo walleriana y cromatólisis de las células ganglionares retinianas en perros tratados durante 14 semanas con 180 mg/kg/día, una dosis que dio como resultado un nivel plasmático medio del fármaco similar al observado con la dosis de 60 mg/kg/día. Se observaron lesiones vasculares del SNC, caracterizadas por hemorragia y edema perivasculares, infiltración de células mononucleares en los espacios perivasculares, depósitos perivasculares de fibrina y necrosis de vasos pequeños, en perros tratados con a dosis de 360 mg/kg/día, una dosis que produjo niveles plasmáticos medios del fármaco aproximadamente 14 veces más altos que los niveles plasmáticos medios del fármaco en humanos que toman 80 mg/día. Se han observado lesiones vasculares del SNC similares con varios otros fármacos de esta clase. Se observaron cataratas en ratas hembras después de dos años de tratamiento con 50 y 100 mg/kg/día (22 y 25 veces el AUC humana a 80 mg/día, respectivamente) y en perros después de los tres meses a 90 mg/kg/día (19 veces) y a los dos años a 50 mg/kg/día (5 veces). Se evaluó el efecto hipocolesterolemiante del ezetimibe en modelos del metabolismo humano del colesterol basados en macacos de la India (Macaca mulatta), perros, ratas y ratones alimentados con una dieta rica en colesterol. Se constató que la DE 50 del ezetimibe para inhibir la elevación de las concentraciones plasmáticas del colesterol en monos fue de 0.5 µg/kg/día. En perros, ratas y ratones, la DE 50 fue de 7, 30 y 700 µg/kg/día, respectivamente. Estos resultados son congruentes con el hecho de que el ezetimibe sea un potente inhibidor de la absorción del colesterol. En un modelo basado en ratas a las que se administró el metabolito glucurónido del ezetimibe (ezetimibe-glucurónido) por vía intraduodenal, éste resultó tan potente como el ezetimibe en su acción inhibidora de la absorción del colesterol, lo que indica que el metabolito glucurónido tiene una actividad similar a la del fármaco original. En estudios de 1 mes de duración con perros a los que se administró ezetimibe (0.03 a 300 mg/kg/día), la concentración de colesterol en la bilis de la vesícula biliar aumentó de ~2 a 4 veces. Sin embargo, una dosis de 300 mg/kg/día administrada a perros durante un año no dio lugar a cálculos biliares ni causó ningún otro efecto hepatobiliar adverso. En un estudio de 14 días con ratones a los que se administró ezetimibe (0.3 a 5 mg/kg/día) y se alimentó con una dieta baja en grasas o rica en colesterol, la concentración de colesterol en la bilis de la vesícula biliar no se vio afectada o descendió a concentraciones normales, respectivamente. Se llevó a cabo una serie de estudios preclínicos de administración de una sola dosis para determinar la selectividad de ezetimibe en la inhibición de la absorción del colesterol. El ezetimibe inhibió la absorción del 14 C colesterol sin afectar a la de los triglicéridos, los ácidos grasos, los ácidos biliares, la progesterona, el etilestradiol o las vitaminas liposolubles A y D. En estudios de 4 a 12 semanas de duración sobre toxicidad en ratones, el ezetimibe 14 no indujo CLINICAL las isoenzimas STUDIES del citocromo P450 que metabolizan fármacos. En estudios de 14.1 toxicidad Primary se constató Hyperlipidemia una interacción farmacocinética del ezetimibe con las estatinas (el fármaco original o sus metabolitos hidroxiácidos activos) en ratas, perros y conejos. VYTORIN 14 ESTUDIOS VYTORIN CLÍNICOS reduces total-c, LDL-C, Apo B, TG, and non-hdl-c, and increases 14.1 Hiperlipidemia HDL-C Primaria in patients with hyperlipidemia. Maximal to near maximal response is generally achieved within 2 weeks and maintained during chronic therapy. VYTORIN VYTORIN reduce el C-total, el C-LDL, la Apo B, los TG y el C-no HDL, y aumenta el C- VYTORIN is effective in men and women with hyperlipidemia. Experience HDL, en pacientes con hiperlipidemia. En general, la respuesta máxima o casi máxima se in non-caucasians is limited and does not permit a precise estimate of the alcanza en 2 semanas y se mantiene durante el tratamiento crónico. magnitude of the effects of VYTORIN. VYTORIN es eficaz en hombres y mujeres con hiperlipidemia. La experiencia en personas Five no multicenter, caucásicas es double-blind limitada y no studies permite un conducted cálculo preciso with either de la magnitud VYTORIN de or los efectos coadministered de VYTORIN. ezetimibe and simvastatin equivalent to VYTORIN in patients Se realizaron with primary cinco hyperlipidemia estudios multicéntricos are reported: con doble two enmascaramiento were comparisons de with VYTORIN simvastatin, o ezetimibe two y were comparisons coadministrados with en atorvastatin, forma equivalente and one a VYTORIN, was a comparison with rosuvastatin.
EZETIMIBA COMPRIMIDOS 10 mg
 EZETIMIBA COMPRIMIDOS 10 mg Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento. Si tiene cualquier duda o no está seguro
EZETIMIBA COMPRIMIDOS 10 mg Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento. Si tiene cualquier duda o no está seguro
STOP. Mira por ti, controla tu colesterol. Campaña Nacional para el Control del Colesterol. www.controlatucolesterol.org
 Mira por ti, controla tu Campaña Nacional para el Control del Colesterol www.controlatu.org Qué es el? El es una grasa que circula por la sangre y que interviene en muchos procesos del organismo, como
Mira por ti, controla tu Campaña Nacional para el Control del Colesterol www.controlatu.org Qué es el? El es una grasa que circula por la sangre y que interviene en muchos procesos del organismo, como
SIMVASTATINA COMPRIMIDOS RECUBIERTOS DE 10mg-20mg-40mg-80mg
 SIMVASTATINA COMPRIMIDOS RECUBIERTOS DE 10mg-20mg-40mg-80mg Por favor lea cuidadosamente este folleto antes de empezar a tomar su medicamento, inclusive si ya renovó su prescripción. Alguna de la información
SIMVASTATINA COMPRIMIDOS RECUBIERTOS DE 10mg-20mg-40mg-80mg Por favor lea cuidadosamente este folleto antes de empezar a tomar su medicamento, inclusive si ya renovó su prescripción. Alguna de la información
Modificaciones en la Ficha Técnica o Resumen de las Características del Producto y del Prospecto presentadas por la Agencia Europea de Medicamentos
 Anexo II Modificaciones en la Ficha Técnica o Resumen de las Características del Producto y del Prospecto presentadas por la Agencia Europea de Medicamentos Esta Ficha Técnica o Resumen de las Características
Anexo II Modificaciones en la Ficha Técnica o Resumen de las Características del Producto y del Prospecto presentadas por la Agencia Europea de Medicamentos Esta Ficha Técnica o Resumen de las Características
FICHA DE INFORMACIÓN AL PACIENTE: PARACETAMOL
 FICHA DE INFORMACIÓN AL PACIENTE: PARACETAMOL 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Analgésico y antipirético (antitérmico, que reduce la fiebre). 1.2 Cómo actúa este fármaco: Inhibe un enzima que
FICHA DE INFORMACIÓN AL PACIENTE: PARACETAMOL 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Analgésico y antipirético (antitérmico, que reduce la fiebre). 1.2 Cómo actúa este fármaco: Inhibe un enzima que
El sobrepeso puede reducir seriamente la calidad de vida de su perro.
 El sobrepeso puede reducir seriamente la calidad de vida de su perro. Un perro con sobrepeso puede no sentirse tan bien como realmente podría. De hecho, si su perro Tiene problemas a la hora de levantarse
El sobrepeso puede reducir seriamente la calidad de vida de su perro. Un perro con sobrepeso puede no sentirse tan bien como realmente podría. De hecho, si su perro Tiene problemas a la hora de levantarse
Colemin 20 mg comprimidos (simvastatina)
 Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
X-Plain Controlando el Colesterol Sumario
 X-Plain Controlando el Colesterol Sumario Introducción El colesterol es uno de los términos médicos más comunes hoy en día. El colesterol es una sustancia de la textura de la cera, que es muy importante
X-Plain Controlando el Colesterol Sumario Introducción El colesterol es uno de los términos médicos más comunes hoy en día. El colesterol es una sustancia de la textura de la cera, que es muy importante
Una píldora diaria. Tres valores de laboratorio importantes
 Tres valores de laboratorio importantes Una píldora diaria Sensipar una vez al día* ayuda a reducir los niveles de HPT, calcio y fósforo en pacientes con hiperparatiroidismo secundario (HPTS) que reciben
Tres valores de laboratorio importantes Una píldora diaria Sensipar una vez al día* ayuda a reducir los niveles de HPT, calcio y fósforo en pacientes con hiperparatiroidismo secundario (HPTS) que reciben
Guía del entrenador de estilo de vida: Fase de seguimiento
 Guía del entrenador de estilo de vida: Fase de seguimiento Salud del corazón Visión general En esta sesión se presenta el tema de las enfermedades cardíacas, qué son y cuáles son los factores de riesgo
Guía del entrenador de estilo de vida: Fase de seguimiento Salud del corazón Visión general En esta sesión se presenta el tema de las enfermedades cardíacas, qué son y cuáles son los factores de riesgo
Repafet. Rupatadina Tabletas. Rupatadina II.- DENOMINACIÓN GENÉRICA: III.- FORMA FARMACÉUTICA Y FORMULACIÓN:
 Repafet Rupatadina Tabletas II.- DENOMINACIÓN GENÉRICA: Rupatadina III.- FORMA FARMACÉUTICA Y FORMULACIÓN: Cada tableta contiene: Fumarato de Rupatadina equivalente a... 10 mg de Rupatadina Excipiente
Repafet Rupatadina Tabletas II.- DENOMINACIÓN GENÉRICA: Rupatadina III.- FORMA FARMACÉUTICA Y FORMULACIÓN: Cada tableta contiene: Fumarato de Rupatadina equivalente a... 10 mg de Rupatadina Excipiente
ANÁLISIS DE DUPLICIDADES DEL SUBGRUPO TERAPÉUTICO C10 AGENTES MODIFICADORES DE LÍPIDOS
 ANÁLISIS DE ES DEL SUBGRUPO TERAPÉUTICO C10 AGENTES MODIFICADORES DE LÍPIDOS CLASIFICACIÓN Subgrupo Inhibidores de la HMG-CoA reductasa Simvastatina Lovastatina Pravastatina Fluvastatina Atorvastatina
ANÁLISIS DE ES DEL SUBGRUPO TERAPÉUTICO C10 AGENTES MODIFICADORES DE LÍPIDOS CLASIFICACIÓN Subgrupo Inhibidores de la HMG-CoA reductasa Simvastatina Lovastatina Pravastatina Fluvastatina Atorvastatina
CIPROFIBRATO Cápsulas 100 mg
 CIPROFIBRATO Cápsulas 100 mg Lea cuidadosamente este folleto antes de la administración de éste medicamento. Contiene información importante acerca de su tratamiento. Si tiene alguna duda o no está seguro
CIPROFIBRATO Cápsulas 100 mg Lea cuidadosamente este folleto antes de la administración de éste medicamento. Contiene información importante acerca de su tratamiento. Si tiene alguna duda o no está seguro
Sea un miembro activo de su equipo de atención médica. Council on Family Health
 Sea un miembro activo de su equipo de atención médica Council on Family Health en colaboración con el U.S. Department of Health and Human Services Food and Drug Administration Cuando se trata de usar medicamentos,
Sea un miembro activo de su equipo de atención médica Council on Family Health en colaboración con el U.S. Department of Health and Human Services Food and Drug Administration Cuando se trata de usar medicamentos,
El Colesterol y su Nuevo Órgano. Un recurso para la salud cardiovascular después de un trasplante de órgano. Compartir. Informar. Inspirar.
 El Colesterol y su Nuevo Órgano Un recurso para la salud cardiovascular después de un trasplante de órgano Compartir. Informar. Inspirar. Comprender el colesterol en sangre Los términos colesterol en sangre
El Colesterol y su Nuevo Órgano Un recurso para la salud cardiovascular después de un trasplante de órgano Compartir. Informar. Inspirar. Comprender el colesterol en sangre Los términos colesterol en sangre
LLD Abreviado de XANAX
 LLD Abreviado de XANAX Versión: 8.0 Fecha: 12 Diciembre de 2013 Aprobación ARCSA: 3 de Mayo de 2014 1. Presentación: Cada tableta de liberación inmediata contiene XANAX 0.25 mg tabletas: Reg.San. 29637-02-11
LLD Abreviado de XANAX Versión: 8.0 Fecha: 12 Diciembre de 2013 Aprobación ARCSA: 3 de Mayo de 2014 1. Presentación: Cada tableta de liberación inmediata contiene XANAX 0.25 mg tabletas: Reg.San. 29637-02-11
USO SEGURO DE LOS MEDICAMENTOS LMCV 05-2012
 Guía para pacientes acerca del uso seguro de los medicamentos Este corto vital ha sido pensado para ayudar a los pacientes a tomar sus medicinas de forma segura. Conviértase en un paciente informado Disponer
Guía para pacientes acerca del uso seguro de los medicamentos Este corto vital ha sido pensado para ayudar a los pacientes a tomar sus medicinas de forma segura. Conviértase en un paciente informado Disponer
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO INEGY 10 mg/20 mg comprimidos INEGY 10 mg/40 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO INEGY 10 mg/20 mg comprimidos INEGY 10 mg/40 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
Qué es la tarjeta amarilla?
 Qué es la tarjeta amarilla? Es el formulario de recogida de sospechas de reacciones adversas, editada en color amarillo, y distribuida por el Centro Autonómico de Farmacovigilancia del Principado de Asturias
Qué es la tarjeta amarilla? Es el formulario de recogida de sospechas de reacciones adversas, editada en color amarillo, y distribuida por el Centro Autonómico de Farmacovigilancia del Principado de Asturias
PROSPECTO: INFORMACIÓN PARA EL USUARIO. ACIDOS OMEGA-3 CINFA 1000 mg CAPSULAS BLANDAS EFG Esteres etílicos de ácidos grasos omega-3 al 90%
 PROSPECTO: INFORMACIÓN PARA EL USUARIO ACIDOS OMEGA-3 CINFA 1000 mg CAPSULAS BLANDAS EFG Esteres etílicos de ácidos grasos omega-3 al 90% Lea todo el prospecto detenidamente antes de empezar a tomar el
PROSPECTO: INFORMACIÓN PARA EL USUARIO ACIDOS OMEGA-3 CINFA 1000 mg CAPSULAS BLANDAS EFG Esteres etílicos de ácidos grasos omega-3 al 90% Lea todo el prospecto detenidamente antes de empezar a tomar el
EL COLESTEROL LMCV 05-2011 LMCV
 05-2011 El Colesterol Es una sustancia grasa que se encuentra en forma natural en todas las células del organismo. Es utilizado para la formación de tejidos y hormonas; y también interviene en la absorción
05-2011 El Colesterol Es una sustancia grasa que se encuentra en forma natural en todas las células del organismo. Es utilizado para la formación de tejidos y hormonas; y también interviene en la absorción
PANTOK 20 mg comprimidos recubiertos con película (simvastatina)
 Prospecto: Información para el paciente PANTOK 20 mg comprimidos recubiertos con película (simvastatina) Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información
Prospecto: Información para el paciente PANTOK 20 mg comprimidos recubiertos con película (simvastatina) Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información
X-Plain Hipertensión esencial Sumario
 X-Plain Hipertensión esencial Sumario Introducción Hipertensión o presión arterial alta es una condición muy común que afecta a 1 de cada 4 adultos. Hipertensión también se llama el Asesino Silencioso
X-Plain Hipertensión esencial Sumario Introducción Hipertensión o presión arterial alta es una condición muy común que afecta a 1 de cada 4 adultos. Hipertensión también se llama el Asesino Silencioso
Debe utilizarse la dosis eficaz mínima durante el periodo más corto posible a fin de reducir las reacciones adversas.
 ANEXO III 1 ENMIENDAS A INCLUIR EN LAS SECCIONES RELEVANTES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTIENEN NIMESULIDA (FORMULACIONES SISTÉMICAS) El texto añadido aparece
ANEXO III 1 ENMIENDAS A INCLUIR EN LAS SECCIONES RELEVANTES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTIENEN NIMESULIDA (FORMULACIONES SISTÉMICAS) El texto añadido aparece
Capítulo 9 : MÁS VALE PREVENIR: PREVENCION PRIMARIA Y SECUNDARIA LOS 12 CONSEJOS FUNDAMENTALES PARA EVITAR UN ICTUS
 Capítulo 9 : MÁS VALE PREVENIR: PREVENCION PRIMARIA Y SECUNDARIA Dr. Ángel Pérez Sempere El cerebro es nuestro órgano más preciado. Nuestros pensamientos y sentimientos y la relación con nuestro entorno
Capítulo 9 : MÁS VALE PREVENIR: PREVENCION PRIMARIA Y SECUNDARIA Dr. Ángel Pérez Sempere El cerebro es nuestro órgano más preciado. Nuestros pensamientos y sentimientos y la relación con nuestro entorno
Índice de contenidos DESCRIPCIÓN GENERAL A TENER EN CUENTA. Consulte con su especialista si se encuentra en alguno de los siguientes casos:
 Ketoconazol (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL El ketoconazol corresponde
Ketoconazol (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL El ketoconazol corresponde
Qué no cubre esta guía?
 Tratamiento para el colesterol alto Guía para adultos Resumen: El colesterol alto puede producir ataques cardíacos y ataques de cerebro (derrames). El primer paso para controlar su colesterol es comer
Tratamiento para el colesterol alto Guía para adultos Resumen: El colesterol alto puede producir ataques cardíacos y ataques de cerebro (derrames). El primer paso para controlar su colesterol es comer
SUNITINIB CÁPSULAS DURAS DE 12,5-25 y 50 mg
 SUNITINIB CÁPSULAS DURAS DE 12,5-25 y 50 mg Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento. Si tiene cualquier
SUNITINIB CÁPSULAS DURAS DE 12,5-25 y 50 mg Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento. Si tiene cualquier
Anexo III. Modificaciones en las secciones relevantes de la Resumen de las Características del Producto y prospecto
 Anexo III Modificaciones en las secciones relevantes de la Resumen de las Características del Producto y prospecto Nota: Esta Ficha Técnica o Resumen de las Características del producto y prospecto son
Anexo III Modificaciones en las secciones relevantes de la Resumen de las Características del Producto y prospecto Nota: Esta Ficha Técnica o Resumen de las Características del producto y prospecto son
Anticoncepcion de Emergencia
 Anticoncepcion de Emergencia La anticoncepción de emergencia o anticoncepción postcoital se refiere a las píldoras anticonceptivas que tomadas después del acto sexual pueden prevenir el embarazo La anticoncepción
Anticoncepcion de Emergencia La anticoncepción de emergencia o anticoncepción postcoital se refiere a las píldoras anticonceptivas que tomadas después del acto sexual pueden prevenir el embarazo La anticoncepción
MARCO TEORICO. La diabetes es una enfermedad crónica en la cual el cuerpo no puede regular la cantidad de azúcar en la sangre.
 CAPITULO 2 MARCO TEORICO 2.1Que es la Diabetes La diabetes es una enfermedad crónica en la cual el cuerpo no puede regular la cantidad de azúcar en la sangre. Causas La insulina es una hormona producida
CAPITULO 2 MARCO TEORICO 2.1Que es la Diabetes La diabetes es una enfermedad crónica en la cual el cuerpo no puede regular la cantidad de azúcar en la sangre. Causas La insulina es una hormona producida
Diplomático de la Junta Americana de Alergia & Inmunología
 Reacciones de la droga y La mayoría de nosotros hemos tenido problemas con un medicamento u otro. Algunos medicamentos pueden causar un malestar estomacal o sentirse con sueno. Algunas drogas pueden poner
Reacciones de la droga y La mayoría de nosotros hemos tenido problemas con un medicamento u otro. Algunos medicamentos pueden causar un malestar estomacal o sentirse con sueno. Algunas drogas pueden poner
constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético.
 Qué es la glutamina? La glutamina es el más abundante aminoácido libre en el cuerpo humano, y constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético. La glutamina es un
Qué es la glutamina? La glutamina es el más abundante aminoácido libre en el cuerpo humano, y constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético. La glutamina es un
Sesión 20: La Salud del Corazón
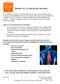 Sesión 20: La Salud del Corazón En los Estados Unidos, la enfermedad de corazón es la principal causa de muerte para ambos, hombres y mujeres. Personas con pre-diabetes o diabetes corren un mayor riesgo
Sesión 20: La Salud del Corazón En los Estados Unidos, la enfermedad de corazón es la principal causa de muerte para ambos, hombres y mujeres. Personas con pre-diabetes o diabetes corren un mayor riesgo
en tratamiento con Toctino ... Nombre de la paciente (alitretinoína) Para el médico Soluciones pensando en ti
 (alitretinoína) Tarjeta Restaura de seguimiento desde el interiorde la Paciente en con Toctino... Nombre de la paciente Para el médico Soluciones pensando en ti www.almirall.es www.solucionesalmirall.com
(alitretinoína) Tarjeta Restaura de seguimiento desde el interiorde la Paciente en con Toctino... Nombre de la paciente Para el médico Soluciones pensando en ti www.almirall.es www.solucionesalmirall.com
Índice de contenidos DESCRIPCIÓN GENERAL A TENER EN CUENTA. Consulte con su especialista si se encuentra en alguno de los siguientes casos:
 Lincomicina (Por via oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL Las lincomicinas corresponden
Lincomicina (Por via oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL Las lincomicinas corresponden
Guía informativa GUIA INFORMATIVA. Servicio Obstetricia y Ginecología
 GUIA INFORMATIVA. 1 INDICE 1. Qué es la Diabetes Gestacional? 2. Puede afectar a mi hijo? 3. Tratamiento. 4. Diabetes Gestacional y Parto. 5. Controles en el posparto. 1. QUE ES LA DIABETES GESTACIONAL?
GUIA INFORMATIVA. 1 INDICE 1. Qué es la Diabetes Gestacional? 2. Puede afectar a mi hijo? 3. Tratamiento. 4. Diabetes Gestacional y Parto. 5. Controles en el posparto. 1. QUE ES LA DIABETES GESTACIONAL?
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Simvastatina Bluefish 10 mg comprimidos recubiertos con película EFG Simvastatina
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Simvastatina Bluefish 10 mg comprimidos recubiertos con película EFG Simvastatina Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve
PROSPECTO: INFORMACIÓN PARA EL USUARIO Simvastatina Bluefish 10 mg comprimidos recubiertos con película EFG Simvastatina Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve
Este medicamento debe ser usado exclusivamente bajo prescripción y vigilancia médica y no puede repetirse sin nueva receta médica.
 DORMID 15mg/3ml MIDAZOLAM5mg/ml Solucióninyectable IndustriaHolandesa Ventabajorecetaarchivada Estemedicamentodebeserusadoexclusivamentebajoprescripciónyvigilanciamédicaynopuederepetirsesin nuevarecetamédica.
DORMID 15mg/3ml MIDAZOLAM5mg/ml Solucióninyectable IndustriaHolandesa Ventabajorecetaarchivada Estemedicamentodebeserusadoexclusivamentebajoprescripciónyvigilanciamédicaynopuederepetirsesin nuevarecetamédica.
Índice de contenidos DESCRIPCIÓN GENERAL. Esteroides Anabólicos (Por via oral)
 Esteroides Anabólicos (Por via oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL Los esteroides anabólicos
Esteroides Anabólicos (Por via oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL Los esteroides anabólicos
Anticoncepción oral sin estrógenos Qué debes saber?
 Anticoncepción oral sin estrógenos Qué debes saber? Anticoncepción oral sin estrógenos Qué debes saber? Qué es la píldora sin estrógenos? Cómo funciona? Cuándo iniciar el tratamiento con la píldora sin
Anticoncepción oral sin estrógenos Qué debes saber? Anticoncepción oral sin estrógenos Qué debes saber? Qué es la píldora sin estrógenos? Cómo funciona? Cuándo iniciar el tratamiento con la píldora sin
-Usar el preservativo, que evita el contagio de otras enfermedades de transmisión sexual.
 Virus del Papiloma Humano (VPH) - Preguntas y respuestas 1. Qué es el virus del Papiloma Humano (VPH)? El virus papiloma humano (VPH) es un virus que se transmite por contacto entre personas infectadas,
Virus del Papiloma Humano (VPH) - Preguntas y respuestas 1. Qué es el virus del Papiloma Humano (VPH)? El virus papiloma humano (VPH) es un virus que se transmite por contacto entre personas infectadas,
GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos
 GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos Industria Alemana EXPENDIO BAJO RECETA Nota importante: Antes de recetar este medicamento, consulte toda la información relativa a su prescripción.
GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos Industria Alemana EXPENDIO BAJO RECETA Nota importante: Antes de recetar este medicamento, consulte toda la información relativa a su prescripción.
(Mifepristona) Tabletas, 200 mg
 (Mifepristona) Tabletas, 200 mg GUÍA DE CÓMO USAR ESTA MEDICINA Información De Contacto Danco Laboratories P.O. Box 4816 New York, NY 10185 1.877.4 EARLY OPTION (1.877.432.7596) www.earlyoptionpill.com
(Mifepristona) Tabletas, 200 mg GUÍA DE CÓMO USAR ESTA MEDICINA Información De Contacto Danco Laboratories P.O. Box 4816 New York, NY 10185 1.877.4 EARLY OPTION (1.877.432.7596) www.earlyoptionpill.com
Ensayos Clínicos en Oncología
 Ensayos Clínicos en Oncología Qué son y para qué sirven? www.seom.org ESP 05/04 ON4 Con la colaboración de: Una parte muy importante de la Investigación en Oncología Médica se realiza a través de Ensayos
Ensayos Clínicos en Oncología Qué son y para qué sirven? www.seom.org ESP 05/04 ON4 Con la colaboración de: Una parte muy importante de la Investigación en Oncología Médica se realiza a través de Ensayos
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Fluvastatina Alter 80 mg comprimidos de liberación prolongada EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Fluvastatina Alter 80 mg comprimidos de liberación prolongada EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento - Conserve este prospecto
PROSPECTO: INFORMACIÓN PARA EL USUARIO Fluvastatina Alter 80 mg comprimidos de liberación prolongada EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento - Conserve este prospecto
Introducción. Nuevos anticoagulantes orales
 Progresos en la prevención del ACV asociado a la fibrilación auricular Dabigatrán, rivaroxabán y apixabán son anticoagulantes orales nuevos que pueden ser una alternativa a la warfarina en el tratamiento
Progresos en la prevención del ACV asociado a la fibrilación auricular Dabigatrán, rivaroxabán y apixabán son anticoagulantes orales nuevos que pueden ser una alternativa a la warfarina en el tratamiento
INFORMACION PARA RESCRIBIR AMPLIA
 INFORMACION PARA RESCRIBIR AMPLIA BEZAFISAL MR BEZAFIBRATO Agente antilipidémico Laboratorios Cryopharma, S.A. de C.V INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERICAL Y GENÉRICO 1.1 Nombre comercial:
INFORMACION PARA RESCRIBIR AMPLIA BEZAFISAL MR BEZAFIBRATO Agente antilipidémico Laboratorios Cryopharma, S.A. de C.V INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERICAL Y GENÉRICO 1.1 Nombre comercial:
APRENDIENDO CON NEFRON SUPERHEROE
 APRENDIENDO CON NEFRON SUPERHEROE COLESTEROL Y ENFERMEDAD RENAL CRÓNICA. Qué es el colesterol? El colesterol es una sustancia parecida a la grasa que se encuentra en la sangre. Su cuerpo puede producir
APRENDIENDO CON NEFRON SUPERHEROE COLESTEROL Y ENFERMEDAD RENAL CRÓNICA. Qué es el colesterol? El colesterol es una sustancia parecida a la grasa que se encuentra en la sangre. Su cuerpo puede producir
La FDA advierte que el uso de inhibidores del SGLT2 para la diabetes puede provocar una grave concentración de ácido en la sangre
 La FDA advierte que el uso de inhibidores del SGLT2 para la diabetes puede provocar una grave concentración de ácido en la sangre Aviso de seguridad [05-15-2015] La Administración de Alimentos y Medicamentos
La FDA advierte que el uso de inhibidores del SGLT2 para la diabetes puede provocar una grave concentración de ácido en la sangre Aviso de seguridad [05-15-2015] La Administración de Alimentos y Medicamentos
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Zulex 333 mg Comprimidos recubiertos Acamprosato
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Zulex 333 mg Comprimidos recubiertos Acamprosato Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto, ya que puede
PROSPECTO: INFORMACIÓN PARA EL USUARIO Zulex 333 mg Comprimidos recubiertos Acamprosato Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto, ya que puede
3. Los medicamentos en el organismo
 3. Los medicamentos en el organismo Un medicamento es una sustancia que se administra con el objeto de provocar algún cambio en el organismo. Después de haber entrado y hasta que salga del cuerpo, el medicamento
3. Los medicamentos en el organismo Un medicamento es una sustancia que se administra con el objeto de provocar algún cambio en el organismo. Después de haber entrado y hasta que salga del cuerpo, el medicamento
FICHA TÉCNICA. STREPSILS pastillas para chupar sabor miel y limón
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor miel y limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor miel y limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
Hall V, Hernández LE, Rocha M. Centro Nacional de Información de Medicamentos
 Análisis del estado de salud y comportamientos de los pacientes con hipercolesterolemia encuestados en la Encuesta Nacional de Salud para Costa Rica 2006, Centro Centroamericano de Población-Universidad
Análisis del estado de salud y comportamientos de los pacientes con hipercolesterolemia encuestados en la Encuesta Nacional de Salud para Costa Rica 2006, Centro Centroamericano de Población-Universidad
Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes
 Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes antes de hidroxiurea después de hidroxiurea Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes 1 Este documento
Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes antes de hidroxiurea después de hidroxiurea Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes 1 Este documento
Cómo Mantener los Niveles de Colesterol Bajo Control?
 Cómo Mantener los Niveles de Colesterol Bajo Control? Programa de Promoción y Educación en Salud PMC Medicare Choice, Inc. PM C-PRD-015-012710-S Objetivos Al completar este tutorial educativo, los participantes
Cómo Mantener los Niveles de Colesterol Bajo Control? Programa de Promoción y Educación en Salud PMC Medicare Choice, Inc. PM C-PRD-015-012710-S Objetivos Al completar este tutorial educativo, los participantes
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ácidos Omega 3 ratiopharm 1000 mg cápsulas blandas EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula blanda contiene 1.000
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ácidos Omega 3 ratiopharm 1000 mg cápsulas blandas EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula blanda contiene 1.000
Estudios Pre-clínicos y Clínicos
 Estudios Pre-clínicos y Clínicos Rocío Ramírez Herrera Dictaminadoras Especializadas Norma Edith Soto Ruíz DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS 1 ESTUDIOS PRECLÍNICOS Conjunto
Estudios Pre-clínicos y Clínicos Rocío Ramírez Herrera Dictaminadoras Especializadas Norma Edith Soto Ruíz DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS 1 ESTUDIOS PRECLÍNICOS Conjunto
ANEXO CONDICIONES O RESTRICCIONES RESPECTO AL USO SEGURO Y EFICAZ DEL MEDICAMENTO A APLICAR POR LOS ESTADOS MIEMBROS
 ANEXO CONDICIONES O RESTRICCIONES RESPECTO AL USO SEGURO Y EFICAZ DEL MEDICAMENTO A APLICAR POR LOS ESTADOS MIEMBROS 1 Los Estados Miembros se tienen que asegurar de que se apliquen todas las condiciones
ANEXO CONDICIONES O RESTRICCIONES RESPECTO AL USO SEGURO Y EFICAZ DEL MEDICAMENTO A APLICAR POR LOS ESTADOS MIEMBROS 1 Los Estados Miembros se tienen que asegurar de que se apliquen todas las condiciones
Prospecto: información para el usuario. Calcitonina Almirall 100 UI/ml solución inyectable. Calcitonina sintética de salmón
 Prospecto: información para el usuario Calcitonina Almirall 100 UI/ml solución inyectable Calcitonina sintética de salmón Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
Prospecto: información para el usuario Calcitonina Almirall 100 UI/ml solución inyectable Calcitonina sintética de salmón Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
FICHA TÉCNICA. Excipientes con efecto conocido: 1,38 g de sacarosa y 1,10 g de glucosa.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor ciruela 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor ciruela 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
Anexo II. Conclusiones científicas y motivos para la suspensión de las autorizaciones de comercialización presentados por la EMA
 Anexo II Conclusiones científicas y motivos para la suspensión de las autorizaciones de comercialización presentados por la EMA 5 Conclusiones científicas Resumen general de la evaluación científica de
Anexo II Conclusiones científicas y motivos para la suspensión de las autorizaciones de comercialización presentados por la EMA 5 Conclusiones científicas Resumen general de la evaluación científica de
Qué es la artritis reumatoide?
 Qué es la artritis reumatoide? La artritis reumatoide es una enfermedad que afecta las articulaciones o coyunturas. Causa dolor, hinchazón y rigidez. Si una rodilla o mano tiene artritis reumatoide, usualmente
Qué es la artritis reumatoide? La artritis reumatoide es una enfermedad que afecta las articulaciones o coyunturas. Causa dolor, hinchazón y rigidez. Si una rodilla o mano tiene artritis reumatoide, usualmente
SIM EXPRESS Información dirigida a los profesionales de la salud Teriflunomida
 COLEGIO DE FARMACÉUTICOS DE LA PROVINCIA DE SANTA FE 1ª Circunscripción DAP DEPARTAMENTO DE ACTUALIZACIÓN PROFESIONAL SIM Sistema de Información de Medicamentos 23/04/2015 SIM EXPRESS Información dirigida
COLEGIO DE FARMACÉUTICOS DE LA PROVINCIA DE SANTA FE 1ª Circunscripción DAP DEPARTAMENTO DE ACTUALIZACIÓN PROFESIONAL SIM Sistema de Información de Medicamentos 23/04/2015 SIM EXPRESS Información dirigida
27/03/2012. Colesterol: Funciones. Colesterol: No siempre es villano. - Membranas celulares (tracto digestivo y piel) -Precursor de sales biliares
 7/0/0 Colesterol: Funciones Colesterol: No siempre es villano El colesterol es el lípido característico de los tejidos animales y desempeña funciones esenciales - Membranas celulares (tracto digestivo
7/0/0 Colesterol: Funciones Colesterol: No siempre es villano El colesterol es el lípido característico de los tejidos animales y desempeña funciones esenciales - Membranas celulares (tracto digestivo
Aprenda a manejar su. Colesterol. Si tiene diabetes. Lechuga. Maíz. Tomates
 Aprenda a manejar su Si tiene diabetes Lechuga Maíz Tomates ER FRONT COV Aprenda a manejar su CoSiletienestdiaeberotes l Lechuga íz Ma Toma tes Cómo entender este folleto Este folleto explica la importancia
Aprenda a manejar su Si tiene diabetes Lechuga Maíz Tomates ER FRONT COV Aprenda a manejar su CoSiletienestdiaeberotes l Lechuga íz Ma Toma tes Cómo entender este folleto Este folleto explica la importancia
Resultado positivo del síndrome de Down
 Programa de Detección Prenatal de California Los resultados de la prueba inicial del primer trimestre Positive T21 1T Spanish El resultado de su prueba inicial de sangre es: Resultado positivo del síndrome
Programa de Detección Prenatal de California Los resultados de la prueba inicial del primer trimestre Positive T21 1T Spanish El resultado de su prueba inicial de sangre es: Resultado positivo del síndrome
ALERGIA A MEDICAMENTOS
 ALERGIA A MEDICAMENTOS 1 QUE REACCIONES ADVERSAS PUEDEN CAUSAR LOS MEDICAMENTOS? Los medicamentos tienen como función curar enfermedades pero sin embargo en ocasiones pueden causar problemas. Dentro de
ALERGIA A MEDICAMENTOS 1 QUE REACCIONES ADVERSAS PUEDEN CAUSAR LOS MEDICAMENTOS? Los medicamentos tienen como función curar enfermedades pero sin embargo en ocasiones pueden causar problemas. Dentro de
Qué es el herpes genital?
 Qué es el herpes genital? Es una infección de transmisión sexual muy extendida causada por el virus del herpes simple (VHS) de tipo 2 (VHS-2) y de tipo 1 (VHS-1), que también es causa habitual del herpes
Qué es el herpes genital? Es una infección de transmisión sexual muy extendida causada por el virus del herpes simple (VHS) de tipo 2 (VHS-2) y de tipo 1 (VHS-1), que también es causa habitual del herpes
INFORMACIÓN PARA EL PACIENTE. Pravastatina ratiopharm 40 mg Comprimidos EFG Pravastatina sódica
 INFORMACIÓN PARA EL PACIENTE Pravastatina ratiopharm 40 mg Comprimidos EFG Pravastatina sódica Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya
INFORMACIÓN PARA EL PACIENTE Pravastatina ratiopharm 40 mg Comprimidos EFG Pravastatina sódica Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya
Disminuyendo mi riesgo de infarto, protegiendo mi corazón.
 Disminuyendo mi riesgo de infarto, protegiendo mi corazón. A partir de los 45 años de edad es necesario realizar una evaluación del riesgo cardiovascular de rutina. Los médicos de la Unidad de Atención
Disminuyendo mi riesgo de infarto, protegiendo mi corazón. A partir de los 45 años de edad es necesario realizar una evaluación del riesgo cardiovascular de rutina. Los médicos de la Unidad de Atención
EFECTOS ADVERSOS: POSOLOGIA
 POSOLOGIA NILOTINIB se administra por vía oral. La dosis recomendada es según prescripción médica. CÓMO se debe TOMAR Nilotinib? Debe tomarlo sin alimentos, es decir, 1 hora antes o dos horas después de
POSOLOGIA NILOTINIB se administra por vía oral. La dosis recomendada es según prescripción médica. CÓMO se debe TOMAR Nilotinib? Debe tomarlo sin alimentos, es decir, 1 hora antes o dos horas después de
FICHA TÉCNICA. Pastillas circulares de color rosa con sabor a fresa y el icono de Strepsils grabado en ambos lados.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor fresa 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor fresa 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
La presión arterial y su nuevo órgano. Un recurso para la salud cardiovascular después de un trasplante de órgano. Compartir. Informar. Inspirar.
 La presión arterial y su nuevo órgano Un recurso para la salud cardiovascular después de un trasplante de órgano Compartir. Informar. Inspirar. Comprender la presión arterial La presión arterial es la
La presión arterial y su nuevo órgano Un recurso para la salud cardiovascular después de un trasplante de órgano Compartir. Informar. Inspirar. Comprender la presión arterial La presión arterial es la
El comienzo del tratamiento con Tracleer. Todo lo que los pacientes y sus familias deben saber
 El comienzo del tratamiento con Tracleer Todo lo que los pacientes y sus familias deben saber Qué es Tracleer (bosentan)? Este folleto le ofrecerá una reseña de los beneficios y los riesgos del tratamiento
El comienzo del tratamiento con Tracleer Todo lo que los pacientes y sus familias deben saber Qué es Tracleer (bosentan)? Este folleto le ofrecerá una reseña de los beneficios y los riesgos del tratamiento
DE SALUD WISEWOMAN. División de Salud Pública Oficina de Salud Familiar
 INFORMACIÓN DE SALUD MI WISEWOMAN División de Salud Pública Oficina de Salud Familiar INFORMACIÓN DE MI SALUD Este folleto le da los resultados de las lecturas de la evaluación de su diabetes, enfermedades
INFORMACIÓN DE SALUD MI WISEWOMAN División de Salud Pública Oficina de Salud Familiar INFORMACIÓN DE MI SALUD Este folleto le da los resultados de las lecturas de la evaluación de su diabetes, enfermedades
Calcitonina Almirall 100 UI Solución inyectable Calcitonina sintética de salmón
 Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
Cosas que debería saber acerca de la preeclampsia
 Cosas que debería saber acerca de la preeclampsia La preeclampsia es mucho más frecuente de lo que la gente piensa de hecho, es la complicación grave más común del embarazo. La preeclampsia puede ser una
Cosas que debería saber acerca de la preeclampsia La preeclampsia es mucho más frecuente de lo que la gente piensa de hecho, es la complicación grave más común del embarazo. La preeclampsia puede ser una
RESUMEN GENERAL DE LA EVALUACIÓN CIENTÍFICA DE LOS MEDICAMENTOS A BASE DE ÁCIDO VALPROICO/VALPROATO (véase el anexo I)
 ANEXO II CONCLUSIONES CIENTÍFICAS Y MOTIVOS PARA LA MODIFICACIÓN DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO PRESENTADOS POR LA AGENCIA EUROPEA DE MEDICAMENTOS 108 CONCLUSIONES CIENTÍFICAS
ANEXO II CONCLUSIONES CIENTÍFICAS Y MOTIVOS PARA LA MODIFICACIÓN DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO PRESENTADOS POR LA AGENCIA EUROPEA DE MEDICAMENTOS 108 CONCLUSIONES CIENTÍFICAS
Cómo es tener diabetes tipo 2?
 Cómo es tener diabetes tipo 2? Según los Centros para el Control y la Prevención de Enfermedades (Centers for Disease Control and Prevention, CDC), hay casi 26 millones de personas con diabetes en los
Cómo es tener diabetes tipo 2? Según los Centros para el Control y la Prevención de Enfermedades (Centers for Disease Control and Prevention, CDC), hay casi 26 millones de personas con diabetes en los
Índice de contenidos DESCRIPCIÓN GENERAL A TENER EN CUENTA. Consulte con su especialista si se encuentra en alguno de los siguientes casos:
 Cloroquina (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL La cloroquina es un medicamento
Cloroquina (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL La cloroquina es un medicamento
APRENDIENDO CON NEFRON SUPERHEROE
 APRENDIENDO CON NEFRON SUPERHEROE DIABETES - UN FACTOR DE RIESGO PARA LA ENFERMEDAD RENAL La Diabetes mellitus, generalmente conocida como diabetes, es una enfermedad en la que su cuerpo no produce suficiente
APRENDIENDO CON NEFRON SUPERHEROE DIABETES - UN FACTOR DE RIESGO PARA LA ENFERMEDAD RENAL La Diabetes mellitus, generalmente conocida como diabetes, es una enfermedad en la que su cuerpo no produce suficiente
FOLLETO DE INFORMACION AL PACIENTE
 FOLLETO DE INFORMACION AL PACIENTE DIANORMAX Comprimidos 80 mg Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento.
FOLLETO DE INFORMACION AL PACIENTE DIANORMAX Comprimidos 80 mg Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento.
Agencia Española de Medicamentos y Productos Sanitarios AEMPS
 Nota informativa Agencia Española de Medicamentos y Productos Sanitarios AEMPS VICTRELIS (BOCEPREVIR): INTERACCIÓN CON LOS INHIBIDORES DE LA PROTEASA DEL VIH ATAZANAVIR, DARUNAVIR Y LOPINAVIR Fecha de
Nota informativa Agencia Española de Medicamentos y Productos Sanitarios AEMPS VICTRELIS (BOCEPREVIR): INTERACCIÓN CON LOS INHIBIDORES DE LA PROTEASA DEL VIH ATAZANAVIR, DARUNAVIR Y LOPINAVIR Fecha de
Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento.
 Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
ENSAYOS CLÍNICOS. Guía para padres y tutores
 ENSAYOS CLÍNICOS Guía para padres y tutores PARA PADRES Y TUTORES Los niños no son pequeños adultos En este folleto encontrará información sobre los ensayos clínicos en general y los ensayos clínicos en
ENSAYOS CLÍNICOS Guía para padres y tutores PARA PADRES Y TUTORES Los niños no son pequeños adultos En este folleto encontrará información sobre los ensayos clínicos en general y los ensayos clínicos en
Qué es? Los Antimaláricos en Reumatología
 30 Qué es? Los Antimaláricos en Reumatología 30 Qué es? Los Antimaláricos en Reumatología Son un grupo de medicamentos (también llamados antipalúdicos) que se han usado clásicamente para tratar el paludismo
30 Qué es? Los Antimaláricos en Reumatología 30 Qué es? Los Antimaláricos en Reumatología Son un grupo de medicamentos (también llamados antipalúdicos) que se han usado clásicamente para tratar el paludismo
Mifepristona combinada con misoprostol por vía vaginal. La píldora abortiva en las etapas iniciales del embarazo
 Mifepristona combinada con misoprostol por vía vaginal La píldora abortiva en las etapas iniciales del embarazo Protegiendo la salud de las mujeres Promoviendo el respeto a sus derechos reproductivos Ipas
Mifepristona combinada con misoprostol por vía vaginal La píldora abortiva en las etapas iniciales del embarazo Protegiendo la salud de las mujeres Promoviendo el respeto a sus derechos reproductivos Ipas
La mayoría de exposiciones no ocasionan una infección. Después de una exposición, el riesgo de infección depende de factores como los siguientes:
 Exposición a la sangre Lo que deben saber los trabajadores de la salud Departamento de Salud y Servicios Humanos Centros para el Control y la Prevención de Enfermedades Exposiciones ocupacionales a la
Exposición a la sangre Lo que deben saber los trabajadores de la salud Departamento de Salud y Servicios Humanos Centros para el Control y la Prevención de Enfermedades Exposiciones ocupacionales a la
Diabetes mellitus tipo 1.
 2. Cómo se diagnostica y qué tipos de diabetes existen? La diabetes sólo se puede diagnosticar por alguno de los siguientes métodos: 1. Análisis de Glucemia realizado en cualquier momento del día (incluso
2. Cómo se diagnostica y qué tipos de diabetes existen? La diabetes sólo se puede diagnosticar por alguno de los siguientes métodos: 1. Análisis de Glucemia realizado en cualquier momento del día (incluso
Índice de contenidos DESCRIPCIÓN GENERAL A TENER EN CUENTA. Valsartan e hidroclorotiazida (Por vía oral)
 Valsartan e hidroclorotiazida (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL La combinación
Valsartan e hidroclorotiazida (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL La combinación
Una nueva opción puede ayudar a hombres y mujeres transgénero que tienen sexo con hombres a reducir su riesgo de contraer el VIH/SIDA.
 EL ESTUDIO MTN 017 Una nueva opción puede ayudar a hombres y mujeres transgénero que tienen sexo con hombres a reducir su riesgo de contraer el VIH/SIDA. Nos gustaría explicarle acerca de un estudio que
EL ESTUDIO MTN 017 Una nueva opción puede ayudar a hombres y mujeres transgénero que tienen sexo con hombres a reducir su riesgo de contraer el VIH/SIDA. Nos gustaría explicarle acerca de un estudio que
POR QUÉ HABLAR DE COLESTEROL?
 La información médica brindada en este artículo, no es apta para ser usada con fines de diagnóstico o tratamiento, no debe utilizarse como material educativo para un paciente, no establece relación de
La información médica brindada en este artículo, no es apta para ser usada con fines de diagnóstico o tratamiento, no debe utilizarse como material educativo para un paciente, no establece relación de
X-Plain La pancreatitis Sumario
 X-Plain La pancreatitis Sumario La pancreatitis es una enfermedad poco común que provoca la inflamación del páncreas. A pesar de ser una enfermedad poco común, casi 80,000 norteamericanos padecen de pancreatitis
X-Plain La pancreatitis Sumario La pancreatitis es una enfermedad poco común que provoca la inflamación del páncreas. A pesar de ser una enfermedad poco común, casi 80,000 norteamericanos padecen de pancreatitis
Autor: Dres. Freynhagen R, Serpell M, Latymer M y colaboradores Fuente: SIIC Pain Practice 1-11, Nov 2013. Introducción y objetivos
 Importancia de la titulación 05 ENE 15 Seguridad de la pregabalina para el tratamiento de los pacientes con dolor neuropático La pregabalina es una droga de primera línea para el tratamiento de pacientes
Importancia de la titulación 05 ENE 15 Seguridad de la pregabalina para el tratamiento de los pacientes con dolor neuropático La pregabalina es una droga de primera línea para el tratamiento de pacientes
Hipercolesterolemia Colesterol-LDL Colesterol-HDL Colesterol-VLDL Colesterol ideal Colesterol en el límite alto Colesterol alto Colesterol muy alto
 Hipercolesterolemia El colesterol es una sustancia necesaria para la vida, siendo un constituyente fundamental de las membranas de las células (sus envolturas) y de diferentes hormonas. Dado que se trata
Hipercolesterolemia El colesterol es una sustancia necesaria para la vida, siendo un constituyente fundamental de las membranas de las células (sus envolturas) y de diferentes hormonas. Dado que se trata
Controlando Su Dolor Parte 1: Aprendiendo sobre el dolor de cáncer de próstata
 Controlando Su Dolor Parte 1: Aprendiendo sobre el dolor de cáncer de próstata La siguiente información está basada en las experiencias generales de muchos pacientes con cáncer de próstata. Su experiencia
Controlando Su Dolor Parte 1: Aprendiendo sobre el dolor de cáncer de próstata La siguiente información está basada en las experiencias generales de muchos pacientes con cáncer de próstata. Su experiencia
Marcadores tumorales
 Marcadores tumorales Uno de los retos más importantes de la medicina actual es el tratamiento del cáncer. Muchas veces el diagnóstico precoz va a ser importante para el éxito de dicho tratamiento. No se
Marcadores tumorales Uno de los retos más importantes de la medicina actual es el tratamiento del cáncer. Muchas veces el diagnóstico precoz va a ser importante para el éxito de dicho tratamiento. No se
X-Plain Coumadin - Introducción para los nuevos usuarios Sumario
 X-Plain Coumadin - Introducción para los nuevos usuarios Sumario La formación de coágulos de sangre es común en pacientes con enfermedad de los vasos sanguíneos o del corazón. Los coágulos de sangre pueden
X-Plain Coumadin - Introducción para los nuevos usuarios Sumario La formación de coágulos de sangre es común en pacientes con enfermedad de los vasos sanguíneos o del corazón. Los coágulos de sangre pueden
FICHA TECNICA. Adultos y niños: Aplicar cinco veces al día aproximadamente cada cuatro horas omitiendo la aplicación de la noche.
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Teva 5% crema EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Aciclovir (D.O.E.)... 50 mg Excipientes. Ver 6.1 3. FORMA FARMACEUTICA
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Teva 5% crema EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Aciclovir (D.O.E.)... 50 mg Excipientes. Ver 6.1 3. FORMA FARMACEUTICA
