Estudia un día en la U.M.H.
|
|
|
- Belén Vera Parra
- hace 6 años
- Vistas:
Transcripción
1 Estudia un día en la U.M.H. Buscando respuestas, resolviendo enigmas cuáles son las leyes que rigen los cambios de la Naturaleza? La Química en acción II Acerca del calor y del color: cambios que acompañan a las reacciones químicas Marzo Mayo de 2010
2 Materia y energía: la cara y la cruz de una misma moneda Cambios energéticos que acompañan a las reacciones químicas Podemos definir la Química como la Ciencia que se dedica a estudiar las transformaciones que se producen en el Cosmos. Vivimos en un Universo en constante metamorfosis en el que se produce la transformación continua de la materia. Pero toda trasformación de la materia (desde unos ciertos reactivos hasta dar lugar a una serie de productos) está acompañada de absorción o producción de energía, especialmente en forma de calor. Podemos considerar una reacción química como el proceso en el que una serie de especies químicas inicialmente presentes (reactivos) se transforman en otras especies químicas que denominamos productos. Solemos representar dicha transformación de forma esquemática de la siguiente forma: reactivos productos Si tomamos como ejemplo la formación de yoduro de hidrógeno, HI (g), a partir de hidrógeno, H2 (g), y yodo, I2 (g), podemos representar la reacción química como: H ( g) I ( g) 2 HI ( g) 2 2 Sin embargo, la transformación de los reactivos en productos implica la ruptura de ciertos enlaces químicos presentes en las moléculas de reactivos y la formación de nuevos enlaces químicos en las moléculas de productos. En el ejemplo anterior, la reacción química implica la ruptura del enlace que mantiene unidos los átomos de H en la molécula de H-H, la ruptura del enlace que mantiene unidos los átomos de I en la molécula de I-I y la formación de dos enlace H-I. Para completar la información que nos da la reacción química ajustada (un mol de H2 reacciona con un mol de I2 para dar lugar a dos moles de H-I), incluimos la cantidad de energía absorbida o cedida cuando se produce tal transformación química: H ( g) I ( g) 2 HI ( g) H = 35,96 kj 2 2 Esto es lo que conocemos como una ecuación termoquímica: incluye tanto la información estequiométrica (transformación de la materia: un mol de H2 reacciona con un mol de I2 para dar lugar a dos moles de H-I) como la energética (cuando un mol de H2 reacciona con un mol de I2 para dar lugar a dos moles de H-I se liberan 35,96 kj de energía en forma de calor). El signo del cambio de entalpía, H, indica si la reacción química supone la liberación o absorción de energía en forma de calor. Decimos que una reacción es exotérmica cuando H es negativa e implica que la transformación de reactivos en productos implica la liberación de energía en forma de calor. Por el contrario, la reacción será endotérmica ( H es positiva) cuando se absorba energía en forma de calor al producirse la transformación de reactivos en productos. En la presente experiencia, veremos cómo la disolución de dos sales tendrá un efecto opuesto en lo que se refiere a la liberación de energía en forma de calor
3 1.- Disolución de CaCl2(s) en agua: un ejemplo de reacción exotérmica Consideremos, en primer lugar, la disolución del cloruro de calcio anhidro, CaCl2 en agua. El CaCl2 es un compuesto iónico muy soluble en agua que, en disolución, se disocia en los iones componentes, Ca 2 y Cl -, los cuales interaccionan fuertemente con las moléculas de agua. La ecuación termoquímica que representa el proceso de la disolución del CaCl2(s) nos indica que es un proceso fuertemente exotérmico: CaCl s Ca ac Cl ac H kj 2 2( ) ( ) 2 ( ) = 82,8 Por tanto, al disolver CaCl2 en agua se producirá la liberación de energía en forma de calor (82,8 kj por cada mol de CaCl2 disuelto). Procedimiento Utilizando una espátula limpia, toma una cantidad de CaCl2 sólido (el equivalente a una cucharada de azucar) y vierte el sólido en el pesa muestras (plato de plástico). Llena una pipeta Pasteur de plástico con agua destilada y vierte su contenido sobre el sólido que está en el pesa muestras. Ayudándote de la espátula y colocando el pesa muestras sobre la palma de tu mano, remueve la dispersión para facilitar la disolución completa del CaCl2. Observarás que, a medida que la sal se disuelve, se libera una enorme cantidad de energía en forma de calor que aumenta la temperatura de la disolución. 2.- Disolución de NH4NO3(s) en agua: un ejemplo de reacción endotérmica Consideremos, ahora, la disolución del nitrato de amonio, NH4NO3 en agua. Como todos los compuestos iónicos, el NH4NO3 de disocia al ser disuelto en agua en los iones componentes, NH4 (amonio) y NO3 - (nitrato), los cuales interaccionan fuertemente con las moléculas de agua. La disolución de NH4NO3 en agua es un proceso endotérmico: NH NO ( s) NH ( ac) NO ( ac) H = 26,6 kj Por tanto, al disolver NH4NO3 en agua se producirá la absorción de energía en forma de calor (26,6 kj por cada mol de NH4NO3 disuelto). Procedimiento Utilizando una espátula limpia, toma una cantidad de NH4NO3 sólido (el equivalente a una cucharada de azucar) y vierte el sólido en el pesa muestras (plato de plástico). Llena una pipeta Pasteur de plástico con agua destilada y vierte su contenido sobre el sólido que está en el pesa muestras. Ayudándote de la espátula y colocando el pesa muestras sobre la palma de tu mano, remueve la dispersión para facilitar la disolución completa del NH4NO3. Observarás que, a medida que la sal se disuelve, se absorbe de energía en forma de calor que produce una drástica disminución de la temperatura de la disolución
4 Las aventuras de las moléculas coloreadas: Visualización de algunas reacciones químicas mediante el cambio de color Mientras que algunas trasformaciones químicas son evidentes al ojo humano (como, por ejemplo, las reacciones de disolución que vimos en el apartado anterior), otras no lo son porque no se produce ningún cambio en el aspecto exterior (color, textura o estado de agregación) cuando los reactivos son trasformados en productos. Así, por ejemplo, cuando un ácido fuerte (tal como el HCl) reacciona con una base fuerte (tal como NaOH), los protones, H, del ácido y los iones hidroxilo, OH -, de la base reaccionan para dar agua: H ( ac) OH ( ac) H O ( l) Sin embargo, tanto las disoluciones de reactivos (HCl y NaOH) y la disolución final (H2O) son incoloras, por lo que ningún cambio es detectable por el ojo humano. El color de una determinada especie química depende de cómo la radiación electromagnética interacciona con sus moléculas y, por tanto, tiene una relación directa con la estructura de dicha molécula (los tipos de enlaces existentes, los átomos que les unen y su geometría).. En este apartado utilizaremos diversas especies químicas que al reaccionar dan lugar a productos de distinto color Reacciones ácido base: indicadores colorimétricos.. Un indicador colorimétrico ácido base es un par ácido-base que tiene la propiedad que su forma ácida tiene un color y su forma básica tiene otro. En particular el azul de timol es un indicador cuya forma ácida, HA, es de color amarillo y su forma básica es de color azul: HA ( ac) A ( ac) H ( ac) amarillo azul El azul de timol es un ácido débil, por lo que el equilibrio anterior se encuentra desplazado hacia la izquierda (la disolución de azul de timol en agua es amarilla). Sin embargo, si añadimos OH - a la disolución, los protones, H, presentes en ella serán neutralizados: - H ( ac) OH ( ac) H 2O ( l) De acuerdo con el principio de L Chatelier, al disminuir la concentración de protones (producto) el equilibrio se desplazará hacia la derecha. Así, al añadir OH - se produce la transformación de HA (amarillo) en A - (azul): HA ( ac) OH A ( ac) H ( ac) amarillo azul Por tanto, si a la disolución inicial de azul de timol (amarilla) se le añade OH - la disolución se transformará en azul (al transformarse HA, amarillo, en A -, azul). Finalmente, y de acuerdo con el principio de L Chatelier, si posteriormente se añaden protones a la disolución de A - (azul), el equilibrio se desplazará hacia la izquierda dando lugar a HA y cambiando el color de la disolución nuevamente a amarillo: HA ( ac) A ( ac) H ( ac) amarillo H azul
5 Procedimiento: Utilizando la probeta de 50 ml, añade 40 ml de agua destilada al vaso de precipitados de 50 ml y ponlo el agitador magnético sometido a una agitación suave. Utilizando una pipeta Pasteaur limpia, añade 20 gotas (gota a gota) de la disolución de indicador (azul de timol). Observarás que la disolución es amarilla, indicando que la especie mayoritaria es la forma ácida del indicador, HA. Utilizando una pipeta Pasteaur limpia, añade unas 15 gotas (gota a gota) de la disolución de NaOH de concentración 0,1 M (hasta que el color de la disolución se hace azul). Observarás que, a medida que añades una mayor cantidad de OH -, el color de la disolución cambia gradualmente de amarillo a (indicando que la especie mayoritaria es la forma básica del indicador, A - ). Utilizando una pipeta Pasteaur limpia, añade unas gota a gota un volumen de la disolución de HCl de concentración 0,1 M (hasta que el color de la disolución se hace amarillo). Observarás que la reacción de disociación del ácido HA para dar lugar a A - y H es reversible y se rige de acuerdo al principio de L Chatelier. 2.- Reacciones de asociación: indicadores metalocrómicoss.. Un indicador metalocrómico es una especie química capaz de unirse a un catión metálico (Fe 2, Cu 2, Mg 2, Ca 2, Al 3, etc.) y que tiene la propiedad que su forma libre (no asociada al metal) tiene un color y su forma complejada (unida al metal) tiene otro. En particular el negro de eriocromo T es de color azul en ausencia de metal y estoma el color rojo cuando se une al metal, Mg 2, por ejemplo: Procedimiento: Indicador Mg Indicador Mg azul rojo vino 2 2 Toma 2 tubos de ensayo limpios y, usando la probeta de 10 ml, añade 5 ml de la disolución de negro de eriocromo T en cada uno de ellos. Utilizando una pipeta Pasteaur limpia, añade al primer tubo gota a gota un volumen de la disolución de Mg 2 hasta que se produzca el cambio de color del indicador (cada 2 3 gotas invierte el tubo para homogeneizar la disolución). Repite los procedimientos del apartado anterior con el 2º tubo de ensayo (que contiene la disolución de negro de eriocromo T) y la disolución de Cu Formación de complejos entre el Cu 2 y el NH3. Muchos catones de metales de transición de la tabla periódica (Cu 2, Zn 2, Co 2, etc.) tienen capacidad de formar compuestos de coordinación con ligandos que posean pares solitarios en su estructura tales como el amoníaco, NH3: ( ) 2 2 Cu ac NH3 ac Cu NH3 ac 4 ( ) 4 ( ) ( ) - 4 -
6 En el caso del Cu 2, una de las propiedades características de estos complejos de coordinación es que aumentan de forma sustancial la intensidad del color azul característico del catión Cu 2 en disolución acuosa. Como ejemplo clarificador, demostraremos que, al contrario del negro de eriocromo T que formaba complejos tanto con Cu 2 como con Mg 2, el amoníaco es incapaz de interaccionar con el Mg 2. Procedimiento: Toma 2 tubos de ensayo limpios y, usando la probeta de 10 ml, añade 5 ml de la disolución de Cu 2 en el primero y 5 ml de la disolución de Mg 2 en el segundo. Utilizando una pipeta Pasteaur limpia, añade al primer tubo 10 gotas de la disolución de amoníaco, NH3, hasta que se produzca el cambio de color del indicador (cada 2 3 gotas invierte el tubo para homogeneizar la disolución). Repite los procedimientos del apartado anterior con el 2º tubo de ensayo (que contiene la disolución de Mg 2 ) y la disolución de NH3 En el primer tubo, observarás que a medida que añades NH3 el color débilmente azulado de la disolución (debido a la presencia de Cu 2 ) se hace más fuerte. Esto es debido a que el complejo formado, Cu(NH3)4 2 es de un color azul mucho más intenso que el propio catión Cu 2. No se observará cambio alguno en el 2º tubo de ensaya, ya que el Mg 2 no forma complejos de coordinación con el amoníaco. 4.- Reacciones de oxidación reducción: obtención de yodo, I2. Las reacciones de oxidación reducción se caracterizan porque se produce la transferencia de electrones entre dos especies de los reactivos para dar lugar a los productos. En particular, analizaremos la reacción de oxidación del yoduro, I -, para dar lugar al yodo, I2, por acción del peróxido de hidrógeno, H2O2 (cuya disolución acuosa se conoce como agua oxigenada): Oxidación : 2 I ( ac) I ( ac) 2 e Re ducción : H O ( ac) 2 H ( ac) 2 e 2 H O ( l) H O ( ac) 2 I ( ac) 2 H ( ac) 2 H O ( l) I ( ac) Las disoluciones de los tres reactivos (H2O2, I - y H ) son incoloras mientras que el yodo tiene un característico color amarillento. Por tanto, podemos detectar que la reacción se ha llevado a cabo por el cambio de color que implica la transformación de I - en I2. Procedimiento: Toma 1 tubo de ensayo limpio y, usando la probeta de 10 ml, añade 3 ml de la disolución de I - de concentración 0,1 M y, seguidamente, 5 ml de la disolución 0,1 M de HCl. Utilizando una pipeta Pasteaur limpia, añade 10 gotas de la disolución de H2O2 (ac), hasta que se produzca el cambio de color del indicador (cada 2 3 gotas invierte el tubo para homogeneizar la disolución). Observarás que el color de la disolución cambia de color indicando la formación de yodo, I
Química. Equilibrio ácido-base Nombre:
 Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Estudia un día en la U.M.H.
 Estudia un día en la U.M.H. Buscando respuestas, resolviendo enigmas cuáles son las leyes que rigen los cambios de la Naturaleza? La Química en acción I Acerca de la reversibilidad de las reacciones químicas:
Estudia un día en la U.M.H. Buscando respuestas, resolviendo enigmas cuáles son las leyes que rigen los cambios de la Naturaleza? La Química en acción I Acerca de la reversibilidad de las reacciones químicas:
TRANSFORMACIONES QUÍMICAS
 TRANSFORMACIONES QUÍMICAS CAMBIOS FÍSICOS Y CAMBIOS QUÍMICOS Todas las sustancias pueden transformarse y pasar de un estado inicial a otro final si se las somete a determinadas condiciones. Por ejemplo,
TRANSFORMACIONES QUÍMICAS CAMBIOS FÍSICOS Y CAMBIOS QUÍMICOS Todas las sustancias pueden transformarse y pasar de un estado inicial a otro final si se las somete a determinadas condiciones. Por ejemplo,
PRÁCTICAS DE EQUILIBRIO QUÍMICO
 PRÁCTICAS DE EQUILIBRIO QUÍMICO Le Chatelier PAU RESUELTOS Julio FG 2012 Para estudiar experimentalmente el equilibrio en disolución: Fe 3+ (ac) + 6 SCN - (ac) [Fe(SCN) 6 ] 3- (ac), se prepara una disolución
PRÁCTICAS DE EQUILIBRIO QUÍMICO Le Chatelier PAU RESUELTOS Julio FG 2012 Para estudiar experimentalmente el equilibrio en disolución: Fe 3+ (ac) + 6 SCN - (ac) [Fe(SCN) 6 ] 3- (ac), se prepara una disolución
PRÁCTICA Nº 6 EQUILIBRIO QUÍMICO
 PRÁCTICA Nº 6 EQUILIBRIO QUÍMICO OBJETIVOS Comprobar la perturbación en un sistema en equilibrio de complejos de cobalto (II), cuando se modifican la concentración de las sustancias implicadas y la temperatura.
PRÁCTICA Nº 6 EQUILIBRIO QUÍMICO OBJETIVOS Comprobar la perturbación en un sistema en equilibrio de complejos de cobalto (II), cuando se modifican la concentración de las sustancias implicadas y la temperatura.
JUNIO FASE ESPECÍFICA. QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Disponemos de los pares redox (Fe 2+ /Fe) y (O 2 /H 2 O), con potenciales estándar de reducción 0,44 V y +1,23 V, respectivamente. Con ellos
JUNIO 2011. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Disponemos de los pares redox (Fe 2+ /Fe) y (O 2 /H 2 O), con potenciales estándar de reducción 0,44 V y +1,23 V, respectivamente. Con ellos
QUÍMICA. Si no indican los estados de agregación de todas las sustancias se restan 0,25 puntos. (0,5 puntos)
 OPCIÓN A QUÍMICA. 1. (2,5 puntos) Las entalpías estándar de formación del CO 2 (g) y del H 2 O(l) son -393,5 kj mol -1 y -285,8 kj mol -1, respectivamente. La entalpía estándar de combustión del ácido
OPCIÓN A QUÍMICA. 1. (2,5 puntos) Las entalpías estándar de formación del CO 2 (g) y del H 2 O(l) son -393,5 kj mol -1 y -285,8 kj mol -1, respectivamente. La entalpía estándar de combustión del ácido
MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES PREGUNTAS
 MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES a. El examen de química consistirá en 30 preguntas de tipo test b. La duración del examen será de 1,5 horas. c. Sólo hay que elegir una respuesta por
MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES a. El examen de química consistirá en 30 preguntas de tipo test b. La duración del examen será de 1,5 horas. c. Sólo hay que elegir una respuesta por
Aplicación de la Ley de Hess: ΔHº (kj/mol)
 QUÍMICA. OPCIÓN A 1. (2,5 puntos) La reacción de metano, CH 4 (g), con cloro, Cl 2 (g), en condiciones estándar, produce cloruro de hidrógeno, HCl(g), y cloroformo, CHCl 3 (g). Calcule la variación de
QUÍMICA. OPCIÓN A 1. (2,5 puntos) La reacción de metano, CH 4 (g), con cloro, Cl 2 (g), en condiciones estándar, produce cloruro de hidrógeno, HCl(g), y cloroformo, CHCl 3 (g). Calcule la variación de
8/12/2014. Examinar y clasificar una serie de reacciones como: Precipitación Neutralización {ácido-base} Oxidación-reducción Complejación.
 Cambios Químicos Química General Laboratorio I QUIM 3003 Ileana Nieves Martínez http://quimicacem.blogspot.com/2009/04/los-cambiosquimicos-y-fisicos.html Objetivos Examinar y clasificar una serie de reacciones
Cambios Químicos Química General Laboratorio I QUIM 3003 Ileana Nieves Martínez http://quimicacem.blogspot.com/2009/04/los-cambiosquimicos-y-fisicos.html Objetivos Examinar y clasificar una serie de reacciones
QUÍMICA. OPCIÓN A. 1. (2,5 puntos)
 1. (2,5 puntos) QUÍMICA. OPCIÓN A La combustión completa de 40 g de acetona, C 3 H 6 O(l), libera 1234,5 kj. Si las entalpías estándar de formación del CO 2 (g) y del H 2 O(l) son -393,5 y -285,8 kj mol
1. (2,5 puntos) QUÍMICA. OPCIÓN A La combustión completa de 40 g de acetona, C 3 H 6 O(l), libera 1234,5 kj. Si las entalpías estándar de formación del CO 2 (g) y del H 2 O(l) son -393,5 y -285,8 kj mol
JUNIO FASE GENERAL QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
JULIO FASE ESPECÍFICA QUÍMICA. OPCIÓN A
 JULIO 2011. FASE ESPECÍFICA 1. (2,5 puntos) QUÍMICA. OPCIÓN A Calcule la entalpía estándar de formación del metanol líquido a partir de los siguientes datos: ΔHº f [H 2 O(l)] = - 285,5 kj/mol; ΔHº f [CO
JULIO 2011. FASE ESPECÍFICA 1. (2,5 puntos) QUÍMICA. OPCIÓN A Calcule la entalpía estándar de formación del metanol líquido a partir de los siguientes datos: ΔHº f [H 2 O(l)] = - 285,5 kj/mol; ΔHº f [CO
+ F(g) Prueba de evaluación de Bachillerato para el acceso a la Universidad (EBAU) Curso QUÍMICA OPCIÓN A. 1.
 QUÍMICA OPCIÓN A 1. (2,5 puntos) Dibuje el ciclo de Born-Haber y calcule la energía de red (ΔH red) del KF(s) a partir de los siguientes datos: Entalpía estándar de formación del KF(s) [ΔH f(kf)] = - 567,4
QUÍMICA OPCIÓN A 1. (2,5 puntos) Dibuje el ciclo de Born-Haber y calcule la energía de red (ΔH red) del KF(s) a partir de los siguientes datos: Entalpía estándar de formación del KF(s) [ΔH f(kf)] = - 567,4
XX OLIMPIADA DE QUÍMICA CUESTIONES
 XX OLIMPIADA DE QUÍMICA CUESTIONES 1º) Se quema con una cerilla un poco de alcohol en un plato hasta que no quede nada de líquido. Indica cual de las siguientes proposiciones es la correcta: a) Los gases
XX OLIMPIADA DE QUÍMICA CUESTIONES 1º) Se quema con una cerilla un poco de alcohol en un plato hasta que no quede nada de líquido. Indica cual de las siguientes proposiciones es la correcta: a) Los gases
QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A
 1. (2,5 puntos) QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A Las entalpías estándar de combustión del C(s), H 2 (g) y propano gas, C 3 H 8 (g), son -394, -286 y -2220 kj/mol, respectivamente: i. Calcule la entalpía
1. (2,5 puntos) QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A Las entalpías estándar de combustión del C(s), H 2 (g) y propano gas, C 3 H 8 (g), son -394, -286 y -2220 kj/mol, respectivamente: i. Calcule la entalpía
Práctica 12. Equilibrios de óxido-reducción. Estados de oxidación y potenciales estándar
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Problema 1. Práctica 12. Equilibrios de óxido-reducción. Estados de oxidación y potenciales
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Problema 1. Práctica 12. Equilibrios de óxido-reducción. Estados de oxidación y potenciales
UNIDAD 3. EQULIBRIO QUÍMICO
 UNIDAD 3. EQULIBRIO QUÍMICO Equilibrio químico y características Constantes de equilibrio: K c y K p Grado de disociación Cociente de reacción Factores que afectan al equilibrio químico. Principio de Le
UNIDAD 3. EQULIBRIO QUÍMICO Equilibrio químico y características Constantes de equilibrio: K c y K p Grado de disociación Cociente de reacción Factores que afectan al equilibrio químico. Principio de Le
JUNIO FASE ESPECÍFICA
 JUNIO 2012. FASE ESPECÍFICA OPCIÓN A QUÍMICA. 1. (2,5 puntos) La combustión de amoniaco, NH 3 (g), genera NO(g) y H 2 O(g), liberándose 226 kj/mol de amoniaco en condiciones estándar. i. Escriba la ecuación
JUNIO 2012. FASE ESPECÍFICA OPCIÓN A QUÍMICA. 1. (2,5 puntos) La combustión de amoniaco, NH 3 (g), genera NO(g) y H 2 O(g), liberándose 226 kj/mol de amoniaco en condiciones estándar. i. Escriba la ecuación
Práctica 12. Equilibrios de óxido-reducción. Estados de oxidación y potenciales estándar
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Problema 1. Práctica 12. Equilibrios de óxido-reducción. Estados de oxidación y potenciales
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Problema 1. Práctica 12. Equilibrios de óxido-reducción. Estados de oxidación y potenciales
Equilibrio químico EQUILIBRIO QUÍMICO QUÍMICA 2º
 Equilibrio químico Qué es un equilibrio químico? En una reacción química reversible como: a A + b B c C + d D se dan dos reacciones al mismo tiempo, por un lado A y B reaccionan para dar C y D y, conforme
Equilibrio químico Qué es un equilibrio químico? En una reacción química reversible como: a A + b B c C + d D se dan dos reacciones al mismo tiempo, por un lado A y B reaccionan para dar C y D y, conforme
QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA
 QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA 2016 Equipo docente: Profesora Titular: Dra. Graciela Valente Profesora Adjunta: Dra. Cecilia Medaura Jefes de Trabajos
QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA 2016 Equipo docente: Profesora Titular: Dra. Graciela Valente Profesora Adjunta: Dra. Cecilia Medaura Jefes de Trabajos
Reacciones de precipitación
 Reacciones de precipitación Criterios de evaluación Aplicar el concepto de equilibrio químico para predecir la evolución de un sistema y resolver problemas de equilibrios homogéneos, en particular en reacciones
Reacciones de precipitación Criterios de evaluación Aplicar el concepto de equilibrio químico para predecir la evolución de un sistema y resolver problemas de equilibrios homogéneos, en particular en reacciones
Cómo se puede modificar la situación de equilibrio?
 Cómo se puede modificar la situación de equilibrio? Cambiando la constante de equilibrio Cambiando la temperatura Sin cambiar la constante de equilibrio Cambiando el resto de condiciones Principio de Le
Cómo se puede modificar la situación de equilibrio? Cambiando la constante de equilibrio Cambiando la temperatura Sin cambiar la constante de equilibrio Cambiando el resto de condiciones Principio de Le
PRÁCTICA 18 EQUILIBRIOS DE SOLUBILIDAD. ESTIMACIÓN DEL PRODUCTO DE SOLUBILIDAD DEL HIDRÓXIDO DE ZINC.
 PRÁCTICA 18 EQUILIBRIOS DE SOLUBILIDAD. ESTIMACIÓN DEL PRODUCTO DE SOLUBILIDAD DEL HIDRÓXIDO DE ZINC. OBJETIVOS Determinar experimentalmente si se forma o no un determinado compuesto insoluble. Determinar
PRÁCTICA 18 EQUILIBRIOS DE SOLUBILIDAD. ESTIMACIÓN DEL PRODUCTO DE SOLUBILIDAD DEL HIDRÓXIDO DE ZINC. OBJETIVOS Determinar experimentalmente si se forma o no un determinado compuesto insoluble. Determinar
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO I)
 PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO I) Las preguntas de este tipo constan de un enunciado y de cuatro posibilidades de respuesta entre las cuales debe escoger la que considere correcta
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO I) Las preguntas de este tipo constan de un enunciado y de cuatro posibilidades de respuesta entre las cuales debe escoger la que considere correcta
PRÁCTICA Nº 7 EQUILIBRIO QUÍMICO
 PRÁCTICA Nº 7 EQUILIBRIO QUÍMICO OBJETIVOS Comprobar la perturbación en un sistema en equilibrio de complejos de cobalto (II), cuando se modifican la concentración de las sustancias implicadas y la temperatura.
PRÁCTICA Nº 7 EQUILIBRIO QUÍMICO OBJETIVOS Comprobar la perturbación en un sistema en equilibrio de complejos de cobalto (II), cuando se modifican la concentración de las sustancias implicadas y la temperatura.
TRABAJO PRÁCTICO N 7 EQUILIBRIO QUÍMICO
 TRABAJO PRÁCTICO N 7 EQUILIBRIO QUÍMICO Algunos conceptos teóricos: Reacciones reversibles: Es probable que todas las reacciones químicas puedan producirse en ambos sentidos, pero en muchos casos la magnitud
TRABAJO PRÁCTICO N 7 EQUILIBRIO QUÍMICO Algunos conceptos teóricos: Reacciones reversibles: Es probable que todas las reacciones químicas puedan producirse en ambos sentidos, pero en muchos casos la magnitud
QUÍMICA. Solución: i. Reacción de reducción: la que presente el potencial estándar de reducción más alto. Si sólo escribe correctamente la ecuación.
 QUÍMICA OPCIÓN A 1. (2,5 puntos) Dispone de los pares redox (Cr 2 O 2-7 /Cr 3+ ) y (Ag + /Ag), cuyos potenciales estándar de reducción en medio ácido son, respectivamente, + 1,33 y + 0,80 V. Con ellos
QUÍMICA OPCIÓN A 1. (2,5 puntos) Dispone de los pares redox (Cr 2 O 2-7 /Cr 3+ ) y (Ag + /Ag), cuyos potenciales estándar de reducción en medio ácido son, respectivamente, + 1,33 y + 0,80 V. Con ellos
EQUILIBRIO QUIMICO. Equilibrio en soluciones. FUNDAMENTO TEORICO (principio de Lechatelier) Objetivos
 Departamento de Química Practica Nº 5-2 EQUILIBRIO QUIMICO Equilibrio en soluciones Objetivos 1. Observar la reversibilidad de un equilibrio químico por efecto de la temperatura. 2. Estudiar las reacciones
Departamento de Química Practica Nº 5-2 EQUILIBRIO QUIMICO Equilibrio en soluciones Objetivos 1. Observar la reversibilidad de un equilibrio químico por efecto de la temperatura. 2. Estudiar las reacciones
TEMA 6 Termoquímica y Equilibrio Químico
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE INGENIERÍA DIVISIÓN DE CIENCIAS BÁSICAS TEMA 6 Termoquímica y Equilibrio Químico Ana Laura Pérez Martínez Academia de Química; 2016 2 Ana Laura Pérez
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE INGENIERÍA DIVISIÓN DE CIENCIAS BÁSICAS TEMA 6 Termoquímica y Equilibrio Químico Ana Laura Pérez Martínez Academia de Química; 2016 2 Ana Laura Pérez
QUÍMICA. Indique el electrodo que actuará como ánodo y el que actuará como cátodo y calcule el potencial estándar de la pila.
 QUÍMICA OPCIÓN A 1. (2,5 puntos) Se construye una pila voltaica con los siguientes electrodos: Electrodo estándar MnO - 4 /Mn 2+ en medio ácido sulfúrico. Las disoluciones del electrodo son de permanganato
QUÍMICA OPCIÓN A 1. (2,5 puntos) Se construye una pila voltaica con los siguientes electrodos: Electrodo estándar MnO - 4 /Mn 2+ en medio ácido sulfúrico. Las disoluciones del electrodo son de permanganato
HCl. NaCl + CO. AgCl + NaNO. Al SO + H H SO. CaO + CO. Na2CO. ZnSO. Hg + CuCl. MgO ZnCl. REACCIONES QUíMICAS
 Dadas las siguientes reacciones químicas, contesta: Qué sustancias son reactivos? Cuáles son productos?. Ajústalas a) H + Cl HCl b) CH5OH + O c) HCl + NaHCO NaCl + CO d) NaCl + AgNO AgCl + NaNO e) CO +
Dadas las siguientes reacciones químicas, contesta: Qué sustancias son reactivos? Cuáles son productos?. Ajústalas a) H + Cl HCl b) CH5OH + O c) HCl + NaHCO NaCl + CO d) NaCl + AgNO AgCl + NaNO e) CO +
TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN
 TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN Las reacciones químicas de óxido - reducción (reacciones redox) son aquellas en las cuales se produce una transferencia de electrones. Son las reacciones donde se producen
TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN Las reacciones químicas de óxido - reducción (reacciones redox) son aquellas en las cuales se produce una transferencia de electrones. Son las reacciones donde se producen
TERMOQUÍMICA. ENTALPÍA DE DISOLUCIÓN
 TERMOQUÍMICA. ENTALPÍA DE DISOLUCIÓN M. C. Q. Alfredo Velásquez Márquez Objetivos de la práctica El alumno: 1. Conocerá el concepto sobre el cual se basa el funcionamiento de las compresas instantáneas
TERMOQUÍMICA. ENTALPÍA DE DISOLUCIÓN M. C. Q. Alfredo Velásquez Márquez Objetivos de la práctica El alumno: 1. Conocerá el concepto sobre el cual se basa el funcionamiento de las compresas instantáneas
2º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD
 º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD Indice 1. Equilibrios heterogéneos.. Solubilidad. Reglas de solubilidad. 3. Reacciones de precipitación. 4. Producto de solubilidad. 5. Factores que modifican
º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD Indice 1. Equilibrios heterogéneos.. Solubilidad. Reglas de solubilidad. 3. Reacciones de precipitación. 4. Producto de solubilidad. 5. Factores que modifican
C(grafito) + ½ O 2 (g) + Cl 2 (g) COCl 2 (g)
 QUÍMICA. OPCIÓN A 1. (2,5 puntos) Las entalpías estándar de combustión del C(grafito) y del CO(g) son -393,5 y -283 kj/mol, respectivamente. La entalpía estándar de la reacción: CO(g) + 2 (g) CO 2 (g)
QUÍMICA. OPCIÓN A 1. (2,5 puntos) Las entalpías estándar de combustión del C(grafito) y del CO(g) son -393,5 y -283 kj/mol, respectivamente. La entalpía estándar de la reacción: CO(g) + 2 (g) CO 2 (g)
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre 2006 PRIMERA PARTE
 1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
OPCIÓN A. Solución: Solución:
 OPCIÓN A CUESTIÓN 1.- Considera los compuestos NH 3, CH 4 y HF e indica razonadamente: a) Qué tipo de enlace presentan. b) Cuál o cuáles son polares. c) Aquéllos compuestos con enlace de hidrógeno. d)
OPCIÓN A CUESTIÓN 1.- Considera los compuestos NH 3, CH 4 y HF e indica razonadamente: a) Qué tipo de enlace presentan. b) Cuál o cuáles son polares. c) Aquéllos compuestos con enlace de hidrógeno. d)
Reacciones Químicas. Que es una reacción química?
 Reacciones Químicas Tema 11 Química General Que es una reacción química? proceso en el cual un grupo de sustancias denominadas reactivos se trasforman en otro grupo denominados productos. Evidencia para
Reacciones Químicas Tema 11 Química General Que es una reacción química? proceso en el cual un grupo de sustancias denominadas reactivos se trasforman en otro grupo denominados productos. Evidencia para
Práctica 12. Equilibrios de óxido reducción. Estados de oxidación y potenciales estándar
 Equipo: Nombre: Nombre: Nombre: Problema 1. Práctica 12. Equilibrios de óxido reducción. Estados de oxidación y potenciales estándar Qué equilibrios de óxido reducción se pueden observar en la reacción
Equipo: Nombre: Nombre: Nombre: Problema 1. Práctica 12. Equilibrios de óxido reducción. Estados de oxidación y potenciales estándar Qué equilibrios de óxido reducción se pueden observar en la reacción
QG II Influencia de la temperatura sobre el equilibrio Página 1
 8. Influencia de la temperatura en el equilibrio químico Experimento 1 Problema Encontrar la relación entre la absorción o desprendimiento de calor en una reacción química, con el sentido en que se desplaza
8. Influencia de la temperatura en el equilibrio químico Experimento 1 Problema Encontrar la relación entre la absorción o desprendimiento de calor en una reacción química, con el sentido en que se desplaza
REACCIONES DE PRECIPITACIÓN
 REACCIONES DE PRECIPITACIÓN CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA REACCIONES DE PRECIPITACIÓN Aquellas que tienen lugar entre iones en disolución que forman compuestos insolubles. Se establece
REACCIONES DE PRECIPITACIÓN CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA REACCIONES DE PRECIPITACIÓN Aquellas que tienen lugar entre iones en disolución que forman compuestos insolubles. Se establece
NOTA CALI/ORDEN/PRES ORTOGRAFÍA PUNTUACIÓN EXPRESIÓN NOTA FINAL
 1.- Formule o nombre los compuestos siguientes: a) Nitrito de escandio b) Peróxido de plata c) Ácido 2-hidroxiprop-2-enoico d) NH 4 H 2 PO 4 e) Y(CN) 3 f) C H 2 =CHCON(CH 3 ) 2 Res. a) Sc(NO 2 ) 3 ; b)
1.- Formule o nombre los compuestos siguientes: a) Nitrito de escandio b) Peróxido de plata c) Ácido 2-hidroxiprop-2-enoico d) NH 4 H 2 PO 4 e) Y(CN) 3 f) C H 2 =CHCON(CH 3 ) 2 Res. a) Sc(NO 2 ) 3 ; b)
una reacción química Según la teoría cinéticomolecular
 REACCIONES QUÍMICAS Qué es una reacción química? Según la teoría cinéticomolecular una reacción química consiste en las roturas de las moléculas de las sustancias iniciales, reordenándose los átomos de
REACCIONES QUÍMICAS Qué es una reacción química? Según la teoría cinéticomolecular una reacción química consiste en las roturas de las moléculas de las sustancias iniciales, reordenándose los átomos de
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE.
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
EQUILIBRIO QUÍMICO. Cuando ocurre una reacción química, termina agotándose siempre, al menos, uno de los reactivos?
 EQUILIBRIO QUÍMICO Cuando ocurre una reacción química, termina agotándose siempre, al menos, uno de los reactivos? DEFINICIÓN DE EQUILIBRIO QUÍMICO Las reacciones que ocurren en un único sentido se llaman
EQUILIBRIO QUÍMICO Cuando ocurre una reacción química, termina agotándose siempre, al menos, uno de los reactivos? DEFINICIÓN DE EQUILIBRIO QUÍMICO Las reacciones que ocurren en un único sentido se llaman
XXIX OLIMPIADA DE QUÍMICA Fase Local EXTREMADURA Nombre:
 TEST DE PREGUNTAS MULTIRRESPUESTA (4 puntos) Se deberá marcar con una cruz en la HOJA de RESPUESTAS (al final del test) la respuesta correcta de cada pregunta (sólo hay una respuesta válida en cada pregunta).
TEST DE PREGUNTAS MULTIRRESPUESTA (4 puntos) Se deberá marcar con una cruz en la HOJA de RESPUESTAS (al final del test) la respuesta correcta de cada pregunta (sólo hay una respuesta válida en cada pregunta).
PROBLEMA 1. Se hace reaccionar 50 gramos de calcio con ácido clorhídrico 2 M para dar hidrógeno gaseoso y cloruro de calcio.
 PROBLEMA. Se hace reaccionar 50 gramos de calcio con ácido clorhídrico 2 M para dar hidrógeno gaseoso y cloruro de calcio. a) Calcular el volumen de disolución de ácido clorhídrico necesario para que reaccione
PROBLEMA. Se hace reaccionar 50 gramos de calcio con ácido clorhídrico 2 M para dar hidrógeno gaseoso y cloruro de calcio. a) Calcular el volumen de disolución de ácido clorhídrico necesario para que reaccione
Reacciones. Reacciones acido y base Combustión. Precipitación I MEDIO
 Reacciones Combustión Es la reacción de una sustancia, llamada combustible, con oxígeno, al que se le llama comburente, en la reacción se forman dióxido de carbono y agua y se desprende gran cantidad de
Reacciones Combustión Es la reacción de una sustancia, llamada combustible, con oxígeno, al que se le llama comburente, en la reacción se forman dióxido de carbono y agua y se desprende gran cantidad de
Práctica 11: Equilibrios de Solubilidad
 Equipo: Nombre: Nombre: Nombre: Práctica 11: Equilibrios de Solubilidad PROBLEMAS: Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, Cu (S) y Cu 2 [Fe(CN)
Equipo: Nombre: Nombre: Nombre: Práctica 11: Equilibrios de Solubilidad PROBLEMAS: Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, Cu (S) y Cu 2 [Fe(CN)
II MINIOLIMPIADA DE QUÍMICA DE CANTABRIA CUESTIONARIO TIPO TEST (Parte II) 27 de mayo de 2016
 Sección Territorial de Cantabria de la II MINIOLIMPIADA DE QUÍMICA DE CANTABRIA CUESTIONARIO TIPO TEST (Parte II) 27 de mayo de 2016 Nombre y apellidos: Conteste en la Hoja de Respuestas. Sólo hay una
Sección Territorial de Cantabria de la II MINIOLIMPIADA DE QUÍMICA DE CANTABRIA CUESTIONARIO TIPO TEST (Parte II) 27 de mayo de 2016 Nombre y apellidos: Conteste en la Hoja de Respuestas. Sólo hay una
C/ Fernando Poo 5 Madrid (Metro Delicias o Embajadores).
 Junio 2012-2013 OPCION A Problema 1: Z=9 = = Periodo 2, Grupo 17 =Flúor=F Z=11 = =Periodo 3, Grupo 1 =Sodio=Na Potencial de ionización: energía necesaria para arrancar un electrón de un átomo. El segundo
Junio 2012-2013 OPCION A Problema 1: Z=9 = = Periodo 2, Grupo 17 =Flúor=F Z=11 = =Periodo 3, Grupo 1 =Sodio=Na Potencial de ionización: energía necesaria para arrancar un electrón de un átomo. El segundo
QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g)
![QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g) QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g)](/thumbs/49/25837773.jpg) OPCIÓN A QUÍMICA. 1. (2,5 puntos) Construya el ciclo de Born-aber y calcule la energía de red (Δ red ) del KCl(s) a partir de los siguientes datos: Entalpía estándar de formación del KCl(s) [Δ f (KCl)]
OPCIÓN A QUÍMICA. 1. (2,5 puntos) Construya el ciclo de Born-aber y calcule la energía de red (Δ red ) del KCl(s) a partir de los siguientes datos: Entalpía estándar de formación del KCl(s) [Δ f (KCl)]
qreac. + qsln.= 0 qreac. = -qsln.
 PRÁCTICA Nº 4 TERMODINÁMICA OBJETIVOS Determinar la variación de entalpía de una reacción de oxido reducción. Identificar los procesos endotérmicos y exotérmicos, mediante análisis cualitativo. I.ASPECTOS
PRÁCTICA Nº 4 TERMODINÁMICA OBJETIVOS Determinar la variación de entalpía de una reacción de oxido reducción. Identificar los procesos endotérmicos y exotérmicos, mediante análisis cualitativo. I.ASPECTOS
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO. Nombre: Nombre:
 Equipo: LABORATORIO DE QUÍMICA GENERAL II Nombre: Nombre: Nombre: Práctica 7 Influencia de la temperatura en el equilibrio químico Problema: Encontrar la relación entre la absorción o desprendimiento de
Equipo: LABORATORIO DE QUÍMICA GENERAL II Nombre: Nombre: Nombre: Práctica 7 Influencia de la temperatura en el equilibrio químico Problema: Encontrar la relación entre la absorción o desprendimiento de
QUÍMICA 2º BACHILLERATO
 1.-/ Para los compuestos poco solubles CuBr, Ba(IO 3 ) 2 y Fe(OH) 3 : a) Escriba la ecuación de equilibrio de solubilidad en agua. b) La expresión del producto de solubilidad. c) El valor de la solubilidad
1.-/ Para los compuestos poco solubles CuBr, Ba(IO 3 ) 2 y Fe(OH) 3 : a) Escriba la ecuación de equilibrio de solubilidad en agua. b) La expresión del producto de solubilidad. c) El valor de la solubilidad
Examen opcional de Química de 2º de Bachillerato
 Examen opcional de Química de 2º de Bachillerato Nombre: Fecha: 1. Se han obtenido los siguientes resultados para la reacción A + B C a una determinada temperatura: Experiencia [A] 0 (moles L -1 ) [B]
Examen opcional de Química de 2º de Bachillerato Nombre: Fecha: 1. Se han obtenido los siguientes resultados para la reacción A + B C a una determinada temperatura: Experiencia [A] 0 (moles L -1 ) [B]
JULIO FASE GENERAL QUÍMICA. OPCIÓN A
 JULIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A Las entalpías estándar de combustión del C 2 H 2 (g), C 2 H 6 (g) y del H 2 (g), son -1300, -1560 y -286 kj/mol, respectivamente: i. Calcule la
JULIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A Las entalpías estándar de combustión del C 2 H 2 (g), C 2 H 6 (g) y del H 2 (g), son -1300, -1560 y -286 kj/mol, respectivamente: i. Calcule la
a) Una disolución acuosa 0,01 M de ácido nítrico tiene ph = 2. ph = log [H+] = log(0,01) = 2
![a) Una disolución acuosa 0,01 M de ácido nítrico tiene ph = 2. ph = log [H+] = log(0,01) = 2 a) Una disolución acuosa 0,01 M de ácido nítrico tiene ph = 2. ph = log [H+] = log(0,01) = 2](/thumbs/58/41715107.jpg) 1 PAU Química. Septiembre 2011. OPCIÓN A Pregunta 1A. Para los elementos A, B, C y D, de números atómicos 3, 10, 20 y 35, respectivamente: a) Escriba la configuración electrónica de cada uno de ellos.
1 PAU Química. Septiembre 2011. OPCIÓN A Pregunta 1A. Para los elementos A, B, C y D, de números atómicos 3, 10, 20 y 35, respectivamente: a) Escriba la configuración electrónica de cada uno de ellos.
TRBAJO PRÁCTICO N 5: ph. Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes.
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
FÍSICA Y QUÍMICA Solucionario ÁCIDOS Y BASES
 FÍSICA Y QUÍMICA Solucionario ÁCIDOS Y BASES 1.* Calculad la molaridad de las siguientes disoluciones. a) Añadimos 3,6 moles de NaCl a 0,5 l de agua. 7 M b) Añadimos 2,5 moles de NaCl a 0,4 l de agua.
FÍSICA Y QUÍMICA Solucionario ÁCIDOS Y BASES 1.* Calculad la molaridad de las siguientes disoluciones. a) Añadimos 3,6 moles de NaCl a 0,5 l de agua. 7 M b) Añadimos 2,5 moles de NaCl a 0,4 l de agua.
Práctica 11 Equilibrios de Solubilidad
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: Nombre: Nombre: Nombre: Nombre: Nombre: 1 PROBLEMAS: Práctica 11 Equilibrios de Solubilidad
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: Nombre: Nombre: Nombre: Nombre: Nombre: 1 PROBLEMAS: Práctica 11 Equilibrios de Solubilidad
6. Termoquímica. Transformaciones químicas. mica. Andrés s Cedillo, AT
 Transformaciones químicas Andrés s Cedillo, AT-250 cedillo@xanum.uam.mx www.fqt.izt.uam.mx/cedillo 6. Termoquímica mica 6.1. Definiciones 6.2. Calorimetría 6.3. Entalpía 6.4. Cálculos termoquímicos micos
Transformaciones químicas Andrés s Cedillo, AT-250 cedillo@xanum.uam.mx www.fqt.izt.uam.mx/cedillo 6. Termoquímica mica 6.1. Definiciones 6.2. Calorimetría 6.3. Entalpía 6.4. Cálculos termoquímicos micos
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE
 COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE 1 2 3 4 PRACTICA # 1 NOMENCLATURA QUÍMICA OBJETIVO DE LA PRÁCTICA: Identificar los aniones y cationes que forman
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE 1 2 3 4 PRACTICA # 1 NOMENCLATURA QUÍMICA OBJETIVO DE LA PRÁCTICA: Identificar los aniones y cationes que forman
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Junio Fase general OPCIÓN A
 1 PAU Química. Junio 2010. Fase general OPCIÓN A Cuestión 1A. El elemento de número atómico 12 se combina fácilmente con el elemento de número atómico 17. Indique: a) La configuración electrónica de los
1 PAU Química. Junio 2010. Fase general OPCIÓN A Cuestión 1A. El elemento de número atómico 12 se combina fácilmente con el elemento de número atómico 17. Indique: a) La configuración electrónica de los
Práctica 4: Termoquímica: Valoraciones
 Práctica 4: Termoquímica: Valoraciones Ingeniería agrónoma grado en hortofruticultura y jardinería Jorge Cerezo Martínez Objetivos Comprender el fundamento de las valoraciones químicas. Aplicar la metodología
Práctica 4: Termoquímica: Valoraciones Ingeniería agrónoma grado en hortofruticultura y jardinería Jorge Cerezo Martínez Objetivos Comprender el fundamento de las valoraciones químicas. Aplicar la metodología
XXVII OLIMPIADA DE QUÍMICA Fase Local EXTREMADURA Nombre:
 EXTREMADURA - 014 TEST DE PREGUNTAS MULTIRRESPUESTA (4 puntos) Se deberá marcar con una cruz en la HOJA de RESPUESTAS (al final del test) la respuesta correcta de cada pregunta (sólo hay una respuesta
EXTREMADURA - 014 TEST DE PREGUNTAS MULTIRRESPUESTA (4 puntos) Se deberá marcar con una cruz en la HOJA de RESPUESTAS (al final del test) la respuesta correcta de cada pregunta (sólo hay una respuesta
Práctica 11: Equilibrios de Solubilidad
 Equipo: PROBLEMAS: Nombre: Nombre: Nombre: Práctica 11: Equilibrios de Solubilidad Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, Cu (S) y Cu 2 [Fe(CN)
Equipo: PROBLEMAS: Nombre: Nombre: Nombre: Práctica 11: Equilibrios de Solubilidad Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, Cu (S) y Cu 2 [Fe(CN)
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Curso 2009-2010 INSTRUCCIONES Y CRITERIOS GENERALES DE CALIFICACIÓN
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Curso 2009-2010 INSTRUCCIONES Y CRITERIOS GENERALES DE CALIFICACIÓN
OPCIÓN A. = 0,789 g ml 1 30,4 ml = 23,98 g.
 OPCIÓN A PROBLEMA 2.- En el proceso de elaboración del vino, la glucosa fermenta para producir etanol según la siguiente reacción (no ajustada): C 6 H 12 O 6 (aq) C 2 H 5 OH (aq) + CO 2 (g). a) Si, en
OPCIÓN A PROBLEMA 2.- En el proceso de elaboración del vino, la glucosa fermenta para producir etanol según la siguiente reacción (no ajustada): C 6 H 12 O 6 (aq) C 2 H 5 OH (aq) + CO 2 (g). a) Si, en
EXAMEN II QUÍMICA de 2º Bto. A 2ª Evaluación Viernes,
 EXAMEN II QUÍMICA de 2º Bto. A 2ª Evaluación Viernes, 26-2-2015 NOMBRE:............................................................................. NOTA: 1.- (2,00 puntos) Nombra o formula las siguientes
EXAMEN II QUÍMICA de 2º Bto. A 2ª Evaluación Viernes, 26-2-2015 NOMBRE:............................................................................. NOTA: 1.- (2,00 puntos) Nombra o formula las siguientes
CUESTIONARIOS FÍSICA 4º ESO
 DPTO FÍSICA QUÍMICA. IES POLITÉCNICO CARTAGENA CUESTIONARIOS FÍSICA º ESO UNIDADES 8 y 10 Átomos, elementos y compuestos. Las reacciones químicas Mª Teresa Gómez Ruiz 2010 HTTP://WWW. POLITECNICOCARTAGENA.
DPTO FÍSICA QUÍMICA. IES POLITÉCNICO CARTAGENA CUESTIONARIOS FÍSICA º ESO UNIDADES 8 y 10 Átomos, elementos y compuestos. Las reacciones químicas Mª Teresa Gómez Ruiz 2010 HTTP://WWW. POLITECNICOCARTAGENA.
PVQ28-1.**. Mezcla de Fe/S con ácido sulfúrico reaccionando sobre sulfato de cobre(ii)
 PROBLEMAS VISUALES DE QUÍMICA PVQ8-1.**. Mezcla de Fe/S con ácido sulfúrico reaccionando sobre sulfato de cobre(ii) En A se disponen 5,6 de Fe y 3,g de azufre,y 10mL de ácido sulfúrico 6N,y en B, 30mL
PROBLEMAS VISUALES DE QUÍMICA PVQ8-1.**. Mezcla de Fe/S con ácido sulfúrico reaccionando sobre sulfato de cobre(ii) En A se disponen 5,6 de Fe y 3,g de azufre,y 10mL de ácido sulfúrico 6N,y en B, 30mL
REPASO DE SELECTIVIDAD TEMAS 1, 2, 3, 4, 5, 6
 REPASO DE SELECTIVIDAD TEMAS 1, 2, 3, 4, 5, 6 1.- Un litro de CO 2 se encuentra en condiciones normales. Calcula: a.- El número de moles que contiene. b.- El número de moléculas de CO 2 presentes. c.-
REPASO DE SELECTIVIDAD TEMAS 1, 2, 3, 4, 5, 6 1.- Un litro de CO 2 se encuentra en condiciones normales. Calcula: a.- El número de moles que contiene. b.- El número de moléculas de CO 2 presentes. c.-
disolución 4. Reacciones en Transformaciones químicas Andrés s Cedillo, AT
 Transformaciones químicas Andrés s Cedillo, AT-250 cedillo@xanum.uam.mx www.fqt.izt.uam.mx/cedillo 4. Reacciones en disolución 4.1. Concentración 4.2. Reacciones de precipitación base Cap. 3 4.1. Concentración
Transformaciones químicas Andrés s Cedillo, AT-250 cedillo@xanum.uam.mx www.fqt.izt.uam.mx/cedillo 4. Reacciones en disolución 4.1. Concentración 4.2. Reacciones de precipitación base Cap. 3 4.1. Concentración
Electroquímic a a tu alcance
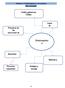 Práctica 2. Electroquímica a tu alcance Mapa conceptual Celdas galvánicas Celdas electroquímicas Principios de las reacciones de óxido reducción Leyes de Faraday Electroquímic a a tu alcance Electrólisi
Práctica 2. Electroquímica a tu alcance Mapa conceptual Celdas galvánicas Celdas electroquímicas Principios de las reacciones de óxido reducción Leyes de Faraday Electroquímic a a tu alcance Electrólisi
CAMBIOS QUÍMICOS ACTIVIDADES DE REFUERZO ACTIVIDADES FICHA 1
 FICHA 1 DE REFUERZO 1. Escribe la fórmula y calcula la masa mo lecular de las siguientes sustancias: a) Dióxido de azufre. b) Hidruro de potasio. c) Ácido sulfúrico. d) Cloruro de berilio. 2. En un laboratorio
FICHA 1 DE REFUERZO 1. Escribe la fórmula y calcula la masa mo lecular de las siguientes sustancias: a) Dióxido de azufre. b) Hidruro de potasio. c) Ácido sulfúrico. d) Cloruro de berilio. 2. En un laboratorio
TERMODINÁMICA - PREGUNTAS DE TEST
 TERMODINÁMICA - PREGUNTAS DE TEST Grupo A: DEFINICIONES DE VARIABLES. CONCEPTOS GENERALES Grupo B: MAQUINAS TÉRMICAS: Grupo C: PRIMER PRINCIPIO: Grupo D: SEGUNDO PRINCIPIO: Grupo E: ESPONTANEIDAD DE LAS
TERMODINÁMICA - PREGUNTAS DE TEST Grupo A: DEFINICIONES DE VARIABLES. CONCEPTOS GENERALES Grupo B: MAQUINAS TÉRMICAS: Grupo C: PRIMER PRINCIPIO: Grupo D: SEGUNDO PRINCIPIO: Grupo E: ESPONTANEIDAD DE LAS
Compuesto Kps Ca(OH) CaCO CaF
 XXXI OLIMPIADA QUÍMICA ARAGÓN 2018 1.- Indique la serie en la que los iones están dispuestos en orden creciente del radio iónico. a) Mg 2+ < K + < Ca 2+ < S 2 < Cl b) Mg 2+ < Ca 2+ < K + < Cl < S 2 c)
XXXI OLIMPIADA QUÍMICA ARAGÓN 2018 1.- Indique la serie en la que los iones están dispuestos en orden creciente del radio iónico. a) Mg 2+ < K + < Ca 2+ < S 2 < Cl b) Mg 2+ < Ca 2+ < K + < Cl < S 2 c)
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA. 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué?
 REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
Hoja Junio-13 PAU Alicante Química 2º BAT FerMates
 Hoja Junio-13 PAU Alicante Química 2º BAT FerMates Soluciones (versión β) http://www.fermates.com/seccion-10/quimica.htm Op A c1.- Considere los elementos X e Y cuyos números atómicos son 8 y 17, respectivamente,
Hoja Junio-13 PAU Alicante Química 2º BAT FerMates Soluciones (versión β) http://www.fermates.com/seccion-10/quimica.htm Op A c1.- Considere los elementos X e Y cuyos números atómicos son 8 y 17, respectivamente,
Nombre Grupo. Unidad 6 Ácido-base
 Nombre Grupo OPCIÓN A Unidad 6 Ácido-base 1. (2 p) a) Calcule el ph de una disolución 0.1 M de hidróxido potásico. El hidróxido potásico, como base fuerte que es, está completamente disociada en disolución
Nombre Grupo OPCIÓN A Unidad 6 Ácido-base 1. (2 p) a) Calcule el ph de una disolución 0.1 M de hidróxido potásico. El hidróxido potásico, como base fuerte que es, está completamente disociada en disolución
LABORATORIO # 5 TITULO : ANALISIS CUALITATIVO DE CATIONES Y ANIONES.
 LABORATORIO # 5 TITULO : ANALISIS CUALITATIVO DE CATIONES Y ANIONES. OBJETIVO: Mostrar al estudiante como los iones metálicos y algunos aniones pueden separarse e identificarse, en base a reacciones químicas
LABORATORIO # 5 TITULO : ANALISIS CUALITATIVO DE CATIONES Y ANIONES. OBJETIVO: Mostrar al estudiante como los iones metálicos y algunos aniones pueden separarse e identificarse, en base a reacciones químicas
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER
 LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
QUÍMICA. En el transcurso de la reacción se rompen y se forman enlaces, y
 OPCIÓN A QUÍMICA. 1. (2,5 puntos) A partir de los siguientes datos: Molécula Enlaces ΔH enlace (kj mol -1 ) H 2 H H - 436 O 2 O O - 496 H 2 O O-H - 463 Estime la entalpía estándar de formación de la molécula
OPCIÓN A QUÍMICA. 1. (2,5 puntos) A partir de los siguientes datos: Molécula Enlaces ΔH enlace (kj mol -1 ) H 2 H H - 436 O 2 O O - 496 H 2 O O-H - 463 Estime la entalpía estándar de formación de la molécula
Práctica 13. Equilibrios de solubilidad
 Práctica 13. Equilibrios de solubilidad ELABORADO POR: LAURA GASQUE SILVA ENUNCIADO A RESPONDER AL FINAL DE LA PRÁCTICA En sales poco solubles cuando el valor de (K ps /pk ps ), se (incrementa/disminuye),
Práctica 13. Equilibrios de solubilidad ELABORADO POR: LAURA GASQUE SILVA ENUNCIADO A RESPONDER AL FINAL DE LA PRÁCTICA En sales poco solubles cuando el valor de (K ps /pk ps ), se (incrementa/disminuye),
QUÍMICA. ii. Justifique si la reacción del apartado i) será, o no será, espontánea. (1,0 punto)
 OPCIÓN A QUÍMICA. 1. (2,5 puntos) Las entalpías estándar de formación del NH 3 (g) y del H 2 O(l) son -46,11 y -285,8 kj mol -1, respectivamente. La variación de la entalpía estándar para la reacción:
OPCIÓN A QUÍMICA. 1. (2,5 puntos) Las entalpías estándar de formación del NH 3 (g) y del H 2 O(l) son -46,11 y -285,8 kj mol -1, respectivamente. La variación de la entalpía estándar para la reacción:
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Curso 2012-2013 INSTRUCCIONES Y CRITERIOS GENERALES DE CALIFICACIÓN
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Curso 2012-2013 INSTRUCCIONES Y CRITERIOS GENERALES DE CALIFICACIÓN
EQUILIBRIO QUÍMICO. Concentraciones molares, presiones y constantes K c y K p.
 EQUILIBRIO QUÍMICO Concentraciones molares, presiones y constantes K c y K p. 1.- La formación del N 2 O 4 se explica mediante las dos reacciones siguientes: 2 NO (g) + O 2 (g) 2 NO 2 (g); 2 NO 2 (g) N
EQUILIBRIO QUÍMICO Concentraciones molares, presiones y constantes K c y K p. 1.- La formación del N 2 O 4 se explica mediante las dos reacciones siguientes: 2 NO (g) + O 2 (g) 2 NO 2 (g); 2 NO 2 (g) N
ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES
 VII 1 PRÁCTICA 7 ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES FORMACIÓN DE PRECIPITADOS Y DISOLUCIÓN DE LOS MISMOS POR FORMACIÓN DE COMPLEJOS FUNDAMENTO DE LA PRÁCTICA En esta práctica llevaremos a cabo
VII 1 PRÁCTICA 7 ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES FORMACIÓN DE PRECIPITADOS Y DISOLUCIÓN DE LOS MISMOS POR FORMACIÓN DE COMPLEJOS FUNDAMENTO DE LA PRÁCTICA En esta práctica llevaremos a cabo
INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN
 INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN Lo básico que debes saber de Química General 14-1 LA SOLUBILIDAD DE ELECTROLITOS FUERTES POCO SOLUBLES Compuesto Solubilidad Electrolito NaCl BaSO
INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN Lo básico que debes saber de Química General 14-1 LA SOLUBILIDAD DE ELECTROLITOS FUERTES POCO SOLUBLES Compuesto Solubilidad Electrolito NaCl BaSO
TEMA VII: SOLUBILIDAD
 TEA VII: SOLUBILIDAD 1.- Defina el concepto de solubilidad. Exprese la relación existente entre la solubilidad y el producto de la solubilidad para una sal A m B n. Se define Solubilidad, (S), a la cantidad
TEA VII: SOLUBILIDAD 1.- Defina el concepto de solubilidad. Exprese la relación existente entre la solubilidad y el producto de la solubilidad para una sal A m B n. Se define Solubilidad, (S), a la cantidad
INTRUCCIONES PARA LA RECUPERACIÓN
 INTRUCCIONES PARA LA RECUPERACIÓN Se entrega una relación de actividades. Dichas actividades deberán ser entregadas antes de la fecha límite de entrega, pudiéndose ser consultado el profesor cuantas veces
INTRUCCIONES PARA LA RECUPERACIÓN Se entrega una relación de actividades. Dichas actividades deberán ser entregadas antes de la fecha límite de entrega, pudiéndose ser consultado el profesor cuantas veces
PROBLEMAS TIPO DE CINÉTICA Y EQUILIBRIO
 PROBLEMAS TIPO DE CINÉTICA Y EQUILIBRIO De equilibrio con todas las cantidades iniciales 1) En un recipiente de un litro de capacidad, en el que previamente se ha hecho el vacío, se introducen 0,1 moles
PROBLEMAS TIPO DE CINÉTICA Y EQUILIBRIO De equilibrio con todas las cantidades iniciales 1) En un recipiente de un litro de capacidad, en el que previamente se ha hecho el vacío, se introducen 0,1 moles
