Acreditación de las unidades de fase I en Catalunya
|
|
|
- Mariano Belmonte de la Cruz
- hace 5 años
- Vistas:
Transcripción
1 Acreditación de las unidades de fase I en Catalunya II Jornada sobre ensayos clínicos de fase I en España Barcelona, 14 de junio de 2017 Teresa Martí Guixà Jefe de la Sección de Control de la Investigación y la Farmacovigilancia Servicio de Control Farmacéutico y Productos Sanitarios Subdirección General de Ordenación y Calidad Sanitarias y Farmacéuticas Dirección General de Ordenación Profesional y Regulación Sanitaria
2 Antecedentes Octubre Publicación en Requisitos técnico-sanitarios de las unidades donde se llevan a cabo ensayos clínicos con medicamentos sin finalidad terapéutica para los sujetos que participan en ellos Basado en Facilities for non-patient volunteer studies (ABPI 1988) Enero 2007: Puesta en marcha: Registro de voluntarios de ensayos clínicos (RVAC) De octubre 2006 a enero 2007: Inspección y acreditación unidades de fase I Publicación de guías: ABPI, EMA y MHRA 2
3 Objetivos Ampliación a ensayos clínicos: Primera administración en humanos Personas enfermas Beneficio terapéutico esperable Garantizar: Protección de las personas (voluntarios sanos y/o enfermos): salud derechos y bienestar La calidad científica y técnica de los ensayos clínicos Potenciar la investigación clínica en Catalunya 3
4 Publicación Abril Professionals Recerca 4
5 Contenido Evaluación y gestión de riesgos Personal Instalaciones Procedimientos normalizados de trabajo Equipamiento Gestión de participantes Gestión de datos Programa de garantía de calidad 5
6 Evaluación y gestión de riesgos Evaluación continua del balance beneficio-riesgo del medicamento en investigación: Responsabilidad compartida: promotor investigador Documentación: Identificación riesgos información disponible Evaluación riesgos revisión y aprobación formal Medidas de minimización de riesgos: personal, equipamiento, procedimientos, Archivo y distribución Revisión periódica y si cambios en protocolo o unidad Comunicación con promotor: mecanismo y frecuencia 6
7 Personal Personal técnico: médico y de enfermería: Dirección unidad = médico Dirección estudios clínicos: médico especialista en farmacología clínica otros profesionales con 2 años de experiencia en el área o tipo de estudios Si EC riesgo elevado Responsable de archivo Responsable de garantía de calidad independiente EC Propio o ajeno Documentación y registros: CV, DPT y formación presencia permanente de un médico 7
8 Instalaciones (1) Puertas y pasillos deben permitir el paso de una camilla Acceso fácil y rápido a un servicio de urgencias: centro hospitalario: directamente centro extrahospitalario: mediante ambulancia medicalizada acuerdo para la atención de urgencias: Soporte vital en la unidad y durante el traslado Deben garantizar: confortabilidad confidencialidad e intimidad acceso restringido al personal autorizado supervisión por personal técnico durante el ingreso 8
9 Instalaciones (2) Zona de tratamiento y seguimiento si EC con ingreso camas con sistemas de alarma y seguridad servicios sanitarios y duchas con cierres que permitan acceder en caso de emergencia Zona de descanso Zona de conservación de medicamentos Zona de procesamiento de especímenes Funcionamiento según BPL si bioanálisis Zona administrativa: archivo Zona de gestión de residuos y lavado de materiales 9
10 Procedimientos normalizados de trabajo (PNT) Aprobados por la dirección de la unidad Revisión y actualización: como mínimo cada 3 años archivo histórico El personal debe conocer y seguir los procedimientos registros de lectura Disponibles en el lugar de aplicación de las actividades Técnicamente válidos Listado de PNT Si protocolo PNT prevalece el protocolo 10
11 Actividades y registros de: calibración y/o verificación mantenimiento Equipamiento Sistema de alarma en aseos, duchas, salas y zona descanso: control periódico funcionamiento Sistema de llamada de emergencia. Teléfono + línea telefónica Sistema de suministro eléctrico alternativo Camas o sillones reclinables Neveras y congeladores + termómetros si análisis especímenes Mínimo en cada planta 11
12 Gestión de participantes Evitar la participación en varios ensayos clínicos (RVAC): simultánea secuencial: sin respectar periodo blanqueo Sistema de identificación de voluntarios Criterios de inclusión y exclusión: anamnesis e historia clínica contacto con médico responsable si procede Sistema de localización y contacto: unidad unidad participantes médico AP o especialista 12
13 Gestión de participantes - RVAC Registro de voluntarios de ensayos clínicos (RVAC) Vinculado al registro central de asegurados del CatSalut Voluntarios sanos Datos de participación de cada voluntario: fecha última administración fecha final período blanqueo unidad Datos a 18/10/2016: 1677 registros (60 % y 40 % ) 3 unidades de fase I con pacientes: CIM San Pablo (77.9 %), IMIM Mar (17,8 %) y UPIC Germans Trias (4,3 %) 129 voluntarios en período de blanqueo: (117 CIM San Pablo y 12 IMIM-Hospital del Mar) 13
14 Gestión de datos Obtención y conservación de datos personales conforme a las BPC y la Ley 15/1999 (LOPD): datos especialmente protegidos inscripción del fichero de investigación en la Agencia de Protección de Datos Sistemas informatizados validados Archivo en papel o electrónico: de cada ensayo clínico 25 años post final ensayo de la unidad: personal, PNT, garantía de calidad, mientras la unidad exista 14
15 Programa de garantía de calidad Personal de garantía de calidad: Independiente Formación en BPC y procedimientos de la unidad Propio o externo Tener copia de PNT y acceso a protocolos de estudios Programa de garantía de calidad: PNT aprobados por dirección Auditorías periódicas: frecuencia y contenido mínimo 1 / año auditorías visitas monitorización Registros e informes: a dirección (fecha envío y recepción) respuesta y seguimiento medidas correctoras 15
16 Cifras y calendario de actividades 8 unidades de fase I: voluntarios sanos, enfermos y mixtas vinculadas a centros hospitalarios Inspección y certificación: voluntaria desde junio 2016: 3 inspecciones realizadas 5 inspecciones pendientes 16
17 Unidades de fase I en Catalunya (1) Unidad de fase I. Centro de Investigación de Medicamentos (CIM). Instituto de Investigación. Hospital de la Santa Cruz y San Pablo. Barcelona Unidad de Investigación Clínica. Instituto Hospital del Mar de Investigaciones Médicas IMIM. Barcelona Unidad Polivalente de Investigación Clínica (UPIC). Servicio de Farmacología Clínica. Hospital Universitario Germans Trias i Pujol. Badalona Unidad de ensayos clínicos. IDIBELL Hospital Universitario de Bellvitge. L Hospitalet de Llobregat 17
18 Unidades de fase I en Catalunya (1) Unidad de Investigación de Terapia Molecular de Cáncer (UITM). VHIO. Hospital Universitario Valle de Hebrón. Barcelona Inther Unit. Instituto de Enfermedades Oncológicas y Hematológicas. Hospital Clínico de Barcelona. Barcelona Unidad de investigación clínica. Hospital San Juan de Dios. Esplugues de Llobregat Programa de desarrollo de ensayos clínicos en fases iniciales en cáncer y medicina adaptada Instituto Catalán de Oncología. L Hospitalet de Llobregat 18
19 Muchas gracias!! Servicio de Control Farmacéutico y Productos Sanitarios Dirección General de Ordenación Profesional y Regulación Sanitaria Departamento de Salud Travessera de les Corts, (Pavelló Ave Maria) controlfarmaceutic.salut@gencat.cat Tel Fax Teresa Martí Guixà Tel/Fax: t.marti@gencat.cat
Requisitos técnico-sanitarios de las unidades donde se llevan a cabo ensayos clínicos en fase temprana con medicamentos en la Comunidad de Madrid
 Requisitos técnico-sanitarios de las unidades donde se llevan a cabo ensayos clínicos en fase temprana con medicamentos en la Comunidad de Madrid Este documento especifica los requisitos técnico-sanitarios
Requisitos técnico-sanitarios de las unidades donde se llevan a cabo ensayos clínicos en fase temprana con medicamentos en la Comunidad de Madrid Este documento especifica los requisitos técnico-sanitarios
Guía de Unidades de Investigación Clínica de Fase I en España
 PROYECTO Investigación Clínica en Medicamentos Guía de Unidades de Investigación Clínica de Fase I en España Joan Costa H. Germans Trias i Pujol III Conferencia Anual de las Plataformas Tecnológicas de
PROYECTO Investigación Clínica en Medicamentos Guía de Unidades de Investigación Clínica de Fase I en España Joan Costa H. Germans Trias i Pujol III Conferencia Anual de las Plataformas Tecnológicas de
UNIDAD DE INVESTIGACIÓN CLÍNICA
 UNIDAD DE INVESTIGACIÓN CLÍNICA UBICACIÓN 2 espacios ubicados dentro del complejo hospitalario Reina Sofía: - Unidad del Hospital Provincial (377.5m²) - Unidad de Investigación Clínica, dos plantas, anexo
UNIDAD DE INVESTIGACIÓN CLÍNICA UBICACIÓN 2 espacios ubicados dentro del complejo hospitalario Reina Sofía: - Unidad del Hospital Provincial (377.5m²) - Unidad de Investigación Clínica, dos plantas, anexo
Ensayo Clínico. Otros puntos de vista PROMOTOR
 Ensayo Clínico. Otros puntos de vista PROMOTOR Gema Sanz Directora Operaciones Clínicas Fases en la ejecución de un Ensayo Clínico. FASE INICIAL: hasta presentación a evaluación Estudiar la viabilidad
Ensayo Clínico. Otros puntos de vista PROMOTOR Gema Sanz Directora Operaciones Clínicas Fases en la ejecución de un Ensayo Clínico. FASE INICIAL: hasta presentación a evaluación Estudiar la viabilidad
Guía de Unidades de Investigación Clínica de Fase I en España
 PROYECTO Investigación Clínica en Medicamentos Guía de Unidades de Investigación Clínica de Fase I en España Cándido Hernández Introducción a la Guía La Guía de Unidades de Investigación Clínica de Fase
PROYECTO Investigación Clínica en Medicamentos Guía de Unidades de Investigación Clínica de Fase I en España Cándido Hernández Introducción a la Guía La Guía de Unidades de Investigación Clínica de Fase
Curso especialista en Coordinación de Investigación Clinica en ensayos clinicos (CIC - Study Coordinator)
 Curso especialista en Coordinación de Investigación Clinica en ensayos clinicos (CIC - Study Coordinator) CURSO 2016 CURSO ESPECIALISTA EN COORDINACIÓN DE INVESTIGACIÓN CLÍNICA EN ENSAYOS CLÍNICOS (CIC-STUDY
Curso especialista en Coordinación de Investigación Clinica en ensayos clinicos (CIC - Study Coordinator) CURSO 2016 CURSO ESPECIALISTA EN COORDINACIÓN DE INVESTIGACIÓN CLÍNICA EN ENSAYOS CLÍNICOS (CIC-STUDY
Normas de Buena Práctica Clínica El papel de la autoridad sanitaria. Consecuencias del incumplimiento para promotores e investigadores
 Normas de Buena Práctica Clínica El papel de la autoridad sanitaria. Consecuencias del incumplimiento para promotores e investigadores Carmen Aguado D. G. Ordenación e Inspección Consejería de Sanidad
Normas de Buena Práctica Clínica El papel de la autoridad sanitaria. Consecuencias del incumplimiento para promotores e investigadores Carmen Aguado D. G. Ordenación e Inspección Consejería de Sanidad
INDUSTRIA FARMACEUTICA. Emili Esteve Sala Director del Departamento Técnico
 BUENA PRACTICA CLINICA. PERSPECTIVA DESDE LA INDUSTRIA FARMACEUTICA Emili Esteve Sala Director del Departamento Técnico 1 EL CICLO DE LOS MEDICAMENTOS La investigación es esencial para la industria farmacéutica,
BUENA PRACTICA CLINICA. PERSPECTIVA DESDE LA INDUSTRIA FARMACEUTICA Emili Esteve Sala Director del Departamento Técnico 1 EL CICLO DE LOS MEDICAMENTOS La investigación es esencial para la industria farmacéutica,
Tiempos y exigencias del ensayo. Problemática para cumplirlos. Visión del monitor. Beatriz Pardo (Geicam)
 Tiempos y exigencias del ensayo. Problemática para cumplirlos. Visión del monitor Beatriz Pardo (Geicam) Gran reto. Desarrollo de los medicamentos del futuro Cada 20 minutos se diagnostica una mujer de
Tiempos y exigencias del ensayo. Problemática para cumplirlos. Visión del monitor Beatriz Pardo (Geicam) Gran reto. Desarrollo de los medicamentos del futuro Cada 20 minutos se diagnostica una mujer de
Criterios para el Buen Funcionamiento de. Investigación Clínica en México Abril 2018
 Criterios para el Buen Funcionamiento de Establecimientos donde se realiza Investigación Clínica en México Abril 2018 Siguiente Paso del Primer Registro Nacional de Investigadores y Establecimientos donde
Criterios para el Buen Funcionamiento de Establecimientos donde se realiza Investigación Clínica en México Abril 2018 Siguiente Paso del Primer Registro Nacional de Investigadores y Establecimientos donde
Versión 00 Fecha: 12 de Enero de 2011 Página 1 de 6
 PROCESO DE GESTIÓN DE CONTRATOS DE ENSAYOS CLÍNICOS Y ESTUDIOS POSAUTORIZACIÓN DEL HOSPITAL UNIVERSITARI VALL D HEBRON (HUVH) Y EL VALL D HEBRON INSTITUT DE RECERCA (VHIR) Los ensayos clínicos y estudios
PROCESO DE GESTIÓN DE CONTRATOS DE ENSAYOS CLÍNICOS Y ESTUDIOS POSAUTORIZACIÓN DEL HOSPITAL UNIVERSITARI VALL D HEBRON (HUVH) Y EL VALL D HEBRON INSTITUT DE RECERCA (VHIR) Los ensayos clínicos y estudios
PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA LA CONTRATACIÓN DE UN SERVICIO DE CONTRACT RESEARCH ORGANISATION (CRO) PARA ENSAYO CLÍNICO BIOMEDE (PNCP
 PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA LA CONTRATACIÓN DE UN SERVICIO DE CONTRACT RESEARCH ORGANISATION (CRO) PARA ENSAYO CLÍNICO BIOMEDE (PNCP 01/17) 1. OBJETO DEL CONTRATO El objeto del presente procedimiento
PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA LA CONTRATACIÓN DE UN SERVICIO DE CONTRACT RESEARCH ORGANISATION (CRO) PARA ENSAYO CLÍNICO BIOMEDE (PNCP 01/17) 1. OBJETO DEL CONTRATO El objeto del presente procedimiento
MEMORIA ANUAL DE ACTIVIDADES 2011 COMITÉ DE BIOÉTICA ASISTENCIAL DEPARTAMENTO DE SALUD DE SAGUNTO
 Comité de Bioética Asistencial MEMORIA ANUAL DE ACTIVIDADES 2011 COMITÉ DE BIOÉTICA ASISTENCIAL DEPARTAMENTO DE SALUD DE SAGUNTO Acreditado por el Consejo Asesor de Bioética de la Comunidad Valenciana
Comité de Bioética Asistencial MEMORIA ANUAL DE ACTIVIDADES 2011 COMITÉ DE BIOÉTICA ASISTENCIAL DEPARTAMENTO DE SALUD DE SAGUNTO Acreditado por el Consejo Asesor de Bioética de la Comunidad Valenciana
TEMARIO PARA MÉDICOS EN ADMISIÓN Y DOCUMENTACIÓN CLÍNICA
 TEMARIO PARA MÉDICOS EN ADMISIÓN Y DOCUMENTACIÓN CLÍNICA 1. Constitución Española de 1978. Principios Fundamentales. Derechos y deberes fundamentales de los Españoles. La protección de la Salud en la Constitución.
TEMARIO PARA MÉDICOS EN ADMISIÓN Y DOCUMENTACIÓN CLÍNICA 1. Constitución Española de 1978. Principios Fundamentales. Derechos y deberes fundamentales de los Españoles. La protección de la Salud en la Constitución.
Curso especialista en gestión administrativa de ensayos clinicos (Clinical Trial Assistant-CTA)
 i Curso especialista en gestión administrativa de ensayos clinicos (Clinical Trial Assistant-CTA) CURSO - 2013 1 CURSO ESPECIALISTA EN GESTIÓN ADMINISTRATIVA DE EN- SAYOS CLÍNICOS (CTA) PRESENTACIÓN Si
i Curso especialista en gestión administrativa de ensayos clinicos (Clinical Trial Assistant-CTA) CURSO - 2013 1 CURSO ESPECIALISTA EN GESTIÓN ADMINISTRATIVA DE EN- SAYOS CLÍNICOS (CTA) PRESENTACIÓN Si
La estrategia en I+D de la Industria Farmacéutica. Mercedes Francés Departamento Técnico Farmaindustria
 La estrategia en I+D de la Industria Farmacéutica Mercedes Francés Departamento Técnico Farmaindustria Agenda Posicionamiento de la Industria Farmacéutica en I+D Estrategias en I+D de la Industria Farmacéutica
La estrategia en I+D de la Industria Farmacéutica Mercedes Francés Departamento Técnico Farmaindustria Agenda Posicionamiento de la Industria Farmacéutica en I+D Estrategias en I+D de la Industria Farmacéutica
la situación de las Unidades de Ensayos Clínicos de los Servicios de hospitales españoles Grupo de Ensayos Clínicos de la SEFH
 Encuesta sobre la situación de las Unidades de Ensayos Clínicos de los Grupo de Ensayos Clínicos de la SEFH Servicios de Farmacia de los hospitales españoles María Tordera Servicio de Farmacia Hospital
Encuesta sobre la situación de las Unidades de Ensayos Clínicos de los Grupo de Ensayos Clínicos de la SEFH Servicios de Farmacia de los hospitales españoles María Tordera Servicio de Farmacia Hospital
CEDULA DE EVALUACIÓN DE FARMACIA HOSPITALARIA PERSPECTIVA DESDE UN HOSPITAL PUBLICO
 HOSPITAL INFANTIL DE MÉXICO FEDERICO GOMEZ INSTITUTO NACIONAL DE SALUD CEDULA DE EVALUACIÓN DE FARMACIA HOSPITALARIA PERSPECTIVA DESDE UN HOSPITAL PUBLICO Servicios Farmacéuticos Hospitalarios LF. ERIKA
HOSPITAL INFANTIL DE MÉXICO FEDERICO GOMEZ INSTITUTO NACIONAL DE SALUD CEDULA DE EVALUACIÓN DE FARMACIA HOSPITALARIA PERSPECTIVA DESDE UN HOSPITAL PUBLICO Servicios Farmacéuticos Hospitalarios LF. ERIKA
DESARROLLO CLÍNICO DE LOS MEDICAMENTOS
 V EDICIÓN LA BUENA PRÁCTICA CLÍNICA EN LOS ENSAYOS CLÍNICOS 7-8 de ABRIL de 2015 DESARROLLO CLÍNICO DE LOS MEDICAMENTOS Dra. Dolores Ochoa Mazarro Servicio de Farmacología Clínica Hospital Universitario
V EDICIÓN LA BUENA PRÁCTICA CLÍNICA EN LOS ENSAYOS CLÍNICOS 7-8 de ABRIL de 2015 DESARROLLO CLÍNICO DE LOS MEDICAMENTOS Dra. Dolores Ochoa Mazarro Servicio de Farmacología Clínica Hospital Universitario
MANEJO DE LA MEDICACIÓN DEL ENSAYO CLÍNICO PAPEL DE LA FARMACIA HOSPITALARIA
 MANEJO DE LA MEDICACIÓN DEL ENSAYO CLÍNICO PAPEL DE LA FARMACIA HOSPITALARIA CALIDAD DEL ENSAYO CLINICO CALIDAD DEL PROTOCOLO DISEÑO METODOLOGIA DE TRABAJO CALIDAD DE LOS INVESTIGADORES control pacientes
MANEJO DE LA MEDICACIÓN DEL ENSAYO CLÍNICO PAPEL DE LA FARMACIA HOSPITALARIA CALIDAD DEL ENSAYO CLINICO CALIDAD DEL PROTOCOLO DISEÑO METODOLOGIA DE TRABAJO CALIDAD DE LOS INVESTIGADORES control pacientes
Póliza de Salud MAPFRE. Condiciones 2018
 Póliza de Salud MAPFRE Condiciones 2018 LA PRIMERA PÓLIZA MÉDICA PARA EL MUNDO DEL TENIS MAPFRE crea la primera póliza médica para tenistas, adaptada a sus necesidades. En colaboración con el Dr. Ángel
Póliza de Salud MAPFRE Condiciones 2018 LA PRIMERA PÓLIZA MÉDICA PARA EL MUNDO DEL TENIS MAPFRE crea la primera póliza médica para tenistas, adaptada a sus necesidades. En colaboración con el Dr. Ángel
MODELOS ORGANIZATIVOS EN LA INVESTIGACIÓN CLÍNICA EN TERAPIAS AVANZADAS Y SITUACIÓN EN ANDALUCÍA
 MODELOS ORGANIZATIVOS EN LA INVESTIGACIÓN CLÍNICA EN TERAPIAS AVANZADAS Y SITUACIÓN EN ANDALUCÍA Natividad Cuende MD, MPH, PhD Directora de la Iniciativa Andaluza en Terapias Avanzadas Adjunta a la Coordinación
MODELOS ORGANIZATIVOS EN LA INVESTIGACIÓN CLÍNICA EN TERAPIAS AVANZADAS Y SITUACIÓN EN ANDALUCÍA Natividad Cuende MD, MPH, PhD Directora de la Iniciativa Andaluza en Terapias Avanzadas Adjunta a la Coordinación
GRUPO DE EECC DE LA SEFH
 GESTIÓN DE LA INVESTIGACIÓN CLÍNICA EN ONCOLOGÍA GRUPO DE EECC DE LA SEFH Cristina González Pérez HM Hospitales 23 de noviembre de 2016 DISTRIBUCIÓN EECC EN GRUPO HM En junio acabo Farmacia y luego
GESTIÓN DE LA INVESTIGACIÓN CLÍNICA EN ONCOLOGÍA GRUPO DE EECC DE LA SEFH Cristina González Pérez HM Hospitales 23 de noviembre de 2016 DISTRIBUCIÓN EECC EN GRUPO HM En junio acabo Farmacia y luego
Tema 8. SERVICIOS DE FARMACIA DE HOSPITALES. LEGISLACIÓN EN ESTRUCTURAS DE FARMACIA DE ATENCIÓN PRIMARIA. Legislación y deontología farmacéutica
 Tema 8. SERVICIOS DE FARMACIA DE HOSPITALES. LEGISLACIÓN EN ESTRUCTURAS DE FARMACIA DE ATENCIÓN PRIMARIA Legislación y deontología farmacéutica 1 SERVICIOS DE FARMACIA DE HOSPITALES. 2 1. LEGISLACIÓN ESTATAL
Tema 8. SERVICIOS DE FARMACIA DE HOSPITALES. LEGISLACIÓN EN ESTRUCTURAS DE FARMACIA DE ATENCIÓN PRIMARIA Legislación y deontología farmacéutica 1 SERVICIOS DE FARMACIA DE HOSPITALES. 2 1. LEGISLACIÓN ESTATAL
COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS COMISIÓN DE AUTORIZACIÓN SANITARIA LA REGULACIÓN DE LOS ENSAYOS CLÍNICOS EN MÉXICO
 COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS COMISIÓN DE AUTORIZACIÓN SANITARIA LA REGULACIÓN DE LOS ENSAYOS CLÍNICOS EN MÉXICO DRA. ELIZABETH ROJAS SERAFIN ENSAYOS CLÍNICOS 1 CONTENIDO
COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS COMISIÓN DE AUTORIZACIÓN SANITARIA LA REGULACIÓN DE LOS ENSAYOS CLÍNICOS EN MÉXICO DRA. ELIZABETH ROJAS SERAFIN ENSAYOS CLÍNICOS 1 CONTENIDO
DE PROTECCIÓN DE DATOS PERSONALES EN EL ÁMBITO DE LA INVESTIGACIÓN CLÍNICA Y DE LA FARMACOVIGILANCIA
 CÓDIGO TIPO DE INVESTIGACIÓN CLÍNICA Y FARMACOVIGILANCIA CÓDIGO ASPECTOS TIPO DE GENERALES FARMAINDUSTRIA DE PROTECCIÓN DE DATOS PERSONALES EN EL ÁMBITO DE LA INVESTIGACIÓN CLÍNICA Y DE LA FARMACOVIGILANCIA
CÓDIGO TIPO DE INVESTIGACIÓN CLÍNICA Y FARMACOVIGILANCIA CÓDIGO ASPECTOS TIPO DE GENERALES FARMAINDUSTRIA DE PROTECCIÓN DE DATOS PERSONALES EN EL ÁMBITO DE LA INVESTIGACIÓN CLÍNICA Y DE LA FARMACOVIGILANCIA
TRANSPORTE ESPECIAL DE PACIENTES
 TRANSPORTE ESPECIAL DE PACIENTES NORMATIVIDAD Resolución 1043 de 2006. Resolución 1441 de 2013. ICONTEC NORMA TECNICA DE CALIDAD 3729 DE 2007. Establece estándares para la habilitación. ANEXO TECNICO.
TRANSPORTE ESPECIAL DE PACIENTES NORMATIVIDAD Resolución 1043 de 2006. Resolución 1441 de 2013. ICONTEC NORMA TECNICA DE CALIDAD 3729 DE 2007. Establece estándares para la habilitación. ANEXO TECNICO.
REQUISITOS DEL CEIC-E PARA LA AUTORIZACIÓN DE ENSAYOS CLÍNICOS
 REQUISITOS DEL CEIC-E PARA LA AUTORIZACIÓN DE ENSAYOS CLÍNICOS NO EXISTEN PLAZOS DE ENVÍO PARA PARA LOS ENSAYOS CLÍNICOS CON MEDICAMENTOS Y PRODUCTOS SANITARIOS Evaluación por el CEIC E cuando actúa como
REQUISITOS DEL CEIC-E PARA LA AUTORIZACIÓN DE ENSAYOS CLÍNICOS NO EXISTEN PLAZOS DE ENVÍO PARA PARA LOS ENSAYOS CLÍNICOS CON MEDICAMENTOS Y PRODUCTOS SANITARIOS Evaluación por el CEIC E cuando actúa como
Decreto 195/2015, de 4 de Agosto, del Consejo de Gobierno, por el que se establece la estructura orgánica de la Consejería de Sanidad.
 Decreto 195/2015, de 4 de Agosto, del Consejo de Gobierno, por el que se establece la estructura orgánica de la Consejería de Sanidad. Artículo 1: competencias del consejero de sanidad. Coordinacioń y
Decreto 195/2015, de 4 de Agosto, del Consejo de Gobierno, por el que se establece la estructura orgánica de la Consejería de Sanidad. Artículo 1: competencias del consejero de sanidad. Coordinacioń y
IV EDICION LA BUENA PRACTICA CLINICA EN LOS ENSAYOS CLÍNICOS MONITORIZACIÓN DE LOS ENSAYOS CLÍNICOS
 IV EDICION LA BUENA PRACTICA CLINICA EN LOS ENSAYOS CLÍNICOS MONITORIZACIÓN DE LOS ENSAYOS CLÍNICOS 8-4-2015 Juan Diego López de la Reina Maroto ÍNDICE 1. El Monitor de los ensayos clínicos 2. Selección
IV EDICION LA BUENA PRACTICA CLINICA EN LOS ENSAYOS CLÍNICOS MONITORIZACIÓN DE LOS ENSAYOS CLÍNICOS 8-4-2015 Juan Diego López de la Reina Maroto ÍNDICE 1. El Monitor de los ensayos clínicos 2. Selección
Programa de Bancos de Tumores
 Programa de Bancos de Tumores RTICCC Madrid 31.03.2004 Coordinadores: Enrique de Álava Pedro L Fernández Manuel M Morente OBJETIVOS Promoción de Bancos de Tumores en los hospitales de la Red. Estandarización
Programa de Bancos de Tumores RTICCC Madrid 31.03.2004 Coordinadores: Enrique de Álava Pedro L Fernández Manuel M Morente OBJETIVOS Promoción de Bancos de Tumores en los hospitales de la Red. Estandarización
Actividades del Grupo TECNO. Proyectos Futuros.
 Actividades del Grupo TECNO. Proyectos Futuros. Dra. Ana Alvarez ( H. Ramón y Cajal, Madrid) Dr. Carlos Codina ( H. Clinic, Barcelona) Dra. Amelia de la Rubia (H. Virgen de la Arreixaca) Dra. Ana Herranz
Actividades del Grupo TECNO. Proyectos Futuros. Dra. Ana Alvarez ( H. Ramón y Cajal, Madrid) Dr. Carlos Codina ( H. Clinic, Barcelona) Dra. Amelia de la Rubia (H. Virgen de la Arreixaca) Dra. Ana Herranz
AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE MEDICINA NUCLEAR
 AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE MEDICINA NUCLEAR - REQUISITOS MÍNIMOS PARA LA ACREDITACIÓN DE LA COMISIÓN NACIONAL DE LA ESPECIALIDAD - HOSPITAL COMUNIDAD : FECHA: DATOS GENERALES Nombre actualizado
AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE MEDICINA NUCLEAR - REQUISITOS MÍNIMOS PARA LA ACREDITACIÓN DE LA COMISIÓN NACIONAL DE LA ESPECIALIDAD - HOSPITAL COMUNIDAD : FECHA: DATOS GENERALES Nombre actualizado
III CURSO PARA INVESTIGADORES SOBRE NORMAS DE BPC PROCEDIMIENTO DE AUTORIZACIÓN DE UN ENSAYO CLÍNICO
 III CURSO PARA INVESTIGADORES SOBRE NORMAS DE BPC PROCEDIMIENTO DE AUTORIZACIÓN DE UN ENSAYO CLÍNICO Antes de realizar un EC con medicamentos se debe contar con: Dictamen favorable del CEIC Conformidad
III CURSO PARA INVESTIGADORES SOBRE NORMAS DE BPC PROCEDIMIENTO DE AUTORIZACIÓN DE UN ENSAYO CLÍNICO Antes de realizar un EC con medicamentos se debe contar con: Dictamen favorable del CEIC Conformidad
Auditorías internas de calidad: de la teoría a la práctica
 Auditorías internas de calidad: de la teoría a la práctica María-José Jiménez ICO-Hospital Germans Trias i Pujol Barcelona, 20 de mayo de 2015 Servicio Hematología Introducción: Activo desde apertura hospital
Auditorías internas de calidad: de la teoría a la práctica María-José Jiménez ICO-Hospital Germans Trias i Pujol Barcelona, 20 de mayo de 2015 Servicio Hematología Introducción: Activo desde apertura hospital
1.- RESUMEN COMPOSICIÓN Y ESTRUCTURACIÓN. Presidente. Dr. A. Moreno González Servicio de Farmacología Clínica. Vicepresidente
 1.- RESUMEN COMPOSICIÓN Y ESTRUCTURACIÓN Presidente Dr. A. Moreno González Servicio de Farmacología Clínica Vicepresidente Dr. J. M. Ladero Quesada Servicio de Aparato Digestivo Secretaria Dra. M. García
1.- RESUMEN COMPOSICIÓN Y ESTRUCTURACIÓN Presidente Dr. A. Moreno González Servicio de Farmacología Clínica Vicepresidente Dr. J. M. Ladero Quesada Servicio de Aparato Digestivo Secretaria Dra. M. García
SEGUIMIENTO DE LOSENSAYOS CLÍNICOS ALBA SERRANO RUIZ RESPONSABLE DPTO. EECC FIB. HOSPITAL U. DE LA PRINCESA
 SEGUIMIENTO DE LOSENSAYOS CLÍNICOS ALBA SERRANO RUIZ RESPONSABLE DPTO. EECC FIB. HOSPITAL U. DE LA PRINCESA 88888888 Aprobación CEIC/CEIC de Referencia Inicio EECC Autorización de la AEMPS Conformidad
SEGUIMIENTO DE LOSENSAYOS CLÍNICOS ALBA SERRANO RUIZ RESPONSABLE DPTO. EECC FIB. HOSPITAL U. DE LA PRINCESA 88888888 Aprobación CEIC/CEIC de Referencia Inicio EECC Autorización de la AEMPS Conformidad
Sección Ensayos Clínicos Agencia Nacional de Medicamentos Instituto de Salud Pública de Chile
 Regulación de Ensayos Clínicos en Chile Sección Ensayos Clínicos Agencia Nacional de Medicamentos Instituto de Salud Pública de Chile 11/mayo/2012 Marco legal y normativa Constitución Política del Estado
Regulación de Ensayos Clínicos en Chile Sección Ensayos Clínicos Agencia Nacional de Medicamentos Instituto de Salud Pública de Chile 11/mayo/2012 Marco legal y normativa Constitución Política del Estado
Protocolización de un ensayo clínico
 Protocolización de un ensayo clínico Ana Aldea Perona Servicio Canario de la Salud DIRECCIÓN GENERAL DE FARMACIA Objetivo de la sesión Conocer los mínimos requeridos por la norma, en relación a un protocolo
Protocolización de un ensayo clínico Ana Aldea Perona Servicio Canario de la Salud DIRECCIÓN GENERAL DE FARMACIA Objetivo de la sesión Conocer los mínimos requeridos por la norma, en relación a un protocolo
Normas de buena práctica clínica (BPC)
 Normas de buena práctica clínica (BPC) 17.Sep - 31.Oct Cód. @19-18 Edición 2018 Tipo de actividad Cursos Online Fecha 17.Sep - 31.Oct Idiomas Español- castellano Validez académica 30 horas DIRECCIÓN Iciar
Normas de buena práctica clínica (BPC) 17.Sep - 31.Oct Cód. @19-18 Edición 2018 Tipo de actividad Cursos Online Fecha 17.Sep - 31.Oct Idiomas Español- castellano Validez académica 30 horas DIRECCIÓN Iciar
COMITÉS DE ÉTICA DE LA INVESTIGACIÓN (CEI): IMPLICACIONES ÉTICAS DEL SEGUIMIENTO DE LOS ESTUDIOS
 COMITÉS DE ÉTICA DE LA INVESTIGACIÓN (CEI): IMPLICACIONES ÉTICAS DEL SEGUIMIENTO DE LOS ESTUDIOS Iciar Alfonso Farnós Arantza Hernández, Carlos Romeo Casabona, Paloma Acevedo CEIC de Euskadi Qué es el
COMITÉS DE ÉTICA DE LA INVESTIGACIÓN (CEI): IMPLICACIONES ÉTICAS DEL SEGUIMIENTO DE LOS ESTUDIOS Iciar Alfonso Farnós Arantza Hernández, Carlos Romeo Casabona, Paloma Acevedo CEIC de Euskadi Qué es el
Máster on-line de 'Monitorización de ensayos clínicos'. 3ª edición
 Máster on-line de 'Monitorización de ensayos clínicos'. 3ª edición CURSO 2015-2016 PREINSCRIPCIÓN 24/07/15 hasta el 30/09/15 MATRÍCULA 24/07/15 hasta el 30/09/15 IMPORTE MATRÍCULA 2900 EXPEDICIÓN DE TÍTULOS
Máster on-line de 'Monitorización de ensayos clínicos'. 3ª edición CURSO 2015-2016 PREINSCRIPCIÓN 24/07/15 hasta el 30/09/15 MATRÍCULA 24/07/15 hasta el 30/09/15 IMPORTE MATRÍCULA 2900 EXPEDICIÓN DE TÍTULOS
Preparación de una Auditoría en los Ensayos Clínicos. D. Manuel Román Martínez Servicio de Farmacología Clínica Hospital Universitario de la Princesa
 Preparación de una Auditoría en los Ensayos Clínicos. D. Manuel Román Martínez Servicio de Farmacología Clínica Hospital Universitario de la Princesa Índice Introducción Procedimiento de la Auditoría.
Preparación de una Auditoría en los Ensayos Clínicos. D. Manuel Román Martínez Servicio de Farmacología Clínica Hospital Universitario de la Princesa Índice Introducción Procedimiento de la Auditoría.
II CURSO TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS
 SOCIEDAD ESPAÑOLA DE DE HEMATOLOGÍA Y HEMOTERAPIA Sociedad Española de Transfusión y Terapia Celular II CURSO TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS Organizado por la Fundación Española de Hematología
SOCIEDAD ESPAÑOLA DE DE HEMATOLOGÍA Y HEMOTERAPIA Sociedad Española de Transfusión y Terapia Celular II CURSO TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS Organizado por la Fundación Española de Hematología
Hoja informativa nº 13: del 28 de agosto al 3 de setiembre
 POCS 217 Introducción En el año 24 el Departamento de Salud y el CatSalut pusieron en marcha por primera vez un plan de actuación para prevenir los efectos de las olas de calor sobre la salud (POCS) en
POCS 217 Introducción En el año 24 el Departamento de Salud y el CatSalut pusieron en marcha por primera vez un plan de actuación para prevenir los efectos de las olas de calor sobre la salud (POCS) en
Pontificia Universidad Católica del Ecuador
 CURSO DE ACTUALIZACIÓN PARA COMITÉS DE ÉTICA EN INVESTIGACIÓN CON SERES HUMANOS (CEISH) EN ECUADOR Fecha de inicio: 5 de octubre de 2015 Fecha de finalización: 20 de diciembre 2015 Duración: 90 horas en
CURSO DE ACTUALIZACIÓN PARA COMITÉS DE ÉTICA EN INVESTIGACIÓN CON SERES HUMANOS (CEISH) EN ECUADOR Fecha de inicio: 5 de octubre de 2015 Fecha de finalización: 20 de diciembre 2015 Duración: 90 horas en
La investigación clínica en fases tempranas en la nueva regulación de EC
 La investigación clínica en fases tempranas en la nueva regulación de EC César Hernández García Jefe Departamento Medicamentos de Uso Humano Agencia Española de Medicamentos y Productos Sanitarios. Autorización
La investigación clínica en fases tempranas en la nueva regulación de EC César Hernández García Jefe Departamento Medicamentos de Uso Humano Agencia Española de Medicamentos y Productos Sanitarios. Autorización
Epidermolisis bullosa
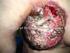
 Terapias Epidermolisis bullosa Terapias Enfermedad RARA. Grave Se caracteriza por una erupción de ampollas en la piel de forma espontánea o por traumatismos mínimos Cáncer mama metastáscio Terapias Luces
Terapias Epidermolisis bullosa Terapias Enfermedad RARA. Grave Se caracteriza por una erupción de ampollas en la piel de forma espontánea o por traumatismos mínimos Cáncer mama metastáscio Terapias Luces
EL NUEVO ROL DE LOS CEIm Cristina Avendaño Solá Presidente CEIC Puerta de Hierro
 EL NUEVO ROL DE LOS CEIm Cristina Avendaño Solá Presidente CEIC Puerta de Hierro 15 de marzo de 2016 (18) Corresponde a cada Estado miembro implicado determinar qué organismos deben participar en la evaluación
EL NUEVO ROL DE LOS CEIm Cristina Avendaño Solá Presidente CEIC Puerta de Hierro 15 de marzo de 2016 (18) Corresponde a cada Estado miembro implicado determinar qué organismos deben participar en la evaluación
Ministerio de la Protección Social. República de Colombia
 BENEFICIOS El paciente conserva su medio habitual (domicilio). Ofrece las mismas actividades que en el hospital pero en casa. Promueve la pronta recuperación en su entorno, disminuye el tiempo de hospitalización.
BENEFICIOS El paciente conserva su medio habitual (domicilio). Ofrece las mismas actividades que en el hospital pero en casa. Promueve la pronta recuperación en su entorno, disminuye el tiempo de hospitalización.
DE LA ESPECIALIDAD DE OBSTETRICIA Y GINECOLOGÍA
 AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE OBSTETRICIA Y GINECOLOGÍA HOSPITAL COMUNIDAD : FECHA: DATOS GENERALES Nombre actualizado del Hospital: Dependencia Patrimonial: Gestionado por: Institución que solicita
AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE OBSTETRICIA Y GINECOLOGÍA HOSPITAL COMUNIDAD : FECHA: DATOS GENERALES Nombre actualizado del Hospital: Dependencia Patrimonial: Gestionado por: Institución que solicita
Nueva Regulación de Ensayos clínicos en la UE y en ES Reglamento 536/2014 y Real Decreto 1090/2015
 Industria y Pacientes: Un encuentro necesario. Nueva Regulación de Ensayos clínicos en la UE y en ES Reglamento 536/2014 y Real Decreto 1090/2015 15 de marzo de 2016, Real Academia Nacional de Farmacia
Industria y Pacientes: Un encuentro necesario. Nueva Regulación de Ensayos clínicos en la UE y en ES Reglamento 536/2014 y Real Decreto 1090/2015 15 de marzo de 2016, Real Academia Nacional de Farmacia
Hallazgos Inspecciones Acreditación n de CEICs - Madrid
 Hallazgos Inspecciones Acreditación n de CEICs - Madrid CURSO de BPC Área de Control Farmacéutico y P. Sanitarios CONSEJERÍA DE SANIDAD- MADRID Marta Gallego Romero Valencia- 12 Junio 2015 Normativa Directiva
Hallazgos Inspecciones Acreditación n de CEICs - Madrid CURSO de BPC Área de Control Farmacéutico y P. Sanitarios CONSEJERÍA DE SANIDAD- MADRID Marta Gallego Romero Valencia- 12 Junio 2015 Normativa Directiva
INAN5006 Técnico de Calidad de la Industria Alimentaria
 INAN5006 Técnico de Calidad de la Industria Alimentaria Duración: 100 horas Modalidad: Online Coste Bonificable: 750 Objetivos del curso La calidad en la producción y transformación de los alimentos es
INAN5006 Técnico de Calidad de la Industria Alimentaria Duración: 100 horas Modalidad: Online Coste Bonificable: 750 Objetivos del curso La calidad en la producción y transformación de los alimentos es
Indicaciones para los investigadores del IDIBELL en relación a la firma de comunicaciones de investigación
 Indicaciones para los investigadores del IDIBELL en relación a la firma de comunicaciones de investigación Introducción El IDIBELL es un instituto de investigación promovido por cuatro socios científicos
Indicaciones para los investigadores del IDIBELL en relación a la firma de comunicaciones de investigación Introducción El IDIBELL es un instituto de investigación promovido por cuatro socios científicos
Tiempos de Acceso Regional de Productos Hospitalarios
 Tiempos de Acceso Regional de Productos Hospitalarios Míriam Solozabal 1, Sonia Fraile 2, Vanessa Gómez 1 1 RWI, QuintilesIMS; 2 Hospital Offering development, QuintilesIMS 7 de Septiembre del 2017 Copyright
Tiempos de Acceso Regional de Productos Hospitalarios Míriam Solozabal 1, Sonia Fraile 2, Vanessa Gómez 1 1 RWI, QuintilesIMS; 2 Hospital Offering development, QuintilesIMS 7 de Septiembre del 2017 Copyright
PNT - 1 PROCEDIMIENTO DE PREPARACIÓN, APROBACIÓN, DISTRIBUCIÓN Y REVISIÓN DE LOS PNTs DEL CEIm ÁREA DE SALUD VALLADOLID ESTE.
 PNT - 1 PROCEDIMIENTO DE PREPARACIÓN, APROBACIÓN, DISTRIBUCIÓN Y REVISIÓN DE LOS PNTs DEL CEIm ÁREA DE SALUD VALLADOLID ESTE. Versión: 4, de 22 de marzo de 2018 Abreviaturas: Comité de Ética de la Investigación
PNT - 1 PROCEDIMIENTO DE PREPARACIÓN, APROBACIÓN, DISTRIBUCIÓN Y REVISIÓN DE LOS PNTs DEL CEIm ÁREA DE SALUD VALLADOLID ESTE. Versión: 4, de 22 de marzo de 2018 Abreviaturas: Comité de Ética de la Investigación
DOCUMENTO DE POSICIONAMIENTO DE LA SOCIEDAD ESPAÑOLA DE FARMACIA HOSPITALARIA SOBRE LOS MEDICAMENTOS BIOSIMILARES
 DOCUMENTO DE POSICIONAMIENTO DE LA SOCIEDAD ESPAÑOLA DE FARMACIA HOSPITALARIA SOBRE LOS MEDICAMENTOS BIOSIMILARES Se define un medicamento biosimilar como aquel que contiene una versión de una sustancia
DOCUMENTO DE POSICIONAMIENTO DE LA SOCIEDAD ESPAÑOLA DE FARMACIA HOSPITALARIA SOBRE LOS MEDICAMENTOS BIOSIMILARES Se define un medicamento biosimilar como aquel que contiene una versión de una sustancia
AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE FARMACOLOGÍA CLÍNICA - REQUISITOS MÍNIMOS PARA LA ACREDITACIÓN DE LA COMISIÓN NACIONAL DE LA ESPECIALIDAD -
 AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE FARMACOLOGÍA CLÍNICA - REQUISITOS MÍNIMOS PARA LA ACREDITACIÓN DE LA COMISIÓN NACIONAL DE LA ESPECIALIDAD - HOSPITAL COMUNIDAD : FECHA: DATOS GENERALES Nombre actualizado
AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE FARMACOLOGÍA CLÍNICA - REQUISITOS MÍNIMOS PARA LA ACREDITACIÓN DE LA COMISIÓN NACIONAL DE LA ESPECIALIDAD - HOSPITAL COMUNIDAD : FECHA: DATOS GENERALES Nombre actualizado
Mitos y realidades de la Investigación Clínica. Rol del Farmacéutico.
 Mitos y realidades de la Investigación Clínica. Rol del Farmacéutico. ESTUDIO DE FARMACOLOGÍA CLÍNICA Es un estudio sistemático científico realizado con un ingrediente farmacéutico activo (IFA) aplicados
Mitos y realidades de la Investigación Clínica. Rol del Farmacéutico. ESTUDIO DE FARMACOLOGÍA CLÍNICA Es un estudio sistemático científico realizado con un ingrediente farmacéutico activo (IFA) aplicados
XIII Congreso de La Sociedad Española de Investigaciones Quirúrgicas
 XIII Congreso de La Sociedad Española de Investigaciones Quirúrgicas Programa Definitivo BARCELONA 7-8 OCTUBRE 2004 LA PEDRERA JUEVES 7 de octubre 08.00-08.30h ENTREGA DE LA DOCUMENTACIÓN 08.30-08.45h
XIII Congreso de La Sociedad Española de Investigaciones Quirúrgicas Programa Definitivo BARCELONA 7-8 OCTUBRE 2004 LA PEDRERA JUEVES 7 de octubre 08.00-08.30h ENTREGA DE LA DOCUMENTACIÓN 08.30-08.45h
Congreso Médico Nacional
 Congreso Médico Nacional Reglamento De Buenas Prácticas de Farmacovigilancia Decreto N 39417-S 09 de noviembre de 2016 Dra. Xiomara Vega Cruz 1985 Inicia Plan Piloto en la CCSS. 1991Ingreso al Programa
Congreso Médico Nacional Reglamento De Buenas Prácticas de Farmacovigilancia Decreto N 39417-S 09 de noviembre de 2016 Dra. Xiomara Vega Cruz 1985 Inicia Plan Piloto en la CCSS. 1991Ingreso al Programa
XXI CURSO DE ACTUALIZACIÓN EN GINECOLOGÍA ONCOLÓGICA Dentro del programa de formación continuada de la SEGO Solicitados los créditos de la SEAFORMEC
 Universitat Autònoma de Barcelona Consorci Sanitari de Barcelona Institut Municipal d'assistència Sanitària Servicio de Obstetricia y Ginecología Hospital Universitario del Mar Bajo los auspicios de la
Universitat Autònoma de Barcelona Consorci Sanitari de Barcelona Institut Municipal d'assistència Sanitària Servicio de Obstetricia y Ginecología Hospital Universitario del Mar Bajo los auspicios de la
Acceso de los pacientes a los ensayos clínicos en la geogra2a nacional: Es viable?
 y Productos Sanitarios Acceso de los pacientes a los ensayos clínicos en la geogra2a nacional: Es viable? Encarnación Cruz Martos Subdirectora General de C. Farmacia y P.S. Comunidad de Madrid REQUISITOS
y Productos Sanitarios Acceso de los pacientes a los ensayos clínicos en la geogra2a nacional: Es viable? Encarnación Cruz Martos Subdirectora General de C. Farmacia y P.S. Comunidad de Madrid REQUISITOS
DECLARACIÓN RESPONSABLE PARA LA RENOVACIÓN DE LA AUTORIZACIÓN SANITARIA DE FUNCIONAMIENTO DE CENTROS, SERVICIOS Y ESTABLECIMIENTOS SANITARIOS
 DECLARACIÓN RESPONSABLE PARA LA REVACIÓN DE LA AUTORIZACIÓN SANITARIA DE FUNCIONAMIENTO DE CENTROS, SERVICIOS Y ESTABLECIMIENTOS SANITARIOS (Artículo 14 del Decreto 69/2008, de 26 febrero) D/Dª., mayor
DECLARACIÓN RESPONSABLE PARA LA REVACIÓN DE LA AUTORIZACIÓN SANITARIA DE FUNCIONAMIENTO DE CENTROS, SERVICIOS Y ESTABLECIMIENTOS SANITARIOS (Artículo 14 del Decreto 69/2008, de 26 febrero) D/Dª., mayor
Ensayos Clínicos en Cuba. Experiencias y desafíos. XI Encuentro de Autoridades Competentes en Medicamentos de los Países Iberoamericanos
 Ensayos Clínicos en Cuba. Experiencias y desafíos XI Encuentro de Autoridades Competentes en Medicamentos de los Países Iberoamericanos Junio, 2016 En Cuba Década de los 80 Desarrollo acelerado de la Industria
Ensayos Clínicos en Cuba. Experiencias y desafíos XI Encuentro de Autoridades Competentes en Medicamentos de los Países Iberoamericanos Junio, 2016 En Cuba Década de los 80 Desarrollo acelerado de la Industria
Documentos básicos sobre la ética en la experimentación humana
 REQUERIMIENTOS ÉTICOS Y LEGALES EN LA INVESTIGACIÓN CON MEDICAMENTOS. LOS COMITÉS ÉTICOS DE INVESTIGACIÓN CLÍNICA Rosa Morros Pedrós Dept. Farmacologia, Toxicologia i Terapèutica Universitat Autònoma de
REQUERIMIENTOS ÉTICOS Y LEGALES EN LA INVESTIGACIÓN CON MEDICAMENTOS. LOS COMITÉS ÉTICOS DE INVESTIGACIÓN CLÍNICA Rosa Morros Pedrós Dept. Farmacologia, Toxicologia i Terapèutica Universitat Autònoma de
PROCEDIMIENTOS NORMALIZADOS DE TRABAJO DEL COMITÉ DE ÉTICA DE LA INVESTIGACIÓN CON MEDICAMENTOS DEL ÁREA DE SALUD DE BURGOS Y SORIA
 PROCEDIMIENTOS NORMALIZADOS DE TRABAJO DEL COMITÉ DE ÉTICA DE LA INVESTIGACIÓN CON MEDICAMENTOS DEL ÁREA DE SALUD DE BURGOS Y SORIA COMPOSICIÓN Y REQUISITOS DE LOS MIEMBROS: Código: PNT. 3 Versión: 1 Fecha
PROCEDIMIENTOS NORMALIZADOS DE TRABAJO DEL COMITÉ DE ÉTICA DE LA INVESTIGACIÓN CON MEDICAMENTOS DEL ÁREA DE SALUD DE BURGOS Y SORIA COMPOSICIÓN Y REQUISITOS DE LOS MIEMBROS: Código: PNT. 3 Versión: 1 Fecha
Papel de las Comisiones Clínicas
 Posicionamiento terapéutico: Papel de las Comisiones Clínicas Francesc Puigventós Servei de Farmàcia. Hospital Universitari Son Dureta. Palma de Mallorca II CURSO. Posicionamiento de los medicamentos en
Posicionamiento terapéutico: Papel de las Comisiones Clínicas Francesc Puigventós Servei de Farmàcia. Hospital Universitari Son Dureta. Palma de Mallorca II CURSO. Posicionamiento de los medicamentos en
Cáncer de mama avanzado
 Cáncer de mama avanzado Santander 1 de Julio 2016 Tàrsila Ferro Directora de Cuidados Instituto Catalán de Oncología Profesora Universidad de Barcelona Definiciones Cáncer de mama recurrente o recurrencia:
Cáncer de mama avanzado Santander 1 de Julio 2016 Tàrsila Ferro Directora de Cuidados Instituto Catalán de Oncología Profesora Universidad de Barcelona Definiciones Cáncer de mama recurrente o recurrencia:
FICHA DE EVALUACION PROTOCOLO: CONTENIDO ASPECTOS FORMALES A SER EVALUADOS. 1 Presentar protocolo en idioma español, en soporte papel e informático
 C.E.I.C D.N.S.FF.AA. FICHA DE EVALUACION PROTOCOLO: CONTENIDO ASPECTOS FORMALES A SER EVALUADOS 1 Presentar protocolo en idioma español, en soporte papel e informático 2 Solicitud de autorización para
C.E.I.C D.N.S.FF.AA. FICHA DE EVALUACION PROTOCOLO: CONTENIDO ASPECTOS FORMALES A SER EVALUADOS 1 Presentar protocolo en idioma español, en soporte papel e informático 2 Solicitud de autorización para
DOCUMENTACIÓN DE LOS PROYECTOS A EVALUAR Y CIRCUITOS
 DOCUMENTACIÓN DE LOS PROYECTOS A EVALUAR Y CIRCUITOS Entrega de la documentación Sra. Anuska Linares Comité Ético de Investigación Clínica. Secretaría Técnica Centro de Medicina Regenerativa de Barcelona
DOCUMENTACIÓN DE LOS PROYECTOS A EVALUAR Y CIRCUITOS Entrega de la documentación Sra. Anuska Linares Comité Ético de Investigación Clínica. Secretaría Técnica Centro de Medicina Regenerativa de Barcelona
Los ensayos clínicos con muestras biológicas
 Los ensayos clínicos con muestras biológicas Visión de un miembro de un CEIC alexis.rodriguez@vhir.org CEIC del Hospital Universitari Vall d Hebron Asuntos a debatir Necesidad (o no?) de un acuerdo de
Los ensayos clínicos con muestras biológicas Visión de un miembro de un CEIC alexis.rodriguez@vhir.org CEIC del Hospital Universitari Vall d Hebron Asuntos a debatir Necesidad (o no?) de un acuerdo de
II CURSO DE ATENCIÓN FARMACÉUTICA INTEGRAL EN ONCOLOGIA
 II CURSO DE ATENCIÓN FARMACÉUTICA INTEGRAL EN ONCOLOGIA PREPROGRAMA Audiencia: Titulación: Programa: Inscripción: 16 plazas Farmacéuticos especialistas en Farmacia Hospitalaria Actividad relacionada con
II CURSO DE ATENCIÓN FARMACÉUTICA INTEGRAL EN ONCOLOGIA PREPROGRAMA Audiencia: Titulación: Programa: Inscripción: 16 plazas Farmacéuticos especialistas en Farmacia Hospitalaria Actividad relacionada con
Mejora de los procesos en los Laboratorios Clínicos de SALUD
 P036/09 Mejora de los procesos en los Laboratorios Clínicos de SALUD Fecha de aprobación de programa: Mayo 2009 Fechas curso: 1ª Edición: 15 de Junio de 2009 Horario: de 9:30 a 14:00 Duración: 4,5 horas.
P036/09 Mejora de los procesos en los Laboratorios Clínicos de SALUD Fecha de aprobación de programa: Mayo 2009 Fechas curso: 1ª Edición: 15 de Junio de 2009 Horario: de 9:30 a 14:00 Duración: 4,5 horas.
AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE ALERGOLOGÍA - REQUISITOS MÍNIMOS PARA LA ACREDITACIÓN DE LA COMISIÓN NACIONAL DE LA ESPECIALIDAD - HOSPITAL
 AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE ALERGOLOGÍA - REQUISITOS MÍNIMOS PARA LA ACREDITACIÓN DE LA COMISIÓN NACIONAL DE LA ESPECIALIDAD - HOSPITAL COMUNIDAD : FECHA: DATOS GENERALES Nombre actualizado
AUDITORÍA DOCENTE DE LA ESPECIALIDAD DE ALERGOLOGÍA - REQUISITOS MÍNIMOS PARA LA ACREDITACIÓN DE LA COMISIÓN NACIONAL DE LA ESPECIALIDAD - HOSPITAL COMUNIDAD : FECHA: DATOS GENERALES Nombre actualizado
Evolución y Estado Actual de la Investigación Clínica en el Hospital U i P La Fe. Dña. Begoña Jeweinat Figuerola
 Evolución y Estado Actual de la Investigación Clínica en el Hospital U i P La Fe Dña. Begoña Jeweinat Figuerola Quiénes somos? El Instituto de Investigación Sanitaria La Fe es la entidad que dirige la
Evolución y Estado Actual de la Investigación Clínica en el Hospital U i P La Fe Dña. Begoña Jeweinat Figuerola Quiénes somos? El Instituto de Investigación Sanitaria La Fe es la entidad que dirige la
REQUISITOS DEL CEIC DE EUSKADI PARA LA EVALUACIÓN DE ENSAYOS CLÍNICOS Y ENMIENDAS RELEVANTES:
 REQUISITOS DEL CEIC DE EUSKADI PARA LA EVALUACIÓN DE ENSAYOS CLÍNICOS Y ENMIENDAS RELEVANTES: NOTA IMPORTANTE: Los archivos contenidos en los CDs deben nombrarse con un título que los identifique claramente,
REQUISITOS DEL CEIC DE EUSKADI PARA LA EVALUACIÓN DE ENSAYOS CLÍNICOS Y ENMIENDAS RELEVANTES: NOTA IMPORTANTE: Los archivos contenidos en los CDs deben nombrarse con un título que los identifique claramente,
SISTEMAS DE INFORMACION EN AE Y AP SISTEMAS DE INFORMACION EN AE Y AP
 SISTEMA DE INFORMACION SANITARIA Se define como un mecanismo para la recogida, procesado, análisis y transmisión de la información necesaria para organizar y hacer funcionar los servicios sanitarios, así
SISTEMA DE INFORMACION SANITARIA Se define como un mecanismo para la recogida, procesado, análisis y transmisión de la información necesaria para organizar y hacer funcionar los servicios sanitarios, así
Estructuras de apoyo a los ensayos clínicos en Terapias Avanzadas
 Estructuras de apoyo a los ensayos clínicos en Terapias Avanzadas Natividad Cuende MD, MPH, PhD Directora Ejecutiva Iniciativa Andaluza en Terapias Avanzadas MARCO LEGAL: MEDICAMENTO Imagen MARCO LEGAL:
Estructuras de apoyo a los ensayos clínicos en Terapias Avanzadas Natividad Cuende MD, MPH, PhD Directora Ejecutiva Iniciativa Andaluza en Terapias Avanzadas MARCO LEGAL: MEDICAMENTO Imagen MARCO LEGAL:
COMISIÓN DE EVALUACIÓN DE PROTOCOLOS/PROYECTOS DE INVESTIGACIÓN XERENCIA DE ATENCIÓN PRIMARIA DE VIGO
 COMISIÓN DE EVALUACIÓN DE PROTOCOLOS/PROYECTOS DE INVESTIGACIÓN XERENCIA DE ATENCIÓN PRIMARIA DE VIGO CONSIDERACIONES PREVIAS Toda la investigación en humanos está sujeta a normas éticas internacionales
COMISIÓN DE EVALUACIÓN DE PROTOCOLOS/PROYECTOS DE INVESTIGACIÓN XERENCIA DE ATENCIÓN PRIMARIA DE VIGO CONSIDERACIONES PREVIAS Toda la investigación en humanos está sujeta a normas éticas internacionales
Joaquín Delgadillo Belén Ruiz-Antorán
 Joaquín Delgadillo Belén Ruiz-Antorán At Actualizar los datos existentes it t en la base de dt datos desocios de la Sociedad d Española de Farmacología Clínica. Recopilar y documentar información importante
Joaquín Delgadillo Belén Ruiz-Antorán At Actualizar los datos existentes it t en la base de dt datos desocios de la Sociedad d Española de Farmacología Clínica. Recopilar y documentar información importante
PLAN CURRICULAR MAESTRÍA EN INVESTIGACIÓN CLÍNICA
 PLAN CURRICULAR MAESTRÍA EN INVESTIGACIÓN CLÍNICA SUMILLA: La maestría en investigación clínica es un grado académico con un plan de estudios de base amplia. Este programa de maestría cubre los principios
PLAN CURRICULAR MAESTRÍA EN INVESTIGACIÓN CLÍNICA SUMILLA: La maestría en investigación clínica es un grado académico con un plan de estudios de base amplia. Este programa de maestría cubre los principios
CEIC: estructura y funciones
 CEIC: estructura y funciones Dr. Francisco Abad Santos Presidente del CEIC Hospital Universitario de la Princesa Introducción La investigación médica es necesaria, pero está sujeta a normas éticas que
CEIC: estructura y funciones Dr. Francisco Abad Santos Presidente del CEIC Hospital Universitario de la Princesa Introducción La investigación médica es necesaria, pero está sujeta a normas éticas que
OPOSICIONES MEDICO SACYL OPE 2015 CUESTIONARIO DERECHOS Y DEBERES EN RELACIÓN CON LA SALUD
 CUESTIONARIO DERECHOS Y DEBERES EN RELACIÓN CON LA SALUD 1. Según el artículo 7.1 de la Ley 41/2002, de 14 de noviembre, toda persona tiene derecho a que se respete el carácter confidencial de los datos
CUESTIONARIO DERECHOS Y DEBERES EN RELACIÓN CON LA SALUD 1. Según el artículo 7.1 de la Ley 41/2002, de 14 de noviembre, toda persona tiene derecho a que se respete el carácter confidencial de los datos
XXIII CURSO DE ACTUALIZACIÓN EN GINECOLOGÍA ONCOLÓGICA
 Universitat Autònoma de Barcelona Consorci Sanitari de Barcelona Institut Municipal d'assistència Sanitària Servicio de Obstetricia y Ginecología Hospital Universitario del Mar Bajo los auspicios de la
Universitat Autònoma de Barcelona Consorci Sanitari de Barcelona Institut Municipal d'assistència Sanitària Servicio de Obstetricia y Ginecología Hospital Universitario del Mar Bajo los auspicios de la
Unidad Central de Enayos Clínicos, para facilitar el acceso de los enfermos a nuevos fármacos
 NUEVOS SERVICIOS Unidad Central de Enayos Clínicos, para facilitar el acceso de los enfermos a nuevos fármacos El nuevo servicio integra todos los recursos del hospital para potenciar y agilizar los trabajos
NUEVOS SERVICIOS Unidad Central de Enayos Clínicos, para facilitar el acceso de los enfermos a nuevos fármacos El nuevo servicio integra todos los recursos del hospital para potenciar y agilizar los trabajos
Sociedades Operadoras Callao y VMT Salud SAC. Sociedades Operadoras Villa María del Triunfo y Callao Salud S. A. C.
 Sociedades Operadoras Villa María del Triunfo y Callao Salud S. A. C. JORNADA INTERNACIONAL SOBRE LA HISTORIA CLÍNICA ELECTRÓNICA E INTEROPERABILIDAD EN EL SECTOR SALUD Implementación de la Historia Clínica
Sociedades Operadoras Villa María del Triunfo y Callao Salud S. A. C. JORNADA INTERNACIONAL SOBRE LA HISTORIA CLÍNICA ELECTRÓNICA E INTEROPERABILIDAD EN EL SECTOR SALUD Implementación de la Historia Clínica
10.- PROCEDIMIENTO PARA LA RECEPCIÓN DEL PACIENTE Y DEL EXPEDIENTE CLÍNICO PARA SU INGRESO A HOSPITALIZACIÓN VÍA CONSULTA EXTERNA
 Hoja: 1 de 6 10.- PROCEDIMIENTO PARA LA RECEPCIÓN DEL PACIENTE Y DEL EXPEDIENTE CLÍNICO PARA SU INGRESO A HOSPITALIZACIÓN VÍA CONSULTA EXTERNA Hoja: 2 de 6 1.0 Propósito 1.1 Contar con los procedimientos
Hoja: 1 de 6 10.- PROCEDIMIENTO PARA LA RECEPCIÓN DEL PACIENTE Y DEL EXPEDIENTE CLÍNICO PARA SU INGRESO A HOSPITALIZACIÓN VÍA CONSULTA EXTERNA Hoja: 2 de 6 1.0 Propósito 1.1 Contar con los procedimientos
NAC. Anatomía patológica en la SIMPOSIO DE CALIDAD EN ANATOMÍA PATOLOGICA. Isabel de la Villa Jefe de Departamento de Sanidad ENAC
 SIMPOSIO DE CALIDAD EN ANATOMÍA PATOLOGICA NAC Anatomía patológica en la 15189 15 de diciembre de 2011 Isabel de la Villa Jefe de Departamento de Sanidad ENAC 1 Qué es la acreditación? Declaración por
SIMPOSIO DE CALIDAD EN ANATOMÍA PATOLOGICA NAC Anatomía patológica en la 15189 15 de diciembre de 2011 Isabel de la Villa Jefe de Departamento de Sanidad ENAC 1 Qué es la acreditación? Declaración por
INSTRUCTIVO EXTERNO Procedimiento para el Registro de Organizaciones de Investigación por Contrato (OIC) y Centros de Investigación (CI)
 Contrato (OIC) y Centros de Investigación (CI) Versión [1.0] Coordinación Técnica de Certificaciones, Autorizaciones y BPs Sanitarias Dirección Técnica de Ensayos Clínicos Febrero, 2018 Página 3 de 8 CONTROL
Contrato (OIC) y Centros de Investigación (CI) Versión [1.0] Coordinación Técnica de Certificaciones, Autorizaciones y BPs Sanitarias Dirección Técnica de Ensayos Clínicos Febrero, 2018 Página 3 de 8 CONTROL
MESA REDONDA: MANEJO DE MEDICAMENTOS BIOPELIGROSOS
 JORNADAS DE FARMACIA HOSPITALARIA SVFH MESA REDONDA: MANEJO DE MEDICAMENTOS BIOPELIGROSOS Dr. Julio Muelas Tirado Jefe de Servicio de Ordenación, Control y Vigilancia de Productos Farmacéuticos. Dirección
JORNADAS DE FARMACIA HOSPITALARIA SVFH MESA REDONDA: MANEJO DE MEDICAMENTOS BIOPELIGROSOS Dr. Julio Muelas Tirado Jefe de Servicio de Ordenación, Control y Vigilancia de Productos Farmacéuticos. Dirección
