Ficha de trabajo X (refuerzo) Ficha de trabajo IX (refuerzo) UNIDAD 3 Ficha de trabajo I (refuerzo)
|
|
|
- José Antonio Botella Jiménez
- hace 5 años
- Vistas:
Transcripción
1 2. La masa de 500 ml de mercurio líquido será de 8,3 kg. 3. Los volúmenes de los gases serán: 2,155 L de agua; 668,7 L de butano, y 843,1 L de etanol. C 1. La temperatura de fusión es de 10 C. 2. La temperatura de ebullición es de 50 C. 3. A 57 C será vapor, y a 3 C, sólido. 4. El gráfico es el siguiente: Calor eliminado (J) Ficha de trabajo IX (refuerzo) A La temperatura de 283 K se corresponde con 10 C. A esa temperatura, el agua, el etanol y el mercurio se encuentran en estado líquido, y el butano, en estado gaseoso. El volumen de cada sustancia es: V agua = 1 L V butano = 0,4 kl V etanol = 1,24 L V mercurio = 60,2 ml El estado de agregación a 60 C es gas, y a 23 C, líquido. La representación gráfica es la siguiente: Calor suministrado (J) Ficha de trabajo X (refuerzo) A Tramo I. Se trata de un sólido que se está calentando y, por tanto, aumentando su temperatura. Las partículas que forman el sólido no se mueven con libertad, pero sí vibran respecto de una posición de equilibrio. Al ir aumentando la temperatura, la velocidad de las partículas también lo hace, y por ello la vibración es mayor, y la estructura del sólido no es tan rígida. Tramo II. Se trata del cambio de estado que denominamos fusión. Las partículas del sólido han alcanzado ya una vibración tal que comienzan a moverse independientemente unas de otras; el sólido comienza a fundirse y aparece el líquido. Tramo III. Se trata de un líquido que se está calentando; al aumentar la temperatura, las partículas del líquido se mueven haciendo cada vez recorridos mayores. Tramo IV. Se trata del cambio de estado de líquido a gas; en su movimiento, las partículas de líquido se distancia entre sí, pasando el conjunto a estado gaseoso. Tramo V. Se trata de un gas calentándose; la energía suministrada se invierte en aumentar la velocidad de las partículas del gas y, por tanto, la temperatura. Para que se produzca la ebullición, es necesario que el líquido se encuentre a la temperatura de cambio de estado; sin embargo, en la evaporación esto no es necesario. La evaporación es un fenómeno que se da en la superficie de los líquidos. Las moléculas que se encuentran allí necesitan relativamente poca energía para poder pasar al estado vapor, por esto la evaporación ocurre a temperaturas inferiores a la de ebullición. UNIDAD 3 Ficha de trabajo I (refuerzo) A Si la materia se puede separar por métodos físicos, se trata de mezclas, que son homogéneas si son uniformes en todas sus partes, y heterogéneas en caso contrario. GRUPO ANAYA, S.A. Física y Química 3º ESO. Material fotocopiable autorizado. 228
2 C Si la materia no se puede separar por métodos físicos, se trata de sustancias puras, que serán compuestos si se pueden separar por métodos químicos, y elementos, en caso contrario. SISTEMA Agua de mar Mahonesa Diamante Gel de sílice Lodo Petróleo Coltán Argón SISTEMA Freón 22 Aceite de oliva TIPO DE SISTEMA Mezcla homogénea Mezcla homogénea Sustancia pura (elemento) Sustancia pura (compuesto) Mezcla heterogénea TIPO DE SISTEMA Mezcla homogénea Mezcla homogénea Sustancia pura sencilla Sustancia pura compuesto Mezcla homogénea NATURAL/ SINTÉTICO Natural Natural Natural Sintético Sintético Ficha de trabajo II (refuerzo) y, además, estas sustancias son miscibles entre sí. 2. Destilación. Las temperaturas de ebullición son diferentes, y las sustancias componentes de la mezcla no se separarían por decantación. 3. Filtración. Se trata de sólidos y líquidos no miscibles. 4. Lavado. La sal es soluble en agua. Ficha de trabajo III (ampliación) A 1. Primero utilizaremos una centrifugación para separar el sólido del lodo; después, separamos el contaminante del agua por destilación. 2. Utilizaremos una cristalización combinada con una filtración. Primero, disolvemos la mezcla en agua caliente y la filtramos para separar el sólido insoluble. Después, dejamos cristalizar la sal por evaporación del agua. 3. Utilizaremos una separación magnética para separar las virutas de hierro; a continuación, filtramos el aceite y separamos así la arena y la grava. Después de un lavado de los sólidos, los separamos por tamizado, donde quedará retenida la grava y pasará la arena. GRUPO ANAYA, S.A. Física y Química 3º ESO. Material fotocopiable autorizado. A La destilación nos permite separar mezclas homogéneas, ya que sus componentes tendrán diferentes temperaturas de ebullición. La cristalización sirve para separar mezclas homogéneas, en función de la solubilidad de sus componentes a distintas temperaturas. Con la filtración podemos separar mezclas heterogéneas, dado que el tamaño de las partículas de sus componentes son diferentes. Con la decantación y la centrifugación separamos mezclas heterogéneas, dada la diferente densidad de sus componentes. Destilación: refrigerante, matraz de fondo redondo, termómetro y pie. Filtración: embudo, pie y aro. Cristalización: cristalizador. Decantación: pie y aro. C 1. Destilación. Las temperaturas de ebullición del agua y del alcohol son diferentes, Ficha de trabajo IV (refuerzo) A 1. F; 2. F; 3. V; 4. V. 1. Disolvente, alcohol; soluto, agua. 2. Disolvente, aire; soluto, vapor de agua. C 3. Disolvente, aceite; solutos, leche o huevo (según receta), sal y limón. 4. Disolvente, agua; solutos, sales. SOLUTO DISOLVENTE Amalgamas Sólido Sólido ebida gaseosa Gas Líquido Aerosol Sólido o líquido Gas Nubes Vapor Gas D Las partículas de disolvente, que están en continuo movimiento, rodean a las de soluto y las transportan desde el cristal hasta el seno del líquido, formándose así la disolu- 229
3 ción. SI aumentamos la temperatura o agitamos, favorecemos la velocidad del proceso, pues aumenta la velocidad de las partículas de disolvente. Ficha de trabajo V (refuerzo) A 1. La representación gráfica es la siguiente: S (g/100 g) Disolver 65 g de la sal en 200 g de agua significa que por cada 100 de agua hay 32,5 g de sal. A 20 C, la solubilidad es de 35 g de sal por cada 100 g de agua; por tanto, podemos decir que es una disolución concentrada. 3. Una disolución saturada a 40 C presenta 37 g de sal por cada 100 de agua. Al enfriar la disolución, la solubilidad disminuye hasta 32 g de sal disueltos por cada 100 g de agua; por tanto, por cada 100 g de agua «sobran» 5 g de sal, que precipitarían. 1. La representación gráfica es la siguiente: S (mg/l) En este caso, la solubilidad disminuye con la temperatura, mientras que en el anterior aumenta. Esto es así porque los gases disminuyen su solubilidad en agua al aumentar la temperatura, y las sales la disminuyen. 3. Al aumentar la temperatura, disminuye la solubilidad. La consecuencia medioambiental es la contaminación térmica del agua, por la que disminuye la cantidad de oxígeno disuelto en aguas de ríos o embalses si sobre ellos se vierte un caudal considerable de agua a mayor temperatura. Una de las fuentes de contaminación pueden ser las centrales de producción de energía eléctrica, bien sean térmicas o nucleares, o cualquier otro tipo de industria que utilice agua en procesos de enfriamiento. 4. A partir de los datos de la tabla, tomando las solubilidades a las temperaturas de 15 C y 25 C, calculamos la disminución de la solubilidad dividiendo la diferencia entre el valor de referencia que, en este caso, es la solubilidad a 15 C: 9,76 8, = 16,9% 9,76 C 1. F. Se diluyen mejor los sólidos finamente divididos, porque se aumenta el contacto entre el soluto y el disolvente; así, las partículas del sólido están más accesibles a las del disolvente. 2. V; 3. V. 4. F. Una disolución de gas en agua disminuye la cantidad de gas disuelto al aumentar su temperatura, por lo que no conseguiríamos disolver más gas (pasar de saturada a concentrada) aumentando la temperatura. Ficha de trabajo VI (ampliación) A Para calcular los datos de solubilidad en g/l, solo tenemos que considerar que 1 kg de agua ocupa un volumen de 1 L (a partir del dato de la densidad del agua), y deducir entonces que los datos que nos dan y los que nos piden están referidos al mismo volumen de agua. La conversión es, en este caso, directa. Los valores de la solubilidad, expresados en g/l de agua, son, por tanto: N 2 : 0,018 g/l. O 2 : 0,039 g/l. : 1,45 g/l. NH 3 : 4,7 g/l. HCl: 6,95 g/l. 230
4 C D E Para calcular los datos de solubilidad en L/L, debemos considerar la densidad de los gases para calcular el volumen que ocupa la masa de gas que está disuelta en agua (que es unas mil veces menor que la del agua, según los datos que nos dan), y calcular de este modo (ponemos como ejemplo el HCl): 6,95 g HCl 1 L agua 1 L HCl L HCl = 4,65 1,49 g HCl L agua Por tanto, los valores de la solubilidad, expresados en L/L de agua, son: N 2 : 0,02 L/L. O 2 : 0,03 L/L. : 0,81 L/L. NH 3 : 6,76 L/L. HCl: 4,65 L/L. En realidad no corresponden a una concentración expresada en % volumen, pues el denominador solo se refiere al disolvente, y no a la disolución. Debemos suponer aditividad de volúmenes. Si tomamos 1 L de agua y para el caso del, resulta: 0, = 45% 0, Los valores de la concentración, expresada en % en volumen, son, entonces, para cada caso: N 2 : 2%. O 2 : 3%. : 45%. NH 3 : 87%. HCl: 82%. Sucede con los resultados del NH 3 y del HCl, lo que significa que, en volumen, y con la aproximación considerada, es mayor el volumen del soluto que el del disolvente. El HCl y el NH 3, pues son mucho más solubles en agua que los demás. La inhalación conjunta del, N 2 y O 2, o cualquiera de los dos primeros y el O 2, en las proporciones adecuadas, no supone ningún riesgo para la salud; de hecho, son los gases mayoritarios presentes en la atmósfera que respiramos (teniendo en cuenta que la proporción de oxígeno y nitrógeno es la mayor). Es decir, el y el N 2 no son causantes directos de daños en nuestro organismo; solo son perjudiciales si su concentración es tal que desplacen la cantidad de oxígeno vital y se produzca anoxia. El NH 3 y el HCl irritan las vías respiratorias altas, y en dosis elevadas pueden causar daños mayores. Dado que el umbral de detección del NH 3 para el ser humano es muy bajo, resulta muy sencillo «oler a amoniaco» y evitar así estar expuestos a él. Ficha de trabajo VII (refuerzo) A En un vaso de leche (250 ml) se ingiere: Proteínas: 7,75 ml. Hidratos de carbono: 11,5 ml. De los anteriores, azúcares: 11,5 ml. Grasas: 9 ml. De las anteriores, saturadas: 6 ml. Calcio: 0,3 ml. Sodio: 0,1 ml. 1. La masa de grasas saturadas es de 2,4 g, y la masa total de grasas, 3,6 g; por tanto, el porcentaje de grasas saturadas respecto del total de grasas será: 2,4 g 100 = 67% 3,6 g 2. Como 120 mg es el 15% C.D.R., el 100% CDR será: = 800 mg Ca 15 Para conseguir esa cantidad (800 mg = = 0,8 g), y teniendo en cuenta que la concentración de calcio es de 1,2 g/l, necesitaremos: 0,8 g Ca = 0,67 L de leche 1,2 g Ca/L 3. El calcio es uno de los nutrientes más beneficiosos de la leche. Para que parezca que hay una gran cantidad de calcio en este producto, se ofrece la cantidad d en mg, puesto que así la cifra es mayor. 231
5 4. Habría que conocer la densidad de la leche. Para ello, podríamos pesar un matraz aforado de un litro vacío y lleno de leche. Por diferencia entre estas dos masas medidas, tendríamos la masa de un litro de leche y, aplicando la expresión de la densidad y operando, el valor de esta última. 1. Es la densidad del medicamento. 2. A la concentración de medicamento en el cuerpo del paciente que se puede suministrar por toma. 3. Si el niño tiene una masa de 15 kg, necesitará: 15 mg 15 kg = 225 mg de medicamento kg A partir de la densidad, obtenemos el volumen necesario, expresado en ml: V = m d = 225 mg = 2,25 ml 100 mg/ml 4. Es la concentración de principio activo en el medicamento (jarabe). 5. Si ingiere 2,25 ml, y por cada ml hay 90 mg de principio activo, los mg de principio activo que ingiere el niño se calculan como sigue: 2,25 ml 90 mg /ml = 202,5 mg C Proteínas: 10,0%. Hidratos de carbono: 50,7%. De los anteriores, azúcares: 2,8%. Grasas: 1,9%. De las anteriores, saturadas: 1,1%. Fibra alimentaria: 5,2%. Sodio: 0,035%. Equivalente en sal del sodio: 0,087%. 1. El porcentaje de grasas saturadas respecto del total de grasas se calcula como sigue: 1,1 g 100 = 57,9% 1,9 g 2. La sal común lleva sodio. El equivalente en sal es la cantidad de sal que llevaría la pasta para aportar la misma cantidad de sodio que la que se muestra en el análisis; se calcula así: 0,035 g 100 = 40,2% 0,087 g Ficha de trabajo VIII (ampliación) A 1. En el caso de una mezcla heterogénea, las sustancias que la componen realmente ocupan volúmenes distintos (pensemos en el agua y el aceite) y no se llegan a mezclar; en este caso, sí podemos considerar que el volumen final es la suma de los volúmenes de las sustancias por separado. 2. Esta afirmación es falsa. Las partículas que componen cada sustancia individual, al mezclarse, pasan a ocupar en parte el mismo volumen. Esta «intersección» de volúmenes no nos permite sumar los volúmenes de las sustancias individuales sin cometer un error. 3. En este caso la afirmación es correcta, pues no se trata más que de dos porciones de la misma sustancia. La aditividad de volúmenes supone la siguiente aproximación: = V disolvente Para poder cuantificar qué error se comete al utilizar la igualdad anterior, debemos comparar ambas magnitudes: y (V disolvente ). Una forma de compararlas es hacer un cociente entre ellas; para ello, pondremos la mayor de ellas en el denominador y calcularemos el % de una frente a otra; la diferencia hasta el 100% es error que se comete. Una vez establecido qué debemos calcular, vamos a detallar cómo calculamos las magnitudes que deben ser comparadas; el volumen de disolución es: = m disolución d disolución Y el de disolvente más soluto: = m disolvente d disolvente + m soluto V soluto El error que se comete se cuantifica de la siguiente manera: Error (%) = V disolvente
6 Ficha de trabajo IX (refuerzo) A 1. La densidad de una disolución y la expresión de su concentración se diferencian en que la densidad hace referencia a la masa del total de disolución que ocupa un determinado volumen de ella, mientras que la concentración es la relación entre la masa únicamente de soluto y un determinado volumen de disolución. Los valores de las concentraciones y densidades pedidas se muestran en la tabla que aparece después de la solución del apartado Se podrían expresar, por ejemplo, en % masa. Los valores que corresponden a esta concentración se muestran en la tabla. 2. Utilizamos como suposición que el volumen de la disolución es la suma de los volúmenes de soluto y de disolvente, lo que supone una aproximación conocida como aditividad de volúmenes: m soluto %masa = 100 m soluto + m disolvente %volumen = V soluto V soluto + V disolvente 100 Las concentraciones pedidas se muestran en la tabla: (METANOL+ AGUA) (AMONIACO+ AGUA) (N-HEPTANO+ N-OCTANO) % MASA 4,2 28, , ,2 0, ,2 La cantidad de disolución que hay que coger en cada caso es: 2 L; 100 cl; 25 L; 850 g. % VOL 5,2 31,0 20,4 1. Tendremos que expresar las masas de soluto y disolvente en las mismas unidades; por ejemplo, gramos. Así, 0,726 kg de agua son 726 g de agua. La concentración resulta: 74 g %masa = 74 g g = 9,25% Ficha de trabajo X (refuerzo) A 1. Utilizamos la densidad y las masas de soluto y de disolvente: d = m V 8 V = m d Los volúmenes pedidos se incluyen en las tablas: METANOL DENSIDAD DE LA (g/l) CONCEN- TRACIÓN (g/l) CONCEN- TRACIÓN (%) 842 8,3 1,0 AMO- NIACO 30 N- HEPTANO 2. La concentración de la disolución es mayor, ya que hay más cantidad de soluto por cada 100 g de disolución. 3. La cantidad de la segunda disolución pedida es: 100 mg disolución 500 mg soluto = 15 mg soluto = mg 3,3 g de disolución MASA DE SOLUTO (g) C La tabla completa es: DENSIDAD DE SOLUTO (g/ml) VOLUMEN DE SOLUTO (ml) 0,791 0,89 0,684 12, ,3 73,1 CONCENTRACIÓN DE CANTIDAD DE SOLUTO CANTIDAD DE MASA DE DISOLVENTE (g) DENSIDAD DE DISOLVENTE (g/ml) VOLUMEN DE DISOLVENTE (ml) AGUA AGUA N-OCTANO , ,5 250 g/l 0,150 mg 6 dl 12% en masa 6 g 50 g 1 mg/l 0,3 mg 34 dl 25% volumen 12 ml 48 ml 233
d (g/cm 3 ) d (kg/l) Masa Volumen a) Un kilogramo de etanol ocupa más volumen que un kilogramo de acetona.
 La materia. Los líquidos Ficha de trabajo 1 Nombre y apellidos:... Curso:... Fecha: La densidad de los líquidos El líquido más abundante es el agua, cuya densidad es de 1 kg/l; debido a ello, estamos habituados
La materia. Los líquidos Ficha de trabajo 1 Nombre y apellidos:... Curso:... Fecha: La densidad de los líquidos El líquido más abundante es el agua, cuya densidad es de 1 kg/l; debido a ello, estamos habituados
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
Todo lo que vemos es materia
 Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Tema 4: Sustancias puras y mezclas
 Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
PROBLEMAS MEZCLAS Y DISOLUCIONES
 PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
1 Propiedades de la materia
 1 La materia 1 Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Cuando nos referimos
1 La materia 1 Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Cuando nos referimos
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
Tema 7. Las mezclas. Introducción
 Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
Métodos de separación en mezclas
 Los métodos de separación están basados en las diferentes propiedades físicas (como la densidad, la temperatura de ebullición, la solubilidad, el estado de agregación, etc.) de las sustancias que componen
Los métodos de separación están basados en las diferentes propiedades físicas (como la densidad, la temperatura de ebullición, la solubilidad, el estado de agregación, etc.) de las sustancias que componen
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Nombre y apellidos:...
 1 Señala las opciones correctas: a) El conocimiento científico surge de la necesidad de dar respuesta a un problema basado en hechos a los que se quiere dar explicación. b) El conocimiento científico es
1 Señala las opciones correctas: a) El conocimiento científico surge de la necesidad de dar respuesta a un problema basado en hechos a los que se quiere dar explicación. b) El conocimiento científico es
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES.
 EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química.
 Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
TEMA 3.- Naturaleza de la. materia (II)
 TEMA 3.- Naturaleza de la 1.- Concepto de mezcla. Tipos. materia (II) ÍNDICE GENERAL 2.- Separación de los componentes de una mezcla. 2.1.- Separación de los componentes de mezclas heterogéneas. 2.1.1.-
TEMA 3.- Naturaleza de la 1.- Concepto de mezcla. Tipos. materia (II) ÍNDICE GENERAL 2.- Separación de los componentes de una mezcla. 2.1.- Separación de los componentes de mezclas heterogéneas. 2.1.1.-
Si el precio de la plata es 820 euros/kg y el del oro es euros/kg, qué volumen de plata tendría el mismo precio que medio kilogramo de oro?.
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Si el precio de la plata es 820 euros/kg y el del oro es 42 120 euros/kg, qué volumen de plata tendría el mismo precio que medio kilogramo de oro?. La
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Si el precio de la plata es 820 euros/kg y el del oro es 42 120 euros/kg, qué volumen de plata tendría el mismo precio que medio kilogramo de oro?. La
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Tema 3 CLASIFICACIÓN DE LA MATERIA
 Clasificación de la materia 1 Tema 3 CLASIFICACIÓN DE LA MATERIA 1. ÁTOMOS Y MOLÉCULAS... 1 2. SUSTANCIAS PURAS Y MEZCLAS.... 2 2.1. SUSTANCIAS PURAS... 2 2.2. MEZCLAS... 2 3. SEPARACIÓN DE LOS COMPONENTES
Clasificación de la materia 1 Tema 3 CLASIFICACIÓN DE LA MATERIA 1. ÁTOMOS Y MOLÉCULAS... 1 2. SUSTANCIAS PURAS Y MEZCLAS.... 2 2.1. SUSTANCIAS PURAS... 2 2.2. MEZCLAS... 2 3. SEPARACIÓN DE LOS COMPONENTES
TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
1. Disoluciones una disolución es cualquier mezcla homogénea disolvente soluto Medidas de composición
 1. Disoluciones En general, una disolución es cualquier mezcla homogénea. Por ejemplo, el aire, mezcla de nitrógeno, oxígeno y otros gases en proporciones menores; o el bronce, que es una aleación metálica
1. Disoluciones En general, una disolución es cualquier mezcla homogénea. Por ejemplo, el aire, mezcla de nitrógeno, oxígeno y otros gases en proporciones menores; o el bronce, que es una aleación metálica
La diversidad de la materia
 La diversidad de la materia Física y Química Los sistemas materiales Oxford University Press España, S. A. Física y Química 3º ESO 2 Un sistema material es una porción de materia que se aísla física o
La diversidad de la materia Física y Química Los sistemas materiales Oxford University Press España, S. A. Física y Química 3º ESO 2 Un sistema material es una porción de materia que se aísla física o
LA MATERIA Y SU DIVERSIDAD
 LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
 Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES IES La Magdalena. Avilés. Asturias Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir
DISOLUCIONES IES La Magdalena. Avilés. Asturias Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir
TEMA 3: MEZCLAS REFLEXIÓN INICIAL
 TEMA 3: MEZCLAS REFLEXIÓN INICIAL El aire que respiramos es una mezcla de muchos gases: nitrógeno, oxígeno, dióxido de carbono Casi todos los materiales naturales o artificiales de nuestro entorno son
TEMA 3: MEZCLAS REFLEXIÓN INICIAL El aire que respiramos es una mezcla de muchos gases: nitrógeno, oxígeno, dióxido de carbono Casi todos los materiales naturales o artificiales de nuestro entorno son
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
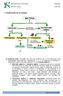 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
LA DIVERSIDAD DE LA MATERIA
 Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
2.-. Realiza los siguientes cambios de unidades, expresando el resultado en notación científica: b. 0,2 l a cm3. m s a km f. 1500
 Curso 3º ESO Asignatura: FÍSICA Y QUÍMICA Alumn@: Curso: La resolución de estas actividades debe ser individual, y nunca copia de otro/a compañero/a. 1. Asocia cada cantidad con su magnitud indicando el
Curso 3º ESO Asignatura: FÍSICA Y QUÍMICA Alumn@: Curso: La resolución de estas actividades debe ser individual, y nunca copia de otro/a compañero/a. 1. Asocia cada cantidad con su magnitud indicando el
TEMA 2: DIVERSIDAD DE LA MATERIA
 TEMA 2: DIVERSIDAD DE LA MATERIA 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.- Propiedades generales y características de la materia.
TEMA 2: DIVERSIDAD DE LA MATERIA 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.- Propiedades generales y características de la materia.
SUSTANCIA PURA ELEMENTO COMPUESTO 1
 SUSTANCIA PURA ELEMENTO COMPUESTO 1 MATERIA MEZCLA Sustancia pura Sistema material en el que se han combinado dos o más sustancias Mezcla de agua y azúcar Mezcla homogénea Sistema formado por dos o más
SUSTANCIA PURA ELEMENTO COMPUESTO 1 MATERIA MEZCLA Sustancia pura Sistema material en el que se han combinado dos o más sustancias Mezcla de agua y azúcar Mezcla homogénea Sistema formado por dos o más
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
U.D. 2 LA MATERIA. Para describir un cuerpo o un sistema material, necesitamos conocer sus propiedades. Así, distinguimos entre:
 U.D. 2 LA MATERIA 1. Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Para describir
U.D. 2 LA MATERIA 1. Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Para describir
INTRODUCCIÓN DISOLUCIONES
 QUIMICA COMUN INTRODUCCIÓN DISOLUCIONES EBULLICIÓN V/S EVAPORACIÓN Ambos conceptos tienen relación con la presión de vapor. La presión de vapor es la fuerza que tienen las moléculas de un líquido para
QUIMICA COMUN INTRODUCCIÓN DISOLUCIONES EBULLICIÓN V/S EVAPORACIÓN Ambos conceptos tienen relación con la presión de vapor. La presión de vapor es la fuerza que tienen las moléculas de un líquido para
03 DISOLUCIONES. 2 Observando la curva de solubilidad del clorato potásico, responder:
 03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
CONTENIDOS MÍNIMOS Y CRITERIOS DE EVALUACIÓN
 4 La materia: estados de agregación. Objetivos Observar el aspecto y otras características de la materia, en sus diversos estados de agregación: sólido, líquido y gaseoso. Distinguir y aplicar a ejercicios
4 La materia: estados de agregación. Objetivos Observar el aspecto y otras características de la materia, en sus diversos estados de agregación: sólido, líquido y gaseoso. Distinguir y aplicar a ejercicios
TEST DE REPASO 2 FÍSICA Y QUÍMICA DE 2º ESO. TEMAS 2, 3, 4 y 5
 TEST DE REPASO 2 FÍSICA Y QUÍMICA DE 2º ESO TEMAS 2, 3, 4 y 5 1º) La bureta es un instrumento para medir: a) masas b) densidades c) volúmenes 1º) La bureta es un instrumento para medir: a) masas b) densidades
TEST DE REPASO 2 FÍSICA Y QUÍMICA DE 2º ESO TEMAS 2, 3, 4 y 5 1º) La bureta es un instrumento para medir: a) masas b) densidades c) volúmenes 1º) La bureta es un instrumento para medir: a) masas b) densidades
La materia y los cambios químicos 4. Sustancias puras y mezclas
 4. Sustancias puras y mezclas Materia Sustancias puras Formadas por un único tipo de componente Mezclas Formada por dos o más sustancias puras Elementos Formados por la misma clase de átomos Compuestos
4. Sustancias puras y mezclas Materia Sustancias puras Formadas por un único tipo de componente Mezclas Formada por dos o más sustancias puras Elementos Formados por la misma clase de átomos Compuestos
LA MATERIA: ESTADOS DE AGREGACIÓN
 LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
Actividades para repasar el examen de septiembre
 Actividades para repasar el examen de septiembre 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes y de
Actividades para repasar el examen de septiembre 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes y de
TEST DE REPASO 1 FÍSICA Y QUÍMICA DE 2º ESO. TEMAS 1, 2, 3, 4 y parte del 5
 TEST DE REPASO 1 FÍSICA Y QUÍMICA DE 2º ESO TEMAS 1, 2, 3, 4 y parte del 5 1º) Indica cuál de estas frases sobre la manera de trabajar de los científicos es incorrecta: a) Los científicos observan la naturaleza
TEST DE REPASO 1 FÍSICA Y QUÍMICA DE 2º ESO TEMAS 1, 2, 3, 4 y parte del 5 1º) Indica cuál de estas frases sobre la manera de trabajar de los científicos es incorrecta: a) Los científicos observan la naturaleza
TEMA 3: Composición de la Materia
 TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
FÍSICA Y QUÍMICA 2º ESO Tema 2: LA MATERIA Mezclas y Soluciones. Sustancias puras y mezclas
 Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
TEST DE REPASO 1 FÍSICA Y QUÍMICA DE 2º ESO TEMAS 1, 2, 3 Y 4
 TEST DE REPASO 1 FÍSICA Y QUÍMICA DE 2º ESO TEMAS 1, 2, 3 Y 4 1º) El volumen es la propiedad de los cuerpos que indica: a) cuánto ocupa b) cuán compacto es c) cuánta materia contiene 1º) El volumen es
TEST DE REPASO 1 FÍSICA Y QUÍMICA DE 2º ESO TEMAS 1, 2, 3 Y 4 1º) El volumen es la propiedad de los cuerpos que indica: a) cuánto ocupa b) cuán compacto es c) cuánta materia contiene 1º) El volumen es
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
Sustituir fotografía. Sustituir texto
 Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Soluciones y unidades de concentración
 MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
Soluciones y unidades de concentración
 Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
2. Métodos de separación de los componentes de una mezcla.
 TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía.
 1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
1. La materia: sustancias puras y mezclas
 RESUMEN de la UNIDAD 3. DIVERSIDAD DE LA MATERIA 1. La materia: sustancias puras y mezclas La principal clasificación que se hace de la materia es en sustancias puras y mezclas. Las sustancias puras tienen
RESUMEN de la UNIDAD 3. DIVERSIDAD DE LA MATERIA 1. La materia: sustancias puras y mezclas La principal clasificación que se hace de la materia es en sustancias puras y mezclas. Las sustancias puras tienen
Disoluciones y cálculos de concentraciones
 Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas:
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas: Plomo ; acero ; mercurio ; óxido de hierro
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas: Plomo ; acero ; mercurio ; óxido de hierro
Sistemas materiales. Materia. Propiedades. Sólido Líquido Gaseoso Generales Epecíficas. Homogéneas o Disoluciones. Heterogéneas
 Sistemas materiales Materia Propiedades Sólido Líquido Gaseoso Generales Epecíficas Mezclas Sustancias puras Heterogéneas Homogéneas o Disoluciones Elementos Compuestos físicos químicos químicos Decantación
Sistemas materiales Materia Propiedades Sólido Líquido Gaseoso Generales Epecíficas Mezclas Sustancias puras Heterogéneas Homogéneas o Disoluciones Elementos Compuestos físicos químicos químicos Decantación
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
LOS GASES Y LAS DISOLUCIONES. Departamento de Física y Química 3º ESO
 LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
oluciones del apartado «Resuelve problemas»
 S oluciones del apartado «Resuelve problemas» Pág. 1 19 Un café con azúcar es una mezcla homogénea o heterogénea? Es una disolución de sólidos (café y azúcar) en agua. 20 Un material formado por moléculas
S oluciones del apartado «Resuelve problemas» Pág. 1 19 Un café con azúcar es una mezcla homogénea o heterogénea? Es una disolución de sólidos (café y azúcar) en agua. 20 Un material formado por moléculas
CURSO 2016 / Tema 3. Sistemas. materiales. Física y química para 2º ESO. Nombre..
 CURSO 2016 / 2017 Tema 3. Sistemas materiales. Física y química para 2º ESO Nombre.. Índice general: 1. Concepto de mezcla. Tipos. 2. Las disoluciones. 3. Tipos de disoluciones. 3.1. Según el estado físico
CURSO 2016 / 2017 Tema 3. Sistemas materiales. Física y química para 2º ESO Nombre.. Índice general: 1. Concepto de mezcla. Tipos. 2. Las disoluciones. 3. Tipos de disoluciones. 3.1. Según el estado físico
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO
 ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
SOLUCIONES SOLIDA LIQUIDA GASEOSA. mezclas homogéneas de dos sustancias: SEGÚN EL ESTADO FISICO DEL SOLVENTE
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Recuperación Pendientes 2º ESO Temas 0, 1, 2 y 3. Primera parte Nombre:
 Recuperación Pendientes 2º ESO Temas 0, 1, 2 y 3. Primera parte Nombre: 1 Señala las opciones correctas: a) El conocimiento científico surge de la necesidad de dar respuesta a un problema basado en hechos
Recuperación Pendientes 2º ESO Temas 0, 1, 2 y 3. Primera parte Nombre: 1 Señala las opciones correctas: a) El conocimiento científico surge de la necesidad de dar respuesta a un problema basado en hechos
MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS
 MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS Concentración de una disolución 1º.- Calcula la masa de nitrato de hierro (II), Fe(NO 3 ) 2, existente en 100 ml de disolución acuosa al 6 % en masa. Dato:
MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS Concentración de una disolución 1º.- Calcula la masa de nitrato de hierro (II), Fe(NO 3 ) 2, existente en 100 ml de disolución acuosa al 6 % en masa. Dato:
La materia y sus propiedades
 La materia y sus propiedades Las sustancias puras simples: ELEMENTOS QUÍMICOS Los elementos químicos Algunos pueden encontrarse fácilmente en nuestro entorno Hierro (Fe) Cobre (Cu) ASPECTO HOMOGÉNEO Oxígeno
La materia y sus propiedades Las sustancias puras simples: ELEMENTOS QUÍMICOS Los elementos químicos Algunos pueden encontrarse fácilmente en nuestro entorno Hierro (Fe) Cobre (Cu) ASPECTO HOMOGÉNEO Oxígeno
FICHA 5: DISOLUCIONES %masa y % volumen
 FICHA 5: DISOLUCIONES %masa y % volumen 1. Calcula el % en masa de una disolución que contiene 30 g de soluto en 1 L de agua. Sol.: 2,9% 2. El vinagre es una disolución de ácido acético en agua al 3% en
FICHA 5: DISOLUCIONES %masa y % volumen 1. Calcula el % en masa de una disolución que contiene 30 g de soluto en 1 L de agua. Sol.: 2,9% 2. El vinagre es una disolución de ácido acético en agua al 3% en
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
TEMA 13: LA MATERIA, BASE DEL UNIVERSO
 TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
DIVERSIDAD DE LA MATERIA TEMA 3
 DIVERSIDAD DE LA MATERIA TEMA 3 Cómo se presenta la materia Sistema homogéneos Sistemas materiales que tienen el mismo aspecto en cualquiera de sus partes. Ejemplo: agua, leche, gelatina Sistemas heterogéneos
DIVERSIDAD DE LA MATERIA TEMA 3 Cómo se presenta la materia Sistema homogéneos Sistemas materiales que tienen el mismo aspecto en cualquiera de sus partes. Ejemplo: agua, leche, gelatina Sistemas heterogéneos
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración SGUICES010CB33-A16V1 Ítem Alternativa Habilidad 1 D Reconocimiento 2 A Reconocimiento 3 C
SOLUCIONARIO Guía Estándar Anual Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración SGUICES010CB33-A16V1 Ítem Alternativa Habilidad 1 D Reconocimiento 2 A Reconocimiento 3 C
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 1) CURSO 2011/12 Nombre y apellidos: LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES 1. A qué es igual 1 kg? a) 10 t b) 1000 t c) 1000 g d) 0,001
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 1) CURSO 2011/12 Nombre y apellidos: LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES 1. A qué es igual 1 kg? a) 10 t b) 1000 t c) 1000 g d) 0,001
Universidad de La Frontera Fac. Ing.Cs. y Adm. Dpto. Cs. Químicas. Soluciones. Prof. Josefina Canales
 Universidad de La Frontera Fac. Ing.Cs. y Adm. Dpto. Cs. Químicas Soluciones Prof. Josefina Canales Una disolución es una mezcla homogénea de dos o más sustancias. Soluto El más pequeño (en masa) de los
Universidad de La Frontera Fac. Ing.Cs. y Adm. Dpto. Cs. Químicas Soluciones Prof. Josefina Canales Una disolución es una mezcla homogénea de dos o más sustancias. Soluto El más pequeño (en masa) de los
UNIDAD II. Transformaciones de la materia. Tema 2: Clasificación de la materia.
 UNIDAD II. Transformaciones de la materia. Tema 2: Clasificación de la materia. Qué es materia? Es todo lo que tiene masa y volumen. CLASIFICACIÓN DE LA MATERIA: Según: A. Estado de agregación. B. Composición.
UNIDAD II. Transformaciones de la materia. Tema 2: Clasificación de la materia. Qué es materia? Es todo lo que tiene masa y volumen. CLASIFICACIÓN DE LA MATERIA: Según: A. Estado de agregación. B. Composición.
IES ALONSO QUESADA Física y Química 3º ESO Trabajo Científico. Estados de la materia. Clasificación de la materia.
 IES ALONSO QUESADA Física y Química 3º ESO Trabajo Científico. Estados de la materia. Clasificación de la materia. 1) Contesta las siguientes preguntas: a - Cuáles son los pasos del método científico?.
IES ALONSO QUESADA Física y Química 3º ESO Trabajo Científico. Estados de la materia. Clasificación de la materia. 1) Contesta las siguientes preguntas: a - Cuáles son los pasos del método científico?.
III MINIOLIMPIADA DE QUÍMICA DE CANTABRIA CUESTIONARIO TIPO TEST (Parte I) 5 de mayo de 2017
 Sección Territorial de Cantabria de la III MINIOLIMPIADA DE QUÍMICA DE CANTABRIA CUESTIONARIO TIPO TEST (Parte I) 5 de mayo de 2017 Nombre y apellidos: Conteste en la Hoja de Respuestas. Sólo hay una respuesta
Sección Territorial de Cantabria de la III MINIOLIMPIADA DE QUÍMICA DE CANTABRIA CUESTIONARIO TIPO TEST (Parte I) 5 de mayo de 2017 Nombre y apellidos: Conteste en la Hoja de Respuestas. Sólo hay una respuesta
TEMA 2: Diversidad de la materia. T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1
 TEMA 2: Diversidad de la materia T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1 ESQUEMA DE LA UNIDAD 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.-
TEMA 2: Diversidad de la materia T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1 ESQUEMA DE LA UNIDAD 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.-
Materia: FÍSICA Y QUÍMICA 3º E.S.O Curso
 ACTIVIDADES FÍSICA Y QUÍMICA 3º ESO PROGRAMA DE REFUERZO. PRIMERA PARTE 1.-Calcular el tanto por ciento en peso y en volumen de una disolución que se prepara al disolver 40 ml de ácido nítrico cuya densidad
ACTIVIDADES FÍSICA Y QUÍMICA 3º ESO PROGRAMA DE REFUERZO. PRIMERA PARTE 1.-Calcular el tanto por ciento en peso y en volumen de una disolución que se prepara al disolver 40 ml de ácido nítrico cuya densidad
INTRUCCIONES PARA LA RECUPERACIÓN
 INTRUCCIONES PARA LA RECUPERACIÓN Se entrega una relación de actividades. Dichas actividades deberán ser entregadas antes de la fecha límite de entrega, pudiéndose ser consultado el profesor cuantas veces
INTRUCCIONES PARA LA RECUPERACIÓN Se entrega una relación de actividades. Dichas actividades deberán ser entregadas antes de la fecha límite de entrega, pudiéndose ser consultado el profesor cuantas veces
2. LOS ESTADOS DE LA MATERIA. Nuria Montiel Guardiola - 1 -
 1. LA MATERIA La materia es todo aquello que existe, tiene masa y ocupa lugar en un espacio. Las cosas materiales se pueden medir y contar y las cosas inmateriales no. 2. LOS ESTADOS DE LA MATERIA Nuria
1. LA MATERIA La materia es todo aquello que existe, tiene masa y ocupa lugar en un espacio. Las cosas materiales se pueden medir y contar y las cosas inmateriales no. 2. LOS ESTADOS DE LA MATERIA Nuria
El aire de la atmósfera (78% N 2 ; 21% O 2 ; 1% Ar, He, CO 2 y vapor de agua) y el agua del mar son ejemplos de soluciones.
 SOLUCIONES la materia se presenta, con mayor frecuencia, en forma de mezcla de sustancias puras. dentro de éstas mezclas hay que distinguir las: I) mezclas propiamente dichas II) y las soluciones. El aire
SOLUCIONES la materia se presenta, con mayor frecuencia, en forma de mezcla de sustancias puras. dentro de éstas mezclas hay que distinguir las: I) mezclas propiamente dichas II) y las soluciones. El aire
TEMA 4.- LA MATERIA QUE NOS RODEA
 TEMA 4.- LA MATERIA QUE NOS RODEA MATERIA Y SUSTANCIA Módulo 2 La MATERIA está formada por átomos y moléculas Tiene masa y volumen Llamamos SUSTANCIA a cada una de las distintas formas de materia CUERPOS
TEMA 4.- LA MATERIA QUE NOS RODEA MATERIA Y SUSTANCIA Módulo 2 La MATERIA está formada por átomos y moléculas Tiene masa y volumen Llamamos SUSTANCIA a cada una de las distintas formas de materia CUERPOS
SOLUCIONES EJERCICIOS DE QUÍMICA. 1ºBCT. TEMAS 2 Y 3
 SOLUCIONES EJERCICIOS DE QUÍMICA. 1ºBCT. TEMAS 2 Y 3 1. Como la presión se mantiene constante utilizamos la Ley de Charles y Gay Lussac que dice que a presión constante el volumen que ocupa un gas es proporcional
SOLUCIONES EJERCICIOS DE QUÍMICA. 1ºBCT. TEMAS 2 Y 3 1. Como la presión se mantiene constante utilizamos la Ley de Charles y Gay Lussac que dice que a presión constante el volumen que ocupa un gas es proporcional
CLASIFICACIONES DE LA MATERIA. Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia.
 CLASIFICACIONES DE LA MATERIA Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia. LA MATERIA Es todo aquello que ocupa un sitio en el espacio, se puede tocar,
CLASIFICACIONES DE LA MATERIA Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia. LA MATERIA Es todo aquello que ocupa un sitio en el espacio, se puede tocar,
1º ESO IES MURIEDAS Bonifacio San Millán
 1º ESO IES MURIEDAS Bonifacio San Millán En las mezclas se aprecia, a simple vista, que están formadas por varios componentes En las mezclas NO se aprecia, a simple vista, que están formadas por varios
1º ESO IES MURIEDAS Bonifacio San Millán En las mezclas se aprecia, a simple vista, que están formadas por varios componentes En las mezclas NO se aprecia, a simple vista, que están formadas por varios
1 Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es:
 IES Menéndez Tolosa 3º ESO (Física y Química) Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es: ( ) %peso = masade + masade 00 Completar las definiciones:
IES Menéndez Tolosa 3º ESO (Física y Química) Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es: ( ) %peso = masade + masade 00 Completar las definiciones:
DISOLUCIONES 1.- QUÉ ES UNA DISOLUCIÓN?
 DISOLUCIONES 1.- QUÉ ES UNA DISOLUCIÓN? Disoluciones, en química, mezclas homogéneas de dos o más sustancias. El soluto es el componente que se encuentra en distinto estado físico que la disolución; y
DISOLUCIONES 1.- QUÉ ES UNA DISOLUCIÓN? Disoluciones, en química, mezclas homogéneas de dos o más sustancias. El soluto es el componente que se encuentra en distinto estado físico que la disolución; y
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia. Sistemas materiales Sustancias puras Mezclas Un solo componente Dos o mas componentes Simples Compuestas Homogénas Heterogénas Un solo tipo de átomo.
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia. Sistemas materiales Sustancias puras Mezclas Un solo componente Dos o mas componentes Simples Compuestas Homogénas Heterogénas Un solo tipo de átomo.
COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10
 COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10 NOTA: ALGUNAS DE LAS PREGUNTAS PRESENTES EN ESTE CUESTIONARIO SON PREGUNTAS LIBERADAS POR EL ICFES ENTRE LOS AÑOS DE 2009 A 2011. Como
COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10 NOTA: ALGUNAS DE LAS PREGUNTAS PRESENTES EN ESTE CUESTIONARIO SON PREGUNTAS LIBERADAS POR EL ICFES ENTRE LOS AÑOS DE 2009 A 2011. Como
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA
 FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
