FICHA TÉCNICA. Calcipotriol/Betametasona Teva 50 microgramos/g + 0,5 mg/g pomada
|
|
|
- Aarón Mora Pérez
- hace 6 años
- Vistas:
Transcripción
1 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Calcipotriol/Betametasona Teva 50 microgramos/g + 0,5 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50 microgramos de calcipotriol (anhidro) y 0,5 mg de betametasona (como 0,643 mg betametasona dipropionato). Excipientes con efecto conocido: Un gramo de pomada contiene 50 microgramos de butilhidroxitolueno (E321) Para consultar la lista completa de excipientes, ver sección FORMA FARMACÉUTICA Pomada. De blanquecina a amarilla. 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Tratamiento tópico de la psoriasis vulgaris estable en placas susceptible al tratamiento tópico en adultos. 4.2 Posología y forma de administración Posología Calcipotriol/Betametasona Teva 50 microgramos/g + 0,5 mg/g pomada debe aplicarse sobre el área afectada una vez al día. El periodo de tratamiento recomendado es de 4 semanas. Existe experiencia con tratamientos repetidos de hasta 52 semanas con Calcipotriol/Betametasona. Si es necesario continuar o reiniciar el tratamiento pasadas las 4 semanas, el tratamiento debe continuar tras evaluación médica y bajo supervisión médica periódica. Cuando se emplean medicamentos que contienen calcipotriol, la dosis máxima diaria no debe exceder los 15 g. El área de superficie corporal tratada con medicamentos que contienen calcipotriol no debe ser superior al 30 % (ver sección 4.4). Poblaciones especiales Insuficiencia renal y hepática No se ha evaluado la seguridad y eficacia de Calcipotriol/Betametasona pomada en pacientes con insuficiencia renal grave o trastornos hepáticos graves. Población pediátrica No se ha establecido la seguridad y eficacia de Calcipotriol/Betametasona pomada en niños menores de 18 años. Los datos actualmente disponibles en niños de 12 a 17 años se describen en las secciones 4.8 y 5.1, pero no puede hacerse ninguna recomendación posológica. 1 de 8
2 Forma de administración Calcipotriol/Betametasona pomada debe aplicarse en el área afectada. Con el fin de conseguir un efecto óptimo, no se recomienda ducharse o bañarse inmediatamente después de la aplicación de Calcipotriol/Betametasona pomada. 4.3 Contraindicaciones Hipersensibilidad a los principios activos o a alguno de los excipientes incluidos en la sección 6.1. Calcipotriol/Betametasona pomada está contraindicado en psoriasis eritrodérmica, exfoliativa y pustular. Debido al contenido en calcipotriol, Calcipotriol/Betametasona pomada está contraindicado en pacientes con trastornos conocidos del metabolismo del calcio. Debido al contenido en corticosteroide, Calcipotriol/Betametasona pomada está contraindicado en las siguientes situaciones: lesiones víricas de la piel (por ejemplo herpes o varicela), infecciones fúngicas o bacterianas de la piel, infecciones parasitarias, manifestaciones cutáneas relacionadas con tuberculosis o sífilis, dermatitis perioral, piel atrófica, estrías atróficas, fragilidad de las venas de la piel, ictiosis, acné vulgaris, acné rosácea, rosácea, úlceras, heridas, prurito perianal y genital. 4.4 Advertencias y precauciones especiales de empleo Efectos sobre el sistema endocrino Calcipotriol/Betametasona pomada contiene un potente esteroide del grupo III y debe evitarse el tratamiento concomitante con otros esteroides. Las reacciones adversas debidas al tratamiento sistémico con corticosteroides, tales como la supresión adrenocortical o el impacto sobre el control metabólico de la diabetes mellitus pueden ocurrir también durante el tratamiento tópico con corticosteroides debido a la absorción sistémica. Debe evitarse la aplicación bajo vendaje oclusivo puesto que esto incrementa la absorción sistémica de los corticosteroides. Debe evitarse la aplicación en zonas extensas de piel dañada y bajo vendajes oclusivos, en membranas mucosas o en pliegues cutáneos puesto que esto incrementa la absorción sistémica de los corticosteroides (ver sección 4.8). En un estudio llevado a cabo en pacientes con psoriasis extensa en el cuero cabelludo y en el cuerpo, en el que se usaron dosis altas de calcipotriol/betametasona gel (aplicación en el cuero cabelludo) y dosis altas de calcipotriol/betametasona pomada (aplicación en el cuerpo), 5 de 32 pacientes mostraron un descenso en el límite de la respuesta del cortisol al estímulo de la hormona adrenocorticotrópica (ACTH) después de 4 semanas de tratamiento (ver sección 5.1). Efectos sobre el metabolismo del calcio Debido al contenido en calcipotriol, puede producirse hipercalcemia si se supera la dosis máxima diaria (15 g). Sin embargo, el calcio sérico se normaliza rápidamente cuando el tratamiento se interrumpe. El riesgo de hipercalcemia es mínimo cuando se siguen las recomendaciones referentes a calcipotriol. Debe evitarse el tratamiento de más del 30 % de la superficie corporal (ver sección 4.2). Reacciones adversas locales La piel de la cara y los genitales es muy sensible a los corticosteroides. El medicamento no debe usarse en esas áreas. Debe instruirse al paciente para un correcto uso del medicamento con el fin de evitar la aplicación y contacto accidental con la cara, boca y ojos. Deben lavarse las manos después de cada aplicación para evitar el contacto accidental con esas áreas. Infecciones concomitantes de la piel Cuando las lesiones se infectan secundariamente, éstas deben tratarse con antimicrobianos. Sin embargo, si la infección empeora, debe interrumpirse el tratamiento con corticosteroides. Interrupción del tratamiento 2 de 8
3 Cuando se trata la psoriasis con corticosteroides tópicos, puede existir riesgo de producirse una psoriasis pustular generalizada o efectos rebote cuando se interrumpe el tratamiento. Por tanto, debe continuar la supervisión médica durante el periodo post-tratamiento. Empleo a largo plazo Con el empleo a largo plazo existe un mayor riesgo de reacciones adversas corticosteroideas locales y sistémicas. El tratamiento debe interrumpirse en caso de reacciones adversas relacionadas con el empleo a largo plazo del corticosteroide (ver sección 4.8). Usos no evaluados No hay experiencia con el empleo de calcipotriol/betametasona pomada en psoriasis guttata. Tratamiento concomitante y exposición UV No hay experiencia con el empleo de este medicamento en el cuero cabelludo. Calcipotriol/Betametasona pomada para lesiones de psoriasis en el cuerpo se ha empleado en combinación con calcipotriol/betametasona gel para lesiones de psoriasis en el cuero cabelludo, pero no existe experiencia de la combinación de calcipotriol/betametasona con otros productos antipsoriásicos tópicos en la misma zona de tratamiento, otros medicamentos antipsoriásicos admisnistrados sistémicamente o con fototerapia. Durante el tratamiento con calcipotriol/betametasona pomada, se recomienda que los médicos aconsejen a los pacientes que limiten o eviten la exposición excesiva a la luz natural o artificial. Únicamente debe emplearse calcipotriol tópico con radiación UV si el médico y el paciente consideran que los beneficios potenciales superan a los riesgos potenciales (ver sección 5.3). Calcipotriol/betametasona pomada contiene butilhidroxitolueno (E321). Éste puede producir reacciones locales en la piel (como dermatitis de contacto), o irritación de los ojos y membranas mucosas. 4.5 Interacción con otros medicamentos y otras formas de interacción No se han realizado estudios de interacciones. 4.6 Fertilidad, embarazo y lactancia Embarazo No existen datos suficientes sobre el uso de calcipotriol/betametasona pomada en mujeres embarazadas. Estudios en animales con glucocorticoides han mostrado toxicidad reproductiva (ver sección 5.3), pero un número de estudios epidemiológicos no han revelado anomalías congénitas entre los recién nacidos de mujeres tratadas con corticosteroides durante el embarazo. Se desconoce el riesgo potencial en humanos. Por tanto, durante el embarazo, únicamente debe emplearse calcipotriol/betametasona pomada cuando el beneficio potencial justifique el riesgo potencial. Lactancia Betametasona se excreta en leche materna, pero el riesgo de un efecto adverso en el lactante parece improbable con dosis terapéuticas. No existen datos sobre la excreción de calcipotriol en leche materna. Se debe tener precaución al prescribir calcipotriol/betametasona pomada a mujeres en periodo de lactancia. Debe instruirse a la paciente para que no use calcipotriol/betametasona pomada en el pecho durante la lactancia. Fertilidad Los estudios realizados en ratas con dosis orales de calcipotriol o betametasona dipropionato no han demostrado alteraciones en la fertilidad de machos y hembras. 4.7 Efectos sobre la capacidad para conducir y utilizar máquinas La influencia de Calcipotriol/Betametasona sobre la capacidad para conducir y utilizar máquinas es nula o insignificante. 3 de 8
4 4.8 Reacciones adversas El programa de ensayos clínicos para calcipotriol/betametasona pomada ha incluido a más de pacientes y ha mostrado que puede esperarse que aproximadamente el 10 % de los pacientes experimenten una reacción adversa no grave. Estas reacciones adversas son normalmente leves y abarcan principalmente diversas reacciones cutáneas como erupción, prurito y sensación de quemazón. Raramente se ha notificado psoriasis pustular. Se ha notificado efecto rebote tras la finalización del tratamiento, pero su frecuencia es no conocida. En base a los resultados de los ensayos clínicos y el empleo post-comercialización se enumeran a continuación las reacciones adversas para calcipotriol/betametasona pomada. Las reacciones adversas se enumeran según la Clasificación de Órganos y Sistemas de MedDRA, enumerándose las reacciones adversas individuales empezando por las más frecuentemente notificadas. Dentro de cada grupo de frecuencia, las reacciones adversas se enumeran en orden decreciente de gravedad. Se ha empleado la siguiente terminología con el fin de clasificar las frecuencias de las reacciones adversas: Muy frecuentes > 1/10 Frecuentes >1/100 a <1/10 Poco frecuentes > 1/1.000 a <1/100 Raras > 1/ a <1/1.000 Muy raras < 1/ Frecuencia no conocida (no puede estimarse a partir de los datos disponibles) Trastornos de la piel y del tejido subcutáneo Frecuentes Poco frecuentes Raras Prurito Erupción Sensación de quemazón de la piel Exacerbación de la psoriasis Irritación o dolor de la piel Dermatitis Eritema Foliculitis Cambios de pigmentación en el lugar de aplicación Psoriasis pustular Trastornos generales y alteraciones en el lugar de administración Frecuencia no conocida Efecto rebote ver sección 4.4 Las siguientes reacciones adversas se consideran relacionadas con los grupos farmacológicos de calcipotriol y betametasona, respectivamente: Calcipotriol Las reacciones adversas incluyen reacciones en el lugar de aplicación, prurito, irritación cutánea, sensación de quemazón y picor, piel seca, eritema, rash, dermatitis, eczema, empeoramiento de la psoriasis, fotosensibilidad e hipersensibilidad incluyendo casos raros de angioedema y edema facial. 4 de 8
5 En muy raras ocasiones pueden aparecer efectos sistémicos después del uso tópico causando hipercalcemia o hipercalciuria (ver sección 4.4). Betametasona (como dipropionato) Pueden producirse reacciones locales tras el uso tópico, especialmente durante tratamientos prolongados, incluyendo atrofia cutánea, telangiectasia, estrías, foliculitis, hipertricosis, dermatitis perioral, dermatitis alérgica de contacto, despigmentación y coloide miliar. Cuando se trata la psoriasis, puede existir un riesgo de psoriasis pustular generalizada. Las reacciones sistémicas debidas a la administración tópica de corticosteroides son raras en adultos, sin embargo, pueden ser graves. Puede producirse supresión adrenocortical, cataratas, infecciones, efecto sobre el control metabólico de la diabetes mellitus e incremento de la presión intraocular, especialmente tras un tratamiento a largo plazo. Las reacciones sistémicas se producen con mayor frecuencia cuando se aplica bajo oclusión (plástico, pliegues cutáneos), cuando se aplica en zonas extensas y durante tratamientos a largo plazo (ver sección 4.4). Población pediátrica En un estudio abierto no controlado, 33 adolescentes de entre años con psoriasis vulgaris fueron tratados con Calcipotriol/Betametasona pomada durante 4 semanas con un máximo de 56 g a la semana. No se observaron nuevos acontecimientos adversos ni se identificaron complicaciones relacionadas con el efecto corticosteroideo sistémico. Sin embargo, el tamaño del estudio no permite obtener conclusiones firmes relativas al perfil de seguridad de Calcipotriol/Betametasona pomada en niños y adolescentes. Notificación de sospecha de reacciones adversas: Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano Website: Sobredosis El empleo de dosis superiores a la recomendada puede ocasionar una elevación del calcio sérico, el cual se normaliza rápidamente cuando se interrumpe el tratamiento. El uso prolongado excesivo de corticosteroides tópicos puede suprimir las funciones pituitaria- adrenal dando lugar a insuficiencia adrenal secundaria, que habitualmente es reversible. En tales casos, está indicado el tratamiento sintomático. En caso de toxicidad crónica, el tratamiento corticosteroide debe interrumpirse gradualmente. Se ha notificado que debido a un mal uso, un paciente con psoriasis eritrodérmica extensa tratado con 240 g de Calcipotriol/Betametasona pomada a la semana (correspondiente a una dosis diaria de aproximadamente 34 g) durante 5 meses (dosis máxima diaria recomendada de 15 g), desarrolló síndrome de Cushing y psoriasis pustular tras la interrupción brusca del tratamiento. 5. PROPIEDADES FARMACOLÓGICAS 5.1 Propiedades farmacodinámicas Grupo farmacoterapéutico: Antipsoriásicos. Otros antipsoriásicos para uso tópico. Calcipotriol, combinaciones. Código ATC: D05AX52 5 de 8
6 Calcipotriol es un análogo de la vitamina D. Los resultados in vitro sugieren que calcipotriol induce la diferenciación e inhibe la proliferación de los queratinocitos. Esta es la base propuesta para su efecto en la psoriasis. Como otros corticosteroides tópicos, betametasona dipropionato tiene propiedades antiinflamatorias, antipruriginosas, vasoconstrictoras e inmunosupresoras, sin curar, sin embargo, la enfermedad subyacente. Mediante oclusión puede incrementarse el efecto, debido a una mayor penetración en el estrato córneo. La incidencia de reacciones adversas incrementará a causa de ello. El mecanismo de la actividad antiinflamatoria de los esteroides tópicos es, en general, incierto. En un estudio de seguridad, llevado a cabo en 634 pacientes con psoriasis, se ha estudiado el empleo de tratamientos repetidos de calcipotriol/betametasona pomada administrado una vez al día, en caso necesario, sólo o alternando con Calcipotriol pomada, durante 52 semanas, comparado con el empleo de Calcipotriol pomada durante 48 semanas tras un tratamiento inicial con calcipotriol/betametasona pomada. Notificaron reacciones adversas un 21,7 % de los pacientes del grupo tratado con calcipotriol/betametasona pomada, un 29,6 % de los pacientes del grupo tratado alternativamente con calcipotriol/betametasona pomada/ Calcipotriol y un 37,9 % de los pacientes del grupo tratado con Calcipotriol. Las reacciones adversas notificadas por más del 2 % de los pacientes tratados con calcipotriol/betametasona pomada fueron prurito (5,8 %) y psoriasis (5,3 %). Notificaron acontecimientos adversos posiblemente relacionados con el empleo a largo plazo de un corticosteroide (por ejemplo, atrofia cutánea, foliculitis, despigmentación, furúnculos y púrpura) un 4,8 % de los pacientes del grupo calcipotriol/betametasona pomada, un 2,8 % del grupo tratado de forma alternativa con calcipotriol/betametasona pomada/ Calcipotriol y un 2,9 % del grupo tratado con Calcipotriol. Se determinó la respuesta adrenal a la ACTH mediante la medida de los niveles séricos de cortisol en pacientes con psoriasis extensa en cuero cabelludo y cuerpo, empleando hasta 106 g por semana combinando calcipotriol/betametasona gel y calcipotriol/betametasona pomada. Se observó un descenso en el límite de la respuesta del cortisol al estímulo con ACTH a los 30 minutos, en 5 de 32 pacientes (15,6 %) tras 4 semanas de tratamiento y en 2 de 11 pacientes (18,2 %) que fueron tratados durante 8 semanas. En todos los casos, los niveles séricos de cortisol fueron normales a los 60 minutos del estímulo con ACTH. En estos pacientes no se evidenció cambio en el metabolismo del calcio. Por tanto, respecto a la supresión del HPA, este estudio muestra cierta evidencia de que dosis muy elevadas de calcipotriol/betametasona gel y pomada pueden tener un débil efecto sobre el eje HPA. Población pediátrica Se determinó la respuesta adrenal al estímulo con ACTH en un estudio no controlado de 4 semanas, en 33 adolescentes de 12 a 17 años con psoriasis en el cuerpo, que emplearon hasta 56 g de Calcipotriol/Betametasona pomada a la semana. No se notificaron casos de supresión del eje HPA. No se notificó hipercalcemia, pero un paciente experimentó un incremento de calcio en orina posiblemente relacionado con el tratamiento. 5.2 Propiedades farmacocinéticas Los ensayos clínicos llevados a cabo con pomada marcada radiactivamente indican que la absorción sistémica de calcipotriol y betametasona a partir de la formulación de Calcipotriol/Betametasona pomada es inferior al 1 % de la dosis (2,5 g) cuando se aplica sobre piel normal (625 cm 2 ) durante 12 horas. La aplicación en placas psoriásicas y bajo vendaje oclusivo puede incrementar la absorción de los corticosteroides tópicos. La absorción a través de piel dañada es aproximadamente del 24 %. Tras la exposición sistémica, ambas sustancias activas calcipotriol y betametasona dipropionato se metabolizan de forma rápida y amplia. La unión a proteínas es aproximadamente del 64 %. La vida media de eliminación plasmática tras administración intravenosa es de 5-6 horas. Debido a la formación de un depósito en la piel, la eliminación tras aplicación cutánea es del orden de días. La betametasona se metaboliza especialmente en hígado, pero también en los riñones a glucurónido y ésteres de sulfato. Calcipotriol se excreta principalmente en heces (ratas y cerdos enanos) y betametasona dipropionato en 6 de 8
7 orina (ratas y ratones). En ratas, los estudios de distribución tisular llevados a cabo con calciporiol y betametasona dipropionato marcados radiactivamente, respectivamente, mostraron que el mayor nivel de radiactividad se encontraba en hígado y riñones. Calcipotriol y betametasona dipropionato estuvieron por debajo del límite inferior de cuantificación en todas las muestras de sangre de 34 pacientes tratados durante 4 u 8 semanas con Calcipotriol/Betametasona gel y Calcipotriol/Betametasona pomada para psoriasis extensa que abarcaba el cuerpo y el cuero cabelludo. En algunos pacientes se cuantificó un metabolito de calcipotriol y un metabolito de betametasona dipropionato. 5.3 Datos preclínicos sobre seguridad Los estudios con corticosteroides llevados a cabo en animales han mostrado toxicidad reproductiva (fisura palatina, malformaciones esqueléticas). Los estudios de toxicidad reproductiva con la administración oral a largo plazo de corticosteroides a ratas, evidenciaron una gestación prolongada y un parto difícil y prolongado. Además, se observó una reducción en la supervivencia de la camada, en el peso corporal y en la evolución del peso corporal. No se produjeron alteraciones de la fertilidad. Se desconoce la relevancia en humanos. Un estudio de carcinogénesis dérmica con calcipotriol llevado a cabo en ratones no mostró riesgos especiales para los seres humanos. Estudios de foto(co)carcinogénesis en ratones sugieren que calcipotriol puede incrementar el efecto de la radiación UV para inducir tumores cutáneos. No se han llevado a cabo estudios de carcinogénesis o fotocarcinogénesis con betametasona dipropionato. 6. DATOS FARMACÉUTICOS 6.1 Lista de excipientes Parafina líquida Polioxipropilén-15 estearil éter Parafina blanca suave Butilhidroxitolueno (E321) 6.2 Incompatibilidades En ausencia de estudios de compatibilidad, este medicamento no debe mezclarse con otros. 6.3 Periodo de validez 3 años Tras la primera apertura: 1 año 6.4 Precauciones especiales de conservación No conservar a temperatura superior a 25ºC. 6.5 Naturaleza y contenido del envase Tubos de aluminio con cierre de HDPE (polietileno de alta densidad). El interior del tubo está recubierto con resina epoxi fenólica. 7 de 8
8 Tamaños de tubo: 30, 60 y 120 g. Puede que solamente estén comercializados algunos tamaños de envases. 6.6 Precauciones especiales de eliminación y otras manipulaciones Ninguna especial. 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Teva Pharma, S.L.U. C/ Anabel Segura, 11. Edificio Albatros B, 1ª planta Alcobendas, Madrid España 8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN 9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN Noviembre FECHA DE LA REVISIÓN DEL TEXTO Agosto de 8
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50
Nueva propuesta de. RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO para Daivobet pomada
 15 de Septiembre de 2003 Nueva propuesta de RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO para Daivobet pomada 1. NOMBRE DEL MEDICAMENTO Daivobet pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Calcipotriol
15 de Septiembre de 2003 Nueva propuesta de RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO para Daivobet pomada 1. NOMBRE DEL MEDICAMENTO Daivobet pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Calcipotriol
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. DAIVONEX Crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DAIVONEX Crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Calcipotriol 50 microgramos/g (como hidrato). Para la lista completa de excipientes, ver sección 6.1. 3.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DAIVONEX Crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Calcipotriol 50 microgramos/g (como hidrato). Para la lista completa de excipientes, ver sección 6.1. 3.
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Prenamid 50 microgramos/g + 0,5 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Prenamid 50 microgramos/g + 0,5 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50 microgramos de calcipotriol (como monohidrato)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Prenamid 50 microgramos/g + 0,5 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50 microgramos de calcipotriol (como monohidrato)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Daivobet 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Para Daivobet pomada
 agencia española de medicamentos y productos sanitarios RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Para Daivobet pomada 1. DENOMINACIÓN DEL MEDICAMENTO Daivobet 50 microgramos/g + 0,5 mg/g pomada 2. COMPOSICIÓN
agencia española de medicamentos y productos sanitarios RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Para Daivobet pomada 1. DENOMINACIÓN DEL MEDICAMENTO Daivobet 50 microgramos/g + 0,5 mg/g pomada 2. COMPOSICIÓN
Un gramo de pomada contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona (como dipropionato).
 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona
1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona
FICHA TÉCNICA. No exceder la dosis máxima de 480 mg de simeticona (4 comprimidos masticables) al día.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 120 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona.. 120 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 120 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona.. 120 mg Excipientes con efecto conocido:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Enstilar 50 microgramos/g + 0,5 mg/g espuma cutánea. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de espuma cutánea contiene
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Enstilar 50 microgramos/g + 0,5 mg/g espuma cutánea. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de espuma cutánea contiene
Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona (como dipropionato).
 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/g + 0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona
1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/g + 0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona
FICHA TÉCNICA. - Hipersensibilidad conocida al principio activo o a cualquiera de los excipientes. - Rosácea. - Acné vulgar. - Dermatitis perioral.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Declobán 500 microgramos/g pomada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 500 microgramos de propionato de clobetasol 500 microgramos
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Declobán 500 microgramos/g pomada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 500 microgramos de propionato de clobetasol 500 microgramos
Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona (como dipropionato).
 1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona
1. NOMBRE DEL MEDICAMENTO Daivobet 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona
FICHA TÉCNICA. 3. FORMA FARMACÉUTICA Solución cutánea. Solución incolora, transparente ó ligeramente traslúcida y ligeramente viscosa.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Clobisdin 500 microgramos/ml solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución cutánea contiene 500 microgramos de clobetasol propionato
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Clobisdin 500 microgramos/ml solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución cutánea contiene 500 microgramos de clobetasol propionato
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO Xamiol 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona
1. NOMBRE DEL MEDICAMENTO Xamiol 50 microgramos/0,5 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel contiene 50 microgramos de calcipotriol (como monohidrato) y 0,5 mg de betametasona
Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol.
 1. NOMBRE DEL MEDICAMENTO TROSID 280 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol. Para consultar la
1. NOMBRE DEL MEDICAMENTO TROSID 280 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol. Para consultar la
FICHA TÉCNICA. El tratamiento debe comenzarse lo antes posible tras el primer signo de infección.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Fenivir 10 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 10 mg de penciclovir. Excipientes con efecto conocido: alcohol cetoestearílico
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Fenivir 10 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 10 mg de penciclovir. Excipientes con efecto conocido: alcohol cetoestearílico
FICHA TÉCNICA. Cada gramo de crema contiene 100 mg de docosanol. Excipiente con efecto conocido: 50 mg propilenglicol/gramo de crema.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Erazaban 100 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 100 mg de docosanol. Excipiente con efecto conocido: 50 mg propilenglicol/gramo
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Erazaban 100 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 100 mg de docosanol. Excipiente con efecto conocido: 50 mg propilenglicol/gramo
FICHA TÉCNICA. Cada pastilla para chupar contiene 1,2 mg de alcohol 2,4-diclorobencílico y 0,6 mg de amilmetacresol.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Strepsils pastillas para chupar sabor miel y limón 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Cada pastilla para chupar contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Strepsils pastillas para chupar sabor miel y limón 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Cada pastilla para chupar contiene
FICHA TÉCNICA. Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Oculotect 50 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 50 mg de povidona K25. Para consultar la lista
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Oculotect 50 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 50 mg de povidona K25. Para consultar la lista
FICHA TÉCNICA. Excipientes con efecto conocido 1,38 g de sacarosa y 1,10 g glucosa. Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
FICHA TÉCNICA. Excipientes con efecto conocido: 0,458 g de maltitol líquido (E965) y 1,830 g de isomalta (E953).
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
FICHA TÉCNICA. El tratamiento de las enfermedades de ojo seco requiere un régimen individualizado de dosificación.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lipolac 2 mg/g gel oftálmico 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de gel oftálmico contiene 2 mg de carbómero. Para consultar la lista completa de excipientes,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lipolac 2 mg/g gel oftálmico 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de gel oftálmico contiene 2 mg de carbómero. Para consultar la lista completa de excipientes,
Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO bucomax pastillas para chupar sabor menta bucomax pastillas para chupar sabor fresa bucomax pastillas para chupar sabor miel y limón 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
1. NOMBRE DEL MEDICAMENTO bucomax pastillas para chupar sabor menta bucomax pastillas para chupar sabor fresa bucomax pastillas para chupar sabor miel y limón 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. Adultos y adolescentes mayores de 12 años: de 250 a 500 mg al día distribuidos en dos tomas (mañana y noche)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Cada gramo de pomada bucal contiene:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada bucal contiene: Carbenoxolona disódica. 20 mg Excipientes: Para consultar
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada bucal contiene: Carbenoxolona disódica. 20 mg Excipientes: Para consultar
FICHA TÉCNICA. Población pediátrica No se ha establecido la seguridad y eficacia de Sebiprox en niños menores de 12 años. No hay datos disponibles.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Sebiprox 15 mg/g champú 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 100 g de champú contienen 1,5 g de ciclopirox olamina (15 mg/g). Contiene 0,01 mg/g de dipropilenglicol.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Sebiprox 15 mg/g champú 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 100 g de champú contienen 1,5 g de ciclopirox olamina (15 mg/g). Contiene 0,01 mg/g de dipropilenglicol.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Fenistil 1 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Fenistil 1 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de Fenistil gel contiene: dimetindeno maleato. 1 mg Excipiente(s) con efecto conocido: propilenglicol...150
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Fenistil 1 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de Fenistil gel contiene: dimetindeno maleato. 1 mg Excipiente(s) con efecto conocido: propilenglicol...150
FICHA TÉCNICA. En caso de no observarse mejoría clínica después de 4 semanas de tratamiento, se deberá comprobar que el diagnóstico es correcto.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 20 mg de ketoconazol. Excipiente con efecto conocido : cada
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 20 mg de ketoconazol. Excipiente con efecto conocido : cada
Prospecto: información para el usuario. Calcipotriol/Betametasona ratiopharm 50 microgramos/g + 0,5 mg/g pomada
 Prospecto: información para el usuario Calcipotriol/Betametasona ratiopharm 50 microgramos/g + 0,5 mg/g pomada Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: información para el usuario Calcipotriol/Betametasona ratiopharm 50 microgramos/g + 0,5 mg/g pomada Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: información para el usuario. Detramax 2,5 mg/g+ 15 mg/g pomada. Hidrocortisona / Propanocaína hidrocloruro
 Prospecto: información para el usuario Detramax 2,5 mg/g+ 15 mg/g pomada Hidrocortisona / Propanocaína hidrocloruro Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
Prospecto: información para el usuario Detramax 2,5 mg/g+ 15 mg/g pomada Hidrocortisona / Propanocaína hidrocloruro Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA. Excipiente(s) con efecto conocido: Cada gramo de crema contiene 90 mg de alcohol cetoestearílico emulsificante tipo A
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Teva 50 mg/g crema EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Aciclovir: 50 mg Excipiente(s) con efecto conocido: Cada
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Teva 50 mg/g crema EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Aciclovir: 50 mg Excipiente(s) con efecto conocido: Cada
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea
 FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FICHA TECNICA. Excipiente(s) con efecto conocido: Cada gramo de crema contiene 90 mg de alcohol cetoestearílico emulsificante tipo A
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Teva 50 mg/g crema EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Aciclovir : 50 mg Excipiente(s) con efecto conocido: Cada
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Teva 50 mg/g crema EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Aciclovir : 50 mg Excipiente(s) con efecto conocido: Cada
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Cellufresh 5 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Cellufresh 5 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. 2.1 Descripción general
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Las cápsulas son ovales, con el cuerpo y la tapa de color blanco.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Las cápsulas son ovales, con el cuerpo y la tapa de color blanco.
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Ultra Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Ultra Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TÉCNICA. Posología Administrar cuando sea necesario, o según criterio médico. Como norma general administrar:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Citrato/Lauril sulfoacetato 450 mg/ 45 mg solución rectal Citrato de sodio / Lauril sulfoacetato de sodio 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Citrato/Lauril sulfoacetato 450 mg/ 45 mg solución rectal Citrato de sodio / Lauril sulfoacetato de sodio 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por
FICHA TÉCNICA. Sorbitol líquido (no cristalizante); 1 ml de jarabe contiene 495,6 mg de sorbitol (E 420).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bisolvon Expectorante jarabe Extracto seco de hojas de hiedra 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa 1 ml de jarabe de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bisolvon Expectorante jarabe Extracto seco de hojas de hiedra 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa 1 ml de jarabe de
FICHA TÉCNICA. Normoreum 400 mg comprimidos recubiertos con película
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
FICHA TÉCNICA. Cada gramo de pomada contiene 10 mg de hidrocortisona acetato (1%).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DERMOSA HIDROCORTISONA 10 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 10 mg de hidrocortisona acetato (1%). Excipientes con
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DERMOSA HIDROCORTISONA 10 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 10 mg de hidrocortisona acetato (1%). Excipientes con
FICHA TÉCNICA. Niños menores de 1 año: no se ha establecido la seguridad y eficacia de Thrombocid Forte en niños menores de 1 año.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Thrombocid Forte 5 mg/g pomada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene: Pentosano polisulfato sódico...5 mg Excipientes: Alcohol
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Thrombocid Forte 5 mg/g pomada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene: Pentosano polisulfato sódico...5 mg Excipientes: Alcohol
FICHA TÉCNICA. En general, la duración del tratamiento no debe exceder de cuatro semanas.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lexxema 1 mg/ml solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de Lexxema solución cutánea contiene: Metilprednisolona aceponato... 1 mg (0,1%)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lexxema 1 mg/ml solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de Lexxema solución cutánea contiene: Metilprednisolona aceponato... 1 mg (0,1%)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 5,9 gramos de Macrogol 3350. Excipientes con efecto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 5,9 gramos de Macrogol 3350. Excipientes con efecto
FICHA TÉCNICA. KETOISDIN 400 mg óvulos está indicado en adultos para el tratamiento local de
 1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
FICHA TÉCNICA. Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Agua para preparaciones inyectables 1 g por
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Agua para preparaciones inyectables 1 g por
FICHA TÉCNICA. BENZAC wash 50 mg/g gel: cada gramo de gel contiene 50 miligramos de Peróxido de benzoilo.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BENZAC wash 50 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA BENZAC wash 50 mg/g gel: cada gramo de gel contiene 50 miligramos de Peróxido de benzoilo. Para
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BENZAC wash 50 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA BENZAC wash 50 mg/g gel: cada gramo de gel contiene 50 miligramos de Peróxido de benzoilo. Para
FICHA TÉCNICA. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución contiene 100 mg de simeticona. Excipientes con efecto conocido:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 100 mg/ml gotas orales en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución contiene 100 mg de simeticona. Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 100 mg/ml gotas orales en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución contiene 100 mg de simeticona. Excipientes con efecto conocido:
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Betnovate 1 mg/g solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de solución contiene: Betametasona
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Betnovate 1 mg/g solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de solución contiene: Betametasona
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Artific 3,20 mg/ml colirio en solución. Artific 3,20 mg/ml colirio en solución en envase unidosis. 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Artific 3,20 mg/ml colirio en solución. Artific 3,20 mg/ml colirio en solución en envase unidosis. 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA ADVERTENCIA TRIÁNGULO NEGRO 1. NOMBRE DEL MEDICAMENTO. Monovo 1 mg/g emulsión cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 ADVERTENCIA TRIÁNGULO NEGRO FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Monovo 1 mg/g emulsión cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Descripción general Composición cualitativa y cuantitativa Cada
ADVERTENCIA TRIÁNGULO NEGRO FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Monovo 1 mg/g emulsión cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Descripción general Composición cualitativa y cuantitativa Cada
100 g de champú contienen 1,5 g de Ciclopirox Olamina (15 mg/g) Véase la lista de excipientes en la sección 6.1.
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO CICLOPIROX OLAMINA CAPITEC 15 mg/g CHAMPÚ 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 100 g de champú contienen 1,5 g de Ciclopirox Olamina (15 mg/g) Véase la
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO CICLOPIROX OLAMINA CAPITEC 15 mg/g CHAMPÚ 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 100 g de champú contienen 1,5 g de Ciclopirox Olamina (15 mg/g) Véase la
Marca de fantasía Nombre. Dovobet 50 microgram/0,5 mg/g gel. 50 µg/g + 0,5 mg/g. Dovobet 50. microgram/g + mg/g. mg/g.
 ANEXO I RELACIÓN DE LOS NOMBRES DEL MEDICAMENTO, FORMA(S) FARMACÉUTICA(S), DOSIS, VÍA(S) DE ADMINISTRACIÓN, SOLICITANTE(S), TITULAR(ES) DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN EN LOS ESTADOS MIEMBROS 1
ANEXO I RELACIÓN DE LOS NOMBRES DEL MEDICAMENTO, FORMA(S) FARMACÉUTICA(S), DOSIS, VÍA(S) DE ADMINISTRACIÓN, SOLICITANTE(S), TITULAR(ES) DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN EN LOS ESTADOS MIEMBROS 1
Prospecto: información para el usuario. HEMORRANE 10 mg/g pomada rectal Acetato de hidrocortisona
 Prospecto: información para el usuario HEMORRANE 10 mg/g pomada rectal Acetato de hidrocortisona Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
Prospecto: información para el usuario HEMORRANE 10 mg/g pomada rectal Acetato de hidrocortisona Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
Cada ml de solución cutánea contiene 10 mg de clorhexidina digluconato. Para consultar la lista completa de excipientes, ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO Normosept 10 mg/ ml solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución cutánea contiene 10 mg de clorhexidina digluconato Para consultar la lista completa
1. NOMBRE DEL MEDICAMENTO Normosept 10 mg/ ml solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución cutánea contiene 10 mg de clorhexidina digluconato Para consultar la lista completa
FICHA TÉCNICA. Viscotears está indicado para el alivio sintomático de la irritación y la sequedad ocular en adultos.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Viscotears 2 mg/g Gel oftálmico 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel oftálmico contiene 2 mg de carbómero. Para consultar la lista completa
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Viscotears 2 mg/g Gel oftálmico 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de gel oftálmico contiene 2 mg de carbómero. Para consultar la lista completa
Ficha técnica Página 1
 1. NOMBRE DEL MEDICAMENTO: Difur 120 mg cápsulas duras. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada cápsula contiene 120 mg de extracto seco de rizoma de Polypodium leucotomos L. (DER nativo 4-6:1)
1. NOMBRE DEL MEDICAMENTO: Difur 120 mg cápsulas duras. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada cápsula contiene 120 mg de extracto seco de rizoma de Polypodium leucotomos L. (DER nativo 4-6:1)
FICHA TÉCNICA. Cada 5 ml de jarabe contienen 15 mg de clorhidrato de ambroxol (DCI)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ambroxol cinfa 15 mg/5 ml jarabe EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Cada 5 ml de jarabe contienen 15 mg de clorhidrato
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ambroxol cinfa 15 mg/5 ml jarabe EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Cada 5 ml de jarabe contienen 15 mg de clorhidrato
FICHA TÉCNICA. Supositorios incoloros semitransparentes envasados en blíster de aluminio-polietileno.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SUPOSITORIOS DE GLICERINA MICRALAX ADULTOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Supositorios incoloros semitransparentes envasados en
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SUPOSITORIOS DE GLICERINA MICRALAX ADULTOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Supositorios incoloros semitransparentes envasados en
FICHA TÉCNICA. Para consultar la lista completa de excipientes, ver sección 6.1.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Alonga 50 mg/g Gel 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene 50 mg de aciclovir. Excipientes: Cada gramo de gel contiene 0,9
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Alonga 50 mg/g Gel 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene 50 mg de aciclovir. Excipientes: Cada gramo de gel contiene 0,9
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Fucibet 20 mg/g + 1 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de crema contiene 20 mg de
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Fucibet 20 mg/g + 1 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de crema contiene 20 mg de
FICHA TÉCNICA. Cada gramo de crema de Aciclovir Sandoz 50 mg/g crema contiene 50 mg de aciclovir.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Sandoz 50 mg/g crema EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema de Aciclovir Sandoz 50 mg/g crema contiene 50 mg de aciclovir. Excipientes
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Sandoz 50 mg/g crema EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema de Aciclovir Sandoz 50 mg/g crema contiene 50 mg de aciclovir. Excipientes
Prospecto: información para el usuario. CORTISON CHEMICETINA 5 mg/g+ 10 mg/g pomada Hidrocortisona acetato/ Cloranfenicol
 Prospecto: información para el usuario CORTISON CHEMICETINA 5 mg/g+ 10 mg/g pomada Hidrocortisona acetato/ Cloranfenicol Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
Prospecto: información para el usuario CORTISON CHEMICETINA 5 mg/g+ 10 mg/g pomada Hidrocortisona acetato/ Cloranfenicol Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Bel Labial 50 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bel Labial 50 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 gramos de crema contienen 5 g de aciclovir. Excipientes: Alcohol cetoestearílico, Parahidroxibenzoato
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bel Labial 50 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 gramos de crema contienen 5 g de aciclovir. Excipientes: Alcohol cetoestearílico, Parahidroxibenzoato
FICHA TÉCNICA. Azelastina hidrocloruro al 0,05% (0,5 mg/ml). Cada gota contiene 0,015 mg de azelastina hidrocloruro
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Azelastina MABO 0,5 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Azelastina hidrocloruro al 0,05% (0,5
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Azelastina MABO 0,5 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Azelastina hidrocloruro al 0,05% (0,5
FICHA TÉCNICA. Pomada untuosa, de consistencia espesa semisólida y de color blanquecino.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VapoRub pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50 mg de alcanfor, 50 mg de esencia de trementina, 27,5 mg de mentol, 15 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VapoRub pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de pomada contiene 50 mg de alcanfor, 50 mg de esencia de trementina, 27,5 mg de mentol, 15 mg
Prospecto: información para el usuario. Menaderm Neomicina 0,25 mg/ 7,2 mg/ g crema Beclometasona dipropionato/ Neomicina (sulfato)
 Prospecto: información para el usuario Menaderm Neomicina 0,25 mg/ 7,2 mg/ g crema Beclometasona dipropionato/ Neomicina (sulfato) Lea todo el prospecto detenidamente antes de empezar a usar este medicamento,
Prospecto: información para el usuario Menaderm Neomicina 0,25 mg/ 7,2 mg/ g crema Beclometasona dipropionato/ Neomicina (sulfato) Lea todo el prospecto detenidamente antes de empezar a usar este medicamento,
FICHA TÉCNICA. Alivio local de los síntomas ocasionados por el herpes labial, tales como: picor, escozor u hormigueo.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR SANDOZ 50 mg/g crema EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 50 mg de aciclovir. Excipientes con efecto conocido: Cada
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR SANDOZ 50 mg/g crema EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 50 mg de aciclovir. Excipientes con efecto conocido: Cada
Posología Adultos y adolescentes mayores de 12 años: administrar 30 ml (195 mg) cada 4 horas. La dosis máxima mg / 24 h.
 1. NOMBRE DEL MEDICAMENTO Frispec 6,5 mg/ ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de jarabe contiene: Guaifenesina 6,5 mg Excipientes con efecto conocido: Parahidroxibenzoato de metilo
1. NOMBRE DEL MEDICAMENTO Frispec 6,5 mg/ ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de jarabe contiene: Guaifenesina 6,5 mg Excipientes con efecto conocido: Parahidroxibenzoato de metilo
FICHA TÉCNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
 F.T. 24/11 Febrero 2001 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BETNOVATE, Crema. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 100 g de crema contienen: Betametasona (D.C.I.), (17-Valerato) 0,1 g (1
F.T. 24/11 Febrero 2001 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BETNOVATE, Crema. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 100 g de crema contienen: Betametasona (D.C.I.), (17-Valerato) 0,1 g (1
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Fucidine 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de fusidato de
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Fucidine 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de fusidato de
FICHA TÉCNICA. BENZAC gel está indicado para el tratamiento sintomático del acné vulgar moderado.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BENZAC 50 mg/g gel BENZAC 100 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA BENZAC 50 mg/g gel: cada gramo de gel contiene 50 mg de Peróxido de benzoilo BENZAC
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO BENZAC 50 mg/g gel BENZAC 100 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA BENZAC 50 mg/g gel: cada gramo de gel contiene 50 mg de Peróxido de benzoilo BENZAC
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Un gramo de crema contiene 50 mg de aciclovir y 10 mg de hidrocortisona.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Zoviduo 50mg/g y 10mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de crema contiene 50 mg de aciclovir y 10 mg de hidrocortisona.
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Zoviduo 50mg/g y 10mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de crema contiene 50 mg de aciclovir y 10 mg de hidrocortisona.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ecotam 10 mg/g crema. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ecotam 10 mg/g crema. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 10 mg de nitrato de econazol (equivalentes a 8,58 mg de econazol base).
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ecotam 10 mg/g crema. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 10 mg de nitrato de econazol (equivalentes a 8,58 mg de econazol base).
FICHA TÉCNICA. Un gramo de crema contiene 50 mg de aciclovir y 10 mg de hidrocortisona.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Zoviduo 50mg/g y 10mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de crema contiene 50 mg de aciclovir y 10 mg de hidrocortisona. Excipientes con
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Zoviduo 50mg/g y 10mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un gramo de crema contiene 50 mg de aciclovir y 10 mg de hidrocortisona. Excipientes con
Para el alivio del acné pápulo-pustuloso, leve a moderado, de la zona facial. Para el tratamiento tópico de la rosácea pápulo-pustulosa.
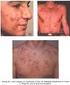 1. NOMBRE DEL MEDICAMENTO Zelaika 150 mg/g gel. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de Zelaika 150 mg/g gel contiene 150 mg de ácido azelaico (D.O.E.). Excipientes: 1 mg ácido benzoico/g gel
1. NOMBRE DEL MEDICAMENTO Zelaika 150 mg/g gel. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de Zelaika 150 mg/g gel contiene 150 mg de ácido azelaico (D.O.E.). Excipientes: 1 mg ácido benzoico/g gel
FICHA TÉCNICA. Cada gramo de pomada contiene 20 mg de mupirocina (como mupirocina cálcica).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bactroban nasal 20 mg/g pomada nasal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina (como mupirocina cálcica). Para
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bactroban nasal 20 mg/g pomada nasal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina (como mupirocina cálcica). Para
FICHA TÉCNICA. 1 g de Lexxema 1 mg/g pomada contiene 1 mg de Metilprednisolona aceponato (0,1%)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lexxema 1 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de Lexxema 1 mg/g pomada contiene 1 mg de Metilprednisolona aceponato (0,1%) Para consultar la
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lexxema 1 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de Lexxema 1 mg/g pomada contiene 1 mg de Metilprednisolona aceponato (0,1%) Para consultar la
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. CUSICROM FUERTE OFTÁLMICO 40 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO CUSICROM FUERTE OFTÁLMICO 40 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución contiene 40 mg de cromoglicato de sodio. Descripción
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO CUSICROM FUERTE OFTÁLMICO 40 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución contiene 40 mg de cromoglicato de sodio. Descripción
FICHA TÉCNICA. Afecciones agudas y crónicas de las vías respiratorias que requieran tratamiento secretolítico.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MUXIMED JARABE EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 5 ml de jarabe contiene 15 mg de ambroxol (hidrocloruro). Excipientes: ácido benzoico (E210) 10 mg,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MUXIMED JARABE EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 5 ml de jarabe contiene 15 mg de ambroxol (hidrocloruro). Excipientes: ácido benzoico (E210) 10 mg,
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 agencia española de medicamentos y productos sanitarios FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO MOMETASONA MEDE 0,1% solución cutánea EFG 2. COMPOSICIÓN CUALITATIVA
agencia española de medicamentos y productos sanitarios FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO MOMETASONA MEDE 0,1% solución cutánea EFG 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ambroxol Apotex 3 mg/ ml jarabe EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ambroxol Apotex 3 mg/ ml jarabe EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de jarabe contienen 3 mg de ambroxol hidrocloruro. Excipiente(s) con efecto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ambroxol Apotex 3 mg/ ml jarabe EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de jarabe contienen 3 mg de ambroxol hidrocloruro. Excipiente(s) con efecto
FICHA TÉCNICA. 1 ml contiene 55,74 mg de clorhidrato de amorolfina (equivalente a 50 mg de amorolfina)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Amorolfina Teva 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene 55,74 mg de clorhidrato de amorolfina (equivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Amorolfina Teva 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene 55,74 mg de clorhidrato de amorolfina (equivalente
FICHA TÉCNICA. Excipientes con efecto conocido : Alcohol estearílico 70 mg, propilenglicol 120 mg, parahidroxibenzoato de metilo 0.8 mg.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Calmiox Rectal 1 mg/g crema rectal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema rectal contiene: Hidrocortisona buteprato...1 mg Excipientes con
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Calmiox Rectal 1 mg/g crema rectal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema rectal contiene: Hidrocortisona buteprato...1 mg Excipientes con
1 NOMBRE DEL PRODUCTO Y FORMA FARMACEUTICA 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3 PARTICULARIDADES FARMACÉUTICAS
 Diprogenta Crema (Dipropionato de Betametasona - Sulfato de Gentamicina) Diprogenta 0,05% - 0,1% Ungüento (Dipropionato de Betametasona - Sulfato de Gentamicina) 1 NOMBRE DEL PRODUCTO Y FORMA FARMACEUTICA
Diprogenta Crema (Dipropionato de Betametasona - Sulfato de Gentamicina) Diprogenta 0,05% - 0,1% Ungüento (Dipropionato de Betametasona - Sulfato de Gentamicina) 1 NOMBRE DEL PRODUCTO Y FORMA FARMACEUTICA
Solubalm 0,5 mg/g mg/g crema Fluorometolona/ Urea
 Prospecto: información para el usuario Solubalm 0,5 mg/g + 100 mg/g crema Fluorometolona/ Urea Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
Prospecto: información para el usuario Solubalm 0,5 mg/g + 100 mg/g crema Fluorometolona/ Urea Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
FICHA TÉCNICA. 1 g de Lexxema 1 mg/g crema contiene 1 mg de Metilprednisolona aceponato (0,1%)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lexxema 1 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de Lexxema 1 mg/g crema contiene 1 mg de Metilprednisolona aceponato (0,1%) Excipientes con efecto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lexxema 1 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de Lexxema 1 mg/g crema contiene 1 mg de Metilprednisolona aceponato (0,1%) Excipientes con efecto
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Menaderm Simple 0,25 mg/g ungüento Beclometasona dipropionato
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Menaderm Simple 0,25 mg/g ungüento Beclometasona dipropionato Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve este prospecto,
PROSPECTO: INFORMACIÓN PARA EL USUARIO Menaderm Simple 0,25 mg/g ungüento Beclometasona dipropionato Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve este prospecto,
FICHA TÉCNICA. 1 ml de Amorolfina Mylan contiene 55,70 mg de clorhidrato de amorolfina equivalente a 50 mg de amorolfina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Amorolfina Mylan 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de Amorolfina Mylan contiene 55,70 mg de clorhidrato de amorolfina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Amorolfina Mylan 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de Amorolfina Mylan contiene 55,70 mg de clorhidrato de amorolfina
La solución cutánea se debe aplicar con un suave masaje sobre la piel o el cuero cabelludo. No se deben usar apósitos oclusivos (ver sección 4.4).
 1. NOMBRE DEL MEDICAMENTO Diprosalic solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de solución cutánea contiene: Betametasona (como dipropionato)...... 0,5 mg (0,05 %) (0,64 mg
1. NOMBRE DEL MEDICAMENTO Diprosalic solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de solución cutánea contiene: Betametasona (como dipropionato)...... 0,5 mg (0,05 %) (0,64 mg
FICHA TÉCNICA. Polisacárido Vi de Salmonella typhi (cepa Ty2)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Typherix, solución inyectable en jeringa precargada Vacuna de polisacárido antitifoideo. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml de la vacuna
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Typherix, solución inyectable en jeringa precargada Vacuna de polisacárido antitifoideo. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml de la vacuna
FICHA TÉCNICA. Parches Sor Virginia Extracto de Capsicum frutescens 2,59%
 Página: 1 de 1 ÍNDICE: 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS: 4.1 Indicaciones terapéuticas 4.2 Posología y forma de administración
Página: 1 de 1 ÍNDICE: 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS: 4.1 Indicaciones terapéuticas 4.2 Posología y forma de administración
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. EchinaMed Junior, comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO EchinaMed Junior, comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 comprimido [Aprox. 300 mg] contiene: 380 mg de tintura (Relación droga extracto (1:12-13))
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO EchinaMed Junior, comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 comprimido [Aprox. 300 mg] contiene: 380 mg de tintura (Relación droga extracto (1:12-13))
Prospecto: información para el usuario. Diprosalic pomada Betametasona dipropionato / Ácido salicílico
 Prospecto: información para el usuario Diprosalic pomada Betametasona dipropionato / Ácido salicílico Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
Prospecto: información para el usuario Diprosalic pomada Betametasona dipropionato / Ácido salicílico Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
FICHA TÉCNICA. Población pedíatrica No se ha establecido la seguridad y eficacia en niños menores de 14 años
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Tanagel 250 mg Polvo para suspensión oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Principio activo: - Gelatina tanato... 250mg Para consultar
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Tanagel 250 mg Polvo para suspensión oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Principio activo: - Gelatina tanato... 250mg Para consultar
FICHA TÉCNICA. Tratamiento sintomático del acné vulgar en adultos y adolescentes mayores de 12 años.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Skinoren 200 mg/g Crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.2 Composición cualitativa y cuantitativa 1 g de Skinoren contiene 200 mg (20%) de ácido azelaico
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Skinoren 200 mg/g Crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.2 Composición cualitativa y cuantitativa 1 g de Skinoren contiene 200 mg (20%) de ácido azelaico
