Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto
|
|
|
- Cristián Cárdenas Serrano
- hace 5 años
- Vistas:
Transcripción
1 1 October EMA/PRAC/621122/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC el 3-6 de septiembre de 2018 El texto de la información sobre el medicamento de este documento se ha extraído del documento «Recomendaciones del PRAC sobre señales» que contiene el texto completo de las recomendaciones del PRAC para la actualización de la información sobre el producto, así como algunas normas generales sobre la gestión de las señales. Dicho documento se puede encontrar aquí (solo en inglés). El texto nuevo que se debe añadir a la información sobre el medicamento aparece subrayado. El texto actual que se debe suprimir aparece tachado. 1. Alemtuzumab Infección por citomegalovirus (EPITT nº ) 4.4. Advertencias y precauciones especiales de empleo Infecciones Se han notificado infecciones por citomegalovirus (CMV), incluidos casos de reactivación del CMV, en pacientes tratados con LEMTRADA. La mayoría de los casos se produjeron en los 2 meses siguientes a la administración de alemtuzumab. Antes del inicio el tratamiento, se podría considerar la evaluación del estado serológico inmunitario de acuerdo a las directrices locales. Tabla 1 Infecciones e infestaciones: infección por citomegalovirus-frecuencia poco frecuente 1 Intended publication date. The actual publication date can be checked on the webpage dedicated to PRAC recommendations on safety signals. 30 Churchill Place Canary Wharf London E14 5EU United Kingdom Telephone +44 (0) Facsimile +44 (0) Send a question via our website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 Prospecto 2. Qué necesita saber antes de empezar a recibir LEMTRADA Advertencias y precauciones Infecciones Se han notificado infecciones por un virus llamado citomegalovirus en pacientes tratados con LEMTRADA. La mayoría de los casos se produjeron en los 2 meses siguientes a la administración de alemtuzumab. Informe a su médico de inmediato si tiene síntomas de infección, como fiebre o ganglios inflamados. Poco frecuentes (pueden afectar a 1 de cada 100 pacientes) Infecciones:, infección por citomegalovirus 2. Fumarato de dimetilo (Tecfidera)-Púrpura trombocitopénica inmune y trombocitopenia (EPITT nº ) Ficha Técnica o Resumen de las Características del Producto Tabla de reacciones adversas Trastornos de la sangre y del sistema linfático Frecuencia «Poco frecuentes»: Trombocitopenia Prospecto Efectos adversos poco frecuentes Pueden afectar a hasta 1 de cada 100 pacientes: - reducción de las plaquetas sanguíneas EMA/PRAC/621122/2018 Página 2/6
3 3. Duloxetina Enfermedad pulmonar intersticial (EPITT nº ) Tabla de reacciones adversas Trastornos respiratorios, torácicos y mediastínicos Frecuencia «Raras»: Enfermedad pulmonar intersticial X X Frecuencia estimada basada en ensayos clínicos controlados con placebo y Frecuencia «Raras»: Neumonía eosinofílica Y Y Frecuencia estimada de reacciones adversas notificadas durante el seguimiento de la comercialización; no se han observado en ensayos clínicos controlados con placebo. Prospecto Efectos adversos raros (pueden afectar a hasta 1 de cada personas) Tos, sibilancias y falta de aliento, que pueden ir acompañados de de fiebre alta 4. Fluoroquinolonas para uso sistémico e inhalado 2 Aneurisma y disección aórticos (EPITT nº ) 4.4. Advertencias y precauciones especiales de empleo Los estudios epidemiológicos informan de un aumento del riesgo de aneurisma y disección aórticos tras la administración de fluoroquinolonas, en particular en población de edad avanzada. Por consiguiente, las fluoroquinolonas solo se deben utilizar tras una evaluación cuidadosa del beneficio/riesgo y tras considerar otras opciones terapéuticas en pacientes con antecedentes familiares de aneurisma, en pacientes diagnosticados de aneurisma aórtico y/o disección aórtica preexistentes o en presencia de otros factores de riesgo o trastornos que predispongan para aneurisma y disección aórticos (por ejemplo, síndrome de Marfan, síndrome vascular de Ehlers-Danlos, arteritis de Takayasu, arteritis de células gigantes, enfermedad de Behçet, hipertensión, aterosclerosis conocida). En caso de dolor abdominal, torácico o de espalda repentino, se indicará a los pacientes que consulten de inmediato a un médico en un servicio de urgencias. 2 Ciprofloxacino; flumequina; levofloxacino; lomefloxacino; moxifloxacino; norfloxacino; ofloxacino; pefloxacino; prulifloxacino; rufloxacino. EMA/PRAC/621122/2018 Página 3/6
4 Prospecto 2. Qué necesita saber antes de empezar a tomar [producto] Advertencias y precauciones Consulte a su médico antes de empezar a tomar [producto]. - si le han diagnosticado un aumento de tamaño o un «bulto» de un vaso sanguíneo de gran tamaño (aneurisma aórtico o aneurisma de un vaso de gran tamaño periférico). - si ha sufrido un episodio previo de disección aórtica (desgarro de la pared de la aorta). - si tiene antecedentes familiares de aneurisma aórtico o disección aórtica u otros factores de riesgo o trastornos predisponentes (p. ej., trastornos del tejido conjuntivo como el síndrome de Marfan o el síndrome vascular de Ehlers-Danlos, o trastornos vasculares como arteritis de Takayasu, arteritis de células gigantes, enfermedad de Behçet, hipertensión arterial o aterosclerosis conocida). Si siente un dolor fuerte y repentino en el abdomen, el pecho o la espalda, acuda inmediatamente a un servicio de urgencias. 5. Hidroclorotiazida Cáncer de piel (EPITT nº ) 4.4. Advertencias y precauciones especiales Cáncer de piel no-melanoma Se ha observado un aumento del riesgo de cáncer de piel no-melanoma (CPNM) [carcinoma basocelular (CBC) y carcinoma de células escamosas (CEC)] con la exposición a dosis acumuladas crecientes de hidroclorotiazida (HCTZ) en dos estudios epidemiológicos, con base en el Registro Nacional Danés de cáncer. Los efectos fotosensibilizantes de la HCTZ podrían actuar como un posible mecanismo del CPNM. Se informará a los pacientes tratados con HCTZ del riesgo de CPNM y se les indicará que se revisen de manera periódica la piel en busca de lesiones nuevas y que informen de inmediato cualquier lesión de la piel sospechosa. Se indicarán a los pacientes las posibles medidas preventivas, como limitar la exposición a la luz solar y a los rayos UV y, en caso de exposición, utilizar protección adecuada para reducir al mínimo el riesgo de cáncer de piel. Las lesiones de piel sospechosas se deben evaluar de for ma rápida, incluidos los análisis histológicos de biopsias. Además, puede ser necesario reconsiderar el uso de HCTZ en pacientes que hayan experimentado previamente un CPNM (ver también sección 4.8). Neoplasias benignas, malignas y no especificadas (incluidos quistes y pólipos) Frecuencia «no conocida»: Cáncer de piel no-melanoma (carcinoma basocelular y carcinoma de células escamosas) EMA/PRAC/621122/2018 Página 4/6
5 Descripción de determinadas reacciones adversas Cáncer de piel no-melanoma: con base en los datos disponibles de estudios epidemiológicos, se ha observado una asociación dependiente de la dosis acumulada entre HCTZ y el CPNM (ver también las secciones 4.4 y 5.1) Propiedades farmacodinámicas Cáncer de piel no-melanoma: con base en los datos disponibles de estudios epidemiológicos, se ha observado una asociación dependiente de la dosis acumulada entre HCTZ y el CPNM. En un estudio se incluyó a una población formada por casos de CBC y casos de CCE emparejados con y controles de la población, respectivamente. El uso de dosis altas de HCTZ ( mg acumulados) se asoció a una OR ajustada de 1,29 (IC del 95%: 1,23-1,35) para el CBC y de 3,98 (IC del 95%: 3,68-4,31) para el CCE. Se observó una clara relación entre la dosis acumulada y la respuesta tanto en el CBC como en el CCE. Otro estudio mostró una posible asociación entre el cáncer de labio (CCE) y la exposición a HCTZ: 633 casos de cáncer de labios se emparejaron con controles de la población, utilizando una estrategia de muestreo basada en el riesgo. Se demostró una relación entre la dosis acumulada y la respuesta con una OR ajustada de 2,1 (IC del 95%: 1,7-2,6) que aumentó hasta una OR de 3,9 (3,0-4,9) con el uso de dosis altas (~ mg) y una OR de 7,7 (5,7-10,5) con la dosis acumulada más alta (~ mg) (ver también sección 4.4). Prospecto 2. Qué necesita saber antes de empezar a tomar X Advertencias y precauciones Consulte a su médico <o> <farmacéutico> <o enfermero> antes de empezar a <tomar> <usar> X - si ha tenido cáncer de piel o si le aparece una lesión de la piel inesperada durante el tratamiento. El tratamiento con hidroclorotiazida, en particular su uso a largo plazo a dosis altas, puede aumentar el riesgo de algunos tipos de cáncer de piel y labios (cáncer de piel nomelanoma). Proteja la piel de la exposición al sol y a los rayos UV mientras esté <tomando> <usando> X Frecuencia «no conocida»: Cáncer de piel y labios (cáncer de piel no-melanoma) 6. Ipilimumab Infección gastrointestinal por citomegalovirus (EPITT nº ) 4.4. Advertencias y precauciones especiales Trastornos gastrointestinales relacionados con el sistema inmunitario: Se debe vigilar a los pacientes en cuanto a signos y síntomas gastrointestinales que puedan ser indicativos de colitis o perforación gastrointestinal relacionadas con el sistema inmunitario. La EMA/PRAC/621122/2018 Página 5/6
6 presentación clínica puede incluir diarrea, aumento de los movimientos intestinales, dolor abdominal o hematoquecia, con o sin fiebre. La diarrea o la colitis que se produce después del inicio del tratamiento con ipilimumab se deben evaluar rápidamente para descartar etiologías infecciosas u otras etiologías alternativas. En los ensayos clínicos, la colitis relacionada con el sistema inmunitario se asoció a evidencias de inflamación mucosa, con o sin ulceraciones, e infiltración linfocitaria y neutrofílica. Se han notificado casos poscomercialización de infección/reactivación del citomegalovirus (CMV) en pacientes con colitis relacionada con el sistema inmunitario refractaria a los corticoesteroides. Tras la presentación de diarrea o colitis se debe realizar un estudio en heces para descartar causas infecciosas u otras causas alternativas. La experiencia en ensayos clínicos sobre el manejo de la diarrea o la colitis refractaria a los corticoesteroides es limitada. Sin embargo, se puedese debe valorar la adición de un agente inmunodepresor alternativo al régimen de corticoesteroides en la colitis relacionada con el sistema inmunitario refractaria a los corticoesteroides si se excluyen otras causas (incluida la infección/reactivación del citomegalovirus (CMV) evaluada mediante PCR viral en biopsia y otras etiologías víricas, bacterianas y parasitarias). En los ensayos clínicos, se añadió una dosis única de infliximab 5 mg/kg a menos que estuviera contraindicado. No se debe utilizar infliximab si se sospecha perforación gastrointestinal o sepsis (ver el Resumen de Características del Producto de infliximab). EMA/PRAC/621122/2018 Página 6/6
Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto
 25 January 2018 EMA/PRAC/35608/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC en su reunión
25 January 2018 EMA/PRAC/35608/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC en su reunión
Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto:
 17 December 2015 EMA/PRAC/835774/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto: Adoptado por el PRAC, 30
17 December 2015 EMA/PRAC/835774/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto: Adoptado por el PRAC, 30
Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
 23 April 2015 EMA/PRAC/273926/2015 Pharmacovigilance Risk Assessment Committee Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto Adoptado por el PRAC
23 April 2015 EMA/PRAC/273926/2015 Pharmacovigilance Risk Assessment Committee Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto Adoptado por el PRAC
Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto
 25 February 2016 EMA/PRAC/137780/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto Adoptado por el PRAC el
25 February 2016 EMA/PRAC/137780/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto Adoptado por el PRAC el
Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto
 15 September 2016 EMA/PRAC/603550/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC el 30
15 September 2016 EMA/PRAC/603550/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC el 30
Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
 22 de enero de 2015 EMA/PRAC/63326/2015 Comité para la Determinación del Riesgo en farmacovigilancia Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
22 de enero de 2015 EMA/PRAC/63326/2015 Comité para la Determinación del Riesgo en farmacovigilancia Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
Para más información sobre el tratamiento con Simponi, el paciente deberá leer el prospecto o consultar a su médico o farmacéutico.
 EMA/412395/2016 EMEA/H/C/000992 Resumen del EPAR para el público general golimumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo la Agencia ha evaluado
EMA/412395/2016 EMEA/H/C/000992 Resumen del EPAR para el público general golimumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo la Agencia ha evaluado
En el mieloma múltiple, un cáncer de un tipo de glóbulos blancos denominados células de descarga, Revlimid se utiliza:
 EMA/113870/2017 EMEA/H/C/000717 Resumen del EPAR para el público lenalidomida El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia ha evaluado
EMA/113870/2017 EMEA/H/C/000717 Resumen del EPAR para el público lenalidomida El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia ha evaluado
Para más información sobre el tratamiento con Keytruda, el paciente deberá leer el prospecto o consultar a su médico o farmacéutico.
 EMA/524789/2017 EMEA/H/C/003820 Resumen del EPAR para el público general pembrolizumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia
EMA/524789/2017 EMEA/H/C/003820 Resumen del EPAR para el público general pembrolizumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia
Información general sobre Opdivo y sobre los motivos por los que se autoriza su uso en la UE
 EMA/489091/2018 EMEA/H/C/003985 Información general sobre Opdivo y sobre los motivos por los que se autoriza su uso en la UE Qué es Opdivo y para qué se utiliza? Opdivo es un medicamento contra el cáncer
EMA/489091/2018 EMEA/H/C/003985 Información general sobre Opdivo y sobre los motivos por los que se autoriza su uso en la UE Qué es Opdivo y para qué se utiliza? Opdivo es un medicamento contra el cáncer
Para obtener información práctica sobre el tratamiento con Opdivo, el paciente deberá leer el prospecto o consultar a su médico o farmacéutico.
 EMA/691693/2017 EMEA/H/C/003985 Resumen del EPAR para el público general nivolumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia ha
EMA/691693/2017 EMEA/H/C/003985 Resumen del EPAR para el público general nivolumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia ha
Anexo III. Modificaciones a las secciones relevantes de ficha técnica y prospecto
 Anexo III Modificaciones a las secciones relevantes de ficha técnica y prospecto Nota: La ficha técnica o resumen de las características del producto y el prospecto pueden necesitar ser actualizados posteriormente
Anexo III Modificaciones a las secciones relevantes de ficha técnica y prospecto Nota: La ficha técnica o resumen de las características del producto y el prospecto pueden necesitar ser actualizados posteriormente
Guía de usuario para los informes de web
 Protección de la salud de los pacientes Esta guía de usuario para los informes de web facilita información sobre tipos de datos, presentacion, interpretación y funcionalidades del informe de web. 1. Tipos
Protección de la salud de los pacientes Esta guía de usuario para los informes de web facilita información sobre tipos de datos, presentacion, interpretación y funcionalidades del informe de web. 1. Tipos
Guía para la interpretación de informes espontáneos de presuntas reacciones adversas a medicamentos
 30 de enero de 2017 Inspecciones, Farmacovigilancia de Medicamentos de Uso Humano y Comités EMA/749446/2016 Revisión 1* Guía para la interpretación de informes espontáneos de presuntas reacciones adversas
30 de enero de 2017 Inspecciones, Farmacovigilancia de Medicamentos de Uso Humano y Comités EMA/749446/2016 Revisión 1* Guía para la interpretación de informes espontáneos de presuntas reacciones adversas
Materiales educativos para los profesionales sanitarios y los pacientes que utilizan el medicamento antidiabético Suliqua
 19 de enero de 2017 EMA/747766/2016 Materiales educativos para los profesionales sanitarios y los pacientes que utilizan el medicamento antidiabético Suliqua Medidas para reducir el riesgo de confusión
19 de enero de 2017 EMA/747766/2016 Materiales educativos para los profesionales sanitarios y los pacientes que utilizan el medicamento antidiabético Suliqua Medidas para reducir el riesgo de confusión
Información general sobre Metacam y sobre los motivos por los que se autoriza su uso en la UE
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Información general sobre Metacam y sobre los motivos por los que se autoriza su uso en la UE Qué es Metacam y para qué se utiliza? Metacam es un medicamento antiinflamatorio
EMA/CVMP/259397/2006 EMEA/V/C/000033 Información general sobre Metacam y sobre los motivos por los que se autoriza su uso en la UE Qué es Metacam y para qué se utiliza? Metacam es un medicamento antiinflamatorio
REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS (Fase II)
 REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS (Fase II) INFORME NOVIEMBRE 2008 Índice Descripción del registro con todos los tratamientos biológicos...
REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS (Fase II) INFORME NOVIEMBRE 2008 Índice Descripción del registro con todos los tratamientos biológicos...
REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS (Fase II)
 REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS (Fase II) INFORME JUNIO 2007 Descripción del registro con todos los tratamientos biológicos Desde la creación
REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS (Fase II) INFORME JUNIO 2007 Descripción del registro con todos los tratamientos biológicos Desde la creación
Metacam. meloxicam. Qué es Metacam y para qué se utiliza? Resumen del EPAR para el público general
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Resumen del EPAR para el público general meloxicam El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo la Agencia
EMA/CVMP/259397/2006 EMEA/V/C/000033 Resumen del EPAR para el público general meloxicam El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo la Agencia
La EMA confirma las recomendaciones para minimizar el riesgo de LMP, una infección cerebral, con Tysabri
 25/04/2016 EMA/266665/2016 La EMA confirma las recomendaciones para minimizar el riesgo de LMP, una infección Se deberá considerar la realización de resonancias magnéticas más frecuentes en los pacientes
25/04/2016 EMA/266665/2016 La EMA confirma las recomendaciones para minimizar el riesgo de LMP, una infección Se deberá considerar la realización de resonancias magnéticas más frecuentes en los pacientes
ANEXO III ENMIENDA DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y PROSPECTO
 ANEXO III ENMIENDA DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y PROSPECTO 1 ENMIENDA A INCLUIR EN LAS SECCIONES RELEVANTES DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL
ANEXO III ENMIENDA DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y PROSPECTO 1 ENMIENDA A INCLUIR EN LAS SECCIONES RELEVANTES DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL
Información general sobre Eylea y sobre los motivos por los que se autoriza su uso en la UE
 EMA/481361/2018 EMEA/H/C/002392 Información general sobre Eylea y sobre los motivos por los que se autoriza su uso en la UE Qué es Eylea y para qué se utiliza? Eylea es un medicamento que se usa para tratar
EMA/481361/2018 EMEA/H/C/002392 Información general sobre Eylea y sobre los motivos por los que se autoriza su uso en la UE Qué es Eylea y para qué se utiliza? Eylea es un medicamento que se usa para tratar
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 42 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN CABERGOLINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 42 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN CABERGOLINA 4.2 Posología y forma
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea
 FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS)_Agosto_2016
 KEYTRUDA (pembrolizumab) Información para pacientes Keytruda es un medicamento biológico Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios
KEYTRUDA (pembrolizumab) Información para pacientes Keytruda es un medicamento biológico Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios
Anexo I. Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización
 Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización 1 Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización 1 Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
ANEXO III MODIFICACIONES AL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y AL PROSPECTO
 ANEXO III MODIFICACIONES AL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y AL PROSPECTO Estas modificaciones del SPC (ficha técnica) y prospecto entran en vigor en el momento de la Decisión de la Comisión.
ANEXO III MODIFICACIONES AL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y AL PROSPECTO Estas modificaciones del SPC (ficha técnica) y prospecto entran en vigor en el momento de la Decisión de la Comisión.
INFORMACIÓN DE SEGURIDAD PARA PROFESIONALES SANITARIOS
 Stelara (ustekinumab) INFORMACIÓN DE SEGURIDAD PARA PROFESIONALES SANITARIOS Por favor, además de la ficha técnica del producto (FT) lea detenidamente esta guía. Por favor, informe a sus pacientes sobre
Stelara (ustekinumab) INFORMACIÓN DE SEGURIDAD PARA PROFESIONALES SANITARIOS Por favor, además de la ficha técnica del producto (FT) lea detenidamente esta guía. Por favor, informe a sus pacientes sobre
Prospecto: información para el paciente. Carnicor 200 mg/ml solución inyectable L-carnitina
 Prospecto: información para el paciente Carnicor 200 mg/ml solución inyectable L-carnitina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
Prospecto: información para el paciente Carnicor 200 mg/ml solución inyectable L-carnitina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
CANCER DE ESTOMAGO. Distribución del cáncer gástrico a nivel mundial, Año 2012
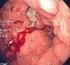 El adenocarcinoma gástrico es una neoplasia maligna que se origina, en la mayoría de los casos, a partir de las células glandulares del tejido gástrico, representa entre 90 y 95% de todas las neoplasias
El adenocarcinoma gástrico es una neoplasia maligna que se origina, en la mayoría de los casos, a partir de las células glandulares del tejido gástrico, representa entre 90 y 95% de todas las neoplasias
CUESTIONARIO PARA NIÑOS Y ADOLESCENTES
 Punto de vista acerca del consumo de medicamentos Por qué preguntamos? El Comité Pediátrico (PDCO) trabaja con la Agencia Europea de Medicamentos, y es su trabajo asegurarse de que los medicamentos para
Punto de vista acerca del consumo de medicamentos Por qué preguntamos? El Comité Pediátrico (PDCO) trabaja con la Agencia Europea de Medicamentos, y es su trabajo asegurarse de que los medicamentos para
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
Avastin se utiliza para el tratamiento de adultos con los siguientes tipos de cáncer en combinación con otros medicamentos contra el cáncer:
 EMA/175824/2015 EMEA/H/C/000582 Resumen del EPAR para el público general bevacizumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de
EMA/175824/2015 EMEA/H/C/000582 Resumen del EPAR para el público general bevacizumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de
vacuna antineumocócica polisacárida conjugada (13-valente, adsorbida)
 EMA/90006/2015 EMEA/H/C/001104 Resumen del EPAR para el público general vacuna antineumocócica polisacárida conjugada (13-valente, adsorbida) El presente documento resume el Informe Público Europeo de
EMA/90006/2015 EMEA/H/C/001104 Resumen del EPAR para el público general vacuna antineumocócica polisacárida conjugada (13-valente, adsorbida) El presente documento resume el Informe Público Europeo de
Anexo III. Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto
 Anexo III Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto Nota: Esta Ficha Técnica, Etiquetado y Prospecto son el resultado del proceso de arbitraje.
Anexo III Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto Nota: Esta Ficha Técnica, Etiquetado y Prospecto son el resultado del proceso de arbitraje.
Anexo III. Modificaciones en las secciones relevantes de la información del producto
 Anexo III Modificaciones en las secciones relevantes de la información del producto Nota: Estas modificaciones de las secciones relevantes de la Ficha Técnica y Prospecto son el resultado del proceso de
Anexo III Modificaciones en las secciones relevantes de la información del producto Nota: Estas modificaciones de las secciones relevantes de la Ficha Técnica y Prospecto son el resultado del proceso de
Anexo III. Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos
 Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
FICHA TÉCNICA. Adultos y adolescentes mayores de 12 años: de 250 a 500 mg al día distribuidos en dos tomas (mañana y noche)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
VÓMITOS Y DIARREA EN LA CONSULTA DEL PEDIATRA: BUSCANDO CAUSAS.
 VÓMITOS Y DIARREA EN LA CONSULTA DEL PEDIATRA: BUSCANDO CAUSAS. 1 Grupo de patología infecciosa de la AEPap Mª Ángeles Suárez Rodríguez. Septiembre de 2014 MOTIVO DE CONSULTA Paciente de 7 años y 10 meses
VÓMITOS Y DIARREA EN LA CONSULTA DEL PEDIATRA: BUSCANDO CAUSAS. 1 Grupo de patología infecciosa de la AEPap Mª Ángeles Suárez Rodríguez. Septiembre de 2014 MOTIVO DE CONSULTA Paciente de 7 años y 10 meses
UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C.
 UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C. I CONGRESO INTERNACIONAL DE ONCOLOGÍA: Avances y Retos AVANCES RECIENTES EN LA ADMINISTRACION DE QUIMIOTERAPIA EN CANCER DE MAMA
UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C. I CONGRESO INTERNACIONAL DE ONCOLOGÍA: Avances y Retos AVANCES RECIENTES EN LA ADMINISTRACION DE QUIMIOTERAPIA EN CANCER DE MAMA
Corro un riesgo importante al tomar la medicación? Puedo prevenir los efectos secundarios?
 Programas educativos en adherencia terapéutica dirigido a pacientes con enfermedad inflamatoria intestinal. Corro un riesgo importante al tomar la medicación? Puedo prevenir los efectos secundarios? Dr.
Programas educativos en adherencia terapéutica dirigido a pacientes con enfermedad inflamatoria intestinal. Corro un riesgo importante al tomar la medicación? Puedo prevenir los efectos secundarios? Dr.
Comunicación dirigida a profesionales sanitarios
 Comunicación dirigida a profesionales sanitarios Tecfidera (dimetilfumarato): Nuevas recomendaciones para minimizar el riesgo de leucoencefalopatía multifocal progresiva. Intensificación de las medidas
Comunicación dirigida a profesionales sanitarios Tecfidera (dimetilfumarato): Nuevas recomendaciones para minimizar el riesgo de leucoencefalopatía multifocal progresiva. Intensificación de las medidas
Cuadernillo destinado a aquellos pacientes a quienes se les haya prescrito tratamiento con XALKORI (crizotinib)
 Cuadernillo destinado a aquellos pacientes a quienes se les haya prescrito tratamiento con XALKORI (crizotinib) Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
Cuadernillo destinado a aquellos pacientes a quienes se les haya prescrito tratamiento con XALKORI (crizotinib) Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
MANUAL EDUCATIVO PARA PACIENTES PÚRPURA DE HENOCH SCHÖNLEIN
 32 MANUAL EDUCATIVO PARA PACIENTES PÚRPURA DE HENOCH SCHÖNLEIN 2 PÚRPURA DE HENOCH SCHÖNLEIN María Fernanda Reina Ávila Fellow Reumatología Pediátrica Universidad El Bosque Qué es Púrpura de Henoch Schönlein?
32 MANUAL EDUCATIVO PARA PACIENTES PÚRPURA DE HENOCH SCHÖNLEIN 2 PÚRPURA DE HENOCH SCHÖNLEIN María Fernanda Reina Ávila Fellow Reumatología Pediátrica Universidad El Bosque Qué es Púrpura de Henoch Schönlein?
FICHA TÉCNICA. 250 mg
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii CNCM I-745 250 mg Excipientes
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii CNCM I-745 250 mg Excipientes
Síndrome de Johnson, Características, Síntomas, Causas, Diagnóstico y Tratamientos
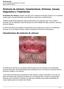 Síndrome de Johnson, Características, Síntomas, Causas, Diagnóstico y Tratamientos El síndrome de Johnson, también conocido como síndrome de Stevens-Johnson, es un trastorno cutáneo grave, que generalmente
Síndrome de Johnson, Características, Síntomas, Causas, Diagnóstico y Tratamientos El síndrome de Johnson, también conocido como síndrome de Stevens-Johnson, es un trastorno cutáneo grave, que generalmente
Todas las Edades- Sexo Masculino No. de Orden Diagnóstico Masculino
 según Lista Internacional de Enfermedades de la CIE-10 Todas las Edades- Sexo Masculino No. de Orden Diagnóstico Masculino 1 Otras infecciones agudas de las vías respiratorias superiores 591,677 2 Faringitis
según Lista Internacional de Enfermedades de la CIE-10 Todas las Edades- Sexo Masculino No. de Orden Diagnóstico Masculino 1 Otras infecciones agudas de las vías respiratorias superiores 591,677 2 Faringitis
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Descripción general
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Descripción general Las cápsulas son ovales, con el cuerpo y la tapa de color blanco.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Descripción general Las cápsulas son ovales, con el cuerpo y la tapa de color blanco.
FOB-Transferrina + Calprotectina-Lactoferrina Combo Card. CerTest Biotec
 FOB-Transferrina + Calprotectina-Lactoferrina Combo Card CerTest Biotec www.certest.es 1 Índice Hemoglobina (FOB) Transferrina Transferrina versus Hemoglobina (FOB) Calprotectina Lactoferrina Calprotectina
FOB-Transferrina + Calprotectina-Lactoferrina Combo Card CerTest Biotec www.certest.es 1 Índice Hemoglobina (FOB) Transferrina Transferrina versus Hemoglobina (FOB) Calprotectina Lactoferrina Calprotectina
Anexo III. Modificaciones de las secciones pertinentes de la información sobre el producto
 Anexo III Modificaciones de las secciones pertinentes de la información sobre el producto Nota: Estas modificaciones de las secciones pertinentes de la información sobre el producto son el resultado del
Anexo III Modificaciones de las secciones pertinentes de la información sobre el producto Nota: Estas modificaciones de las secciones pertinentes de la información sobre el producto son el resultado del
Síndrome de Behcet, Características, Síntomas, Causas, Diagnóstico y Tratamiento
 Síndrome de Behcet, Características, Síntomas, Causas, Diagnóstico y Tratamiento El síndrome de Behcet, tambien conocido como la "enfermedad de la Ruta de la Seda" es un trastorno en donde el sistema inmunitario
Síndrome de Behcet, Características, Síntomas, Causas, Diagnóstico y Tratamiento El síndrome de Behcet, tambien conocido como la "enfermedad de la Ruta de la Seda" es un trastorno en donde el sistema inmunitario
Anexo III Modificaciones a las secciones relevantes de la Ficha Técnica o Resumen de las características del producto y Prospecto
 Anexo III Modificaciones a las secciones relevantes de la Ficha Técnica o Resumen de las características del producto y Prospecto 34/42 A. FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 4.1.
Anexo III Modificaciones a las secciones relevantes de la Ficha Técnica o Resumen de las características del producto y Prospecto 34/42 A. FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 4.1.
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Ultra Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Ultra Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. 2.1 Descripción general
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Las cápsulas son ovales, con el cuerpo y la tapa de color blanco.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Las cápsulas son ovales, con el cuerpo y la tapa de color blanco.
MANUAL EDUCATIVO PARA PACIENTES VASCULITIS ANCA POSITIVO
 15 MANUAL EDUCATIVO PARA PACIENTES VASCULITIS ANCA POSITIVO 5 VASCULITIS ANCA POSITIVO Fernando Vela Lozada Medicina Interna Fellow de Reumatología Universidad Nacional de Colombia Generalidades Las vasculitis
15 MANUAL EDUCATIVO PARA PACIENTES VASCULITIS ANCA POSITIVO 5 VASCULITIS ANCA POSITIVO Fernando Vela Lozada Medicina Interna Fellow de Reumatología Universidad Nacional de Colombia Generalidades Las vasculitis
Actualización de temas GINA Dra. Patricia Arizmendi Agosto 2014
 Actualización de temas GINA 2014 Dra. Patricia Arizmendi Agosto 2014 Definición Enfermedad caracterizada por la inflamación crónica de la vía aérea. Definida por la presencia de síntomas de la esfera respiratoria
Actualización de temas GINA 2014 Dra. Patricia Arizmendi Agosto 2014 Definición Enfermedad caracterizada por la inflamación crónica de la vía aérea. Definida por la presencia de síntomas de la esfera respiratoria
FICHA TÉCNICA. 250 mg. Cápsulas duras Las cápsulas son ovales, con el cuerpo y la tapa de color blanco
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii CNCM I-745 Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii CNCM I-745 Excipientes con efecto conocido:
Modificaciones de la información de los medicamentos autorizados por procedimiento nacional que contienen: 5-fluorouracilo (administración i.v.
 DEPARTAMENTO DE MEDICAMENTOS DE USO HUMANO División de Farmacoepidemiología y Farmacovigilancia Modificaciones de la información de los medicamentos autorizados por procedimiento nacional que contienen:
DEPARTAMENTO DE MEDICAMENTOS DE USO HUMANO División de Farmacoepidemiología y Farmacovigilancia Modificaciones de la información de los medicamentos autorizados por procedimiento nacional que contienen:
Se puede presentar de tres formas diferentes: crónica, subaguda y aguda.
 Sindrome de Lofgren El síndrome de Lofgren es también denominado sarcoidosis aguda. Refiere al crecimiento de granulomas (células inflamatorias) en diversas partes del cuerpo, con fuerte presencia en los
Sindrome de Lofgren El síndrome de Lofgren es también denominado sarcoidosis aguda. Refiere al crecimiento de granulomas (células inflamatorias) en diversas partes del cuerpo, con fuerte presencia en los
La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos.
 Pág. 1 de 5 La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos. El objetivo es difundir información sobre la seguridad y eficacia de los medicamentos basados
Pág. 1 de 5 La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos. El objetivo es difundir información sobre la seguridad y eficacia de los medicamentos basados
Prevención y tratamiento de las toxicidades de la inmunoterapia y de la terapia dirigida
 Prevención y tratamiento de las toxicidades de la inmunoterapia y de la terapia dirigida Dr. Joaquín Fra Rodríguez Hospital Universitario Río Hortega Valladolid TODO CAMBIÓ A PARTIR DEL 2010 Introducción
Prevención y tratamiento de las toxicidades de la inmunoterapia y de la terapia dirigida Dr. Joaquín Fra Rodríguez Hospital Universitario Río Hortega Valladolid TODO CAMBIÓ A PARTIR DEL 2010 Introducción
PANENDOSCOPIA ORAL. -Siempre que se detecte o se sospeche la presencia de un sangrado en la parte alta del tubo digestivo.
 PANENDOSCOPIA ORAL 1. Qué es una panendoscopia oral? Es un procedimiento que permite explorar el esófago, el estómago y el duodeno y obtener multitud de información con un mínimo de molestias para el paciente.
PANENDOSCOPIA ORAL 1. Qué es una panendoscopia oral? Es un procedimiento que permite explorar el esófago, el estómago y el duodeno y obtener multitud de información con un mínimo de molestias para el paciente.
E F E C T O S A D V E R S O S E N Q U I N O L O N A S
 BOLETIN N 20 / 2015 N M B R E D E L T R A B A J O E F E C T O S A D V E R S O S E N Q U I N O L O N A S SAN JUAN / SEPTIEMBRE 2015 Las fluoroquinolonas constituyen el grupo de antibacterianos que ha experimentado
BOLETIN N 20 / 2015 N M B R E D E L T R A B A J O E F E C T O S A D V E R S O S E N Q U I N O L O N A S SAN JUAN / SEPTIEMBRE 2015 Las fluoroquinolonas constituyen el grupo de antibacterianos que ha experimentado
Comunicación Dirigida a Profesionales Sanitarios. Madrid, 13 de Mayo 2013
 Madrid, 13 de Mayo 2013 Comunicación Dirigida a Profesionales Sanitarios Información importante respecto a las restricciones de utilización de ranelato de estroncio (Protelos /Osseor ) tras el análisis
Madrid, 13 de Mayo 2013 Comunicación Dirigida a Profesionales Sanitarios Información importante respecto a las restricciones de utilización de ranelato de estroncio (Protelos /Osseor ) tras el análisis
Prospecto: información para el paciente. Bisolvon Mucolítico infantil 0,8 mg/ml jarabe Bromhexina hidrocloruro
 Prospecto: información para el paciente Bisolvon Mucolítico infantil 0,8 mg/ml jarabe Bromhexina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
Prospecto: información para el paciente Bisolvon Mucolítico infantil 0,8 mg/ml jarabe Bromhexina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO YERVOY 5 mg/ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO YERVOY 5 mg/ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml
Lo último publicado en EPOC
 Lo último publicado en EPOC Publicaciones y Avances en Antibióticos ticos y Antivíricos en reagudizaciones de EPOC JC Martín Escudero Antibióticos ticos en las agudizaciones de EPOC? 11 ensayos con 917
Lo último publicado en EPOC Publicaciones y Avances en Antibióticos ticos y Antivíricos en reagudizaciones de EPOC JC Martín Escudero Antibióticos ticos en las agudizaciones de EPOC? 11 ensayos con 917
REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS. (Fase II)
 REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS (Fase II) INFORME NOVIEMBRE 2010 NOTA: Este informe se ha generado únicamente con la información de los 14
REGISTRO ESPAÑOL DE ACONTECIMIENTOS ADVERSOS DE TERAPIAS BIOLÓGICAS EN ENFERMEDADES REUMÁTICAS (Fase II) INFORME NOVIEMBRE 2010 NOTA: Este informe se ha generado únicamente con la información de los 14
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
FICHA TÉCNICA. Alivio sintomático del estreñimiento ocasional en adultos y niños mayores de 6 años.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ordelax 756,6 mg/ml líquido oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de líquido oral contiene: Parafina líquida...756,6 mg. Para consultar la lista
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ordelax 756,6 mg/ml líquido oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de líquido oral contiene: Parafina líquida...756,6 mg. Para consultar la lista
MEDICAMENTOS SUJETOS A SEGUIMIENTO ADICIONAL
 MEDICAMENTOS SUJETOS A SEGUIMIENTO ADICIONAL v.1 actualización: 17 de mayo de 2013 Fecha de publicación: 17 de mayo de 2013 CORREO ELECTRÓNICO smhaem@aemps.es Página 1 de 6 C/ CAMPEZO, 1 EDIFICIO 8 28022
MEDICAMENTOS SUJETOS A SEGUIMIENTO ADICIONAL v.1 actualización: 17 de mayo de 2013 Fecha de publicación: 17 de mayo de 2013 CORREO ELECTRÓNICO smhaem@aemps.es Página 1 de 6 C/ CAMPEZO, 1 EDIFICIO 8 28022
Anexo I. Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización.
 Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización. Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización. Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
Cuadro DEFUNCIONES EN LA REPÚBLICA, POR GRUPOS DE EDAD, SEGÚN CAUSA Y SEXO: AÑO 2016
 Causa y sexo Total Menores de 1 1 a 4 5 a 9 10 a 14 15 a 19 20 a 24 TOTAL 18,882 1,046 291 90 105 267 346 Hombres 10,859 567 162 47 60 185 274 Mujeres 8,023 479 129 43 45 82 72 001-025 Ciertas enfermedades
Causa y sexo Total Menores de 1 1 a 4 5 a 9 10 a 14 15 a 19 20 a 24 TOTAL 18,882 1,046 291 90 105 267 346 Hombres 10,859 567 162 47 60 185 274 Mujeres 8,023 479 129 43 45 82 72 001-025 Ciertas enfermedades
FICHA TÉCNICA. Bencidamina hidrocloruro... 3 mg (equivalente a 2,68 mg de bencidamina).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO TANTUM VERDE 3 mg Pastillas para chupar sabor eucalipto 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada pastilla para chupar contiene: Composición cualitativa y cuantitativa
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO TANTUM VERDE 3 mg Pastillas para chupar sabor eucalipto 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada pastilla para chupar contiene: Composición cualitativa y cuantitativa
La Ciproterona acetato- Etinilestradiol como principios activos a dosis fija en Anticonceptivos orales y riesgo de Eventos Tromboembólicos.
 Pág. 1 de 6 La Ciproterona acetato- Etinilestradiol como principios activos a dosis fija en Anticonceptivos orales y riesgo de Eventos Tromboembólicos. El objetivo es difundir información sobre la seguridad
Pág. 1 de 6 La Ciproterona acetato- Etinilestradiol como principios activos a dosis fija en Anticonceptivos orales y riesgo de Eventos Tromboembólicos. El objetivo es difundir información sobre la seguridad
INFORMACIÓN PARA EL PACIENTE COLONOSCOPIA. DIAGNÓSTICA O TERAPÉUTICA (Endoscopia digestiva baja)
 INFORMACIÓN PARA EL PACIENTE COLONOSCOPIA DIAGNÓSTICA O TERAPÉUTICA (Endoscopia digestiva baja) COLONOSCOPIA DIAGNÓSTICA O TERAPÉUTICA ( E n d o s c o p i a d i g e s t i v a b a j a ) En este documento
INFORMACIÓN PARA EL PACIENTE COLONOSCOPIA DIAGNÓSTICA O TERAPÉUTICA (Endoscopia digestiva baja) COLONOSCOPIA DIAGNÓSTICA O TERAPÉUTICA ( E n d o s c o p i a d i g e s t i v a b a j a ) En este documento
NOMBRE: FECHA NACIMIENTO: FECHA: MR#
 Page 1 of 6 NOMBRE: FECHA NACIMIENTO: FECHA: MR# POR CUALES RAZONES NOS VISITA HOY? QUIEN LO/A MANDO A NOSOTROS? DOCTOR/OTRO CUAL DOCTOR? QUE CIRUGIA A TENIDO Y CUANDO? (Listar) 1. 2. 3. 4. 5. 6. 7. LA
Page 1 of 6 NOMBRE: FECHA NACIMIENTO: FECHA: MR# POR CUALES RAZONES NOS VISITA HOY? QUIEN LO/A MANDO A NOSOTROS? DOCTOR/OTRO CUAL DOCTOR? QUE CIRUGIA A TENIDO Y CUANDO? (Listar) 1. 2. 3. 4. 5. 6. 7. LA
PROSPECTO: INFORMACIÓN PARA EL USUARIO RANITIDINA MABO 300 mg comprimidos recubiertos EFG (Ranitidina clorhidrato)
 PROSPECTO: INFORMACIÓN PARA EL USUARIO RANITIDINA MABO 300 mg comprimidos recubiertos EFG (Ranitidina clorhidrato) Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque
PROSPECTO: INFORMACIÓN PARA EL USUARIO RANITIDINA MABO 300 mg comprimidos recubiertos EFG (Ranitidina clorhidrato) Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque
ANEXO III Modificaciones a las secciones relevantes de Ficha Técnica y Prospecto
 ANEXO III Modificaciones a las secciones relevantes de Ficha Técnica y Prospecto Nota: Si procede, la ficha técnica o resumen de las características del producto y el prospecto pueden necesitar ser actualizados
ANEXO III Modificaciones a las secciones relevantes de Ficha Técnica y Prospecto Nota: Si procede, la ficha técnica o resumen de las características del producto y el prospecto pueden necesitar ser actualizados
Índice de contenidos DESCRIPCIÓN GENERAL A TENER EN CUENTA. Consulte con su especialista si se encuentra en alguno de los siguientes casos:
 Colchicina (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL La colchicina se usa para prevenir
Colchicina (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL La colchicina se usa para prevenir
Cuadro DEFUNCIONES EN LA REPÚBLICA, POR GRUPOS DE EDAD, SEGÚN CAUSA Y SEXO: AÑO Total. Total
 Causa y sexo Menores de 1 Menores de 5 1 2 3 4 5 a 9 10 a 14 15 a 19 TOTAL... 18,182 1,231 935 154 72 41 29 93 109 265 Hombres... 10,403 697 541 82 40 24 10 56 60 185 Mujeres... 7,779 534 394 72 32 17
Causa y sexo Menores de 1 Menores de 5 1 2 3 4 5 a 9 10 a 14 15 a 19 TOTAL... 18,182 1,231 935 154 72 41 29 93 109 265 Hombres... 10,403 697 541 82 40 24 10 56 60 185 Mujeres... 7,779 534 394 72 32 17
Introducción al programa de trabajo de la Agencia para 2015
 7 agosto 2015 EMA/372784/2015 Director Ejecutivo Adjunto Introducción al programa de trabajo de la Agencia para 2015 Por Andreas Pott, Director Ejecutivo Adjunto Prioridades de la EMA y circunstancias
7 agosto 2015 EMA/372784/2015 Director Ejecutivo Adjunto Introducción al programa de trabajo de la Agencia para 2015 Por Andreas Pott, Director Ejecutivo Adjunto Prioridades de la EMA y circunstancias
ENFERMEDAD PULMONAR INTERSTICIAL GRANULOMATOSA-LINFOCÍTICA JOSE ESPINOZA PEREZ COMPLEJO HOSPITALARIO LA MANCHA CENTRO ALCAZAR DE SAN JUAN
 ENFERMEDAD PULMONAR INTERSTICIAL GRANULOMATOSA-LINFOCÍTICA JOSE ESPINOZA PEREZ COMPLEJO HOSPITALARIO LA MANCHA CENTRO ALCAZAR DE SAN JUAN Introducción La enfermedad pulmonar intersticial granulomatosa-linfocítica
ENFERMEDAD PULMONAR INTERSTICIAL GRANULOMATOSA-LINFOCÍTICA JOSE ESPINOZA PEREZ COMPLEJO HOSPITALARIO LA MANCHA CENTRO ALCAZAR DE SAN JUAN Introducción La enfermedad pulmonar intersticial granulomatosa-linfocítica
Dermatomiositis juvenil
 www.printo.it/pediatric-rheumatology/mx/intro Dermatomiositis juvenil Versión de 2016 1. QUÉ ES LA DERMATOMIOSITIS JUVENIL? 1.1 Qué tipo de enfermedad es? La dermatomiositis juvenil (DMJ) es una enfermedad
www.printo.it/pediatric-rheumatology/mx/intro Dermatomiositis juvenil Versión de 2016 1. QUÉ ES LA DERMATOMIOSITIS JUVENIL? 1.1 Qué tipo de enfermedad es? La dermatomiositis juvenil (DMJ) es una enfermedad
17 DE NOVIEMBRE: DÍA MUNDIAL DE LA LUCHA CONTRA EL CÁNCER DE PULMÓN
 17 DE NOVIEMBRE: DÍA MUNDIAL DE LA LUCHA CONTRA EL CÁNCER DE PULMÓN El Centro de Especialistas en Análisis Biológicos CEABI Distrito II adhiere a la campaña por el Día Mundial de la lucha contra el cáncer
17 DE NOVIEMBRE: DÍA MUNDIAL DE LA LUCHA CONTRA EL CÁNCER DE PULMÓN El Centro de Especialistas en Análisis Biológicos CEABI Distrito II adhiere a la campaña por el Día Mundial de la lucha contra el cáncer
CUESTIONARIO INFECCIONES 14 MESES
 CUESTIONARIO INFECCIONES 14 MESES IDNUM NIÑO: FECH FECHA CUESTIONARIO ACTUAL: / / ENTREVISTADOR: FECHA ÚLTIMA ENTREVISTA: / / ENTREVISTADO: Nota: Dado que muchas preguntas ya se han formulado en la entrevista
CUESTIONARIO INFECCIONES 14 MESES IDNUM NIÑO: FECH FECHA CUESTIONARIO ACTUAL: / / ENTREVISTADOR: FECHA ÚLTIMA ENTREVISTA: / / ENTREVISTADO: Nota: Dado que muchas preguntas ya se han formulado en la entrevista
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Otilonio Qualigen 40 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 40 mg de otilonio bromuro. Para
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Otilonio Qualigen 40 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 40 mg de otilonio bromuro. Para
Excipientes con efecto conocido: Lactosa monohidrato 6,5 mg Sacarosa 92,30 mg Para consultar la lista completa de excipientes, ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula dura contiene: Saccharomyces boulardii 50 mg. Excipientes con efecto conocido: Lactosa
1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula dura contiene: Saccharomyces boulardii 50 mg. Excipientes con efecto conocido: Lactosa
Principales causas de mortalidad general Tláhuac 2007
 Principales causas de mortalidad general 359,431 Total 1,349 375.3 1 Diabetes mellitus 251 69.8 2 Enfermedades del corazón 227 63.2 3 Tumores malignos 159 44.2 4 Enfermedades del Hígado 81 22.5 5 Accidentes
Principales causas de mortalidad general 359,431 Total 1,349 375.3 1 Diabetes mellitus 251 69.8 2 Enfermedades del corazón 227 63.2 3 Tumores malignos 159 44.2 4 Enfermedades del Hígado 81 22.5 5 Accidentes
PARA PERSONAS TRATADAS CON XELJANZ,
 SPANISH XELJANZ Este folleto está dirigido a personas a quienes se ha prescrito XELJANZ. Encontrará más información en el prospecto de envase incluido en el fármaco. PARA PERSONAS TRATADAS CON XELJANZ,
SPANISH XELJANZ Este folleto está dirigido a personas a quienes se ha prescrito XELJANZ. Encontrará más información en el prospecto de envase incluido en el fármaco. PARA PERSONAS TRATADAS CON XELJANZ,
Andrea Bailén Vergara R1 HGUA Tutor: Pedro Alcalá Minagorre 24 febrero 2015
 Andrea Bailén Vergara R1 HGUA Tutor: Pedro Alcalá Minagorre 24 febrero 2015 Índice 1. Casos 2. Epidemiología 3. Espectro de enfermedad por B. Hanselae 4. Etiopatogenia 5. Manifestaciones clínicas 6. Diagnóstico
Andrea Bailén Vergara R1 HGUA Tutor: Pedro Alcalá Minagorre 24 febrero 2015 Índice 1. Casos 2. Epidemiología 3. Espectro de enfermedad por B. Hanselae 4. Etiopatogenia 5. Manifestaciones clínicas 6. Diagnóstico
En la audiencia pública, se tendrá debidamente en cuenta el efecto terapéutico del medicamento.
 13 de abril de 2016 EMA/389918/2016 Normas reguladoras del procedimiento para la organización y realización de audiencias públicas en el Comité para la Evaluación de Riesgos en Farmacovigilancia (PRAC)
13 de abril de 2016 EMA/389918/2016 Normas reguladoras del procedimiento para la organización y realización de audiencias públicas en el Comité para la Evaluación de Riesgos en Farmacovigilancia (PRAC)
21 REUNIÓN ANUAL DEBUT DE LEUCEMIAS EN URGENCIAS PEDIÁTRICAS: ESTUDIO RETROSPECTIVO DE LA SOCIEDAD ESPAÑOLA DE URGENCIAS DE PEDIATRÍA
 DEBUT DE LEUCEMIAS EN URGENCIAS PEDIÁTRICAS: ESTUDIO RETROSPECTIVO Maria Gual Sánchez, Miguel Angel Molina Gutiérrez, Pedro Maria Rubio Aparicio, Diego Plaza López de Sabando, Ana Sastre Urgelles, Santos
DEBUT DE LEUCEMIAS EN URGENCIAS PEDIÁTRICAS: ESTUDIO RETROSPECTIVO Maria Gual Sánchez, Miguel Angel Molina Gutiérrez, Pedro Maria Rubio Aparicio, Diego Plaza López de Sabando, Ana Sastre Urgelles, Santos
