La EMA confirma las recomendaciones para minimizar el riesgo de LMP, una infección cerebral, con Tysabri
|
|
|
- Guillermo Crespo Sandoval
- hace 5 años
- Vistas:
Transcripción
1 25/04/2016 EMA/266665/2016 La EMA confirma las recomendaciones para minimizar el riesgo de LMP, una infección Se deberá considerar la realización de resonancias magnéticas más frecuentes en los pacientes expuestos a un mayor riesgo El 16 de febrero de 2016, la EMA finalizó su revisión del riesgo conocido de leucoencefalopatía multifocal progresiva (LMP) con el medicamento para la esclerosis múltiple Tysabri (natalizumab) y confirmó las recomendaciones iniciales 1 dirigidas a minimizar el riesgo. La LMP es una infección cerebral rara causada por el virus John Cunningham (JC). Este virus es muy frecuente entre la población en general y normalmente es inofensivo; sin embargo, puede dar lugar a LMP en personas cuyo sistema inmunitario está debilitado. Los síntomas más frecuentes de LMP son debilidad progresiva, dificultades en el habla y en la comunicación, cambios en la visión y en ocasiones cambios en el estado de ánimo o en la conducta. La LMP es una patología muy grave que puede dar lugar a discapacidad grave o muerte. Estudios recientes sugieren que la detección y el tratamiento tempranos de la LMP cuando la enfermedad es asintomática (todavía está en los estadios iniciales y no muestra ningún síntoma) pueden mejorar los resultados de los pacientes. Los casos asintomáticos de LMP pueden detectarse con resonancias magnéticas (RM) y los expertos en el área de RM y esclerosis múltiple concuerdan en que unos protocolos de RM más sencillos (que habiliten procedimientos más breves y limiten también la carga para los pacientes sometidos a las resonancias) permiten la identificación de las lesiones de LMP. Todos los pacientes que toman Tysabri se deben someter a RM completas al menos una vez al año, pero basándose en los nuevos datos, la EMA ha recomendado que en el caso de los pacientes con mayor riesgo de LMP se considere la realización de RM más frecuentes (p. ej. cada entre 3 y 6 meses), utilizando protocolos más sencillos. Si se localizan lesiones que indiquen la presencia de LMP, el protocolo de RM se deberá ampliar para incluir RM ponderadas en T1 con realce por contraste y se deberá considerar la realización de pruebas en el líquido cefalorraquídeo para detectar la presencia del virus JC. Nuevos datos procedentes de estudios clínicos a gran escala indican también que, en pacientes a los que no se ha tratado con inmunosupresores (medicamentos que reducen la actividad del sistema inmunitario) antes de comenzar con Tysabri, el nivel de anticuerpos en sangre contra el virus JC ( índice de anticuerpos ) guarda relación con el nivel de riesgo de LMP. A la luz de las nuevas pruebas, se considera que los pacientes presentan un mayor riesgo de desarrollar LMP si: 1 Recomendaciones del PRAC publicadas en 11 de febrero de Churchill Place Canary Wharf London E14 5EU United Kingdom Telephone +44 (0) Facsimile +44 (0) Send a question via our website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 han dado un resultado positivo en una prueba de virus JC y han recibido tratamiento con Tysabri durante más de 2 años y han utilizado un inmunosupresor antes de comenzar con Tysabri o no han utilizado inmunosupresores y presentan un elevado índice de anticuerpos contra el virus JC. En estos pacientes, solo deberá mantenerse el tratamiento con Tysabri si los beneficios superan a los riesgos. Si se sospecha la existencia de LMP en cualquier momento, se debe interrumpir el tratamiento con Tysabri hasta que haya quedado excluida la posibilidad de LMP. Las recomendaciones de la EMA se basan en una revisión inicial efectuada por su Comité para la Evaluación de Riesgos en Farmacovigilancia (PRAC). Las recomendaciones del PRAC fueron enviadas al Comité de Medicamentos de Uso Humano (CHMP), que las confirmó y adoptó su dictamen definitivo. El dictamen del CHMP se envió a continuación a la Comisión Europea, que emitió una decisión definitiva jurídicamente vinculante y válida para toda la UE. Información destinada a los pacientes Se sabe que la leucoencefalopatía multifocal progresiva (LMP, una infección cerebral grave) es un riesgo poco frecuente del medicamento para la esclerosis múltiple Tysabri. Se han publicado nuevas recomendaciones que pueden contribuir a la detección temprana de la LMP y a mejorar los resultados en los pacientes. Su riesgo de LMP depende de varios factores, como el hecho de que presente anticuerpos contra el virus JC en la sangre (un signo de que ha estado expuesto al virus que provoca la LMP) y cuál es su nivel, durante cuánto tiempo ha recibido tratamiento con Tysabri y si ha recibido tratamiento o no con medicamentos que supriman su sistema inmunitario antes de comenzar con Tysabri. Su médico le podrá aconsejar sobre el riesgo de desarrollar LMP, teniendo en cuenta estos factores. Antes de iniciar el tratamiento con Tysabri, y a continuación con regularidad durante el tratamiento, su médico realizará análisis de sangre para medir el nivel de anticuerpos frente al virus JC, así com RM a fin de supervisar su patología. Su médico también comprobará los signos y síntomas que indiquen la presencia de LMP. Estas pruebas pueden realizarse con más frecuencia si se considera que usted presenta un mayor riesgo de LMP. Si se sospecha la existencia de LMP, su médico interrumpirá el tratamiento con Tysabri hasta que pueda descartarse la LMP. Los síntomas de LMP pueden ser similares a los de un ataque de esclerosis múltiple e incluyen debilidad progresiva, dificultades del habla y la comunicación, problemas de visión y a veces cambios en el estado de ánimo o en la conducta. Si cree que su enfermedad está empeorando o aprecia cualquier síntoma inusual al usar Tysabri o durante los 6 meses después de interrumpir el tratamiento con Tysabri, consulte a su médico lo antes posible. En la tarjeta de alerta para el paciente que le ha entregado su médico se incluye información adicional sobre el riesgo de LMP con Tysabri. Es importante que lea esta tarjeta atentamente. Lleve esta tarjeta consigo y asegúrese de que su pareja o su cuidador conoce su contenido. Si tiene alguna duda o pregunta, consulte a su médico, enfermero o farmacéutico. EMA/266665/2016 Página 2/2
3 Información destinada a los profesionales sanitarios Los factores de riesgo conocidos para el desarrollo de LMP en pacientes tratados con Tysabri son la presencia de anticuerpos contra el virus JC, el tratamiento con Tysabri durante más de dos años y el uso anterior de inmunosupresores. Los datos agrupados de estudios clínicos de a gran escala indican que, en pacientes que no han empleado anteriormente inmunosupresores, el nivel de respuesta de anticuerpos frente al virus JC (índice) guarda relación con el nivel de riesgo de LMP. Basándose en estos datos, se dispone de estimaciones actualizadas sobre el riesgo de LMP 2 en pacientes con un resultado positivo de anticuerpos contra el JC tratados con Tysabri, tal y como se muestra en la Tabla 1 a continuación: Tabla1: Estimaciones del riesgo de LMP por pacientes en pacientes con un resultado positivo de anticuerpos frente al virus JC* Duración del tratamiento con Tysabri Sin uso anterior de inmunosupresores Sin valor del Índice de 0,9 Índice de 0,9 Índice de más índice o menos a 1,5 de 1,5 Uso anterior de inmunosupresores 1-12 meses 0,1 0,1 0,1 0,2 0, meses 0,6 0,1 0,3 0,9 0, meses 2 0,2 0, meses 4 0, meses 5 0, meses 6 0, *De la información para el médico de Tysabri y de las directrices de tratamiento Las estimaciones actualizadas del riesgo que aparecen arriba muestran que el riesgo de desarrollar LMP es pequeño e inferior a lo que se había estimado anteriormente, con valores del índice de anticuerpos de 0,9 o menos, y que aumenta considerablemente en pacientes con valores del índice por encima de 1,5 que han recibido tratamiento con Tysabri durante más de 2 años. En pacientes que dieron un resultado negativo de anticuerpos frente al virus JC, la estimación del riesgo de LMP permanece sin cambios con un valor de 0,1 por cada pacientes. La información para el médico y las directrices de tratamiento de Tysabri actualizadas incluirán información más detallada sobre la estratificación del riesgo, el diagnóstico y el tratamiento de la LMP. Los profesionales sanitarios deberán seguir estas recomendaciones: Antes de iniciar el tratamiento con Tysabri, se deberá advertir a pacientes y a cuidadores sobre el riesgo de LMP. Se deberá indicar a los pacientes que acudan al médico si piensan que su enfermedad está empeorando o si notan cualquier síntoma nuevo o inusual. Antes de comenzar el tratamiento, deberá disponerse de una RM de base (generalmente en un plazo de 3 meses) como referencia, y se deberá realizar un test basal de anticuerpos frente al VJC para respaldar la estratificación del riesgo de LMP. 2 Las estimaciones del riesgo de LMP se obtuvieron utilizando el método de tabla de vida basándose en una cohorte agrupada de pacientes que participaron en los estudios clínicos STRATIFY-2, TOP, TYGRIS y STRATA. Se realizó una mayor estratificación del riesgo de LMP mediante intervalos del índice de anticuerpos frente al virus JC en pacientes sin uso anterior de inmunosupresores, combinando el riesgo anual global con la distribución del índice de anticuerpos. EMA/266665/2016 Página 3/3
4 Durante el tratamiento con Tysabri se deberá monitorizar a los pacientes a intervalos regulares para detectar signos y síntomas de una nueva alteración neurológica y se deberá realizar una RM cerebral completa al menos una vez al año durante todo el tiempo que dure el tratamiento. En el caso de los pacientes con un mayor riesgo de LMP, se deberá analizara la conveniencia de realizar RM más frecuentes (p. ej. cada 3-6 meses) utilizando un protocolo abreviado (p. ej. FLAIR, ponderada en T2 o ponderada en difusión), ya que la detección temprana de la LMP en pacientes asintomáticos se asocia a unos mejores resultados de la LMP. Se deberá estudiar la realización de LMP en el diagnóstico diferencial de cualquier paciente que presente síntomas neurológicos y/o nuevas lesiones cerebrales en la RM. Se han comunicado casos de LMP asintomática basándose en la RM y en resultados positivos de ADN del virus JC en el LCR. Si se sospecha la existencia de LMP, el protocolo de RM se deberá ampliar para incluir resonancia ponderada en T1 con realce por contraste y se deberán considerar la conveniencia de tests de LCR para detectar la presencia de ADN del virus JC utilizando una RCP ultrasensible. Si se sospecha en cualquier momento la existencia de LMP, se debe interrumpir el tratamiento con Tysabri hasta que se haya excluido la posibilidad de LMP. Se deberán realizar pruebas de anticuerpos frente al virus JC cada 6 meses en pacientes con resultados de anticuerpos negativos. Los pacientes que presentan bajos valores del índice y no tienen antecedentes de un uso anterior de inmunosupresores deberán someterse también a pruebas cada 6 meses, una vez que alcancen los 2 años de tratamiento. Al cabo de 2 años de tratamiento, será necesario volver a informar a los pacientes sobre el riesgo de LMP con Tysabri. Se aconsejará a los pacientes y cuidadores que permanezcan vigilantes ante el riesgo de LMP hasta 6 meses después de abandonar el tratamiento con Tysabri. Más información sobre el medicamento Tysabri es un medicamento utilizado para el tratamiento de adultos con esclerosis múltiple (EM) muy activa, una enfermedad neurológica en la que una inflamación destruye las vainas protectoras que rodean a las células nerviosas. Tysabri se utiliza en el tipo de EM conocido como EM recidivanteremitente, en la que el paciente sufre ataques (recaídas) entre períodos sin síntomas (remisiones). Se utiliza cuando la enfermedad ha dejado de responder al beta-interferón o acetato de glatiramer (otros tipos de medicamento utilizados en la EM), o es severa y empeora rápidamente. El principio activo de Tysabri, natalizumab, es un anticuerpo monoclonal (un tipo de proteína) que se ha creado para reconocer y acoplarse a una parte específica de una proteína denominada α4β1 integrina. Esta proteína se encuentra en la superficie de la mayoría de leucocitos (los glóbulos blancos de la sangre que intervienen en el proceso inflamatorio). Al acoplarse a la integrina, el natalizumab evita que los leucocitos pasen de la sangre al cerebro, con lo que se reduce la inflamación y la lesión nerviosa causada por la EM. Tysabri fue autorizado en la Unión Europea en junio de EMA/266665/2016 Página 4/4
5 Más información sobre el procedimiento La revisión de Tysabri se inició el 7 de mayo de 2015 a petición de la Comisión Europea, de conformidad con el Artículo 20 del Reglamento (CE) n.º 726/2004. La revisión fue realizada en primer lugar por el Comité para la Evaluación de Riesgos en Farmacovigilancia (PRAC), el comité responsable de evaluar los problemas de seguridad en los medicamentos de uso humano, que formuló una serie de recomendaciones. Las recomendaciones del PRAC se enviaron al Comité de Medicamentos de Uso Humano (CHMP), el responsable de todas las cuestiones relativas a los medicamentos de uso humano, que adoptó el dictamen definitivo de la Agencia. El dictamen del CHMP se remitió a la Comisión Europea, que emitió una decisión final legalmente vinculante para todos los Estados miembros de la UE el 25/04/2016. Datos de contacto de nuestra oficina de prensa Monika Benstetter Tel. +44 (0) Correo electrónico: press@ema.europa.eu EMA/266665/2016 Página 5/5
Anexo IV. Conclusiones científicas
 Anexo IV Conclusiones científicas 38 Conclusiones científicas Las pruebas científicas sobre la leucoencefalopatía multifocal progresiva (LMP) en pacientes tratados con Tysabri son cada vez más numerosas.
Anexo IV Conclusiones científicas 38 Conclusiones científicas Las pruebas científicas sobre la leucoencefalopatía multifocal progresiva (LMP) en pacientes tratados con Tysabri son cada vez más numerosas.
Comunicación dirigida a profesionales sanitarios
 Comunicación dirigida a profesionales sanitarios Tecfidera (dimetilfumarato): Nuevas recomendaciones para minimizar el riesgo de leucoencefalopatía multifocal progresiva. Intensificación de las medidas
Comunicación dirigida a profesionales sanitarios Tecfidera (dimetilfumarato): Nuevas recomendaciones para minimizar el riesgo de leucoencefalopatía multifocal progresiva. Intensificación de las medidas
Materiales educativos para los profesionales sanitarios y los pacientes que utilizan el medicamento antidiabético Suliqua
 19 de enero de 2017 EMA/747766/2016 Materiales educativos para los profesionales sanitarios y los pacientes que utilizan el medicamento antidiabético Suliqua Medidas para reducir el riesgo de confusión
19 de enero de 2017 EMA/747766/2016 Materiales educativos para los profesionales sanitarios y los pacientes que utilizan el medicamento antidiabético Suliqua Medidas para reducir el riesgo de confusión
Para más información sobre el tratamiento con Keytruda, el paciente deberá leer el prospecto o consultar a su médico o farmacéutico.
 EMA/524789/2017 EMEA/H/C/003820 Resumen del EPAR para el público general pembrolizumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia
EMA/524789/2017 EMEA/H/C/003820 Resumen del EPAR para el público general pembrolizumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia
Para más información sobre el tratamiento con Simponi, el paciente deberá leer el prospecto o consultar a su médico o farmacéutico.
 EMA/412395/2016 EMEA/H/C/000992 Resumen del EPAR para el público general golimumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo la Agencia ha evaluado
EMA/412395/2016 EMEA/H/C/000992 Resumen del EPAR para el público general golimumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo la Agencia ha evaluado
Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto
 25 January 2018 EMA/PRAC/35608/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC en su reunión
25 January 2018 EMA/PRAC/35608/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC en su reunión
Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto
 25 February 2016 EMA/PRAC/137780/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto Adoptado por el PRAC el
25 February 2016 EMA/PRAC/137780/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto Adoptado por el PRAC el
Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
 23 April 2015 EMA/PRAC/273926/2015 Pharmacovigilance Risk Assessment Committee Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto Adoptado por el PRAC
23 April 2015 EMA/PRAC/273926/2015 Pharmacovigilance Risk Assessment Committee Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto Adoptado por el PRAC
Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
 22 de enero de 2015 EMA/PRAC/63326/2015 Comité para la Determinación del Riesgo en farmacovigilancia Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
22 de enero de 2015 EMA/PRAC/63326/2015 Comité para la Determinación del Riesgo en farmacovigilancia Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto:
 17 December 2015 EMA/PRAC/835774/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto: Adoptado por el PRAC, 30
17 December 2015 EMA/PRAC/835774/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de la información sobre el producto: Adoptado por el PRAC, 30
GUÍA DEL MEDICAMENTO. TYSABRI (natalizumab)
 GUÍA DEL MEDICAMENTO TYSABRI (natalizumab) Lea la Guía del Medicamento antes de comenzar a usar TYSABRI y antes de cada infusión. Puede haber información nueva. Esta Guía del Medicamento no reemplaza una
GUÍA DEL MEDICAMENTO TYSABRI (natalizumab) Lea la Guía del Medicamento antes de comenzar a usar TYSABRI y antes de cada infusión. Puede haber información nueva. Esta Guía del Medicamento no reemplaza una
Criterios diagnósticos para la Esclerosis Múltiple. Evolución de los criterios de Mc Donald.
 Criterios diagnósticos para la Esclerosis Múltiple. Evolución de los criterios de Mc Donald. Poster no.: S-0890 Congreso: SERAM 2012 Tipo del póster: Presentación Electrónica Educativa Autores: A. Joaquín
Criterios diagnósticos para la Esclerosis Múltiple. Evolución de los criterios de Mc Donald. Poster no.: S-0890 Congreso: SERAM 2012 Tipo del póster: Presentación Electrónica Educativa Autores: A. Joaquín
Información general sobre Eylea y sobre los motivos por los que se autoriza su uso en la UE
 EMA/481361/2018 EMEA/H/C/002392 Información general sobre Eylea y sobre los motivos por los que se autoriza su uso en la UE Qué es Eylea y para qué se utiliza? Eylea es un medicamento que se usa para tratar
EMA/481361/2018 EMEA/H/C/002392 Información general sobre Eylea y sobre los motivos por los que se autoriza su uso en la UE Qué es Eylea y para qué se utiliza? Eylea es un medicamento que se usa para tratar
Para obtener información práctica sobre el tratamiento con Opdivo, el paciente deberá leer el prospecto o consultar a su médico o farmacéutico.
 EMA/691693/2017 EMEA/H/C/003985 Resumen del EPAR para el público general nivolumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia ha
EMA/691693/2017 EMEA/H/C/003985 Resumen del EPAR para el público general nivolumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia ha
Preguntas más frecuentes
 13 de febrero de 2017 EMA/527628/2011 Rev. 1 Dirección Este documento contiene respuestas a las preguntas más frecuentes recibidas por la Agencia Europea de Medicamentos (EMA). Si no encuentra aquí la
13 de febrero de 2017 EMA/527628/2011 Rev. 1 Dirección Este documento contiene respuestas a las preguntas más frecuentes recibidas por la Agencia Europea de Medicamentos (EMA). Si no encuentra aquí la
Restricciones de uso de los medicamentos que contienen domperidona
 1 de septiembre de 2014 EMA/465179/2014 Restricciones de uso de los medicamentos que contienen domperidona El 23 de abril de 2014, el Grupo de Coordinación de los Procedimientos de Reconocimiento Mutuo
1 de septiembre de 2014 EMA/465179/2014 Restricciones de uso de los medicamentos que contienen domperidona El 23 de abril de 2014, el Grupo de Coordinación de los Procedimientos de Reconocimiento Mutuo
Guía para la interpretación de informes espontáneos de presuntas reacciones adversas a medicamentos
 30 de enero de 2017 Inspecciones, Farmacovigilancia de Medicamentos de Uso Humano y Comités EMA/749446/2016 Revisión 1* Guía para la interpretación de informes espontáneos de presuntas reacciones adversas
30 de enero de 2017 Inspecciones, Farmacovigilancia de Medicamentos de Uso Humano y Comités EMA/749446/2016 Revisión 1* Guía para la interpretación de informes espontáneos de presuntas reacciones adversas
En el mieloma múltiple, un cáncer de un tipo de glóbulos blancos denominados células de descarga, Revlimid se utiliza:
 EMA/113870/2017 EMEA/H/C/000717 Resumen del EPAR para el público lenalidomida El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia ha evaluado
EMA/113870/2017 EMEA/H/C/000717 Resumen del EPAR para el público lenalidomida El presente documento resume el Informe Público Europeo de Evaluación (EPAR) para. En él se explica cómo la Agencia ha evaluado
Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto
 15 September 2016 EMA/PRAC/603550/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC el 30
15 September 2016 EMA/PRAC/603550/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Recomendaciones del PRAC sobre señales: nuevo texto de información sobre el producto Adoptado por el PRAC el 30
Esclerosis Múltiple. Dra. Irene Treviño Frenk Neuróloga, Especialista en Esclerosis Múltiple Departamento de Neurología y Psiquiatría
 Esclerosis Múltiple Dra. Irene Treviño Frenk Neuróloga, Especialista en Esclerosis Múltiple Departamento de Neurología y Psiquiatría ESCLEROSIS MÚLTIPLE Qué es la esclerosis múltiple? La esclerosis múltiple
Esclerosis Múltiple Dra. Irene Treviño Frenk Neuróloga, Especialista en Esclerosis Múltiple Departamento de Neurología y Psiquiatría ESCLEROSIS MÚLTIPLE Qué es la esclerosis múltiple? La esclerosis múltiple
Guía del medicamento para el paciente
 Guía del medicamento para el paciente Guía del medicamento para el paciente GUÍA DEL MEDICAMENTO TYSABRI (tai-sa-bri) (natalizumab) inyectable, para uso intravenoso Lea esta Guía del medicamento antes
Guía del medicamento para el paciente Guía del medicamento para el paciente GUÍA DEL MEDICAMENTO TYSABRI (tai-sa-bri) (natalizumab) inyectable, para uso intravenoso Lea esta Guía del medicamento antes
CUESTIONARIO PARA NIÑOS Y ADOLESCENTES
 Punto de vista acerca del consumo de medicamentos Por qué preguntamos? El Comité Pediátrico (PDCO) trabaja con la Agencia Europea de Medicamentos, y es su trabajo asegurarse de que los medicamentos para
Punto de vista acerca del consumo de medicamentos Por qué preguntamos? El Comité Pediátrico (PDCO) trabaja con la Agencia Europea de Medicamentos, y es su trabajo asegurarse de que los medicamentos para
Tratamiento modificador de enfermedad en pacientes con diagnóstico de
 GUÍA DE PRÁCTICA CLÍNICA gpc Tratamiento modificador de enfermedad en pacientes con diagnóstico de ESCLEROS MULTIPLE Guía de referencia rápida Catálogo maestro de guías de práctica clínica: SSA-417-10
GUÍA DE PRÁCTICA CLÍNICA gpc Tratamiento modificador de enfermedad en pacientes con diagnóstico de ESCLEROS MULTIPLE Guía de referencia rápida Catálogo maestro de guías de práctica clínica: SSA-417-10
JUNTO CON TYSABRI PARA LA EM REMITENTE RECIDIVANTE
 SI RECIBE TRATAMIENTO CON (NATALIZUMAB) JUNTO CON TYSABRI PARA LA EM REMITENTE RECIDIVANTE Lea detenidamente el prospecto de información que acompaña a este medicamento. 1 Este folleto es un complemento
SI RECIBE TRATAMIENTO CON (NATALIZUMAB) JUNTO CON TYSABRI PARA LA EM REMITENTE RECIDIVANTE Lea detenidamente el prospecto de información que acompaña a este medicamento. 1 Este folleto es un complemento
La Agencia Europea de Medicamentos recomienda cambios en el uso de la metoclopramida
 20 de diciembre de 2013 EMA/13239/2014 Corr. 1 La Agencia Europea de Medicamentos recomienda cambios en el uso de la El principal objetivo de los cambios es reducir el riesgo de efectos neurológicos secundarios
20 de diciembre de 2013 EMA/13239/2014 Corr. 1 La Agencia Europea de Medicamentos recomienda cambios en el uso de la El principal objetivo de los cambios es reducir el riesgo de efectos neurológicos secundarios
En la audiencia pública, se tendrá debidamente en cuenta el efecto terapéutico del medicamento.
 13 de abril de 2016 EMA/389918/2016 Normas reguladoras del procedimiento para la organización y realización de audiencias públicas en el Comité para la Evaluación de Riesgos en Farmacovigilancia (PRAC)
13 de abril de 2016 EMA/389918/2016 Normas reguladoras del procedimiento para la organización y realización de audiencias públicas en el Comité para la Evaluación de Riesgos en Farmacovigilancia (PRAC)
Preguntas más frecuentes
 4 de noviembre de 2011 EMA/527628/2011 Dirección Este documento contiene respuestas a las preguntas más frecuentes recibidas por la Agencia Europea de Medicamentos. Si no encuentra aquí la respuesta a
4 de noviembre de 2011 EMA/527628/2011 Dirección Este documento contiene respuestas a las preguntas más frecuentes recibidas por la Agencia Europea de Medicamentos. Si no encuentra aquí la respuesta a
Anexo III. Modificaciones a las secciones relevantes de ficha técnica y prospecto
 Anexo III Modificaciones a las secciones relevantes de ficha técnica y prospecto Nota: La ficha técnica o resumen de las características del producto y el prospecto pueden necesitar ser actualizados posteriormente
Anexo III Modificaciones a las secciones relevantes de ficha técnica y prospecto Nota: La ficha técnica o resumen de las características del producto y el prospecto pueden necesitar ser actualizados posteriormente
Introducción al programa de trabajo de la Agencia para 2015
 7 agosto 2015 EMA/372784/2015 Director Ejecutivo Adjunto Introducción al programa de trabajo de la Agencia para 2015 Por Andreas Pott, Director Ejecutivo Adjunto Prioridades de la EMA y circunstancias
7 agosto 2015 EMA/372784/2015 Director Ejecutivo Adjunto Introducción al programa de trabajo de la Agencia para 2015 Por Andreas Pott, Director Ejecutivo Adjunto Prioridades de la EMA y circunstancias
Guía de usuario para los informes de web
 Protección de la salud de los pacientes Esta guía de usuario para los informes de web facilita información sobre tipos de datos, presentacion, interpretación y funcionalidades del informe de web. 1. Tipos
Protección de la salud de los pacientes Esta guía de usuario para los informes de web facilita información sobre tipos de datos, presentacion, interpretación y funcionalidades del informe de web. 1. Tipos
Introducción al programa de trabajo de la Agencia para 2016
 8 de febrero de 2016 EMA/171279/2016 Director ejecutivo Introducción al programa de trabajo de la Agencia para 2016 Por Guido Rasi, Director Ejecutivo Prioridades de la EMA e influencias clave La red europea
8 de febrero de 2016 EMA/171279/2016 Director ejecutivo Introducción al programa de trabajo de la Agencia para 2016 Por Guido Rasi, Director Ejecutivo Prioridades de la EMA e influencias clave La red europea
Información general sobre Opdivo y sobre los motivos por los que se autoriza su uso en la UE
 EMA/489091/2018 EMEA/H/C/003985 Información general sobre Opdivo y sobre los motivos por los que se autoriza su uso en la UE Qué es Opdivo y para qué se utiliza? Opdivo es un medicamento contra el cáncer
EMA/489091/2018 EMEA/H/C/003985 Información general sobre Opdivo y sobre los motivos por los que se autoriza su uso en la UE Qué es Opdivo y para qué se utiliza? Opdivo es un medicamento contra el cáncer
SI ESTÁ RECIBIENDO TRATAMIENTO CON TYSABRI (NATALIZUMAB) TYSABRI PARA LA ESCLEROSIS MÚLTIPLE (EM) REMITENTE RECIDIVANTE
 SI ESTÁ RECIBIENDO TRATAMIENTO CON TYSABRI (NATALIZUMAB) TYSABRI PARA LA ESCLEROSIS MÚLTIPLE (EM) REMITENTE RECIDIVANTE 2 Este folleto es un complemento a la información que el profesional sanitario ofrece
SI ESTÁ RECIBIENDO TRATAMIENTO CON TYSABRI (NATALIZUMAB) TYSABRI PARA LA ESCLEROSIS MÚLTIPLE (EM) REMITENTE RECIDIVANTE 2 Este folleto es un complemento a la información que el profesional sanitario ofrece
Toctino (alitretinoína)
 1 GUÍA PARA EL PACIENTE Información importante de seguridad para la paciente a tratamiento con PARA LA PACIENTE Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos
1 GUÍA PARA EL PACIENTE Información importante de seguridad para la paciente a tratamiento con PARA LA PACIENTE Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos
Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS)_Agosto_2016
 KEYTRUDA (pembrolizumab) Información para pacientes Keytruda es un medicamento biológico Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios
KEYTRUDA (pembrolizumab) Información para pacientes Keytruda es un medicamento biológico Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios
Información para Profesionales de la Salud
 El Comité de Medicamentos de Uso Humano (CHMP) adoptó una opinión basada en la recomendación del Comité de Evaluación del Riesgo de Farmacovigilancia (PRAC) sobre Esmya Budapest, Hungría 01 junio 2018
El Comité de Medicamentos de Uso Humano (CHMP) adoptó una opinión basada en la recomendación del Comité de Evaluación del Riesgo de Farmacovigilancia (PRAC) sobre Esmya Budapest, Hungría 01 junio 2018
Neuritis Optica. Su médico piensa que usted ha tenido un episodio de neuritis óptica. Esta es la causa más
 Neuritis Optica Su médico piensa que usted ha tenido un episodio de neuritis óptica. Esta es la causa más común de pérdida visual súbita en un paciente joven. Se asocia comúnmente con dolor alrededor del
Neuritis Optica Su médico piensa que usted ha tenido un episodio de neuritis óptica. Esta es la causa más común de pérdida visual súbita en un paciente joven. Se asocia comúnmente con dolor alrededor del
El sistema europeo de regulación de medicamentos
 El sistema europeo de regulación de medicamentos Un enfoque uniforme para la regulación de los medicamentos en toda la Unión Europea An agency of the European Union El sistema europeo de regulación de
El sistema europeo de regulación de medicamentos Un enfoque uniforme para la regulación de los medicamentos en toda la Unión Europea An agency of the European Union El sistema europeo de regulación de
BIOMARCADORES: SU UTILIDAD EN ESCLEROSIS MÚLTIPLE (EM)
 BIOMARCADORES: SU UTILIDAD EN ESCLEROSIS MÚLTIPLE (EM) Dr. Daniel Raul Zuin Fundación Cerebro y Mente: Director Universidad de Mendoza: Profesor Titular Neurología Definición: Se considera como biomarcador
BIOMARCADORES: SU UTILIDAD EN ESCLEROSIS MÚLTIPLE (EM) Dr. Daniel Raul Zuin Fundación Cerebro y Mente: Director Universidad de Mendoza: Profesor Titular Neurología Definición: Se considera como biomarcador
INFORMACIÓN IMPORTANTE PARA EL PACIENTE
 Si experimenta cualquier po de efecto adverso, consulte a su médico o farmacéu co, incluso si se trata de posibles efectos adveros que no aparecen en el prospecto. También puede comunicarlos directamente
Si experimenta cualquier po de efecto adverso, consulte a su médico o farmacéu co, incluso si se trata de posibles efectos adveros que no aparecen en el prospecto. También puede comunicarlos directamente
ENFERMEDAD DE CREUTZFELDT-JAKOB: hallazgos en Resonancia Magnética.
 ENFERMEDAD DE CREUTZFELDT-JAKOB: hallazgos en Resonancia Magnética. Poster no.: S-0668 Congreso: SERAM 2012 Tipo del póster: Presentación Electrónica Educativa Autores: 1 2 3 B. Sanchez Cordon, G. Liaño
ENFERMEDAD DE CREUTZFELDT-JAKOB: hallazgos en Resonancia Magnética. Poster no.: S-0668 Congreso: SERAM 2012 Tipo del póster: Presentación Electrónica Educativa Autores: 1 2 3 B. Sanchez Cordon, G. Liaño
vacuna antineumocócica polisacárida conjugada (13-valente, adsorbida)
 EMA/90006/2015 EMEA/H/C/001104 Resumen del EPAR para el público general vacuna antineumocócica polisacárida conjugada (13-valente, adsorbida) El presente documento resume el Informe Público Europeo de
EMA/90006/2015 EMEA/H/C/001104 Resumen del EPAR para el público general vacuna antineumocócica polisacárida conjugada (13-valente, adsorbida) El presente documento resume el Informe Público Europeo de
Esclerosis múltiple: síntomas y tratamientos
 Esclerosis múltiple: síntomas y tratamientos La esclerosis múltiple, o EM, es una enfermedad de larga duración que puede afectar su cerebro, la médula espinal y los nervios ópticos en sus ojos. Puede causar
Esclerosis múltiple: síntomas y tratamientos La esclerosis múltiple, o EM, es una enfermedad de larga duración que puede afectar su cerebro, la médula espinal y los nervios ópticos en sus ojos. Puede causar
Comunicación dirigida a Profesionales Sanitarios
 Comunicación dirigida a Profesionales Sanitarios Julio de 2015 XGEVA (denosumab): medidas establecidas para minimizar el riesgo de osteonecrosis mandibular Estimado Profesional Sanitario, Amgen S.A. de
Comunicación dirigida a Profesionales Sanitarios Julio de 2015 XGEVA (denosumab): medidas establecidas para minimizar el riesgo de osteonecrosis mandibular Estimado Profesional Sanitario, Amgen S.A. de
Comprender su tratamiento con Tecfidera. Información para pacientes a los que se les ha recetado el tratamiento con Tecfidera.
 Comprender su tratamiento con Tecfidera Información para pacientes a los que se les ha recetado el tratamiento con Tecfidera. Contenidos Tratamiento con Tecfidera Información sobre la esclerosis múltiple
Comprender su tratamiento con Tecfidera Información para pacientes a los que se les ha recetado el tratamiento con Tecfidera. Contenidos Tratamiento con Tecfidera Información sobre la esclerosis múltiple
ANEXO III Modificaciones a las secciones relevantes de Ficha Técnica y Prospecto
 ANEXO III Modificaciones a las secciones relevantes de Ficha Técnica y Prospecto Nota: Si procede, la ficha técnica o resumen de las características del producto y el prospecto pueden necesitar ser actualizados
ANEXO III Modificaciones a las secciones relevantes de Ficha Técnica y Prospecto Nota: Si procede, la ficha técnica o resumen de las características del producto y el prospecto pueden necesitar ser actualizados
Avastin se utiliza para el tratamiento de adultos con los siguientes tipos de cáncer en combinación con otros medicamentos contra el cáncer:
 EMA/175824/2015 EMEA/H/C/000582 Resumen del EPAR para el público general bevacizumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de
EMA/175824/2015 EMEA/H/C/000582 Resumen del EPAR para el público general bevacizumab El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de
Intervención enfermera en el Uso adecuado del Medicamento y Productos Sanitarios
 Intervención enfermera en el Uso adecuado del Medicamento y Productos Sanitarios Contenidos Introducción Uso Adecuado del Medicamento Selección e información de medicamentos Farmacovigilancia Módulo de
Intervención enfermera en el Uso adecuado del Medicamento y Productos Sanitarios Contenidos Introducción Uso Adecuado del Medicamento Selección e información de medicamentos Farmacovigilancia Módulo de
PARA USTED, si está recibiendo Tysabri (natalizumab) como tratamiento para EM remitente recidivante
 PARA USTED, si está recibiendo Tysabri (natalizumab) como tratamiento para EM remitente recidivante Lea detenidamente el prospecto de información que acompaña a este medicamento. 1 SI RECIBE TRATAMIENTO
PARA USTED, si está recibiendo Tysabri (natalizumab) como tratamiento para EM remitente recidivante Lea detenidamente el prospecto de información que acompaña a este medicamento. 1 SI RECIBE TRATAMIENTO
PROGRAMA PROVINCIAL DE FARMACOVIGILANCIA
 PROGRAMA PROVINCIAL DE FARMACOVIGILANCIA BOLETÍN INFORMATIVO: Nº 09/2016 NOVEDADES NACIONALES E INTERNACIONALES EN SEGURIDAD DE MEDICAMENTOS NOVEDADES INTERNACIONALES DE AGENCIAS REGULADORAS INHIBIDORES
PROGRAMA PROVINCIAL DE FARMACOVIGILANCIA BOLETÍN INFORMATIVO: Nº 09/2016 NOVEDADES NACIONALES E INTERNACIONALES EN SEGURIDAD DE MEDICAMENTOS NOVEDADES INTERNACIONALES DE AGENCIAS REGULADORAS INHIBIDORES
Diagnóstico de la. enfermedad de. T1m61n! Alzheimer
 enfermedad de Alzheimer T1m61n! La demencia es un término general utilizado para nombrar una disminución severa en la habilidad mental de las personas. Esta disminución es lo suficientemente grave como
enfermedad de Alzheimer T1m61n! La demencia es un término general utilizado para nombrar una disminución severa en la habilidad mental de las personas. Esta disminución es lo suficientemente grave como
Anexo IV. Conclusiones científicas
 Anexo IV Conclusiones científicas 1 Conclusiones científicas Se han notificado cuatro casos de lesión hepática grave que condujo a un trasplante hepático desde la autorización de comercialización de Esmya.
Anexo IV Conclusiones científicas 1 Conclusiones científicas Se han notificado cuatro casos de lesión hepática grave que condujo a un trasplante hepático desde la autorización de comercialización de Esmya.
ÍNDICE PRÓLOGO PRESENTACIÓN CAPÍTULO 1 QUÉ ES LA ESCLEROSIS MÚLTIPLE Y POR QUÉ SE PRODUCE?..
 ÍNDICE PRÓLOGO... 19 PRESENTACIÓN... 23 CAPÍTULO 1 QUÉ ES LA ESCLEROSIS MÚLTIPLE Y POR QUÉ SE PRODUCE?.. 25 1. Qué es la esclerosis múltiple?... 26 2. Qué es el Sistema Nervioso Central?... 26 3. Cuántas
ÍNDICE PRÓLOGO... 19 PRESENTACIÓN... 23 CAPÍTULO 1 QUÉ ES LA ESCLEROSIS MÚLTIPLE Y POR QUÉ SE PRODUCE?.. 25 1. Qué es la esclerosis múltiple?... 26 2. Qué es el Sistema Nervioso Central?... 26 3. Cuántas
DICTAMEN DEFINITIVO DEL COMITÉ DE ESPECIALIDADES FARMACÉUTICAS DE CONFORMIDAD CON EL ARTÍCULO 12 DE LA DIRECTIVA 75/319/CEE MODIFICADA, PARA
 The European Agency for the Evaluation of Medicinal Products Human Medicines Evaluation Unit CPMP/375/97-ES DICTAMEN DEFINITIVO DEL COMITÉ DE ESPECIALIDADES FARMACÉUTICAS DE CONFORMIDAD CON EL ARTÍCULO
The European Agency for the Evaluation of Medicinal Products Human Medicines Evaluation Unit CPMP/375/97-ES DICTAMEN DEFINITIVO DEL COMITÉ DE ESPECIALIDADES FARMACÉUTICAS DE CONFORMIDAD CON EL ARTÍCULO
Anexo III. Modificaciones de las secciones relevantes del Resumen de las características del producto y prospecto
 Anexo III Modificaciones de las secciones relevantes del Resumen de las características del producto y prospecto Nota: Este resumen de las características del producto y prospecto son el resultado del
Anexo III Modificaciones de las secciones relevantes del Resumen de las características del producto y prospecto Nota: Este resumen de las características del producto y prospecto son el resultado del
Anexo II. Conclusiones científicas
 Anexo II Conclusiones científicas 7 Conclusiones científicas Solu-Medrol 40 mg polvo y disolvente para solución inyectable (en adelante, «Solu-Medrol») contiene metilprednisolona y, como excipiente, lactosa
Anexo II Conclusiones científicas 7 Conclusiones científicas Solu-Medrol 40 mg polvo y disolvente para solución inyectable (en adelante, «Solu-Medrol») contiene metilprednisolona y, como excipiente, lactosa
INFORMACIÓN DE SEGURIDAD PARA PROFESIONALES SANITARIOS
 Stelara (ustekinumab) INFORMACIÓN DE SEGURIDAD PARA PROFESIONALES SANITARIOS Por favor, además de la ficha técnica del producto (FT) lea detenidamente esta guía. Por favor, informe a sus pacientes sobre
Stelara (ustekinumab) INFORMACIÓN DE SEGURIDAD PARA PROFESIONALES SANITARIOS Por favor, además de la ficha técnica del producto (FT) lea detenidamente esta guía. Por favor, informe a sus pacientes sobre
El suscrito, FRANCISCO SALVADOR LÓPEZ BRITO, Senador de la República de la LXIII
 Dr. Francisco Salvador López Brito Senador de la República El suscrito, FRANCISCO SALVADOR LÓPEZ BRITO, Senador de la República de la LXIII Legislatura del Congreso de la Unión, Integrante del Grupo Parlamentario
Dr. Francisco Salvador López Brito Senador de la República El suscrito, FRANCISCO SALVADOR LÓPEZ BRITO, Senador de la República de la LXIII Legislatura del Congreso de la Unión, Integrante del Grupo Parlamentario
ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
 ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS
ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS
Protocolo HIA Etapa 1 Evaluación HIA 1:
 Protocolo HIA El protocolo de Evaluación de Lesión en la Cabeza (HIA) es un proceso de tres etapas creado por World Rugby para contribuir a la identificación, diagnóstico y manejo de eventos que incluyen
Protocolo HIA El protocolo de Evaluación de Lesión en la Cabeza (HIA) es un proceso de tres etapas creado por World Rugby para contribuir a la identificación, diagnóstico y manejo de eventos que incluyen
NUEVA ESTRATEGIA DEL PROGRAMA DE PREVENCIÓN Y DETECCIÓN PRECOZ DEL CÁNCER DE CUELLO DE ÚTERO 2008
 NUEVA ESTRATEGIA DEL PROGRAMA DE PREVENCIÓN Y DETECCIÓN PRECOZ DEL CÁNCER DE CUELLO DE ÚTERO 2008 El Programa de prevención y detección precoz de cáncer de cuello de útero tiene como objetivo general disminuir
NUEVA ESTRATEGIA DEL PROGRAMA DE PREVENCIÓN Y DETECCIÓN PRECOZ DEL CÁNCER DE CUELLO DE ÚTERO 2008 El Programa de prevención y detección precoz de cáncer de cuello de útero tiene como objetivo general disminuir
EchinaMed gotas orales en solución
 EchinaMed gotas orales en solución PROSPECTO: información para el usuario Lea todo el prospecto detenidamente porque tiene información importante para Ud. Este medicamento puede obtenerse sin receta, para
EchinaMed gotas orales en solución PROSPECTO: información para el usuario Lea todo el prospecto detenidamente porque tiene información importante para Ud. Este medicamento puede obtenerse sin receta, para
Entendiendo la. Esclerosis Múltiple
 Entendiendo la Esclerosis Múltiple Qué es la Esclerosis Múltiple Esclerosis múltiple o enfermedad desmielinizante es una enfermedad autoinmunitaria que afecta el cerebro y la médula espinal (sistema nervioso
Entendiendo la Esclerosis Múltiple Qué es la Esclerosis Múltiple Esclerosis múltiple o enfermedad desmielinizante es una enfermedad autoinmunitaria que afecta el cerebro y la médula espinal (sistema nervioso
deterioro de la visión causado por un edema macular provocado por la diabetes;
 EMA/677928/2015 EMA/H/C/002392 Resumen del EPAR para el público general aflibercept El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de Medicamentos
EMA/677928/2015 EMA/H/C/002392 Resumen del EPAR para el público general aflibercept El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de Medicamentos
Es una enfermedad autoinmune que afecta al sistema nervioso central (el cerebro y la médula espinal).
 Esclerosis Multiple Es una enfermedad autoinmune que afecta al sistema nervioso central (el cerebro y la médula espinal). Causas, incidencia y factores de riesgo La esclerosis múltiple (EM) generalmente
Esclerosis Multiple Es una enfermedad autoinmune que afecta al sistema nervioso central (el cerebro y la médula espinal). Causas, incidencia y factores de riesgo La esclerosis múltiple (EM) generalmente
Recomendaciones para prevenir el ataque cerebrovascular (ACV) Viernes, 26 de Octubre de :22
 El control de factores de riesgo como la hipertensión arterial y la adopción de hábitos saludables por parte de la población son fundamentales para prevenir el Ataque Cerebrovascular (ACV), que provoca
El control de factores de riesgo como la hipertensión arterial y la adopción de hábitos saludables por parte de la población son fundamentales para prevenir el Ataque Cerebrovascular (ACV), que provoca
Unidad de Consulta Diagnóstica. Complejo Alzheimer Fundación Reina Sofía y Fundación CIEN
 Unidad de Consulta Diagnóstica Complejo Alzheimer Fundación Reina Sofía y Fundación CIEN LA UNIDAD DE CONSULTA DIAGNÓSTICA DEL CENTRO ALZHEIMER FUNDACIÓN REINA SOFÍA Introducción La demencia conlleva por
Unidad de Consulta Diagnóstica Complejo Alzheimer Fundación Reina Sofía y Fundación CIEN LA UNIDAD DE CONSULTA DIAGNÓSTICA DEL CENTRO ALZHEIMER FUNDACIÓN REINA SOFÍA Introducción La demencia conlleva por
Comprender su tratamiento con Tecfidera
 Comprender su tratamiento con Tecfidera Información para pacientes a los que se les ha recetado el tratamiento con Tecfidera. (dimetilfumarato) Contenidos Sobre la esclerosis múltiple (EM) Qué es la EM?
Comprender su tratamiento con Tecfidera Información para pacientes a los que se les ha recetado el tratamiento con Tecfidera. (dimetilfumarato) Contenidos Sobre la esclerosis múltiple (EM) Qué es la EM?
Comprender su tratamiento con Tecfidera
 Comprender su tratamiento con Tecfidera Información para pacientes a los que se les ha recetado el tratamiento con Tecfidera. (dimetilfumarato) Contenidos Sobre la esclerosis múltiple (EM) Qué es la EM?
Comprender su tratamiento con Tecfidera Información para pacientes a los que se les ha recetado el tratamiento con Tecfidera. (dimetilfumarato) Contenidos Sobre la esclerosis múltiple (EM) Qué es la EM?
Cerca del 70% de los casos de esclerosis múltiple (EM) se presentan en edades entre los 20 y 40 años
 Detección temprana, mejor diagnóstico Esclerosis múltiple, enfermedad de jóvenes Cerca del 70% de los casos de esclerosis múltiple (EM) se presentan en edades entre los 20 y 40 años En Colombia hay cerca
Detección temprana, mejor diagnóstico Esclerosis múltiple, enfermedad de jóvenes Cerca del 70% de los casos de esclerosis múltiple (EM) se presentan en edades entre los 20 y 40 años En Colombia hay cerca
Cuando se diluye (ver sección 6.6), la solución para perfusión contiene aproximadamente 2,6 mg/ml de natalizumab.
 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones
Unidad de Consulta Diagnóstica. Complejo Alzheimer Fundación Reina Sofía y Fundación CIEN
 Unidad de Consulta Diagnóstica Complejo Alzheimer Fundación Reina Sofía y Fundación CIEN LA UNIDAD DE CONSULTA DIAGNÓSTICA DEL CENTRO ALZHEIMER FUNDACIÓN REINA SOFÍA Introducción La demencia conlleva por
Unidad de Consulta Diagnóstica Complejo Alzheimer Fundación Reina Sofía y Fundación CIEN LA UNIDAD DE CONSULTA DIAGNÓSTICA DEL CENTRO ALZHEIMER FUNDACIÓN REINA SOFÍA Introducción La demencia conlleva por
CRITERIOS DE UTILIZACION DE INMUNOMODULADORES 1 PARA EL TRATAMIENTO DE LA ESCLEROSIS MULTIPLE
 DIRECCION GENERAL DE FARMACIA Y PRODUCTOS SANITARIOS. COMITÉ ASESOR DE LA ESCLEROSIS MULTIPLE. CRITERIOS DE UTILIZACION DE INMUNOMODULADORES 1 PARA EL TRATAMIENTO DE LA ESCLEROSIS MULTIPLE Estos criterios
DIRECCION GENERAL DE FARMACIA Y PRODUCTOS SANITARIOS. COMITÉ ASESOR DE LA ESCLEROSIS MULTIPLE. CRITERIOS DE UTILIZACION DE INMUNOMODULADORES 1 PARA EL TRATAMIENTO DE LA ESCLEROSIS MULTIPLE Estos criterios
Tema 17. Registro de medicamentos. Legislación y deontología farmacéutica
 Tema 17. Registro de medicamentos Legislación y deontología farmacéutica 1 ESTATAL DISPOSICIONES LEGALES REAL DECRETO 1345/2007, de 11 de octubre, por el que se regula el procedimiento de autorización,
Tema 17. Registro de medicamentos Legislación y deontología farmacéutica 1 ESTATAL DISPOSICIONES LEGALES REAL DECRETO 1345/2007, de 11 de octubre, por el que se regula el procedimiento de autorización,
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 42 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN CABERGOLINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 42 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN CABERGOLINA 4.2 Posología y forma
Anexo III. Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto
 Anexo III Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto Nota: Esta Ficha Técnica, Etiquetado y Prospecto son el resultado del proceso de arbitraje.
Anexo III Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto Nota: Esta Ficha Técnica, Etiquetado y Prospecto son el resultado del proceso de arbitraje.
ESCLEROSIS MULTIPLE. La EM no es ni contagiosa, ni hereditaria, ni mortal.
 ESCLEROSIS MULTIPLE La esclerosis múltiple (EM) es la más común de las enfermedades inflamatorias que dañan la cubierta de las fibras nerviosas (mielina) del Sistema Nervioso Central (SNC). En los adultos
ESCLEROSIS MULTIPLE La esclerosis múltiple (EM) es la más común de las enfermedades inflamatorias que dañan la cubierta de las fibras nerviosas (mielina) del Sistema Nervioso Central (SNC). En los adultos
Conceptos Jurídicos y Normativa sobre las RAM de uso humano en España
 Conceptos Jurídicos y Normativa sobre las RAM de uso humano en España Vamos a realizar una muy breve aproximación a conceptos jurídicos y normativa asociada a las Reacciones Adversas a los Medicamentos
Conceptos Jurídicos y Normativa sobre las RAM de uso humano en España Vamos a realizar una muy breve aproximación a conceptos jurídicos y normativa asociada a las Reacciones Adversas a los Medicamentos
TASIGNA (NILOTINIB) INFORMACIÓN DE SEGURIDAD PARA EL PACIENTE
 TASIGNA (NILOTINIB) INFORMACIÓN DE SEGURIDAD PARA EL PACIENTE Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), julio 2015 Índice
TASIGNA (NILOTINIB) INFORMACIÓN DE SEGURIDAD PARA EL PACIENTE Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), julio 2015 Índice
UNIVERSIDAD DE GRANADA Departamento de Personalidad, Evaluación y Tratamiento Psicológico
 UNIVERSIDAD DE GRANADA Departamento de Personalidad, Evaluación y Tratamiento Psicológico Alteraciones atencionales y de la función ejecutiva en Esclerosis Múltiple: su relación con la velocidad de procesamiento
UNIVERSIDAD DE GRANADA Departamento de Personalidad, Evaluación y Tratamiento Psicológico Alteraciones atencionales y de la función ejecutiva en Esclerosis Múltiple: su relación con la velocidad de procesamiento
POR UN NUEVO PLAN DE ACTUACIÓN PARA LA ERRADICACIÓN DEL VIRUS DE LA HEPATITIS C (VHC)
 POR UN NUEVO PLAN DE ACTUACIÓN PARA LA ERRADICACIÓN DEL VIRUS DE LA HEPATITIS C (VHC) La hepatitis C es la inflamación del hígado debido a la infección por un virus. La infección por el virus C de la hepatitis
POR UN NUEVO PLAN DE ACTUACIÓN PARA LA ERRADICACIÓN DEL VIRUS DE LA HEPATITIS C (VHC) La hepatitis C es la inflamación del hígado debido a la infección por un virus. La infección por el virus C de la hepatitis
Ministerio de Salud Pública. Resumen de la evidencia para las personas con Esclerosis Múltiple y sus familiares
 Ministerio de Salud Pública. Resumen de la evidencia para las personas con Esclerosis Múltiple y sus familiares Guía de Práctica Clínica para el manejo del tratamiento con drogas inmunomoduladoras e inmunosupresoras
Ministerio de Salud Pública. Resumen de la evidencia para las personas con Esclerosis Múltiple y sus familiares Guía de Práctica Clínica para el manejo del tratamiento con drogas inmunomoduladoras e inmunosupresoras
Es la inflamación del nervio óptico que puede causar una pérdida súbita y parcial de la visión en el ojo afectado.
 Neuritis óptica Es la inflamación del nervio óptico que puede causar una pérdida súbita y parcial de la visión en el ojo afectado. Causas, incidencia y factores de riesgo La causa de la neuritis óptica
Neuritis óptica Es la inflamación del nervio óptico que puede causar una pérdida súbita y parcial de la visión en el ojo afectado. Causas, incidencia y factores de riesgo La causa de la neuritis óptica
FARMACOVIGILANCIA Información destinada a los profesionales de la salud
 FARMACOVIGILANCIA Información destinada a los profesionales de la salud 02/05/12 Finasteride. Riesgo de disfunción sexual y cáncer de mama. ANMAT. Desde la comercialización de finasteride en la Unión Europea
FARMACOVIGILANCIA Información destinada a los profesionales de la salud 02/05/12 Finasteride. Riesgo de disfunción sexual y cáncer de mama. ANMAT. Desde la comercialización de finasteride en la Unión Europea
Aspectos más destacados del informe anual 2009
 4 octubre 2010 EMA/615505/2010 Oficina del Director Ejecutivo Aspectos más destacados del informe anual 2009 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom Telephone +44 (0)20 741 8400 Facsimil
4 octubre 2010 EMA/615505/2010 Oficina del Director Ejecutivo Aspectos más destacados del informe anual 2009 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom Telephone +44 (0)20 741 8400 Facsimil
Actividades de la Agencia Europea del Medicamento en apoyo al plan de acción de la Comisión Europea sobre resistencias a los antibióticos.
 Actividades de la Agencia Europea del Medicamento en apoyo al plan de acción de la Comisión Europea sobre resistencias a los antibióticos. Día Europeo para el Uso Prudente de los Antibióticos Presentado
Actividades de la Agencia Europea del Medicamento en apoyo al plan de acción de la Comisión Europea sobre resistencias a los antibióticos. Día Europeo para el Uso Prudente de los Antibióticos Presentado
Caso 2: 1ª RM: aumento de señal en la corteza cerebral en difusión y FLAIR, con ganglios de la base normales. 2ª RM: aparece aumento de señal en
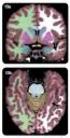 RESULTADOS: En todos los casos encontramos alteraciones características a nivel cortical y/o en los ganglios basales en fases iniciales de la enfermedad. Caso 1: 1ª RM: aumento de señal en T2, FLAIR y
RESULTADOS: En todos los casos encontramos alteraciones características a nivel cortical y/o en los ganglios basales en fases iniciales de la enfermedad. Caso 1: 1ª RM: aumento de señal en T2, FLAIR y
Esclerosis Múltiple. Dra. Noemi Miguel Valencia. En conmemoración del día Mundial de la Esclerosis Múltiple a celebrarse el próximo 28 de Mayo.
 Esclerosis Múltiple En conmemoración del día Mundial de la Esclerosis Múltiple a celebrarse el próximo 28 de Mayo. En México existen entre 12 y 15 mil personas diagnosticadas con Esclerosis Múltiple, padecimiento
Esclerosis Múltiple En conmemoración del día Mundial de la Esclerosis Múltiple a celebrarse el próximo 28 de Mayo. En México existen entre 12 y 15 mil personas diagnosticadas con Esclerosis Múltiple, padecimiento
ARIPIPRAZOL En adolescentes contrastorno Bipolar I
 ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
DEMENCIA? QUÉ ES LA DEMENCIA?
 PRESENTA QUÉ ES LA? QUÉ ES LA? La demencia es el trastorno de un grupo de procesos mentales entre los cuales podemos mencionar: memoria; razonamiento; planeamiento; aprendizaje; atención; lenguaje; percepción;
PRESENTA QUÉ ES LA? QUÉ ES LA? La demencia es el trastorno de un grupo de procesos mentales entre los cuales podemos mencionar: memoria; razonamiento; planeamiento; aprendizaje; atención; lenguaje; percepción;
LEFLUNOMIDA. Información sobre seguridad para los profesionales sanitarios
 LEFLUNOMIDA Información sobre seguridad para los profesionales sanitarios Leflunomida es un fármaco antirreumático modificador de la enfermedad" (FARME) indicado para el tratamiento de pacientes adultos
LEFLUNOMIDA Información sobre seguridad para los profesionales sanitarios Leflunomida es un fármaco antirreumático modificador de la enfermedad" (FARME) indicado para el tratamiento de pacientes adultos
Conclusiones científicas y motivos de las conclusiones
 Anexo II Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización y explicación pormenorizada de las diferencias con respecto a la recomendación
Anexo II Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización y explicación pormenorizada de las diferencias con respecto a la recomendación
La Clínica Veterinaria Eurovet os explica como proteger a su gato contra las corizas
 Publicado en 12598 el 26/04/2013 La Clínica Veterinaria Eurovet os explica como proteger a su gato contra las corizas El coriza del gato es una de las razones principales de consulta del veterinario. La
Publicado en 12598 el 26/04/2013 La Clínica Veterinaria Eurovet os explica como proteger a su gato contra las corizas El coriza del gato es una de las razones principales de consulta del veterinario. La
Farmacovigilancia. Curso de Diplomado en Sanidad
 Farmacovigilancia Curso de Diplomado en Sanidad 2010 FARMACOVIGILANCIA Conjunto de procedimientos de detección, registro y evaluación de las reacciones adversas, para la determinación de su incidencia,
Farmacovigilancia Curso de Diplomado en Sanidad 2010 FARMACOVIGILANCIA Conjunto de procedimientos de detección, registro y evaluación de las reacciones adversas, para la determinación de su incidencia,
Cada año, más de mujeres desarrollan cáncer de seno y mueren aproximadamente. causa. Se estima que 1 de cada 17 mujeres puede desarrollar
 Cada año, más de 8.686 mujeres desarrollan cáncer de seno y mueren aproximadamente 2.649 por esta causa. Se estima que 1 de cada 17 mujeres puede desarrollar la enfermedad a lo largo de su vida. RECUERDA
Cada año, más de 8.686 mujeres desarrollan cáncer de seno y mueren aproximadamente 2.649 por esta causa. Se estima que 1 de cada 17 mujeres puede desarrollar la enfermedad a lo largo de su vida. RECUERDA
INSTRUCCIONES PARA LA SOLICITUD DE CLASIFICACIÓN DE ESTUDIOS POSAUTORIZACIÓN DE TIPO OBSERVACIONAL CON MEDICAMENTOS DE USO HUMANO
 SUBRIRECCIÓN GENERAL DE MEDICAMENTOS DE USO HUMANO INSTRUCCIONES PARA LA SOLICITUD DE CLASIFICACIÓN DE ESTUDIOS POSAUTORIZACIÓN DE TIPO OBSERVACIONAL CON MEDICAMENTOS DE USO HUMANO 09/03/2011 De acuerdo
SUBRIRECCIÓN GENERAL DE MEDICAMENTOS DE USO HUMANO INSTRUCCIONES PARA LA SOLICITUD DE CLASIFICACIÓN DE ESTUDIOS POSAUTORIZACIÓN DE TIPO OBSERVACIONAL CON MEDICAMENTOS DE USO HUMANO 09/03/2011 De acuerdo
Tema 14 (Atención enfermera al recién nacido en riesgo)
 Tema 14 (Atención enfermera al recién nacido en riesgo) La quimioprofilaxis de la madre en caso de cultivos positivos para EGB: a. Es de dos dosis de penicilina separadas de 12 horas b. Dos dosis de aciclovir
Tema 14 (Atención enfermera al recién nacido en riesgo) La quimioprofilaxis de la madre en caso de cultivos positivos para EGB: a. Es de dos dosis de penicilina separadas de 12 horas b. Dos dosis de aciclovir
Valoración y semiología de patologías del Adulto (1) EU Tania Vásquez S. Enfermería Medico-Quirúrgica
 Valoración y semiología de patologías del Adulto (1) EU Tania Vásquez S. Enfermería Medico-Quirúrgica 1 2016 VALORACIÓN Valoración Es la recogida sistemática y continua, organización, validación y registro
Valoración y semiología de patologías del Adulto (1) EU Tania Vásquez S. Enfermería Medico-Quirúrgica 1 2016 VALORACIÓN Valoración Es la recogida sistemática y continua, organización, validación y registro
