PRINCIPIOS INMEDIATOS INORGÁNICOS: EL AGUA y LAS SALES MINERALES (2-3 sesiones)
|
|
|
- Ramona Sánchez Iglesias
- hace 8 años
- Vistas:
Transcripción
1 PRINCIPIOS INMEDIATOS INORGÁNICOS: EL AGUA y LAS SALES MINERALES (2-3 sesiones)
2 11.- COMPONENTES MOLECULARES DE LOS SERES VIVOS Los elementos biológicamente importantes Las moléculas que componen los seres vivos - Moléculas inorgánicas - Agua: - Estructura molecular. Polaridad de la molécula. - Función biológica - El agua como disolvente. Dispersiones y disoluciones - Ionización del agua. Ácidos y bases. - Sales minerales - Funciones de los aniones: - Amortiguadores. - Mantenimiento del equilibrio osmótico - Funciones específicas de los cationes.
3 - Bioelementos y oligoelementos. Los bioelementos. Introducción. Bioelementos primarios, Grupo del C e H; grupo del N, S y P. Bioelementos secundarios; bioelementos abundantes; Oligoelementos. - Los enlaces químicos y su importancia en biología. - Moléculas e iones inorgánicos: agua y sales minerales. Biomoléculas o principios inmediatos Introducción y esquema. El agua la vida se apoya en su comportamiento anormal; Introducción 1 ; Enlaces por puentes de H y estructura reticular del agua líquida; Asociación de moléculas de agua mediante enlaces de hidrógeno. Propiedades del agua; Funciones del agua en los seres vivos. ionización del agua y escala de ph, sólo el concepto. Las sales minerales - Fisicoquímica de las dispersiones acuosas. Difusión, ósmosis y diálisis. Introducción. Propiedades de las disoluciones verdaderas, ósmosis, estabilidad del grado de acidez o ph, disoluciones o disoluciones amortiguadoras. Mantenimiento de concentraciones osmóticas adecuadas, presión osmótica, diálisis, y difusión. Propiedades de las dispersiones coloidales, formas sol y gel, separación por diálisis 2.
4 ELEMENTOS BIOGÉNICOS: MACROELEMENTOS Y OLIGOELEMENTOS Cuando se analiza la materia viva se comprueba que está formada esencialmente por agua, sales minerales (principios inmediatos inorgánicos) y por compuestos ricos en carbono (principios inmediatos orgánicos), de cuatro tipos, glúcidos, lípidos, proteínas y ác. nucleicos. Los elementos que forman parte de los seres vivos se denominan elementos biogénicos o bioelementos, y son solo unos pocos de la tabla periódica. Algunos de ellos aparecen en los seres vivos en cantidades importantes, y se denominan macroelementos. Otros aparecen en cantidades accesorias (insignificantes), aunque son esenciales para la vida. Reciben el nombre de microelementos u oligoelementos (oligo=poco).
5 Los principales macroelementos son: Bioelementos primarios: carbono, hidrógeno, oxígeno y nitrógeno (CHON). Su masa atómica es baja (C=12, H=1, O=16, N=14) y son muy abundantes en la corteza terrestre, en la atmósfera y en la biosfera. Son muy solubles en agua por lo que pueden ser fácilmente incorporados o desechados de los líquidos orgánicos. Los cuatro constituyen el 96% de la materia viva. El carbono y el nitrógeno poseen igual afinidad para unirse con el oxígeno que con el hidrógeno, por lo que pueden pasar con facilidad al estado oxidado (CO 2 ) o reducido (NH 3 ). Bioelementos seundarios: son los otros macroelementos que entran a formar parte de los seres vivos, aunque en menor cantidad (4% en total), son: S (azufre), P (fósforo), Na (sodio), K (potasio), Ca (calcio), Mg (magnesio) y Cl (cloro). Azufre (S): forma parte de muchas proteínas. Se encuentra en dos a.a, la cisterna y la metionina. Fósforo (P): interviene en muchos compuestos orgánicos (fosfolípidos, ac. nucleicos etc.). Sodio (Na), Potasio (K) y Cloro (Cl): intervienen en las membranas celulares, especialmente en las de las células nerviosas y musculares haciendo que se genere un potencial de reposo o un potencial de acción. Calcio (Ca): interviene en la contracción de las celulas musculares. Es imprescindible para que se formen los puentes entre la actina y miosina que permiten la contracción. Magnesio (Mg): interviene también en muchas reacciones metabólicas y es imprescindible para que las plantas verdes puedan formar clorofila.
6 Los oligoelementos más importantes son: - Hierro (Fe): forma parte de la hemoglobina y de otros pigmentos circulatorios de vertebrados, siempre en relación con el transporte de oxígeno. También forma parte de los pigmentos respiratorios (citocromos). - Cobre: forma parte de la hemocianina (hemos=hierro, ciano=azul), que es el pigmento circulatorio de artrópodos y moluscos. Este pigmento cumple una función similar a la de la hemoglobina. - Manganeso: interviene también en muchas reacciones metabólicas. - Cinc: forma parte de diversos enzimas. - Iodo: forma parte de la tiroxina u hormona tiroidea. - Cobalto: necesario para la síntesis de la Vitamina B 12.
7
8 EL AGUA El agua es uno de los principales componentes de los seres vivos. Aproximadamente, el contenido de agua puede oscilar entre un 10% y un 90% del peso del individuo. Poseen un 10% determinadas estructuras en estado de latencia (ej. semillas) y un 90% algunos animales acuáticos (medusas, algunos vegetales como las algas o ciertos hongos, etc...). En los primates (hombres), el contenido de agua es aproximadamente del 70%. El contenido de agua disminuye a medida que se envejece.
9 ESTRUCTURA MOLECULAR DE LA MOLÉCULA DE AGUA El agua está formada por dos átomos de hidrógeno y uno de oxígeno que comparten dos pares de electrones, es decir, el hidrógeno y el oxígeno están unidos mediante dos enlaces covalentes. Pero estos electrones son atraídos con más fuerza hacia el átomo de oxígeno, por lo que en conjunto, la molécula de agua es dipolar (tiene 2 polos y es soluble en agua). Uno de esos polos (el positivo) lo constituyen los dos átomos de hidrógeno y el otro polo (el negativo) lo constituye el átomo de oxígeno. Polaridad de la molécula de agua
10
11 De todas formas, en conjunto, el agua es una sustancia neutra, porque las moléculas de agua interaccionan de forma ordenada de modo que el polo negativo de una molécula se une con el polo positivo de otra. Entonces se establecen entre ambas moléculas puentes o enlaces de hidrógeno. Un enlace de hidrógeno (veremos más tarde que son muy frecuente en las macromoléculas orgánicas) es un enlace más débil que el covalente, pero sin embargo estos enlaces le dan al agua una estabilidad considerable.
12 Los enlaces de hidrógeno aseguran una cohesión entre las moléculas de agua, de diferente intensidad según sea el estado de la misma. A 0º C se establecen enlaces de H entre todas las moléculas de agua y aseguran una cohesión tal que se forman cristales de hielo. Cuando el hielo se licua (funde), los enlaces de hidrógeno se rompen aproximadamente en una proporción del 15%, de modo que el agua líquida tiene una estructura parcialmente ordenada en la que los enlaces de hidrógeno se rompen y se crean constantemente. A mayor temperatura, mayor cantidad de enlaces de hidrógeno se romperán. En estado de vapor los puentes de H desaparecen. El agua tiene su máxima densidad a 4 grados. Es la única sustancia que es más densa en estado líquido que en estado sólido.
13 Estructura del hielo
14
15 PROPIEDADES DERIVADAS DE SU ESTRUCTURA MOLECULAR. (Repasar los conceptos de disolución verdadera y disolución coloidal.) 1. El agua es un disolvente universal que permite solvatar fácilmente los iones en disolución (las moléculas polares de agua tienden a separar a las sustancias iónicas, como NaCl, en sus iones constituyentes, esos iones quedan solvatados o hidratados) y también moléculas polares como proteínas, hidratos de carbono, etc.. Esta propiedad es debida a la polaridad de las moléculas de agua, que establecen puentes de hidrógeno con alcoholes, azúcares con grupos OH, aminoácidos y proteínas con grupos que presentan cargas + y -. Por ello el agua es el medio en el que se producen las reacciones del organismo y es un medio de transporte. Las moléculas que se disuelven con facilidad en el agua reciben el nombre de moléculas hidrófilas (o polares). Otras moléculas carecen de regiones polares (las grasas, los hidrocarburos) y son insolubles en agua, reciben el nombre de hidrófobas (o no polares). Incluso existen sustancias con una zona polar y otra no polar (sustancias anfipáticas o polares, en este caso polar significa con dos polos). Estas sustancias tienden a disponerse con sus regiones no polares alejadas del agua y con sus regiones polares en contacto con el agua.
16 Solvatación: las moléculas de agua separan los iones e impiden que se vuelvan a juntar.
17 2. El agua es líquida a temperatura ambiente, que es la temperatura a la que se desarrolla la vida. Esta propiedad es debida también a su estructura molecular, especialmente a la formación de un determinado número de puentes de H. Esta propiedad es muy importante porque en congelación no se desarrolla la vida. 3. El agua tiene una tensión superficial bastante alta, solo superada por el mercurio. La tensión superficial es una medida de la cohesión de de las moléculas de una sustancia. Hace que los líquidos tengan sus moléculas unidas en superficie (gotas de agua que gotean de un grifo) y que en ocasiones, como ocurre en el mercurio, esas moléculas tiendan a no adherirse a nada más. También permite que numerosos invertebrados puedan desplazarse sobre su superficie sin hundirse. Sin embargo, el agua, al poseer cargas eléctricas positivas y negativas, si tiene apetencia por otras moléculas, muy especialmente por superficies que tengan cargas. Esto hace que el agua moje (que pueda revestir superficies). Tensión superficial alta Fot.: Geni Alvarez
18 El agua reviste superficies Tensión superficial alta Fot.: Geni Alvarez
19 Fot.: Geni Alvarez
20 Gerris lacustris Neil A. Campbell, Jane B. Reece. Biología. ISBN: Ed. Panamericana, 7 edición, 2007.
21 4. El agua puede penetrar en el interior de volúmenes por capilaridad e imbibición. La capilaridad permite su ascenso por tubos de vidrio muy finos (capilar = cabello) y sobre todo permite que se desplace lentamente por los pequeños espacios existentes entre las partículas del suelo y llegue así a las raíces de las plantas. A este fenómeno se debe en parte la ascensión de la savia bruta desde las raíces hasta las hojas, a través de los vasos leñosos. Imbibición es la penetración capilar de las moléculas de agua en sustancias como madera o gelatina. Esto permite que las semillas se embeban en agua y puedan germinar.
22 Xilema Pelos absorbentes unicelulares Fot.: Geni Alvarez
23 Fot.: Geni Alvarez
24 5. El calor específico del agua es más o menos el doble que el del aceite o el del alcohol, y cuatro veces mayor que el del aire. El calor específico es la cantidad de calor que una sustancia dada requiere para que ocurra un aumento dado de su temperatura (buscar definición de caloría, el calor específico del agua es de 1 cal/ C g ). El alto calor específico del agua es también consecuencia de los enlaces de H. Esto se traduce en que aunque los seres vivos generan calor por su actividad metabólica no aumentan demasiado su temperatura, por su gran contenido en agua. Por la misma razón tampoco se pierde calor de una forma muy rápida. Los organismos que viven en los océanos están en un ambiente cuya temperatura es relativamente constante. Por lo tanto el agua es un buen regulador térmico. De igual manera el agua tiene un gran calor de evaporación. Para evaporarse se tienen que romper los enlaces de hidrógeno, y eso requiere una energía que se obtiene del ser vivo del cual se evapora, por lo tanto la evaporación tiene un efecto refrigerante. Para evaporar un gramo de agua se precisan 540 calorías, a una temperatura de 20º C. 6. Cuando se congela, al contrario que la mayoría de los líquidos, disminuye la densidad, porque se forman 4 enlaces de hidrógeno en cada molécula que hace que las moléculas se alejen unas de otras. Al disminuir la densidad, aumenta el volumen, por lo tanto el hielo flota sobre el agua líquida. Esto preserva los ecosistemas acuáticos porque el hielo hace de capa impermeable superficial e impide que se congele el resto de la charca, de modo que por debajo de ese hielo la temperatura sería aproximadamente de 4 grados centígrados, puesto que esa temperatura es aquella a la cual la densidad es máxima.
25 FUNCIONES DEL AGUA Muchas de ellas ya las hemos ido diciendo al hablar de las propiedades del agua y como consecuencia de ellas, pero las repetimos ordenadas y sin explicar en esta ocasión. - Función disolvente de las sustancias. Esta función es básica para la vida, ya que tanto los líquidos intracelulares como los extracelulares en los que se producen las reacciones metabólicas son disoluciones acuosas. - Función estructural del agua: el agua mantiene la arquitectura (volumen y forma) de las células. Esto es especialmente importante en las células animales que carecen de una pared rígida de celulosa. - Función de transporte: debido a su poder como disolvente universal. - Función mecánica amortiguadora de pequeños traumatismos. Por ejemplo: el agua de da flexibilidad a los tejidos y se encuentra en las articulaciones como lubricante. - Función termorreguladora, debida a su elevado calor específico y a su elevado calor de evaporación y al hecho de ser menos densa cuando se congela.
26 IONIZACIÓN DEL AGUA El agua pura puede disociarse en iones OH - (iones hidroxilo u oxidrilo) y H 3 O + (protones hidratados). Esta capacidad de disociación es muy débil, de modo que el agua pura se puede considerar una mezcla de agua molecular (H 2 O), protones hidratados (H 3 O + ) e hidroxilos (OH - ). El producto iónico del agua a 25º C es: K w = [H + ][OH - ] = El producto iónico es constante, por tanto, la [H+] en el agua pura es de Para cuantificar la [H+] en cualquier disolución orgánica se utiliza una escala logarítmica. Se define el ph (presión de protones) como el logaritmo en base 10 de 1 partido por la [H+] ( o menos el logaritmo en base 10 de la [H+]) Disolución ácida ph<7 Disolución neutra ph= 7 Disolución básica o alcalina ph>7 ph= log (1/ [H+] )
27 Algunos valores de ph:
28 LAS SALES MINERALES Constituyen también un componente inorgánico de los seres vivos. Se encuentran fundamentalmente de dos maneras: precipitadas o disueltas en forma de iones. Se encuentran de forma precipitada formando estructuras sólidas, ej. el CaCO 3 (carbonato cálcico) en las conchas de los moluscos, el CaHPO 4 (fosfato cálcico) en los huesos, el SiO 2 (cuarzo) en las valvas de diatomeas y en las paredes de las células de muchas gramíneas etc.. Las sales que se encuentran disueltas dan lugar a aniones y a cationes. Los principales aniones son: Cl -, SO 4 2-, PO 4 3-, HPO 4 2-, H 2 PO 4-, NO 3-, HCO 3 - y los principales cationes son Na +, K +, Ca 2+, Mg 2+
29 Diatomeas (Bacillariophyceae). Individuos aislados de nivel protófito. Objetivo x 40 Fot.: Geni Alvarez
30 Diatomeas sobre un alga verde filamentosa (Cladophora) Diatomeas Objetivo x 40 Fot.: Geni Alvarez
31 Diatomeas sobre un alga verde filamentosa (Cladophora) Objetivo x 40 Fot.: Geni Alvarez
32 Diatomeas sobre un alga verde filamentosa (Cladophora) Objetivo x 40 Fot.: Geni Alvarez
33 FUNCIONES DE LAS SALES MINERALES 1. Estructural: cuando las sales se encuentran precipitadas (no solubles), contribuyen a la arquitectura de huesos, dientes, caparazones... Esqueleto interno de vertebrados, en el que encontramos : fosfatos, cloruros, y carbonatos de calcio. Caparazones de carbonato cálcico de crustáceos y moluscos. Endurecimiento de células vegetales, como en gramíneas (impregnación con sílice de las paredes celulares). Otolitos del oído interno, formados por cristales de carbonato cálcico (equilibrio). 2. Reguladoras de los procesos osmóticos: es importante que a ambos lados de la membrana celular, los iones se distribuyan adecuadamente para que la presión osmótica permanezca constante. Se llama presión osmótica (π) a la presión que ejerce cualquier ión disuelto en un líquido. Este fenómeno es muy importante porque las membranas celulares se comportan como membranas semipermeables, es decir, dejan pasar a su través de forma pasiva el agua, pero no las sustancias disueltas en ella. Cuando ponemos en contacto dos disoluciones de distinta concentración separadas por una membrana semipermeable, se produce un paso de agua desde la disolución de menor presión osmótica (hipotónica) a la de mayor presión osmótica (hipertónica), tratando de igualarlas. Se llaman disoluciones isotónicas a aquellas que tienen la misma presión osmótica, mientras que se dice que una disolución es hipotónica respecto de otra que es hipertónica si su presión osmótica es menor. Si sumergimos células en una disolución hipertónica, tendería a salir agua de ellas y la célula podría morir por desecación. A este fenómeno se le denomina plasmolisis. En las células vegetales se retrae en contenido celular y la membrana y el citoplasma se separan de la pared (la célula se plasmoliza). En el caso de las células animales se produce la destrucción de la célula es por deshidratación (crenación o arrugado de un eritrocito). Si por el contrario, colocamos a las células en una disolución hipotónica (agua destilada), el agua penetraría en la célula y se produciría el fenómeno de turgencia. Si el fenómeno se produce en una célula vegetal (agua de lluvia hipotónica), la célula no se dañaría por la existencia de la pared (de hecho, este fenómeno es saludable para la mayoría de las células vegetales: necesitan de la turgencia para su alargamiento y crecimiento), pero si se trata de una célula animal, ésta moriría por rotura de la membrana (hemólisis de un eritrocito).
34
35 Presión osmótica en células vegetales (patata). Soluciones de glucosa 1,5 M 0,5 M 0 M 1,5 M 0,5 M 0 M 0 M: agua destilada
36 3. Las sales son reguladoras del equilibrio ácido-base. En los seres vivos se dan una gran cantidad de reacciones metabólicas, la mayoría de las cuales tienen que transcurrir en un medio aproximadamente neutro. Sin embargo, como consecuencia de esas reacciones metabólicas, se liberan fundamentalmente productos ácidos o básicos. Se llama sistema amortiguador del ph (o sistema tampón) a aquel que evita los cambios importantes de ph. Los principales sistemas amortiguadores del ph en los seres vivos son las proteínas, pero también son muy importantes los sistemas amortiguadores salinos. Uno de los más importantes lo constituye el formado por el ácido carbónico (ácido débil) y el ión bicarbonato. H 2 CO 3 /HCO 3 -. El ácido actúa como dador de protones y la sal actúa como aceptor de protones. En los seres vivos hay un equilibrio entre las dos sustancias, de modo que la relación normal suele ser de 1/20. Cuando se produce un exceso de protones aumenta la acidez. Entonces el ión bicarbonato, presente en el plasma sanguíneo, capta esos protones y se forma ácido carbónico que se transforma rápidamente en CO 2 y H 2 O. El CO 2 se elimina a través de los pulmones y el agua se queda en el plasma. H + + HCO 3 - H 2 CO 3 CO 2 + H 2 O A través del riñón se pueden eliminar directamente protones (para eliminar la acidez) o se pueden retener si se elimina el ión bicarbonato (que es el que retiene los H +).
37 4. Los cationes son importantes para mantener el equilibrio iónico de las células. Muchos cationes son necesarios e imprescindibles para el correcto funcionamiento de determinados tipos celulares. Por ejemplo, el Na + y el K + son imprescindibles para que haya excitabilidad en los tejidos muscular y nervioso. El Ca 2+ es imprescindible para la contracción muscular, para que se formen los puentes entre la actina y la miosina y se produzca la contracción. Pero si falta Ca 2+ en sangre (hipocalcemia) se produce una contracción permanente y violenta de los músculos. Esta contracción se denomina tetania*. *Aunque el Ca 2+ se necesita para formar los puentes entre dos proteínas contráctiles del sistema muscular, la actina y la miosina, es decir, es imprescindible en el músculo para que se produzca la contracción, la falta de Ca 2+ en sangre (hipocalcemia), produce tetania porque el Ca 2+ es un impedimento esteárico (físico), que se une a los canales de acetil colina disminuyendo la entrada de este neurotransmisor a la célula nerviosa. Si falta el Ca 2+ en sangre se produce una mayor entrada de acetil colina y por lo tanto una hiperexcitabilidad del sistema nervioso que provoca las contracciones musculares permanentes y violentas.
38 UNIDADES DE MEDIDA EN BIOLOGÍA 1 mm = 10 3 µm (micrómetros) 1 µm = 10 3 nm o mµ (nanómetros o milimicras) 1 nm = 10 Å (Angstroms) Por lo tanto: 1nm = 10-9 m (metros) 1 Å = m (metros)
39 OIL RIG (plataforma petrolífera) Oxidation is lost of electrons (también pérdida de protones). Reduction is gain of electrons (también ganancia de protones)
4º E.S.O. Colegio San Agustín Sevilla TEMA 1: EL AGUA
 1.1. INTRODUCCIÓN 4º E.S.O. Colegio San Agustín Sevilla TEMA 1: EL AGUA El agua es una materia básica para la vida y está presente en la mayoría de los procesos físicos y químicos que se desarrollan a
1.1. INTRODUCCIÓN 4º E.S.O. Colegio San Agustín Sevilla TEMA 1: EL AGUA El agua es una materia básica para la vida y está presente en la mayoría de los procesos físicos y químicos que se desarrollan a
hidratos de carbono lípidos, proteínas, vitaminas sales minerales y agua principios inmediatos aminoácidos ácidos grasos esenciales
 A pesar de la diversidad en su composición, los análisis químicos revelan que todos los alimentos presentan seis grupos de sustancias comunes, denominadas nutritivas, en distinta proporción: hidratos de
A pesar de la diversidad en su composición, los análisis químicos revelan que todos los alimentos presentan seis grupos de sustancias comunes, denominadas nutritivas, en distinta proporción: hidratos de
Actividad: Qué es la anomalía del agua?
 Nivel: 1º Medio Subsector: Ciencias químicas Unidad temática: El agua Actividad: Seguramente ya has escuchado sobre la anomalía del agua. Sabes en qué consiste y qué es algo anómalo? Se dice que algo es
Nivel: 1º Medio Subsector: Ciencias químicas Unidad temática: El agua Actividad: Seguramente ya has escuchado sobre la anomalía del agua. Sabes en qué consiste y qué es algo anómalo? Se dice que algo es
El agua como disolvente
 hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
Tema 1. Introducción
 Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO
 ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO 1 Puede formarse un enlace iónico entre átomos de un mismo elemento químico? Por qué? No. El enlace químico se produce entre átomos con valores muy diferentes
ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO 1 Puede formarse un enlace iónico entre átomos de un mismo elemento químico? Por qué? No. El enlace químico se produce entre átomos con valores muy diferentes
2º E.S.O. - CIENCIAS DE LA NATURALEZA
 2º E.S.O. - CIENCIAS DE LA NATURALEZA En la actualidad se conocen más de 1.800.000 especies de seres vivos distintos (hay muchas otras aun por descubrir). Los seres vivos se diferencian de la materia inerte
2º E.S.O. - CIENCIAS DE LA NATURALEZA En la actualidad se conocen más de 1.800.000 especies de seres vivos distintos (hay muchas otras aun por descubrir). Los seres vivos se diferencian de la materia inerte
1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos.
 VALENCIA (COMUNIDAD VALENCIANA) / JUNIO 00. COU / BIOLOGIA / BIOMOLECULAS / OPCION A / EJERCICIO 1 OPCION A 1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos. La actividad
VALENCIA (COMUNIDAD VALENCIANA) / JUNIO 00. COU / BIOLOGIA / BIOMOLECULAS / OPCION A / EJERCICIO 1 OPCION A 1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos. La actividad
TEMA 3. PROPIEDADES QUÍMICAS DEL SUELO. Los elementos químicos en el suelo Capacidad de intercambio catiónico El ph suelo Conductividad eléctrica
 TEMA 3. PROPIEDADES QUÍMICAS DEL SUELO Los elementos químicos en el suelo Capacidad de intercambio catiónico El ph suelo Conductividad eléctrica 1. Los elementos químicos en el suelo. 1.1. Situación de
TEMA 3. PROPIEDADES QUÍMICAS DEL SUELO Los elementos químicos en el suelo Capacidad de intercambio catiónico El ph suelo Conductividad eléctrica 1. Los elementos químicos en el suelo. 1.1. Situación de
Ablandamiento de agua mediante el uso de resinas de intercambio iónico.
 Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
La Absorción del Agua
 La Absorción del Agua Importancia del Agua en las Plantas Es el cons5tuyente principal del protoplasma celular, en ocasiones representa hasta el 95% del peso total de la planta. Es el solvente en el que
La Absorción del Agua Importancia del Agua en las Plantas Es el cons5tuyente principal del protoplasma celular, en ocasiones representa hasta el 95% del peso total de la planta. Es el solvente en el que
FÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación GAS LÍQUIDO SÓLIDO
 Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
CONDUCTIVIDAD Y ph PRACTICA Nº 7
 CONDUCTIVIDAD Y ph PRACTICA Nº 7 OBJETO DE LA PRÁCTICA: MEDIDA DE CONDUCTIVIDAD Y MANEJO DE SUS UNIDADES RELACIÓN CONDUCTIVIDAD-SALINIDAD- Nº DE PURGAS RELACIÓN CONDUCTIVIDAD-EROSIÓN/CORROSIÓN MANEJO DEL
CONDUCTIVIDAD Y ph PRACTICA Nº 7 OBJETO DE LA PRÁCTICA: MEDIDA DE CONDUCTIVIDAD Y MANEJO DE SUS UNIDADES RELACIÓN CONDUCTIVIDAD-SALINIDAD- Nº DE PURGAS RELACIÓN CONDUCTIVIDAD-EROSIÓN/CORROSIÓN MANEJO DEL
El Agua. 2H2O(l) 2H2 (g) +O2 (g) Puentes de hidrogeno
 El Agua. El agua es un compuesto covalente, formado por Hidrógeno y Oxígeno (H 2 O).Puesto que el Oxígeno es mas covalente que el Hidrógeno, el enlace O-H es covalente polar. La electrolisis (aplicación
El Agua. El agua es un compuesto covalente, formado por Hidrógeno y Oxígeno (H 2 O).Puesto que el Oxígeno es mas covalente que el Hidrógeno, el enlace O-H es covalente polar. La electrolisis (aplicación
1.- Indica semejanzas y diferencias entre los siguientes conceptos:
 Ejercicios resueltos aparato excretor 1.- Indica semejanzas y diferencias entre los siguientes conceptos: a) Excreción y defecación: La excreción supone la eliminación de los productos de desecho procedentes
Ejercicios resueltos aparato excretor 1.- Indica semejanzas y diferencias entre los siguientes conceptos: a) Excreción y defecación: La excreción supone la eliminación de los productos de desecho procedentes
 TEMA 22 1. Qué diferencia hay entre un órgano y un tejido?. Realizar un esquema de los tejidos básicos indicando sus características más sobresalientes. 2. La homeostasis es el mantenimiento del medio
TEMA 22 1. Qué diferencia hay entre un órgano y un tejido?. Realizar un esquema de los tejidos básicos indicando sus características más sobresalientes. 2. La homeostasis es el mantenimiento del medio
TEMA 2: LA FUNCIÓN DE NUTRICIÓN
 TEMA 2: LA FUNCIÓN DE NUTRICIÓN INDICE: 1. 2. La función de nutrición La nutrición en animales 2.1 El proceso digestivo 2.2 La respiración 2.2.1Tipos de respiración 2.3 El transporte de sustancias 2.3.1
TEMA 2: LA FUNCIÓN DE NUTRICIÓN INDICE: 1. 2. La función de nutrición La nutrición en animales 2.1 El proceso digestivo 2.2 La respiración 2.2.1Tipos de respiración 2.3 El transporte de sustancias 2.3.1
IES Menéndez Tolosa 3º ESO (Física y Química)
 IES Menéndez Tolosa 3º ESO (Física y Química) 1 De las siguientes mezclas, cuál no es heterogénea? a) azúcar y serrín. b) agua y aceite. c) agua y vino d) arena y grava. La c) es una mezcla homogénea.
IES Menéndez Tolosa 3º ESO (Física y Química) 1 De las siguientes mezclas, cuál no es heterogénea? a) azúcar y serrín. b) agua y aceite. c) agua y vino d) arena y grava. La c) es una mezcla homogénea.
1. LA NUTRICIÓN Y LA SALUD La nutrición es un factor clave para las personas porque...
 NUTRICIÓN, SALUD Y ACTIVIDAD FÍSICA ESQUEMA 1. LA NUTRICIÓN Y LA SALUD 2. LOS PRINCIPIOS INMEDIATOS 3. LA FUNCIÓN ENERGÉTICA DE LOS ALIMENTOS 4. HÁBITOS DE ALIMENTACIÓN Y SALUD 1. LA NUTRICIÓN Y LA SALUD
NUTRICIÓN, SALUD Y ACTIVIDAD FÍSICA ESQUEMA 1. LA NUTRICIÓN Y LA SALUD 2. LOS PRINCIPIOS INMEDIATOS 3. LA FUNCIÓN ENERGÉTICA DE LOS ALIMENTOS 4. HÁBITOS DE ALIMENTACIÓN Y SALUD 1. LA NUTRICIÓN Y LA SALUD
CONDICIONES Y RECURSOS
 CONDICIONES Y RECURSOS Uno de los objetivos de la ecología es comprender la distribución y abundancia de las especies y para ello es importante ver el efecto que sobre ella tienen diversos efectos. Destacamos:
CONDICIONES Y RECURSOS Uno de los objetivos de la ecología es comprender la distribución y abundancia de las especies y para ello es importante ver el efecto que sobre ella tienen diversos efectos. Destacamos:
Soluciones Electrolíticas María de la Luz Velázquez Monroy & Miguel Ángel Ordorica Vargas
 Introducción Soluciones Electrolíticas María de la Luz Velázquez Monroy & Miguel Ángel Ordorica Vargas Siguiendo los trabajos de Humphrey Davy, sobre electrolisis de metales, en 1834, Michael Faraday inició
Introducción Soluciones Electrolíticas María de la Luz Velázquez Monroy & Miguel Ángel Ordorica Vargas Siguiendo los trabajos de Humphrey Davy, sobre electrolisis de metales, en 1834, Michael Faraday inició
SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO
 Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
El agua. El agua. Se pueden ver muy bien los 4 puentes de hidrógeno que forma la molécula de agua central.
 El agua El agua es una de las sustancias más peculiares conocidas. Es una molécula pequeña y sencilla, pero tras su aparente simplicidad presenta una complejidad sorprendente que la hace especialmente
El agua El agua es una de las sustancias más peculiares conocidas. Es una molécula pequeña y sencilla, pero tras su aparente simplicidad presenta una complejidad sorprendente que la hace especialmente
Sistemas de ingreso, intercambio y transporte de sustancias en el organismo. Sistema Circulatorio
 Sistema circulatorio Observe y explore comprensivamente esta presentación Sistemas de ingreso, intercambio y transporte de sustancias en el organismo: Sistema circulatorio. Esta le permitirá avanzar y
Sistema circulatorio Observe y explore comprensivamente esta presentación Sistemas de ingreso, intercambio y transporte de sustancias en el organismo: Sistema circulatorio. Esta le permitirá avanzar y
BIOELEMENTOS AGUA Y SALES MINERALES
 BIOELEMENTOS AGUA Y SALES MINERALES BIOELEMENTOS PROPIEDADES Capas electrónicas externas incompletas ENLACES COVALENTES Nº atómico bajo ENLACES ESTABLES Oxígeno y Nitrógeno electronegativos BIOMOLÉCULAS
BIOELEMENTOS AGUA Y SALES MINERALES BIOELEMENTOS PROPIEDADES Capas electrónicas externas incompletas ENLACES COVALENTES Nº atómico bajo ENLACES ESTABLES Oxígeno y Nitrógeno electronegativos BIOMOLÉCULAS
TEMA 3. LA MATERIA: CÓMO SE PRESENTA
 APUNTES FÍSICA Y QUÍMICA 3º ESO TEMA 3. LA MATERIA: CÓMO SE PRESENTA Completa el siguiente mapa conceptual MATERIA 1. Sustancias puras y mezclas. Elementos y compuestos Define: - Sustancia pura: - Elemento:
APUNTES FÍSICA Y QUÍMICA 3º ESO TEMA 3. LA MATERIA: CÓMO SE PRESENTA Completa el siguiente mapa conceptual MATERIA 1. Sustancias puras y mezclas. Elementos y compuestos Define: - Sustancia pura: - Elemento:
LA NUTRICIÓN DE LAS PLANTAS LOS ABONOS
 FERTILIZACIÓN LA NUTRICIÓN DE LAS PLANTAS LOS ABONOS NECESIDADES DE LAS PLANTAS: LUZ, AIRE, AGUA, SUELO Y NUTRIENTES Las plantas están compuestas de agua y sustancias minerales. FOTOSÍNTESIS I ABSORCIÓN
FERTILIZACIÓN LA NUTRICIÓN DE LAS PLANTAS LOS ABONOS NECESIDADES DE LAS PLANTAS: LUZ, AIRE, AGUA, SUELO Y NUTRIENTES Las plantas están compuestas de agua y sustancias minerales. FOTOSÍNTESIS I ABSORCIÓN
Resultado: a) K ps = 6,81 10 11 M 4 ; b) No hay precipitado.
 PRUEBA GENERAL OPCIÓN A PROBLEMA.- La solubilidad del Cr(OH) 3 es 0,13 mg ml 1 : a) Determina la constante de solubilidad K ps del hidróxido de cromo (III). b) Se tiene una disolución de CrCl 3 de concentración
PRUEBA GENERAL OPCIÓN A PROBLEMA.- La solubilidad del Cr(OH) 3 es 0,13 mg ml 1 : a) Determina la constante de solubilidad K ps del hidróxido de cromo (III). b) Se tiene una disolución de CrCl 3 de concentración
De cualquier manera, solo estudiaremos en esta unidad los compuestos inorgánicos.
 Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
PRÁCTICA 4 DETERMINACIÓN DE LA CONCENTRACIÓN IÓNICA TOTAL DEL AGUA POTABLE, USANDO LA CROMATOGRAFÍA DE INTERCAMBIO IÓNICO
 PRÁCTICA 4 DETERMINACIÓN DE LA CONCENTRACIÓN IÓNICA TOTAL DEL AGUA POTABLE, USANDO LA CROMATOGRAFÍA DE INTERCAMBIO IÓNICO 1.- FUNDAMENTO TEÓRICO. 1.1.- Materiales de intercambio iónico. El intercambio
PRÁCTICA 4 DETERMINACIÓN DE LA CONCENTRACIÓN IÓNICA TOTAL DEL AGUA POTABLE, USANDO LA CROMATOGRAFÍA DE INTERCAMBIO IÓNICO 1.- FUNDAMENTO TEÓRICO. 1.1.- Materiales de intercambio iónico. El intercambio
BIOELEMENTOS AGUA Y SALES MINERALES
 BIOELEMENTOS AGUA Y SALES MINERALES BIOELEMENTOS PROPIEDADES Capas electrónicas externas incompletas ENLACES COVALENTES Nº atómico bajo ENLACES ESTABLES Oxígeno y Nitrógeno electronegativos BIOMOLÉCULAS
BIOELEMENTOS AGUA Y SALES MINERALES BIOELEMENTOS PROPIEDADES Capas electrónicas externas incompletas ENLACES COVALENTES Nº atómico bajo ENLACES ESTABLES Oxígeno y Nitrógeno electronegativos BIOMOLÉCULAS
J. L. Sánchez Guillén. IES Pando - Oviedo Departamento de Biología y Geología 1
 J. L. Sánchez Guillén IES Pando - Oviedo Departamento de Biología y Geología 1 El agua es la molécula más abundante en los medios orgánicos. Un 70% del peso celular está formado por moléculas de agua.
J. L. Sánchez Guillén IES Pando - Oviedo Departamento de Biología y Geología 1 El agua es la molécula más abundante en los medios orgánicos. Un 70% del peso celular está formado por moléculas de agua.
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA
 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA PROGRAMA DE INGENIERIA DE ALIMENTOS 211612 TRANSFERENCIA DE MASA ACTIVIDAD 11 RECONOCIMIENTO UNIDAD 3 BOGOTA D.C. Extracción líquido - líquido La extracción líquido-líquido,
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA PROGRAMA DE INGENIERIA DE ALIMENTOS 211612 TRANSFERENCIA DE MASA ACTIVIDAD 11 RECONOCIMIENTO UNIDAD 3 BOGOTA D.C. Extracción líquido - líquido La extracción líquido-líquido,
2.3 SISTEMAS HOMOGÉNEOS.
 2.3 SISTEMAS HOMOGÉNEOS. 2.3.1 DISOLUCIONES. Vemos que muchos cuerpos y sistemas materiales son heterogéneos y podemos observar que están formados por varias sustancias. En otros no podemos ver que haya
2.3 SISTEMAS HOMOGÉNEOS. 2.3.1 DISOLUCIONES. Vemos que muchos cuerpos y sistemas materiales son heterogéneos y podemos observar que están formados por varias sustancias. En otros no podemos ver que haya
Es la disciplina que estudia las estructuras corporales y sus interrelaciones.
 Anatomía Es la disciplina que estudia las estructuras corporales y sus interrelaciones. Fisiología Es la disciplina que estudia la función de los diferentes aparatos y sistemas del organismo. Fisiología
Anatomía Es la disciplina que estudia las estructuras corporales y sus interrelaciones. Fisiología Es la disciplina que estudia la función de los diferentes aparatos y sistemas del organismo. Fisiología
BIOMOLÉCULAS: PROTEÍNAS
 FICHA PARA EL DOCENTE Objetivos Introducir al alumno en los conceptos de aminoácidos y proteínas. Detallar los diferentes tipos de aminoácidos, sus funciones e importancia. Discutir nociones básicas acerca
FICHA PARA EL DOCENTE Objetivos Introducir al alumno en los conceptos de aminoácidos y proteínas. Detallar los diferentes tipos de aminoácidos, sus funciones e importancia. Discutir nociones básicas acerca
FUERZAS INTERMOLECULARES
 FUERZAS INTERMOLECULARES Lic. Lidia Iñigo Las fuerzas intermoleculares, como su nombre lo indica, son las fuerzas que unen moléculas. Ya deberías saber que no todas las sustancias forman moléculas. Existen
FUERZAS INTERMOLECULARES Lic. Lidia Iñigo Las fuerzas intermoleculares, como su nombre lo indica, son las fuerzas que unen moléculas. Ya deberías saber que no todas las sustancias forman moléculas. Existen
Dar a conocer la capacidad de disolución del agua frente a otras sustancias.
 MINISTERIO DE EDUCACION Actividad 1: Agua en la vida II. Laboratorio: Solubilidad del agua 1. Tema: AGUA DISOLVENTE UNIVERSAL 2. Objetivo: Dar a conocer la capacidad de disolución del agua frente a otras
MINISTERIO DE EDUCACION Actividad 1: Agua en la vida II. Laboratorio: Solubilidad del agua 1. Tema: AGUA DISOLVENTE UNIVERSAL 2. Objetivo: Dar a conocer la capacidad de disolución del agua frente a otras
Sistema formado por varias substancias en el que a simple vista se distinguen los diferentes componentes.
 PRINCIPIOS BASICOS Sistema homogéneo : ( DISOLUCIONES ) Sistema integrado por varias substancias no distinguibles a simple vista, pero que se pueden separar por procedimientos físicos. por Ejem. : cambios
PRINCIPIOS BASICOS Sistema homogéneo : ( DISOLUCIONES ) Sistema integrado por varias substancias no distinguibles a simple vista, pero que se pueden separar por procedimientos físicos. por Ejem. : cambios
LOS FACTORES DEL ECOSISTEMA
 CICLO AANZADO / 1 Grado Semana icha 1º 14 5 SECUNDARIA CIENCIA, AMBIENTE Y SALUD LOS ACTORES DEL ECOSISTEMA 1. Escucha con atención : Los factores ambientales afectan directamente el desarrollo y crecimiento
CICLO AANZADO / 1 Grado Semana icha 1º 14 5 SECUNDARIA CIENCIA, AMBIENTE Y SALUD LOS ACTORES DEL ECOSISTEMA 1. Escucha con atención : Los factores ambientales afectan directamente el desarrollo y crecimiento
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO. Modelo Curso 2010-2011
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
ALIMENTACIÓN Y DEPORTE
 CURSO NIVEL III Entrenador Nacional de Fútbol y Fútbol Sala Técnico deportivo Superior. ALIMENTACIÓN Y DEPORTE Apuntes del curso de entrenadores de fútbol y fútbol sala Nivel 3, impartido por la Escuela
CURSO NIVEL III Entrenador Nacional de Fútbol y Fútbol Sala Técnico deportivo Superior. ALIMENTACIÓN Y DEPORTE Apuntes del curso de entrenadores de fútbol y fútbol sala Nivel 3, impartido por la Escuela
Química, desarrollo histórico y relación con otras ciencias
 Química, desarrollo histórico y relación con otras ciencias La definición de química hace una división entre la época antigua y la moderna; en la primera los procesos químicos eran realizados por artesanos
Química, desarrollo histórico y relación con otras ciencias La definición de química hace una división entre la época antigua y la moderna; en la primera los procesos químicos eran realizados por artesanos
2.4 - Tejido muscular
 2.4 - Tejido muscular Los animales poseemos un tejido contráctil especializado: el tejido muscular Está formado por células con gran cantidad de fibras contráctiles internas Estas fibras están formadas
2.4 - Tejido muscular Los animales poseemos un tejido contráctil especializado: el tejido muscular Está formado por células con gran cantidad de fibras contráctiles internas Estas fibras están formadas
UNIDAD 4: LAS DISOLUCIONES
 UNIDAD 4: LAS DISOLUCIONES Lee atentamente: 1. EL AGUA QUE BEBEMOS ES UNA MEZCLA DE VARIAS SUSTANCIAS El agua que se puede beber recibe el nombre de agua potable. El agua que bebemos contiene, además de
UNIDAD 4: LAS DISOLUCIONES Lee atentamente: 1. EL AGUA QUE BEBEMOS ES UNA MEZCLA DE VARIAS SUSTANCIAS El agua que se puede beber recibe el nombre de agua potable. El agua que bebemos contiene, además de
H + =10-7 y ph=7. H + <10-7 y ph>7.
 REACCIÓN DEL SUELO Las letras ph son una abreviación de "pondus hydrogenii", traducido como potencial de hidrógeno, y fueron propuestas por Sorensen en 1909, que las introdujo para referirse a concentraciones
REACCIÓN DEL SUELO Las letras ph son una abreviación de "pondus hydrogenii", traducido como potencial de hidrógeno, y fueron propuestas por Sorensen en 1909, que las introdujo para referirse a concentraciones
ESTRUCTURA DE LA MATERIA QCA 09 ANDALUCÍA
 1.- Considere el elemento cuya configuración electrónica es 1s 2 2s 2 2p 6 3s 2 3p 4. a) De qué elemento se trata? b) Justifique el periodo y el grupo del sistema periódico a los que pertenece. c) Cuál
1.- Considere el elemento cuya configuración electrónica es 1s 2 2s 2 2p 6 3s 2 3p 4. a) De qué elemento se trata? b) Justifique el periodo y el grupo del sistema periódico a los que pertenece. c) Cuál
GEOMETRÍA MOLECULAR. Lic. Lidia Iñigo
 GEOMETRÍA MOLECULAR Lic. Lidia Iñigo Hemos dicho al estudiar uniones químicas que un enlace covalente es polar cuando existe cierta diferencia de electronegatividad entre los átomos que se unen. La magnitud
GEOMETRÍA MOLECULAR Lic. Lidia Iñigo Hemos dicho al estudiar uniones químicas que un enlace covalente es polar cuando existe cierta diferencia de electronegatividad entre los átomos que se unen. La magnitud
Trabajo Práctico N o 1
 1 Trabajo Práctico N o 1 Soluciones y diluciones OBJETIVOS - Conocer todas las formas de indicar la concentración química de una solución. - Ser capaz de calcular la concentración de una solución a partir
1 Trabajo Práctico N o 1 Soluciones y diluciones OBJETIVOS - Conocer todas las formas de indicar la concentración química de una solución. - Ser capaz de calcular la concentración de una solución a partir
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10
 CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
Tema 7: Solubilidad. (Fundamentos de Química, Grado en Física) Equilibrio químico Enero Mayo, 2011 1 / 24
 Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
UNIDAD 3 AGUA, DE DÓNDE, PARA QUÉ Y DE QUIÉN?
 UNIDAD 3 AGUA, DE DÓNDE, PARA QUÉ Y DE QUIÉN? 3.1 Tanta agua y nos podemos morir de sed Las aguas por su origen se clasifican en meteóricas (lluvia, granizo, nieve) y telúricas (ríos, manantiales, mares).
UNIDAD 3 AGUA, DE DÓNDE, PARA QUÉ Y DE QUIÉN? 3.1 Tanta agua y nos podemos morir de sed Las aguas por su origen se clasifican en meteóricas (lluvia, granizo, nieve) y telúricas (ríos, manantiales, mares).
Tema 1: Sustancias puras, mezclas y disoluciones
 Tema 1: Sustancias puras, mezclas y disoluciones 1.- Tipos de materia Recordemos que materia es todo aquello que tiene masa y volumen. Toda la materia está formada por elementos químicos (recuerda la tabla
Tema 1: Sustancias puras, mezclas y disoluciones 1.- Tipos de materia Recordemos que materia es todo aquello que tiene masa y volumen. Toda la materia está formada por elementos químicos (recuerda la tabla
Introducción a la fisiología: la célula y la fisiología general
 I Introducción a la fisiología: la célula y la fisiología general 1 Organización funcional del cuerpo humano y control del «medio interno» 2 La célula y sus funciones 3 Control genético de la síntesis
I Introducción a la fisiología: la célula y la fisiología general 1 Organización funcional del cuerpo humano y control del «medio interno» 2 La célula y sus funciones 3 Control genético de la síntesis
PIP 4º ESO IES SÉNECA TRABAJO EXPERIMENTAL EN FÍSICA Y QUÍMICA
 MEZCLAS Las mezclas son agrupaciones de dos o más sustancias puras en proporciones variables. Si presentan un aspecto uniforme son homogéneas y también se denominan disoluciones, como la de azúcar en agua.
MEZCLAS Las mezclas son agrupaciones de dos o más sustancias puras en proporciones variables. Si presentan un aspecto uniforme son homogéneas y también se denominan disoluciones, como la de azúcar en agua.
Ciencias Naturales 5º Primaria Tema 7: La materia
 1. La materia que nos rodea Propiedades generales de la materia Los objetos materiales tienes en común dos propiedades, que se llaman propiedades generales de la materia: Poseen masa. La masa es la cantidad
1. La materia que nos rodea Propiedades generales de la materia Los objetos materiales tienes en común dos propiedades, que se llaman propiedades generales de la materia: Poseen masa. La masa es la cantidad
atmosférico es mayor; más aún, si las posibilidades de reciclado natural de mismo se reducen al disminuir los bosques y la vegetación en general.
 TODAS LAS PREGUNTAS SON DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA. RESPONDA LAS PREGUNTAS 45 A 51 DE ACUERDO CON Ciclo del Carbono El ciclo del carbono es la sucesión de transformaciones que presenta el
TODAS LAS PREGUNTAS SON DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA. RESPONDA LAS PREGUNTAS 45 A 51 DE ACUERDO CON Ciclo del Carbono El ciclo del carbono es la sucesión de transformaciones que presenta el
Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante
 Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante Objetivos: Los estudiantes serán capaces de Explicar cuáles moléculas hacen que muchas de las plantas tengan hojas verdes
Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante Objetivos: Los estudiantes serán capaces de Explicar cuáles moléculas hacen que muchas de las plantas tengan hojas verdes
Definición de la célula
 Página 1 de 8 La Célula: estructura interna y metabolismo Definición de la célula La célula se entiende como la unidad mínima de un organismo capaz de actuar de manera autónoma en su funcionamiento y reproducción.
Página 1 de 8 La Célula: estructura interna y metabolismo Definición de la célula La célula se entiende como la unidad mínima de un organismo capaz de actuar de manera autónoma en su funcionamiento y reproducción.
El corazón, al tener paredes musculares, puede dilatarse y contraerse, lo que le permite bombear la sangre.
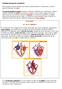 Fisiología del aparato circulatorio El corazón, al tener paredes musculares, puede dilatarse y contraerse, lo que le permite bombear la sangre. El corazón bombea la sangre de forma continua, mediante dos
Fisiología del aparato circulatorio El corazón, al tener paredes musculares, puede dilatarse y contraerse, lo que le permite bombear la sangre. El corazón bombea la sangre de forma continua, mediante dos
Química 2º Bach. Ácido-base 28/02/05
 Química 2º Bach. Ácido-base 28/02/05 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [3 PUNTOS / UNO] 1. Calcula el ph de una solución obtenida al disolver 20 L de amoníaco, medidos a 10 0 C y 2,0 atm
Química 2º Bach. Ácido-base 28/02/05 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [3 PUNTOS / UNO] 1. Calcula el ph de una solución obtenida al disolver 20 L de amoníaco, medidos a 10 0 C y 2,0 atm
QUÍMICA DEL AGUA. Año de realización: 2011-2012. PROFESOR/A Ana Karina Boltes Espínola
 QUÍMICA DEL AGUA MASTER EN INGENIERÍA Y GESTIÓN DEL AGUA Año de realización: 011-01 PROFESOR/A Ana Karina Boltes Espínola INGENIERÍA Y GESTIÓN DEL AGUA/Antonio Rodríguez Fernández-Alba Índice 1. PROPIEDADES
QUÍMICA DEL AGUA MASTER EN INGENIERÍA Y GESTIÓN DEL AGUA Año de realización: 011-01 PROFESOR/A Ana Karina Boltes Espínola INGENIERÍA Y GESTIÓN DEL AGUA/Antonio Rodríguez Fernández-Alba Índice 1. PROPIEDADES
Lo esencial sobre el agua
 Lo esencial sobre el agua Prefacio Contenido El agua potable es el alimento más importante y la base de un buen nivel de higiene. Se utiliza en las áreas más diversas de la vida: como bebida, para preparar
Lo esencial sobre el agua Prefacio Contenido El agua potable es el alimento más importante y la base de un buen nivel de higiene. Se utiliza en las áreas más diversas de la vida: como bebida, para preparar
Práctica 1: Observación de fenómenos osmóticos en epidermis de cebolla
 Práctica 1: Observación de fenómenos osmóticos en epidermis de cebolla 1. A qué se debe la gran extensión de la coloración de la célula tras la tinción con rojo neutro? Al sumergir la epidermis en la disolución
Práctica 1: Observación de fenómenos osmóticos en epidermis de cebolla 1. A qué se debe la gran extensión de la coloración de la célula tras la tinción con rojo neutro? Al sumergir la epidermis en la disolución
3.1. ÁCIDOS Y BASES. HA (ac) H + (ac) + A - (ac)
 3.1. ÁCIDOS Y BASES Según la teoría de Arrhenius, ácido es toda sustancia capaz de dar iones hidrógeno (H ) como uno de sus productos iónicos de disociación en agua : HA H A - El ion H, denominado protón
3.1. ÁCIDOS Y BASES Según la teoría de Arrhenius, ácido es toda sustancia capaz de dar iones hidrógeno (H ) como uno de sus productos iónicos de disociación en agua : HA H A - El ion H, denominado protón
La electrólisis CONTENIDOS. Electrolitos. Iones. Carga eléctrica negativa. www.codelcoeduca.cl
 La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
Guía para el docente El agua Propiedades físicas y químicas del agua. Guía para el docente
 Guía para el docente Descripción curricular: - Nivel: 1º Medio - Subsector: Ciencias químicas - Unidad temática: - Palabras claves: Anomalía del agua, densidad, dureza del agua. - Contenidos curriculares:
Guía para el docente Descripción curricular: - Nivel: 1º Medio - Subsector: Ciencias químicas - Unidad temática: - Palabras claves: Anomalía del agua, densidad, dureza del agua. - Contenidos curriculares:
PREGUNTAS DE TEST SOBRE ÁCIDOS Y BASES
 PREGUNTAS DE TEST SOBRE ÁCIDOS Y BASES A GENERALIDADES B DEFINICION DE ph C ACIDOS Y BASES FUERTES D ACIDOS Y BASES DEBILES: E DISOLUCIONES DE SALES: F DISOLUCIONES TAMPON: G VALORACIONES ACIDOBASE: H
PREGUNTAS DE TEST SOBRE ÁCIDOS Y BASES A GENERALIDADES B DEFINICION DE ph C ACIDOS Y BASES FUERTES D ACIDOS Y BASES DEBILES: E DISOLUCIONES DE SALES: F DISOLUCIONES TAMPON: G VALORACIONES ACIDOBASE: H
La Bioquímica y los Bioelementos. 1.Los elementos de la vida 2.Las biomoléculas 3.El agua 4.Las sales minerales
 La Bioquímica y los Bioelementos 1.Los elementos de la vida 2.Las biomoléculas 3.El agua 4.Las sales minerales LOS ELEMENTOS DE LA VIDA Los ss.vv. (seres vivos) están constituidos por materia y, por
La Bioquímica y los Bioelementos 1.Los elementos de la vida 2.Las biomoléculas 3.El agua 4.Las sales minerales LOS ELEMENTOS DE LA VIDA Los ss.vv. (seres vivos) están constituidos por materia y, por
DISOLUCIONES Y ESTEQUIOMETRÍA
 DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
E4B.S2007. a) HCl + H 2 O Cl + H 3 O + ácido1 base2 base1 ácido2. b) NH 3 + H 2 O NH 4 + + OH base1 ácido2 ácido1 base2
 TEMA 6. ACIDOS Y BASES E1B.S009 Para las especies CN, HF y CO 3, en disolución acuosa: a) Escriba, según corresponda, la fórmula del ácido o de la base conjugados. b) Justifique, mediante la reacción correspondiente,
TEMA 6. ACIDOS Y BASES E1B.S009 Para las especies CN, HF y CO 3, en disolución acuosa: a) Escriba, según corresponda, la fórmula del ácido o de la base conjugados. b) Justifique, mediante la reacción correspondiente,
UNIDAD 2: LA TIERRA COMO PLANETA
 UNIDAD 2: LA TIERRA COMO PLANETA 1.EL INTERIOR DE LA TIERRA Lee con atención El interior de nuestro planeta está formado por materiales que se encuentran a altas temperaturas. Los materiales que forman
UNIDAD 2: LA TIERRA COMO PLANETA 1.EL INTERIOR DE LA TIERRA Lee con atención El interior de nuestro planeta está formado por materiales que se encuentran a altas temperaturas. Los materiales que forman
SUAVIZACIÓN CONCEPTOS BÁSICOS
 SUAVIZACIÓN CONCEPTOS BÁSICOS Revisemos algunos conceptos que utilizarás para el diseño de los equipos del sistema de suavización, recuerda que muchos ya los has visto en cursos anteriores y que esto es
SUAVIZACIÓN CONCEPTOS BÁSICOS Revisemos algunos conceptos que utilizarás para el diseño de los equipos del sistema de suavización, recuerda que muchos ya los has visto en cursos anteriores y que esto es
Si el agua que llega a la superficie terrestre entra en contacto con minerales de caliza (carbonato de calcio) ocurre la disolución del mineral.
 COMPOSICIÓN QUÍMICA DE LAS AGUAS POTABLES Ingeniería de Tratamiento y Acondicionamiento de Aguas 2.0 INTERPRETACIÓN DE LOS ANÁLISIS DE AGUA Un análisis químico del agua nos indica que sustancias se encuentran
COMPOSICIÓN QUÍMICA DE LAS AGUAS POTABLES Ingeniería de Tratamiento y Acondicionamiento de Aguas 2.0 INTERPRETACIÓN DE LOS ANÁLISIS DE AGUA Un análisis químico del agua nos indica que sustancias se encuentran
Las membranas conforman los límites de las células; están constituidas por una bicapa lipídica
 Células y membranas Las membranas conforman los límites de las células; están constituidas por una bicapa lipídica Los orgánulos: son compartimentos rodeados de membrana situadas en el interior de las
Células y membranas Las membranas conforman los límites de las células; están constituidas por una bicapa lipídica Los orgánulos: son compartimentos rodeados de membrana situadas en el interior de las
U.T.N. F.R.Ro DEPTO. DE INGENIERÍA QUIMICA CATEDRA DE INTEGRACIÓN II PAG. 1
 U.T.N. F.R.Ro DEPTO. DE INGENIERÍA QUIMICA CATEDRA DE INTEGRACIÓN II PAG. 1 Introducción: En una planta química, para obtener el producto final deseado, el proceso se realiza en varias etapas, que podrían
U.T.N. F.R.Ro DEPTO. DE INGENIERÍA QUIMICA CATEDRA DE INTEGRACIÓN II PAG. 1 Introducción: En una planta química, para obtener el producto final deseado, el proceso se realiza en varias etapas, que podrían
La Hidrosfera. El agua es una de las sustancias que más abunda a nuestro alrededor.
 La Hidrosfera El agua es una de las sustancias que más abunda a nuestro alrededor. En estado sólido se encuentra en las regiones polares y en las cimas de las altas montañas. Es agua en estado sólido la
La Hidrosfera El agua es una de las sustancias que más abunda a nuestro alrededor. En estado sólido se encuentra en las regiones polares y en las cimas de las altas montañas. Es agua en estado sólido la
El término alcalinidad no debe confundirse con alcalino, que indica la situación en donde el nivel de ph
 CONTROL DE LA ALCALINIDAD DE AGUAS DE RIEGO La mayoría de la nuestra aguas de riego contienen bicarbonatos disueltos, las que son bases y por lo tanto agregan al suelo material de encalado. El riego con
CONTROL DE LA ALCALINIDAD DE AGUAS DE RIEGO La mayoría de la nuestra aguas de riego contienen bicarbonatos disueltos, las que son bases y por lo tanto agregan al suelo material de encalado. El riego con
I) Biomoléculas 2) El agua I-2 EL AGUA
 I-2 EL AGUA IMPRTANCIA DEL AGUA PARA LS SERES VIVS El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. No es de extrañar entonces que el agua sea una sustancia esencial
I-2 EL AGUA IMPRTANCIA DEL AGUA PARA LS SERES VIVS El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. No es de extrañar entonces que el agua sea una sustancia esencial
TREN DE FILTRACIÓN DE AGUA
 TREN DE FILTRACIÓN DE AGUA Fluj 4 1 2 3 5 DESCRIPCIÓN DEL SISTEMA 1. FILTRO DE SEDIMENTOS 1 El Primer paso en el proceso de filtración de agua. El filtro de sedimentos elimina las partículas suspendidas
TREN DE FILTRACIÓN DE AGUA Fluj 4 1 2 3 5 DESCRIPCIÓN DEL SISTEMA 1. FILTRO DE SEDIMENTOS 1 El Primer paso en el proceso de filtración de agua. El filtro de sedimentos elimina las partículas suspendidas
EL VALOR ECOLÓGICO DEL AGUA
 1 Capítulo VALOR ECOLÓGICO DEL AGUA Capítulo 1 EL VALOR ECOLÓGICO DEL AGUA Los conceptos Para comenzar a reflexionar sobre el valor ecológico del agua, es necesario un acercamiento a los tres conceptos
1 Capítulo VALOR ECOLÓGICO DEL AGUA Capítulo 1 EL VALOR ECOLÓGICO DEL AGUA Los conceptos Para comenzar a reflexionar sobre el valor ecológico del agua, es necesario un acercamiento a los tres conceptos
Egileak: A.Ferreira.P, A.Santamaría.S, C.Khaldi.H
 Egileak: A.Ferreira.P, A.Santamaría.S, C.Khaldi.H Composición de los alimentos A pesar de la diversidad en su composición, los análisis químicos revelan que todos los alimentos presentan seis grupos de
Egileak: A.Ferreira.P, A.Santamaría.S, C.Khaldi.H Composición de los alimentos A pesar de la diversidad en su composición, los análisis químicos revelan que todos los alimentos presentan seis grupos de
TEMA 11. MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN
 TEMA 11. MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN 1. Destilación 2. Extracción 3. Sublimación 4. Cristalización 5. Cromatografía 6. Fórmulas empíricas y moleculares 2 Tema 11 TEMA 11. Métodos físicos
TEMA 11. MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN 1. Destilación 2. Extracción 3. Sublimación 4. Cristalización 5. Cromatografía 6. Fórmulas empíricas y moleculares 2 Tema 11 TEMA 11. Métodos físicos
1. La magnitud 0,0000024mm expresada en notación científica es: a) 2,4 10 6 mm b) 2,4 10 5 mm c) 24 10 5 mm d) 24 10 6 mm
 Se responderá escribiendo un aspa en el recuadro correspondiente a la respuesta correcta o a la que con carácter más general suponga la contestación cierta más completa en la HOJA DE RESPUESTAS. Se facilitan
Se responderá escribiendo un aspa en el recuadro correspondiente a la respuesta correcta o a la que con carácter más general suponga la contestación cierta más completa en la HOJA DE RESPUESTAS. Se facilitan
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS FUNDAMENTOS ESPECTROSCOPICOS ORBITALES ATÓMICOS
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS FUNDAMENTOS ESPECTROSCOPICOS Integrantes: Walter Bermúdez Lizbeth Sánchez Curso: Jueves 10:00 a 12:00 ORBITALES ATÓMICOS 1.- Definición de
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS FUNDAMENTOS ESPECTROSCOPICOS Integrantes: Walter Bermúdez Lizbeth Sánchez Curso: Jueves 10:00 a 12:00 ORBITALES ATÓMICOS 1.- Definición de
MÓDULO: GESTIÓN DE RESIDUOS TEMA: DESMINERALIZACIÓN
 MÓDULO: GESTIÓN DE RESIDUOS TEMA: DESMINERALIZACIÓN DOCUMENTACIÓN ELABORADA POR: NIEVES CIFUENTES MASTER EN INGENIERIÁ MEDIOAMBIENTAL Y GESTIÓN DEL AGUA ÍNDICE 1. INTRODUCCIÓN 2. INTERCAMBIO IÓNICO 3.
MÓDULO: GESTIÓN DE RESIDUOS TEMA: DESMINERALIZACIÓN DOCUMENTACIÓN ELABORADA POR: NIEVES CIFUENTES MASTER EN INGENIERIÁ MEDIOAMBIENTAL Y GESTIÓN DEL AGUA ÍNDICE 1. INTRODUCCIÓN 2. INTERCAMBIO IÓNICO 3.
Las técnicas para separar mezclas no pueden alterar la naturaleza de las sustancias que se desea separar.
 CONTENIDOS: Las técnicas para separar mezclas no pueden alterar la naturaleza de las sustancias que se desea separar. 1. Tamización 2. Filtración 3. Separación magnética 4. Decantación 5. Cristalización
CONTENIDOS: Las técnicas para separar mezclas no pueden alterar la naturaleza de las sustancias que se desea separar. 1. Tamización 2. Filtración 3. Separación magnética 4. Decantación 5. Cristalización
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016
 REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
Biocenosis : conjunto de seres vivos de un ecosistema. Se organizan
 Biocenosis : conjunto de seres vivos de un ecosistema. Se organizan en Organismo : cada ser vivo individual Población : formada por seres vivos de la misma especie Comunidad : formada por diversas poblaciones
Biocenosis : conjunto de seres vivos de un ecosistema. Se organizan en Organismo : cada ser vivo individual Población : formada por seres vivos de la misma especie Comunidad : formada por diversas poblaciones
III. DIFUSION EN SOLIDOS
 Metalografía y Tratamientos Térmicos III - 1 - III. DIFUSION EN SOLIDOS III.1. Velocidad de procesos en sólidos Muchos procesos de producción y aplicaciones en materiales de ingeniería están relacionados
Metalografía y Tratamientos Térmicos III - 1 - III. DIFUSION EN SOLIDOS III.1. Velocidad de procesos en sólidos Muchos procesos de producción y aplicaciones en materiales de ingeniería están relacionados
Hidrosfera. 1) En las aguas epicontinentales se incluyen el mar Caspio, el Aral y el mar Muerto, además de lagos, ríos, etc.
 Hidrosfera Formación Cuando la Tierra se fue formando, hace unos 4600 millones de años, las altas temperaturas hacían que toda el agua estuviera en forma de vapor. Al enfriarse por debajo del punto de
Hidrosfera Formación Cuando la Tierra se fue formando, hace unos 4600 millones de años, las altas temperaturas hacían que toda el agua estuviera en forma de vapor. Al enfriarse por debajo del punto de
3. Comprensión Lectora
 3. Comprensión Lectora Prelectura. Consiste en realizar una lectura muy rápida de todo lo que se ha de estudiar con el fin de sacar una idea general sobre el contenido del texto. Lectura comprensiva. Se
3. Comprensión Lectora Prelectura. Consiste en realizar una lectura muy rápida de todo lo que se ha de estudiar con el fin de sacar una idea general sobre el contenido del texto. Lectura comprensiva. Se
EQUILIBRIO ÁCIDO-BASE
 EQUIIBRIO ÁCIDO-BASE Electrolito y no electrolito os electrolitos son sustancias (ácidos, bases y sales) que al disolverse en agua o fundidos, pueden conducir la corriente eléctrica. os electrolitos pueden
EQUIIBRIO ÁCIDO-BASE Electrolito y no electrolito os electrolitos son sustancias (ácidos, bases y sales) que al disolverse en agua o fundidos, pueden conducir la corriente eléctrica. os electrolitos pueden
Bolilla 7: Propiedades de los Líquidos
 Bolilla 7: Propiedades de los Líquidos 1 Bolilla 7: Propiedades de los Líquidos Estudiaremos propiedades de los líquidos, derivadas de las fuerzas de cohesión entre las moléculas que lo componen. Además
Bolilla 7: Propiedades de los Líquidos 1 Bolilla 7: Propiedades de los Líquidos Estudiaremos propiedades de los líquidos, derivadas de las fuerzas de cohesión entre las moléculas que lo componen. Además
MANUAL PRACTICO DE NUTRICIÒN
 www.nutrimedperu.com MANUAL PRACTICO DE NUTRICIÒN Lic. Nutricionista: Castrejón Miguel ángel Portocarrero No de Colegiatura: CNP: 3904 Email: mpc2804@nutrimedperu.com Web: www.nutrimedperu.com Introducción
www.nutrimedperu.com MANUAL PRACTICO DE NUTRICIÒN Lic. Nutricionista: Castrejón Miguel ángel Portocarrero No de Colegiatura: CNP: 3904 Email: mpc2804@nutrimedperu.com Web: www.nutrimedperu.com Introducción
UNIDAD 6: La parte líquida de la Tierra.
 UNIDAD 6: La parte líquida de la Tierra. Como recordaras de la unidad 5, la parte externa del planeta Tierra tiene estas capas: La atmósfera: formada por gases, entre los que abundan el oxígeno y el nitrógeno.
UNIDAD 6: La parte líquida de la Tierra. Como recordaras de la unidad 5, la parte externa del planeta Tierra tiene estas capas: La atmósfera: formada por gases, entre los que abundan el oxígeno y el nitrógeno.
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 EL AGUA: VOLÚMENES Y COMPOSICIÓN DE LOS LÍQUIDOS CORPORALES La vida comenzó en el agua del mar, y las condiciones que reinaban en aquel ambiente primigenio marcaron las características químicas de la materia
EL AGUA: VOLÚMENES Y COMPOSICIÓN DE LOS LÍQUIDOS CORPORALES La vida comenzó en el agua del mar, y las condiciones que reinaban en aquel ambiente primigenio marcaron las características químicas de la materia
Yo como, tú comes, él come Todos comemos?... y qué comemos?
 8vo Básico> Ciencias naturales Ciclos Biogeoquímicos Yo como, tú comes, él come Todos comemos?... y qué comemos? A quién se va a comer el ratón en realidad; al hongo, al oso, al cuervo, al otro ratón,
8vo Básico> Ciencias naturales Ciclos Biogeoquímicos Yo como, tú comes, él come Todos comemos?... y qué comemos? A quién se va a comer el ratón en realidad; al hongo, al oso, al cuervo, al otro ratón,
SÓLIDOS I. Tipos de sólidos. Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada.
 SÓLIDOS I Tipos de sólidos Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada. Sólidos amorfos: no presentan estructuras ordenadas. 1 Sólidos cristalinos Hay posiciones
SÓLIDOS I Tipos de sólidos Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada. Sólidos amorfos: no presentan estructuras ordenadas. 1 Sólidos cristalinos Hay posiciones
