ELECTROFORESIS Definición
|
|
|
- Ana Isabel Río Lagos
- hace 9 años
- Vistas:
Transcripción
1 ELECTROFORESIS
2 ELECTROFORESIS Definición: Método de análisis basado en la migración diferencial de sustancias en solución cargadas eléctricamente, por efecto de la aplicación de un campo eléctrico.
3 Aplicación n a: a Proteínas en general ADN y ARN Nucleótidos Aminoácidos Polisacáridos Fosfolípidos.
4 CLASIFICACION: a) Según n el soporte: Geles de poliacrilamida Geles de agarosa Tiras de acetato de celulosa Geles de almidón Papel de filtro b) Según n las características de la moléculas a separar: * Carga * Peso molecular (P.M.) * Punto isoeléctrico (p.i) * Combinaciones de las anteriores
5 TEORIA Una partícula cargada eléctricamente con la carga q colocada en un medio determinado y bajo la acción n de un campo eléctrico se verá sometida a dos fuerzas: A) la fuerza de atracción o fuerza propulsora,, llamada fuerza eléctrica (Fe( Fe) B) la fuerza resistente,, llamada resistencia viscosa (Fs( Fs). A) Fuerza eléctrica: (1) Fe = E. q Fe E = ---- = q V E : campo eléctrico V : diferencia de potencial aplicada sobre la longitud ( l ) I q : carga de la partícula
6 B) Resistencia viscosa: : ( 2 ) Fs = 6π π η r v η = viscosidad del medio r = radio de la partícula v = velocidad de la partícula La partícula es empujada por la Fe y su velocidad (v)( aumenta hasta un valor tal que ambas fuerzas se equilibran: E. q = 6π η r v Fe = Fs q Despejando la velocidad tenemos: (3) v = E π η r
7 q q En cambio, el factor depende del medio ( η ) y de la partícula π η r r q Esta relación: ----, se llama Movilidad Electroforética tica 6π η r q y se representa por la letra µ. µ = 6π η r Según (3) la velocidad será: v = E. µ, v = V/l. µ La velocidad de la partícula (v) en una electroforesis es proporcional al campo aplicado (E) y a su Movilidad Electroforética (µ).
8 Electroforesis en tiras de acetato de celulosa Cátodo Siembra Anodo - +
9 Cátodo Siembra Anodo Fuente de Poder (V)
10 Siembra Cátodo Anodo Fuente de Poder (V)
11 Cátodo ++ Siembra +- Anodo Fuente de Poder (V)
12 Cátodo ++ Siembra +- Anodo Fuente de Poder (V)
13 Cátodo ++ Siembra +- Anodo Fuente de Poder (V)
14 Cátodo ++ Siembra +- Anodo Fuente de Poder (V)
15 Carga de aminoácidos en función n del Glicina COOH ph H 3 N + C H H
16 Carga de aminoácidos en función n del Glicina COOH ph COO- H 3 N + C H H 3 N + C H H H pk 1 : 2.34 ph NaOH
17 Carga de aminoácidos en función n del Glicina COOH ph COO- COO- H 3 N + C H H 3 N + C H H 2 N C H H H H pk 1 : 2.34 pk 2 : 9.6 ph NaOH pi: 5.97
18 Ejercicio: Para separar una mezcla de proteínas se realizó una electroforesis con un buffer ph= 4.5. De acuerdo a la siguiente tabla de datos, conteste: Proteína pi a b c d e A. La proteína e migró al cátodo. B. Las proteínas a y d migraron al cátodo. C. La proteína a está más alejada que la e del lugar de siembra. D. La proteína e está más alejada que la a del lugar de siembra.
19 Ejercicio Cuál es el mejor buffer para separar estas cuatro proteínas: Proteína pi a b c d Buffer ph
20 Electroforesis de Proteínas 1) SDS-PAGE 2) Enfoque iso-el eléctrico (Iso-electric focusing) 3)2-D D PAGE (PAGE Bidimensional)
21 SDS - PAGE Geles de poliacrilamida 2β-Mercaptoetanol? El dodecil sulfato de sodio (SDS) es un detergente aniónico que desnaturaliza proteínas envolviendo el esqueleto polipeptídico y les confiere carga negativa.
22 PROCEDIMIENTO 1. Armado del soporte 2. Formación del gel 3. Siembra de la muestra 4. Corrida 5. Fijación y Coloración 6. Desteñido 7. Secado 8. Análisis
23 Siembra - +
24 Determinación n de Pesos Moleculares por SDS-PAGE Banda 1 Banda 2 Muestra St. (PM) Movilidad relativa de una Proteína (Rf). También llamado relación al frente. Rf= Distancia Recorrida por Proteína. Distancia Recorrida por Colorante Azul de Bromofenol PM Curva de Calibración de proteínas por SDS- PAGE al 12 % y = x R 2 = 0, ,2 0,4 0,6 0,8 1 Rf (cm) B1=5.43 cm B2=5.55 cm D.R.Col = 9.4 cm. Calcular el Rf y el PM para cada muestra.
25 Electroforesis de Proteínas 1) SDS-PAGE 2) Enfoque iso-el eléctrico (Iso-electric focusing) 3)2-D D PAGE (PAGE Bidimensional)
26 Dos corridas: 1) Enfoque de anfolitos, gradiente de ph. 2) Enfoque de proteínas. Enfoque iso-el eléctrico (Iso-electric focusing) NaOH ph 10 3 H 3 PO 4
27 Electroforesis de Proteínas 1) SDS-PAGE 2) Enfoque iso-el eléctrico (Iso-electric focusing) 3)2-D D PAGE (PAGE Bidimensional)
28 2-D PAGE (PAGE Bidimensional) Electroenfoque (Separación por pi) SDS-PAGE (Separación por Peso Molecular)
29 ELECTROFORESIS Uso en la profesión veterinaria, fundamentalmente en la separación e identificación de sustancias de componentes biológicos, especialmente líquidos como: suero, orina, líquido cefaloraquídeo, líquido de punciones, leche, etc.
30 Análisis de proteínas lácteas l por electroforesis Las proteínas de la leche se dividen en dos grupos: A) Caseínas son las que precipitan a ph 4.6 a 20ºC. Están compuestas por las fracciones αs1, αs2, β y κ; corresponden al 80 % del total de proteínas lácteas. B) Proteínas del suero: α-lactalbúmina y β-lactoglobulina. Las caseínas son muy importantes por su valor nutritivo y también por su influencia sobre los derivados lácteos. Hay alta correlación entre contenido de caseínas y rendimiento quesero; también influyen sobre características tales como el sabor, textura, etc. Objetivo 1: Separar e identificar las fracciones de caseínas bovinas y caprinas por SDS-PAGE.
31 Resultados
32 SDS-PAGE Caseínas Bovinas Caseínas Caprinas St. St. St. St. M M M αs 2 αs 1 β κ C.B. C.B. C.B.S. β-cn C.B.: Muestras individuales bovinas C.B.S.: St. de Caseína Bovina (Sigma) β-cn.: St. de beta-caseína (Sigma). C.B.S. C.S. C.T. αs 2 αs 1 y β C.B.S.: St. de Caseína Bovina (Sigma) C.S.: St. de Caseína Caprina (Sigma). C.T.: Muestra de Caseína Caprina de la raza Toggenburg. κ
33 Objetivo 2: Estudiar la actividad proteolítica de la enzima Pepsina porcina sobre la B.S.A. (Albúmina Sérica Bovina)
34 Resultado Tiempo en minutos en degradación de BSA por Pepsina porcina. BSA (min) St St. Pocillos: 1: St (PM): 14.3, 18.4, 24, 34.7, 45, 66 KD. 2: (BSA) a tiempo 0 con Pepsina. 3: Idem 2 pero a t: 10 minutos. 4: a 20 min. 5: a 30 min. 6: a 45 min 7: a 60 min. 8: St igual que en pocillo 1 P:
35 Hemoglobina Hemoglobina (PM=64500): formada por cuatro cadenas polipeptídicas, dos cadenas α (141 aa) y dos cadenas β (146 aa).cada subunidad tiene un grupo Hemo con un átomo de Hierro en estado ferroso (Fe 2 +) que son los que convierten a la Hb en una proteína cromogénica. Objetivo 3: Evaluar el comportamiento de la Hemoglobina corrida por SDS-PAGE, bajo condiciones desnaturalizantes.
36 Resultados
37 SDS-PAGE aplicado a Hemoglobina (Hb) PM aprox. SDS-PAGE (12%) Tinción con Azul de Coomasie Hb (BSA) SUERO
38 SDS-PAGE aplicado a Hemoglobina (Hb) PM aprox. SDS-PAGE (12%) Tinción con Azul de Coomasie SDS-PAGE (15%) Sin tinción PM aprox Hb (BSA) SUERO Hb en diferentes concentraciones
39 Ejercicios 1) Se realiza una electroforesis en un buffer ph 7.6, de una mezcla de tres proteínas (a, b y c) cuyos pi son: pi (a) = 4.3 pi (b) = 5.6 pi (c) = 8.3 De acuerdo con estos datos: A) las proteínas (a) y (b) migrarán al ánodo. B) las proteínas (b) y (c) migrarán al ánodo. C) las proteínas (a) y (b) migrarán al cátodo. D) la proteína (b) migrará al cátodo.
40 2) Se desea separar por electroforesis una mezcla de tres proteínas (I, II, y III) utilizando un buffer ph 5.2 Teniendo en cuenta los siguientes datos: pi P.M. I II III Puede predecirse que: A) la proteína I se dirigirá al ánodo, y las proteínas II y III al cátodo. B) II estará más alejada que I del lugar de siembra. C) III estará más cerca del ánodo que I y II. D) I estará más alejada que II del lugar de siembra.
41 3) Se realizó la electroforesis bidimensional de una muestra de suero normal canino. A partir de los siguientes datos identifique las proteínas. PROTEINAS PM pi Albúmina α1-globulina α2-globulina β-globulina γ-globulina ph 2 ph 9
42 3) Se realizó la electroforesis bidimensional de una muestra de suero normal canino. A partir de los siguientes datos identifique las proteínas. PROTEINAS PM pi Albúmina α1-globulina α2-globulina β-globulina γ-globulina ph 2 ph 9 Electroenfoque SDS-PAGE
43 4) La figura adjunta muestra un gel SDS-PAGE. Las proteínas han sido teñidas con azul de coomassie. Se han aplicado 5 muestras distintas: 1,2 y 3.) Proceso de Purificación. 4.) Proteína Purificada 5.) El material purificado (banda C) con tres marcadores de peso molecular A, B y D. St. P.M. A B D D P.M. Curva de calibración de estándares de P.M. por SDS-PAGE. y = x R 2 = 0, A B D 0 0,2 0,4 0,6 0,8 1 Rf Cuál es el peso molecular de la proteína pura?
44 5) La protein-kinasa dependiente de camp de mamíferos muestra un peso molecular en condiciones nativas de En SDS-PAGE esta proteína da lugar a una banda de y otra de Cómo se explican estos resultados?
ELECTROFORESIS BIDIMENSIONAL (ISOELECTROENFOQUE y SDS-PAGE) Isoelectroenfoque (IEF)
 ELECTROFORESIS BIDIMENSIONAL (ISOELECTROENFOQUE y SDS-PAGE) Introducción Como bien sabemos, la electroforesis es un método de separación de moléculas biológicas que se basa en la migración de las mismas
ELECTROFORESIS BIDIMENSIONAL (ISOELECTROENFOQUE y SDS-PAGE) Introducción Como bien sabemos, la electroforesis es un método de separación de moléculas biológicas que se basa en la migración de las mismas
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B
 ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
ELECTROFORESIS. Objetivo de la clase. *fundamentos *procedimientos *algunas aplicaciones. Conocer los métodos electroforéticos
 ELECTROFORESIS Objetivo de la clase Conocer los métodos electroforéticos *fundamentos *procedimientos *algunas aplicaciones Definición de electroforesis Proceso de separación que se basa en la diferente
ELECTROFORESIS Objetivo de la clase Conocer los métodos electroforéticos *fundamentos *procedimientos *algunas aplicaciones Definición de electroforesis Proceso de separación que se basa en la diferente
PRÓTIDOS. 2.27 En el esquema se representa la fórmula general de un aminoácido. Indica qué es lo tapado con los recuadros del 1 al 4.
 PRÓTIDOS 2.27 En el esquema se representa la fórmula general de un aminoácido. Indica qué es lo tapado con los recuadros del 1 al 4. 2.28 - Se podrían separar los distintos aminoácidos de una mezcla en
PRÓTIDOS 2.27 En el esquema se representa la fórmula general de un aminoácido. Indica qué es lo tapado con los recuadros del 1 al 4. 2.28 - Se podrían separar los distintos aminoácidos de una mezcla en
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE FUNDAMENTO TEÓRICO La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo eléctrico. Las moléculas se separan
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE FUNDAMENTO TEÓRICO La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo eléctrico. Las moléculas se separan
Electroforesis de proteínas en geles de poliacrilamida
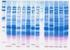 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa
 Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS. Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo (+)
 GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
Introducción. Electroforesis zonal Campo aplicado a un soporte estabilizante Muestra dispuesta sobre una zona reducida del soporte
 Introducción Técnica analítica separativa: Transporte de moléculas cargadas bajo la acción de un campo eléctrico Movilidad electroforética depende de: La carga de la molécula Depende del medio ph Fuerza
Introducción Técnica analítica separativa: Transporte de moléculas cargadas bajo la acción de un campo eléctrico Movilidad electroforética depende de: La carga de la molécula Depende del medio ph Fuerza
Monitoreo de un proceso de purificación de proteínas. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDS-PAGE. Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE)
 ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa.
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
Metodos de purificación
 Metodos de purificación Basado en las siguientes propiedades proteicas: Tamaño Solubilidad Carga Adsorción Afinidad CAROLINA VITA Característica Tamaño Solubidad Polaridad Carga Procedimientos Dialisis
Metodos de purificación Basado en las siguientes propiedades proteicas: Tamaño Solubilidad Carga Adsorción Afinidad CAROLINA VITA Característica Tamaño Solubidad Polaridad Carga Procedimientos Dialisis
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
Biomoléculas Orgánicas II
 Biomoléculas Orgánicas II INTRODUCCIÓN Tal como se vio en la clase anterior, los elementos químicos se organizan de tal forma que aumentan su complejidad y desarrollan funciones que son específicas. En
Biomoléculas Orgánicas II INTRODUCCIÓN Tal como se vio en la clase anterior, los elementos químicos se organizan de tal forma que aumentan su complejidad y desarrollan funciones que son específicas. En
EXPERIMENTO 3. CURVAS DE TITULACION DE AMINOACIDOS. DETERMINACION DE VALORES DE pk
 EXPERIMENTO 3 CURVAS DE TITULACION DE AMINOACIDOS. DETERMINACION DE VALORES DE pk REQUISITOS Repasar los conceptos sobre las propiedades de los aminoácidos (AA), reacciones ácido base, ph, pk, soluciones
EXPERIMENTO 3 CURVAS DE TITULACION DE AMINOACIDOS. DETERMINACION DE VALORES DE pk REQUISITOS Repasar los conceptos sobre las propiedades de los aminoácidos (AA), reacciones ácido base, ph, pk, soluciones
Electroforesis de proteínas
 Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
Proyecto de Fin de Cursos
 Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Aminoácidos. 7. Sobre la actividad óptica de los aminoácidos es cierto que:
 Aminoácidos 1. La valoración de valina con hidróxido sódico, conduce a la obtención de dos pks. La reacción de valoración que se produce al pk2 de 9,62 es: a) COOH + OH- --> -COO- + H2O. b) COOH + -NH2
Aminoácidos 1. La valoración de valina con hidróxido sódico, conduce a la obtención de dos pks. La reacción de valoración que se produce al pk2 de 9,62 es: a) COOH + OH- --> -COO- + H2O. b) COOH + -NH2
Técnicas de Caracterización y purificación
 Técnicas de Caracterización y purificación hidrofobicidad carga Propiedades de las proteínas utilizadas para caracterizar y purificar Carga Tamaño Forma Actividad biologica Hidrofobicidad PM Estabilidad
Técnicas de Caracterización y purificación hidrofobicidad carga Propiedades de las proteínas utilizadas para caracterizar y purificar Carga Tamaño Forma Actividad biologica Hidrofobicidad PM Estabilidad
7. Medida del ph: Disoluciones reguladoras. Precipitación isoeléctrica de la caseína
 7. Medida del ph: Disoluciones reguladoras. Precipitación isoeléctrica de la caseína José Peinado Peinado, Fermín Toribio Meléndez-Valdés Departamento de Bioquímica y Biología Molecular, Campus Universitario
7. Medida del ph: Disoluciones reguladoras. Precipitación isoeléctrica de la caseína José Peinado Peinado, Fermín Toribio Meléndez-Valdés Departamento de Bioquímica y Biología Molecular, Campus Universitario
CÁTEDRA DE QUÍMICA ORGÁNICA- 2012. Trabajo Práctico N 5: Aminoácidos y Proteínas. Carreras: Zootecnia y Medicina Veterinaria
 bjetivo del Trabajo Práctico: ÁTEDRA DE QUÍMA RGÁNA- 2012 Trabajo Práctico N 5: Aminoácidos y Proteínas arreras: Zootecnia y Medicina Veterinaria ) Realizar reacciones de caracterización de proteínas:
bjetivo del Trabajo Práctico: ÁTEDRA DE QUÍMA RGÁNA- 2012 Trabajo Práctico N 5: Aminoácidos y Proteínas arreras: Zootecnia y Medicina Veterinaria ) Realizar reacciones de caracterización de proteínas:
Diagnóstico Avanzado en Enfermedades Tropicales
 Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
BLOQUE I.- CUÁL ES LA COMPOSICIÓN DE LOS SERES VIVOS? LAS MOLÉCULAS DE LA VIDA
 BLOQUE I.- CUÁL ES LA COMPOSICIÓN DE LOS SERES VIVOS? LAS MOLÉCULAS DE LA VIDA UNIDAD DIDÁCTICA 1. Bioelementos y biomoléculas. Agua y sales minerales. Describir qué es la biología. Conocer las características
BLOQUE I.- CUÁL ES LA COMPOSICIÓN DE LOS SERES VIVOS? LAS MOLÉCULAS DE LA VIDA UNIDAD DIDÁCTICA 1. Bioelementos y biomoléculas. Agua y sales minerales. Describir qué es la biología. Conocer las características
PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG. 1 de 20 2 de 10 1 moneda de 1 10 monedas monedas monedas de 0.
 PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG Para saber lo que tengo debo separar las partes y cuantificar 1 de 20 2 de 10 1 moneda de 1 10 monedas 0.20 4 monedas 0.10 3 monedas
PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG Para saber lo que tengo debo separar las partes y cuantificar 1 de 20 2 de 10 1 moneda de 1 10 monedas 0.20 4 monedas 0.10 3 monedas
El agua. El agua es extraordinariamente abundante en la tierra y es indispensable para la vida.
 Sumario Las moléculas de los seres vivos: 1. El agua 2. El papel central del carbono 3. Moléculas orgánicas. Control de la actividad celular Fuente de energía para las células Proceso de fotosíntesis El
Sumario Las moléculas de los seres vivos: 1. El agua 2. El papel central del carbono 3. Moléculas orgánicas. Control de la actividad celular Fuente de energía para las células Proceso de fotosíntesis El
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS
 ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
PREGUNTAS PAU PROTEÍNAS
 PREGUNTAS PAU PROTEÍNAS EJERCICIO 1 a) Cuáles son las unidades estructurales de las proteínas? [0 2] b) Escriba su fórmula general [0 2]. c) Atendiendo a la variedad de radicales cite cuatro tipos de dichas
PREGUNTAS PAU PROTEÍNAS EJERCICIO 1 a) Cuáles son las unidades estructurales de las proteínas? [0 2] b) Escriba su fórmula general [0 2]. c) Atendiendo a la variedad de radicales cite cuatro tipos de dichas
REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ]
![REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ] REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ]](/thumbs/40/20899659.jpg) REGULACIÓN DEL ph Teoría Acido-Base - Anfolitos Que es el ph??? Por lo común lo vemos representado como ph = - log [H ] Estrictamente, ph = - log a H En soluciones diluídas expresarlo en concentración
REGULACIÓN DEL ph Teoría Acido-Base - Anfolitos Que es el ph??? Por lo común lo vemos representado como ph = - log [H ] Estrictamente, ph = - log a H En soluciones diluídas expresarlo en concentración
AMINOACIDOS. Aminoácidos: Moléculas orgánicas sencillas, que representan la unidad estructural de las proteínas. 12/04/2012
 AMINOACIDOS Aminoácidos: Moléculas orgánicas sencillas, que representan la unidad estructural de las proteínas. 1 FORMULA GENERAL H átomo carbono α grupo amino NH 2 C COOH grupo carboxilo R cadena lateral
AMINOACIDOS Aminoácidos: Moléculas orgánicas sencillas, que representan la unidad estructural de las proteínas. 1 FORMULA GENERAL H átomo carbono α grupo amino NH 2 C COOH grupo carboxilo R cadena lateral
RESULTADOS Y DISCUSIONES. El análisis por medio de electroforesis a demostrado ser uno de los
 39 RESULTADOS Y DISCUSIONES El análisis por medio de electroforesis a demostrado ser uno de los mejores métodos de separación para complejos proteicos, además de necesitar cantidades muy pequeñas de muestra.
39 RESULTADOS Y DISCUSIONES El análisis por medio de electroforesis a demostrado ser uno de los mejores métodos de separación para complejos proteicos, además de necesitar cantidades muy pequeñas de muestra.
BIOLOGIA CELULAR Y MOLECULAR. LABORATORIO No 8: ELECTROFORESIS EN GELES DE AGAROSA
 BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 8: ELECTROFORESIS EN GELES DE AGAROSA 1. INTRODUCCIÓN Para detectar los productos o fragmentos de ADN obtenidos después de varios de los procedimientos realizados
BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 8: ELECTROFORESIS EN GELES DE AGAROSA 1. INTRODUCCIÓN Para detectar los productos o fragmentos de ADN obtenidos después de varios de los procedimientos realizados
EL EMPLEO DE ANÁLISIS BIOQUÍMICOS Y MOLECULARES EN EL EXAMEN DHE MOLECULARES EN EL EXAMEN DHE
 X Curso de Formación sobre la Protección de las Obtenciones Vegetales para Países Iberoamericanos Montevideo (URUGUAY) 12 al 16 de Diciembre de 2011 EL EMPLEO DE ANÁLISIS BIOQUÍMICOS Y MOLECULARES EN EL
X Curso de Formación sobre la Protección de las Obtenciones Vegetales para Países Iberoamericanos Montevideo (URUGUAY) 12 al 16 de Diciembre de 2011 EL EMPLEO DE ANÁLISIS BIOQUÍMICOS Y MOLECULARES EN EL
GUÍA N 1: Unidades de medida y Leyes Ponderales. 1.- Convierta las siguientes unidades de temperatura en C, F y K según corresponda:
 1 PRIMERA PARTE: Ejercicios de desarrollo. GUÍA N 1: Unidades de medida y Leyes Ponderales. Considerando las siguientes tablas de conversión de unidades del SISTEMA INTERNACIONAL DE UNIDADES (S.I.), desarrolla
1 PRIMERA PARTE: Ejercicios de desarrollo. GUÍA N 1: Unidades de medida y Leyes Ponderales. Considerando las siguientes tablas de conversión de unidades del SISTEMA INTERNACIONAL DE UNIDADES (S.I.), desarrolla
PRUEBA DE ACCESO A LA UNIVERSIDAD PARA MAYORES DE 25 AÑOS PRUEBA ESPECÍFICA QUÍMICA
 PRUEBA DE ACCESO A LA UNIVERSIDAD PARA MAYORES DE 5 AÑOS QUÍMICA 1.- Cómo se nombra este compuesto? Seleccione la respuesta correcta a) -in-propano b) butano c) butino d) 1-in-propano CH C CH CH.- Una
PRUEBA DE ACCESO A LA UNIVERSIDAD PARA MAYORES DE 5 AÑOS QUÍMICA 1.- Cómo se nombra este compuesto? Seleccione la respuesta correcta a) -in-propano b) butano c) butino d) 1-in-propano CH C CH CH.- Una
SEPARACIÓN DE BIOMOLÉCULAS
 CÁTEDRA: BIOQUÍMICA Carreras: Farmacia Profesorado en Química Licenciatura en Química Lic. en C. y T. de los Alimentos SEPARACIÓN DE BIOMOLÉCULAS 1) Suponga que desea purificar por cromatografía de intercambio
CÁTEDRA: BIOQUÍMICA Carreras: Farmacia Profesorado en Química Licenciatura en Química Lic. en C. y T. de los Alimentos SEPARACIÓN DE BIOMOLÉCULAS 1) Suponga que desea purificar por cromatografía de intercambio
BIOLOGIA CELULAR Y MOLECULAR. LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE)
 BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE) 1. INTRODUCCIÓN Uno de los métodos que permite la purificación y separación de proteínas de un organismo
BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE) 1. INTRODUCCIÓN Uno de los métodos que permite la purificación y separación de proteínas de un organismo
La materia. Clasificación de la materia
 27 de marzo de 2005 Contenidos 1 Introducción La materia 2 La materia Qué es la materia? Materia es todo aquello que tiene masa y posee volumen. La materia Qué es la materia? Materia es todo aquello que
27 de marzo de 2005 Contenidos 1 Introducción La materia 2 La materia Qué es la materia? Materia es todo aquello que tiene masa y posee volumen. La materia Qué es la materia? Materia es todo aquello que
PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS. Es un ácido capaz de formar sales con iones cargados
 Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
Tema 5. Propiedades de transporte
 Tema 5 Propiedades de transporte 1 TEMA 5 PROPIEDADES DE TRANSPORTE 1. TEORÍA CINÉTICA DE LOS GASES POSTULADOS DE LA TEORÍA CINÉTICA DE LOS GASES INTERPRETACIÓN CINÉTICO MOLECULAR DE LA PRESIÓN Y LA TEMPERATURA
Tema 5 Propiedades de transporte 1 TEMA 5 PROPIEDADES DE TRANSPORTE 1. TEORÍA CINÉTICA DE LOS GASES POSTULADOS DE LA TEORÍA CINÉTICA DE LOS GASES INTERPRETACIÓN CINÉTICO MOLECULAR DE LA PRESIÓN Y LA TEMPERATURA
3.1. Cuantificación de proteínas totales. 3.2. Técnicas de separación de proteínas. Análisis de proteínas específicas.
 TEMA 3: Métodos para el análisis de proteínas 3.1. Cuantificación de proteínas totales. 3.2. Técnicas de separación de proteínas. Análisis de proteínas específicas. INTRODUCCIÓN A lo largo de este tema
TEMA 3: Métodos para el análisis de proteínas 3.1. Cuantificación de proteínas totales. 3.2. Técnicas de separación de proteínas. Análisis de proteínas específicas. INTRODUCCIÓN A lo largo de este tema
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
ÁCIDO-BASE. ÁCIDO: Sustancia que en disolución acuosa disocia cationes H +. BASE: Sustancia que en disolución acuosa disocia aniones OH.
 ÁCIDO-BASE Ácidos: 1. CARACTERÍSTICAS DE ÁCIDOS Y BASES. Tienen sabor agrio, son corrosivos para la piel, enrojecen ciertos colorantes, vegetales. Disuelven sustancias, atacan a los metales desprendiendo
ÁCIDO-BASE Ácidos: 1. CARACTERÍSTICAS DE ÁCIDOS Y BASES. Tienen sabor agrio, son corrosivos para la piel, enrojecen ciertos colorantes, vegetales. Disuelven sustancias, atacan a los metales desprendiendo
PROPIEDADES FISICAS Y QUIMICAS DE LOS ALIMENTOS II SEMINARIOS PROPIEDADES FUNCIONALES: GELIFICACIÓN FORMACIÓN DE FILMS
 Propiedades Físicas y Químicas de los Alimentos II Página 1 de 6 PROPIEDADES FISICAS Y QUIMICAS DE LOS ALIMENTOS II SEMINARIOS PROPIEDADES FUNCIONALES: GELIFICACIÓN FORMACIÓN DE FILMS 1. Describa qué entiende
Propiedades Físicas y Químicas de los Alimentos II Página 1 de 6 PROPIEDADES FISICAS Y QUIMICAS DE LOS ALIMENTOS II SEMINARIOS PROPIEDADES FUNCIONALES: GELIFICACIÓN FORMACIÓN DE FILMS 1. Describa qué entiende
GLOSARIO Ácidos grasos Ácidos grasos esenciales Agua Aminoácidos Aminoácidos proteicos Azúcares simples
 GLOSARIO Ácidos grasos: Son la base estructural de las grasas. Existen dos tipos: Saturados: Son los sólidos a temperatura ambiente, como la carne animal. Insaturados: Son líquidos a temperatura ambiente,
GLOSARIO Ácidos grasos: Son la base estructural de las grasas. Existen dos tipos: Saturados: Son los sólidos a temperatura ambiente, como la carne animal. Insaturados: Son líquidos a temperatura ambiente,
Técnicas de Estudio de las células
 Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
CLASIFICACIÓN SEGÚN SU POLARIDAD NO POLARES POLARES NEUTROS ACIDOS BASICOS
 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
PRÁCTICA 4: ANÁLISIS DE PROTEÍNAS
 PRÁCTICA 4: ANÁLISIS DE PROTEÍNAS 1. DETERMINACIÓN DE LA PROTEÍNA BRUTA POR EL MÉTODO DE KJELDAHL. 1.1. FUNDAMENTO: En los análisis de rutina se suele determinar el contenido de nitrógeno total y expresar
PRÁCTICA 4: ANÁLISIS DE PROTEÍNAS 1. DETERMINACIÓN DE LA PROTEÍNA BRUTA POR EL MÉTODO DE KJELDAHL. 1.1. FUNDAMENTO: En los análisis de rutina se suele determinar el contenido de nitrógeno total y expresar
MATERIALES Y MÉTODOS. Tipo de Estudio. Muestra
 MATERIALES Y MÉTODOS Tipo de Estudio Experimental. Este tipo de estudio tiene como característica primordial el poder manipular y controlar las variables, siendo en este caso la fuerza iónica y el ph.
MATERIALES Y MÉTODOS Tipo de Estudio Experimental. Este tipo de estudio tiene como característica primordial el poder manipular y controlar las variables, siendo en este caso la fuerza iónica y el ph.
EQUILIBRIO ÁCIDO-BASE.
 EQUILIBRIO ÁCIDOBASE. 1. PROPIEDADES DE ÁCIDOS Y BASES. 2. TEORÍA DE ARRHENIUS. 3. TEORÍA DE BRONSTED Y LOWRY. 4. TEORÍA DE LEWIS. 5. FUERZAS DE ÁCIDOS Y BASES. CONSTANTES DE DISOCIACIÓN. 6. EQUILIBRIO
EQUILIBRIO ÁCIDOBASE. 1. PROPIEDADES DE ÁCIDOS Y BASES. 2. TEORÍA DE ARRHENIUS. 3. TEORÍA DE BRONSTED Y LOWRY. 4. TEORÍA DE LEWIS. 5. FUERZAS DE ÁCIDOS Y BASES. CONSTANTES DE DISOCIACIÓN. 6. EQUILIBRIO
Trabajo Práctico de Laboratorio 5
 Trabajo Práctico de Laboratorio 5 Tema: Aminoácidos y proteínas Fundamentación teórica AMIÁCIDS Propiedades químicas Los aminoácidos poseen en su estructura un grupo ácido y un grupo básico, por lo cual
Trabajo Práctico de Laboratorio 5 Tema: Aminoácidos y proteínas Fundamentación teórica AMIÁCIDS Propiedades químicas Los aminoácidos poseen en su estructura un grupo ácido y un grupo básico, por lo cual
UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS
 UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS Lee atentamente: 1. LA MISMA SUSTANCIA EN LOS TRES ESTADOS Todos los cuerpos están formados por sustancias: las personas, los coches, los muebles, el aire, etc. Todas
UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS Lee atentamente: 1. LA MISMA SUSTANCIA EN LOS TRES ESTADOS Todos los cuerpos están formados por sustancias: las personas, los coches, los muebles, el aire, etc. Todas
PURIFICACION PARCIAL DE LA CASEINA PRESENTE EN
 EXPERIMENTO 9 PURIFICACION PARCIAL DE LA CASEINA PRESENTE EN LA LECHE Y DETERMINACION DE SU PESO MOLECULAR Y DEL PRODUCTO DE LA HIDROLISIS POR LA ENZIMA BROMELINA DE LA PIÑA MEDIANTE ELECTROFORESIS REQUISITOS
EXPERIMENTO 9 PURIFICACION PARCIAL DE LA CASEINA PRESENTE EN LA LECHE Y DETERMINACION DE SU PESO MOLECULAR Y DEL PRODUCTO DE LA HIDROLISIS POR LA ENZIMA BROMELINA DE LA PIÑA MEDIANTE ELECTROFORESIS REQUISITOS
Cátedra de Introducción a la Química para Ciencias Naturales - UNLP. ph I - EQUILIBRIO ÁCIDO-BASE
 ph I - EQUILIBRIO ÁCIDO-BASE En este y en el siguiente grupo de Trabajos Prácticos se estudiarán equilibrios que ocurren en solución acuosa. Debe tenerse en cuenta que, a pesar de tener diferentes denominaciones,
ph I - EQUILIBRIO ÁCIDO-BASE En este y en el siguiente grupo de Trabajos Prácticos se estudiarán equilibrios que ocurren en solución acuosa. Debe tenerse en cuenta que, a pesar de tener diferentes denominaciones,
UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A
 UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A CUESTIÓN.- Cuál de las siguientes reacciones nunca será espontánea independientemente del valor de la temperatura?, cuál será
UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A CUESTIÓN.- Cuál de las siguientes reacciones nunca será espontánea independientemente del valor de la temperatura?, cuál será
Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon.
 Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
Electroforesis en gel de poliacrilamida y electrotransferencia
 Electroforesis en gel de poliacrilamida y electrotransferencia INDICE ELECTROFORESIS Fundamento y características Tipos de electroforesis: libre y de zona Electroforesis en papel, acetato de celulosa Electroforesis
Electroforesis en gel de poliacrilamida y electrotransferencia INDICE ELECTROFORESIS Fundamento y características Tipos de electroforesis: libre y de zona Electroforesis en papel, acetato de celulosa Electroforesis
Tema 6 Cuantificación de proteínas
 Tema 6 Cuantificación de proteínas Procedimiento de estudio de proteínas Selección de fuente Fraccionamiento de células Centrifugación Cromatografía Cromatografía en capa fina Cromatografía en columna
Tema 6 Cuantificación de proteínas Procedimiento de estudio de proteínas Selección de fuente Fraccionamiento de células Centrifugación Cromatografía Cromatografía en capa fina Cromatografía en columna
(VI) Metabolismo de los ácidos biliares y la bilirrubina
 Bioquímica hepática (VI) Metabolismo de los ácidos biliares y la bilirrubina Prof. J.V. Castell Metabolismo de los ácidos biliares 1. Bilis: composición y funciones 2. Degradación oxidativa del colesterol.
Bioquímica hepática (VI) Metabolismo de los ácidos biliares y la bilirrubina Prof. J.V. Castell Metabolismo de los ácidos biliares 1. Bilis: composición y funciones 2. Degradación oxidativa del colesterol.
CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara
 CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara OBJETIVOS 1.- Estudiar la cinética de la reacción de hidrólisis ácida del acetato de metilo en disolución
CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara OBJETIVOS 1.- Estudiar la cinética de la reacción de hidrólisis ácida del acetato de metilo en disolución
FÍSICA Y QUÍMICA 3ºESO
 TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3ºESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. Por ejemplo siempre tienen
TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3ºESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. Por ejemplo siempre tienen
TEMA 3. CLASIFICACIÓN DE LA MATERIA.
 TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3º ESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. - Elemento. Es una sustancia
TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3º ESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. - Elemento. Es una sustancia
Purificación de proteínas
 Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
Solución: Serie problemas para entregar ÁCIDO-BASE
 Solución: Serie problemas para entregar ÁCIDO-BASE 1.- El ácido metanoico, HCOOH, es un ácido débil porque en disolución acuosa no está totalmente disociado. Al disolver 4,6 g de ácido metanoico en 1 litro
Solución: Serie problemas para entregar ÁCIDO-BASE 1.- El ácido metanoico, HCOOH, es un ácido débil porque en disolución acuosa no está totalmente disociado. Al disolver 4,6 g de ácido metanoico en 1 litro
TECNOLOGIA DE LOS ALIMENTOS
 ~ TECNOLOGIA DE LOS ALIMENTOS VOLUMEN 1 COMPONENTES DE LOS ALIMENTOS Y PROCESOS Juan A. Ordóñez Pereda (editor) María Isabel Cambero Rodríguez Leónides Fernández Álvarez María Luisa García Sanz Gonzalo
~ TECNOLOGIA DE LOS ALIMENTOS VOLUMEN 1 COMPONENTES DE LOS ALIMENTOS Y PROCESOS Juan A. Ordóñez Pereda (editor) María Isabel Cambero Rodríguez Leónides Fernández Álvarez María Luisa García Sanz Gonzalo
Descripción de los 3 estados de la materia. Química General II Estados líquido y sólido. Diagrama de Fases
 Descripción de los 3 estados de la materia Química General II Estados líquido y sólido. Diagrama de Fases Estado Líquido El estado líquido se caracteriza por: Retener su volumen pero no su forma. No poder
Descripción de los 3 estados de la materia Química General II Estados líquido y sólido. Diagrama de Fases Estado Líquido El estado líquido se caracteriza por: Retener su volumen pero no su forma. No poder
1.2 LA MATERIA Y LOS CAMBIOS
 1.2 LA MATERIA Y LOS CAMBIOS Por equipo definir que es átomo, molécula y de que están formados Equipo Átomo Molécula 1 2 3 4 5 6 7 8 ÁTOMO 1. Un átomo es eléctricamente neutro. tiene el mismo número
1.2 LA MATERIA Y LOS CAMBIOS Por equipo definir que es átomo, molécula y de que están formados Equipo Átomo Molécula 1 2 3 4 5 6 7 8 ÁTOMO 1. Un átomo es eléctricamente neutro. tiene el mismo número
DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS
 DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS Se le llama fluido a toda aquella sustancia continua que puede fluir. Los fluidos pueden ser gaseosos y líquidos. Esta es la diferencia fundamental entre un sólido, cuya
DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS Se le llama fluido a toda aquella sustancia continua que puede fluir. Los fluidos pueden ser gaseosos y líquidos. Esta es la diferencia fundamental entre un sólido, cuya
DOGMA CENTRAL DE LA BIOLOGÍA MOLECULAR (Francis Crick 1970) (Excepción de la transcriptasa inversa) ADN Transcripción ARN traducción PROTEINAS
 DOGMA CENTRAL DE LA BIOLOGÍA MOLECULAR (Francis Crick 1970) (Excepción de la transcriptasa inversa) ADN Transcripción ARN traducción PROTEINAS TRANSCRIPCIÓN DEL CÓDIGO: BIOSÍNTESIS DE ARN Se sintetiza
DOGMA CENTRAL DE LA BIOLOGÍA MOLECULAR (Francis Crick 1970) (Excepción de la transcriptasa inversa) ADN Transcripción ARN traducción PROTEINAS TRANSCRIPCIÓN DEL CÓDIGO: BIOSÍNTESIS DE ARN Se sintetiza
Determinación de proteínas
 Determinación de proteínas Curso EMA 2013 Ing. Agr. Marta del Puerto Métodos para determinar proteínas Se basan en: a. Propiedad de las proteínas de absorber luz en el UV absorción A=280nm a. Capacidad
Determinación de proteínas Curso EMA 2013 Ing. Agr. Marta del Puerto Métodos para determinar proteínas Se basan en: a. Propiedad de las proteínas de absorber luz en el UV absorción A=280nm a. Capacidad
Buscando la textura adecuada: Carrageninas
 Buscando la textura adecuada: Carrageninas La textura en los alimentos es algo tan importante como el sabor, convirtiéndose de hecho en un factor determinante en la aceptación de un producto por parte
Buscando la textura adecuada: Carrageninas La textura en los alimentos es algo tan importante como el sabor, convirtiéndose de hecho en un factor determinante en la aceptación de un producto por parte
9. MEDIDA DE LA DENSIDAD DE LÍQUIDOS
 9. MEDIDA DE LA DENSIDAD DE LÍQUIDOS OBJETIVO El objetivo de la practica es determinar la densidad de líquidos utilizando la balanza de Möhr y su aplicación a la determinación de la densidad de disoluciones
9. MEDIDA DE LA DENSIDAD DE LÍQUIDOS OBJETIVO El objetivo de la practica es determinar la densidad de líquidos utilizando la balanza de Möhr y su aplicación a la determinación de la densidad de disoluciones
Separación de biomoléculas
 Separación de biomoléculas Cromatografía. Aspectos generales, técnicas involucradas. FPLC, HPLC. Electroforesis. Conceptos generales y aplicaciones. Geles de poliacrilamida y agarosa. Isoelectroenfoque.
Separación de biomoléculas Cromatografía. Aspectos generales, técnicas involucradas. FPLC, HPLC. Electroforesis. Conceptos generales y aplicaciones. Geles de poliacrilamida y agarosa. Isoelectroenfoque.
PROPIEDADES DE LOS FLUIDOS
 PROPIEDADES DE LOS FLUIDOS CRUDO Objetivo: Determinar las propiedades importantes del Crudo, tales como la Densidad, Gravedad API, Viscosidad Cinemática y Viscosidad Dinámica; utilizando diferentes métodos.
PROPIEDADES DE LOS FLUIDOS CRUDO Objetivo: Determinar las propiedades importantes del Crudo, tales como la Densidad, Gravedad API, Viscosidad Cinemática y Viscosidad Dinámica; utilizando diferentes métodos.
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo
 Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
EL MANTENIMIENTO DE LA VIDA TEMA 1
 EL MANTENIMIENTO DE LA VIDA TEMA 1 INDICE 1. Seres vivos y funciones vitales 2. La composición química de los seres vivos 3. Las células 3.1 Conocimiento histórico de la célula 3.2 Cómo son las células?
EL MANTENIMIENTO DE LA VIDA TEMA 1 INDICE 1. Seres vivos y funciones vitales 2. La composición química de los seres vivos 3. Las células 3.1 Conocimiento histórico de la célula 3.2 Cómo son las células?
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM. ACIDOS Y BASES, ph, BUFFERS
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H +
 Reacciones ácido-base 1 Brønsted-Lowry (1923) Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H + CH 3 COOH (aq) + H 2 O (l) H 3 O + (aq) + CH 3 COO (aq)
Reacciones ácido-base 1 Brønsted-Lowry (1923) Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H + CH 3 COOH (aq) + H 2 O (l) H 3 O + (aq) + CH 3 COO (aq)
Transferencia de material genético II. 1) Aislamiento de plásmidos Lisis alcalina
 Transferencia de material genético II 1) Aislamiento de plásmidos Lisis alcalina ESQUEMA GENERAL SESIÓN I: TRANSFORMAR cepas de E. coli con un plásmido. Verificar que hay células transformantes de acuerdo
Transferencia de material genético II 1) Aislamiento de plásmidos Lisis alcalina ESQUEMA GENERAL SESIÓN I: TRANSFORMAR cepas de E. coli con un plásmido. Verificar que hay células transformantes de acuerdo
LOS NUTRIENTES MOLÉCULAS QUÍMICAS SENCILLAS QUE EL ORGANISMO EXTRAE DE LOS ALIMENTOS Y QUE UTILIZA PARA LLEVAR A CABO SUS FUNCIONES METABÓLICAS
 LOS NUTRIENTES MOLÉCULAS QUÍMICAS SENCILLAS QUE EL ORGANISMO EXTRAE DE LOS ALIMENTOS Y QUE UTILIZA PARA LLEVAR A CABO SUS FUNCIONES METABÓLICAS GLÚCIDOS TAMBIEN DENOMINADOS AZÚCARES E HIDRATOS DE CARBONO
LOS NUTRIENTES MOLÉCULAS QUÍMICAS SENCILLAS QUE EL ORGANISMO EXTRAE DE LOS ALIMENTOS Y QUE UTILIZA PARA LLEVAR A CABO SUS FUNCIONES METABÓLICAS GLÚCIDOS TAMBIEN DENOMINADOS AZÚCARES E HIDRATOS DE CARBONO
EJERCICIOS DEL CAPÍTULO 9 - ELECTROMAGNETISMO
 EJERCICIOS DEL CAPÍTULO 9 - ELECTROMAGNETISMO C9. 1 Aceleramos iones de los isótopos C-12, C-13 y C-14 con una d.d.p. de 100 kv y los hacemos llegar a un espectrógrafo de masas perpendicularmente a la
EJERCICIOS DEL CAPÍTULO 9 - ELECTROMAGNETISMO C9. 1 Aceleramos iones de los isótopos C-12, C-13 y C-14 con una d.d.p. de 100 kv y los hacemos llegar a un espectrógrafo de masas perpendicularmente a la
ELECTROFORESIS Fundamento.
 ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
----------SOLUCIÓN ---------- 1. (b) 8. (a) 2. (a) 29. (b) 30. (c) 22. (d) 23. (b) 24. (a) 25. (b) 26. (d) 27. (c) 28. (a)
 29. Si la presión externa del ambiente que rodea a un líquido aumenta, qué le pasa a la temperatura a la que hierve? a) disminuye b) aumenta c) no cambia d) no se puede saber 30. Las gotas de agua que
29. Si la presión externa del ambiente que rodea a un líquido aumenta, qué le pasa a la temperatura a la que hierve? a) disminuye b) aumenta c) no cambia d) no se puede saber 30. Las gotas de agua que
5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
LIQUIDOS. Propiedades:
 LIQUIDOS Los líquidos se caracterizan por su volumen fijo y forma variable. Las fuerzas intermoleculares son mayores que en los gases, pero al igual que en estos, sus partículas están en movimiento constante.
LIQUIDOS Los líquidos se caracterizan por su volumen fijo y forma variable. Las fuerzas intermoleculares son mayores que en los gases, pero al igual que en estos, sus partículas están en movimiento constante.
Capítulo I. En el caso de este estudio, encontramos como factor determinante a los
 Capítulo I 1.1 Planteamiento del problema En el caso de este estudio, encontramos como factor determinante a los estudiantes que se encuentran en el proceso de su desarrollo académico para realizar la
Capítulo I 1.1 Planteamiento del problema En el caso de este estudio, encontramos como factor determinante a los estudiantes que se encuentran en el proceso de su desarrollo académico para realizar la
Tema 7.- Genética Molecular. Biología y Geología 4º ESO: Genética Molecular
 Tema 7.- Genética Molecular 1 El ADN, la molécula de la herencia El ADN (ácido desoxirribonucléico), es el portador de la información genética y es el responsable de las características biológicas de un
Tema 7.- Genética Molecular 1 El ADN, la molécula de la herencia El ADN (ácido desoxirribonucléico), es el portador de la información genética y es el responsable de las características biológicas de un
Todo lo que puedas imaginar está compuesto por átomos.
 Todo lo que puedas imaginar está compuesto por átomos. El átomo es la partícula más pequeña de un elemento químico (materia formada por átomos iguales) y posee las características del mismo. Cuando se
Todo lo que puedas imaginar está compuesto por átomos. El átomo es la partícula más pequeña de un elemento químico (materia formada por átomos iguales) y posee las características del mismo. Cuando se
NUTRICIÓN Y ALIMENTACIÓN
 NUTRICIÓN Y ALIMENTACIÓN Los nutrientes son los diferentes compuestos químicos que contienen los alimentos y coinciden básicamente con nuestros componentes corporales INORGÁNICOS Y ORGÁNICOS COMPONENTES
NUTRICIÓN Y ALIMENTACIÓN Los nutrientes son los diferentes compuestos químicos que contienen los alimentos y coinciden básicamente con nuestros componentes corporales INORGÁNICOS Y ORGÁNICOS COMPONENTES
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL
 CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD A. CROMATOGRAFÍA DE INTERCAMBIO IÓNICO. Usos 1.- Purificar Proteínas 2.- Concentrar Proteínas Ventajas
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD A. CROMATOGRAFÍA DE INTERCAMBIO IÓNICO. Usos 1.- Purificar Proteínas 2.- Concentrar Proteínas Ventajas
Atraviesan completamente la membrana. Insertadas en la membrana, pero no la atraviesan del todo
 Estructura de membranas II. Proteínas de membrana Javier Corzo Periféricas Se pueden separar sin alterar la estructura de la membrana Dominio transmembrana formado por hélices alfa Atraviesan completamente
Estructura de membranas II. Proteínas de membrana Javier Corzo Periféricas Se pueden separar sin alterar la estructura de la membrana Dominio transmembrana formado por hélices alfa Atraviesan completamente
APUNTES DE FÍSICA Y QUÍMICA 4º DE ESO UNIDAD DIDÁCTICA 3 REACCIONES QUÍMICAS 1.- REACCIONES ÁCIDO- BASE
 APUNTES DE FÍSICA Y QUÍMICA 4º DE ESO UNIDAD DIDÁCTICA 3 REACCIONES QUÍMICAS 1.- REACCIONES ÁCIDO- BASE La reacción entre un ácido y una base se llama neutralización. Durante este proceso se forma una
APUNTES DE FÍSICA Y QUÍMICA 4º DE ESO UNIDAD DIDÁCTICA 3 REACCIONES QUÍMICAS 1.- REACCIONES ÁCIDO- BASE La reacción entre un ácido y una base se llama neutralización. Durante este proceso se forma una
