Estabilidad de Alquenos Sistemas conjugados. Resonancia. Aromaticidad.
|
|
|
- Raúl Calderón Lara
- hace 7 años
- Vistas:
Transcripción
1 Estabilidad de Alquenos Sistemas conjugados. Resonancia. Aromaticidad. Preparado por Licda. Nora Guzmán Basado en: Dr. Carlos A. Rius, Depto.Química Orgánica, Facultad de Química,UNAM. Lic. Mario M. Rodas, Depto. Química Orgánica, Depto. Q. Orgánica, Escuela de Química, Facultad de CC. QQ. y Farmacia, USAC. John McMurry, Química Orgánica, 7ª. Ed, Cap.6, 14, 15. Química Orgánica I- Sección D 2014 USAC Facultad de CC.QQ. y Farmacia
2 Hidrogenación de los alquenos. Cuando se trata un alqueno con hidrógeno en presencia de platino como catalizador, el hidrógeno se adiciona al doble enlace, convirtiendo el alqueno en un alcano. La hidrogenación es ligeramente exotérmica, desprendiendo entre 20 y 30 kcal (80 a 120 kj) por mol de hidrógeno consumido. Considérese la hidrogenación del 1-buteno y del trans-2-buteno. La adición de hidrógeno a través del enlace doble se considera una reacción de reducción porque el número de enlaces C-H aumenta. Cuanto más sustituido sea el enlace doble, más estable será el compuesto y más bajo será el calor de hidrogenación.
3 Energías relativas de los alquenos. Energías relativas de los enlaces π comparadas con el etileno (los números son aproximados).
4 Energías relativas de los alquenos. Cuanto más sustituido está el doble enlace, menor es el calor de hidrogenación y tiene mayor estabilidad. Entre isómeros geométricos, el isómero trans es más estable que el cis. El trans-2-buteno es más estable que el 1-buteno en 2.7 kcal/mol (11 kj/mol). Los enlaces dobles más sustituidos liberan menos calor cuando son hidrogenados, por lo que se considera que son más estables.
5 Estabilidad de los alquenos. El isómero con el doble enlace más sustituido tiene mayor separación angular entre los grupos alquilo voluminosos Cuanto mayor sea la separación entre los grupos, se producirá menos interacción estérica y mayor estabilidad.
6 Diagrama de energía de reacción para la hidrogenación de los alquenos.
7 Alquenos cíclicos Otra diferencia entre los alquenos cíclicos y acíclicos es la relación entre los isómeros cis y trans. En los alquenos acíclicos, los isómeros trans generalmente son más estables, pero los isómeros trans de los cicloalquenos pequeños son raros y los que tienen anillos de menos de ocho átomos de carbono son inestables a temperatura ambiente Los cicloalquenos que tienen menos de ocho átomos de carbono son cis. El trans-cicloocteno se puede aislar y es estable a temperatura ambiente, pero su isómero cis es aún más estable.
8 Sistemas conjugados Los dobles enlaces pueden interaccionar entre ellos si están separados por un enlace sencillo. A estos dobles enlaces se les llama conjugados. Los dobles enlaces que están separados por dos o más enlaces sencillos interaccionan muy poco entre ellos y se les llama dobles enlaces aislados. Los dobles enlaces conjugados son más estables que los aislados. Experimentan las mismas reacciones que los alquenos.
9 Calor de hidrogenación de los enlaces conjugados. En los dienos conjugados, el calor de hidrogenación es menor que la suma del de los doble enlaces individuales Cuanto menos calor se libera durante la hidrogenación, se considera que el compuesto es más estable. Los dobles enlaces conjugados tienen una estabilidad extra.
10 Energías relativas de dienos conjugados, aislados y acumulados comparadas con los alquinos. Energías relativas de dienos conjugados, aislados y acumulados comparadas con los alquinos, basadas en los calores de hidrogenación (kcal/mol). Un dieno acumulado tiene una energía comparable con la de los alquinos. Los dienos conjugados tienen energías más bajas que los dobles enlaces aislados
11 Estructura del 1,3-butadieno. Estructura del 1,3-butadieno en su conformación más estable. El enlace sencillo central carbono-carbono de 1.48 Å es más corto que el de 1.54 Å (longitud de un enlace sencillo de un alcano) debido a su carácter parcial de doble enlace. Hay una pequeña cantidad de solapamiento a través del enlace central C-C que le da un carácter parcial de doble enlace.
12 OM del 1,3-butadieno y del etileno. En el 1,3-butadieno y en el etileno, los OM enlazantes están llenos y los OM antienlazantes están vacíos. La energía media de los electrones es ligeramente más baja en el butadieno. Esta disminución de energía es la energía de estabilización por resonancia del dieno conjugado Debido a que los dobles enlaces de 1,3-butadieno están conjugados, la energía del OM es menor en el 1,3- butadieno que en el etileno.
13 Transición π - π* del etileno. La absorción de un fotón de 171 nm excita a un electrón desde el OM enlazante π del etileno al OM antienlazante π*. La absorción no se puede detectar en el espectrómetro UV porque requiere luz de una energía superior a la de UV.
14 La transición π - π* del 1,3-butadieno En el 1,3-butadieno, la transición π - π* absorbe a 217 nm (129 kcal/mol), comparado con los 171 nm (164 kcal/ mol) en el etileno. Esta absorción a mayor longitud de onda (menor energía) se debe a que entre el HOMO y el LUMO del butadieno hay menor energía que entre el HOMO y el LUMO del etileno. Cuanto más conjugado esté el sistema, más larga será la longitud de onda (menor energía) de la transición electrónica
15 Absorción ultravioleta máxima de algunas moléculas representativas. Adviértase que la adición de enlaces dobles conjugados aumenta λ. Cuanto más conjugado esté el sistema, más larga será la longitud de onda (menor energía) de la transición electrónica
16 Localización Deslocalización de Electrones Veamos donde hay electrones n o π en las siguientes estructuras:
17 Localización Deslocalización de Electrones En el grupo nitro: Dónde están los electrones n o π, en cuál átomo? Podremos localizarlos exactamente?
18 Localización Deslocalización de Electrones Existen electrones que no podemos localizar fácilmente, es decir no están entre 2 átomos formando un enlace, sino pueden estar en 3 o más átomos deslocalizados
19 Localización Deslocalización de Electrones La siguiente gráfica ilustra muy bien esta deslocalización: 1,4-hexadieno (aislado) 1,3-hexadieno (conjugado)
20 Deslocalización de Electrones Movimiento electrónico Los Dobles Enlaces conjugados, pueden deslocalizar sus electrones en los orbitales p disponibles, es decir los electrones se mueven en todo el sistema
21 Resonancia y Deslocalización Entonces, si los electrones se encuentran deslocalizados, entonces se pueden representar localizados en otra parte de la molécula.
22 Hibrido de Resonancia y Estructuras Resonantes A estas formas diferentes de representar a los electrones, se llaman estructuras de resonancia, ya que no son compuestos diferentes, sino representaciones del mismo compuesto resonancia El híbrido de resonancia, es la representación REAL de sus estructuras de resonancia
23 Movimiento Electrónico: Deslocalización Hibrido de Resonancia
24 Reglas de Resonancia Regla 1: Todas las Estructuras deben ser estructuras de Lewis válidas para el compuesto O O O H 3 C C O H 3 C C O O Carbono de 10 electrones NO NO NO!!! De esta regla nace que el movimiento de electrones nunca puede ir hacia un carbono sp 3
25 Reglas de Resonancia Regla 2: Sólo se puede cambiar los electrones de una posición a otra, nunca los nucleos y los enlaces deben permanecer inalterados. H H C H O C CH 3 H C H OH C CH 3 O O H C H C CH 3 OK H C H C CH 3
26 Reglas de Resonancia Regla 3: La estabilización por resonancia sirve más cuando se deslocaliza una carga en un átomo
27 Reglas de Resonancia Estructuras más estables colaboran en mayor grado al híbrido de resonancia; el híbrido se les asemeja más. Mayor estabilidad de las Estructuras de Resonancia y del Híbrido: ü menor separación de cargas opuestas entre átomos. ü con uno o más átomos con cargas formales: la que refleja el comportamiento electronegativo de los átomos. ü similar o equivalente estabilidad de las estructuras de resonancia que contribuyen al híbrido. ü mayor cantidad de estructuras resonantes CH 3 O N O CH 3 O N O + estable _ : :.... N C O : : N C O + estable CH 3 N O O equivalentes CH 3 N O O
28 Reglas de Resonancia Todas las estructura de resonancia contribuyentes deben tener el mismo número de electrones y la misma carga neta, aunque la carga formal neta sobre un átomo puede variar entre distintas estructuras. Todas las estructura de resonancia contribuyentes deben deben tener el mismo número de e - desapareados. CH 3 (a) N O: : O :.. y CH 3 (b) N : O.. : : O.. : : (24 e -, carga neta = 0) (26 e -, carga neta = -2).. O: CH 3 N (a) : O :.. CH 3 N : (e - apareados) (2e - desapareados) + estable y (c). : O.. O.. :.
29 Catión alilo. Cuando se calienta el bromuro de alilo en presencia de un buen disolvente ionizante, se ioniza formando el catión alilo, grupo alilo con una carga positiva. A los análogos más sustituidos se les denomina cationes alílicos. La carga positiva se deslocaliza entre los dos átomos de carbono mediante la resonancia, dando como resultado mayor estabilidad al catión alilo que la de los cationes no conjugados.
30 Orbitales moleculares del sistema alílico Los tres orbitales p del sistema alílico son paralelos entre sí, permitiendo el solapamiento extendido entre C1-C2 y C2-C3. Debido a su estabilización por resonancia, el catión alilo y los cationes alílicos sustituidos son casi tan estables como los carbocationes terciarios sencillos, tales como el catión terc-butilo.
31 Bromación alílica radicálica. Al igual que los cationes alílicos, los radicales alílicos están estabilizados mediante deslocalización por resonancia.
32 Estructura y Estabilidad del Benceno Benceno es insaturado es menos reactivo que los alquenos típicos y no da las reaccions usuales de los alquenos Ciclohexenoe reacciona rápidamente con Br 2 dando el producto de addición 1,2-dibromociclohexano Benceno reacciona lentamente con Br 2 y da el producto de sustitución C 6 H 5 Br
33 Estructura y Estabilidad del Benceno Una idea cuantitativa de la estabilidad del benceno se obitene de los calores de hidrogenación Benceno es 150 kj/mol (36 kcal/mol) mas estable de lo que se esperaría para el ciclohexatrieno
34 Estructura y Estabilidad del Benceno Longitud de enlace Carbono-Carbono y ángulos en el benceno Todos los enlaces carbono-carbono son de 139 pm de longitud Intermedios entre enlace simple C-C (154 pm) y los típicos dobles enlaces (134 pm) Benceno es plano Todos los ángulos de enlaces C-C-C son de 120 Los 6 átomos de carbono son híbridos sp 2 con el orbital p perpendicular al plano del anillo
35 Estructura y Estabilidad del Benceno Los 6 átomos de carbono y los 6 orbitales p en el benceno son equivlentes. Cada orbital p traslapa igualmente bien con ambos orbitales p vecinos, dando lugar a la representación del benceno en la cual los 6 electrones π están completamente deslocalizados alrededor del anillo. Benceno es un híbrido de dos formas equivalentes, ninguna de las cuales por si sola es verdadera La verdadera estructura es intermedia a las dos formas resonantes.
36 Estructura y Estabilidad del Benceno Diagrama de Orbitales Moleculares π del benceno y de Niveles de Energía del sistema cíclico conjugado
37 Estructura y Estabilidad del Benceno Diagrama de Orbitales Moleculares π del Benceno: de la combinación cíclica de 6 orbitales atómicos p, resultan los 6 orbitales moleculares π del benceno Los 3 orbitales moleculares de menor energía, denotados por ψ 1, ψ 2, y ψ 3, son combinaciones enlazantes ψ 2 y ψ 3 tienen la misma energía, por lo que se consideran estar degenerados Los 3 orbitales moleculares de mayor energía, denotados por ψ 4, ψ 5 y ψ 6, son combinaciones de antienlace ψ 4 y ψ 5 tienen la misma energía por lo que se consideran estar degenerados ψ 3 y ψ 4 tienen nodos que pasan por los carbonos anulares, por lo que no existe densidad electrónica sobre estos carbonos Los 6 electrones p ocupan los 3 orbitales moleculares enlazantes y están deslocalizados en todo el sistema conjugado Diagrama de Niveles de Energía de los 6 orbitales moleculares π del benceno: Existe un sólo OM de baja energía, ψ 1, conteniendo un par de electrones ψ 2 y ψ 3, son un par de orbitles degenerados, llenándose con dos pares de electrones. El resultado es una molécula aromática estable con 6 electrones π con orbitales de enlace llenos (diagrama de capa π llena )
38 Aromaticidad y la Regla de Hückel 4n + 2 Características comunes del Benceno y otra moléculas aromáticas similares: Estructura cíclica, conjugada y plana: todos los átomos que conforman el anillo son híbridos sp 2, presentando la misma longitud de enlace entre ellos y ángulos de enlace de 120 o Estabilidad inusual: altos valores de energía de resonancia, descolalización o conjugación (benceno es 150 kj/mol (36 kcal/mol) más estable que el ciclohexa-1,3,5-trieno) Son Híbridos de Resonancia Sufren reacciones de sustitución, lo que mantiene la conjugación cíclica y no de adición electrofílica que destruiría la conjugación como ocurre a los alquenos.
39 Aromaticidad y la Regla de Hückel 4n + 2 La regla de Hückel: # e - π = 4n + 2 Teoría planteada en 1931 por el físico alemán Erich Hückel Una molécula es aromática sólo si tiene un sistema monocíclico conjugado plano y contiene un total de electrones π igual a 4n + 2, donde n es un número entero (n = 0, 1, 2, 3, ) Una molécula es aromática solo si presenta un sistema monocíclico plano y conjugado que contiene un total de 2, 6, 10, 14, 18, electrones π Moléculas con 4n electrones π (4, 8, 12, 16, ) no puede ser aromática, por lo que se dicen ser antiaromáticas ya que la deslocalización de sus electrones π la lleva a su desestablización. O bien, en 4n + 2, n es un número fraccionario. Las moléculas que fallan en alguno de los requisitos (sistema cíclico plano y conjugado) se consideran no aromáticas
40 Aromaticidad y la Regla de Hückel 4n + 2 Ejemplos: Ciclobutadieno Contiene 4 electrones π Están localizados en dos dobles enlaces y no deslocalizados alrededor del anillo Antiaromático Altamente reactivo, inestable, se logrópreparar hasta 1965
41 Aromaticidad y la Regla de Hückel 4n + 2 Benceno Contiene 6 electrones π (4n + 2 = 6, donde n = 1) Aromático
42 Aromaticidad y la Regla de Hückel 4n + 2 Ciclooctatetraeno Contiene 8 electrones π Los electrones π estan localizados en 4 dobles enlaces y no deslocalizados alrededor del anillo No aromático La molécula no es plana, tiene forma de tubo No tiene conjugación cíclica pues los orbitales p vecinos no tienen la alineación paralela para traslapar Reacciona como polieno de cadena abierta
43 Aromaticidad y la Regla de Hückel 4n + 2 Diagrama de Niveles de Energía de Moléculas Cíclicas Conjugadas (4n + 2 e - π) Diagrama de Polígono de Hückel Siempre existe un solo OM de menor energía, arriba del cual los restantes OM de mayor energía se posicionan por pares degenerados. Cuando los electrones llenan los diferentes OM, primeramente un par llena el orbital de menor energía y luego dos pares llenan cada uno de los n niveles de mayor energía sucesivos un total de 4n + 2. Cualquier otro número conducirá a semillenar un nivel de energía enlazante y por lo tanto a desestabilizar al compuesto.
44 Compuestos Aromáticos Policíclicos Aromaticidad del Naftaleno Naftaleno tiene un sistema cíclico de electrones π conjugados, con traslape de orbitales p tanto en la periferia de los 10 C de la molécula como a través del enlace central 10 es un número de Hückel (4n + 2 cuando n = 2) por lo que existe deslocalización electrónica π y consecuente aromaticidad en el naftaleno
45 Iones Aromáticos de Carbono : Carbaniones Se observa un carbanión híbrido sp 2 : Anion ciclopentadienilo Cíclico: Si Conjugado: Si Plano: Si Hückel: Si (6 electrones π, n=1) Conclusión: es un compuesto Aromático
46 Iones Aromáticos de Carbono : Carbocationes Se observa un carbocatión» híbrido sp 2 Catión cicloheptatrienilo Catión ciclopropenilo Cíclico: Si Conjugado: Si Plano: Si Hückel: Si (6 e - π, n=1, 2 e - π, n=0)
47 Heterociclos Aromáticos Los compuestos Heterocíclicos también pueden ser aromáticos Piridina: similar al benceno en su estructura de electrones π : heterociclo de seis miembros con N en su anillo Cada uno de los 6 C sp 2 y el átomo de N que también es híbrido sp 2, tienen un orbital p perpendicular al plano del anillo y cada orbitl p contiene un electrón π, lo que aporta el total de 6 electrones π El par electrónico n (libre) se encuentra en un orbital sp 2 en el plano del anillo y no forma parte del sistema aromático π (nube π aromática)
48 Heterociclos Aromáticos Pirrol es un heterociclo de 5 miembros con 6 electrones π Aromático Cada C sp 2 contribuye con 1 electrón π al sexteto aromático El N sp 2 -contribuye con 2 electrones (su par libre, n ) el cual ocupa el orbital p
49 Ejemplo Resuelto Determinando la aromaticidad de un heterocilo El Tiofeno es un heterociclo azufrado que sufre reacciones típicas de sustitución aromática más bien que reacciones de adición. Por qué el tiofeno es aromático?
50 Ejemplo Resuelto Determinando la aromaticidad de un heterocilo Estrategia Recuerde los requerimientos para la aromaticidad Molécula plana, cíclica, conjugada con 4n + 2 electrones π Observe cómo estos requerimientos se aplican al tiofeno
51 Ejemplo Resuelto Determinando la aromaticidad de un heterocilo Solución Tiofeno es el análogo azufrado del pirrol El átomo de azufre está hibridado sp 2 y tiene un par de electrones libres en un orbital p perpendicular al plano del anillo. Además el azufre tiene un segundo par de electrones libres en el plano del anillo en un orbital sp 2
Sistemas conjugados. Resonancia. Aromaticidad.
 Sistemas conjugados. Resonancia. Aromaticidad. Preparado por Licda. Nora Guzmán Basado en: Dr. Carlos A. Rius, Depto.Química Orgánica, Facultad de Química,UNAM. Lic. Mario M. Rodas, Depto. Química Orgánica,
Sistemas conjugados. Resonancia. Aromaticidad. Preparado por Licda. Nora Guzmán Basado en: Dr. Carlos A. Rius, Depto.Química Orgánica, Facultad de Química,UNAM. Lic. Mario M. Rodas, Depto. Química Orgánica,
CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS
 CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Departamento de Química Orgánica Sistemas Conjugados Los sistemas insaturados
CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Departamento de Química Orgánica Sistemas Conjugados Los sistemas insaturados
Isomería Resonancia: Deslocalización Electrónica
 Isomería Resonancia: Deslocalización Electrónica Facultad de.qq y Farmacia USA Química rgánica I (Q) 2016 Preparado por Licda. Nora Guzmán Isómeros Son compuestos que presentan la misma fórmula molecular,
Isomería Resonancia: Deslocalización Electrónica Facultad de.qq y Farmacia USA Química rgánica I (Q) 2016 Preparado por Licda. Nora Guzmán Isómeros Son compuestos que presentan la misma fórmula molecular,
Dienos aislados. Dienos conjugados. Dienos acumulados (alenos)
 TEMA 10.- Hidrocarburos poliinsaturados. Clasificación. Dienos conjugados. Reacciones de adición. Cicloadiciones. Reacciones de Diels-Alder. Un dieno es un compuesto orgánico que tiene dos enlaces dobles.
TEMA 10.- Hidrocarburos poliinsaturados. Clasificación. Dienos conjugados. Reacciones de adición. Cicloadiciones. Reacciones de Diels-Alder. Un dieno es un compuesto orgánico que tiene dos enlaces dobles.
Carbocationes. sp 3. Formación de Carbocationes
 arbocationes Los carbocationes son intermediarios orgánicos en los que el carbono está cargado positivamente. Una gran cantidad de reacciones orgánicas proceden a través de la formación de carbocationes.
arbocationes Los carbocationes son intermediarios orgánicos en los que el carbono está cargado positivamente. Una gran cantidad de reacciones orgánicas proceden a través de la formación de carbocationes.
ESTRUCTURA Y ESTABILIDAD DEL BENCENO
 BENCENO ESTRUCTURA Y ESTABILIDAD DEL BENCENO El Benceno reacciona lentamente con Br 2 para dar bromobenceno (en donde el Br reemplaza (o sustituye) al H) Esta es una reacción de sustitución más que una
BENCENO ESTRUCTURA Y ESTABILIDAD DEL BENCENO El Benceno reacciona lentamente con Br 2 para dar bromobenceno (en donde el Br reemplaza (o sustituye) al H) Esta es una reacción de sustitución más que una
TEORÍA DE ORBITALES MOLECULARES DE HÜCKEL
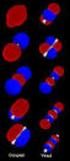 TEORÍA DE ORBITALES MOLECULARES DE HÜCKEL Principios básicos. El método de orbitales moleculares de Hückel (HMO) constituye la aproximación más simple de la teoría de orbitales moleculares. Su aplicación
TEORÍA DE ORBITALES MOLECULARES DE HÜCKEL Principios básicos. El método de orbitales moleculares de Hückel (HMO) constituye la aproximación más simple de la teoría de orbitales moleculares. Su aplicación
Mecanismo de las reacciones orgánicas
 TEMA 3.- Mecanismos e intermedios de reacción. Tipos de reacciones. Reacciones concertadas y reacciones por pasos. Tipos de mecanismos. Nucleófilos y electrófilos. Intermedios de reacción: iones carbonio,
TEMA 3.- Mecanismos e intermedios de reacción. Tipos de reacciones. Reacciones concertadas y reacciones por pasos. Tipos de mecanismos. Nucleófilos y electrófilos. Intermedios de reacción: iones carbonio,
QUíMICA DEL CARBONO. 1. Consulta tu tabla periódica y completa la siguiente información acerca del carbono.
 El Carbono es un elemento que da origen a una gran variedad de compuestos. En 1807, Berzellius clasificó los productos químicos en inorgánicos: los que proceden de la materia inanimada, como el CO, CO
El Carbono es un elemento que da origen a una gran variedad de compuestos. En 1807, Berzellius clasificó los productos químicos en inorgánicos: los que proceden de la materia inanimada, como el CO, CO
Estructuras de Lewis
 Estructuras de Lewis La forma más sencilla de simbolizar la estructura electrónica y el enlace en una molécula covalente es mediante estructuras de Lewis. ada electrón de valencia se representan mediante
Estructuras de Lewis La forma más sencilla de simbolizar la estructura electrónica y el enlace en una molécula covalente es mediante estructuras de Lewis. ada electrón de valencia se representan mediante
Unidad 1.3.4: Conjugación y resonancia en alquenos. Química Orgánica I Facultad de CC.QQ. Y Farmacia USAC Primer semestre 2017
 Unidad 1.3.4: Conjugación y resonancia en alquenos Química Orgánica I Facultad de CC.QQ. Y Farmacia USAC Primer semestre 2017 Dienos conjugados Son compuestos que presentan dos enlaces dobles C-C, separados
Unidad 1.3.4: Conjugación y resonancia en alquenos Química Orgánica I Facultad de CC.QQ. Y Farmacia USAC Primer semestre 2017 Dienos conjugados Son compuestos que presentan dos enlaces dobles C-C, separados
Enlace químico: moléculas diatómicas
 Química General e Inorgánica A Enlace químico: moléculas diatómicas Tema 5 Los electrones de valencia son los electrones del nivel exterior de un átomo. Los electrones de valencia son los electrones que
Química General e Inorgánica A Enlace químico: moléculas diatómicas Tema 5 Los electrones de valencia son los electrones del nivel exterior de un átomo. Los electrones de valencia son los electrones que
Qué es la química orgánica?
 Nivel: 2.º Medio Subsector: Ciencias químicas Unidad temática: Qué es la química orgánica? La química orgánica es una ciencia cuyo objetivo es el estudio de los compuestos que contienen el elemento carbono
Nivel: 2.º Medio Subsector: Ciencias químicas Unidad temática: Qué es la química orgánica? La química orgánica es una ciencia cuyo objetivo es el estudio de los compuestos que contienen el elemento carbono
Resonancia. No siempre existe una única estructura de Lewis que pueda explicar las propiedades de una molécula o ión.
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica 5 Año Tema VI: Resonancia Prof.
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica 5 Año Tema VI: Resonancia Prof.
Tema 10 Sistemas insaturados conjugados
 Tema 10 Sistemas insaturados conjugados Sistemas alílicos. Estructura de los dienos conjugados. Calores de hidrogenación de dienos. Síntesis de dienos. Reactividad de los dienos conjugados. La reacción
Tema 10 Sistemas insaturados conjugados Sistemas alílicos. Estructura de los dienos conjugados. Calores de hidrogenación de dienos. Síntesis de dienos. Reactividad de los dienos conjugados. La reacción
UNIDAD 2A: ESTRUCTURA DE LOS COMPUESTOS ORGÁNICOS
 UNIDAD 2A: ESTRUCTURA DE LOS COMPUESTOS ORGÁNICOS Para comprender el comportamiento de un compuesto orgánico es necesario conocer: Composición: FÓRMULA MOLECULAR Estructura: FÓRMULA ESTRUCTURAL Configuración:
UNIDAD 2A: ESTRUCTURA DE LOS COMPUESTOS ORGÁNICOS Para comprender el comportamiento de un compuesto orgánico es necesario conocer: Composición: FÓRMULA MOLECULAR Estructura: FÓRMULA ESTRUCTURAL Configuración:
TEMA 8.- TEORÍA DE ENLACE QUÍMICO Y GEOMETRÍA MOLECULAR.
 TEMA 8.- TEORÍA DE ENLACE QUÍMICO Y GEOMETRÍA MOLECULAR. 1. Geometría Molecular. Modelo de repulsión de par electrónico en la capa de valencia (VSEPR). 2. Polaridad de las especies químicas polinucleares.
TEMA 8.- TEORÍA DE ENLACE QUÍMICO Y GEOMETRÍA MOLECULAR. 1. Geometría Molecular. Modelo de repulsión de par electrónico en la capa de valencia (VSEPR). 2. Polaridad de las especies químicas polinucleares.
Enlaces químicos II: Geometría molecular e hibridación de orbitales atómicos
 Enlaces químicos II: Geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Modelo de repulsión de
Enlaces químicos II: Geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Modelo de repulsión de
Enlace covalente: Teoría del enlace de valencia. Hibridación.
 Enlace covalente: Teoría del enlace de valencia. Hibridación. Valencia covalente o covalencia de un elemento: número de electrones que comparte con otros átomos. Un átomo puede desaparear electrones promocionándolos
Enlace covalente: Teoría del enlace de valencia. Hibridación. Valencia covalente o covalencia de un elemento: número de electrones que comparte con otros átomos. Un átomo puede desaparear electrones promocionándolos
UNIDAD 1 (P.XIII) Objetivos
 UNIDAD 1 (P.XIII) Objetivos 1. Calcule el IDH en compuestos insaturados 2. Interprete el valor de IDH y proponga compuestos que cumplan un IDH determinado. 3. Dibuje las estructuras de resonancia de compuestos
UNIDAD 1 (P.XIII) Objetivos 1. Calcule el IDH en compuestos insaturados 2. Interprete el valor de IDH y proponga compuestos que cumplan un IDH determinado. 3. Dibuje las estructuras de resonancia de compuestos
Química Orgánica I. Clase 2. Cont.
 Química Orgánica I Clase 2. Cont. Características Generales Orbitales Atómicos Orbitales íbridos Geometría Ejemplos Enlaces C-C Triples Alquinos Dobles Alquenos Sencillos Alcanos Longitudes de Enlace vs.
Química Orgánica I Clase 2. Cont. Características Generales Orbitales Atómicos Orbitales íbridos Geometría Ejemplos Enlaces C-C Triples Alquinos Dobles Alquenos Sencillos Alcanos Longitudes de Enlace vs.
El enlace iónico. Los cationes y los aniones están unidos por la fuerza electroestática.
 El enlace iónico Los elementos con bajas energías de ionización tienden a formar cationes, en cambio los elementos con alta afinidad electrónicas tienden a formar aniones. Los metales alcalinos (IA) y
El enlace iónico Los elementos con bajas energías de ionización tienden a formar cationes, en cambio los elementos con alta afinidad electrónicas tienden a formar aniones. Los metales alcalinos (IA) y
DIENOS. Los dienos conjugados son aquellos donde los enlaces dobles se alternan con enlaces simples. Ej: 1,3-pentadieno CH 2 =CH-CH=CH-CH 3
 Teoría de Química Orgánica I DIENOS Un hidrocarburo que contiene dos dobles enlaces se denomina dieno y la relación entre los dobles enlaces puede clasificarse como aislados, conjugados o acumulados. Los
Teoría de Química Orgánica I DIENOS Un hidrocarburo que contiene dos dobles enlaces se denomina dieno y la relación entre los dobles enlaces puede clasificarse como aislados, conjugados o acumulados. Los
Definición Bronsted-Lowry
 TEMA 4.- Acidos y bases. Propiedades ácido-base de los compuestos orgánicos. Grupos funcionales con carácter ácido. Grupos funcionales con carácter básico. Fuerza de los ácidos. Fuerza de las bases. Acidez
TEMA 4.- Acidos y bases. Propiedades ácido-base de los compuestos orgánicos. Grupos funcionales con carácter ácido. Grupos funcionales con carácter básico. Fuerza de los ácidos. Fuerza de las bases. Acidez
Modelo de repulsión de pares de electrones en la capa de valencia Forma molecular y polaridad molecular. Hibridación de orbitales y enlaces múltiples
 GEOMETRÍA MOLECULAR Y TEORÍADE ENLACE Modelo de repulsión de pares de electrones en la capa de valencia Forma molecular y polaridad molecular Teoría de enlace de valencia Hibridación de orbitales y enlaces
GEOMETRÍA MOLECULAR Y TEORÍADE ENLACE Modelo de repulsión de pares de electrones en la capa de valencia Forma molecular y polaridad molecular Teoría de enlace de valencia Hibridación de orbitales y enlaces
TEMA 4 EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS
 TEMA 4 EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS 1. Efecto inductivo. 2. Efecto conjugativo. 3. Resonancia y orbitales deslocalizados. 4. Resonancia y aromaticidad. Fundamentos de Química Orgánica 51
TEMA 4 EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS 1. Efecto inductivo. 2. Efecto conjugativo. 3. Resonancia y orbitales deslocalizados. 4. Resonancia y aromaticidad. Fundamentos de Química Orgánica 51
TEORÍA DEL ENLACE DE VALENCIA
 Esta teoría supone que: TEORÍA DEL ENLACE DE VALENCIA Dos átomos forman un enlace covalente cuando se superponen o solapan orbitales atómicos de ambos, originando una zona común de alta densidad electrónica
Esta teoría supone que: TEORÍA DEL ENLACE DE VALENCIA Dos átomos forman un enlace covalente cuando se superponen o solapan orbitales atómicos de ambos, originando una zona común de alta densidad electrónica
EL ENLACE QUÍMICO. La unión consiste en que uno o más electrones de valencia de algunos de los átomos se introduce en la esfera electrónica del otro.
 EL ENLACE QUÍMICO Electrones de valencia La unión entre los átomos se realiza mediante los electrones de la última capa exterior, que reciben el nombre de electrones de valencia. La unión consiste en que
EL ENLACE QUÍMICO Electrones de valencia La unión entre los átomos se realiza mediante los electrones de la última capa exterior, que reciben el nombre de electrones de valencia. La unión consiste en que
MODELO DE RESPUESTAS
 209 1/5 UNIVERSIDAD NACIONAL ABIERTA VICERRECTORADO ACADEMICO AREA: INGENIERÍA CARRERA: INGENIERIA INDUSTRIAL S ASIGNATURA: QUIMICA GENERAL CÓDIGO: 209 MOMENTO: VERSION: 1 ECHA DE APLICACIÓN: 16/02/13
209 1/5 UNIVERSIDAD NACIONAL ABIERTA VICERRECTORADO ACADEMICO AREA: INGENIERÍA CARRERA: INGENIERIA INDUSTRIAL S ASIGNATURA: QUIMICA GENERAL CÓDIGO: 209 MOMENTO: VERSION: 1 ECHA DE APLICACIÓN: 16/02/13
Tema 11 Reacciones radicalarias. Generalidades. Halogenación de alcanos. Halogenación alílica. Adición radicalaria de HBr a alquenos
 Tema 11 Reacciones radicalarias Generalidades. Halogenación de alcanos. Halogenación alílica. Adición radicalaria de HBr a alquenos 1 Reacciones radicalarias Recordemos: Un radical es un intermedio reactivo
Tema 11 Reacciones radicalarias Generalidades. Halogenación de alcanos. Halogenación alílica. Adición radicalaria de HBr a alquenos 1 Reacciones radicalarias Recordemos: Un radical es un intermedio reactivo
El estudio se centrará en los compuestos heterocíclicos insaturados (alternados) aromáticos
 TEMA 5: ETRUCTURA Y PRPIEDADE GEERALE Aromaticidad en compuestos heterocíclicos El estudio se centrará en los compuestos heterocíclicos insaturados (alternados) aromáticos - Los no aromáticos tienen unas
TEMA 5: ETRUCTURA Y PRPIEDADE GEERALE Aromaticidad en compuestos heterocíclicos El estudio se centrará en los compuestos heterocíclicos insaturados (alternados) aromáticos - Los no aromáticos tienen unas
HIDROCARBUROS AROMATICOS. Hidrocarburos aromáticos monocíclicos
 TEMA 11.- Benceno y aromaticidad. Concepto de aromaticidad: estructura del benceno y energía de estabilización. Propiedades generales. Reacciones de adición y oxidación. HIDROCARBUROS AROMATICOS Se les
TEMA 11.- Benceno y aromaticidad. Concepto de aromaticidad: estructura del benceno y energía de estabilización. Propiedades generales. Reacciones de adición y oxidación. HIDROCARBUROS AROMATICOS Se les
a) Comenta los elementos de simetría que posee la molécula, indicando cuantos tipos diferentes de orbitales moleculares posee la
 Segundo parcial de Química Física. 4 de Junio de 21 1) a) Explica por qué la función de onda ψ = φ1s( r1) φ2s( r2), no es una función de onda correcta para la configuración 1s 1 2s 1 del átomo de e. uáles
Segundo parcial de Química Física. 4 de Junio de 21 1) a) Explica por qué la función de onda ψ = φ1s( r1) φ2s( r2), no es una función de onda correcta para la configuración 1s 1 2s 1 del átomo de e. uáles
ACIDOS Y BASES. QUÍMICA ORGÁNICA I (Q) Facultad de CC.QQ. y Farmacia USAC Segundo Semestre 2014
 ACIDOS Y BASES QUÍMICA ORGÁNICA I (Q) Facultad de CC.QQ. y Farmacia USAC Segundo Semestre 2014 Ácidos y Bases Los términos acido y base pueden tener diferente significado, dependiendo del contexto. La
ACIDOS Y BASES QUÍMICA ORGÁNICA I (Q) Facultad de CC.QQ. y Farmacia USAC Segundo Semestre 2014 Ácidos y Bases Los términos acido y base pueden tener diferente significado, dependiendo del contexto. La
TEMA 1. QUÍMICA ORGÁNICA.
 TEMA 1. QUÍMICA ORGÁNICA. I. TIPOS DE REACTIVOS ORGÁNICOS: En las reacciones químicas se distingue entre dos tipos de reactivos: I.1. Sustrato. Es la molécula reaccionante más grande. En el transcurso
TEMA 1. QUÍMICA ORGÁNICA. I. TIPOS DE REACTIVOS ORGÁNICOS: En las reacciones químicas se distingue entre dos tipos de reactivos: I.1. Sustrato. Es la molécula reaccionante más grande. En el transcurso
TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS.
 TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS. 1. Estructuras de resonancia. 1.1. Contribución de las estructuras resonantes. 1.2. Cómo dibujar estructuras resonantes 2. Efecto inductivo. 3. Efecto
TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS. 1. Estructuras de resonancia. 1.1. Contribución de las estructuras resonantes. 1.2. Cómo dibujar estructuras resonantes 2. Efecto inductivo. 3. Efecto
Benceno y compuestos aromáticos
 Benceno y compuestos aromáticos Aparte de las características físicas del benceno, que no resultan explicadas por las estructuras de 1,3,5-ciclohexatrieno, existen una serie de propiedades químicas del
Benceno y compuestos aromáticos Aparte de las características físicas del benceno, que no resultan explicadas por las estructuras de 1,3,5-ciclohexatrieno, existen una serie de propiedades químicas del
Problemas numéricos y Cuestiones. Capítulo 6
 1. Escriba las estructuras de Lewis para los siguientes compuestos iónicos: (a) cloruro de calcio; (b) sulfuro de bario; c) óxido de litio; d) fluoruro de sodio; e) nitruro de magnesio Todas estas estructuras
1. Escriba las estructuras de Lewis para los siguientes compuestos iónicos: (a) cloruro de calcio; (b) sulfuro de bario; c) óxido de litio; d) fluoruro de sodio; e) nitruro de magnesio Todas estas estructuras
Unidad 2 Hidrocarburos Aromáticos y Heterociclos Aromáticos. Química orgánica I Químicos Escuela de vacaciones junio 2016 Licda. Jaqueline Carrera.
 Unidad 2 Hidrocarburos Aromáticos y Heterociclos Aromáticos Química orgánica I Químicos Escuela de vacaciones junio 2016 Licda. Jaqueline Carrera. Estructura del benceno Deslocalización de electrones o
Unidad 2 Hidrocarburos Aromáticos y Heterociclos Aromáticos Química orgánica I Químicos Escuela de vacaciones junio 2016 Licda. Jaqueline Carrera. Estructura del benceno Deslocalización de electrones o
QUÍMICA DEL CARBONO Principales Tipos de Reacciones Orgánicas
 1/5 DEL ARBN Para realizar un estudio completo de los compuestos de carbono, es necesario también conocer las propiedades químicas de los mismos, es decir, su reactividad. Una parte muy importante de la
1/5 DEL ARBN Para realizar un estudio completo de los compuestos de carbono, es necesario también conocer las propiedades químicas de los mismos, es decir, su reactividad. Una parte muy importante de la
7-2.- Propiedades periódicas de los elementos. UdeC/FCQ/M E König Unidad 7 (7-2)
 7-2.- Propiedades periódicas de los elementos. 1 7-2. Propiedades periódicas de los elementos Todo comportamiento físico y químico de los elementos se basa fundamentalmente en las configuraciones electrónicas
7-2.- Propiedades periódicas de los elementos. 1 7-2. Propiedades periódicas de los elementos Todo comportamiento físico y químico de los elementos se basa fundamentalmente en las configuraciones electrónicas
ALCANOS. Estructura y propiedades
 TEMA 5.- idrocarburos y alcanos. idrocarburos: tipos y clasificación. idrocarburos saturados. Características generales. Formas de representación espacial. Análisis conformacional. Reactividad. Los hidrocarburos
TEMA 5.- idrocarburos y alcanos. idrocarburos: tipos y clasificación. idrocarburos saturados. Características generales. Formas de representación espacial. Análisis conformacional. Reactividad. Los hidrocarburos
Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento conteste las siguientes preguntas.
 EXPERIMENTO 3 Reacción de Hidrocarburos Fecha: Sección de laboratorio: Nombre del estudiante: Grupo #: Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento conteste
EXPERIMENTO 3 Reacción de Hidrocarburos Fecha: Sección de laboratorio: Nombre del estudiante: Grupo #: Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento conteste
UNIVERSDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA ORGANICA III. Integrante: Fecha de entrega: 26/06/2011 Giselle Velasco
 UNIVERSDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA ORGANICA III Integrante: Fecha de entrega: 6/06/011 Giselle Velasco Carrera: Quimica Pura. Trabajo # Tema: Acidez de los Acidos Carboxílicos
UNIVERSDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA ORGANICA III Integrante: Fecha de entrega: 6/06/011 Giselle Velasco Carrera: Quimica Pura. Trabajo # Tema: Acidez de los Acidos Carboxílicos
Tema 3. Enlace químico
 Tema 3. Enlace químico Teoría de Lewis Enlace iónico Enlace covalente Parámetros de enlace Forma de las moléculas Polaridad de las moléculas Teoría del enlace de valencia Enlace químico Modo de combinarse
Tema 3. Enlace químico Teoría de Lewis Enlace iónico Enlace covalente Parámetros de enlace Forma de las moléculas Polaridad de las moléculas Teoría del enlace de valencia Enlace químico Modo de combinarse
Estructura atómica: tipos de enlaces
 Estructura atómica: tipos de enlaces Estructura de los átomos Modelo atómico de Bohr Masa (g) Carga (C) Protón 1.673 x 10-24 1.602 x 10-19 Neutrón 1.675 x 10-24 0 Electrón 9.109 x 10-28 1.602 x 10-19 Los
Estructura atómica: tipos de enlaces Estructura de los átomos Modelo atómico de Bohr Masa (g) Carga (C) Protón 1.673 x 10-24 1.602 x 10-19 Neutrón 1.675 x 10-24 0 Electrón 9.109 x 10-28 1.602 x 10-19 Los
Tendencias Periódicas- Problemas de Revisión
 Tendencias Periódicas- Problemas de Revisión PSI Química Nombre Tamaño atómico 1. Ordena los siguientes elementos según su tamaño atómico creciente: P, Cs, Sn, F, Sr, Tl 2. Ordena los siguientes elementos
Tendencias Periódicas- Problemas de Revisión PSI Química Nombre Tamaño atómico 1. Ordena los siguientes elementos según su tamaño atómico creciente: P, Cs, Sn, F, Sr, Tl 2. Ordena los siguientes elementos
León Felipe Otálvaro Tamayo 1 REACCIONES ÁCIDO-BASE
 León Felipe tálvaro Tamayo 1 REACCINES ÁCID-BASE emos visto que en general, las reacciones en química orgánica ocurren entre nucleófilos y electrófilos, de cara a que un enlace es formado entre el centro
León Felipe tálvaro Tamayo 1 REACCINES ÁCID-BASE emos visto que en general, las reacciones en química orgánica ocurren entre nucleófilos y electrófilos, de cara a que un enlace es formado entre el centro
QUÍMICA INORGÁNICA AVANZADA COMPUESTOS DE COORDINACIÓN
 QUÍMICA INORGÁNICA AVANZADA COMPUESTOS DE COORDINACIÓN Enlace Cualquier teoría de enlace en compuestos de coordinación debe explicar el comportamiento experimental de los compuestos: datos termodinámicos
QUÍMICA INORGÁNICA AVANZADA COMPUESTOS DE COORDINACIÓN Enlace Cualquier teoría de enlace en compuestos de coordinación debe explicar el comportamiento experimental de los compuestos: datos termodinámicos
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2013 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 01 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción B Reserva 1, Ejercicio, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción B Reserva
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 01 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción B Reserva 1, Ejercicio, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción B Reserva
Resolución de ejercicios PRÁCTICO 12
 Resolución de ejercicios PRÁCTIC 12 1) a) bservando la estructura de Lewis de la molécula BeH 2 podemos decir que el átomo de Be se une a dos átomos de H mediante dos enlaces simples. Una hibridación de
Resolución de ejercicios PRÁCTIC 12 1) a) bservando la estructura de Lewis de la molécula BeH 2 podemos decir que el átomo de Be se une a dos átomos de H mediante dos enlaces simples. Una hibridación de
LA TABLA PERIÓDICA. 2ºbachillerato QUÍMICA
 LA TABLA PERIÓDICA 2ºbachillerato QUÍMICA 1 A lo lo largo de la la historia, los químicos han intentado ordenar los elementos de forma agrupada, de tal manera que aquellos que posean propiedades similares
LA TABLA PERIÓDICA 2ºbachillerato QUÍMICA 1 A lo lo largo de la la historia, los químicos han intentado ordenar los elementos de forma agrupada, de tal manera que aquellos que posean propiedades similares
Qué estudiamos en Química Orgánica? ÁTOMOS Y ELECTRONES! ENLACE QUÍMICO
 Química Orgánica I Qué estudiamos en Química Orgánica? Cómo los compuestos orgánicos reaccionan: Rompimiento y formación de enlaces. Enlaces que se forman cuando átomos comparten electrones, enlaces que
Química Orgánica I Qué estudiamos en Química Orgánica? Cómo los compuestos orgánicos reaccionan: Rompimiento y formación de enlaces. Enlaces que se forman cuando átomos comparten electrones, enlaces que
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2011 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 011 QUÍMICA TEMA : ENLACES QUÍMICOS Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción A Reserva, Ejercicio, Opción A Reserva, Ejercicio, Opción B Septiembre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 011 QUÍMICA TEMA : ENLACES QUÍMICOS Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción A Reserva, Ejercicio, Opción A Reserva, Ejercicio, Opción B Septiembre,
Química del carbono: estudio de algunas funciones orgánicas
 Química del carbono: estudio de algunas funciones orgánicas Contenidos Estructura y enlaces en moléculas orgánicas: geometría y polaridad. Isomería geométrica. Relación entre fuerzas intermoleculares y
Química del carbono: estudio de algunas funciones orgánicas Contenidos Estructura y enlaces en moléculas orgánicas: geometría y polaridad. Isomería geométrica. Relación entre fuerzas intermoleculares y
Comparación entre los calores de hidrogenación del 1-penteno y del trans-2-penteno. 2.6 Kcal/mol. Hº = kcal/mol
 Química rgánica Tema 8. Dienos 1 Tema 8. Dienos conjugados: estructura y estabilidad. Reacciones de adición a dienos conjugados. ontrol cinético y control termodinámico en la adición de al 1,3- butadieno.
Química rgánica Tema 8. Dienos 1 Tema 8. Dienos conjugados: estructura y estabilidad. Reacciones de adición a dienos conjugados. ontrol cinético y control termodinámico en la adición de al 1,3- butadieno.
6.1. LAS CARACTERÍSTICAS DE LOS SERES VIVOS. Átomos y estructura atómica
 6.1. LAS CARACTERÍSTICAS DE LOS SERES VIVOS En este epígrafe se desarrollan las características que diferencian a los seres vivos. Una de ellas es la complejidad molecular, que se debe a la inmensa variedad
6.1. LAS CARACTERÍSTICAS DE LOS SERES VIVOS En este epígrafe se desarrollan las características que diferencian a los seres vivos. Una de ellas es la complejidad molecular, que se debe a la inmensa variedad
Dienos conjugados y polienos.
 DIENOS Y POLIENOS Dienos conjugados y polienos. Cuando los dobles enlaces están separados por dos o más enlaces sencillos no interaccionan entre ellos y se les denomina enlaces dobles aislados, como en
DIENOS Y POLIENOS Dienos conjugados y polienos. Cuando los dobles enlaces están separados por dos o más enlaces sencillos no interaccionan entre ellos y se les denomina enlaces dobles aislados, como en
UNIDAD 6 RESONANCIA, AROMATICIDAD Y TAUTOMERÍA
 UIDAD 6 RESOAIA, AROMATIIDAD Y TAUTOMERÍA ómo muestran los calores de hidrogenación la estabilidad de los alquenos El calor de hidrogenación de un alqueno es la diferencia de energía entre el alqueno de
UIDAD 6 RESOAIA, AROMATIIDAD Y TAUTOMERÍA ómo muestran los calores de hidrogenación la estabilidad de los alquenos El calor de hidrogenación de un alqueno es la diferencia de energía entre el alqueno de
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS
 REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS Reacciones Inorgánicas En general son rápidas y sencillas, especialmente las iónicas en solución acuosa porque los reactivos ya están listos para reaccionar. Reacciones
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS Reacciones Inorgánicas En general son rápidas y sencillas, especialmente las iónicas en solución acuosa porque los reactivos ya están listos para reaccionar. Reacciones
Área Académica: Química Orgánica. Tema: Introducción y conceptos básicos. Profesor(a) : Quím. Diana Graciela Ballesteros Rico
 Área Académica: Química Orgánica Tema: Introducción y conceptos básicos. Profesor(a) : Quím. Diana Graciela Ballesteros Rico Periodo: Enero-Junio de 2012 Topic: Introduction and basic concepts. Abstract
Área Académica: Química Orgánica Tema: Introducción y conceptos básicos. Profesor(a) : Quím. Diana Graciela Ballesteros Rico Periodo: Enero-Junio de 2012 Topic: Introduction and basic concepts. Abstract
HIBRIDACIÓN. Antes de tratar de establecer qué hibridación presenta un determinado átomo, se debe tener en cuenta lo siguiente:
 M. C. Q. Alfredo Velásquez Márquez Profesor de la acultad de Ingeniería de la UNAM velasquez777@yahoo.com.mx HIBRIDACIÓN El proceso de hibridación consiste en la combinación (igualación energética) de
M. C. Q. Alfredo Velásquez Márquez Profesor de la acultad de Ingeniería de la UNAM velasquez777@yahoo.com.mx HIBRIDACIÓN El proceso de hibridación consiste en la combinación (igualación energética) de
León Felipe Otálvaro Tamayo 1 TÓPICO 3 LA LÓGICA DE LAS REACCIONES QUÍMICAS (MECANISMOS).
 León Felipe tálvaro Tamayo 1 TÓPI 3 LA LÓGIA DE LAS REAINES QUÍMIAS (MEANISMS). Un mecanismo es una descripción paso a paso de cómo las reacciones químicas ocurren. ada paso implica algún tipo de formación
León Felipe tálvaro Tamayo 1 TÓPI 3 LA LÓGIA DE LAS REAINES QUÍMIAS (MEANISMS). Un mecanismo es una descripción paso a paso de cómo las reacciones químicas ocurren. ada paso implica algún tipo de formación
TEMA 2 REACTIVIDAD QUÍMICA Y REACCIONES ORGÁNICAS
 TEMA 2 REATIVIDAD QUÍMIA Y REAIONES ORGÁNIAS 1. Introducción. 2. Tipos de reacciones orgánicas. 3. Reacciones características de los grupos funcionales. 4. aracterísticas de las reacciones orgánicas. 5.
TEMA 2 REATIVIDAD QUÍMIA Y REAIONES ORGÁNIAS 1. Introducción. 2. Tipos de reacciones orgánicas. 3. Reacciones características de los grupos funcionales. 4. aracterísticas de las reacciones orgánicas. 5.
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Modelo 2007/2008 PRIMERA PARTE
 1 PAU Química. Modelo 2007/2008 PRIMERA PARTE Cuestión 1. Para cada uno de los elementos con la siguiente configuración electrónica en los niveles de energía más externos: A=2s 2 2p 4 ; B=2s 2 ; C= 3s
1 PAU Química. Modelo 2007/2008 PRIMERA PARTE Cuestión 1. Para cada uno de los elementos con la siguiente configuración electrónica en los niveles de energía más externos: A=2s 2 2p 4 ; B=2s 2 ; C= 3s
NIVELES DE ENERGÍA, SUBNIVELES, ORBITALES Y ELECTRONES
 Universidad de San Carlos de Guatemala Escuela de Formación de Profesores de Enseñanza Media Programa Académico Preparatorio Curso: Química NIVELES DE ENERGÍA, SUBNIVELES, ORBITALES Y ELECTRONES PAP-QUÍMICA
Universidad de San Carlos de Guatemala Escuela de Formación de Profesores de Enseñanza Media Programa Académico Preparatorio Curso: Química NIVELES DE ENERGÍA, SUBNIVELES, ORBITALES Y ELECTRONES PAP-QUÍMICA
Los números indican los niveles de energía. 2s 2p Las letras la forma del orbital. 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p
 1s Los números indican los niveles de energía. 2s 2p Las letras la forma del orbital. 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p Diagrama de orbitales: Consiste en dibujar los orbitales como cuadrados
1s Los números indican los niveles de energía. 2s 2p Las letras la forma del orbital. 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p Diagrama de orbitales: Consiste en dibujar los orbitales como cuadrados
Química de Alimentos. Manual de Experimentos de Química Orgánica II (1407).
 PRÁCTICA 1 Identificación Espectroscópica de Compuestos Orgánicos. Taller de Espectroscopia de Infrarrojo. I. OBJETIVOS. a) Conocer los principios fundamentales que rigen la interacción energía-materia
PRÁCTICA 1 Identificación Espectroscópica de Compuestos Orgánicos. Taller de Espectroscopia de Infrarrojo. I. OBJETIVOS. a) Conocer los principios fundamentales que rigen la interacción energía-materia
Tema 12. PREPARACIÓN DE ALQUENOS
 Tema 12. PREPARACIÓN DE ALQUENOS 2.- Principales familias de compuestos orgánicos: Tema 11. Alcanos Tema 12. Alquenos (I) Tema 13. Alquenos (II) Tema 14. Alquinos. Tema 15. Hidrocarburos aromáticos (I).
Tema 12. PREPARACIÓN DE ALQUENOS 2.- Principales familias de compuestos orgánicos: Tema 11. Alcanos Tema 12. Alquenos (I) Tema 13. Alquenos (II) Tema 14. Alquinos. Tema 15. Hidrocarburos aromáticos (I).
Elemento químico: es el conjunto formado por átomos del mismo número atómico (Z)
 Tabla Periodica En 1913, al realizar experiencias de bombardeo de varios elementos químicos con rayos X, Moseley percibió que el comportamiento de cada elemento químico estaba relacionado con la cantidad
Tabla Periodica En 1913, al realizar experiencias de bombardeo de varios elementos químicos con rayos X, Moseley percibió que el comportamiento de cada elemento químico estaba relacionado con la cantidad
ESTRUCTURA DE LA MATERIA.
 Repaso de los modelos atómicos. ESTRUCTURA DE LA MATERIA. 1.- Razona si son verdaderas o falsas las siguientes afirmaciones: a) cuando un electrón pasa de un estado fundamental a un excitado emite energía;
Repaso de los modelos atómicos. ESTRUCTURA DE LA MATERIA. 1.- Razona si son verdaderas o falsas las siguientes afirmaciones: a) cuando un electrón pasa de un estado fundamental a un excitado emite energía;
MODELO ATÓMICO DE DALTON 1808
 ESTRUCTURA ATÓMICA MODELO ATÓMICO DE DALTON 1808 Sienta las bases para la estequiometría de composición y la estequiometría de reacción. 1. Un elemento se compone de partículas extremadamente pequeñas,
ESTRUCTURA ATÓMICA MODELO ATÓMICO DE DALTON 1808 Sienta las bases para la estequiometría de composición y la estequiometría de reacción. 1. Un elemento se compone de partículas extremadamente pequeñas,
PROGRAMA QUÍMICA 2015-2016
 PROGRAMA QUÍMICA 2015-2016 1. Conceptos comunes. Transformaciones físicas y químicas. Leyes ponderales de la química. Masas atómicas y masas moleculares. Número de Avogadro. Mol. Fórmula empírica y fórmula
PROGRAMA QUÍMICA 2015-2016 1. Conceptos comunes. Transformaciones físicas y químicas. Leyes ponderales de la química. Masas atómicas y masas moleculares. Número de Avogadro. Mol. Fórmula empírica y fórmula
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2012
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 01 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 01 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
Química Inorgánica Tema 3. Química Inorgánica en Solución Sección 3.1 Teoría Ácido - Base
 Química Inorgánica Tema 3. Química Inorgánica en Solución Sección 3.1 Teoría - Conceptos: Arrehenius Brønsted Lowry Lewis Pearson 1 Estabilidad Arrehnius Brønsted-Lowry Efecto nivelador Fuerza s s y s
Química Inorgánica Tema 3. Química Inorgánica en Solución Sección 3.1 Teoría - Conceptos: Arrehenius Brønsted Lowry Lewis Pearson 1 Estabilidad Arrehnius Brønsted-Lowry Efecto nivelador Fuerza s s y s
Modelo atómico de la materia. Tabla periódica, configuración electrónica y propiedades periódicas
 Eje temático: Modelo atómico de la materia Enlace químico Química orgánica Disoluciones químicas Contenido: Propiedades periódicas: configuración electrónica y tabla periódica Nivel: Segundo medio Modelo
Eje temático: Modelo atómico de la materia Enlace químico Química orgánica Disoluciones químicas Contenido: Propiedades periódicas: configuración electrónica y tabla periódica Nivel: Segundo medio Modelo
ESTRUCTURAS DE LEWIS
 ETRUTURA DE LEWI Las estructuras, diagramas o fórmulas de Lewis (UA, 1916) de una molécula son representaciones bidimensionales sencillas del esqueleto o conectividad de los átomos en la molécula y de
ETRUTURA DE LEWI Las estructuras, diagramas o fórmulas de Lewis (UA, 1916) de una molécula son representaciones bidimensionales sencillas del esqueleto o conectividad de los átomos en la molécula y de
Repaso Química: Compuestos
 Repaso Química: Compuestos Covalentes, formación, fórmulas I. Selección Múltiple. Escoge la mejor contestación para cada aseveración. 1 1. Los elementos en un compuesto covalente A. donan electrones. B.
Repaso Química: Compuestos Covalentes, formación, fórmulas I. Selección Múltiple. Escoge la mejor contestación para cada aseveración. 1 1. Los elementos en un compuesto covalente A. donan electrones. B.
Estructura y Nomenclatura de alquenos y alquinos. Química Orgánica I Segundo Semestre 2014 Facultad de CC.QQ. Y Farmacia USAC
 Estructura y Nomenclatura de alquenos y alquinos Química Orgánica I Segundo Semestre 2014 Facultad de CC.QQ. Y Farmacia USAC Alquenos La fórmula general de los alquenos con un solo enlace doble es CnH2n,
Estructura y Nomenclatura de alquenos y alquinos Química Orgánica I Segundo Semestre 2014 Facultad de CC.QQ. Y Farmacia USAC Alquenos La fórmula general de los alquenos con un solo enlace doble es CnH2n,
Rupturas de enlaces y Clasificación de reacciones orgánicas. Lic. Walter de la Roca Cuéllar Químico
 Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Escuela de Química Departamento de Química Orgánica Química Orgánica I (QQ) Rupturas de enlaces y Clasificación de reacciones
Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Escuela de Química Departamento de Química Orgánica Química Orgánica I (QQ) Rupturas de enlaces y Clasificación de reacciones
PROTONES Y ELECTRONES
 reflexiona Imagina que tienes un tazón de naranjas, plátanos, piñas, bayas, peras y sandía. Cómo identificas cada trozo de fruta? Es muy probable que estés familiarizado con las características de cada
reflexiona Imagina que tienes un tazón de naranjas, plátanos, piñas, bayas, peras y sandía. Cómo identificas cada trozo de fruta? Es muy probable que estés familiarizado con las características de cada
ESTRUCTURAS DE RESONANCIA
 1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
Solución: a) Falso, porque la carga que se apiña en lo que se denomina núcleo es toda la carga positiva.
 ies menéndez tolosa 1 De las siguientes proposiciones, señala las que considere correctas: a) Todos los isótopos de un elemento tienen el mismo número de electrones. b) Dos isótopos de un elemento pueden
ies menéndez tolosa 1 De las siguientes proposiciones, señala las que considere correctas: a) Todos los isótopos de un elemento tienen el mismo número de electrones. b) Dos isótopos de un elemento pueden
TEMA 1: Introducción a la Química. Reacción química: leyes. Mol y Número de Avogadro. Estequiometría y disoluciones.
 TEMA 1: Introducción a la Química. Reacción química: leyes. Mol y Número de Avogadro. Estequiometría y disoluciones. 1. Introducción: sustancias puras (elementos y compuestos); transformaciones de la materia
TEMA 1: Introducción a la Química. Reacción química: leyes. Mol y Número de Avogadro. Estequiometría y disoluciones. 1. Introducción: sustancias puras (elementos y compuestos); transformaciones de la materia
El equilibrio ácido-base en los compuestos orgánicos
 ESTRUCTURA-REACTIVIDAD DE LAS MOLÉCULAS ORGÁNICAS (I) El equilibrio ácido-base en los compuestos orgánicos Teoría de Arrhenius Según la teoría de Arrhenius, desarrollada a finales del siglo XIX, un ácido
ESTRUCTURA-REACTIVIDAD DE LAS MOLÉCULAS ORGÁNICAS (I) El equilibrio ácido-base en los compuestos orgánicos Teoría de Arrhenius Según la teoría de Arrhenius, desarrollada a finales del siglo XIX, un ácido
TEMA VII: Teoría de Gillespie de la repulsión de pares (TRPECV)
 TEMA VII: Teoría de Gillespie de la repulsión de pares (TRPECV) La TRPECV Moléculas de elementos del segundo periodo Moléculas de elementos del tercer periodo y sucesivos La teoría de Lewis sólo explica
TEMA VII: Teoría de Gillespie de la repulsión de pares (TRPECV) La TRPECV Moléculas de elementos del segundo periodo Moléculas de elementos del tercer periodo y sucesivos La teoría de Lewis sólo explica
IES Menéndez Tolosa Dpto. Física y Química 4º ESO - Modelos atómicos 1S
 IES Menéndez Tolosa Dpto. Física y Química 4º ESO - Modelos atómicos 1S 1 Escribe tres isótopos de oxígeno que tengan, y 10 neutrones. Cuál de ellos tendrá mayor Z? 16 17 1 O, O, O Todos ellos tienen el
IES Menéndez Tolosa Dpto. Física y Química 4º ESO - Modelos atómicos 1S 1 Escribe tres isótopos de oxígeno que tengan, y 10 neutrones. Cuál de ellos tendrá mayor Z? 16 17 1 O, O, O Todos ellos tienen el
Universidad Simón Bolívar ESTRUCTURAS LEWIS Y ESTRUCTURAS RESONANTES
 ESTRUCTURAS LEWIS Y ESTRUCTURAS RESONANTES 1 Escribe las estructuras de Lewis de los siguientes compuestos, e indica qué átomos presentan cargas formales en los compuestos que sea necesario: Solución 2.1
ESTRUCTURAS LEWIS Y ESTRUCTURAS RESONANTES 1 Escribe las estructuras de Lewis de los siguientes compuestos, e indica qué átomos presentan cargas formales en los compuestos que sea necesario: Solución 2.1
ESPECTROSCOPÍA ESPECTROSCOPÍA INFRARROJA INTERPRETACIÓN ESPECTRO IR
 ESPECTROSCOPÍA ESPECTROSCOPÍA INFRARROJA INTERPRETACIÓN ESPECTRO IR Espectroscopia infrarroja (Espectroscopia IR) es la rama de la espectroscopia que trata con la parte infrarroja del espectro electromagnético.
ESPECTROSCOPÍA ESPECTROSCOPÍA INFRARROJA INTERPRETACIÓN ESPECTRO IR Espectroscopia infrarroja (Espectroscopia IR) es la rama de la espectroscopia que trata con la parte infrarroja del espectro electromagnético.
ENLACE QUÍMICO. Química 2º bachillerato Enlace químico 1
 ENLACE QUÍMICO 1. El enlace químico. 2. El enlace covalente. 3. Geometría de las moléculas covalentes. 4. Polaridad de enlaces. 5. Teoría del enlace de valencia. 6. El orbital molecular. 7. Moléculas y
ENLACE QUÍMICO 1. El enlace químico. 2. El enlace covalente. 3. Geometría de las moléculas covalentes. 4. Polaridad de enlaces. 5. Teoría del enlace de valencia. 6. El orbital molecular. 7. Moléculas y
TEMA 5 CINÉTICA QUÍMICA
 TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
Estructura de los átomos.
 Estructura de los átomos. Teoría atomística de Demócrito: Átomo, del griego: que no se puede cortar. Demócrito, filósofo griego (s. IV a.c.): Si dividimos la materia de forma sucesiva llegará un momento
Estructura de los átomos. Teoría atomística de Demócrito: Átomo, del griego: que no se puede cortar. Demócrito, filósofo griego (s. IV a.c.): Si dividimos la materia de forma sucesiva llegará un momento
MODELOS ATÓMICOS Y PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. CUESTIONES.
 MODELOS ATÓMICOS Y PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. CUESTIONES. E2A.S2013 Para los siguientes elementos Na, P, S y Cl, diga razonadamente cuál es: a.- El de menor energía de ionización. b.- El
MODELOS ATÓMICOS Y PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. CUESTIONES. E2A.S2013 Para los siguientes elementos Na, P, S y Cl, diga razonadamente cuál es: a.- El de menor energía de ionización. b.- El
Fundamentos de Química 1er Curso de los Grados en Ingeniería de los Recursos Energéticos y de los Recursos Mineros 1
 Departamento de Ingeniería Química y Química Inorgánica Universidad de Cantabria (SPAIN) Fundamentos de Química 1er Curso de los Grados en Ingeniería de los Recursos Energéticos y de los Recursos Mineros
Departamento de Ingeniería Química y Química Inorgánica Universidad de Cantabria (SPAIN) Fundamentos de Química 1er Curso de los Grados en Ingeniería de los Recursos Energéticos y de los Recursos Mineros
REACCIÓN. Las herramientas sintéticas. ticas. Mayor reactividad Vía a externa. Reacción química
 Las herramientas sintéticas ticas 1. onceptos de química orgánica aplicables al diseño de síntesis de fármacos María Font.. Dpto. Química rgánica y Farmacéutica. Sección n de Modelización Molecular. Universidad
Las herramientas sintéticas ticas 1. onceptos de química orgánica aplicables al diseño de síntesis de fármacos María Font.. Dpto. Química rgánica y Farmacéutica. Sección n de Modelización Molecular. Universidad
Unidad 4 (Parte IV) Objetivos. Predecir la reactividad química de compuestos heterocíclicos en función de su estructura.
 Unidad 4 (Parte IV) Objetivos Predecir la reactividad química de compuestos heterocíclicos en función de su estructura. Propiedades químicas de los heterociclos aromáticos de cinco y seis átomos a. Basicidad
Unidad 4 (Parte IV) Objetivos Predecir la reactividad química de compuestos heterocíclicos en función de su estructura. Propiedades químicas de los heterociclos aromáticos de cinco y seis átomos a. Basicidad
Tiene alguna característica especial el átomo de carbono para encontrarse en el 94 % de los compuestos conocidos?
 Unidad 5: Química del Carbono Introducción Teórica La química orgánica abarca el estudio de la mayoría de los compuestos que nos rodean y componen los organismos vivos. Los plásticos, el combustible de
Unidad 5: Química del Carbono Introducción Teórica La química orgánica abarca el estudio de la mayoría de los compuestos que nos rodean y componen los organismos vivos. Los plásticos, el combustible de
Propiedades Periódicas
 Propiedades Periódicas Radio atómico Definición: La mitad de la distancia entre los centros de dos átomos vecinos. Estimar el tamaño de los átomos es un poco complicado debido a la naturaleza difusa de
Propiedades Periódicas Radio atómico Definición: La mitad de la distancia entre los centros de dos átomos vecinos. Estimar el tamaño de los átomos es un poco complicado debido a la naturaleza difusa de
