Procedimiento para la administración de la vacuna frente al Virus del Papiloma Humano (VPH) en la Comunidad Valenciana
|
|
|
- Silvia Montero Olivera
- hace 7 años
- Vistas:
Transcripción
1 Procedimiento para la administración de la vacuna frente al Virus del Papiloma Humano (VPH) en la Comunidad Valenciana Desde la aparición de dos casos de adolescentes que experimentaron una posible reacción adversa inmediatamente tras la administración de la segunda dosis de vacuna frente al Virus del Papiloma Humano (VPH) y la estrecha relación temporal con la vacunación en los dos casos. El Comité de expertos concluyó que la administración de la vacuna pudo actuar como un precipitante del cuadro clínico, pero no se ha encontrado ninguna prueba que apoye una relación biológica con la vacuna. El objetivo de este documento es unificar los criterios de actuación, para la administración de la vacuna frente al Virus del Papiloma Humano (VPH) en adolescentes de 14 años (nacidas entre el 1 de enero y el 31 de diciembre de 1.994), que iniciaron la vacunación en noviembre de Este documento, es complementario al protocolo de vacunación elaborado en su día frente al Virus del Papiloma Humano y que se encuentra disponible en la Web de Vacunas de la Dirección General de Salud Pública ( principales aportaciones/modificaciones del documento hacen referencia a: 1. Dónde realizar la vacunación frente al VPH? 2. Es necesario una nueva autorización? 3. Actualización de la ficha técnica. 4. Intervalo de tiempo entre dosis. 5. Recaptación. 6. Declaración de las reacciones adversas. 7. Resumen de las conclusiones del grupo de expertos. A continuación se explicita la información a cada una de las cuestiones o puntos planteados: 1. Dónde realizar la vacunación frente al VPH? La vacunación se realizará en los centros de salud, una vez administrada la vacuna, recomendar que la niña vacunada permanezca en la sala de espera unos 15 minutos. La declaración del acto vacunal en el Registro de Vacunas Nominal, no debería exceder de 48 horas. En la literatura científica están descritos casos de reacciones adversas por simpatía cuando se administran vacunas simultáneamente a un grupo de personas en un mismo lugar y en un corto periodo de tiempo, por lo que es aconsejable no citar a grupos numerosos. Las niñas se vacunarán en su centro de salud de referencia, independientemente que las dosis anteriores se hubieran declarado en otro centro, por haberse realizado la vacunación en centros docentes.
2 2. Es necesaria una nueva autorización? Aquellas niñas de 14 años que iniciaron la vacunación y fueron autorizadas en su día, consideramos que no precisan una nueva autorización, ya que en la carta que se remitió a los padres/tutores se explicitaba: para que su hija esté correctamente vacunada frente al Virus del Papiloma Humano, es necesario administrar tres dosis (0-2 y 6 meses). De todas formas al producirse la vacunación en el centro de salud si la niña va acompañada por los padres/tutores con la aprobación de estos es suficiente. Las niñas de 14 años, que han recibido dosis previas, si la vacunación se realizó en el centro docente, todas ellas estaban autorizadas ya que era un requisito necesario e imprescindible presentar cumplimentada la autorización, para que le fuera administrada la vacuna. En la Web ( esta disponible la autorización en castellano/valenciano. 3. Información que recoge la actual ficha técnica de Gardasil Las novedades que recoge la actual ficha técnica de Gardasil respecto a la que se remitió en su día, hacen referencia al apartado 4.8 de reacciones adversas y son las que figuran a continuación: 4.8 Reacciones adversas En 5 ensayos clínicos (4 controlados con placebo), se administró a los individuos Gardasil o placebo el día del reclutamiento y aproximadamente 2 y 6 meses después. Se evaluó la seguridad en el total de la población en estudio (4 ensayos) o en un subconjunto predefinido (un ensayo) de la población en estudio, vigilada mediante una tarjeta de registro de vacunación (VRC) durante los 14 días posteriores a cada inyección de Gardasil o placebo. Las siguientes reacciones adversas relacionadas con la vacuna fueron observadas entre los vacunados con Gardasil con una frecuencia de al menos el 1,0% y también en una frecuencia mayor que la observada entre los que recibieron placebo. Están clasificadas por frecuencia de acuerdo a la siguiente convención: [Muy frecuentes (>1/10); Frecuentes (>1/100 a <1/10); Poco frecuentes (>1/1.000 a <1/100); Raras (>1/ a <1/1.000); Muy Raras (<1/10.000), incluyendo notificaciones aisladas] Trastornos generales y alteraciones en el lugar de administración: Muy frecuentes: pirexia. Muy frecuentes: en el lugar de inyección: eritema, dolor, hinchazón. Frecuentes: en el lugar de inyección: hematoma, prurito. Además, en los ensayos clínicos, las reacciones adversas consideradas por el investigador como relacionadas con la vacuna o el placebo fueron observadas a frecuencias inferiores al 1%: Trastornos respiratorios, torácicos y mediastínicos: Muy raras: broncoespasmo. Trastornos de la piel y del tejido subcutáneo: Raras: urticaria.
3 Experiencia post-comercialización Se han notificado espontáneamente acontecimientos adversos en la etapa de postcomercialización de Gardasil que no se han enumerado anteriormente. No es posible estimar la frecuencia para todos los acontecimientos ni establecer una relación causal con la exposición a la vacuna, ya que éstos fueron notificados voluntariamente por una población de tamaño indeterminado. Trastornos de la sangre y del sistema linfático: linfadenopatía. Trastornos del sistema inmunológico: reacciones de hipersensibilidad, incluyendo reacciones anafilácticas/anafilactoides. Trastornos del sistema nervioso: síndrome de Guillain-Barré, mareo, dolor de cabeza, síncope acompañado algunas veces de movimientos tonicoclónicos. Trastornos gastrointestinales: náuseas, vómitos. Trastornos musculoesqueléticos y del tejido conjuntivo: artralgia, mialgia. Trastornos generales y alteraciones en el lugar de administración: astenia, fatiga, malestar. 4. Intervalo de tiempo entre dosis Tal y como consta en el protocolo de VPH que se remitió en su día, el intervalo mínimo recomendado entre la 1ª y la 2ª dosis no debe ser inferior a un mes y entre la 2ª y la 3ª dosis de tres meses. El intervalo máximo entre la 1ª y la 3ª dosis no debe exceder los doce meses. La información científica disponible sobre la efectividad de la vacuna, indica que esta disminuye considerablemente, si no se administran las tres dosis. 5. Recaptación La recaptación de las niñas de 14 años, que les falte alguna dosis de vacuna frente al VPH, se realizará a través del Sistema de Información Vacunal (SIV) en su apartado BackOffice, mediante la utilidad cartas recordatorio a la que tienen acceso los responsables de los centros de salud establecidos desde los departamentos.
4 La administración de la 3ª dosis esta programada entre el 4 y el 30 de mayo de 2009 y la recaptación de la tercera dosis entre el 1 y el 15 de junio. 6. Declaración de reacciones adversas El profesional sanitario tiene el deber y por tanto la responsabilidad, de comunicar a los órganos competentes las sospechas de reacciones adversas de las que tenga conocimiento y que pudieran ser causadas por medicamentos, asegurando así el correcto inicio del sistema de notificación espontánea. El modo de declaración de reacciones adversas en nuestra comunidad se puede realizar bien a través de la tarjeta amarilla en ( remitiéndola a Fármaco vigilancia ó bien a través del RVN (on-line). Esta última opción queda registrada en su historial vacunal y permite identificar de una forma rápida si una persona ha tenido una reacción adversa. La declaración de reacciones adversas es de sospecha e inicialmente solo supone una relación temporo-espacial con la vacuna y no necesariamente de causalidad. 7. Resumen de las conclusiones del grupo de expertos creado por el Ministerio de Sanidad. Las características clínicas y la ausencia de signos eléctricos, de neuroimagen y analíticos indican que los episodios paroxísticos que presentaron las adolescentes de Valencia no se corresponden con una enfermedad o lesión neurológica, cardiológica o sistémica. La misma valoración cabe hacer de los episodios de la adolescente de las Islas Baleares. La estrecha relación temporal con la vacunación en los dos casos de Valencia indica que la administración de la vacuna pudo actuar como un precipitante del cuadro clínico, pero no se ha encontrado ninguna prueba que apoye una relación biológica con la vacuna. La AEMPS y la EMEA descartan que el lote de la vacuna administrado a las adolescentes de Valencia presente defectos de calidad, lo cual, a su vez, es coherente con el hecho epidemiológico de que no se hayan detectado ni en España ni en la Unión Europea casos con un patrón clínico similar a los dos de Valencia, a pesar de haberse distribuido decenas de miles de dosis del mismo lote. Los equipos médicos del Hospital Clínico de Valencia y del Hospital Son Dureta actuaron, en todo momento, de forma correcta. A la luz de la valoración hecha por el Comité de Expertos, así como de la exhaustiva revisión realizada por la AEMPS y el resto de agencias europeas respecto a todos los casos de convulsiones notificados, se considera necesario informar a los profesionales sanitarios de lo siguiente: 1. La administración de las vacunas frente al VPH se puede asociar a síncope y como consecuencia del cual pueden ocurrir movimientos musculares que semejan convulsiones. Se aconseja, por tanto, que se extreme la precaución para evitar dichos síncopes o las caídas derivadas del mismo. De acuerdo con un estudio realizado por el Centro para la Prevención y Control de Enfermedades de los Estados Unidos de América 1 no hay diferencia en la incidencia de síncopes entre las vacunas frente al VPH y otras vacunas que se administran en la adolescencia. 2. Aunque se han notificado casos de convulsiones tanto en España como en otros países tras la administración de las vacunas frente al VPH, el análisis que se ha hecho de los mismos no sugiere
5 que las vacunas incrementen el riesgo. En esta misma línea apunta el estudio mencionado anteriormente 1, donde se muestra que la incidencia de convulsiones que ocurren después de haber administrado las vacunas frente al VPH no es estadísticamente diferente de la incidencia que presentan otras vacunas que se administran también en la adolescencia. 3. De acuerdo con la valoración del Comité de Expertos, la AEMPS concluye que, tanto en los dos casos notificados en Valencia como en el caso notificado en Baleares, la ausencia de una base biológica que explique la posible asociación entre los trastornos paroxísticos presentados y las vacunas, hace muy improbable que dichos cuadros puedan considerarse como reacciones adversas a las mismas. 4. De acuerdo con todos los análisis realizados, tanto la AEMPS como la EMEA confirman que el lote de vacuna involucrado no presenta ningún defecto de calidad. 5. La AEMPS concluye, finalmente, que la relación beneficio-riesgo de las vacunas frente al VPH no ha sufrido variación y sigue siendo favorable. La nota del grupo de expertos esta disponible en: 1 Gee J, Naleway A, Shui I. Vaccine Safety Datalink Project: Monitoring the safety of quadrivalent human papillomavirus vaccine (HPV4). Disponible en y
Documentación básica. Seguridad de las vacunas frente al virus del papiloma humano
 Seguridad de las vacunas frente al virus del papiloma humano Rev Pediatr Aten Primaria. 2009;11:347-52 Tras la aparición de dos casos de cuadros convulsivos en sendas niñas, acaecidos en la ciudad de Valencia
Seguridad de las vacunas frente al virus del papiloma humano Rev Pediatr Aten Primaria. 2009;11:347-52 Tras la aparición de dos casos de cuadros convulsivos en sendas niñas, acaecidos en la ciudad de Valencia
Vacunació contra el VPH
 Vacunació contra el VPH Maig 2009 Direcció general de Salut Pública Dades de la vacunació amb les dues primeres dosis (Nenes 6è primària: 33363) Resultats provisionals: Cobertura 1 D 89,1% Cobertura 2
Vacunació contra el VPH Maig 2009 Direcció general de Salut Pública Dades de la vacunació amb les dues primeres dosis (Nenes 6è primària: 33363) Resultats provisionals: Cobertura 1 D 89,1% Cobertura 2
IM cara anterolateral del muslo en los lactantes o el músculo deltoides de la parte superior del brazo en los niños.
 ESQUEMA CON VACUNAS ESPECIALES VACUNACION NO CUBIERTA POR EL PAN OBLIGATORIO DE SALUD Hepatitis B Anti hepatitis B A partir de los 5 º dosis en la fecha elegida. ª un mes después de la primera dosis. ª
ESQUEMA CON VACUNAS ESPECIALES VACUNACION NO CUBIERTA POR EL PAN OBLIGATORIO DE SALUD Hepatitis B Anti hepatitis B A partir de los 5 º dosis en la fecha elegida. ª un mes después de la primera dosis. ª
Vacuna frente al papilomavirus humano. (Comentarios a las fichas técnicas)
 Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
NORMATIVA VACUNAS HEPATITIS B. Departamento de Vacunas e Inmunizaciones Ministerio de Salud
 NORMATIVA VACUNAS HEPATITIS B Departamento de Vacunas e Inmunizaciones Ministerio de Salud Nuevas incorporaciones en trámite 2015 (Sujetos a modificaciones y aprobación por el Departamento de Asesoría
NORMATIVA VACUNAS HEPATITIS B Departamento de Vacunas e Inmunizaciones Ministerio de Salud Nuevas incorporaciones en trámite 2015 (Sujetos a modificaciones y aprobación por el Departamento de Asesoría
El reservorio es humano y el modo de transmisión es por vía aérea a través de las secreciones nasofaríngeas de la persona infectada.
 Información general Rubéola La rubéola es una infección vírica que es leve en los niños, pero tiene consecuencias graves en las embarazadas porque puede causar muerte fetal o defectos congénitos en el
Información general Rubéola La rubéola es una infección vírica que es leve en los niños, pero tiene consecuencias graves en las embarazadas porque puede causar muerte fetal o defectos congénitos en el
A través de los medios de comunicación tuvimos conocimiento de la retirada de un lote de vacunas de cáncer de cérvix.
 "Todos los seres humanos nacen libres e iguales en dignidad y derechos (...)". Art. 1 de la Declaración Universal de los DD HH "Tots els éssers humans naixen lliures i iguals en dignitat i drets (...)".
"Todos los seres humanos nacen libres e iguales en dignidad y derechos (...)". Art. 1 de la Declaración Universal de los DD HH "Tots els éssers humans naixen lliures i iguals en dignitat i drets (...)".
Los reservorios del virus de la rabia son fundamentalmente animales salvajes, como murciélagos y zorros y animales domésticos, como perros y gatos.
 Información general Rabia La rabia es una zoonosis viral. Es decir, una enfermedad propia de animales, causada por un virus y transmitida ocasionalmente al hombre por diversas especies animales. Se trata
Información general Rabia La rabia es una zoonosis viral. Es decir, una enfermedad propia de animales, causada por un virus y transmitida ocasionalmente al hombre por diversas especies animales. Se trata
Seguridad de las vacunas frente al virus del papiloma humano
 Seguridad de las vacunas frente al virus del papiloma humano Respuesta del Experto a Seguridad de las vacunas frente al virus del papiloma humano Pregunta Estoy haciendo un reportaje sobre las niñas que
Seguridad de las vacunas frente al virus del papiloma humano Respuesta del Experto a Seguridad de las vacunas frente al virus del papiloma humano Pregunta Estoy haciendo un reportaje sobre las niñas que
FICHA TÉCNICA. Polisacárido Vi de Salmonella typhi (cepa Ty2)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Typherix, solución inyectable en jeringa precargada Vacuna de polisacárido antitifoideo. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml de la vacuna
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Typherix, solución inyectable en jeringa precargada Vacuna de polisacárido antitifoideo. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml de la vacuna
Farmacovigilancia. Curso de Diplomado en Sanidad
 Farmacovigilancia Curso de Diplomado en Sanidad 2010 FARMACOVIGILANCIA Conjunto de procedimientos de detección, registro y evaluación de las reacciones adversas, para la determinación de su incidencia,
Farmacovigilancia Curso de Diplomado en Sanidad 2010 FARMACOVIGILANCIA Conjunto de procedimientos de detección, registro y evaluación de las reacciones adversas, para la determinación de su incidencia,
Efectividad y Seguridad después de 175 millones de dosis
 VACUNACION VPH Efectividad y Seguridad después de 175 millones de dosis Dra Mar Ramírez Mena Unidad Ginecología Oncológica y PTGI Hospital Clínico San Carlos. Madrid Conflicto de Intereses: Declaro haber
VACUNACION VPH Efectividad y Seguridad después de 175 millones de dosis Dra Mar Ramírez Mena Unidad Ginecología Oncológica y PTGI Hospital Clínico San Carlos. Madrid Conflicto de Intereses: Declaro haber
sobre Alertas de productos sanitarios, cosméticos y productos de higiene personal. Información dirigida a profesionales sanitarios
 Informe mensual sobre Medicamentos de Uso Humano y Productos Sanitarios Medicamentos Alertas de productos sanitarios, cosméticos y productos de higiene personal. Información dirigida a profesionales sanitarios
Informe mensual sobre Medicamentos de Uso Humano y Productos Sanitarios Medicamentos Alertas de productos sanitarios, cosméticos y productos de higiene personal. Información dirigida a profesionales sanitarios
Monitorización de la seguridad de las vacunas. José A Navarro Alonso Servicio de Prevención Consejería de Sanidad Murcia
 Monitorización de la seguridad de las vacunas José A Navarro Alonso Servicio de Prevención Consejería de Sanidad Murcia Indice Introducción Sistemas de vigilancia Tarjeta Amarilla Sistema Español de Farmacovigilancia
Monitorización de la seguridad de las vacunas José A Navarro Alonso Servicio de Prevención Consejería de Sanidad Murcia Indice Introducción Sistemas de vigilancia Tarjeta Amarilla Sistema Español de Farmacovigilancia
El sarampión puede producir epidemias que causan muchas muertes y meningoencefalitis, que puede dejar secuelas de retraso mental.
 Información general El sarampión El sarampión es una enfermedad muy contagiosa y grave causada por un virus. El único reservorio del mismo es humano, por lo que reúne todas las condiciones para ser eliminado
Información general El sarampión El sarampión es una enfermedad muy contagiosa y grave causada por un virus. El único reservorio del mismo es humano, por lo que reúne todas las condiciones para ser eliminado
3. TERMINOS Y DEFINICIONES:
 Página 1 de 6 1. OBJETIVOS. Este documento establece la metodología a seguir para la discusión, en los grupos de expertos de farmacovigilancia a todos los niveles de las sospechas de Reacción Adversa a
Página 1 de 6 1. OBJETIVOS. Este documento establece la metodología a seguir para la discusión, en los grupos de expertos de farmacovigilancia a todos los niveles de las sospechas de Reacción Adversa a
INFORME ANUAL ESAVI CALDAS 2014
 FO-GA-TD-01-001 03 CONTROLADA 1 DE 8 INFORME ANUAL ESAVI CALDAS 2014 INTRODUCCIÓN: Responsable: Luz Mery Arboleda de Chacón Médica salubrista Dirección Territorial de Salud de Caldas Un evento supuestamente
FO-GA-TD-01-001 03 CONTROLADA 1 DE 8 INFORME ANUAL ESAVI CALDAS 2014 INTRODUCCIÓN: Responsable: Luz Mery Arboleda de Chacón Médica salubrista Dirección Territorial de Salud de Caldas Un evento supuestamente
GRUPO DE TRABAJO DE ENFERMEDADES INFECCIOSAS Y VACUNAS INFORMACIÓN SOBRE VACUNAS NO FINANCIADAS
 INFORMACIÓN SOBRE VACUNAS NO FINANCIADAS VACUNA MENINGOCOCO B En la actualidad hay 2 vacunas frente a meningococo B: Bexsero (para uso a partir de los 2 meses de vida) y Trumemba (para uso a partir de
INFORMACIÓN SOBRE VACUNAS NO FINANCIADAS VACUNA MENINGOCOCO B En la actualidad hay 2 vacunas frente a meningococo B: Bexsero (para uso a partir de los 2 meses de vida) y Trumemba (para uso a partir de
Comunicación Dirigida a Profesionales Sanitarios. Madrid, 13 de Mayo 2013
 Madrid, 13 de Mayo 2013 Comunicación Dirigida a Profesionales Sanitarios Información importante respecto a las restricciones de utilización de ranelato de estroncio (Protelos /Osseor ) tras el análisis
Madrid, 13 de Mayo 2013 Comunicación Dirigida a Profesionales Sanitarios Información importante respecto a las restricciones de utilización de ranelato de estroncio (Protelos /Osseor ) tras el análisis
FICHA TÉCNICA. Polisacárido capsular Vi purificado de Salmonella typhi (cepa Ty2) microgramos
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO TYPHIM Vi, solución inyectable Vacuna antitifoidea de polisacáridos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml contiene: Polisacárido capsular
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO TYPHIM Vi, solución inyectable Vacuna antitifoidea de polisacáridos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml contiene: Polisacárido capsular
ARIPIPRAZOL En adolescentes contrastorno Bipolar I
 ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
SEGURIDAD VACUNAL X JORNADAS SOBRE VACUNAS EN ATENCIÓN PRIMARIA. Valencia, 22 y 23 de Octubre
 Dr. Eliseo Pastor Villalba Dirección General de Salud Pública Unidad de Coordinación y Promoción de la Salud e-mail: pastor_eli@gva.es SEGURIDAD VACUNAL X JORNADAS SOBRE VACUNAS EN ATENCIÓN PRIMARIA Valencia,
Dr. Eliseo Pastor Villalba Dirección General de Salud Pública Unidad de Coordinación y Promoción de la Salud e-mail: pastor_eli@gva.es SEGURIDAD VACUNAL X JORNADAS SOBRE VACUNAS EN ATENCIÓN PRIMARIA Valencia,
Informe Sistema Notificación de Efectos adversos supuestamente atribuibles a la vacunación o inmunización. Año 2015.
 Informe Sistema Notificación de Efectos adversos supuestamente atribuibles a la vacunación o inmunización. Año 2015. Unidad de Inmunizaciones, División Epidemiología - Unidad de Farmacovigilancia, Departamento
Informe Sistema Notificación de Efectos adversos supuestamente atribuibles a la vacunación o inmunización. Año 2015. Unidad de Inmunizaciones, División Epidemiología - Unidad de Farmacovigilancia, Departamento
Farmacovigilancia. Tipos de RAM. Morbilidad y mortalidad asociada al consumo de medicamentos.
 Notificación Espontánea de Reacciones Adversas a Medicamentos () Reacción Medicamento Adversa a Tipos de Cualquier respuesta a un medicamento que sea nociva y no intencionada Se produce a dosis utilizadas
Notificación Espontánea de Reacciones Adversas a Medicamentos () Reacción Medicamento Adversa a Tipos de Cualquier respuesta a un medicamento que sea nociva y no intencionada Se produce a dosis utilizadas
Prospecto: información para el usuario. Typhim Vi, solución inyectable. Vacuna antitifoidea de polisacáridos
 Prospecto: información para el usuario Typhim Vi, solución inyectable Vacuna antitifoidea de polisacáridos Lea todo el prospecto detenidamente antes de que usted o su hijo sea vacunado porque contiene
Prospecto: información para el usuario Typhim Vi, solución inyectable Vacuna antitifoidea de polisacáridos Lea todo el prospecto detenidamente antes de que usted o su hijo sea vacunado porque contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ditanrix Adulto suspensión inyectable Vacuna Antitétanos-difteria (Td)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ditanrix Adulto suspensión inyectable Vacuna Antitétanos-difteria (Td) 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Ditanrix Adulto contiene los toxoides de tétanos
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ditanrix Adulto suspensión inyectable Vacuna Antitétanos-difteria (Td) 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Ditanrix Adulto contiene los toxoides de tétanos
CALENDARIO DE VACUNACIONES DE LA ASOCIACIÓN ESPAÑOLA DE PEDIATRÍA Comité Asesor de Vacunas 2017
 1 de enero de 2017 Esta tabla indica el número de dosis necesarias, según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente.
1 de enero de 2017 Esta tabla indica el número de dosis necesarias, según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente.
NORMAS DE ACTUACIÓN ANTE LA APARICIÓN DE UN CASO HUMANO POR NUEVO VIRUS DE LA GRIPE A/H1N1*
 NORMAS DE ACTUACIÓN ANTE LA APARICIÓN DE UN CASO HUMANO POR NUEVO VIRUS DE LA GRIPE A/H1N1* DEFINICIÓN DE CASO (Esta definición está sujeta a actualización según se disponga de nueva información) Período
NORMAS DE ACTUACIÓN ANTE LA APARICIÓN DE UN CASO HUMANO POR NUEVO VIRUS DE LA GRIPE A/H1N1* DEFINICIÓN DE CASO (Esta definición está sujeta a actualización según se disponga de nueva información) Período
CIRCULAR de 31 de octubre de 2012 de la Dirección General de Salud Pública ACTUACIONES DEL PROGRAMA DE VACUNACIONES EN EDAD ESCOLAR. CURSO 2012/2013.
 CIRCULAR de 31 de octubre de 2012 de la Dirección General de Salud Pública ACTUACIONES DEL PROGRAMA DE VACUNACIONES EN EDAD ESCOLAR. CURSO 2012/2013. 1. JUSTIFICACIÓN 2. ORGANIZACIÓN 3. CRONOGRAMA CONTENIDO
CIRCULAR de 31 de octubre de 2012 de la Dirección General de Salud Pública ACTUACIONES DEL PROGRAMA DE VACUNACIONES EN EDAD ESCOLAR. CURSO 2012/2013. 1. JUSTIFICACIÓN 2. ORGANIZACIÓN 3. CRONOGRAMA CONTENIDO
ACTUALIZACIÓN DEL CALENDARIO DE VACUNACIÓN INFANTIL. Mayo 2018
 ACTUALIZACIÓN DEL CALENDARIO DE VACUNACIÓN INFANTIL Mayo 2018 La Instrucción de 8 de mayo de 2018 de la Dirección General de Salud Pública, ACTUALIZACIÓN DEL CALENDARIO DE VACUNACIÓN INFANTIL, establece
ACTUALIZACIÓN DEL CALENDARIO DE VACUNACIÓN INFANTIL Mayo 2018 La Instrucción de 8 de mayo de 2018 de la Dirección General de Salud Pública, ACTUALIZACIÓN DEL CALENDARIO DE VACUNACIÓN INFANTIL, establece
La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA
 La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA VARICELA Definición: La varicela es una enfermedad infecciosa causada por un virus llamado Varicela zoster (VVZ). Cuando se produce la reactivación
La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA VARICELA Definición: La varicela es una enfermedad infecciosa causada por un virus llamado Varicela zoster (VVZ). Cuando se produce la reactivación
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en jeringa precargada Vacuna antidiftero-tetánica (adsorbida) para adultos y adolescentes. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en jeringa precargada Vacuna antidiftero-tetánica (adsorbida) para adultos y adolescentes. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Capítulo 10 SEGURIDAD VACUNAL Y VIGILANCIA DE EFECTOS ADVERSOS DE LA VACUNACIÓN
 Capítulo 10 SEGURIDAD VACUNAL Y VIGILANCIA DE EFECTOS ADVERSOS DE LA VACUNACIÓN 10.1. EFECTOS ADVERSOS ASOCIADOS A LAS VACUNAS Las vacunas son productos biológicos compuestos por antígeno/s (único o múltiples)
Capítulo 10 SEGURIDAD VACUNAL Y VIGILANCIA DE EFECTOS ADVERSOS DE LA VACUNACIÓN 10.1. EFECTOS ADVERSOS ASOCIADOS A LAS VACUNAS Las vacunas son productos biológicos compuestos por antígeno/s (único o múltiples)
El reservorio de los virus es exclusivamente humano, no existiendo reservorio animal ni vectores implicados.
 Información general Parotiditis La parotiditis es una enfermedad transmisible causada por un agente viral, el virus de la Parotiditis, de la familia Paramyxovirus. La primera manifestación clara y más
Información general Parotiditis La parotiditis es una enfermedad transmisible causada por un agente viral, el virus de la Parotiditis, de la familia Paramyxovirus. La primera manifestación clara y más
FICHA TECNICA. Adultos en prediálisis o en diálisis: 1 dosis (40 µg) de 1 ml en cada inyección.
 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 40 mg Vacuna recombinante antihepatitis B. FICHA TECNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 40microgramos/ ml, suspensión inyectable
1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 40 mg Vacuna recombinante antihepatitis B. FICHA TECNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 40microgramos/ ml, suspensión inyectable
FICHA TÉCNICA. Toxoide diftérico purificado... una dosis inmunizante* Toxoide tetánico purificado...una dosis inmunizante**
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO D.T.VAX Vacuna antidiftero-tetánica adsorbida. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Toxoide diftérico purificado... una dosis inmunizante* Toxoide tetánico
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO D.T.VAX Vacuna antidiftero-tetánica adsorbida. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Toxoide diftérico purificado... una dosis inmunizante* Toxoide tetánico
GARDASIL, UNA VACUNA FRENTE A PAPILOMA HUMANO
 GARDASIL, UNA VACUNA FRENTE A PAPILOMA HUMANO En España, la vacunación frente al virus del papiloma humano (VPH) se ha iniciado durante 2007. Cada Comunidad Autónoma ha decidido el grupo de edad de niñas
GARDASIL, UNA VACUNA FRENTE A PAPILOMA HUMANO En España, la vacunación frente al virus del papiloma humano (VPH) se ha iniciado durante 2007. Cada Comunidad Autónoma ha decidido el grupo de edad de niñas
MINISTERIO DE SALUD PUBLICA CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA
 Acciones a desarrollar en el sistema cubano de PNO: 001 Página 1 de 7 1. OBJETIVO. El presente procedimiento establece la metodología a seguir en caso de notificación de sospecha de reacción adversa de
Acciones a desarrollar en el sistema cubano de PNO: 001 Página 1 de 7 1. OBJETIVO. El presente procedimiento establece la metodología a seguir en caso de notificación de sospecha de reacción adversa de
GRUPO DE TRABAJO DE ENFERMEDADES INFECCIOSAS Y VACUNAS
 Vacunas recomendadas no financiadas: VACUNA MENINGOCOCO B (Bexsero ): Según la ficha técnica, está indicada para la inmunización activa a partir de los 2 meses de edad frente a la enfermedad meningocócica
Vacunas recomendadas no financiadas: VACUNA MENINGOCOCO B (Bexsero ): Según la ficha técnica, está indicada para la inmunización activa a partir de los 2 meses de edad frente a la enfermedad meningocócica
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION
 SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
Vacunas hexavalentes y muerte súbita
 Vacunas hexavalentes y muerte súbita Respuesta del Experto a Vacunas hexavalentes y muerte súbita Pregunta Quisiera saber qué hay de cierto sobre la vacuna hexavalente (DTPa+Hib+Hp B+VPI), si es segura
Vacunas hexavalentes y muerte súbita Respuesta del Experto a Vacunas hexavalentes y muerte súbita Pregunta Quisiera saber qué hay de cierto sobre la vacuna hexavalente (DTPa+Hib+Hp B+VPI), si es segura
GRUPO DE TRABAJO DE ENFERMEDADES INFECCIOSAS Y VACUNAS VACUNAS NO FINANCIADAS RECOMENDADAS
 VACUNAS NO FINANCIADAS RECOMENDADAS VACUNA MENINGOCOCO B En la actualidad hay 2 vacunas frente a meningococo B: Bexsero (para uso a partir de los 2 meses de vida) y Trumemba (para uso partir de 10 años
VACUNAS NO FINANCIADAS RECOMENDADAS VACUNA MENINGOCOCO B En la actualidad hay 2 vacunas frente a meningococo B: Bexsero (para uso a partir de los 2 meses de vida) y Trumemba (para uso partir de 10 años
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO CORREO ELECTRÓNICO Sugerencias_ft@aemps.es C/ CAMPEZO, 1 EDIFICIO 8 28022 MADRID 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO CORREO ELECTRÓNICO Sugerencias_ft@aemps.es C/ CAMPEZO, 1 EDIFICIO 8 28022 MADRID 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en
* cultivados en huevos de gallina embrionados procedentes de pollos sanos ** hemaglutinina
 1. NOMBRE DEL MEDICAMENTO LEVRISON, suspensión inyectable en jeringa precargada. Vacuna antigripal (virus fraccionados, inactivados) 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Virus de la gripe fraccionados*,
1. NOMBRE DEL MEDICAMENTO LEVRISON, suspensión inyectable en jeringa precargada. Vacuna antigripal (virus fraccionados, inactivados) 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Virus de la gripe fraccionados*,
NÚMERO DE DOSIS RECOMENDADO DE CADA VACUNA SEGÚN LA EDAD Asociación Española de Pediatría 2015 Comité Asesor de Vacunas.
 1 de enero de 2015 Esta tabla indica el número de necesarias según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se
1 de enero de 2015 Esta tabla indica el número de necesarias según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se
Generalitat de Catalunya Departamento de Salud Dirección General de Salud Pública
 828 Barcelona Tel 93 22 29 Fax 93 22 29 9 Informe sobre la situación del sarampión en Catalunya. Actualización 25 En septiembre de 1998, el Comité de Expertos en Vacunaciones del Departamento de Sanidad
828 Barcelona Tel 93 22 29 Fax 93 22 29 9 Informe sobre la situación del sarampión en Catalunya. Actualización 25 En septiembre de 1998, el Comité de Expertos en Vacunaciones del Departamento de Sanidad
CALENDARIO DE VACUNACIONES DE LA ASOCIACIÓN ESPAÑOLA DE PEDIATRÍA Comité Asesor de Vacunas 2014
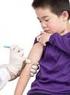 1 Esta tabla indica el número de necesarias, según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se ha de reiniciar
1 Esta tabla indica el número de necesarias, según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se ha de reiniciar
GRUPO DE TRABAJO DE ENFERMEDADES INFECCIOSAS Y VACUNAS
 La manifiesta su satisfacción por la decisión de las Autoridades Sanitarias de incluir en calendario la vacuna contra la varicela en la primera infancia, así como la decisión de permitir la venta en farmacias
La manifiesta su satisfacción por la decisión de las Autoridades Sanitarias de incluir en calendario la vacuna contra la varicela en la primera infancia, así como la decisión de permitir la venta en farmacias
sobre Alertas de productos sanitarios, cosméticos y productos de higiene personal. Información dirigida a profesionales sanitarios
 Informe mensual sobre Medicamentos de Uso Humano y Productos Sanitarios Medicamentos Alertas de productos sanitarios, cosméticos y productos de higiene personal. Información dirigida a profesionales sanitarios
Informe mensual sobre Medicamentos de Uso Humano y Productos Sanitarios Medicamentos Alertas de productos sanitarios, cosméticos y productos de higiene personal. Información dirigida a profesionales sanitarios
Conceptos Jurídicos y Normativa sobre las RAM de uso humano en España
 Conceptos Jurídicos y Normativa sobre las RAM de uso humano en España Vamos a realizar una muy breve aproximación a conceptos jurídicos y normativa asociada a las Reacciones Adversas a los Medicamentos
Conceptos Jurídicos y Normativa sobre las RAM de uso humano en España Vamos a realizar una muy breve aproximación a conceptos jurídicos y normativa asociada a las Reacciones Adversas a los Medicamentos
FICHA TÉCNICA. no menos de 20 Unidades Internaciones (UI) (5 Lf) 1adsorbidos en hidróxido de aluminio hidratado (Al(OH)3)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Boostrix suspensión inyectable en jeringa precargada Vacuna antidiftérica, antitetánica y antitos ferina (componente acelular) (adsorbida, contenido antigénico reducido)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Boostrix suspensión inyectable en jeringa precargada Vacuna antidiftérica, antitetánica y antitos ferina (componente acelular) (adsorbida, contenido antigénico reducido)
EVENTO SUPUESTAMENTE ATRIBUIDO A VACUNACIÓN O INMUNIZACIÓN ESAVI
 En el contexto de la vigilancia epidemiológica, el término o evento supuestamente atribuido a vacunación o inmunización, se utiliza para referirse a cualquier evento clínico que se presenta luego de la
En el contexto de la vigilancia epidemiológica, el término o evento supuestamente atribuido a vacunación o inmunización, se utiliza para referirse a cualquier evento clínico que se presenta luego de la
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. RECOMBIVAX HB 5 mg Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 5 mg Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 5 microgramos/ 0,5 ml, suspensión inyectable
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 5 mg Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 5 microgramos/ 0,5 ml, suspensión inyectable
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. RECOMBIVAX HB 10 mg jeringa precargada Vacuna recombinante antihepatitis B.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 10 mg jeringa precargada Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 10 microgramos /
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 10 mg jeringa precargada Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 10 microgramos /
VACUNACIÓN FRENTE A MENINGOCOCO B (BEXSERO ) Tatiana Amil Pena MIR-4 Pediatría
 VACUNACIÓN FRENTE A MENINGOCOCO B (BEXSERO ) Tatiana Amil Pena MIR-4 Pediatría ÍNDICE Introducción: el meningococo y la enfermedad meningocócica Vacunación frente al meningococo B: Vacuna frente a meningococo
VACUNACIÓN FRENTE A MENINGOCOCO B (BEXSERO ) Tatiana Amil Pena MIR-4 Pediatría ÍNDICE Introducción: el meningococo y la enfermedad meningocócica Vacunación frente al meningococo B: Vacuna frente a meningococo
Informe de Puesta al Día del 16 de noviembre de 2009 al 11 de enero de 2010
 SUBDIRECCIÓN GENERAL DE MEDICAMENTOS DE USO HUMANO Informe sobre sospechas de reacciones adversas asociadas a las vacunas pandémicas frente a la gripe A/H1N1 notificadas al Sistema Español de Farmacovigilancia
SUBDIRECCIÓN GENERAL DE MEDICAMENTOS DE USO HUMANO Informe sobre sospechas de reacciones adversas asociadas a las vacunas pandémicas frente a la gripe A/H1N1 notificadas al Sistema Español de Farmacovigilancia
18 de Agosto del 2016 SEÑOR (A) DIRECTOR(A) COLEGIO PRESENTE
 18 de Agosto del 2016 SEÑOR (A) DIRECTOR(A) COLEGIO PRESENTE Junto con saludar, informo a usted en relación a la Vacunación Escolar del presente año, está dirigida a alumnos de los siguientes cursos: 1
18 de Agosto del 2016 SEÑOR (A) DIRECTOR(A) COLEGIO PRESENTE Junto con saludar, informo a usted en relación a la Vacunación Escolar del presente año, está dirigida a alumnos de los siguientes cursos: 1
PNO: 003 Página 1 de 6 Aprobado por: Dr Julián Pérez Peña Edición: 01 Cargo: Director Fecha:
 Página 1 de 6 Este documento establece la metodología a seguir para el análisis de las sospechas de Reacción Adversa a Medicamentos (RAM) no descritas en el Formulario Nacional de Medicamentos. 1. OBJETIVOS.
Página 1 de 6 Este documento establece la metodología a seguir para el análisis de las sospechas de Reacción Adversa a Medicamentos (RAM) no descritas en el Formulario Nacional de Medicamentos. 1. OBJETIVOS.
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
ANEXO III SECCIONES RELEVANTES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO, ETIQUETADO Y PROSPECTO
 ANEXO III SECCIONES RELEVANTES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO, ETIQUETADO Y PROSPECTO Nota: Estas modificaciones del Resumen de las Características del Producto y del prospecto son las
ANEXO III SECCIONES RELEVANTES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO, ETIQUETADO Y PROSPECTO Nota: Estas modificaciones del Resumen de las Características del Producto y del prospecto son las
PROGRAMA DE PREVENCIÓN Y VIGILANCIA DE LA GRIPE EN LA COMUNIDAD VALENCIANA.
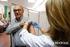 PROGRAMA DE PREVENCIÓN Y VIGILANCIA DE LA GRIPE EN LA COMUNIDAD VALENCIANA. OBJETIVOS. 1. Prevenir las complicaciones y la mortalidad secundarias a la gripe en los grupos de riesgo especialmente susceptibles
PROGRAMA DE PREVENCIÓN Y VIGILANCIA DE LA GRIPE EN LA COMUNIDAD VALENCIANA. OBJETIVOS. 1. Prevenir las complicaciones y la mortalidad secundarias a la gripe en los grupos de riesgo especialmente susceptibles
Para obtener más información sobre el VPH y la vacunación, consulte el dictamen del Comité ACOG: Vacunación con Papilomavirus Humano
 La vacuna contra el VPH es una de las mejores maneras de proteger a las mujeres del cáncer de cuello uterino en el futuro. En los Estados Unidos, la prevalencia de VPH tipo vacuna disminuyó 56% entre las
La vacuna contra el VPH es una de las mejores maneras de proteger a las mujeres del cáncer de cuello uterino en el futuro. En los Estados Unidos, la prevalencia de VPH tipo vacuna disminuyó 56% entre las
Registro y Notificación de acontecimientos y reacciones adversas durante el Ensayo Clínico.
 Registro y Notificación de acontecimientos y reacciones adversas durante el Ensayo Clínico. Dr. Eduardo Fernández Quintana Centro de Farmacovigilancia e Información Terapéutica de Canarias de Canarias.
Registro y Notificación de acontecimientos y reacciones adversas durante el Ensayo Clínico. Dr. Eduardo Fernández Quintana Centro de Farmacovigilancia e Información Terapéutica de Canarias de Canarias.
FÓRMULA CUALI CUANTITATIVA:
 VACUNAANTIGRIPAL VENTABAJORECETA FORMAFARMACÉUTICA: Suspensióninyectableporvíaintramuscular(jeringaprellenadade0,5ml) FÓRMULACUALI CUANTITATIVA: Cadajeringaprellenadade0,5mlcontiene: Antigenosdehemoaglutininayneuraminidasasdelassiguientescepasdevirusinfluenza:
VACUNAANTIGRIPAL VENTABAJORECETA FORMAFARMACÉUTICA: Suspensióninyectableporvíaintramuscular(jeringaprellenadade0,5ml) FÓRMULACUALI CUANTITATIVA: Cadajeringaprellenadade0,5mlcontiene: Antigenosdehemoaglutininayneuraminidasasdelassiguientescepasdevirusinfluenza:
FICHA TÉCNICA. Esta vacuna cumple con la recomendación de la OMS (Hemisferio Norte) y con la decisión de la Unión Europea para la campaña 2017/2018.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VAXIGRIP, suspensión inyectable en jeringa precargada. Vacuna antigripal (virus fraccionados, inactivados). 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Virus de la
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VAXIGRIP, suspensión inyectable en jeringa precargada. Vacuna antigripal (virus fraccionados, inactivados). 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Virus de la
CALENDARIO DE VACUNACIONES DE LA AEP PARA EL AÑO 2015
 CALENDARIO DE VACUNACIONES DE LA AEP PARA EL AÑO 2015 El Comité Asesor de Vacunas (CAV) de la Asociación Española de Pediatría (AEP) actualiza sus recomendaciones de vacunación, en la infancia y la adolescencia,
CALENDARIO DE VACUNACIONES DE LA AEP PARA EL AÑO 2015 El Comité Asesor de Vacunas (CAV) de la Asociación Española de Pediatría (AEP) actualiza sus recomendaciones de vacunación, en la infancia y la adolescencia,
Vacunación frete al virus del papiloma humano
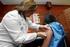 Vacunación frete al virus del papiloma humano Dra. Sonia Tamames Jefe de Servicio de Epidemiología y Promoción de la Salud. Dirección General de Salud Pública de Castilla y León. Virus del Papiloma Humano
Vacunación frete al virus del papiloma humano Dra. Sonia Tamames Jefe de Servicio de Epidemiología y Promoción de la Salud. Dirección General de Salud Pública de Castilla y León. Virus del Papiloma Humano
Prospecto: información para el usuario. PNEUMO 23, solución inyectable en jeringa precargada Vacuna antineumocócica de polisacáridos
 Prospecto: información para el usuario PNEUMO 23, solución inyectable en jeringa precargada Vacuna antineumocócica de polisacáridos Lea todo el prospecto detenidamente antes de que usted o su hijo sean
Prospecto: información para el usuario PNEUMO 23, solución inyectable en jeringa precargada Vacuna antineumocócica de polisacáridos Lea todo el prospecto detenidamente antes de que usted o su hijo sean
FICHA TÉCNICA. Suspensión inyectable en jeringa precargada. La vacuna antihepatitis A (inactivada, adsorbida) es una suspensión blanca y turbia.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Avaxim, suspensión inyectable en jeringa precargada Vacuna antihepatitis A (inactivada, adsorbida) 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Una dosis de 0,5 mililitros
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Avaxim, suspensión inyectable en jeringa precargada Vacuna antihepatitis A (inactivada, adsorbida) 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Una dosis de 0,5 mililitros
PROSPECTO. CANIGEN DHPPi liofilizado y solvente para suspensión inyectable para perros
 DEPARTAMENTO MEDICAMENTOS VETERINARIOS DE PROSPECTO CANIGEN DHPPi liofilizado y solvente para suspensión inyectable para perros 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN
DEPARTAMENTO MEDICAMENTOS VETERINARIOS DE PROSPECTO CANIGEN DHPPi liofilizado y solvente para suspensión inyectable para perros 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN
Recomendaciones para la no utilización de hormona del crecimiento en la recuperación de enfermedades neurológicas cerebrales y periféricas.
 Pág. 1 de 6 Recomendaciones para la no utilización de hormona del crecimiento en la recuperación de enfermedades neurológicas cerebrales y periféricas. El objetivo de esta alerta internacional es difundir
Pág. 1 de 6 Recomendaciones para la no utilización de hormona del crecimiento en la recuperación de enfermedades neurológicas cerebrales y periféricas. El objetivo de esta alerta internacional es difundir
CONTRIBUCIÓN DE LA ENFERMERÍA EN EL PROCESO VACUNAL. Visite la página:
 CONTRIBUCIÓN DE LA ENFERMERÍA EN EL PROCESO VACUNAL. Visite la página: http://www.saludcastillayleon.es/profesionales/es/vacunaciones ACTO VACUNAL CONJUNTO DE PROTOCOLOS, PROCESOS Y TÉCNICAS QUE SE APLICAN
CONTRIBUCIÓN DE LA ENFERMERÍA EN EL PROCESO VACUNAL. Visite la página: http://www.saludcastillayleon.es/profesionales/es/vacunaciones ACTO VACUNAL CONJUNTO DE PROTOCOLOS, PROCESOS Y TÉCNICAS QUE SE APLICAN
Guía para la interpretación de informes espontáneos de presuntas reacciones adversas a medicamentos
 30 de enero de 2017 Inspecciones, Farmacovigilancia de Medicamentos de Uso Humano y Comités EMA/749446/2016 Revisión 1* Guía para la interpretación de informes espontáneos de presuntas reacciones adversas
30 de enero de 2017 Inspecciones, Farmacovigilancia de Medicamentos de Uso Humano y Comités EMA/749446/2016 Revisión 1* Guía para la interpretación de informes espontáneos de presuntas reacciones adversas
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. DENOMINACIÓN DEL MEDICAMENTO Gardasil suspensión inyectable. Vacuna frente al Virus del Papiloma Humano [Tipos 6, 11, 16, 18] (Recombinante, adsorbida).
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. DENOMINACIÓN DEL MEDICAMENTO Gardasil suspensión inyectable. Vacuna frente al Virus del Papiloma Humano [Tipos 6, 11, 16, 18] (Recombinante, adsorbida).
Vacunación en la escuela: Qué está pasando con el Programa de Salut Escolar en Girona?
 Vacunación en la escuela: Qué está pasando con el Programa de Salut Escolar en Girona? Autores: M. Gassiot, N. Camps, M. Danés, A. Quer. Unidad de Vigilancia Epidemiológica de los Servicios Territoriales
Vacunación en la escuela: Qué está pasando con el Programa de Salut Escolar en Girona? Autores: M. Gassiot, N. Camps, M. Danés, A. Quer. Unidad de Vigilancia Epidemiológica de los Servicios Territoriales
Boletín Informativo de Farmacovigilancia de Ceuta nª 7, jul/2009
 SUMARIO: 1. Resultados del Sistema Español de Farmacovigilancia (SEFV-H) en 2007 y 2008. 2. Posible Interacción de clopidogrel (Plavix, Iscover ) con los inhibidores de la bomba de protones. 3. Seguridad
SUMARIO: 1. Resultados del Sistema Español de Farmacovigilancia (SEFV-H) en 2007 y 2008. 2. Posible Interacción de clopidogrel (Plavix, Iscover ) con los inhibidores de la bomba de protones. 3. Seguridad
Prospecto: información para el usuario. Ditanrix Adulto suspensión inyectable. Vacuna antitétanos-difteria
 Prospecto: información para el usuario Ditanrix Adulto suspensión inyectable Vacuna antitétanos-difteria Lea todo el prospecto detenidamente antes de empezar a recibir esta vacuna. - Conserve este prospecto,
Prospecto: información para el usuario Ditanrix Adulto suspensión inyectable Vacuna antitétanos-difteria Lea todo el prospecto detenidamente antes de empezar a recibir esta vacuna. - Conserve este prospecto,
04 de agosto 2015 SEÑOR (A) DIRECTOR(A) COLEGIO PRESENTE
 04 de agosto 2015 SEÑOR (A) DIRECTOR(A) COLEGIO PRESENTE Junto con saludar, informo a usted en relación a la Vacunación Escolar del presente año, esta estará dirigida a alumnos de los siguientes cursos:
04 de agosto 2015 SEÑOR (A) DIRECTOR(A) COLEGIO PRESENTE Junto con saludar, informo a usted en relación a la Vacunación Escolar del presente año, esta estará dirigida a alumnos de los siguientes cursos:
Prospecto: información para el usuario
 Prospecto: información para el usuario Doxium Fuerte 500 mg cápsulas duras Dobesilato de calcio Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
Prospecto: información para el usuario Doxium Fuerte 500 mg cápsulas duras Dobesilato de calcio Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Boostrix suspensión inyectable en jeringa precargada Vacuna antidiftérica, antitetánica y antitos ferina (componente acelular) (adsorbida, contenido antigénico reducido)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Boostrix suspensión inyectable en jeringa precargada Vacuna antidiftérica, antitetánica y antitos ferina (componente acelular) (adsorbida, contenido antigénico reducido)
Fluarix Tetra. Vacuna antigripal tetravalente (virión fraccionado inactivado) suspensión inyectable
 Fluarix Tetra Vacuna antigripal tetravalente (virión fraccionado inactivado) suspensión inyectable COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Fluarix Tetra es una vacuna antigripal inactivada (virión fraccionado),
Fluarix Tetra Vacuna antigripal tetravalente (virión fraccionado inactivado) suspensión inyectable COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Fluarix Tetra es una vacuna antigripal inactivada (virión fraccionado),
Mitos, creencias y coberturas vacunales: el caso de la vacuna frente al VPH
 Mitos, creencias y coberturas vacunales: el caso de la vacuna frente al VPH Jaime García Aguado CS Villablanca Madrid Grupo PrevInfad Mis conflictos de intereses Con la Administración pública: relación
Mitos, creencias y coberturas vacunales: el caso de la vacuna frente al VPH Jaime García Aguado CS Villablanca Madrid Grupo PrevInfad Mis conflictos de intereses Con la Administración pública: relación
FICHA TÉCNICA FLUAD. 1. Denominación distintiva FLUAD. 2. Denominación genérica Vacuna anti-influenza trivalente tipo A y B
 1. Denominación distintiva 2. Denominación genérica Vacuna anti-influenza trivalente tipo A y B 3. Composición cualitativa y cuantitativa A/California/7/2009 (H1N1)pdm09 A/Texas/50/2012 (H3N2) B/Massachusetts/02/2012
1. Denominación distintiva 2. Denominación genérica Vacuna anti-influenza trivalente tipo A y B 3. Composición cualitativa y cuantitativa A/California/7/2009 (H1N1)pdm09 A/Texas/50/2012 (H3N2) B/Massachusetts/02/2012
Anexo III. Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto
 Anexo III Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto Nota: Esta Ficha Técnica, Etiquetado y Prospecto son el resultado del proceso de arbitraje.
Anexo III Correcciones a las secciones relevantes del resumen de las características del producto y del prospecto Nota: Esta Ficha Técnica, Etiquetado y Prospecto son el resultado del proceso de arbitraje.
FICHA TÉCNICA. Virus de la gripe fraccionados*, inactivados, que contienen antígenos equivalentes a:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VACUNA ANTIGRIPAL POLIVALENTE LETI VIRUS FRACCIONADOS SUSPENSIÓN INYECTABLE EN JERINGA PRECARGADA. Vacuna antigripal de virus fraccionados inactivados. 2. COMPOSICIÓN
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VACUNA ANTIGRIPAL POLIVALENTE LETI VIRUS FRACCIONADOS SUSPENSIÓN INYECTABLE EN JERINGA PRECARGADA. Vacuna antigripal de virus fraccionados inactivados. 2. COMPOSICIÓN
UTILIZACIÓN DEL REGISTRO DE VACUNAS PARA LA REALIZACIÓN DE UNA CAMPAÑA DE BARRIDO CON VACUNA TRIPLE VÍRICA
 4º CONGRESO NACIONAL DE LA ASOCIACIÓN ESPAÑOLA DE VACUNOLOGÍA Valencia UTILIZACIÓN DEL REGISTRO DE VACUNAS PARA LA REALIZACIÓN DE UNA CAMPAÑA DE BARRIDO CON VACUNA TRIPLE VÍRICA Programas de Vacunaciones
4º CONGRESO NACIONAL DE LA ASOCIACIÓN ESPAÑOLA DE VACUNOLOGÍA Valencia UTILIZACIÓN DEL REGISTRO DE VACUNAS PARA LA REALIZACIÓN DE UNA CAMPAÑA DE BARRIDO CON VACUNA TRIPLE VÍRICA Programas de Vacunaciones
Anexo IV. Conclusiones científicas
 Anexo IV Conclusiones científicas 1 Conclusiones científicas Se han notificado cuatro casos de lesión hepática grave que condujo a un trasplante hepático desde la autorización de comercialización de Esmya.
Anexo IV Conclusiones científicas 1 Conclusiones científicas Se han notificado cuatro casos de lesión hepática grave que condujo a un trasplante hepático desde la autorización de comercialización de Esmya.
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO PANENZA suspensión inyectable en jeringa precargada Vacuna antigripal (H1N1)v (virus fraccionado inactivado)
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO PANENZA suspensión inyectable en jeringa precargada Vacuna antigripal (H1N1)v (virus fraccionado inactivado)
