TEMA 1.- CONCEPTOS PRELIMINARES
|
|
|
- Francisco Javier Palma Iglesias
- hace 9 años
- Vistas:
Transcripción
1 TEMA 1.- CONCEPTOS PRELIMINARES 1. Introducción. 2. El método científico. 3. Cambios físicos y químicos. 4. Materia y masa. 5. Sustancias, elementos, compuestos y mezclas. 6. Energía y Fuerza 7. Los símbolos y la tabla periódica. 8. Átomos, moléculas e iones. 9. La medición en Química. Unidades del SI. Conversión de unidades. Incertidumbre en la medición y expresión de resultados. Medición de longitud, masa, tiempo, temperatura y unidades derivadas. Masas atómicas y masas fórmula. Cantidad de sustancia: mol, masa molar, número de Avogadro. 10. Estequiometría. La ley de conservación de masa. Las ecuaciones químicas y cálculos estequiométricos. Rendimiento de las reacciones químicas. Determinación de las fórmulas empíricas a partir de la composición. Fórmulas moleculares y estructurales. 1
2 1.- INTRODUCCIÓN Qué es la Química? La Química es una rama de la Ciencia que tiene por objeto el estudio de la materia, sus transformaciones y las correspondientes variaciones de energía que las acompañan Evolución histórica de la Química Importancia de la Química en nuestros días Enfoques de la Química Macroscópico Microscópico Simbólico 2
3 2.- EL MÉTODO CIENTÍFICO. ETAPAS: 1. Definir con claridad el problema. 2. Observación Hacer observaciones cuidadosas Recopilar información Datos o Cualitativa o Cuantitativa 3. Formulación de una LEY. LEY- Enunciado verbal o matemático conciso que expresa relaciones invariables entre fenómenos que siempre se repiten bajo las mismas condiciones. 4. Formulación de una HIPÓTESIS. HIPÓTESIS- Explicación tentativa del conjunto de observaciones. 5. TEORÍA. Principio unificador que explica un grupo de hechos y aquellas leyes que se basan en éstos. 6. MODELO. Estrategia que permite explicar con facilidad la teoría 3
4 2.- EL MÉTODO CIENTÍFICO. Observación (datos) Experimento (comprobación de predicciones) Ley (generalización) Teoría Modelo (explicación) Hipótesis (Predicción) 4
5 3.- CAMBIOS FÍSICOS Y QUÍMICOS. Cambio Químico: Con cambio en la naturaleza de la materia PROPIEDADES QUÍMICAS: (acidez, basicidad, carácter reductor, etc) Cambio Físico: Sin cambio en la naturaleza de la materia PROPIEDADES FÍSICAS: (Color, Peb, densidad) 5
6 4.- MATERIA Y MASA Cantidad de materia masa o volumen Propiedades de la materia Intensivas no dependen de la cantidad de materia (δ, n, etc) Extensivas dependen de la cantidad de materia (m, V, etc) Físicas sin cambio en la naturaleza de la materia (color, P.eb., etc.) Químicas con cambio en la naturaleza de la materia (acidez, basicidad, carácter reductor, etc) Isotropía una propiedad no depende de la dirección de medida Estados de agregación n de la Materia 6
7 5.- ENERGÍA Qué es la energía? Es la capacidad de hacer trabajo Energía Mecánica Cinética (E k ), potencial (E p ) Energía Electromagnética Energía Térmica Etc. Calor y temperatura Calor energía en tránsito Exotérmico se desprende calor Endotérmico se absorbe calor Gravitatoria Electrostática Unidades Joule Temperatura mide Ec promedio de partículas 7
8 6.- SUSTANCIAS, ELEMENTOS, COMPUESTOS Y MEZCLAS Clasificación de la materia MATERIA MATERIA Sustancias Sustancias Puras Puras Composición Composición fija fija No No pueden pueden separarse separarse por por medios medios físicos físicos temperatura temperatura constante constante durante durante el el cambio cambio de de estado estado Mezclas Mezclas Composición Composición variable variable Pueden separarse Pueden por separarse medios por físicos medios físicos Temperatura Temperatura variable variable o o múltiple múltiple durante durante el el cambio cambio de de fase fase Elementos Elementos Sustancias puras más Sustancias puras más simples simples No No pueden pueden descomponerse descomponerse Compuestos Compuestos Sustancias puras formadas Sustancias puras formadas por por dos dos o o más más elementos elementos Pueden Pueden descomponerse descomponerse (separarse por medios (separarse por medios químicos) químicos) Mezclas Mezclas homogéneas homogéneas (Disoluciones) (Disoluciones) Poseen Poseen 2 2 ó ó más más componentes componentes Fase Fase simple simple Mezclas Mezclas heterogéneas heterogéneas Poseen 2 ó más Poseen 2 ó más componentes componentes 2 2 ó ó más más fases fases 8
9 6.- SUSTANCIAS, ELEMENTOS, COMPUESTOS Y MEZCLAS Purificación n e identificación n de sustancias Separación (Purificación) Destilación, extracción Decantación, Filtración, Cromatografía, Identificación Análisis, síntesis 9
10 7.- ÁTOMOS, MOLÉCULAS E IONES. ÁTOMO: Según la teoría atómica de Dalton, es la unidad básica de un elemento que puede intervenir en una combinación química. -Electrones -Protones Isótopos (espectrometría de masas) -Neutrones Símbolo A Z MOLÉCULAS: Conjunto de al menos dos átomos que se mantienen unidos a través de enlaces químicos dando lugar a una entidad eléctricamente neutra. Ej. H2, O2, HCl, CO,... IONES: Átomos o grupos de átomos enlazados que tienen una carga neta positiva o negativa. Cationes. Aniones. 10
11 8.- LOS SÍMBOLOS Y LA TABLA PERIÓDICA. Tabla periódica tomada del enlace: 11
12 9.- LA MEDICIÓN EN QUÍMICA Unidades básicas del S.I. Unidades básicas del Sistema Internacional Propiedad física Nombre de la unidad Longitud Metro m Símbolo Masa Kilogramo kg Tiempo Segundo s Corriente eléctrica Amperio A Temperatura Kelvin K Intensidad luminosa Candela cd Cantidad de sustancia Mol mol Prefijos utilizados con unidades SI Prefijo Símbolo Significado Ejemplo Tera T terametro(tm)=1x10 12 m Giga G gigametro(gm)=1x10 9 m Mega M megametro(Mm)= 1x10 6 m. Kilo K kilómetro(km) = 1x10 3 m. deci d decímetro(dm) = 1x10-1 m centi c centímetro(cm)= 1x10-2 m mili m milímetro(mm) = 1x10-3 m. micro µ micrómetro(µm) =1x10-6 m nano n nanómetro(nm) = 1x10-9 m pico p picómetro(pm) = 1x10-12 m fempto f femptometro(fm) = 1x10-15 m 12
13 9.- LA MEDICIÓN EN QUÍMICA Unidades derivadas Propiedad física Unidades derivadas Nombre de la unidad Símbolo Área Metro cuadrado m 2 Volumen Metro cúbico m 3 Densidad Kilogramo por metro cúbico kg/m 3. Fuerza Newton N (kg.m/s 2 ) Presión Pascal Pa (N.m -2 ) Energía Julio J (kg m 2 s -2 ) Carga eléctrica Coulombio C (A.s) Diferencia de potencial Voltio V (J.C -1 ) Resistencia Ohmio Ω (V.A -1 ) 13
14 9.- LA MEDICIÓN EN QUÍMICA Conversión de unidades Ejemplo: 3 1 kg 1 cm = kg m = 1,05 10 kg m 3-2 g 10,5 cm 1000 g 1 10 m Incertidumbre en la medición y expresión de resultados Notación Científica: N 10 n Cifras significativas: Dígitos que sirven para establecer el valor de una medida 1. Cualquier dígito distinto de cero. 2. Los ceros ubicados entre dos cifras significativas 3. Un número mayor o igual que uno 4. Todos los ceros a la derecha son significativos. 400 : 1,2 o 3 cifras significativas cifra significativa 4, cifras significativas 4, cifras significativas 14
15 9.- LA MEDICIÓN EN QUÍMICA. 5. Adición y sustracción. 6. Multiplicación o división. Aproximación y redondeo Parámetros estadísticos: Media arimética: Se obtiene al dividir la suma de todas las observaciones por el número de observaciones. Mediana: Es el valor que ocupa el lugar central cuando todos los valores observados se ordenan en sentido creciente o decreciente. Moda: es el valor de la variable que más veces se repite. Distribución Normal: 15
16 9.- LA MEDICIÓN EN QUÍMICA. Exactitud y Precisión: Exactitud: Indica la veracidad de un dato en sentido absoluto. Precisión: Grado de esfuerzo o cuidado con que se realiza una medida No exacto. No preciso. No exacto. Preciso. Exacto. Preciso. 16
17 9.- LA MEDICIÓN EN QUÍMICA. Términos Definición * Desviación estándar absoluta, s Desviación estándar relativa (RSD) Desviación estándar de la media, s m Coeficiente de variación, CV s = N i= 1 2 (x x) i N 1 s RSD = x s m = s N s CV = 100% x Varianza s 2 * x i = valor numérico de la iésima medida x = media de N medidas = N i= 1 N x i 17
18 9.- LA MEDICIÓN EN QUÍMICA Masas atómicas y masas fórmula Masa atómica: Masa atómica promedio: Masa fórmula: Ejemplos: Unid. M.A. (u) Unid. M.A. (u) 1 x Na = 1 x 23 3 x H 3 x 1 = 3 1 x H = 1 x 1 1 x P 1 x 31 = 31 1 x O = 1 x 16 4 x O 4 x 16 = 64 NaOH Masa Fórmula = 40 u H 3 PO 4 Masa Fórmula = 98 u 18
19 9.- LA MEDICIÓN EN QUÍMICA Cantidad de sustancia (materia) MOL: El SI define un mol como la cantidad de materia que contiene tantas entidades elementales como átomos hay contenidos en exactamente en 12 gramos de 12 C. Número de Avogadro: x Un mol de átomos de C posee una masa de exactamente 12 g. MASA MOLAR: Es la masa en gramos de un mol de unidades de átomos, moléculas o iones. VOLUMEN MOLAR: Es el volumen ocupado por un mol de átomos, moléculas o iones. 19
20 10.- ESTEQUIOMETRÍA Qué es la estequiometría? Determinación de fórmulas empíricas. Un laboratorio de análisis de vitamina C mostró que su composición porcentual en masa es de: 40.9% de C; 4.57% de H y 54.5% de O. Cuál es su fórmula empírica? C : H : O = 3.41 : 4.53 : 3.41 = 1 : 1.33 : 1 C : H : O = 3 : 4 : 3 C 3 H 4 O Fórmulas moleculares y estructurales. C 2 H 5 O 1 Fórmula molecular Fórmula estructural 20
21 10.- ESTEQUIOMETRÍA Ley de conservación de la materia. La masa total de los productos de una reacción es igual que la masa total de los reactivos de los que proceden. Lavoisier ( ) Ecuaciones químicas y cálculos estequiométricos. Reacción química: ecuaciones químicas: Ej.: el hidrógeno gas (H 2 ) puede reaccionar con oxígeno gas(o 2 ) para dar agua(h 2 0). La ecuación química para esta reacción se escribe: 2 H 2 (g) + O 2 2 H 2 O (l) 21
22 10.- ESTEQUIOMETRÍA. Coeficientes estequiométricos Rendimiento de las reacciones químicas. Reactivo limitante: Rendimiento teórico: La máxima cantidad de producto que puede obtenerse a partir de una cantidad de reactivo. Rendimiento real: La cantidad de producto que se obtiene realmente en una reacción. Rendimiento real < Rendimiento teórico 22
23 10.- ESTEQUIOMETRÍA. LEYES PONDERALES DE LAS R.Q. LEY DE LA CONSERVACIÓN DE LA MATERIA (LAVOISIER) LEY DE LAS PROPORCIONES DEFINIDAS (PROUST) LEY DE LAS PROPORCIONES MÚLTIPLES (DALTON) LEY DE LAS PROPORCIONES EQUIVALENTES (RITCHER) LEYES VOLUMÉTRICAS DE LAS R.Q. LEY DE GAY-LUSSAC O DE LOS VOLÚMENES DE COMBINACIÓN LEY DE AVOGADRO 23
24 10.- ESTEQUIOMETRÍA. LEY DE LAS PROPORCIONES DEFINIDAS (PROUST) Cada vez que dos o más elementos se unen para formar un compuesto determinado, lo hacen siempre en la misma proporción de masas. LEY DE LAS PROPORCIONES MÚLTIPLES (DALTON) Cuando dos elementos se pueden unir para formar más de un compuesto, las cantidades de uno de los Reactivos, se combinarn con masas fijas del otro, guardando entre sí una relación numérica sencilla. LEY DE LAS PROPORCIONES EQUIVALENTES (RITCHER) Si masas de distintos elementos/compuestos, se combinan entre sí con un elemento determinado, cuando Lo hagan entre sí sus masas relativas serán múltiplos o submultiplos de aquellas. 24
25 10.- ESTEQUIOMETRÍA. LEY DE GAY-LUSSAC Cuando dos o más sustancias gaseosas reaccionan entre sí para dar otra sustancia, gaseosa o no, guardan una relación sencilla de números enteros. LEY DE AVOGADRO Volúmenes iguales de gases diferentes, medidos en las mismas condiciones de p y temperatura, contienen el mismo número de moles. 25
26 TEMA 1.- CONCEPTOS PRELIMINARES 1. Introducción. 2. El método científico. 3. Cambios físicos y químicos. 4. Materia y masa. 5. Sustancias, elementos, compuestos y mezclas. 6. Los símbolos y la tabla periódica. 7. Átomos, moléculas e iones. 8. La medición en Química. Unidades del SI. Conversión de unidades. Incertidumbre en la medición y expresión de resultados. Medición de longitud, masa, tiempo, temperatura y unidades derivadas. Masas atómicas y masas fórmula. Cantidad de sustancia: mol, masa molar, número de Avogadro. 9. Estequiometría. La ley de conservación de masa. Las ecuaciones químicas y cálculos estequiométricos. Rendimiento de las reacciones químicas. Determinación de las fórmulas empíricas a partir de la composición. Fórmulas moleculares y estructurales. 26
FENOMENOS DE TRANSPORTE Introducción
 FENOMENOS DE TRANSPORTE Introducción Situación en el plan de estudios BASICAS FUNDAMENTOS I.Q. APLICADAS BALANCES DE MATERIA Y ENERGIA OPERACIONES DE SEPARACION MATEMATICAS FISICA TERMODINAMICA FENOMENOS
FENOMENOS DE TRANSPORTE Introducción Situación en el plan de estudios BASICAS FUNDAMENTOS I.Q. APLICADAS BALANCES DE MATERIA Y ENERGIA OPERACIONES DE SEPARACION MATEMATICAS FISICA TERMODINAMICA FENOMENOS
1.- La materia y clasificación. La materia es cualquier cosa que ocupa un espacio y tiene masas Estados: sólido, líquido, gaseoso
 La Química La Química se encarga del estudio de las propiedades de la materia y de los cambios que en ella se producen. La Química es una ciencia cuantitativa y requiere el uso de mediciones. Las cantidades
La Química La Química se encarga del estudio de las propiedades de la materia y de los cambios que en ella se producen. La Química es una ciencia cuantitativa y requiere el uso de mediciones. Las cantidades
QUÍMICA. La MATERIA REPRESENTACIÓN. Observación Datos Ley Hipótesis Teoría DEFINICIONES BÁSICAS. Propiedades
 QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
I. TEORÍA ATÓMICO-MOLECULAR
 Índice 1. La materia 2. Clasificación de la materia 3. Leyes ponderales 4. Teoría atómica de Dalton 5. Leyes volumétricas 6. La unidad de cantidad de materia: el mol 2 1 La materia Materia es todo aquello
Índice 1. La materia 2. Clasificación de la materia 3. Leyes ponderales 4. Teoría atómica de Dalton 5. Leyes volumétricas 6. La unidad de cantidad de materia: el mol 2 1 La materia Materia es todo aquello
REACCIONES QUÍMICAS. Elementos. Compuestos. CuS
 REACCIONES QUÍMICAS CONTENIDOS Reacciones químicas Leyes de la combinación química en reacciones químicas que dan origen a compuestos comunes Concepto de Mol Relaciones cuantitativas en diversas reacciones
REACCIONES QUÍMICAS CONTENIDOS Reacciones químicas Leyes de la combinación química en reacciones químicas que dan origen a compuestos comunes Concepto de Mol Relaciones cuantitativas en diversas reacciones
Conceptos Fundamentales Notación Científica Magnitudes y Unidades Sistema Internacional de Unidades Conversión de Unidades Análisis Dimensional
 Conceptos Fundamentales Notación Científica Magnitudes y Unidades Sistema Internacional de Unidades Conversión de Unidades Análisis Dimensional Materia: es todo lo que existe en el espacio, en el tiempo
Conceptos Fundamentales Notación Científica Magnitudes y Unidades Sistema Internacional de Unidades Conversión de Unidades Análisis Dimensional Materia: es todo lo que existe en el espacio, en el tiempo
Leyes clásicas de las reacciones químicas
 Leyes clásicas de las reacciones químicas Leyes ponderales Relativas a la masa de reactivos y productos en un reacción química. Instrumento de medida. La balanza - Ley de conservación de la masa. Lavoisier
Leyes clásicas de las reacciones químicas Leyes ponderales Relativas a la masa de reactivos y productos en un reacción química. Instrumento de medida. La balanza - Ley de conservación de la masa. Lavoisier
Estequiometría y Leyes Ponderales
 Estequiometría y Leyes Ponderales Equipo de Educación en Química Verde Centro Interdisciplinario de Líquidos Iónicos Programa de Educación Continua para el Magisterio Introducción Leyes fundamentales de
Estequiometría y Leyes Ponderales Equipo de Educación en Química Verde Centro Interdisciplinario de Líquidos Iónicos Programa de Educación Continua para el Magisterio Introducción Leyes fundamentales de
Teoría es un principio unificador que explica un conjunto de hechos y aquellas leyes que se basan en ellos.
 Página 1 de 6 Repaso de Química 105 I. Método científico Pasos Basicos Observación Representación Interpretación Hipótesis explicación tentativa de un problema. Nos guia para planear experimentos adicionales.
Página 1 de 6 Repaso de Química 105 I. Método científico Pasos Basicos Observación Representación Interpretación Hipótesis explicación tentativa de un problema. Nos guia para planear experimentos adicionales.
DEFINICIONES ELEMENTALES
 DEFINICIONES ELEMENTALES A partir de las leyes pónderales y de la ley de Lavoisier aparece el concepto de peso equivalente ó peso de combinación, que es el peso de un elemento que se combina con un peso
DEFINICIONES ELEMENTALES A partir de las leyes pónderales y de la ley de Lavoisier aparece el concepto de peso equivalente ó peso de combinación, que es el peso de un elemento que se combina con un peso
PENDIENTES DE 3º ESO. DEPARTAMENTO DE FÍSICA Y QUÍMICA. CURSO 13-14
 PENDIENTES DE 3º ESO. DEPARTAMENTO DE FÍSICA Y QUÍMICA. CURSO 13-14 INFORMACIÓN Y CONTENIDOS MÍNIMOS PARA LA EVALUACIÓN Información Para que los alumnos puedan recuperar esta asignatura lo más pronto posible,
PENDIENTES DE 3º ESO. DEPARTAMENTO DE FÍSICA Y QUÍMICA. CURSO 13-14 INFORMACIÓN Y CONTENIDOS MÍNIMOS PARA LA EVALUACIÓN Información Para que los alumnos puedan recuperar esta asignatura lo más pronto posible,
todoesquimica.bligoo.cl
 todoesquimica.bligoo.cl Ley de conservación de la masa (Lavoisier) Ley de proporciones definidas (Proust) Ley de proporciones múltiples (Dalton). Ley de proporciones recíprocas (Ritcher) Ley de volúmenes
todoesquimica.bligoo.cl Ley de conservación de la masa (Lavoisier) Ley de proporciones definidas (Proust) Ley de proporciones múltiples (Dalton). Ley de proporciones recíprocas (Ritcher) Ley de volúmenes
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL UNIDAD II CLASE Nº 1 CIFRAS SIGNIFICATIVAS 1 Sistema de
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL UNIDAD II CLASE Nº 1 CIFRAS SIGNIFICATIVAS 1 Sistema de
Unidad 0 CÁLCULOS QUÍMICOS. Unidad 0. Cálculos químicos
 Unidad 0 CÁLCULOS QUÍMICOS Unidad 0. Cálculos químicos 1 0. Leyes ponderales Leyes que rigen las combinaciones químicas. Se basan en la experimentación y miden cuantitativamente la cantidad de materia
Unidad 0 CÁLCULOS QUÍMICOS Unidad 0. Cálculos químicos 1 0. Leyes ponderales Leyes que rigen las combinaciones químicas. Se basan en la experimentación y miden cuantitativamente la cantidad de materia
Guía Temática de Química
 Guía Temática de Química Introducción a la Química Definición de química y de ciencias afines a ella Diferenciación de las ciencias afines a la química 1 Conceptos básicos de química y el método científico
Guía Temática de Química Introducción a la Química Definición de química y de ciencias afines a ella Diferenciación de las ciencias afines a la química 1 Conceptos básicos de química y el método científico
Reacciones Químicas. Homogéneas.
 Como se sabe, la materia está formada por partículas, dependiendo el comportamiento de esta (la materia) del estado físico en que se encuentran las partículas. Igualmente, sabemos que la materia no es
Como se sabe, la materia está formada por partículas, dependiendo el comportamiento de esta (la materia) del estado físico en que se encuentran las partículas. Igualmente, sabemos que la materia no es
LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas.
 LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas. Química 1º bachillerato La materia 1 1. TEORÍA ATÓMICA DE DALTON
LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas. Química 1º bachillerato La materia 1 1. TEORÍA ATÓMICA DE DALTON
CALENDARIO DE PRÁCTICAS DE QUÍMICA GENERAL I SEMESTRE
 Semana Fecha Número y nombre de la práctica (*) prácticas que pueden omitirse por reducción de sesiones debido a días feriados 01 Presentación, seguridad y entrega de gavetas 1. LA MATERIA Y SUS CAMBIOS
Semana Fecha Número y nombre de la práctica (*) prácticas que pueden omitirse por reducción de sesiones debido a días feriados 01 Presentación, seguridad y entrega de gavetas 1. LA MATERIA Y SUS CAMBIOS
Principios y conceptos básicos de Química
 Principios y conceptos básicos de Química Se estudiarán durante las dos primeras quincenas, estos contenidos están en el tema 2 del libro de texto. Quincena 1ª - Repaso de conceptos estudiados en ESO (Densidad,
Principios y conceptos básicos de Química Se estudiarán durante las dos primeras quincenas, estos contenidos están en el tema 2 del libro de texto. Quincena 1ª - Repaso de conceptos estudiados en ESO (Densidad,
Química General. Tema 5 Estequiometría y Reacciones Químicas
 www.upct.es Química General Tema 5 Estequiometría y Reacciones Químicas Índice 1.- INTRODUCCIÓN.-LOS CÁLCULOS EN QUÍMICA 2.- REACCIONES QUÍMICAS 2.1- INTERPRETACIÓN MACROSCÓPICA (relación en moles) 2.2.-
www.upct.es Química General Tema 5 Estequiometría y Reacciones Químicas Índice 1.- INTRODUCCIÓN.-LOS CÁLCULOS EN QUÍMICA 2.- REACCIONES QUÍMICAS 2.1- INTERPRETACIÓN MACROSCÓPICA (relación en moles) 2.2.-
- Magnitudes y unidades - El S.I. de unidades - Medida y error. Física Física y química 1º 1º Bachillerato
 - Magnitudes y unidades - El S.I. de unidades - Medida y error Física Física y química 1º 1º Bachillerato Magnitud Es todo aquello que puede ser medido Medición Medir Conjunto Es comparar de actos una
- Magnitudes y unidades - El S.I. de unidades - Medida y error Física Física y química 1º 1º Bachillerato Magnitud Es todo aquello que puede ser medido Medición Medir Conjunto Es comparar de actos una
INFORMACIÓN PARA LOS ALUMNOS DE 3º ESO
 INFORMACIÓN PARA LOS ALUMNOS DE 3º ESO DE FISICA Y QUIMICA Curso 2010-2011 1 OBJETIVOS Al finalizar el curso deberás ser capaz de: 1. Dominar la transformación de una unidad en otras. 2. Identificar magnitudes
INFORMACIÓN PARA LOS ALUMNOS DE 3º ESO DE FISICA Y QUIMICA Curso 2010-2011 1 OBJETIVOS Al finalizar el curso deberás ser capaz de: 1. Dominar la transformación de una unidad en otras. 2. Identificar magnitudes
PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA
 PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA UNIDAD 1: MATERIA Y MEDICIÓN CLASE TEMAS SUBTEMAS JUSTIFICACIÓN 1 2 3 MATERIA Y MEDICIÓN La química. Ramas de la química. La materia. Estados de la Materia Clasificación
PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA UNIDAD 1: MATERIA Y MEDICIÓN CLASE TEMAS SUBTEMAS JUSTIFICACIÓN 1 2 3 MATERIA Y MEDICIÓN La química. Ramas de la química. La materia. Estados de la Materia Clasificación
FÍSICA Y QUÍMICA 3º de ESO
 FÍSICA Y QUÍMICA 3º de ESO A) Contenidos (conceptos) UNIDAD 1: La medida. El método científico Fenómenos físicos. Física. Fenómenos químicos. Química. Magnitud física. Unidad de medida. Sistema Internacional
FÍSICA Y QUÍMICA 3º de ESO A) Contenidos (conceptos) UNIDAD 1: La medida. El método científico Fenómenos físicos. Física. Fenómenos químicos. Química. Magnitud física. Unidad de medida. Sistema Internacional
TEMA 2: LEYES Y CONCEPTOS BÁSICOS EN QUÍMICA
 1. SUSTANCIAS PURAS Y MEZCLAS 2. LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS 2.1. LEY DE CONSERVACIÓN DE LA MATERIA Enunciada en 1783 por Lavoisier: La materia ni se crea ni se destruye, únicamente
1. SUSTANCIAS PURAS Y MEZCLAS 2. LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS 2.1. LEY DE CONSERVACIÓN DE LA MATERIA Enunciada en 1783 por Lavoisier: La materia ni se crea ni se destruye, únicamente
PPTCCO007CB33-A17V1 Clase. Leyes y conceptos de la estequiometría
 PPTCCO007CB33-A17V1 Clase Leyes y conceptos de la estequiometría Resumen de la clase anterior El átomo Representado por Divisible en Participan en Protón Neutrón Electrón Caracterizados por Modelos atómicos
PPTCCO007CB33-A17V1 Clase Leyes y conceptos de la estequiometría Resumen de la clase anterior El átomo Representado por Divisible en Participan en Protón Neutrón Electrón Caracterizados por Modelos atómicos
La Física y la Química son ciencias experimentales porque utilizan la experimentación para realizar sus estudios.
 RESUMEN de la UNIDAD 1. LA CIENCIA Y LA MEDIDA 1. La ciencia Se define la ciencia como un conjunto de conocimientos sobre el mundo obtenidos mediante la observación, la experimentación y el razonamiento,
RESUMEN de la UNIDAD 1. LA CIENCIA Y LA MEDIDA 1. La ciencia Se define la ciencia como un conjunto de conocimientos sobre el mundo obtenidos mediante la observación, la experimentación y el razonamiento,
LEYES FUNDAMENTALES DE LA QUÍMICA
 LEYES FUNDAMENTALES DE LA QUÍMICA SUSTANCIAS PURAS Cambios físicos Cambios Químicos TRANSFORMACIÓN No implican cambio de composición Ejemplo: Cambio de fase COMPUESTOS COMBINACIONES QUIMICAS DE ELEMENTOS
LEYES FUNDAMENTALES DE LA QUÍMICA SUSTANCIAS PURAS Cambios físicos Cambios Químicos TRANSFORMACIÓN No implican cambio de composición Ejemplo: Cambio de fase COMPUESTOS COMBINACIONES QUIMICAS DE ELEMENTOS
Prefacio... ix COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3
 ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
Química: conocimientos previos
 Química: conocimientos previos Cálculos estequiométricos Objetivos que el alumno debería alcanzar al terminar el capítulo: Utilizar el concepto de mol para resolver problemas numéricos donde intervengan
Química: conocimientos previos Cálculos estequiométricos Objetivos que el alumno debería alcanzar al terminar el capítulo: Utilizar el concepto de mol para resolver problemas numéricos donde intervengan
PRUEBA EXTRAORDINARIA SEPTIEMBRE FÍSICA Y QUÍMICA DE 3º ESO. CURSO 2012/2013. CEO PUERTO CABRAS. OBJETIVOS, CRITERIOS Y CONTENIDOS MÍNIMOS.
 PRUEBA EXTRAORDINARIA SEPTIEMBRE FÍSICA Y QUÍMICA DE 3º ESO. CURSO 2012/2013. CEO PUERTO CABRAS., CRITERIOS Y MÍNIMOS. Unidad 1. La ciencia: la materia y su medida 1 Conocer el Sistema Internacional de
PRUEBA EXTRAORDINARIA SEPTIEMBRE FÍSICA Y QUÍMICA DE 3º ESO. CURSO 2012/2013. CEO PUERTO CABRAS., CRITERIOS Y MÍNIMOS. Unidad 1. La ciencia: la materia y su medida 1 Conocer el Sistema Internacional de
Las magnitudes físicas y su medida
 Las magnitudes físicas y su medida Podemos interpretar los fenómenos de la naturaleza gracias a que los cuerpos poseen propiedades que pueden ser medidas. Qué es una magnitud física? Una magnitud física
Las magnitudes físicas y su medida Podemos interpretar los fenómenos de la naturaleza gracias a que los cuerpos poseen propiedades que pueden ser medidas. Qué es una magnitud física? Una magnitud física
MOL. Nº AVOGADRO DISOLUCIONES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
MOL. Nº AVOGADRO GASES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
PRÁCTICA N 1: INSTRUMENTOS DE MEDIDA DE LONGITUD, TIEMPO Y MASA. Sistema Internacional de unidades (SI)
 PRÁCTICA N 1: INSTRUMENTOS DE MEDIDA DE LONGITUD, TIEMPO Y MASA Unidad patrón referencia utilizada para determinar el valor de una magnitud, se le asigna un valor unitario Magnitudes Fundamentales: del
PRÁCTICA N 1: INSTRUMENTOS DE MEDIDA DE LONGITUD, TIEMPO Y MASA Unidad patrón referencia utilizada para determinar el valor de una magnitud, se le asigna un valor unitario Magnitudes Fundamentales: del
UNIVERSIDAD AUTONOMA DE CD. JUAREZ INSTITUTO DE INGENIERIA Y TECNOLOGIA CURSO DE QUIMICA ELABORADO POR: ING. VIRGINIA ESTEBANE ORTEGA
 UNIVERSIDAD AUTONOMA DE CD. JUAREZ INSTITUTO DE INGENIERIA Y TECNOLOGIA CURSO DE QUIMICA ELABORADO POR: ING. VIRGINIA ESTEBANE ORTEGA ENERO 2003 Ing. Virginia Estebané 2 CAPITULO 1.- INTRODUCCION: MATERIA
UNIVERSIDAD AUTONOMA DE CD. JUAREZ INSTITUTO DE INGENIERIA Y TECNOLOGIA CURSO DE QUIMICA ELABORADO POR: ING. VIRGINIA ESTEBANE ORTEGA ENERO 2003 Ing. Virginia Estebané 2 CAPITULO 1.- INTRODUCCION: MATERIA
Topografía 1. II semestre, José Francisco Valverde Calderón Sitio web:
 II semestre, 2013 alderón Email: [email protected] Sitio web: www.jfvc.wordpress.com Introducción Cualquier actividad técnica donde se requiera recopilar información espacial, requiere algún proceso de
II semestre, 2013 alderón Email: [email protected] Sitio web: www.jfvc.wordpress.com Introducción Cualquier actividad técnica donde se requiera recopilar información espacial, requiere algún proceso de
índice ~
 - ---------------- índice ~ Página CAPíTULO 1 CONCEPTOS FUNDAMENTALES 23 1. MATERIA 2. MASA Y PESO 3. VOLUMEN 4. MEDICIÓN 4.1 Unidades fundamentales o patrones de medición unidades SI 5. OPERACIONES MATEMÁTICAS
- ---------------- índice ~ Página CAPíTULO 1 CONCEPTOS FUNDAMENTALES 23 1. MATERIA 2. MASA Y PESO 3. VOLUMEN 4. MEDICIÓN 4.1 Unidades fundamentales o patrones de medición unidades SI 5. OPERACIONES MATEMÁTICAS
- Leyes ponderales: Las leyes ponderales relacionan las masas de las sustancias que intervienen en una reacción química.
 FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
CANTIDADES. MEDIDAS NÚMEROS
 ( A) = a 1 CuSCN N O 2NO 2 4 2 Cr O 2 3 CANTIDADES. MEDIDAS NÚMEROS CAPÍTULO 1 1.1. CANTIDAD Y MEDIDA Una ciencia experimental como la Química está ligada al proceso de medición. A su vez las medidas que
( A) = a 1 CuSCN N O 2NO 2 4 2 Cr O 2 3 CANTIDADES. MEDIDAS NÚMEROS CAPÍTULO 1 1.1. CANTIDAD Y MEDIDA Una ciencia experimental como la Química está ligada al proceso de medición. A su vez las medidas que
CENTRO UNIVERSITARIO MONTEJO A.C. Temario Ciencias 3 Énfasis en química. Bloque I. Las características de los materiales
 Bloque I. Las características de los materiales La ciencia y la tecnología en el mundo actual Identifica las aportaciones del conocimiento químico y tecnológico en la satisfacción de necesidades básicas,
Bloque I. Las características de los materiales La ciencia y la tecnología en el mundo actual Identifica las aportaciones del conocimiento químico y tecnológico en la satisfacción de necesidades básicas,
LEYES FUNDAMENTALES DE LA QUÍMICA
 LEYES FUNDAMENTALES DE LA QUÍMICA CONTENIDOS 1.- Sustancias homogéneas y heterogéneas. Elementos y compuestos..- Leyes fundamentales de la Química..1. Ley de conservación de la masa... Ley de las proporciones
LEYES FUNDAMENTALES DE LA QUÍMICA CONTENIDOS 1.- Sustancias homogéneas y heterogéneas. Elementos y compuestos..- Leyes fundamentales de la Química..1. Ley de conservación de la masa... Ley de las proporciones
MOL. Nº AVOGADRO GASES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
CONTENIDOS MÍNIMOS DE CIENCIAS NATURALES 2ºESO PARA LA PRUEBA EXTRAORDINARIA DE SEPTIEMBRE
 CONTENIDOS MÍNIMOS DE CIENCIAS NATURALES 2ºESO PARA LA PRUEBA EXTRAORDINARIA DE SEPTIEMBRE Curso 2014/15 Unidad 1: MOVIMIENTO Y FUERZAS - Magnitudes físicas. Cambios de unidades (factor de conversión).
CONTENIDOS MÍNIMOS DE CIENCIAS NATURALES 2ºESO PARA LA PRUEBA EXTRAORDINARIA DE SEPTIEMBRE Curso 2014/15 Unidad 1: MOVIMIENTO Y FUERZAS - Magnitudes físicas. Cambios de unidades (factor de conversión).
SISTEMA INTERNACIONAL DE UNIDADES ( SI )
 SISTEMA INTERNACIONAL DE UNIDADES ( SI ) Este Sistema surgió como necesidad de adoptar criterios universalmente aceptados en el uso de unidades de medida. Fue aprobado en 1960 después de reuniones diversas
SISTEMA INTERNACIONAL DE UNIDADES ( SI ) Este Sistema surgió como necesidad de adoptar criterios universalmente aceptados en el uso de unidades de medida. Fue aprobado en 1960 después de reuniones diversas
Contenido de Física y Química de la Primera Evaluación
 Contenido de Física y Química de la Primera Evaluación Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura. En tradicional se denominan
Contenido de Física y Química de la Primera Evaluación Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura. En tradicional se denominan
CUESTIONARIOS FÍSICA 4º ESO
 DPTO FÍSICA QUÍMICA. IES POLITÉCNICO CARTAGENA CUESTIONARIOS FÍSICA º ESO UNIDADES 8 y 10 Átomos, elementos y compuestos. Las reacciones químicas Mª Teresa Gómez Ruiz 2010 HTTP://WWW. POLITECNICOCARTAGENA.
DPTO FÍSICA QUÍMICA. IES POLITÉCNICO CARTAGENA CUESTIONARIOS FÍSICA º ESO UNIDADES 8 y 10 Átomos, elementos y compuestos. Las reacciones químicas Mª Teresa Gómez Ruiz 2010 HTTP://WWW. POLITECNICOCARTAGENA.
Ley de conservación de la masa o ley de Lavoisier Ley de las proporciones definidas o ley de Proust
 REPASO DE QUÍMICA 1 Leyes ponderales-1 Ley de conservación de la masa o ley de Lavoisier: En toda reacción química, en un sistema cerrado, la masa de todas las sustancias existentes se conserva. Ley de
REPASO DE QUÍMICA 1 Leyes ponderales-1 Ley de conservación de la masa o ley de Lavoisier: En toda reacción química, en un sistema cerrado, la masa de todas las sustancias existentes se conserva. Ley de
En el siglo XVIII la química estableció las medidas precisas de masa y volúmenes que llevaron a enunciar las llamadas leyes ponderales.
 1. LEYES PONDERALES En el siglo XVIII la química estableció las medidas precisas de masa y volúmenes que llevaron a enunciar las llamadas leyes ponderales. Ley de conservación de la masa de Lavoisier Lavosier
1. LEYES PONDERALES En el siglo XVIII la química estableció las medidas precisas de masa y volúmenes que llevaron a enunciar las llamadas leyes ponderales. Ley de conservación de la masa de Lavoisier Lavosier
Clasificación de la materia hasta el nivel atómico
 1. Estequiometría Clasificación de la materia hasta el nivel atómico Materia puede separarse por un proceso físico? SÍ NO Mezcla es homogénea? Sustancia puede descomponerse por un proceso químico? SÍ NO
1. Estequiometría Clasificación de la materia hasta el nivel atómico Materia puede separarse por un proceso físico? SÍ NO Mezcla es homogénea? Sustancia puede descomponerse por un proceso químico? SÍ NO
Ing. Sol de María Jiménez González
 Ing. Sol de María Jiménez González 1 02 de junio I Tutoría Presencial 16 de junio II Tutoría Presencial Entrega de Tarea 30 de junio: I Examen Ordinario 14 de julio III Tutoría Presencial Entrega de proyecto
Ing. Sol de María Jiménez González 1 02 de junio I Tutoría Presencial 16 de junio II Tutoría Presencial Entrega de Tarea 30 de junio: I Examen Ordinario 14 de julio III Tutoría Presencial Entrega de proyecto
2.2. Definición de la masa y volumen de un sólido y cálculo de su densidad.
 CONTENIDOS MÍNIMOS 2º ESO FYQ U.P.2 2.1. Diferencias y aplicaciones de las propiedades generales y específicas de la materia. 2.2. Definición de la masa y volumen de un sólido y cálculo de su densidad.
CONTENIDOS MÍNIMOS 2º ESO FYQ U.P.2 2.1. Diferencias y aplicaciones de las propiedades generales y específicas de la materia. 2.2. Definición de la masa y volumen de un sólido y cálculo de su densidad.
FUNDAMENTOS DE LA QUÍMICA Química 1º Bachillerato (Ciencias)
 FUNDAMENTOS DE LA QUÍMICA Química 1º Bachillerato (Ciencias) FUNDAMENTOS DE LA QUÍMICA I. La Química. La Química es la ciencia que estudia la materia en relación a su composición, propiedades y transformaciones
FUNDAMENTOS DE LA QUÍMICA Química 1º Bachillerato (Ciencias) FUNDAMENTOS DE LA QUÍMICA I. La Química. La Química es la ciencia que estudia la materia en relación a su composición, propiedades y transformaciones
1. Estequiometría. 1.Estequiometría
 1. Estequiometría Contenidos Reacciones químicas y ecuaciones químicas Mezclas y sustancias puras; compuestos y elementos; moléculas y átomos; iones Reacciones químicas; estequiometría; ecuaciones químicas
1. Estequiometría Contenidos Reacciones químicas y ecuaciones químicas Mezclas y sustancias puras; compuestos y elementos; moléculas y átomos; iones Reacciones químicas; estequiometría; ecuaciones químicas
Examen de Diagnóstico Química I
 Examen de Diagnóstico Química I 1. Son los cuatro elementos básicos que conforman la materia. A) NaCl, NaOH, GaAs, H 2 CO 3 B) Be, Na, Ra, Rf C) Ca, He, Ni, D) ADN, ARN, gen, célula E) C, H, O, N 2. Sustancia
Examen de Diagnóstico Química I 1. Son los cuatro elementos básicos que conforman la materia. A) NaCl, NaOH, GaAs, H 2 CO 3 B) Be, Na, Ra, Rf C) Ca, He, Ni, D) ADN, ARN, gen, célula E) C, H, O, N 2. Sustancia
ESTEQUIOMETRIA. Es la rama de la química que establece relaciones cuantitativas entre: . Elementos en la formación de compuestos
 ESTEQUIOMETRIA Es la rama de la química que establece relaciones cuantitativas entre:. Elementos en la formación de compuestos. Elementos y compuesto involucrados en las reacciones químicas CONCEPTOS DE
ESTEQUIOMETRIA Es la rama de la química que establece relaciones cuantitativas entre:. Elementos en la formación de compuestos. Elementos y compuesto involucrados en las reacciones químicas CONCEPTOS DE
LOS ESTADOS DE LA MATERIA
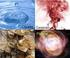 LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Nomenclatura. En tradicional se denominan anhídridos.
 Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura. En tradicional se denominan anhídridos. Tablas de formulación. Hidruros metálicos (M+H)
Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura. En tradicional se denominan anhídridos. Tablas de formulación. Hidruros metálicos (M+H)
UNIDADES Y MEDICIONES
 UNIDADES Y MEDICIONES Introducción Imagina que alguien te esta dando indicaciones para llegar a su casa y te dice lo siguiente: maneja a lo largo de la 11 Sur durante un rato y doblas a la derecha en uno
UNIDADES Y MEDICIONES Introducción Imagina que alguien te esta dando indicaciones para llegar a su casa y te dice lo siguiente: maneja a lo largo de la 11 Sur durante un rato y doblas a la derecha en uno
UNIDAD I. TEMA III. ESTEQUIOMETRÍA
 REPUBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD EXPERIMENTAL SUR DEL LAGO Jesús María Semprúm PROGRAMA DE INGENIERIA DE ALIMENTOS UNIDAD CURRICULAR: QUIMICA GENERAL UNIDAD I. TEMA III. ESTEQUIOMETRÍA Prof.
REPUBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD EXPERIMENTAL SUR DEL LAGO Jesús María Semprúm PROGRAMA DE INGENIERIA DE ALIMENTOS UNIDAD CURRICULAR: QUIMICA GENERAL UNIDAD I. TEMA III. ESTEQUIOMETRÍA Prof.
Técnico Profesional QUÍMICA
 Programa Técnico Profesional QUÍMICA Estequiometría I: leyes y conceptos de la estequiometría Nº Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta una parte del sistema
Programa Técnico Profesional QUÍMICA Estequiometría I: leyes y conceptos de la estequiometría Nº Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta una parte del sistema
Tema 1 CONCEPTOS PRELIMINARES. 1. Introducción
 Tema 1 CONCEPTOS PRELIMINARES 1. Introducción La Química es la rama de la ciencia que estudia la materia y los cambios que ésta pueda tener. Por materia se entiende algo que tiene masa y volumen, es decir,
Tema 1 CONCEPTOS PRELIMINARES 1. Introducción La Química es la rama de la ciencia que estudia la materia y los cambios que ésta pueda tener. Por materia se entiende algo que tiene masa y volumen, es decir,
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA. Ingeniería Química
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA Ingeniería Química Unidad I. Introducción a los cálculos de Ingeniería
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA Ingeniería Química Unidad I. Introducción a los cálculos de Ingeniería
Contenidos mínimos Física y Química 3º ESO
 Contenidos mínimos Física y Química 3º ESO EL TRABAJO CIENTÍFICO Etapas del método científico. Magnitudes y unidades. Cambio de unidades. Sistema Internacional de Unidades (SI). Representación de gráficas
Contenidos mínimos Física y Química 3º ESO EL TRABAJO CIENTÍFICO Etapas del método científico. Magnitudes y unidades. Cambio de unidades. Sistema Internacional de Unidades (SI). Representación de gráficas
Tema 1. Conceptos Básicos en Química
 Tema 1. Conceptos Básicos en Química Química Átomo: números másicos y atómicos Mol Fórmulas empíricas y moleculares Reacciones químicas Gases Disoluciones Qué es la Química? Ciencia que estudia la composición
Tema 1. Conceptos Básicos en Química Química Átomo: números másicos y atómicos Mol Fórmulas empíricas y moleculares Reacciones químicas Gases Disoluciones Qué es la Química? Ciencia que estudia la composición
10 Naturaleza de la materia
 10 Naturaleza de la materia ACTIVIDADES Actividades DE del LADILL interior DE LA UNIDAD de la unidad DIEZ 1. El oígeno se combina con el silicio en una relación de masa 1,14 : 1: a) Qué masa de silicio
10 Naturaleza de la materia ACTIVIDADES Actividades DE del LADILL interior DE LA UNIDAD de la unidad DIEZ 1. El oígeno se combina con el silicio en una relación de masa 1,14 : 1: a) Qué masa de silicio
amperio o ampere A Se define a partir del campo eléctrico
 Sistema Internacional de medidas El Sistema Internacional de Unidades consta de siete unidades básicas, también denominadas unidades fundamentales. De la combinación de las siete unidades fundamentales
Sistema Internacional de medidas El Sistema Internacional de Unidades consta de siete unidades básicas, también denominadas unidades fundamentales. De la combinación de las siete unidades fundamentales
TEMA 7: Problemas de Química
 TEMA 7: Problemas de Química Tema 7: Problemas de Química 1 1.- REACCIONES QUÍMICAS Una reacción química es un proceso en el que se unen varias sustancias llamadas reactivos y se transforman en otras sustancias
TEMA 7: Problemas de Química Tema 7: Problemas de Química 1 1.- REACCIONES QUÍMICAS Una reacción química es un proceso en el que se unen varias sustancias llamadas reactivos y se transforman en otras sustancias
Curso de Ciencias Física 2 año Profesor Javier Ponce. Qué es Ciencia? Qué es Ciencias Físicas?
 Curso de Ciencias Física 2 año Profesor Javier Ponce Qué es Ciencia? Ciencia (en latíns cientia, de scire, conocer ), término que en su sentido más amplio se emplea para referirse al conocimiento sistematizado
Curso de Ciencias Física 2 año Profesor Javier Ponce Qué es Ciencia? Ciencia (en latíns cientia, de scire, conocer ), término que en su sentido más amplio se emplea para referirse al conocimiento sistematizado
Magnitudes, Cantidades: fundamentales y derivadas. Sistema de Unidades. Mediciones.
 Magnitudes, Cantidades: fundamentales y derivadas. Sistema de Unidades. Mediciones. Resumen La física, como los demás ciencias, es una empresa de creación, no simplemente una colección de hechos. La física
Magnitudes, Cantidades: fundamentales y derivadas. Sistema de Unidades. Mediciones. Resumen La física, como los demás ciencias, es una empresa de creación, no simplemente una colección de hechos. La física
CONTENIDOS MÍNIMOS septiembre
 DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
ESTEQUIOMETRIA. Ca + 2 HNO 3 Ca (NO 3 ) 2 + H 2 Relación molar 1 at.gr 2 mol. gr. 1 mol. gr 1 mol. gr Relación en peso 40 g 126 g 164 g 2 g
 ESTEQUIOMETRIA Concepto: Es aquella parte de la Química que se encarga de estudiar las relaciones cuantitativas entre aquellas sustancias que participan en una reacción química. I. Leyes Ponderales II.
ESTEQUIOMETRIA Concepto: Es aquella parte de la Química que se encarga de estudiar las relaciones cuantitativas entre aquellas sustancias que participan en una reacción química. I. Leyes Ponderales II.
Índice. Introducción Capítulo 1: Magnitudes físicas, unidades y análisis dimensional.
 Índice Introducción Capítulo 1: físicas, unidades y análisis dimensional. Introducción Capítulo 1:. Índice Leyes Físicas y cantidades físicas. Sistemas de unidades Análisis dimensional. La medida física.
Índice Introducción Capítulo 1: físicas, unidades y análisis dimensional. Introducción Capítulo 1:. Índice Leyes Físicas y cantidades físicas. Sistemas de unidades Análisis dimensional. La medida física.
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
CLASE Nº 2 ESTEQUIOMETRÍA
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 2 ESTEQUIOMETRÍA 1 Estequiometría Leyes que rigen
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 2 ESTEQUIOMETRÍA 1 Estequiometría Leyes que rigen
La materia. Elaborado por: Nubia Ortega N.
 La materia. Elaborado por: Nubia Ortega N. La materia. Clasificación. Leyes Ponderales: Son las leyes generales que rigen las combinaciones químicas. Se basan en la experimentación y miden cuantitativamente
La materia. Elaborado por: Nubia Ortega N. La materia. Clasificación. Leyes Ponderales: Son las leyes generales que rigen las combinaciones químicas. Se basan en la experimentación y miden cuantitativamente
PREFIJOS MEDIDAS CIFRAS SIGNIFICATIVAS. Prefijo Símbolo Factor de multiplicación
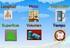 PREFIJOS MEDIDS CIFRS SIGNIFICTIVS 1- Prefijo de múltiplos y submúltiplos: Prefijo Símbolo Factor de multiplicación Tera T x10 12 Giga G x10 9 Mega M x10 6 Kilo K x10 3 Hecto h x10 2 Deca da x10 2 deci
PREFIJOS MEDIDS CIFRS SIGNIFICTIVS 1- Prefijo de múltiplos y submúltiplos: Prefijo Símbolo Factor de multiplicación Tera T x10 12 Giga G x10 9 Mega M x10 6 Kilo K x10 3 Hecto h x10 2 Deca da x10 2 deci
FISICA Y QUIMICA 1º BACHILLERATO A DISTANCIA
 FISICA Y QUIMICA 1º BACHILLERATO A DISTANCIA 2015-2016 INTRODUCCIÓN: La Física y la Química contribuyen al desarrollo de las capacidades recogidas en los objetivos generales de la etapa, especialmente
FISICA Y QUIMICA 1º BACHILLERATO A DISTANCIA 2015-2016 INTRODUCCIÓN: La Física y la Química contribuyen al desarrollo de las capacidades recogidas en los objetivos generales de la etapa, especialmente
LEYES PONDERALES. ESTEQUIOMETRÍA
 LEYES PONDERALES. ESTEQUIOMETRÍA 1 Vamos a aprender Qué son las leyes ponderales. Cómo contribuyeron al establecimiento de las bases de la Química. La importancia del mol como unidad de medida para la
LEYES PONDERALES. ESTEQUIOMETRÍA 1 Vamos a aprender Qué son las leyes ponderales. Cómo contribuyeron al establecimiento de las bases de la Química. La importancia del mol como unidad de medida para la
Cero absoluto: Es la mínima temperatura que se puede alcanzar ( 273ºC).
 LAS BASES DE LA QUÍMICA DEFINICIONES Elemento químico: Sustancia pura cuyos átomos tienen todos el mismo número de protones en su núcleo, es decir, el mismo número atómico (z). Cada elemento químico ocupa
LAS BASES DE LA QUÍMICA DEFINICIONES Elemento químico: Sustancia pura cuyos átomos tienen todos el mismo número de protones en su núcleo, es decir, el mismo número atómico (z). Cada elemento químico ocupa
LAS HERRAMIENTAS DE LA FÍSICA. Ing. Caribay Godoy Rangel
 LAS HERRAMIENTAS DE LA FÍSICA SISTEMA INTERNACIONAL DE UNIDADES (SI) UNIVERSABILIDAD MEDICIÓN ACCESIBILIDAD INVARIANCIA SISTEMA INTERNACIONAL DE Metro (m) UNIDADES (SI) 1889: Diezmillonésima parte de la
LAS HERRAMIENTAS DE LA FÍSICA SISTEMA INTERNACIONAL DE UNIDADES (SI) UNIVERSABILIDAD MEDICIÓN ACCESIBILIDAD INVARIANCIA SISTEMA INTERNACIONAL DE Metro (m) UNIDADES (SI) 1889: Diezmillonésima parte de la
QUÍMICA GENERAL. Introducción:
 QUÍMICA GENERAL Nombre de la asignatura: Química General Datos de identificación Clave: 7162 Semestre: Primer semestre Créditos: Créditos (4 horas teoría y 2 horas de laboratorio ) Total de horas: 64 Horas
QUÍMICA GENERAL Nombre de la asignatura: Química General Datos de identificación Clave: 7162 Semestre: Primer semestre Créditos: Créditos (4 horas teoría y 2 horas de laboratorio ) Total de horas: 64 Horas
TEMA 2: LEYES Y CONCEPTOS BÁSICOS EN QUÍMICA
 TEMA 2: LEYES Y CONCEPTOS BÁSICOS EN QUÍMICA 1. Sustancias, mezclas y combinaciones La materia puede aparecer en dos formas: Homogénea, cuando sus propiedades y su composición son idénticas en cualquier
TEMA 2: LEYES Y CONCEPTOS BÁSICOS EN QUÍMICA 1. Sustancias, mezclas y combinaciones La materia puede aparecer en dos formas: Homogénea, cuando sus propiedades y su composición son idénticas en cualquier
4. Estequiometría Antoine-Laurent de Lavoisier
 4. Estequiometría Antoine-Laurent de Lavoisier (París, 1743 París, en la guillotina, 1794 ) fue un químico francés. Se le considera el padre de la química por sus detallados estudios, entre otros: el estudio
4. Estequiometría Antoine-Laurent de Lavoisier (París, 1743 París, en la guillotina, 1794 ) fue un químico francés. Se le considera el padre de la química por sus detallados estudios, entre otros: el estudio
DEPARTAMENTO DE CIENCIAS NATURALES FÍSICA Y QUÍMICA 2º ESO.
 FÍSICA Y QUÍMICA 2º ESO. PROPUESTA DE ACTIVIDADES PARA LA RECUPERACIÓN DE SEPTIEMBRE. Nota: este cuaderno de actividades es orientativo para el examen de septiembre y no se entrega. El examen de septiembre
FÍSICA Y QUÍMICA 2º ESO. PROPUESTA DE ACTIVIDADES PARA LA RECUPERACIÓN DE SEPTIEMBRE. Nota: este cuaderno de actividades es orientativo para el examen de septiembre y no se entrega. El examen de septiembre
TEMARIO DE QUÍMICA GLOBALES
 TEMARIO DE QUÍMICA GLOBALES Séptimo Básico Unidad 1: Conceptos de materia. Estados de la materia Propiedades de la materia: físicas y químicas Clasificación de la materia: sustancias puras (elementos y
TEMARIO DE QUÍMICA GLOBALES Séptimo Básico Unidad 1: Conceptos de materia. Estados de la materia Propiedades de la materia: físicas y químicas Clasificación de la materia: sustancias puras (elementos y
Bloque 1. Las magnitudes físicas y su medida
 Bloque 1. Las magnitudes físicas y su medida El sistema métrico decimal El sistema internacional de unidades Conversiones de unidades con factores de conversión. Unidades compuestas Magnitudes escalares
Bloque 1. Las magnitudes físicas y su medida El sistema métrico decimal El sistema internacional de unidades Conversiones de unidades con factores de conversión. Unidades compuestas Magnitudes escalares
Generalidades de Mediciones y Magnitudes
 Generalidades de Mediciones y Magnitudes Para la química, en su calidad de ciencia experimental, la medida constituye una operación fundamental ya que sus descripciones del mundo físico se refieren a magnitudes
Generalidades de Mediciones y Magnitudes Para la química, en su calidad de ciencia experimental, la medida constituye una operación fundamental ya que sus descripciones del mundo físico se refieren a magnitudes
Conceptos básicos en estequiometría
 Conceptos básicos en estequiometría Tomado de: http://www.eis.uva.es/~qgintro/esteq/tutorial-01.html El Mol Un mol se define como la cantidad de materia que tiene tantos objetos como el número de átomos
Conceptos básicos en estequiometría Tomado de: http://www.eis.uva.es/~qgintro/esteq/tutorial-01.html El Mol Un mol se define como la cantidad de materia que tiene tantos objetos como el número de átomos
QUÍMICA GENERAL QQ 103 TEORIA ATÓMICA LEYES FUNDAMENTALES DE LA MATERIA, PROPORCIONES DEFINIDAS Y MÚLTIPLES
 QUÍMICA GENERAL QQ 103 TEORIA ATÓMICA LEYES FUNDAMENTALES DE LA MATERIA, PROPORCIONES DEFINIDAS Y MÚLTIPLES Leyes y teorias Leyes son afirmaciones que resumen hechos experimentales referentes a la naturaleza,
QUÍMICA GENERAL QQ 103 TEORIA ATÓMICA LEYES FUNDAMENTALES DE LA MATERIA, PROPORCIONES DEFINIDAS Y MÚLTIPLES Leyes y teorias Leyes son afirmaciones que resumen hechos experimentales referentes a la naturaleza,
LOS ESTADOS DE LA MATERIA
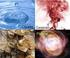 LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
I. Introducción. 1. La materia. Materia es todo lo que nos rodea. Podemos decir que la materia:
 Unidad I: El átomo. I. Introducción. 1. La materia Materia es todo lo que nos rodea. Podemos decir que la materia: Ocupa un lugar en el espacio. Tiene masa. Está formada por átomos. Puede ser percibida
Unidad I: El átomo. I. Introducción. 1. La materia Materia es todo lo que nos rodea. Podemos decir que la materia: Ocupa un lugar en el espacio. Tiene masa. Está formada por átomos. Puede ser percibida
Los átomos no se crean ni se destruyen en una reacción química, solo se redistribuyen.
 LEYES PONDERALES 1. Ley de conservación de la masa o de Lavoisier En cualquier reacción química que ocurra en un sistema cerrado, la masa total de las sustancias existentes se conserva. O lo que es lo
LEYES PONDERALES 1. Ley de conservación de la masa o de Lavoisier En cualquier reacción química que ocurra en un sistema cerrado, la masa total de las sustancias existentes se conserva. O lo que es lo
QUÍMICA IV UNIDAD REACCIONES QUÍMICAS ORGÁNICAS E INORGÁNICAS
 QUÍMICA IV UNIDAD REACCIONES QUÍMICAS ORGÁNICAS E INORGÁNICAS MOL: Es una unidad de cantidad de partículas. El número de partículas que constituye un mol se conoce con el nombre de número de Avogadro (NA)
QUÍMICA IV UNIDAD REACCIONES QUÍMICAS ORGÁNICAS E INORGÁNICAS MOL: Es una unidad de cantidad de partículas. El número de partículas que constituye un mol se conoce con el nombre de número de Avogadro (NA)
Magnitudes. Magnitudes escalares y vectoriales. Unidades. Medidas e Instrumentos de medida. Notación estándar.
 UNIDAD 1 Magnitudes. Magnitudes escalares y vectoriales. Unidades. Medidas e Instrumentos de medida. Notación estándar. Magnitudes: Las magnitudes son propiedades físicas que pueden ser medidas, por ejemplo
UNIDAD 1 Magnitudes. Magnitudes escalares y vectoriales. Unidades. Medidas e Instrumentos de medida. Notación estándar. Magnitudes: Las magnitudes son propiedades físicas que pueden ser medidas, por ejemplo
CONCEPTOS BÁSICOS. Unidades de medida. Preparación de soluciones
 CONCEPTOS BÁSICOS Unidades de medida Unidades básicas del SI Unidades derivadas del SI de uso común Prefijos para múltiplos y submúltiplos decimales Unidades de uso común no propias del SI Preparación
CONCEPTOS BÁSICOS Unidades de medida Unidades básicas del SI Unidades derivadas del SI de uso común Prefijos para múltiplos y submúltiplos decimales Unidades de uso común no propias del SI Preparación
Física y Química 1º Bachillerato LOMCE
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 201 2016 Unidad Didáctica 1 Rev 01 Las Leyes Ponderales y Las Leyes de los Gases Ideales 1.1 Las
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 201 2016 Unidad Didáctica 1 Rev 01 Las Leyes Ponderales y Las Leyes de los Gases Ideales 1.1 Las
MASAS ATOMICAS. 1 u = 1, g 1 g = 6, u
 MASAS ATOMICAS Escala de masa atómica Se define la masa del isótopo 1 C como equivalente a 1 unidades de masa atómica (u) 1 u = 1,6605 10 - g 1 g = 6,01 10 u De esta forma puede construirse una escala
MASAS ATOMICAS Escala de masa atómica Se define la masa del isótopo 1 C como equivalente a 1 unidades de masa atómica (u) 1 u = 1,6605 10 - g 1 g = 6,01 10 u De esta forma puede construirse una escala
LEYES PONDERALES Y ESTEQUIOMETRIA- ESTEQUIOMETRIA (ejercicios)
 LEYES PONDERALES Y ESTEQUIOMETRIA- ESTEQUIOMETRIA (ejercicios) ESTEQUIOMETRIA DE REACCIONES Indicadores de Evaluación: Representan reacciones químicas en una ecuación de reactantes y productos. Formulan
LEYES PONDERALES Y ESTEQUIOMETRIA- ESTEQUIOMETRIA (ejercicios) ESTEQUIOMETRIA DE REACCIONES Indicadores de Evaluación: Representan reacciones químicas en una ecuación de reactantes y productos. Formulan
