ELECTRICIDAD Y MAGNETISMO TRABAJO PRACTICO Nº 10 ELECTROFORESIS
|
|
|
- José Ramón Suárez Rivero
- hace 7 años
- Vistas:
Transcripción
1 ELECTRICIDAD Y MAGNETISMO TRABAJO PRACTICO Nº 10 ELECTROFORESIS CONTENIDOS Velocidad de migración. Movilidad electroforética. Fundamentos y gráficos. Factores que influyen. Tipos de Electroforesis. Equipamiento y Aplicaciones en análisis genético. OBJETIVOS Describir el fenómeno de electroforesis y las técnicas para producirla Discriminar los factores que influyen en la movilidad electroforética Justificar el uso de un campo eléctrico en el proceso de separación de biomoléculas X.1 FUNDAMENTOS TEORICOS Mediante la electroforesis es posible separar moléculas biológicas en dependencia fundamentalmente de su carga bajo la influencia de un campo eléctrico. La electroforesis es un método analítico semipreparativo, en el que se separan biomoléculas, en dependencia entre otros factores de su carga y bajo la acción de un campo eléctrico, fue empleado por primera vez por Tiselius en el año La electroforesis es la migración de solutos iónicos bajo la influencia de un campo eléctrico; estas partículas migran hacia el cátodo o ánodo (electrodos y +), en dependencia de una combinación de su carga, peso molecular y estructura tridimensional. Es de destacar que a escala analítica, los métodos electroforéticos son de alta sensibilidad, poder de resolución y versatilidad, y sirven como método de separación de mezclas complejas de ácidos nucleicos, proteínas y otras biomoléculas, donde aportan un potente criterio de pureza. Se pueden conocer también mediante estas técnicas, las características ácidobásicas de las proteínas presentes en un extracto crudo, lo que da la información necesaria si se pretende realizar una separación cromatográfica basada en diferencias de carga. Es útil además para determinar otros parámetros como peso molecular, punto isoeléctrico y número de cadenas polipeptídicas de las proteínas. La velocidad de migración (v) de la partícula es directamente proporcional al producto de su carga efectiva (q) y el gradiente de potencial eléctrico (E) e 95
2 inversamente proporcional al coeficiente de fricción (f) relativo a la talla y forma de la molécula, o sea, a la resistencia que le ofrece el medio. v = q E / f La movilidad electroforética (Me) es un caso particular de la velocidad de migración de un ión, cuando se aplica un campo eléctrico de 1 V/cm. Su signo es igual al de la carga de la partícula. La movilidad, (u), se define como la velocidad que toma la partícula por unidad de campo, o u= v / E = q / f como la movilidad depende del coeficiente de fricción, que a su vez es función de ciertos parámetros físicos de las moléculas, el valor de u puede dar información acerca del tamaño y forma de la partícula. La velocidad de migración electroforética depende de la densidad de carga, de la molécula (relación carga / peso), del voltaje aplicado y de la porosidad del gel de electroforesis. El voltaje no se puede incrementar indiscriminadamente porque se genera un excesivo calor. En contraste, al aplicar bajo voltaje puede ocurrir una pobre separación, por causa de la difusión por tiempo muy prolongado de la corrida electroforética. La mayoría de las biomacromoléculas (proteínas, ácidos nucleicos y polisacáridos) poseen determinada carga eléctrica con grupos aniónicos y catiónicos capaces de disociarse. La carga neta de la partícula está dada por el ph del medio y puede ser modificada por la interacción con pequeñas moléculas de iones u otras macromoléculas. De lo anterior se deduce que el ph influye sobre la velocidad de migración de las moléculas. En el punto isoeléctrico de la biomolécula, ph al cual su carga neta es cero, esta no migra. Por debajo del punto isoeléctrico tiene carga neta positiva y migra hacia el cátodo, y por encima del punto isoeléctrico tienen carga neta negativa y migra hacia el ánodo. X.1.2 Fundamentos y Gráficos Cuando una mezcla de moléculas ionizadas y con una carga eléctrica neta son colocadas en una campo eléctrico, éstas experimentarán una fuerza de atracción hacia el polo que posea carga opuesta: + Neg + Pos 96
3 Así, si se deja transcurrir un cierto tiempo las moléculas cargadas positivamente se desplazarán hacia el cátodo (el polo negativo) y aquellas cargadas negativamente se desplazarán hacia el ánodo (el polo positivo). El movimiento de las moléculas está gobernado también por dos fuerzas adicionales; por un lado, la fricción con el solvente dificultará este movimiento (es decir, al moverse los solutos chocarán con las moléculas de solvente que están en su camino), lo que genera una fuerza que se opone al movimiento; por otro lado, las moléculas tienen a moverse en forma aleatoria (movimiento browniano) debido a que poseen energía cinética propia. Esto se denomina difusión y sigue la llamada ley de Fick. La energía cinética de las moléculas aumenta con la temperatura, por ello a mayor temperatura mayor difusión. fricción atracción + Pos electrostática + ( +) + Movimiento Browniano La suma de todas estas fuerzas provoca que las moléculas no migren de una manera homogénea, de tal manera que, si la moléculas son colocadas en un cierto lugar de la solución, los iones comenzarán a moverse formando un frente cuya anchura aumentará con el tiempo. + frente + Efecto de + la difusión Atracción Electrostática Para reducir la anchura de este frente podemos reducir el movimiento de las moléculas empleando un medio que oponga más resistencia a dicho movimiento. Una forma común de hacer esto es formar un gel. El gel consiste de un polímero soluble de muy alto peso molecular que atrapa moléculas de agua y forma un tamiz molecular que dificulta el movimiento de los solutos. Consecuentemente, la migración electroforética de las moléculas será más lenta, pero el ensanchamiento del frente se verá reducido también. Si ahora aumentamos la 97
4 intensidad del campo eléctrico, podemos acelerar la migración molecular, pero no por ello variará la difusión y nuestro frente migrará de un modo cada vez más compacto. Así, podemos mejorar la definición del frente aumentando la diferencia de potencial entre los polos y esto estará limitado tan sólo la capacidad de la solución para disipar el calor generado por el paso de la corriente eléctrica. Esto último, debido a que si el calor se acumula se puede hacer hervir a la solución, e incluso descomponer el gel y/o los solutos. La presencia del gel tiene una consecuencia adicional, ya que aquellas moléculas de mayor tamaño hallarán mayor resistencia al avanzar a través de los poros del gel que aquellas moléculas pequeñas. Por lo tanto, la fricción que se observa durante el movimiento electroforético en un gel depende de la masa y la forma de la molécula, en adición a su carga eléctrica. Aunque el solvente puede, por si solo, producir una fricción diferente sobre diversas moléculas, su efecto es muy poco apreciable cuando no existe el entramado del gel. X.1.3 Circunstancias que pueden modificar la electroforesis 1. El ph: uno de los problemas más frecuentes vienen dados por la naturaleza del propio electrolito, ya que el más habitual es el NaCl o el TrisHCl, ambos presentan el ion Cl, que al verse sometido a un campo eléctrico se convierte en un radical libre, y dos de estas forman cloro molecular, que combinado con el agua forman HCl, que se disocia enseguida formando más ion cloruro que continua la reacción, y ClOH, que se disocia formando ClO y protones, que junto a los de la disociación del clorhídrico se dirigen al polo negativo aumentando el ph de la disolución, que aunque está tamponada hay que tener cuidado no dañe la muestra. 2. El Borato: uno de los tampones que se suelen utilizar es el del borato, que presenta el inconveniente de no ser del todo inerte. El resultado, por tanto de una electroforesis puede ser el de unas bandas desdobladas correspondientes a una sola proteína, una pura y una modificada por el borato. La forma de averiguar si en efecto se trata de una modificación o si son dos proteínas se asemeja mucho al que ya vimos en centrifugación, y se trata de recoger una las bandas y volverla a correr, de modo que si se vuelven a obtener dos bandas se tratará de una modificación y si sólo aparece una serán dos proteínas distintas. 3. El calentamiento: durante le proceso de electroforesis, el gel se va calentando debido al paso de corriente eléctrica (Efecto Joule). Este proceso puede llegar a desnaturalizar proteínas, de modo que podrían falsear la electroforesis. X.1.4 Tipos de Electroforesis Existen numerosos métodos de electroforesis pero de manera más general pueden clasificarse en: Electroforesis convencional Electroforesis capilar. 98
5 X Electroforesis Convencional La electroforesis convencional ha sido utilizada durante muchos años para separar especies complejas de elevado peso molecular de interés biológico y bioquímico. Las separaciones se llevan a cabo sobre una capa delgada y plana o placa de un gel semisólido y poroso que contiene un tampón acuoso en el interior de sus poros. Esta será la sustancia encargada de ofrecer resistencia al movimiento de las moléculas, controlando así su migración uniforme. Mediante esta técnica se pueden separar varias muestras simultáneamente. Dichas muestras se depositan sobre el gel, se aplica un potencial de corriente continua a través del mismo durante un tiempo fijo. Cuando las separaciones se han completado se interrumpe el paso de corriente y las especies separadas se tiñen para visualizarse. La electroforesis en gel es muy utilizada en la detección, control de pureza, caracterización, cuantificación (por comparación con controles) así como preparación y purificación (por extracción de bandas desde el gel) de moléculas y fragmentos de DNA y RNA. Los geles que se emplean son geles tridimensionales de polímeros ramificados que tienen los espacios entre ramificación rellenos de líquido. Las redes de polímeros no solo reprimen la convección sino que también actúan como cribas que pueden retardar y hasta bloquear la migración de los analitos poliméricos más grandes. En cambio los iones pequeños pueden moverse libremente a través de la estructura porosa del gel. De este modo la electroforesis en gel tiene dos mecanismos de separación: electroforesis, que separa por la relación carga/tamaño y tamizado, que separa mayormente por tamaño. Los geles más comunes son agarosa y poliacrilamida. La agarosa es un polímero derivado de un polisacárido neutro, que gracias a su poder de gelificación y propiedades físicoquímicas, lo han convertido en el soporte más común para electroforesis en el área de Biología Molecular. La poiliacrilamida es un polímero formado a partir de acrilamida y N,N metilenbisacrilamida. La concentración de ambos reactivos define el grado de reticulación del gel. Ambos geles tienen en común que adquieren la misma forma y están prácticamente libres de cargas iónicas. Esto es importante para evitar que la disolución tampón se desplace por el gel cuando se active el campo eléctrico. Este tipo de electroforesis es ampliamente utilizado en la esfera biotecnológica, aspecto este que se ha podido comprobar a partir de los numerosos resultados que se encuentran en la literatura más actual. Existen otros tipos de electroforesis en gel como son la electroforesis en geles desnaturalizantes de agarosa, electroforesis en campo pulsado y la electroforesis preparativa. Estas técnicas no son de aplicación tan general pero no por ello dejan de ser importantes. X Electroforesis Capilar (CE) La electroforesis capilar es una técnica alternativa de la electroforesis convencional y surge debido a que la velocidad de separación y resolución de los compuestos mejora a medida que aumenta el campo eléctrico aplicado. Esta afirmación no nos permite aumentar el potencial, aun sabiendo que existe una dependencia directa de éste con el campo eléctrico. Esto se debe a que el calentamiento por el efecto Joule aumenta hasta afectar la calidad de la separación. Para solucionar esta dificultad es que se realiza la electroforesis en 99
6 un tubo capilar con un diámetro interno inferior a 0,1 mm y una longitud de 50 cm a 1 m. lo cual aumenta de manera considerable la disipación del calor generado y por lo tanto permite incrementar el voltaje aplicado. El mecanismo de separación está basado en las relaciones carga/masa de los analitos. Su utilidad está en la separación de proteínas y péptidos entre otras sustancias. Entre las ventajas que ofrece la electroforesis capilar se puede apuntar que da lugar a separaciones con volúmenes de muestra extraordinariamente pequeños (de 0,1 a 10 nl), en contraste con la electroforesis convencional en la cual se emplean volúmenes de muestra en el orden de los µl, con una elevada resolución y rapidez. Tipos de electroforesis capilar: La electroforesis capilar en gel combina la técnica de electroforesis con la cromatografía de reparto. Permite la separación en función de la migración electroforética y también en función del peso molecular de las muestras. Se lleva a cabo en una matriz polimérica con estructura de gel poroso, cuyos poros contienen una mezcla tampón donde ocurre la separación. Estos geles están contenidos en un tubo capilar. Los geles utilizados son también de agarosa y poliacrilamida. Electroforesis capilar de zona: es una de las técnicas más importantes y más utilizada debido, probablemente a su simplicidad y elevado poder de separación. Está basada en la separación de los analitos según la relación carga/tamaño. En esta técnica la composición del tampón es constante en toda la zona de separación. El potencial aplicado hace que los diferentes componentes iónicos de la mezcla migren cada uno según su propia movilidad y se separen en zonas que puedan estar completamente resueltas o parcialmente solapadas. Entre las zonas completamente resueltas hay huecos ocupados por el tampón. Su principal inconveniente es que no permite separar los compuestos neutros. Enfoque isoeléctrico: la diferencia de los puntos isoeléctricos de las proteínas se aprovecha para separarlas por el método de isoelectroenfoque. Este método se basa en establecer un gradiente de ph estable en una disolución o gel. Este gradiente se establece por un conjunto de tampones especiales llamados anfolitos que migran por sí mismos hasta que alcanzan sus puntos isoeléctricos. Cuando al gradiente de ph se le introduce una proteína, cada zona intercambia protones con la muestra proteica, generando una separación isoeléctrica conocida como electroenfocado. La isotacoforesis significa electroforesis a velocidad uniforme. Esto significa que el tiempo de recorrido en el capilar bajo condiciones isotacoforéticas es independiente de la velocidad. Es una técnica de separación por desplazamiento. Antes de iniciar la corrida, el capilar se debe llenar con un electrolito líder o guía en un extremo. Este debe tener una gran movilidad y debe ser mayor que la de los componentes a separar. Luego se introduce la muestra seguida del electrolito terminal o cola, cuya movilidad debe ser menor que cualquiera de los componentes de la muestra. 100
7 X.2 PROCEDIMIENTOS Análisis de la variabilidad genética utilizando electroforesis en gel El objetivo de esta técnica es, mediante un método bioquímico, basado en reacciones enzimáticas poder analizar de forma rápida la variabilidad genética que podemos encontrarnos en una población determinada, hay varios métodos para esto, como por ejemplo mediante el análisis de los fenotipos (hay que tener en cuenta los factores ambientales), mediante el estudio de los cromosomas, o mediante la Clonación y posterior secuenciación de ADN, siento este método muy preciso pero a la vez muy costoso. Como decimos, en esta practica utilizaremos la electroforesis de enzimas en gel, y aplicaremos una afirmación teórica, en la que el producto de un gen, será un polipéptido, es decir una proteína, que en nuestro caso, tendrá actividad enzimática. El método consiste en obtener las enzimas de raíz de bulbo( Muscaris comosum) mediante aplastamiento directo, empaparlas en papel secante, e introducir estos papeles en el gel, posteriormente habrá que someterlo a una electroforesis para lograr la migración de las proteínas que será diferencial dependiendo esta diferencia de la carga eléctrica de la proteína. Una vez esto, procederemos a cortar en láminas de 1 mm del bloque de gel sacando tres que serán las que utilizaremos para el experimento, posteriormente induciremos la reacción enzimática, teñiremos, y valoraremos los resultados. X.3.1 Preparado de la Practica Una vez resumido a grandes rasgos lo que pretendemos con esta practica, tenemos que proceder a la preparación de todos los elementos necesarios para la misma. 1. Preparación del gel de Almidón: Lo utilizamos ya procesado comercialmente, preparamos el tampón y mezclamos con el almidón (en polvo, a una concentración del 1012%) llevamos a hervir y apreciamos en ese momento como se densifica notablemente la muestra. En este momento se aparta del fuego, y se vierte en un molde de 5 mm de altura, dejamos solidificar unas cuantas horas. 2. Obtención de las proteínas: En este caso en particular mediante aplastamiento de las raíces que teníamos en remojo, sacaremos las proteínas que quedaran empapadas en tiritas de papel del tipo secante. 3. Inserción de las proteínas al gel: Se hace una ranura a todo el largo del gel, y se van poniendo los papeles de filtro, uno a continuación de otro, pero respetando una separación, ademas se nace necesario que estos toquen el fondo del molde, y ademas pondremos como frente de control que es el azul de bromofenol, que migrará mas rápido que cualquier proteína. 4. Electroforesis: Se hace con un método discontinuo, utilizando LiOH/Borato 0,02 M. PH 8.1, como tampón de electrodos, Tris/Citratos 0.05M ph 8.3, en lo que se refiere a tampón de gel. cristal en la parte superior y realizar el proceso en frío. Respecto a la las características eléctricas se realiza a 250 V y a 25 ma, una vez establecidas las conexiones y en frío, comienzan a migrar los proteínas. Pasadas unas horas, se procede al corte del gen, ( a un milímetro), logrando de esta manera tres planchas de gel. 101
8 Electrodos (LiOH/Bórico): LiOH gramos Acido Borico gramos Agua desionizada...1 Litro. Gel (Tris/Citrato): TRIS gr. Acido cítrico monohidrato gr. Tampón de electrodos ml. Agua desionizada ml 5. Reacción y tinción: Evidentemente ademas de la reacción enzimatica, tenemos que teñir la muestra para poder verla, aplicando estos protocolos Tinción para la Alcohol deshidrogenasa: Tris CLH 0.1 ph a 8.0, (50 ml) Cl2Mg 0.1 M (1 ml) Etanol absoluto (3 ml) NAD ( 0 Mg) PMS Tinción de GlutamatoOxalacetatoTransaminasa: Solución sustrato (25 ml): * AlfaCetoGlutámico: (36.5 mg) * LAspartico: (125 gr.) * PVP: (0.5 gr) *EDTA (50 mg) * PO4HNa (1.42 g.) * Agua desionizada (50 ml) 102
9 Agua desionizada (25 ml) Fast Blue. Esterasas: Betanaftilacetato 1% en acetona, (3ml) AlfaNaftilacetato, 1% en acetona, (3ml) FastBlueRR (50 mg) FastBlueGBC (50 mg) Tampón fosfato: *PO4H2K (0.92 gr) *PO4HNa (0.48g) Agua desionizada (100 Mililitros) X.3.2 Interpretación de los resultados Una vez que tenemos todo lo referente al laboratorio finalizado, nos queda lo mas importante, ver e interpretar teóricamente lo que vemos, aplicar los conocimientos y razonar los resultados, quizá con una sola frase, podamos resumir perfectamente que podemos interpretar: Si dos proteínas tienen la misma movilidad, será que los alelos son iguales, y en consecuencia el organismo será homizigoto, por el contrario, a movilidad desigual, los alelos serán diferentes aceptando en este caso que el individuo es heterozigoto. En realidad lo que vemos es una serie de puntos mas o menos alineados, en los que dependiendo de estos puntos, podemos fácilmente determinar la homozigosis o no del individuo, combinando muchos individuos, podremos entonces analizar la variabilidad genética de una determinada población, también con este método podremos calcular la frecuencia. Sobre el revelado hemos apreciado individuos homozigotos y heterozigotos, simplemente viendo los puntos que han quedado en la placa, hay que tener cuidado con los artefactos propios del revelado, y tener astucia para reconocerlos y descartarlos. 103
ELECTROFORESIS Fundamento.
 ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS. Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo (+)
 GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
Electroforesis de proteínas
 Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
Introducción. Electroforesis zonal Campo aplicado a un soporte estabilizante Muestra dispuesta sobre una zona reducida del soporte
 Introducción Técnica analítica separativa: Transporte de moléculas cargadas bajo la acción de un campo eléctrico Movilidad electroforética depende de: La carga de la molécula Depende del medio ph Fuerza
Introducción Técnica analítica separativa: Transporte de moléculas cargadas bajo la acción de un campo eléctrico Movilidad electroforética depende de: La carga de la molécula Depende del medio ph Fuerza
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B
 ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS
 ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
FUNDAMENTOS. ELECTROFORESIS/ Versión 3.0/ MÓDULO 3/ CÁTEDRA DE FÍSICA/ FFYB/ UBA/
 FUNDAMENTOS. ELECTROFORESIS/ Versión 3.0/ MÓDULO 3/ CÁTEDRA DE FÍSICA/ FFYB/ UBA/ La electroforesis es una técnica separativa que se basa en el fenómeno de migración diferencial que experimentan partículas
FUNDAMENTOS. ELECTROFORESIS/ Versión 3.0/ MÓDULO 3/ CÁTEDRA DE FÍSICA/ FFYB/ UBA/ La electroforesis es una técnica separativa que se basa en el fenómeno de migración diferencial que experimentan partículas
PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA
 INTRODUCCIÓN PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA La electroforesis es una técnica que permite separar moléculas cargadas eléctricamente, entre las cuales se encuentran los ácidos nucleicos (DNA
INTRODUCCIÓN PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA La electroforesis es una técnica que permite separar moléculas cargadas eléctricamente, entre las cuales se encuentran los ácidos nucleicos (DNA
Técnicas de Estudio de las células
 Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon.
 Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
Electroforesis de proteínas en geles de poliacrilamida
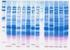 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo
 Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas.
 Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas. La selección de técnicas de purificación depende de las propiedades de las proteínas. Características
Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas. La selección de técnicas de purificación depende de las propiedades de las proteínas. Características
Electroforesis capilar
 Electroforesis capilar LUIS ENRIQUE MENDOZA POSTGRADO EN INGENIERÍA A BIOMÉDICA UNIVERSIDAD DE LOS ANDES MÉRIDA VENEZUELA NOVIEMBRE 2006 Electroforesis capilar AGENDA RESUMEN TIPOS DE ELECTROFORESIS EQUIPO
Electroforesis capilar LUIS ENRIQUE MENDOZA POSTGRADO EN INGENIERÍA A BIOMÉDICA UNIVERSIDAD DE LOS ANDES MÉRIDA VENEZUELA NOVIEMBRE 2006 Electroforesis capilar AGENDA RESUMEN TIPOS DE ELECTROFORESIS EQUIPO
ELECTROFORESIS. Objetivo de la clase. *fundamentos *procedimientos *algunas aplicaciones. Conocer los métodos electroforéticos
 ELECTROFORESIS Objetivo de la clase Conocer los métodos electroforéticos *fundamentos *procedimientos *algunas aplicaciones Definición de electroforesis Proceso de separación que se basa en la diferente
ELECTROFORESIS Objetivo de la clase Conocer los métodos electroforéticos *fundamentos *procedimientos *algunas aplicaciones Definición de electroforesis Proceso de separación que se basa en la diferente
Purificación de Proteínas Parte II
 Purificación de Proteínas Parte II Fase I. Obtención del extracto crudo Lisis celular. Válido para células sin pared celular como las células de tejidos animales, pero no es suficiente para células vegetales
Purificación de Proteínas Parte II Fase I. Obtención del extracto crudo Lisis celular. Válido para células sin pared celular como las células de tejidos animales, pero no es suficiente para células vegetales
Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS
 Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS DICIEMBRE 2006 Tratamiento de Imágenes por Computadora Proyecto
Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS DICIEMBRE 2006 Tratamiento de Imágenes por Computadora Proyecto
Al igual que en la centrifugación también hay dos criterios de separación con el mismo concepto:
 Electroforesis En la técnica de separación anterior hemos utilizado la fuerza centrífuga para que asociada a la diferencia de masa o densidad de las partículas a separar nos las diferencie, ahora vamos
Electroforesis En la técnica de separación anterior hemos utilizado la fuerza centrífuga para que asociada a la diferencia de masa o densidad de las partículas a separar nos las diferencie, ahora vamos
CROMATOGRAFÍA DE AMINOÁCIDOS
 CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS. Es un ácido capaz de formar sales con iones cargados
 Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Tema 6 Cuantificación de proteínas
 Tema 6 Cuantificación de proteínas Procedimiento de estudio de proteínas Selección de fuente Fraccionamiento de células Centrifugación Cromatografía Cromatografía en capa fina Cromatografía en columna
Tema 6 Cuantificación de proteínas Procedimiento de estudio de proteínas Selección de fuente Fraccionamiento de células Centrifugación Cromatografía Cromatografía en capa fina Cromatografía en columna
Técnicas de Caracterización y purificación
 Técnicas de Caracterización y purificación hidrofobicidad carga Propiedades de las proteínas utilizadas para caracterizar y purificar Carga Tamaño Forma Actividad biologica Hidrofobicidad PM Estabilidad
Técnicas de Caracterización y purificación hidrofobicidad carga Propiedades de las proteínas utilizadas para caracterizar y purificar Carga Tamaño Forma Actividad biologica Hidrofobicidad PM Estabilidad
Monitoreo de un proceso de purificación de proteínas. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
Técnicas de Biología Molecular. Biol 3051L
 Técnicas de Biología Molecular Biol 3051L Objetivos El cortar el DNA con enzimas de restricción y hacer corridas de geles usando electroforesis es muchas veces el primer paso para estudiar un gen. En este
Técnicas de Biología Molecular Biol 3051L Objetivos El cortar el DNA con enzimas de restricción y hacer corridas de geles usando electroforesis es muchas veces el primer paso para estudiar un gen. En este
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa.
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
Análisis Instrumental TEMA 10 Y 11. Maracaibo, febrero Profa. Cristina Uzcátegui Arrieta
 Análisis Instrumental TEMA 10 Y 11 Maracaibo, febrero 2018 Profa. Cristina Uzcátegui Arrieta QUÉ ES LA CROMATOGRAFÍA? Agrupa un conjunto importante y diverso de métodos, que permite a los científicos separar
Análisis Instrumental TEMA 10 Y 11 Maracaibo, febrero 2018 Profa. Cristina Uzcátegui Arrieta QUÉ ES LA CROMATOGRAFÍA? Agrupa un conjunto importante y diverso de métodos, que permite a los científicos separar
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa
 Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
PURIFICACIÓN DE ENZIMAS
 PURIFICACIÓN DE ENZIMAS MÉTODOS GENERALES DE EXTRACCIÓN Y PURIFICACIÓN CAMILO BECERRA (TUQ) MARÍA FERNANDA FERRERO (TUQ) INTRODUCCIÓN EN LA NATURALEZA EXISTEN CANTIDADES INIMAGINABLES DE COMPUESTOS, PERO
PURIFICACIÓN DE ENZIMAS MÉTODOS GENERALES DE EXTRACCIÓN Y PURIFICACIÓN CAMILO BECERRA (TUQ) MARÍA FERNANDA FERRERO (TUQ) INTRODUCCIÓN EN LA NATURALEZA EXISTEN CANTIDADES INIMAGINABLES DE COMPUESTOS, PERO
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN.
 Trabajo Práctico 2.2 TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN. Desde el reconocimiento del ADN como "la molécula de la vida", se conoce que en ella se encuentran cifradas las instrucciones que
Trabajo Práctico 2.2 TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN. Desde el reconocimiento del ADN como "la molécula de la vida", se conoce que en ella se encuentran cifradas las instrucciones que
Biocromatografía: intercambio iónico
 Biocromatografía: intercambio iónico Intercambio Iónico Columnas TSK-GEL El método más utilizado en la purificación de proteínas y otras moléculas que presenten carga eléctrica es la Cromatografía de Intercambio
Biocromatografía: intercambio iónico Intercambio Iónico Columnas TSK-GEL El método más utilizado en la purificación de proteínas y otras moléculas que presenten carga eléctrica es la Cromatografía de Intercambio
Los principales mecanismos que intervienen en la separación cromatográfica son:
 TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
Proyecto de Fin de Cursos
 Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
PROBLEMAS ÁCIDO-BASE. 2-1 Indique si la disolución acuosa de las siguientes sales es ácida, básica o neutra. Suponer que todas son 0,1 M.
 PROBLEMAS ÁCIDO-BASE 2-1 Indique si la disolución acuosa de las siguientes sales es ácida, básica o neutra. Suponer que todas son 0,1 M. a) Cloruro potásico b) Fluoruro de metilamonio c) Hipoclorito sódico
PROBLEMAS ÁCIDO-BASE 2-1 Indique si la disolución acuosa de las siguientes sales es ácida, básica o neutra. Suponer que todas son 0,1 M. a) Cloruro potásico b) Fluoruro de metilamonio c) Hipoclorito sódico
MATERIA SERES VIVOS QUE ES LA MATERIA? UNIDAD 2 PARTE 1 LA MATERIA ES TODO AQUELLO QUE OCUPA UN LUGAR EN EL ESPACIO, ES DECIR TIENE MASA Y VOLUMEN
 UNIDAD 2 COMPOSICIÓN N QUÍMICA DE LOS SERES VIVOS PARTE 1 MATERIA QUE ES LA MATERIA? LA MATERIA ES TODO AQUELLO QUE OCUPA UN LUGAR EN EL ESPACIO, ES DECIR TIENE MASA Y VOLUMEN Puede estar en diferentes
UNIDAD 2 COMPOSICIÓN N QUÍMICA DE LOS SERES VIVOS PARTE 1 MATERIA QUE ES LA MATERIA? LA MATERIA ES TODO AQUELLO QUE OCUPA UN LUGAR EN EL ESPACIO, ES DECIR TIENE MASA Y VOLUMEN Puede estar en diferentes
Purificación de proteínas
 Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
1.-EQUILIBRIOS IÓNICOS EN DISOLUCIONES ACUOSAS.
 TEMA 5 EQUILIBRIOS IÓNICOS y SISTEMAS TAMPÓN. GUIÓN. ( 2 sesiones). 1.- EQUILIBRIOS IÓNICOS EN DISOLUCIÓN ACUOSA 2.- CONCEPTO DE SISTEMA TAMPÓN. 3.- IMPORTANCIA DE LA REGULACIÓN DEL PH FISIOLÓGICO. 4.-
TEMA 5 EQUILIBRIOS IÓNICOS y SISTEMAS TAMPÓN. GUIÓN. ( 2 sesiones). 1.- EQUILIBRIOS IÓNICOS EN DISOLUCIÓN ACUOSA 2.- CONCEPTO DE SISTEMA TAMPÓN. 3.- IMPORTANCIA DE LA REGULACIÓN DEL PH FISIOLÓGICO. 4.-
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
DISOLUCIONES QUÍMICAS
 DISOLUCIONES QUÍMICAS Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
DISOLUCIONES QUÍMICAS Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
FISICA QUIMICA
 FISICA QUIMICA 2018-1 DESARROLLO DE LA TEORIA DE LA DISOCIACION ELECTROLITICA. CONDUCCION DE LA ELECTRICIDAD. CONDUCCION ELECTROLITICA. ELECTROLISIS SOLUCIONES Se trata de un caso particular de dispersiones.
FISICA QUIMICA 2018-1 DESARROLLO DE LA TEORIA DE LA DISOCIACION ELECTROLITICA. CONDUCCION DE LA ELECTRICIDAD. CONDUCCION ELECTROLITICA. ELECTROLISIS SOLUCIONES Se trata de un caso particular de dispersiones.
ESTRUCTURA, PROPIEDADES Y FUNCIÓN DE ÁCIDOS NUCLÉICOS. Aislamiento de plásmido
 ESTRUCTURA, PROPIEDADES Y FUNCIÓN DE ÁCIDOS NUCLÉICOS Aislamiento de plásmido Transferencia de material genético intercelular Transformación Conjugación Transformación Transducción Existe algún mecanismo
ESTRUCTURA, PROPIEDADES Y FUNCIÓN DE ÁCIDOS NUCLÉICOS Aislamiento de plásmido Transferencia de material genético intercelular Transformación Conjugación Transformación Transducción Existe algún mecanismo
2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS. 25 Agosto, 2009
 2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS. 25 Agosto, 2009 El genoma haploide de un humano contiene 20,000-25,000 genes que codifican a proteínas. Transportadores Enzimas Receptores Estructurales Hormonas
2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS. 25 Agosto, 2009 El genoma haploide de un humano contiene 20,000-25,000 genes que codifican a proteínas. Transportadores Enzimas Receptores Estructurales Hormonas
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987)
 EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
INTRODUCCIÓN 1 OBJETIVOS 11. CAPÍTULO I 15 Fundamentos de la Electroforesis Capilar
 INTRODUCCIÓN 1 OBJETIVOS 11 CAPÍTULO I 15 Fundamentos de la Electroforesis Capilar 1. CARACTERÍSTICAS DE LA ELECTROFORESIS CAPILAR 17 1.1. Características generales 17 1.2. Descripción del equipo 19 1.3.
INTRODUCCIÓN 1 OBJETIVOS 11 CAPÍTULO I 15 Fundamentos de la Electroforesis Capilar 1. CARACTERÍSTICAS DE LA ELECTROFORESIS CAPILAR 17 1.1. Características generales 17 1.2. Descripción del equipo 19 1.3.
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
ANTECEDENTES. Durante las últimas décadas, la electroforesis en geles de. poliacrilamida ha sido la técnica de elección para el análisis d e la
 5 ANTECEDENTES Durante las últimas décadas, la electroforesis en geles de poliacrilamida ha sido la técnica de elección para el análisis d e la composición proteica de un determinado tipo de célula y el
5 ANTECEDENTES Durante las últimas décadas, la electroforesis en geles de poliacrilamida ha sido la técnica de elección para el análisis d e la composición proteica de un determinado tipo de célula y el
CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE MOVIMIENTO PROF. JOSE MAYORGA
 UNIVERSIDAD DE LOS ANDES FACULTAD DE INGENIERIA INGENIERIA QUIMICA INTRODUCCIÓN A LA INGENIERIA QUIMICA CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE
UNIVERSIDAD DE LOS ANDES FACULTAD DE INGENIERIA INGENIERIA QUIMICA INTRODUCCIÓN A LA INGENIERIA QUIMICA CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas.
 La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
PRUEBA EXTRAORDINARIA DE FÍSICA Y QUÍMICA DE 2º ESO CONTENIDOS, CRITERIOS DE EVALUACIÓN Y ESTÁNDARES DE APRENDIZAJE
 PRUEBA EXTRAORDINARIA DE FÍSICA Y QUÍMICA DE 2º ESO CONTENIDOS, CRITERIOS DE EVALUACIÓN Y ESTÁNDARES DE APRENDIZAJE BLOQUE DE APRENDIZAJE I: LA ACTIVIDAD CIENTÍFICA UNIDAD 1 1. Formula hipótesis para explicar
PRUEBA EXTRAORDINARIA DE FÍSICA Y QUÍMICA DE 2º ESO CONTENIDOS, CRITERIOS DE EVALUACIÓN Y ESTÁNDARES DE APRENDIZAJE BLOQUE DE APRENDIZAJE I: LA ACTIVIDAD CIENTÍFICA UNIDAD 1 1. Formula hipótesis para explicar
Profesor: Carlos Gutiérrez Arancibia
 Objetivo: Reconocer las soluciones químicas y sus características generales, a través de estudios cualitativos y cuantitativos referidas al concepto de concentración en diversas disoluciones. Profesor:
Objetivo: Reconocer las soluciones químicas y sus características generales, a través de estudios cualitativos y cuantitativos referidas al concepto de concentración en diversas disoluciones. Profesor:
PURIFICACIÓN DE PROTEÍNAS
 PURIFICACIÓN DE PROTEÍNAS ESQUEMA DE PURIFICACIÓN DE UNA PROTEÍNA tejido vegetal animal homogeneizar cultivo celular bacterias levaduras células mamíferos PREPARACIÓN EXTRACTO crudo fraccionamiento subcelular
PURIFICACIÓN DE PROTEÍNAS ESQUEMA DE PURIFICACIÓN DE UNA PROTEÍNA tejido vegetal animal homogeneizar cultivo celular bacterias levaduras células mamíferos PREPARACIÓN EXTRACTO crudo fraccionamiento subcelular
Parte B Módulo 1 y 2. Abril 2016
 Parte B Módulo 1 y 2 Abril 2016 La longitud de una columna en la que el soluto experimenta un equilibrio completo entre las dos fases Eficiencia de una separación cromatográfica número de platos teóricos
Parte B Módulo 1 y 2 Abril 2016 La longitud de una columna en la que el soluto experimenta un equilibrio completo entre las dos fases Eficiencia de una separación cromatográfica número de platos teóricos
cromatografía 03/07/2012 INTRODUCCIÓN Etapas de un análisis cuantitativo Curso: Química Analítica II Loreto Ascar 2012 Proceso Analítico
 cromatografía Curso: Química Analítica II Loreto Ascar 2012 INTRODUCCIÓN Cómo determinar un analito en una muestra problema? X Proceso Analítico Etapas de un análisis cuantitativo Elección del método Obtención
cromatografía Curso: Química Analítica II Loreto Ascar 2012 INTRODUCCIÓN Cómo determinar un analito en una muestra problema? X Proceso Analítico Etapas de un análisis cuantitativo Elección del método Obtención
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
CLASIFICACIONES DE LA MATERIA. Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia.
 CLASIFICACIONES DE LA MATERIA Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia. LA MATERIA Es todo aquello que ocupa un sitio en el espacio, se puede tocar,
CLASIFICACIONES DE LA MATERIA Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia. LA MATERIA Es todo aquello que ocupa un sitio en el espacio, se puede tocar,
El agua es u solvente ampliamente utilizado, tanto por su propiedad polar, como también por su carácter inerte frente a muchos solutos.
 SOLUCIONES IONICAS Una solución iónica es aquella en la cual el soluto al disolverse en el solvente se descompone o disicia en iones ( positivos o cationes y negativos o aniones) un ejemplo son las soluciones
SOLUCIONES IONICAS Una solución iónica es aquella en la cual el soluto al disolverse en el solvente se descompone o disicia en iones ( positivos o cationes y negativos o aniones) un ejemplo son las soluciones
TEMA 6: PROTEÍNAS. Definición de proteínas y aminoácidos
 TEMA 6: PROTEÍNAS Dra. Mariana L. Ferramola Bioquímica Lic. en Enfermería 2016 Definición de proteínas y aminoácidos Las proteínas son macromoléculas de gran abundancia. Son polímeros formados por monómeros
TEMA 6: PROTEÍNAS Dra. Mariana L. Ferramola Bioquímica Lic. en Enfermería 2016 Definición de proteínas y aminoácidos Las proteínas son macromoléculas de gran abundancia. Son polímeros formados por monómeros
PRECIPITACIÓN EN BREVE. Francisco José Guerra Millán
 PRECIPITACIÓN EN BREVE Francisco José Guerra Millán www.pacopepe.com.mx BREVE DESCRIPCIÓN La precipitación consiste en la separación química de los componentes de una disolución. Esta separación se realiza
PRECIPITACIÓN EN BREVE Francisco José Guerra Millán www.pacopepe.com.mx BREVE DESCRIPCIÓN La precipitación consiste en la separación química de los componentes de una disolución. Esta separación se realiza
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN. Ingeniería Ambiental
 TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
ESTRUCTURA, PROPIEDADES Y FUNCIÓN DE ÁCIDOS NUCLÉICOS. Aislamiento de plásmido. M. en C. J. Abraham León Domínguez
 ESTRUCTURA, PROPIEDADES Y FUNCIÓN DE ÁCIDOS NUCLÉICOS Aislamiento de plásmido M. en C. J. Abraham León Domínguez La transformación bacteriana es un proceso muy útil en biología molecular. Conjugación Transformación
ESTRUCTURA, PROPIEDADES Y FUNCIÓN DE ÁCIDOS NUCLÉICOS Aislamiento de plásmido M. en C. J. Abraham León Domínguez La transformación bacteriana es un proceso muy útil en biología molecular. Conjugación Transformación
Caracterización de las propiedades de transporte de separadores utilizados en reactores electroquímicos
 PRESENTACIÓN Caracterización de las propiedades de transporte de separadores utilizados en reactores electroquímicos Valentín Pérez Herranz Departamento de Ingeniería Química y Nuclear. Instituto de Seguridad
PRESENTACIÓN Caracterización de las propiedades de transporte de separadores utilizados en reactores electroquímicos Valentín Pérez Herranz Departamento de Ingeniería Química y Nuclear. Instituto de Seguridad
Nombre Periodo Fecha. CONCEPTO CLAVE Todos los seres vivos tienen como base los átomos y sus interacciones.
 Sección 1: Los átomos, los iones y las moléculas CONCEPTO CLAVE Todos los seres vivos tienen como base los átomos y sus interacciones. VOCABULARIO átomo ión molécula elemento compuesto enlace iónico enlace
Sección 1: Los átomos, los iones y las moléculas CONCEPTO CLAVE Todos los seres vivos tienen como base los átomos y sus interacciones. VOCABULARIO átomo ión molécula elemento compuesto enlace iónico enlace
MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES PREGUNTAS
 MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES a. El examen de química consistirá en 30 preguntas de tipo test b. La duración del examen será de 1,5 horas. c. Sólo hay que elegir una respuesta por
MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES a. El examen de química consistirá en 30 preguntas de tipo test b. La duración del examen será de 1,5 horas. c. Sólo hay que elegir una respuesta por
EXTRACCIÓN DE ADN. BIOLOGÍA GENERAL (Evolución y Genética)
 EXTRACCIÓN DE ADN BIOLOGÍA GENERAL (Evolución y Genética) Curso Académico 2015-2016 Abril 2016 INTRODUCCIÓN Y CONCEPTOS Extracción de ADN La extracción de ADN requiere una serie de etapas básicas. En primer
EXTRACCIÓN DE ADN BIOLOGÍA GENERAL (Evolución y Genética) Curso Académico 2015-2016 Abril 2016 INTRODUCCIÓN Y CONCEPTOS Extracción de ADN La extracción de ADN requiere una serie de etapas básicas. En primer
Transferencia de material genético II. 1) Aislamiento de plásmidos Lisis alcalina
 Transferencia de material genético II 1) Aislamiento de plásmidos Lisis alcalina ESQUEMA GENERAL SESIÓN I: TRANSFORMAR cepas de E. coli con un plásmido. Verificar que hay células transformantes de acuerdo
Transferencia de material genético II 1) Aislamiento de plásmidos Lisis alcalina ESQUEMA GENERAL SESIÓN I: TRANSFORMAR cepas de E. coli con un plásmido. Verificar que hay células transformantes de acuerdo
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN
 CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL
 CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD A. CROMATOGRAFÍA DE INTERCAMBIO IÓNICO. Usos 1.- Purificar Proteínas 2.- Concentrar Proteínas Ventajas
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD A. CROMATOGRAFÍA DE INTERCAMBIO IÓNICO. Usos 1.- Purificar Proteínas 2.- Concentrar Proteínas Ventajas
SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS Elaborado por Lic. Fernando Andrade
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO PRACTICA DE LABORATORIO 2014 SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO PRACTICA DE LABORATORIO 2014 SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS
EL ENLACE QUÍMICO (FisQuiWeb)
 EL ENLACE QUÍMICO (FisQuiWeb) Los átomos tienden a unirse unos a otros para formar entidades más complejas. De esta manera se construyen todas las sustancias. Por qué los átomos tienden a unirse y no permanecen
EL ENLACE QUÍMICO (FisQuiWeb) Los átomos tienden a unirse unos a otros para formar entidades más complejas. De esta manera se construyen todas las sustancias. Por qué los átomos tienden a unirse y no permanecen
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 1) CURSO 2011/12 Nombre y apellidos: LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES 1. A qué es igual 1 kg? a) 10 t b) 1000 t c) 1000 g d) 0,001
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 1) CURSO 2011/12 Nombre y apellidos: LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES 1. A qué es igual 1 kg? a) 10 t b) 1000 t c) 1000 g d) 0,001
Diagnóstico Avanzado en Enfermedades Tropicales
 Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL
 CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD B. CROMATOGRAFÍA DE FILTRACIÓN EN GEL. 1. Principios. No requiere la unión de la proteína, lo cual
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD B. CROMATOGRAFÍA DE FILTRACIÓN EN GEL. 1. Principios. No requiere la unión de la proteína, lo cual
ELECTROFORESIS AVANZADA
 Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Disoluciones Químicas
 Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
ANEXOS A: Procedimientos experimentales
 ANEXOS 1 ANEXOS A: Procedimientos experimentales SDS-TRIS-GLICINA-PAGE Procedimiento A.1. Descripción del método de preparación de geles de poliacrilamida. Se trata de un sistema vertical de electroforesis,
ANEXOS 1 ANEXOS A: Procedimientos experimentales SDS-TRIS-GLICINA-PAGE Procedimiento A.1. Descripción del método de preparación de geles de poliacrilamida. Se trata de un sistema vertical de electroforesis,
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN. Ingeniería Ambiental
 TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
SEPARACIONES ANALITICAS POR MÉTODOS DE EXTRACIÓN
 SEPARACIONES ANALITICAS POR MÉTODOS DE EXTRACIÓN Las separaciones por método de extracción, son procesos en las cuales un soluto se distribuye entre dos líquidos inmiscibles entre sí puestos en contacto.
SEPARACIONES ANALITICAS POR MÉTODOS DE EXTRACIÓN Las separaciones por método de extracción, son procesos en las cuales un soluto se distribuye entre dos líquidos inmiscibles entre sí puestos en contacto.
15.1 Laboratorio de Fermentaciones y Biocatálisis
 15.1 Laboratorio de Fermentaciones y Biocatálisis El Laboratorio de Fermentaciones y Biocatálisis es un laboratorio en el que estudiantes del Doctorado en Ciencias Químicas interesados en la Línea de Generación
15.1 Laboratorio de Fermentaciones y Biocatálisis El Laboratorio de Fermentaciones y Biocatálisis es un laboratorio en el que estudiantes del Doctorado en Ciencias Químicas interesados en la Línea de Generación
PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG. 1 de 20 2 de 10 1 moneda de 1 10 monedas monedas monedas de 0.
 PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG Para saber lo que tengo debo separar las partes y cuantificar 1 de 20 2 de 10 1 moneda de 1 10 monedas 0.20 4 monedas 0.10 3 monedas
PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG Para saber lo que tengo debo separar las partes y cuantificar 1 de 20 2 de 10 1 moneda de 1 10 monedas 0.20 4 monedas 0.10 3 monedas
Purificación de proteínas Métodos cromatográficos. M. en C. Esdras Israel Carrizosa Carbajal
 Purificación de proteínas Métodos cromatográficos M. en C. Esdras Israel Carrizosa Carbajal Secuencia experimental típica para purificar una proteína: Obtención de extractos libres de células Seleccionar
Purificación de proteínas Métodos cromatográficos M. en C. Esdras Israel Carrizosa Carbajal Secuencia experimental típica para purificar una proteína: Obtención de extractos libres de células Seleccionar
DISOLUCIONES Y CÀLCULO DE CONCENTRACIONES. MSc. Marilú Cerda Lira
 DISOLUCIONES Y CÀLCULO DE CONCENTRACIONES MSc. Marilú Cerda Lira DISOLUCIONES Y CÀLCULO DE CONCENTRACIONES Introducción Definición Métodos de separación de las soluciones Principales clases de soluciones
DISOLUCIONES Y CÀLCULO DE CONCENTRACIONES MSc. Marilú Cerda Lira DISOLUCIONES Y CÀLCULO DE CONCENTRACIONES Introducción Definición Métodos de separación de las soluciones Principales clases de soluciones
PRACTICA LABORATORIO Nº 1 PROPIEDADES DE LAS PROTEINAS.
 UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE AGRONOMIA DEPARTAMENTO DE QUIMICA Y TECNOLOGIA CATEDRA DE BIOQUÍMICA PRACTICA LABORATORIO Nº 1 PROPIEDADES DE LAS PROTEINAS. INTRODUCCIÓN Las proteínas son
UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE AGRONOMIA DEPARTAMENTO DE QUIMICA Y TECNOLOGIA CATEDRA DE BIOQUÍMICA PRACTICA LABORATORIO Nº 1 PROPIEDADES DE LAS PROTEINAS. INTRODUCCIÓN Las proteínas son
CROMATOGRAFIA. Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA
 CROMATOGRAFIA Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA 1 CROMATOGRAFIA Se basa en el principio general de distribución de un compuesto entre dos fases, una fija o estacionaria (FE) y
CROMATOGRAFIA Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA 1 CROMATOGRAFIA Se basa en el principio general de distribución de un compuesto entre dos fases, una fija o estacionaria (FE) y
Química Básica del Agua
 Química Básica del Agua Índice de este módulo Soluciones iónicas Estructuras iónicas Terminología Índices de saturación S.D.I. TERMINOLOGÍA Ion Partícula cargada eléctricamente, positiva (catión) o negativa
Química Básica del Agua Índice de este módulo Soluciones iónicas Estructuras iónicas Terminología Índices de saturación S.D.I. TERMINOLOGÍA Ion Partícula cargada eléctricamente, positiva (catión) o negativa
OPCIÓN A. = 0,789 g ml 1 30,4 ml = 23,98 g.
 OPCIÓN A PROBLEMA 2.- En el proceso de elaboración del vino, la glucosa fermenta para producir etanol según la siguiente reacción (no ajustada): C 6 H 12 O 6 (aq) C 2 H 5 OH (aq) + CO 2 (g). a) Si, en
OPCIÓN A PROBLEMA 2.- En el proceso de elaboración del vino, la glucosa fermenta para producir etanol según la siguiente reacción (no ajustada): C 6 H 12 O 6 (aq) C 2 H 5 OH (aq) + CO 2 (g). a) Si, en
CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR
 CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR 1.-FUNDAMENTOS DE LA CROMATOGRAFIA DE TAMIZADO MOLECULAR. Las biomoléculas presentan una serie de propiedades físicas (tamaño,
CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR 1.-FUNDAMENTOS DE LA CROMATOGRAFIA DE TAMIZADO MOLECULAR. Las biomoléculas presentan una serie de propiedades físicas (tamaño,
Nombre y apellidos:...
 1 Señala las opciones correctas: a) El conocimiento científico surge de la necesidad de dar respuesta a un problema basado en hechos a los que se quiere dar explicación. b) El conocimiento científico es
1 Señala las opciones correctas: a) El conocimiento científico surge de la necesidad de dar respuesta a un problema basado en hechos a los que se quiere dar explicación. b) El conocimiento científico es
PH y SISTEMAS TAMPÓN
 PH y SISTEMAS TAMPÓN DISOCIACIÓN DEL AGUA.- El agua se disocia de la manera siguiente: HOH H+ OH- El valor de Kéq. a 25ºC es muy pequeña, siendo del orden de 1 8 x 10(-16). Esto significa
PH y SISTEMAS TAMPÓN DISOCIACIÓN DEL AGUA.- El agua se disocia de la manera siguiente: HOH H+ OH- El valor de Kéq. a 25ºC es muy pequeña, siendo del orden de 1 8 x 10(-16). Esto significa
Parámetros cromatográficos
 Parámetros cromatográficos El detector registra cambios en alguna propiedad de eluyente. Los cambios son registrados en función del tiempo. El diagrama de la respuesta del detector en función del tiempo
Parámetros cromatográficos El detector registra cambios en alguna propiedad de eluyente. Los cambios son registrados en función del tiempo. El diagrama de la respuesta del detector en función del tiempo
4º E.S.O. FÍSICA Y QUÍMICA 5. REACCIONES QUÍMICAS. Dpto. de Física y Química. R. Artacho
 4º E.S.O. FÍSICA Y QUÍMICA 5. REACCIONES QUÍMICAS R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. La reacción química: cómo se produce 2. La energía en las reacciones químicas 3. La velocidad
4º E.S.O. FÍSICA Y QUÍMICA 5. REACCIONES QUÍMICAS R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. La reacción química: cómo se produce 2. La energía en las reacciones químicas 3. La velocidad
Disoluciones. Qué es una mezcla? Concepto de Mezcla 12/05/2014
 Disoluciones Profesora: Karina Oñate Fuentes Asignatura: Química- Plan común Nivel: 2º año medio Qué es una mezcla? Los compuestos químicos pueden unirse para reaccionar o mezclarse. En el primer caso
Disoluciones Profesora: Karina Oñate Fuentes Asignatura: Química- Plan común Nivel: 2º año medio Qué es una mezcla? Los compuestos químicos pueden unirse para reaccionar o mezclarse. En el primer caso
Ensayos de restricción
 Ensayos de restricción Vector con inserto= Vector recombinante 6500pb Objetivos de ensayos de restricción de plásmidos Conocer el principio de separación y detección de ácidos nucleicos en geles de agarosa.
Ensayos de restricción Vector con inserto= Vector recombinante 6500pb Objetivos de ensayos de restricción de plásmidos Conocer el principio de separación y detección de ácidos nucleicos en geles de agarosa.
SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS Elaborado por Lic. Fernando Andrade
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO PRACTICA DE LABORATORIO 2016 SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO PRACTICA DE LABORATORIO 2016 SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS
UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE
 Química Analítica UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE 2015 Una solución es una mezcla homogénea de dos o
Química Analítica UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE 2015 Una solución es una mezcla homogénea de dos o
