FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO. Finasterida KERN PHARMA 5 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
|
|
|
- María Pilar Martín Lozano
- hace 6 años
- Vistas:
Transcripción
1 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO Finasterida KERN PHARMA 5 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Para excipientes, ver sección FORMA FARMACÉUTICA Comprimidos recubiertos con película. Los comprimidos son blancos, redondos y marcados con F5 en una de las caras. 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Finasterida KERN PHARMA 5 mg comprimidos está indicada en el tratamiento de la hiperplasia prostática benigna (HPB) sintomática en varones con aumento de tamaño de la próstata con objeto de: Mejorar los síntomas. Reducir el riesgo de retención urinaria aguda. Reducir la necesidad de cirugía, incluidas la resección transuretral de la próstata (RTUP) y la prostatectomía. Finasterida KERN PHARMA 5 mg comprimidos produce regresión del crecimiento prostático, mejora el flujo urinario y mejora los síntomas relacionados con la HPB. 4.2 Posología y forma de administración La posología recomendada es un comprimido diario de 5 mg, con o sin alimentos. Finasterida KERN PHARMA 5 mg comprimidos puede administrarse solo o en combinación con el alfabloqueante doxazosina (ver sección 5.1 Propiedades farmacodinámicas). POSOLOGÍA EN LA INSUFICIENCIA RENAL No es necesario ajustar la dosis de los pacientes con grados variables de insuficiencia renal (aclaramientos de creatinina de hasta sólo 9 ml/min), dado que los estudios farmacocinéticos no indicaron ningún cambio de la eliminación de finasterida. POSOLOGÍA EN LOS PACIENTES DE EDAD AVANZADA No es necesario ajustar la dosis, aunque los estudios farmacocinéticos indicaron que la eliminación de finasterida desciende algo en los pacientes mayores de 70 años.
2 4.3 Contraindicaciones El uso de Finasterida KERN PHARMA 5 mg comprimidos no está indicado en las mujeres ni en los niños. Finasterida KERN PHARMA 5 mg comprimidos está contraindicado en las siguientes situaciones: Hipersensibilidad a finasterida o a cualquiera de los excipientes del medicamento. Embarazo - Utilización en las mujeres que están o pueden estar embarazadas (ver sección 4.6 Embarazo y Exposición a finasterida - Riesgo para el feto varón). 4.4 Advertencias y precauciones especiales de empleo GENERALES Antes de comenzar el tratamiento con Finasterida KERN PHARMA 5 mg comprimidos se debe realizar una evaluación cuidadosa para descartar otras patologías: infección, cáncer de próstata, estenosis, vejiga hipotónica u otros trastornos neurógenos que podrían semejarse a una hiperplasia prostática benigna. Los pacientes con un gran volumen de residuo urinario y/o una disminución intensa del flujo urinario deben ser vigilados cuidadosamente ante la posibilidad de una uropatía obstructiva. Estos pacientes no son candidatos para tratamiento con finasterida. Este medicamento contiene lactosa. Los pacientes con intolerancia hereditaria a galactosa, de insuficiencia de lactasa de Lapp (insuficiencia observada en ciertas poblaciones de Laponia) o problemas de absorción de glucosa o galactosa no deben tomar este medicamento. EFECTOS SOBRE EL APE Y LA DETECCIÓN DEL CÁNCER DE PRÓSTATA No se ha demostrado un efecto clínico beneficioso en los pacientes con cáncer de próstata tratados con 5 mg de finasterida. Se vigiló a pacientes con HPB y niveles de antígeno prostático específico (APE) elevados en estudios clínicos controlados con determinación seriada de APE y biopsias prostáticas repetidas. En estos estudios de HPB, no parecía que 5 mg de finasterida alterasen la tasa de detección del cáncer de próstata, y la incidencia global de cáncer de próstata no varió significativamente en los pacientes tratados con 5 mg de finasterida y con un placebo. Antes de comenzar el tratamiento con Finasterida KERN PHARMA 5 mg comprimidos, y periódicamente durante su administración, se recomienda realizar un tacto rectal y otras evaluaciones dirigidas al diagnóstico del cáncer de próstata. También se utilizan los niveles séricos APE para detectar el cáncer de próstata. Generalmente, un nivel basal de APE > 10 ng/ml (Hybritech) exige realizar una nueva evaluación y considerar la biopsia; si existen niveles de APE comprendidos entre 4 y 10 ng/ml, se recomienda efectuar una nueva evaluación. Existe un solapamiento notable en los niveles de APE entre los varones con y sin cáncer de próstata. Por consiguiente, los valores de APE dentro de los límites de referencia normales en varones con HPB no descartan el cáncer de próstata, independientemente del tratamiento con Finasterida KERN PHARMA 5 mg comprimidos. Un valor basal de APE < 4 ng/ml no excluye la existencia de cáncer de próstata. Finasterida KERN PHARMA 5 mg comprimidos produce un descenso aproximado del 50% de las concentraciones séricas de APE en los pacientes con HPB, incluso con cáncer de próstata. Al evaluar los datos de los niveles séricos de APE en los pacientes con HPB tratados con Finasterida KERN PHARMA 5 mg comprimidos es preciso tener en cuenta este descenso, que no descarta la presencia concomitante de un cáncer de próstata. Dicho descenso es previsible independientemente de los valores de APE, aunque puede variar en cada paciente. En el análisis de los datos del APE de más de pacientes incluidos en el Estudio sobre la eficacia y la seguridad a largo plazo de 5 mg de finasterida (PLESS), realizado durante 4 años según un diseño doble ciego y controlado con placebo, se confirmó que, en los pacientes típicos tratados con 5 mg de finasterida durante al menos seis meses, los valores de APE deben multiplicarse por dos para su comparación con los límites normales
3 de los varones no tratados. Este ajuste permite mantener la sensibilidad y especificidad de la determinación del APE y su capacidad para detectar el cáncer de próstata. Es preciso evaluar cuidadosamente todo aumento sostenido de los niveles del APE en los pacientes tratados con finasterida, sin olvidar el posible incumplimiento del tratamiento con Finasterida KERN PHARMA 5 mg comprimidos. El porcentaje de APE libre no desciende significativamente con Finasterida KERN PHARMA 5 mg comprimidos. La relación de APE libre y total permanece constante incluso bajo la influencia de Finasterida KERN PHARMA 5 mg comprimidos. Cuando el porcentaje de APE libre se utiliza como ayuda en la detección del cáncer de próstata, no es necesario ajustar su valor. INTERACCIONES ENTRE EL FÁRMACO Y LAS PRUEBAS ANALÍTICAS EFECTO SOBRE LOS NIVELES DEL APE La concentración sérica de APE guarda relación con la edad y el volumen de la próstata del paciente, y el volumen prostático guarda relación con la edad del paciente. Al evaluar las determinaciones analíticas del APE es preciso considerar que los niveles del APE descienden en los pacientes tratados con Finasterida KERN PHARMA 5 mg comprimidos. En la mayoría de los pacientes se observa un descenso rápido del APE en los primeros meses de tratamiento, y a partir de este momento los niveles de APE se estabilizan en un nuevo nivel basal. Este nivel basal postratamiento es aproximadamente la mitad del valor previo al tratamiento. Por consiguiente, como norma general, en los pacientes tratados con Finasterida KERN PHARMA 5 mg comprimidos durante al menos seis meses los valores de APE deben multiplicarse por dos a efectos de comparación con los límites normales en varones no tratados. Para una interpretación clínica, ver sección 4.4 Advertencias y precauciones especiales de empleo, Efectos sobre el APE y la detección del cáncer de próstata. 4.5 Interacciones con otros medicamentos y otras formas de interacción No se han identificado interacciones farmacológicas de importancia clínica. Finasterida KERN PHARMA 5 mg comprimidos no parece afectar de forma importante al sistema enzimático de metabolización de fármacos relacionado con el citocromo P450. Se han realizado pruebas en seres humanos con propranolol, digoxina, gliburida, warfarina, teofilina y antipirina sin encontrar interacciones de importancia clínica. OTROS TRATAMIENTOS CONCOMITANTES Aunque no se han realizado estudios específicos sobre interacciones, en los estudios clínicos con 5 mg de finasterida se han utilizado junto con inhibidores de la ECA, paracetamol, ácido acetilsalicílico, alfabloqueantes, betabloqueantes, antagonistas del calcio, nitratos cardíacos, diuréticos, antagonistas H 2, inhibidores de la HMG- CoA reductasa, antiinflamatorios no esteroideos (AINEs), quinolonas y benzodiazepinas sin encontrar indicios de interacciones de importancia clínica. 4.6 Embarazo y lactancia EMBARAZO Finasterida KERN PHARMA 5 mg comprimidos está contraindicada en las mujeres que estén o puedan estar embarazadas (ver sección 4.3 Contraindicaciones).
4 Dada la capacidad que poseen los inhibidores de la 5 -reductasa de tipo II para inhibir la conversión de la testosterona en dihidrotestosterona, estos fármacos, incluida finasterida, pueden producir malformaciones de los genitales externos en los fetos varones cuando se administran a la mujer embarazada. EXPOSICIÓN A FINASTERIDA - RIESGO PARA EL FETO VARÓN Las mujeres que estén o puedan estar embarazadas no deben manipular comprimidos machacados o partidos de Finasterida KERN PHARMA 5 mg comprimidos, dada la posible absorción de finasterida y el consiguiente riesgo potencial para el feto varón. Los comprimidos de Finasterida KERN PHARMA 5 mg comprimidos tienen un recubrimiento que evita el contacto con el producto activo cuando se manipula normalmente, siempre que los comprimidos no se partan ni se machaquen. MADRES LACTANTES No está indicada la utilización de Finasterida KERN PHARMA 5 mg comprimidos en las mujeres. Se desconoce si finasterida se excreta en la leche humana. USO EN NIÑOS No está indicada la utilización de Finasterida KERN PHARMA 5 mg comprimidos en los niños. No se han establecido la seguridad y la eficacia en los niños. 4.7 Efectos sobre la capacidad para conducir y utilizar máquinas No hay datos conocidos que sugieran que Finasterida KERN PHARMA 5 mg comprimidos pueda afectar la capacidad de conducir o manejar maquinaria. 4.8 Reacciones adversas Se han comunicado las siguientes reacciones adversas durante el primer año de ensayos clínicos y/o en el uso después de la comercialización: Aparato reproductor y trastornos mamarios: Frecuentes (>1/100, <1/10): disminución del volumen de eyaculación, impotencia Poco frecuentes (>1/1,000, <1/100): trastornos de la eyaculación, crecimiento mamario, hipersensibilidad mamaria Raras (>1/10,000, <1/1,000): dolor testicular. Trastornos psiquiátricos: Frecuentes (>1/100, <1/10): disminución de la libido. Trastornos de la piel y tejido subcutáneo: Poco frecuentes (>1/1,000, <1/100): erupción cutánea. Trastornos del sistema inmune: Raras (>1/10,000, <1/1,000): reacciones de hipersensibilidad, incluido prurito, urticaria e hinchazón de los labios y la cara.
5 En los años 2 a 4 de un estudio clínico de 4 años de duración, controlado con placebo, en hombres y en estudios de extensión de 5 años de duración (incluyendo 853 pacientes tratados durante 5-6 años), no hubo diferencias significativas entre los grupos de tratamiento en las incidencias de impotencia, disminución de la libido y trastornos de la eyaculación; y la incidencia de nuevas reacciones adversas sexuales relacionadas con el fármaco disminuyó durante el tratamiento. El crecimiento mamario y la hipersensibilidad mamaria aumentaron ligeramente en los años 2 a 4 del estudio PLESS, pero las incidencias de ambos permanecieron por debajo del 2%. La incidencia de erupción cutánea permaneció sin cambios. TRATAMIENTO MÉDICO DE LOS SÍNTOMAS PROSTÁTICOS (MTOPS) El estudio MTOPS comparó finasterida 5 mg/día (n=768), doxazosina 4 u 8 mg/día (n=756), el tratamiento combinado de finasterida 5 mg/día y doxazosina 4 u 8 mg/día (n=786) y placebo (n=737). En este estudio, el perfil de seguridad y tolerabilidad del tratamiento combinado fue normalmente consecuente con los perfiles de los componentes individuales. La incidencia del trastorno de eyaculación en pacientes recibiendo tratamiento combinado fue comparable a la suma de las incidencias de esta reacción adversa para las dos monoterapias. 4.9 Sobredosis Los pacientes han recibido dosis únicas de hasta 400 mg de finasterida y dosis múltiples de hasta 80 mg/día durante tres meses sin que se observaran reacciones adversas. No se recomienda ningún tratamiento específico de la sobredosis de Finasterida KERN PHARMA 5 mg comprimidos. 5. PROPIEDADES FARMACOLÓGICAS 5.1 Propiedades farmacodinámicas Grupo farmacoterapéutico: G04CB Inhibidores de la testosterona-5-alfa reductasa, código ATC: G04CB01. Finasterida un compuesto 4-azasteroideo sintético, es un inhibidor específico de la 5 -reductasa de tipo II, una enzima intracelular que metaboliza la testosterona para convertirla en un andrógeno más potente, la dihidrotestosterona (DHT). En la hiperplasia prostática benigna (HPB), el aumento de tamaño de la próstata depende de la conversión de la testosterona en DHT dentro de la próstata. Finasterida es muy eficaz para reducir la DHT circulante e intraprostática. Finasterida no posee afinidad por los receptores androgénicos. En el Estudio sobre la eficacia y la seguridad a largo plazo de finasterida (PLESS) se valoró el efecto del tratamiento con 5 mg de finasterida sobre los episodios urológicos relacionados con la HPB (intervención quirúrgica [p. ej., resección transuretral de la próstata y prostatectomía] o retención urinaria aguda que exigiera sondaje) durante un período de 4 años en pacientes con síntomas moderados o graves de HPB. En este estudio multicéntrico aleatorizado, doble ciego y controlado con placebo, el tratamiento con 5 mg de finasterida redujo el riesgo de todos los episodios urológicos en un 51% y también se acompañó de una regresión importante y sostenida del volumen de la próstata, y de un aumento sostenido del flujo urinario máximo y de mejoría de los síntomas.
6 La hiperplasia prostática benigna (HPB) se produce en la mayoría de los varones a partir de los 50 años de edad, y su prevalencia aumenta con la edad. Los estudios epidemiológicos indican que el aumento de tamaño de la próstata triplica el riesgo de padecer retención urinaria aguda o tener que someterse a cirugía prostática. Asimismo, la probabilidad de que aparezcan síntomas urinarios moderados o graves o una disminución del flujo urinario es 3 veces mayor en los varones con próstata agrandada que en los que tienen próstatas más pequeñas. El desarrollo y crecimiento de la próstata y el desarrollo posterior de HPB dependen de un andrógeno potente, la dihidrotestosterona (DHT). La testosterona, secretada por los testículos y las glándulas suprarrenales, es convertida rápidamente en DHT por la 5 -reductasa de tipo II, sobre todo en la próstata, el hígado y la piel, en donde más tarde se une de forma preferente a los núcleos celulares de esos tejidos. Finasterida es un inhibidor competitivo de la 5 -reductasa de tipo II humana, con la que forma lentamente un complejo enzimático estable. El recambio de este complejo es sumamente lento (t 1/2 ~ 30 días). Se ha demostrado in vitro e in vivo que finasterida es un inhibidor específico de la 5 -reductasa de tipo II, y que no posee afinidad por los receptores de los andrógenos. Con una dosis única de 5 mg de finasterida se obtenía una reducción rápida de la concentración sérica de DHT, observándose un efecto máximo después de 8 horas. Aunque los niveles plasmáticos de finasterida variaron a lo largo de 24 horas, los niveles séricos de DHT permanecieron constantes durante este período, lo que indica que las concentraciones plasmáticas del fármaco no se relacionan directamente con las concentraciones plasmáticas de DHT. Los datos obtenidos en los estudios descritos a continuación, que demuestran una reducción del riesgo de retención urinaria aguda y de cirugía, mejoría de los síntomas relacionados con la HPB, aumento del flujo urinario máximo y disminución del volumen de la próstata, indican que la finasterida invierte la progresión de la HPB en los varones con aumento del tamaño de la próstata. En un principio se evaluó la administración de 5 mg/día de finasterida en pacientes con síntomas de HPB y aumento de tamaño prostático demostrado por tacto rectal en dos estudios de fase III aleatorizados, doble ciego y controlados con placebo de un año de duración, y en sus extensiones en régimen abierto durante 5 años. De los 536 pacientes aleatorizados inicialmente para recibir 5 mg/día de finasterida, 234 completaron los 5 años adicionales de tratamiento y estaban disponibles para el análisis. Los parámetros de eficacia fueron la puntuación de síntomas, el flujo urinario máximo y el volumen de la próstata. Asimismo, se evaluó finasterida en el PLESS, un estudio multicéntrico aleatorizado, doble ciego y controlado con placebo, de 4 años de duración. En este estudio se valoró el efecto del tratamiento con 5 mg/día de finasterida sobre los síntomas de HPB y los episodios urológicos relacionados con la HPB (intervención quirúrgica [p. ej., resección transuretral de próstata y prostatectomía] o retención urinaria aguda que exigiera sondaje). Se distribuyó aleatoriamente en el estudio a pacientes (1.524 a finasterida, al placebo) de edades comprendidas entre 45 y 78 años con síntomas moderados o graves de HPB y con un crecimiento de la próstata demostrado mediante tacto rectal, de los que pacientes fueron evaluables con respecto a la eficacia. Completaron los 4 años del estudio sujetos (1.000 en el grupo de finasterida y 883 en el de placebo). También se evaluaron el flujo urinario máximo y el volumen de la próstata. EFECTO SOBRE LA RETENCIÓN URINARIA AGUDA Y LA NECESIDAD DE CIRUGÍA En el estudio PLESS de 4 años se requirió cirugía o se produjo retención urinaria aguda que precisó sondaje en el 13,2% de los pacientes que tomaron placebo, en comparación con el 6,6% de los que recibieron 5 mg de finasterida, lo que representa una reducción del 51% del riesgo de cirugía o retención urinaria aguda a lo largo de 4 años. Con 5 mg de finasterida se redujo el riesgo de cirugía en un 55% (10,1% con placebo frente al 4,6% con finasterida), y el de retención urinaria aguda en un 57% (6,6% con placebo frente al 2,8% con finasterida). La reducción del riesgo era evidente entre los grupos de tratamiento en la primera evaluación (4 meses), y se mantuvo
7 a lo largo de los 4 años del estudio. En la tabla 1 siguiente se muestran la frecuencia de aparición y la reducción del riesgo de los episodios urológicos durante el estudio. Tabla 1 TASAS DE EPISODIOS URÓLOGICOS Y REDUCCIÓN DEL RIESGO CON FINASTERIDA A LO LARGO DE 4 AÑOS Porcentaje de Pacientes Episodios urológicos Placebo (n = 1503) Finasterida 5 mg (n = 1513) Reducción del riesgo Cirugía o retención urinaria aguda 13,2% 6,6% 51%* Cirugía TURP 10,1% 8,3% 4,6% 4,2% 55%* 49%* Retención urinaria aguda 6,6% 2,8% 57%* Cirugía relacionada con la HPB * p<0,001 EFECTO SOBRE LA PUNTUACIÓN DE SÍNTOMAS En los dos estudios de fase III de un año de duración, las puntuaciones medias totales de síntomas descendieron ya en la segunda semana en relación con la situación basal. En estos estudios se observó una mejoría importante de los síntomas a los 7 y a los 10 meses en comparación con placebo. Aunque en algunos pacientes se observó una mejoría precoz de los síntomas urinarios, generalmente era necesario un ensayo terapéutico de al menos 6 meses para valorar si se había logrado una respuesta beneficiosa en el alivio de los síntomas. La mejoría de los síntomas de HPB se mantuvo durante el primer año y a lo largo de los 5 años adicionales de los estudios de extensión. En el estudio PLESS de 4 años de duración los pacientes tenían síntomas moderados o graves en la situación basal (media aproximada de 15 puntos en una escala de 0 a 34 puntos). En los pacientes que siguieron en tratamiento durante los 4 años del estudio 5 mg de finasterida mejoraron la puntuación de los síntomas en 3,3 puntos, frente a 1,3 puntos en el grupo de placebo (p <0,001). En los pacientes tratados con 5 mg de finasterida se demostró una mejoría de la puntuación de los síntomas al año, que se mantenía a los 4 años. Las puntuaciones de los síntomas mejoraron en los pacientes tratados con placebo en el primer año, pero empeoraron posteriormente. Los pacientes con síntomas moderados o graves en la situación basal solían experimentar la mayor mejoría de la puntuación de los síntomas. EFECTO SOBRE EL FLUJO URINARIO MÁXIMO En los dos estudios de fase III de un año de duración, el flujo urinario máximo aumentó notablemente a las 2 semanas en comparación con el basal. En estos estudios se observó un aumento importante del flujo urinario máximo a los 4 y a los 7 meses en comparación con placebo. Este efecto se mantuvo durante el primer año y a lo largo de los 5 años adicionales de los estudios de extensión.
8 En el estudio PLESS de 4 años de duración se produjo una clara separación entre los grupos de tratamiento con respecto al flujo urinario máximo en favor de 5 mg de finasterida a los 4 meses, y se mantuvo durante la totalidad del estudio. El flujo urinario máximo medio en la situación basal fue de 11 ml/seg., aproximadamente, en los dos grupos de tratamiento. En los pacientes que permanecieron en tratamiento durante todo el estudio y que tenían datos del flujo urinario evaluables, 5 mg de finasterida aumentaron el flujo urinario máximo en 1,9 ml/seg., frente a 0,2 ml/seg. en el grupo de placebo. EFECTO SOBRE EL VOLUMEN DE LA PRÓSTATA En los dos estudios de fase III de un año de duración, el volumen medio de la próstata en la situación basal osciló entre 40 y 50 cc. En ambos estudios se produjo una reducción importante del volumen prostático en comparación con la situación basal y con placebo en la primera evaluación (3 meses). Este efecto se mantuvo durante el primer año y a lo largo de los 5 años adicionales de los estudios de extensión. En el estudio PLESS de 4 años de duración se valoró anualmente el volumen de la próstata en un subgrupo de pacientes (n = 284) mediante resonancia magnética (RM). En los pacientes tratados con 5 mg de finasterida se redujo el volumen de la próstata en comparación con el basal y con placebo a lo largo de los 4 años del estudio. Dentro del subgrupo de pacientes sometidos a RM que permanecieron en tratamiento durante la totalidad del estudio, 5 mg de finasterida disminuyeron en un 17,9% el volumen de la próstata (desde 55,9 cc en la situación basal a 45,8 cc a los 4 años), en comparación con el aumento del 14,1% (desde 51,3 a 58,5 cc) observado en el grupo de placebo (p <0,001). EL VOLUMEN DE LA PRÓSTATA COMO FACTOR PREDICTIVO DE LA RESPUESTA TERAPÉUTICA En un metaanálisis en el que se combinaron datos de 1 año procedentes de siete estudios doble ciego controlados con placebo de diseño similar, en los que se incluyeron pacientes con HPB sintomática, se demostró que en los pacientes tratados con 5 mg de finasterida la magnitud de la respuesta de los síntomas y el grado de mejoría del flujo urinario máximo fueron mayores en los pacientes con aumento del tamaño prostático (alrededor de 40 cc o mayor) en la situación basal. TRATAMIENTO MÉDICO DE LOS SÍNTOMAS PROSTÁTICOS (MTOPS) El estudio MTOPS (Medical Therapy Of Prostatic Symptoms) fue un estudio de 4 a 6 años de duración, en hombres con HPB sintomática que fueron aleatorizados para recibir finasterida 5 mg/día, doxazosina 4 u 8 mg/día ***, la combinación de finasterida 5 mg/día y doxazosina 4 u 8 mg/día 1** o placebo. El criterio de valoración principal fue el tiempo hasta la evolución clínica de la HPB, definida como un aumento confirmado de > 4 puntos desde el valor inicial en la puntuación de síntomas, retención urinaria aguda, insuficiencia renal relacionada con la HPB, infecciones urinarias recurrentes o urosepsis o incontinencia. En comparación con placebo, el tratamiento con finasterida, doxazosina o el tratamiento combinado produjeron una reducción significativa en el riesgo de la evolución clínica de la HPB del 34, 39 y 66% respectivamente. La mayoría de los acontecimientos (274 de 351) que constituyeron la evolución de la HPB fueron aumentos confirmados de > 4 puntos en la puntuación de síntomas; se redujo el riesgo de la evolución de la puntuación de los síntomas en un 30, 45 y 64% en los grupos de finasterida, doxazosina y la combinación, respectivamente, en comparación con placebo. La retención urinaria aguda puede explicar 41 de los 351 acontecimientos de la evolución de HPB; el riesgo de desarrollar retención urinaria aguda se redujo en un 68, 35 y 81% en los grupos de finasterida, doxazosina y la combinación, respectivamente, en comparación con placebo. Solo los grupos de finasterida y el de tratamiento combinado fueron significativamente diferentes del placebo. *** Dosis ajustada de 1 mg a 4 u 8 mg en un periodo de 3 semanas. 1
9 OTROS ESTUDIOS CLÍNICOS Se realizó un estudio doble ciego y controlado con placebo de 24 semanas de duración en el que se incluyeron 36 pacientes con síntomas moderados o graves de obstrucción urinaria y un flujo máximo inferior a 15 ml/seg. en el que se valoraron los efectos urodinámicos de finasterida en el tratamiento de la obstrucción vesical por HPB mediante técnicas invasivas. En los pacientes tratados con 5 mg de finasterida se demostró un alivio de la obstrucción en comparación con placebo, puesto de manifiesto por una mejoría importante de la presión del detrusor y un aumento del flujo medio. Se evaluó mediante RM el efecto de finasterida sobre el volumen de las zonas periféricas y periuretral de la próstata en un estudio doble ciego y controlado con placebo de un año de duración en el que se incluyeron 20 varones con HPB. Los pacientes tratados con 5 mg de finasterida, pero no los tratados con placebo, experimentaron una disminución importante del tamaño total de la glándula prostática [11,5 ± 3,2 cc (EE)], que se debió fundamentalmente a una reducción [6,2 ± 3 cc] del tamaño de la zona periuretral. Dado que ésta es responsable de la obstrucción del flujo, su reducción puede explicar la respuesta clínica beneficiosa observada en estos pacientes. OTROS DATOS A LARGO PLAZO En el estudio controlado con placebo de 7 años de duración en el que se incluyeron varones sanos, de los cuales tenían datos disponibles para análisis de biopsia prostática por punción, se detectó cáncer de próstata en 803 (18,4%) varones que recibían 5 mg de finasterida y (24,4%) varones que recibían placebo. En el grupo de finasterida, 280 (6,4%) varones tenían cáncer de próstata con puntuaciones de Gleason de 7-10 detectados en la biopsia por punción frente a 237 (5,1%) varones en el grupo placebo. Del total de los casos de cáncer de próstata diagnosticados en este estudio, aproximadamente el 98% fueron clasificados como intracapsulares (fase T1 o T2). Se desconoce la relación entre el uso a largo plazo de 5 mg de finasterida y los tumores con puntuación de Gleason de Propiedades farmacocinéticas En el hombre, después de una dosis oral de 14 C-finasterida, el 39% de la dosis total fue excretada con la orina en forma de metabolitos (prácticamente no existía medicamento intacto en la orina), y el 57% de la dosis total fue excretada con las heces. En este estudio se identificaron dos metabolitos de finasterida que poseen sólo una pequeña fracción de su actividad inhibidora de la 5 -reductasa. En comparación con una dosis intravenosa de referencia, la biodisponibilidad de finasterida administrada por vía oral es de 80% aproximadamente, y no es afectada por la presencia de alimentos. La finasterida alcanza concentraciones plasmáticas máximas aproximadamente dos horas después de la administración, y su absorción es completa en seis u ocho horas. Tiene una semivida de eliminación plasmática de seis horas, y su unión a las proteínas plasmáticas es de 93% aproximadamente. El aclaramiento plasmático de finasterida es de 165 ml/min, y su volumen de distribución es de 76 litros. Un estudio con dosis múltiples demostró una lenta acumulación de pequeñas cantidades de finasterida. Después de administrar dosis diarias de 5 mg, las concentraciones plasmáticas mínimas de finasterida en estado de equilibrio fueron 8 a 10 ng/ml y se mantuvieron estables a lo largo del tiempo. No hay datos disponibles en pacientes con insuficiencia hepática. Finasterida es extensivamente metabolizada en el hígado, principalmente por el citocromo P450 3A4. El índice de eliminación de finasterida está algo disminuido en los hombres de edad avanzada. A medida que aumenta la edad, su semivida se prolonga aproximadamente de seis horas en hombres de 18 a 60 años a ocho horas en los mayores de 70 años. Esta diferencia no tiene ninguna importancia clínica y, por lo tanto, no es necesario reducir la dosificación.
10 En pacientes con insuficiencia renal crónica y aclaramiento de creatinina de 9 a 55 ml/min, la eliminación de una dosis única de 14 C-finasterida no fue diferente a la observada en voluntarios sanos, y tampoco varió su unión a las proteínas plasmáticas. En los pacientes con disfunción renal, una porción de los metabolitos que normalmente se excretan por vía renal fue excretada con las heces. Parece ser, por lo tanto, que la excreción de metabolitos por vía fecal aumenta en proporción con la disminución de su excreción urinaria. No es necesario hacer ningún ajuste de la dosificación en pacientes con disfunción renal que no estén sometidos a diálisis. Se ha hallado finasterida en el líquido cefalorraquídeo (LCR) de pacientes tratados con el mismo durante siete a diez días, pero el medicamento no parece concentrarse preferentemente con el LCR. También se ha recuperado finasterida del semen de sujetos que estaban recibiendo 5 mg diarios de finasterida. La cantidad de finasterida en el semen fue 50 a 100 veces menor que la dosis de finasterida (5 microgramos) y no tuvo ningún efecto sobre las concentraciones circulantes de DHT en hombres adultos. 5.3 Datos preclínicos sobre seguridad La DL 50 oral de finasterida es de aproximadamente 500 mg/kg en ratones machos y hembras, 400 mg/kg en ratas hembras, y mg/kg en ratas machos. Se han evaluado los efectos de la exposición in útero a finasterida durante el período de desarrollo embrionario y fetal en el mono rhesus (entre los días 20 y 100 de gestación), que es una especie con mayor valor predictivo del desarrollo humano que las ratas o los conejos. La administración intravenosa de dosis elevadas de finasterida de hasta 800 ng/día a monas preñadas (al menos 60 a 120 veces mayor que la exposición a finasterida más alta estimada en mujeres embarazadas, a partir del semen de varones tratados con 5 mg/día) no originó ninguna anomalía en los fetos machos. Para confirmar la relevancia del modelo rhesus aplicado al desarrollo fetal de los seres humanos, se administró una dosis oral muy elevada de finasterida (2 mg/kg/día; 20 veces la dosis de 5 mg/día recomendada en los seres humanos o aproximadamente 1-2 millones de veces la exposición a finasterida más alta estimada a partir del semen de varones tratados con 5 mg/día) a monas preñadas, lo que originó anomalías en los genitales externos de los fetos machos. No se observó ninguna otra anomalía en los fetos machos ni anomalías relacionadas con finasterida en los fetos hembras con ninguna dosis. Carcinogénesis y Mutagénesis No se observó ningún indicio de efecto tumorígeno en un estudio en ratas que recibieron hasta 320 mg/kg/día de finasterida durante 24 meses (3.200 veces más que la dosis recomendada en seres humanos). En un estudio de carcinogenicidad de 19 meses en ratones se observó un aumento estadísticamente significativo (p 0,05) en la frecuencia de adenomas testiculares de las células de Leydig con una dosificación de 250 mg/kg/día (2.500 veces mayor que la dosis recomendada en seres humanos); no se observaron adenomas en los ratones que recibieron 2,5 ó 25 mg/kg/día (25 y 250 veces más que la dosis recomendada en seres humanos, respectivamente). No se observó ningún indicio de mutagenicidad en ensayos de mutagénesis bacteriana in vitro, de mutagénesis en células de mamífero, ni de elución alcalina in vitro. En un ensayo de aberración cromosómica in vitro, cuando se trataron células de ovario de hámster chino con concentraciones altas ( mol) de finasterida hubo un ligero aumento de las aberraciones cromosómicas. Esas concentraciones son veces mayores que las concentraciones plasmáticas máximas obtenidas en el hombre con una dosis total de 5 mg. Además, las concentraciones empleadas en los estudios in vitro ( mol) no se pueden alcanzar en un sistema biológico. En un ensayo de aberración cromosómica in vivo en ratones, no se observó ningún aumento de las aberraciones cromosómicas relacionado con el tratamiento, administrando finasterida a la dosis máxima tolerada (250 mg/kg/día, veces mayor que la dosis recomendada en seres humanos).
11 6. DATOS FARMACÉUTICOS 6.1 Lista de excipientes Laurilsulfato de sodio Almidón pregelatinizado de maíz sin gluten Lactosa monohidrato Celulosa microcristalina Glicolato sódico de almidón de patata sin gluten Estearato magnésico Hipromelosa Macrogol 8 estearato. 6.2 Incompatibilidades No se han descrito. 6.3 Período de validez 24 meses. 6.4 Precauciones especiales de conservación No requiere condiciones especiales de conservación. 6.5 Naturaleza y contenido del recipiente Finasterida KERN PHARMA 5 mg comprimidos se presenta en envase de 28 y 500 comprimidos, en blister calendario de Al/PVC-PVDC. 6.6 Instrucciones de uso/manipulación Las mujeres que estén o pudieran estar embarazadas no deben manipular comprimidos aplastados o rotos de Finasterida KERN PHARMA 5 mg comprimidos (ver sección 4.3 Contraindicaciones; Embarazo, y Exposición a finasterida - Riesgo para el feto varón). 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN KERN PHARMA, S.L Pol. Industrial Colón II Venus, Terrassa (Barcelona) 8. NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN FECHA DE LA PRIMERA AUTORIZACIÓN/REVALIDACIÓN DE LA AUTORIZACIÓN Octubre 2005
12 10. FECHA DE REVISIÓN DEL TEXTO
FICHA TÉCNICA. Los comprimidos son blancos, redondos y marcados con F5 en una de las caras.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Pensa 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Pensa 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg de
FICHA TÉCNICA. Cada comprimido recubierto con película contiene 5 mg de finasterida. Excipientes con efecto conocido: 75 mg de lactosa
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Pensa 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Pensa 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg de
Finastar. FINASTAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA. Esta especialidad se presenta como:
 Finastar FINASTAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: FINASTAR 5 mg cuya composición es: - Principio activo: Finasterida 5 mg - Excipientes (ver
Finastar FINASTAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: FINASTAR 5 mg cuya composición es: - Principio activo: Finasterida 5 mg - Excipientes (ver
PROSCAR (finasterida) PROSCAR 5 mg cuya composición es: - Principio activo: Finasterida... 5 mg - Excipientes (ver 6.1), c.s.p...
 FICHA TÉCNICA IPC - 0199 Tracer No. PSC-E-20030237 01/03 PROSCAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: PROSCAR 5 mg cuya composición es: - Principio
FICHA TÉCNICA IPC - 0199 Tracer No. PSC-E-20030237 01/03 PROSCAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: PROSCAR 5 mg cuya composición es: - Principio
FICHA TÉCNICA. La posología recomendada es un comprimido diario de 5 mg, con o sin alimentos.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Mabo 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Mabo 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes:
FICHA TÉCNICA. FINASTERIDA BENEL 5 mg comprimidos recubiertos con película EFG
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO FINASTERIDA BENEL 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida Para
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO FINASTERIDA BENEL 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida Para
FICHA TÉCNICA. finasterida cinfa 5 mg comprimidos recubiertos con película EFG
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO finasterida cinfa 5 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida Para
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO finasterida cinfa 5 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida Para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Finasterida Alter 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Finasterida Alter 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA. Comprimidos de color azul claro, cilíndricos, biconvexos, recubiertos y lisos por ambas caras.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO finasterida cinfa 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO finasterida cinfa 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes:
EUCOPROST (finasterida)
 FICHA TÉCNICA para Médicos IPC 0997a Tracer No. PSC-E-14800 07/99 EUCOPROST (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: EUCOPROST 5 mg cuya composición es:
FICHA TÉCNICA para Médicos IPC 0997a Tracer No. PSC-E-14800 07/99 EUCOPROST (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: EUCOPROST 5 mg cuya composición es:
FINASTERIDA QUALIGEN 5 mg comprimidos recubiertos con película EFG
 1. NOMBRE DEL MEDICAMENTO FINASTERIDA QUALIGEN 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Para consultar la lista
1. NOMBRE DEL MEDICAMENTO FINASTERIDA QUALIGEN 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Para consultar la lista
FICHA TÉCNICA. Los comprimidos son redondos, biconvexos, lisos por ambas caras y de color azul claro.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Apotex 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida Excipientes:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Apotex 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida Excipientes:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Finasterida RANBAXY 5mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida RANBAXY 5mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida RANBAXY 5mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes:
La posología recomendada es un comprimido diario de 5 mg, con o sin alimentos.
 1. NOMBRE DEL MEDICAMENTO PROSCAR 5 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes con efecto conocido: 106,40
1. NOMBRE DEL MEDICAMENTO PROSCAR 5 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes con efecto conocido: 106,40
FICHA TÉCNICA. Cada comprimido recubierto con película contiene 5 mg de finasterida.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida TecniGen 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida TecniGen 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg
Hipersensibilidad a cualquiera de los componentes de este producto.
 PROSCAR 5 mg TABLETAS RECUBIERTAS (Finasteride) PROSCAR (Finasteride) un compuesto sintético 4 azasteroide, es un inhibidor específico de la 5α - reductasa Tipo II, una enzima intracelular que metaboliza
PROSCAR 5 mg TABLETAS RECUBIERTAS (Finasteride) PROSCAR (Finasteride) un compuesto sintético 4 azasteroide, es un inhibidor específico de la 5α - reductasa Tipo II, una enzima intracelular que metaboliza
Comprimidos de color azul, redondos, biconvexos, recubiertos con película, marcados con "F5" en un lado y sin marca alguna en el otro lado.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Finasterida Zentiva 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Finasterida Zentiva 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto
FICHA TÉCNICA. Excipiente con efecto conocido: Lactosa monohidrato 90,95 mg/comprimido.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida NORMON 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto contiene 5 mg de finasterida.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida NORMON 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto contiene 5 mg de finasterida.
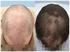
Finasterida está indicada para el tratamiento de las primeras fases de la alopecia androgenética en varones.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Actavis 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Actavis 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg
FICHA TÉCNICA. Comprimido recubierto con película. Comprimido recubierto con película de color azul, redondo, biconvexo, liso por ambas caras.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Combix 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Combix 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg
FICHA TÉCNICA. Excipiente(s) con efecto conocido: lactosa monohidrato 90,9 mg/comprimido recubierto con película.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Sandoz 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto con película contiene 5 mg de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Sandoz 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto con película contiene 5 mg de
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TEALEP 2. Nombre Genérico: FINASTERIDA 3. Forma Farmacéutica y Formulación: Comprimidos. Cada comprimido contiene: Finasterida... 5 mg Excipiente
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TEALEP 2. Nombre Genérico: FINASTERIDA 3. Forma Farmacéutica y Formulación: Comprimidos. Cada comprimido contiene: Finasterida... 5 mg Excipiente
PROSCAR está indicado para tratar y controlar la hiperplasia prostática benigna (HPB) y prevenir trastornos urológicos, para:
 I. NOMBRE COMERCIAL II. NOMBRE GENÉRICO Finasterida, MSD III. FORMA FARMACÉUTICA Y FORMULACIÓN Tabletas Cada Tableta contiene: Finasterida... 5 mg Excipiente... 1 Tableta IV. INDICACIONES TERAPÉUTICAS
I. NOMBRE COMERCIAL II. NOMBRE GENÉRICO Finasterida, MSD III. FORMA FARMACÉUTICA Y FORMULACIÓN Tabletas Cada Tableta contiene: Finasterida... 5 mg Excipiente... 1 Tableta IV. INDICACIONES TERAPÉUTICAS
Prospecto: Información para el usuario Finasterida Kern Pharma 5 mg comprimidos recubiertos con película EFG
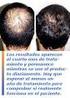 Prospecto: Información para el usuario Finasterida Kern Pharma 5 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
Prospecto: Información para el usuario Finasterida Kern Pharma 5 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
No existen pruebas de que la elevación de la dosis aumente la eficacia. No es necesario ajustar la posología en pacientes con insuficiencia renal.
 Propecia RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DE LA ESPECIALIDAD FARMACÉUTICA PROPECIA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 1 mg de finasterida. 3. FORMA FARMACÉUTICA
Propecia RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DE LA ESPECIALIDAD FARMACÉUTICA PROPECIA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 1 mg de finasterida. 3. FORMA FARMACÉUTICA
FICHA TÉCNICA. Comprimidos recubiertos blancos, redondos y marcados con F y 5 en una de las caras.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida ratiopharm 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida ratiopharm 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5
FICHA TÉCNICA. Cada comprimido recubierto con película contiene 1 mg de finasterida.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Capikern 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg de finasterida.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Capikern 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg de finasterida.
FICHA TÉCNICA. Comprimidos redondos, biconvexos, de color marrón rojizo, de 7 mm de diámetro y con la marca "F1" en una de las caras.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ALOCARE 1 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Finasterida Cada comprimido recubierto con película
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ALOCARE 1 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Finasterida Cada comprimido recubierto con película
FICHA TÉCNICA. Finasterida NORMON no esta indicado en mujeres o niños y adolescentes.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida NORMON 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto contiene 1 mg de finasterida.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida NORMON 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto contiene 1 mg de finasterida.
FICHAS TÉCNICAS. Finasterida NORMON 1 mg comprimidos recubiertos con película EFG Finasterida NORMON 5 mg comprimidos recubiertos con película EFG
 FICHAS TÉCNICAS Finasterida NORMON 1 mg comprimidos recubiertos con película EFG Finasterida NORMON 5 mg comprimidos recubiertos con película EFG RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL
FICHAS TÉCNICAS Finasterida NORMON 1 mg comprimidos recubiertos con película EFG Finasterida NORMON 5 mg comprimidos recubiertos con película EFG RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL
Finasterida Biorga 1 mg comprimidos recubiertos con película EFG. Cada comprimido recubierto con película contiene 1 mg de finasterida.
 1. NOMBRE DEL MEDICAMENTO Finasterida Biorga 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg de finasterida.
1. NOMBRE DEL MEDICAMENTO Finasterida Biorga 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg de finasterida.
Finasterida está indicada para el tratamiento de las primeras fases de la alopecia androgenética en varones.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Actavis 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Actavis 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg
FICHA TÉCNICA. Excipientes con efecto conocido: 0,458 g de maltitol líquido (E965) y 1,830 g de isomalta (E953).
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
FICHAS TÉCNICAS. Finasterida NORMON 1 mg comprimidos recubiertos con película EFG Finasterida NORMON 5 mg comprimidos recubiertos con película EFG
 FICHAS TÉCNICAS Finasterida NORMON 1 mg comprimidos recubiertos con película EFG Finasterida NORMON 5 mg comprimidos recubiertos con película EFG RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL
FICHAS TÉCNICAS Finasterida NORMON 1 mg comprimidos recubiertos con película EFG Finasterida NORMON 5 mg comprimidos recubiertos con película EFG RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL
FICHA TÉCNICA. Excipientes con efecto conocido 1,38 g de sacarosa y 1,10 g glucosa. Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
FICHA TÉCNICA. Cada comprimido recubierto con película contiene 1 mg de finasterida.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Teva 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida Teva 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 1 mg de
Ficha técnica Página 1
 1. NOMBRE DEL MEDICAMENTO: Difur 120 mg cápsulas duras. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada cápsula contiene 120 mg de extracto seco de rizoma de Polypodium leucotomos L. (DER nativo 4-6:1)
1. NOMBRE DEL MEDICAMENTO: Difur 120 mg cápsulas duras. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada cápsula contiene 120 mg de extracto seco de rizoma de Polypodium leucotomos L. (DER nativo 4-6:1)
FICHA TÉCNICA. No hay evidencia de que un aumento en la dosis se traduzca en un aumento en la eficacia.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Predser 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto contiene 1 mg de finasterida. Excipiente(s)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Predser 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto contiene 1 mg de finasterida. Excipiente(s)
Prospecto: información para el usuario. Finasterida pensa 5 mg comprimidos recubiertos con película EFG
 Prospecto: información para el usuario Finasterida pensa 5 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
Prospecto: información para el usuario Finasterida pensa 5 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
FICHA TÉCNICA. LORATADINA KERN PHARMA está indicado para el tratamiento sintomático de rinitis alérgica y urticaria idiopática crónica.
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO LORATADINA KERN PHARMA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Lista de excipientes,
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO LORATADINA KERN PHARMA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Lista de excipientes,
FICHA TÉCNICA. No se requieren ajustes en la dosificación en ancianos o en pacientes con insuficiencia renal.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina ratiopharm 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes: Cada comprimido
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina ratiopharm 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes: Cada comprimido
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
FICHA TÉCNICA 4. DATOS CLÍNICOS
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO EBASTINA ALPROFARMA 10 mg Comprimidos recubiertos con película EFG. EBASTINA ALPROFARMA 20 mg Comprimidos recubiertos con película EFG. 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO EBASTINA ALPROFARMA 10 mg Comprimidos recubiertos con película EFG. EBASTINA ALPROFARMA 20 mg Comprimidos recubiertos con película EFG. 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA. Normoreum 400 mg comprimidos recubiertos con película
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO AVIDART 0,5 MG CÁPSULAS BLANDAS
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO AVIDART 0,5 MG CÁPSULAS BLANDAS 1. DENOMINACIÓN DEL MEDICAMENTO AVIDART 0,5mg, Cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO AVIDART 0,5 MG CÁPSULAS BLANDAS 1. DENOMINACIÓN DEL MEDICAMENTO AVIDART 0,5mg, Cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
I. Denominación distintiva PROPESHIA. II. Denominación genérica. Finasterida. III. Forma Farmacéutica y Formulación PROPESHIA.
 I. Denominación distintiva PROPESHIA II. Denominación genérica Finasterida III. Forma Farmacéutica y Formulación PROPESHIA Tabletas Cada tableta de PROPESHIA contiene finasterida... 1 mg Excipiente c.b.p....
I. Denominación distintiva PROPESHIA II. Denominación genérica Finasterida III. Forma Farmacéutica y Formulación PROPESHIA Tabletas Cada tableta de PROPESHIA contiene finasterida... 1 mg Excipiente c.b.p....
El principio activo es finasterida. Cada comprimido contiene 5 mg de finasterida.
 Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO. FAMVIR comprimidos 125 mg FAMVIR comprimidos 250 mg FAMVIR comprimidos 750 mg
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO FAMVIR comprimidos 125 mg FAMVIR comprimidos 250 mg FAMVIR comprimidos 750 mg 2. COMPOSICION CUALITATIVA Y CUANTITATIVA FAMVIR comprimidos 125 mg: Principio activo
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO FAMVIR comprimidos 125 mg FAMVIR comprimidos 250 mg FAMVIR comprimidos 750 mg 2. COMPOSICION CUALITATIVA Y CUANTITATIVA FAMVIR comprimidos 125 mg: Principio activo
FICHA TÉCNICA. La ranura sirve únicamente para fraccionar y facilitar la deglución pero no para dividir en dosis iguales.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO LORATADINA KORHISPANA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes: Lactosa, 75,50 mg.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO LORATADINA KORHISPANA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes: Lactosa, 75,50 mg.
FICHA TÉCNICA. La duración estimada del tratamiento será de dos semanas.
 FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Finasterida KERN PHARMA 1 mg comprimidos recubiertos con película EFG
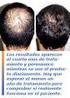 PROSPECTO: INFORMACIÓN PARA EL USUARIO Finasterida KERN PHARMA 1 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este
PROSPECTO: INFORMACIÓN PARA EL USUARIO Finasterida KERN PHARMA 1 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este
ambroxol cinfa 15 mg / 5 ml jarabe EFG
 FICHA TÉCNICA ambroxol cinfa 15 mg / 5 ml jarabe EFG 1. NOMBRE DEL MEDICAMENTO ambroxol cinfa 15 mg/5 ml jarabe EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA 5 ml de jarabe contienen 15 mg de clorhidrato
FICHA TÉCNICA ambroxol cinfa 15 mg / 5 ml jarabe EFG 1. NOMBRE DEL MEDICAMENTO ambroxol cinfa 15 mg/5 ml jarabe EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA 5 ml de jarabe contienen 15 mg de clorhidrato
FICHA TÉCNICA. No se requieren ajustes en la dosificación en ancianos o en pacientes con insuficiencia renal.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina ratiopharm 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina ratiopharm 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes con efecto conocido:
FICHA TECNICA. Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ZULEX 333 mg, Comprimidos recubiertos 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ZULEX 333 mg, Comprimidos recubiertos 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
FICHA TÉCNICA. Adultos y niños mayores de 12 años: máximo 10 mg al día en una única toma
 1. NOMBRE DEL MEDICAMENTO REACTINE 10 mg Comprimidos FICHA TÉCNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de cetirizina (DOE) dihidrocloruro Lista de excipientes, en 6.1
1. NOMBRE DEL MEDICAMENTO REACTINE 10 mg Comprimidos FICHA TÉCNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de cetirizina (DOE) dihidrocloruro Lista de excipientes, en 6.1
ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg. COMPOSICIÓN Cada comprimido recubierto contiene: Excipientes: Según lo aprobado en Registro
 ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg COMPOSICIÓN Cada comprimido recubierto contiene: Anastrozol 1 mg Excipientes: Según lo aprobado en Registro CLASIFICACION TERAPEUTICA Antineoplásico INDICACIONES
ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg COMPOSICIÓN Cada comprimido recubierto contiene: Anastrozol 1 mg Excipientes: Según lo aprobado en Registro CLASIFICACION TERAPEUTICA Antineoplásico INDICACIONES
Comprimidos recubiertos con película de color blanco, oblongo, y ranurado por una cara.
 1. DENOMINACIÓN DEL MEDICAMENTO Cetirizina ACOST Comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cetirizina ACOST comprimidos recubiertos con película : cada comprimido
1. DENOMINACIÓN DEL MEDICAMENTO Cetirizina ACOST Comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cetirizina ACOST comprimidos recubiertos con película : cada comprimido
PROPUESTA DE FICHA TÉCNICA
 PROPUESTA DE FICHA TÉCNICA 1. DENOMINACION DEL MEDICAMENTO EBASTINA COMBIX 20 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película
PROPUESTA DE FICHA TÉCNICA 1. DENOMINACION DEL MEDICAMENTO EBASTINA COMBIX 20 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. 2.1 Descripción general
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Las cápsulas son ovales, con el cuerpo y la tapa de color blanco.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 50 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Las cápsulas son ovales, con el cuerpo y la tapa de color blanco.
1. NOMBRE DEL MEDICAMENTO. Doxazosina COMBINO PHARM 2 mg comprimidos EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
 1. NOMBRE DEL MEDICAMENTO Doxazosina COMBINO PHARM 2 mg comprimidos EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA 2 mg de doxazosina (mesilato). Para excipientes, ver 6.1. 3. FORMA FARMACEUTICA Comprimidos
1. NOMBRE DEL MEDICAMENTO Doxazosina COMBINO PHARM 2 mg comprimidos EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA 2 mg de doxazosina (mesilato). Para excipientes, ver 6.1. 3. FORMA FARMACEUTICA Comprimidos
FICHA TÉCNICA. Adultos y adolescentes mayores de 12 años: de 250 a 500 mg al día distribuidos en dos tomas (mañana y noche)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TÉCNICA. No exceder la dosis máxima de 480 mg de simeticona (4 comprimidos masticables) al día.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 120 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona.. 120 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 120 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona.. 120 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA. 1. DENOMINACIÓN DEL MEDICAMENTO: GLUCOSAMINA GINELADIUS 625 mg comprimidos recubiertos con película
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO: GLUCOSAMINA GINELADIUS 625 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene 750 mg de Hidrocloruro
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO: GLUCOSAMINA GINELADIUS 625 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene 750 mg de Hidrocloruro
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. LORATADINA RANBAXY 10 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO LORATADINA RANBAXY 10 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO LORATADINA RANBAXY 10 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes con efecto conocido:
Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO bucomax pastillas para chupar sabor menta bucomax pastillas para chupar sabor fresa bucomax pastillas para chupar sabor miel y limón 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
1. NOMBRE DEL MEDICAMENTO bucomax pastillas para chupar sabor menta bucomax pastillas para chupar sabor fresa bucomax pastillas para chupar sabor miel y limón 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
PROYECTO DE PROSPECTO PROSCAR FINASTERIDE 5 mg Comprimidos Recubiertos
 INDUSTRIA NORTEAMERICANA PROYECTO DE PROSPECTO PROSCAR FINASTERIDE 5 mg Comprimidos Recubiertos VENTA BAJO RECETA FÓRMULA: Cada comprimido recubierto contiene: Finasteride... 5,0 mg Lactosa... 106,4 mg
INDUSTRIA NORTEAMERICANA PROYECTO DE PROSPECTO PROSCAR FINASTERIDE 5 mg Comprimidos Recubiertos VENTA BAJO RECETA FÓRMULA: Cada comprimido recubierto contiene: Finasteride... 5,0 mg Lactosa... 106,4 mg
FICHA TÉCNICA. Supositorios incoloros semitransparentes envasados en blíster de aluminio-polietileno.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SUPOSITORIOS DE GLICERINA MICRALAX ADULTOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Supositorios incoloros semitransparentes envasados en
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SUPOSITORIOS DE GLICERINA MICRALAX ADULTOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Supositorios incoloros semitransparentes envasados en
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea
 FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Ultra Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Ultra Levura 250 mg granulado para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene: Saccharomyces boulardii 250 mg Excipientes con
PROSPECTO: INFORMACIÓN PARA EL USUARIO. FINASTERIDA APOTEX 5 mg COMPRIMIDOS RECUBIERTOS CON PELÍCULA EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO FINASTERIDA APOTEX 5 mg COMPRIMIDOS RECUBIERTOS CON PELÍCULA EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto,
PROSPECTO: INFORMACIÓN PARA EL USUARIO FINASTERIDA APOTEX 5 mg COMPRIMIDOS RECUBIERTOS CON PELÍCULA EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto,
PROPUESTA DE FICHA TÉCNICA
 PROPUESTA DE FICHA TÉCNICA 1. DENOMINACION DEL MEDICAMENTO EBASTINA COMBIX 10 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película
PROPUESTA DE FICHA TÉCNICA 1. DENOMINACION DEL MEDICAMENTO EBASTINA COMBIX 10 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película
FICHA TÉCNICA. Cada pastilla para chupar contiene 1,2 mg de alcohol 2,4-diclorobencílico y 0,6 mg de amilmetacresol.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Strepsils pastillas para chupar sabor miel y limón 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Cada pastilla para chupar contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Strepsils pastillas para chupar sabor miel y limón 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Cada pastilla para chupar contiene
Prospecto: información para el usuario. Lambdaxel 1 mg comprimidos recubiertos con película EFG Finasterida
 Prospecto: información para el usuario Lambdaxel 1 mg comprimidos recubiertos con película EFG Finasterida Lea todo el prospecto detenidamente antes de tomar el medicamento. Conserve este prospecto ya
Prospecto: información para el usuario Lambdaxel 1 mg comprimidos recubiertos con película EFG Finasterida Lea todo el prospecto detenidamente antes de tomar el medicamento. Conserve este prospecto ya
FICHA TÉCNICA. Cada gramo de crema contiene 100 mg de docosanol. Excipiente con efecto conocido: 50 mg propilenglicol/gramo de crema.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Erazaban 100 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 100 mg de docosanol. Excipiente con efecto conocido: 50 mg propilenglicol/gramo
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Erazaban 100 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 100 mg de docosanol. Excipiente con efecto conocido: 50 mg propilenglicol/gramo
aciclovir cinfa 800 mg - E.F.G. comprimidos dipersables FICHA TÉCNICA
 comprimidos dipersables FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO aciclovir cinfa 800 mg - E.F.G. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 800 mg de aciclovir (D.C.I.) 3. FORMA
comprimidos dipersables FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO aciclovir cinfa 800 mg - E.F.G. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 800 mg de aciclovir (D.C.I.) 3. FORMA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 5,9 gramos de Macrogol 3350. Excipientes con efecto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 5,9 gramos de Macrogol 3350. Excipientes con efecto
Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol.
 1. NOMBRE DEL MEDICAMENTO TROSID 280 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol. Para consultar la
1. NOMBRE DEL MEDICAMENTO TROSID 280 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol. Para consultar la
FICHA TÉCNICA. Alivio a corto plazo (durante dos-tres meses) del edema y síntomas relacionados con la insuficiencia venosa crónica.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA troxerutina cinfa 1000 mg granulado para solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 1000 mg de troxerutina. Para consultar la lista
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA troxerutina cinfa 1000 mg granulado para solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 1000 mg de troxerutina. Para consultar la lista
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Cada gramo de pomada bucal contiene:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada bucal contiene: Carbenoxolona disódica. 20 mg Excipientes: Para consultar
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada bucal contiene: Carbenoxolona disódica. 20 mg Excipientes: Para consultar
FICHA TECNICA. Tratamiento de la intoxicación por Amanita phalloides.
 FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TÉCNICA. Comprimidos recubiertos con película, de color anaranjado, oblongos y ranurados por una cara.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Flebikern 500 mg comprimidos recubiertos con película. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene: Fracción flavonoica
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Flebikern 500 mg comprimidos recubiertos con película. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene: Fracción flavonoica
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA. Adolescentes mayores de 12 años de edad, adultos y personas de edad avanzada: 1 comprimido 3 veces al día.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Valdispertstress comprimidos recubiertos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto contiene: 200 mg de extracto (como extracto seco)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Valdispertstress comprimidos recubiertos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto contiene: 200 mg de extracto (como extracto seco)
FORMA FARMACÉUTICA Y FORMULACIÓN:
 Profidox * Tabletas (Finasteride/alfuzosina) FORMA FARMACÉUTICA Y FORMULACIÓN: Cada TABLETA contiene: Finasteride 5 mg Clorhidrato de alfuzosina 5 mg Excipiente, c.b.p. 1 tableta. INDICACIONES TERAPÉUTICAS:
Profidox * Tabletas (Finasteride/alfuzosina) FORMA FARMACÉUTICA Y FORMULACIÓN: Cada TABLETA contiene: Finasteride 5 mg Clorhidrato de alfuzosina 5 mg Excipiente, c.b.p. 1 tableta. INDICACIONES TERAPÉUTICAS:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Dolovet vet 2,4 g polvo para uso oral. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Principio(s) activo(s): Ketoprofeno
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Dolovet vet 2,4 g polvo para uso oral. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Principio(s) activo(s): Ketoprofeno
SKELID 200 mg comprimidos
 SKELID 200 mg comprimidos 1. DENOMINACIÓN DEL MEDICAMENTO SKELID 200 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Acido tiludrónico (D.C.I.) sal disódica cantidad correspondiente a ácido
SKELID 200 mg comprimidos 1. DENOMINACIÓN DEL MEDICAMENTO SKELID 200 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Acido tiludrónico (D.C.I.) sal disódica cantidad correspondiente a ácido
FICHA TÉCNICA. FAMOTIDINA STADA 20 mg comprimidos recubiertos con película EFG Cada comprimido recubierto contiene:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO FAMOTIDINA STADA 20 mg comprimidos recubiertos con película EFG FAMOTIDINA STADA 40 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO FAMOTIDINA STADA 20 mg comprimidos recubiertos con película EFG FAMOTIDINA STADA 40 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 NORFLOXACINA 400 mg COMPRIMIDOS RECUBIERTOS ANTIBACTERIANO Página 1 NORFLOXACINA 400 mg Comprimidos Recubiertos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 NORFLOXACINA 400 mg COMPRIMIDOS RECUBIERTOS ANTIBACTERIANO Página 1 NORFLOXACINA 400 mg Comprimidos Recubiertos
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO MEDICAMENTOS VETERINARIOS DE RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CAPSTAR 57 mg COMPRIMIDOS PARA PERROS GRANDES 2. COMPOSICIÓN CUALITATIVA
DEPARTAMENTO MEDICAMENTOS VETERINARIOS DE RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CAPSTAR 57 mg COMPRIMIDOS PARA PERROS GRANDES 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA. Posología Administrar cuando sea necesario, o según criterio médico. Como norma general administrar:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Citrato/Lauril sulfoacetato 450 mg/ 45 mg solución rectal Citrato de sodio / Lauril sulfoacetato de sodio 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Citrato/Lauril sulfoacetato 450 mg/ 45 mg solución rectal Citrato de sodio / Lauril sulfoacetato de sodio 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por
20preguntas. frecuentes sobre la salud del hombre CONAC
 20preguntas frecuentes sobre la salud del hombre D E E D U C A C I Ó N CONAC 1 Qué es y para qué sirve la próstata? Es una glándula del sistema reproductor masculino que produce una secreción que es parte
20preguntas frecuentes sobre la salud del hombre D E E D U C A C I Ó N CONAC 1 Qué es y para qué sirve la próstata? Es una glándula del sistema reproductor masculino que produce una secreción que es parte
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Para la lista completa de excipientes, véase la sección 6.1.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO RIMADYL COMPRIMIDOS 50 mg. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Sustancia activa Carprofeno
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO RIMADYL COMPRIMIDOS 50 mg. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Sustancia activa Carprofeno
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO INCURIN 1 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Sustancia activa: estriol
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO INCURIN 1 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Sustancia activa: estriol
