Electroquímica (III) Electrolisis
|
|
|
- Juan Luis Ferreyra Vidal
- hace 10 años
- Vistas:
Transcripción
1 Electroquímica (III) IES La Magdalena. Avilés. Asturias En las celdas electroquímicas, o pilas, se genera una corriente eléctrica mediante una reacción química (se transforma la energía química en energía eléctrica). El proceso inverso: producir una reacción química a partir de una corriente eléctrica, también es posible. Para ello (ver figura) sólo hay que lograr que una corriente eléctrica (continua) pase a través de una sal fundida o una disolución acuosa de un electrolito. La corriente eléctrica produce entonces en ambos electrodos reacciones de oxidación y reducción y el proceso se conoce con el nombre de electrolisis. La electrolisis de las sales fundidas es la más sencilla de explicar teóricamente (aunque en la práctica tiene el inconveniente de que es preciso mantener altas temperaturas con el fin de mantener la sal fundida). Si introducimos dos electrodos en la masa fundida, y los conectamos a una fuente de corriente continua, los iones negativos se dirigen hacia el polo positivo. Una vez allí se oxidan, perdiendo electrones. Como se puede ver, al igual que en las pilas, en el ánodo se produce la oxidación, pero al contrario que en las pilas, en una cuba electrolítica el ánodo es el electrodo positivo. Los iones positivos, de forma análoga, se dirigirán hacia el electrodo negativo, allí captarán electrones y se reducirán. En el cátodo se verifica la reacción de reducción. En una cuba electrolítica el cátodo es el electrodo negativo. Electrodos Tipo reacción Signo Pilas/electrolisis Pilas/electrolisis Pilas Ánodo Oxidación Negativo Positivo Cátodo Reducción Positivo Negativo del cloruro de sodio fundido: Cl (l) Cl (g) + e Ánodo. Oxidación + Na (l) + e Na(s) Cátodo. Re ducción + Cl (l) + Na (l) Cl (g) + Na(s) Como productos observaríamos la formación de cloro gas en el ánodo y de sodio metálico en el cátodo. 1
2 Química º Bachillerato. IES La Magdalena. Avilés. Asturias Si calculamos el potencial estándar para la reacción planteada obtenemos: DATOS: E (Cl /Cl - )= 1,36 V; E (Na + /Na)= -,71 V Cl (l) Cl (g) + e Ánodo. Oxidación. E = 1,36 V Oxid + Na (l) + e Na(s) Cátodo. Re ducción. E =,71 V Re d + Cl (l) + Na (l) Cl (g) + Na(s) E = E + E =,71 V + ( 1,36 V) = 4,7 V Celda Red Oxid Como se ve el potencial estándar para la celda es negativo. La reacción no será espontánea y habrá que comunicar, como mínimo, una diferencia de potencial de 4,7 V para llevarla a cabo. En la realidad la diferencia de potencial necesaria para la electrolisis puede ser bastante mayor, debido a la aparición de sobretensiones, especialmente importantes cuando se desprenden gases o cuando se depositan sustancias sobre el electrodo. Cuando se realizan electrolisis de sustancias en disolución acuosa (mucho más sencillas de realizar en la práctica) es más difícil de prever el resultado de la electrolisis, ya que existen reacciones en competencia en ambos electrodos. El que suceda una u otra dependerá de varios factores, uno de ellos la concentración de la sustancia disuelta. Básicamente los procesos que pueden producirse son: Electrodo positivo (ánodo) Hacia el ánodo se dirigirán los iones negativos (aniones) que experimentarán una reacción de oxidación El que esta reacción se produzca, o no, dependerá de la facilidad con que se oxide el anión (el elemento central, si el anión es poliatómico). Hay aniones que no son oxidables. Esto ocurre cuando el átomo central está en su estado de oxidación más alto. Ocurre esto en los siguientes aniones: NO 3 -, SO 4 -, CO 3 -, HCO 3 -, MnO Otros iones, como el Cl -, pueden oxidarse en el ánodo, dando Cl gas: Cl - (ac) Cl (g) + e - En el ánodo también existe una reacción de competencia debida a la presencia del agua. El agua trata de oxidarse para dar oxígeno (gas) según la siguiente reacción: Electrodo negativo (cátodo) H O O (g) + 4 H + (ac) + 4 e - (E oxd = - 1,3 V) Hacia el cátodo se dirigirán los iones positivos (cationes) que experimentarán una reacción de reducción El que esta reacción se produzca, o no, dependerá de la facilidad con que se reduzca el catión. Hay cationes que son se reducen muy difícilmente. Esto ocurre con los cationes de los metales muy activos (alcalinos y alcalino-térreos). Metales menos activos como el Cu, Cr, Pb, Ag, Ni, Zn... se reducen más fácilmente, razón por la que en la electrolisis de sus sales se depositan en el cátodo en su forma metálica. En el cátodo también existe una reacción de competencia debida a la presencia del agua. El agua trata de reducirse para dar hidrógeno (gas) según: H O + e - H (g) + OH - (ac) (E red = -,83 V)
3 Química º Bachillerato. IES La Magdalena. Avilés. Asturias En la imagen se ha representado la electrolisis de una disolución acuosa de NaHCO 3. La sal estará disociada en iones HCO 3 - y Na +. Los primeros se desplazarán hacia el electrodo positivo, pero debido a que el carbono está en su estado de oxidación más alto, no se oxidará. Si se oxidará, sin embargo, el oxígeno del agua: + HO O (g) + 4H (ac) + 4e E Oxid = 1,3 V Observaremos, por tanto, el desprendimiento de oxígeno en el ánodo. Además, la disolución en esa zona disminuirá su ph debido a la aparición de iones H + (H 3 O + ). Los iones Na + se dirigirán hacia el cátodo, pero no se reducirán, ya que la reacción correspondiente a la reducción del hidrógeno del agua tiene un potencial de reducción considerablemente más alto y, en consecuencia, se verifica con preferencia: H O + e H (g) + OH (ac) E =,83 V Red Observaremos, por tanto, el desprendimiento de hidrógeno en el cátodo. Además, la disolución en esa zona aumentará su ph debido a la aparición de iones OH -. El potencial mínimo que habrá que comunicar para que la electrolisis tenga lugar será (aunque son previsibles sobretensiones considerables debido al desprendimiento de gases en ambos electrodos): H O O (g) + 4 H (ac) + 4e E = 1,3 V + Oxid H O + e H (g) + OH (ac) E =,83 V Re d + 6 H O O (g) + H (g) + 4H (ac) + 4OH (ac) H O O (g) + H (g) E = E + E =,83 V + ( 1,3)V =,6 V Celda Red Oxid 4 H O La electrolisis de un disolución acuosa de NaCl añade alguna dificultad a lo ya visto. El proceso que se desarrolla en el cátodo es previsible y similar a lo visto anteriormente: los iones Na + no se reducirán, ya que la reacción correspondiente a la reducción del hidrógeno del agua tiene un potencial de reducción considerablemente más alto y, en consecuencia, se verifica con preferencia: H O + e H (g) + OH (ac) E =,83 V Red Observaremos, por tanto, el desprendimiento de hidrógeno en el cátodo. Además, la disolución en esa zona aumentará su ph debido a la aparición de iones OH- El proceso anódico, sin embargo, presenta mayor dificultad, ya que existen dos reacciones en competencia: Oxidación del oxígeno del agua para dar oxígeno gaseoso: H O O (g) + 4H (ac) + 4e + Oxidación del ión Cl - para dar cloro gaseoso: Cl (ac) Cl (g) + e El que se obtenga uno u otro no es fácil de prever ya que los potenciales (teóricos) para las semirreacciones correspondientes son muy similares y pueden verse seriamente afectados por las sobretensiones. De manera general podemos decir que se desprenderá oxígeno en disoluciones diluidas, mientras que si la disolución es concentrada la tendencia es a que se desprenda cloro. 3
4 Química º Bachillerato. IES La Magdalena. Avilés. Asturias Ejemplo 1 (Oviedo. 9-1) En el laboratorio se desea realizar la deposición electrolítica de cobre a partir de una disolución acuosa de sulfato de cobre(ii). Dibuje un esquema completo de la cuba electrolítica, indicando el material de laboratorio utilizado Solución: El esquema de la cuba electrolítica y de las reacciones en ambos electrodos se puede ver a la derecha. Consiste en dos electrodos (pueden ser de cobre o de grafito) sumergidos en una disolución acuosa de CuSO 4 y conectados a una fuente de alimentación que suministra corriente continua. Como se puede observar en el esquema el cobre se deposita en el electrodo negativo o cátodo en forma de una masa color marrón oscuro. Se deposita el cobre y no se desprende hidrógeno (que sería una reacción de competencia) debido a que el potencial de reducción del cobre es mucho mayor que en del hidrógeno (ver tabla de potenciales estándar de reducción) En el ánodo se observa el desprendimiento de una gas: oxígeno, ya que el ión SO 4 - no se descarga al estar el azufre en su estado de oxidación más elevado y, en consecuencia, se produce la oxidación del agua a oxígeno gas. Las reacciones correspondientes para ambos electrodos son (como información adicional se dan los potenciales correspondientes leídos en la tabla, aunque no se dan en el enunciado): H O O (g) + 4 H (ac) + 4 e E = 1,3 V + Oxid Cu (ac) + e Cu(s) E =,34 V + Re d Cu (ac) + H O Cu(s) + O (g) + 4 H (ac) E =,34 V + ( 1,3) V =,89 V + + Celda Teóricamente habría que suministrar un voltaje de poco menos de un voltio para que la electrolisis tuviera lugar, pero en la práctica habrá que suministrar un voltaje mayor debido a las sobretensiones derivadas del desprendimiento de oxígeno en el ánodo, y de la deposición del cobre metálico en el ánodo. Las semirreacciones de oxidación y reducción permiten hacer cálculos cuantitativos sobre la cantidad de producto depositado como consecuencia del paso de una corriente de determinada intensidad (I = q/t) si se consideran a los electrones como una sustancia más que interviene en la reacción y se conoce que la carga de 1 mol de electrones es de C (aproximadamente 96 5 C). Esta cantidad recibe el nombre de constante de Faraday (1 Faraday) Ejemplo (Oviedo. 1-13) El calcio metálico puede obtenerse por electrolisis del CaCl fundido. a) Escriba las reacciones que tienen lugar en el ánodo y en el cátodo de la célula electrolítica. b) Si el rendimiento de la célula electrolítica es del 68 %, calcule la masa, en gramos, de Ca(s) y el volumen, el litros, de Cl (g), medido en condiciones normales, que se obtendrán en el proceso cuando se aplique una corriente de 7,5 1 3 A durante 48 h. Solución: DATOS: Ca: 4, u; 1 Faraday= C. R =,8 atmlmol -1 K -1 El CaCl fundido da iones Cl - y Ca +. Por tanto a la hora de electrolizar la masa fundida los iones Ca irán hacia el polo negativo o cátodo y los iones Cl - hacia el electrodo positivo o ánodo, y allí tendrán lugar las correspondientes reacciones de oxidación y reducción: 4
5 Química º Bachillerato. IES La Magdalena. Avilés. Asturias Cl (l) Cl (g) + e Oxidación. Ánodo + + Ca (l) e Ca(s) Re ducción. Cátodo + Cl (l) + Ca (l) Cl (g) + Ca(s) A la vista de la reacción de oxidación podemos concluir que para obtener un mol de cloro gas se necesitan moles de electrones. Los mismos que para obtener un mol de calcio metálico. Como los electrones son transportados por la corriente eléctrica que circula a través de la cuba, conocida la intensidad y el tiempo podemos calcular la carga transportada, los moles de electrones que han circulado y a partir de ahí la cantidad de calcio y cloro producido: Cantidad de cloro obtenido: Cantidad de calcio obtenido: Ejemplo 3 (Oviedo. 11-1) Se desea realizar una electrolisis de 55 ml de una disolución acuosa,196 M de AgNO 3. Para ello se dispone de electrodos de Pt(s), así como del resto del material necesario para realizar la electrolisis. a) Dibuje un esquema de la célula electrolítica utilizada en la electrolisis. Indique el signo del ánodo y del cátodo y el flujo de electrones durante la electrolisis. indicando el material de laboratorio utilizado b) Si la electrolisis se realiza utilizando una corriente eléctrica de 1,84 A durante 1 min, calcule la [Ag + ] en la disolución final. Solución: q I = ; q = I t = 7,5 1 t 9 1,96 1 C DATOS: Constante de Faraday= C a) En la figura se detalla la célula electrolítica utilizada. En el ánodo (electrodo positivo) el agua se oxida a oxígeno, ya que el ión nitrato (NO 3 - ) no se oxida (el nitrógeno está en su estado de oxidación más alto). En el cátodo (polo negativo) el ion Ag + se reduce a plata metálica. Los electrones van del polo positivo al negativo (sentido contrario al que de forma convencional se asigna a la corriente eléctrica). La fuente de alimentación suministra el voltaje necesario para que se produzca la electrolisis. Las semirreacciones que tienen lugar, y la reacción global, son las siguientes: 3 1 mol e C C s 5 1,78 1 s 1 mol Cl mol e =,4 L Cl 1 mol Cl 68 L Cl reales L Cl (teóricos) 1 L Cl teóricos 9 1,96 1 C 1 mol e C 1 mol Ca 4, g Ca mol e 1 mol Ca 9 1,96 1 C = L Cl (teóricos) = 1 99 L Cl reales = g Ca (teóricos) 68 g Ca reales g Ca (teóricos) = g Ca reales 1 g Ca teóricos 5
6 Química º Bachillerato. IES La Magdalena. Avilés. Asturias + H O O (g) + 4 H (ac) + 4 e Oxidación. Ánodo + Ag (ac) + e Ag (s) Re ducción. Cátodo 4 Ag (ac) + H O 4 Ag (s) + O (g) + 4 H (ac) + + b) Sabiendo la intensidad de corriente utilizada y el tiempo empleado podemos calcular la carga y, a partir de ahí los moles de Ag + consumidos: q C I = ; q I t 1,84 t = = s 6 s = 114 C 1 mol e 1mol Ag 114 C C 1 mol e + =,114 moles Ag + Como inicialmente teníamos: 55 ml disol,196 moles Ag 1 ml disol + =,5 moles Ag + Quedarán en disolución tras la electrolisis:,5 moles Ag,114 moles Ag =,386 moles Ag ,386 moles Ag 1 ml disol moles Ag =, ml disol 1Ldisol L disol + Producción electrolítica del aluminio El aluminio es uno de los metales más ampliamente usados debido a sus propiedades: baja densidad, elevada conductividad térmica y eléctrica, buenas propiedades mecánicas (que pueden ser mejoradas si se añaden pequeñas cantidades de cobre, magnesio, manganeso o silicio), dúctil y maleable, bajo punto de fusión (fácil reciclado), resistencia a la corrosión (debido a que en contacto con el oxígeno del aire se forma en la superficie una fina película de Al O 3 que aisla al metal protegiéndolo). El elevado consumo de este metal ( millones de toneladas/año) ha sido posible gracias a su producción industrial mediante el proceso Hall-Hérault, descubierto en 1886 por Hérault (Francia) y Hall (EE. UU), que permite obtener aluminio con un grado de pureza superior al 99%. El proceso de obtención del aluminio empieza con e (Al O 3.H O), que es necesario purificar (proceso Bayer), ya que se encuentra contaminada con sílice (SiO ) y óxidos de otros metales (principalmente Fe, y Ti). Primero se calienta con NaOH para transformar el dióxido de silicio en silicatos solubles: SiO (s) + NaOH(ac) NaSiO 3(ac) + HO El óxido de aluminio se transforma en aluminatos solubles: AlO 3(s) + NaOH(ac) NaAlO (ac) + HO Los óxidos de hierro y titanio no reaccionan y permanecen en estado sólido pudiendo ser separados por filtración. A continuación la disolución (que contiene silicatos y aluminatos) se trata con un ácido para precipitar el hidróxido de aluminio: AlO (ac) + H O (ac) Al(OH) (s) Un vez separado por filtración, el hidróxido se transforma en óxido calentándolo: Al(OH) 3(s) AlO 3(s) + 3 HO 6
7 Química º Bachillerato. IES La Magdalena. Avilés. Asturias El proceso electrolítico (método Hall) se lleva a cabo en cubas especiales (ver figura) en las que la alúmina se disuelve en criolita (1) fundida. La posibilidad de disolver la alúmina en criolita permite realizar el proceso a temperaturas de unos 1 C, temperatura considerablemente inferior al punto de fusión de la alúmina (4 C). El cátodo está formado por variar barras de carbón que se sitúan en el fondo de la cuba y sobre ellas se deposita el aluminio, que a la temperatura del proceso es líquido (T fusal = 66 C). El ánodo está formado por barras de carbón y aquí se desprende oxígeno que se combina con el carbón de los electrodos formándose CO (g). Debido a que los ánodos se consumen es necesario reemplazarlos periódicamente. El proceso se puede esquematizar de la siguiente manera: Disolución de la alúmina: Procesos en los electrodos: 3+ AlO 3(s) Al (ac) + 3 O (ac) 3+ Al + 3 e Al Cátodo. Re ducción O + 4 e O Ánodo. Oxidación Reacción global del proceso Hall: Como resumen final a partir de cuatro toneladas de bauxita se obtienen una tonelada de aluminio: España produce el % del aluminio producido en el mundo, y la planta de Avilés el 5 % del total del aluminio producido en España. Muy interesante es la producción del llamado aluminio secundario, obtenido a partir del reciclado de los productos fabricados con aluminio (latas de refrescos). Como dato, la energía necesaria para producir un kilogramo de aluminio primario (por electrolisis) es de 14 kwh, mientras que la que se precisa para producir idéntica masa de aluminio secundario (por fusión y purificación) es de,7 kwh, lo que supone un ahorro del 95 % de energía. Ejemplo 3 (Oviedo. 11-1) 3+ 4 Al (ac) + 6 O (ac) 4 Al (l) + 3 O (g) AlO 3(criolita) + 3 C(s) 3 CO (g) + 4 Al(s) 4 t bauxita t Al O 3 1 t Al (1) La criolita es una mezcla de fluoruros de aluminio (AlF 3 ) al 4% y sodio (NaF) al 6% 7
8 Química º Bachillerato. IES La Magdalena. Avilés. Asturias El aluminio metal se obtiene industrialmente por electrolisis del óxido de aluminio (Al O 3 ) fundido, utilizando electrodos de carbono. a) Dibuje un esquema de la célula electrolítica utilizada en la electrolisis del Al O 3 fundido. Indique el signo del ánodo, el signo del cátodo y el flujo de electrones durante la electrolisis. b) Si la célula electrolítica se carga con kg de Al O 3 y se hace pasar una corriente eléctrica de 3,5 1 A durante 3 horas, calcule los gramos de aluminio que quedan en la célula después de la electrolisis. DATOS: Al: 7 u; O:16 u. 1 F= C Solución: La cuba electrolítica usada en la producción industrial del aluminio (método Hall) puede verse más arriba, y en ella la alúmina (Al O 3 ) se disuelve en criolita fundida lo que permite trabajar a unos 1 C. Una célula (de laboratorio) podría esquematizarse según se ve en la figura (el aluminio estaría líquido). En el cátodo se produce la siguiente reacción de reducción del Al 3+ : 3+ Al (ac) + 3 e Al (l) Cantidad de carga que ha pasado durante las 3 h (1 8 s) de funcionamiento: C 6 3, s = 3,78 1 C s Masa de aluminio depositado: 6 3,78 1 C Masa de aluminio presente (al inicio) en la cuba: g AlO3 1 mol e C 54 g Al 1 g Al O Luego tras la electrolisis quedarán: 1 mol Al 7 g Al = 35,6 g Al 3 mol e 1 mol Al 3 = 158,8 g Al (158,8 35,6) g Al = 76, g Al (en forma de Al 3+ ) 8
9 Química º Bachillerato. IES La Magdalena. Avilés. Asturias Producción electrolítica del cinc La cinc se obtiene a partir de concentrados de ZnS que se tuestan en hornos (a unos 1 C) para convertirlos en óxido de cinc: 3 ZnS(s) + O (g) ZnO(s) + SO (g) El sólido resultante de la tostación (llamado calcine) es una mezcla de óxido de cinc impurificado con óxidos de otros metales tales como Fe, Pb, Ca, Cu, Co, Cd... El dióxido de azufre resultante, después de purificarlo de las impurezas (mercurio en estado gaseoso entre ellas), se utiliza para obtener ácido sulfúrico: 1 V O 5 SO (g) + O (g) SO 3(g) SO (g) + H O H SO (ac) 3 4 El calcine se somete a dos lixiviaciones () sucesivas con una disolución de ácido sulfúrico obteniéndose una disolución de ZnSO 4 y residuos insolubles de otros metales, como el hierro (jarosita). La disolución de ZnSO 4 se purifica tratándola con cinc en polvo para eliminar el Cu, Cd y Co que se recuperan como subproductos. La disolución purificada se somete a electrolisis con cátodos de aluminio en los que se deposita el cinc: + Zn (ac) + e Zn(s) En el ánodo de plomo y plata (1%) se desprende oxígeno: H O O (g) + 4H (ac) + 4e + La planta que Asturiana de ZINC (AZSA) tiene en San Juan de Nieva es la mayor planta de cinc electrolítico del mundo con una producción de 511 toneladas de cinc anuales. Su producción consiste principalmente en cinc del 99,995%, aleaciones para galvanización y fundición. Además también produce ácido sulfúrico, cementos de cobre y concentrados de plomo y plata. () La lixiviación es una extracción sólido-líquido en la que un disolvente líquido disuelve uno o más componentes de un sólido pulverizado. 9
ELECTRÓLISIS. Electrólisis de sales fundidas
 El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016
 REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
ELECTROQUÍMICA. 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday.
 ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
La electrólisis permite descomponer la Alúmina en aluminio y oxígeno.
 LA OBTENCIÓN DEL ALUMINIO. La primera fase de la obtención del aluminio consiste en aislar la Alúmina (óxido de aluminio) de estos minerales. Para ello lo primero es triturar la Bauxita para obtener un
LA OBTENCIÓN DEL ALUMINIO. La primera fase de la obtención del aluminio consiste en aislar la Alúmina (óxido de aluminio) de estos minerales. Para ello lo primero es triturar la Bauxita para obtener un
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción. Ajuste de reacciones de oxidación-reducción.
 Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
PROBLEMAS QUÍMICA 2º BACHILLERATO
 PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS 1. A través de una cuba electrolítica que contiene una disolución de nitrato de cobalto (II) pasa una corriente eléctrica durante 30 minutos, depositándose
PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS 1. A través de una cuba electrolítica que contiene una disolución de nitrato de cobalto (II) pasa una corriente eléctrica durante 30 minutos, depositándose
ELECTROQUÍMICA. químicas que se producen por acción de una corriente eléctrica.
 ELECTROQUÍMICA La electroquímica estudia los cambios químicos que producen una corriente eléctrica y la generación de electricidad mediante reacciones químicas. Es por ello, que el campo de la electroquímica
ELECTROQUÍMICA La electroquímica estudia los cambios químicos que producen una corriente eléctrica y la generación de electricidad mediante reacciones químicas. Es por ello, que el campo de la electroquímica
DISOLUCIONES Y ESTEQUIOMETRÍA
 DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
ELECTROLISIS. Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción:
 ELECTROLISIS Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción: + + Zn + Cu Zn + Cu se aplica una diferencia de potencial progresivamente creciente que se oponga
ELECTROLISIS Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción: + + Zn + Cu Zn + Cu se aplica una diferencia de potencial progresivamente creciente que se oponga
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 REACCIONES DE TRANSFERENCIA DE ELECTRONES REACCIONES REDOX son aquellas en las que cambian el número de oxidación de algún elemento. En estas reacciones hay intercambio de electrones por lo que no se pueden
REACCIONES DE TRANSFERENCIA DE ELECTRONES REACCIONES REDOX son aquellas en las que cambian el número de oxidación de algún elemento. En estas reacciones hay intercambio de electrones por lo que no se pueden
JULIO 2012. FASE GENERAL QUÍMICA
 OPCIÓN A JULIO 2012. FASE GENERAL QUÍMICA 1. (2,5 puntos) A partir de los siguientes datos de energías de ruptura de enlaces (ED): Molécula Enlaces ED (kj mol -1 ) H 2 H H 436 N 2 N N 946 NH 3 N-H 389
OPCIÓN A JULIO 2012. FASE GENERAL QUÍMICA 1. (2,5 puntos) A partir de los siguientes datos de energías de ruptura de enlaces (ED): Molécula Enlaces ED (kj mol -1 ) H 2 H H 436 N 2 N N 946 NH 3 N-H 389
Metalurgia y Siderurgia
 Bloque 3. Metalurgia de los metales no férreos 3.1 Metalurgia del Aluminio María Luisa Payno Herrera Jesús Se3én Marquínez DPTO. DE CIENCIA E INGENIERÍA DEL TERRENO Y DE LOS MATERIALES Este tema se publica
Bloque 3. Metalurgia de los metales no férreos 3.1 Metalurgia del Aluminio María Luisa Payno Herrera Jesús Se3én Marquínez DPTO. DE CIENCIA E INGENIERÍA DEL TERRENO Y DE LOS MATERIALES Este tema se publica
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA
 ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
Bloque IV: Electrolisis. Prof. Dr. Mª del Carmen Clemente Jul
 Bloque IV: Electrolisis Prof. Dr. Mª del Carmen Clemente Jul ELECTROLISIS PROCESO EN EL QUE SE UTILIZA LA ENERGÍA ELÉCTRICA PARA PROVOCAR UNA REACCIÓN QUÍMICA (REDOX) NO ESPONTÁNEA ELECTROLISIS DEL NaCl
Bloque IV: Electrolisis Prof. Dr. Mª del Carmen Clemente Jul ELECTROLISIS PROCESO EN EL QUE SE UTILIZA LA ENERGÍA ELÉCTRICA PARA PROVOCAR UNA REACCIÓN QUÍMICA (REDOX) NO ESPONTÁNEA ELECTROLISIS DEL NaCl
TRABAJO PRÁCTICO N 6: ELECTRÓLISIS
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
Materiales recopilados por la Ponencia Provincial de Química para Selectividad TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
IES Real Instituto Jovellanos 1º BACHILLERATO. SERIE 17
 1.- Ajustar las siguientes reacciones: a) Propano + oxígeno === dióxido de carbono + agua b) Carbonato de sodio + ácido clorhídrico === cloruro de sodio + agua c) Tribromuro de fósforo + agua === ácido
1.- Ajustar las siguientes reacciones: a) Propano + oxígeno === dióxido de carbono + agua b) Carbonato de sodio + ácido clorhídrico === cloruro de sodio + agua c) Tribromuro de fósforo + agua === ácido
JULIO 2012. FASE ESPECÍFICA. QUÍMICA.
 JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
Completar: Un sistema material homogéneo constituido por un solo componente se llama.
 IES Menéndez Tolosa 3º ESO (Física y Química) 1 Completar: Un sistema material homogéneo constituido por un solo componente se llama. Un sistema material homogéneo formado por dos o más componentes se
IES Menéndez Tolosa 3º ESO (Física y Química) 1 Completar: Un sistema material homogéneo constituido por un solo componente se llama. Un sistema material homogéneo formado por dos o más componentes se
TEMA I: REACCIONES Y ESTEQUIOMETRIA
 TEMA I: REACCIONES Y ESTEQUIOMETRIA 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano que quedan. c) Los gramos
TEMA I: REACCIONES Y ESTEQUIOMETRIA 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano que quedan. c) Los gramos
1. La magnitud 0,0000024mm expresada en notación científica es: a) 2,4 10 6 mm b) 2,4 10 5 mm c) 24 10 5 mm d) 24 10 6 mm
 Se responderá escribiendo un aspa en el recuadro correspondiente a la respuesta correcta o a la que con carácter más general suponga la contestación cierta más completa en la HOJA DE RESPUESTAS. Se facilitan
Se responderá escribiendo un aspa en el recuadro correspondiente a la respuesta correcta o a la que con carácter más general suponga la contestación cierta más completa en la HOJA DE RESPUESTAS. Se facilitan
ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA
 VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES.
 TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
La electrólisis CONTENIDOS. Electrolitos. Iones. Carga eléctrica negativa. www.codelcoeduca.cl
 La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
Reacciones de transferencia de electrones
 Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
Reciclaje del Aluminio
 Reciclaje del Aluminio El aluminio es un metal abundante en la corteza terrestre, sin embargo no se encuentra en estado puro en la naturaleza, sino en forma de óxidos con varios grados de hidratación con
Reciclaje del Aluminio El aluminio es un metal abundante en la corteza terrestre, sin embargo no se encuentra en estado puro en la naturaleza, sino en forma de óxidos con varios grados de hidratación con
EQUILIBRIOS DE SOLUBILIDAD
 EQUILIBRIOS DE SOLUBILIDAD EJERCICIOS Y PROBLEMAS RESUELTOS PROBLEMA 1.- Una disolución saturada de tetraoxofosfato (V) de plata, contiene, 10 5 moles por litro de ion fosfato. Calcula el producto de solubilidad
EQUILIBRIOS DE SOLUBILIDAD EJERCICIOS Y PROBLEMAS RESUELTOS PROBLEMA 1.- Una disolución saturada de tetraoxofosfato (V) de plata, contiene, 10 5 moles por litro de ion fosfato. Calcula el producto de solubilidad
OPCIÓN A Pregunta A1.- Pregunta A2.-
 OPCIÓN A Pregunta A1.- Considere las cuatro configuraciones electrónicas siguientes: (A) 1s 2 2s 2 2p 7, (B) 1s 2 2s 3, (C) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5, y (D) 1s 2 2s 2 2p 6 3s 2. a) Razone cuál(es)
OPCIÓN A Pregunta A1.- Considere las cuatro configuraciones electrónicas siguientes: (A) 1s 2 2s 2 2p 7, (B) 1s 2 2s 3, (C) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5, y (D) 1s 2 2s 2 2p 6 3s 2. a) Razone cuál(es)
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRIMERA PARTE
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A ESTUDIOS UNIVERSITARIOS (LOGSE) Curso 2006-2007 MATERIA: QUÍMICA INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consta de dos partes.
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A ESTUDIOS UNIVERSITARIOS (LOGSE) Curso 2006-2007 MATERIA: QUÍMICA INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consta de dos partes.
QUÍMICA. AgNO 3 (ac) Ag + (ac) + NO 3 - (ac) (0,25 puntos) 0,1 M 0,1 M 0,1 M. (0,25 puntos)
 OPCIÓN A QUÍMICA 1. (2,5 puntos) Se analiza una muestra de 10 ml de una disolución acuosa que contiene ión cloruro, Cl -, mediante la adición de una gota (0,2 ml) de disolución acuosa de nitrato de plata,
OPCIÓN A QUÍMICA 1. (2,5 puntos) Se analiza una muestra de 10 ml de una disolución acuosa que contiene ión cloruro, Cl -, mediante la adición de una gota (0,2 ml) de disolución acuosa de nitrato de plata,
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2011/12 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2011/12 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. Calcule: a) Los moles de metano que quedan. b) Las moléculas
TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. Calcule: a) Los moles de metano que quedan. b) Las moléculas
Circuitos de corriente continua
 Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
REACCIONES DE IONES METÁLICOS
 Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
El E.O. no tiene porqué ser la carga real que tiene un átomo, aunque a veces coincide.
 EQUILIBRIOS DE OXIDACIÓN-REDUCCIÓN (REDOX) 2º BACHILLERATO QUÍMICA 1.- Estado de oxidación. 2.- Concepto de oxidación y reducción. 3.- Ajuste de ecuaciones redox por el método del ión-electrón. 3.1. Reacciones
EQUILIBRIOS DE OXIDACIÓN-REDUCCIÓN (REDOX) 2º BACHILLERATO QUÍMICA 1.- Estado de oxidación. 2.- Concepto de oxidación y reducción. 3.- Ajuste de ecuaciones redox por el método del ión-electrón. 3.1. Reacciones
TEMA 6 La reacción química
 TEMA 6 La reacción química 37. Cuando se calienta el carbonato de bario se desprende dióxido de carbono y queda un residuo de óxido de bario. Calcula: a) La cantidad de carbonato que se calentó si el dióxido
TEMA 6 La reacción química 37. Cuando se calienta el carbonato de bario se desprende dióxido de carbono y queda un residuo de óxido de bario. Calcula: a) La cantidad de carbonato que se calentó si el dióxido
6. Reacciones de precipitación
 6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
DISOLUCIÓN Y PRECIPITACIÓN DE SALES CAPITULO V. 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada
 CAPITULO V DISOLUCIÓN Y PRECIPITACIÓN DE SALES 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada El fenómeno de precipitación, así como el de disolución de precipitados
CAPITULO V DISOLUCIÓN Y PRECIPITACIÓN DE SALES 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada El fenómeno de precipitación, así como el de disolución de precipitados
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO. Modelo Curso 2010-2011
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS
 EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
Ablandamiento de agua mediante el uso de resinas de intercambio iónico.
 Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
ELECTRÓLISIS DEL AGUA FRANCISCO MORENO HUESO. 18 de noviembre de 2013
 18 de noviembre de 2013 Índice General 1 FUNDAMENTO TEÓRICO Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS 3 PROCEDIMIENTO EXPERIMENTAL
18 de noviembre de 2013 Índice General 1 FUNDAMENTO TEÓRICO Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS 3 PROCEDIMIENTO EXPERIMENTAL
ELECTROLISIS DEL AGUA POR
 ELECTROLISIS DEL AGUA POR TEORIA: La electrólisis del agua consiste en un proceso electroquímico en el cual el agua se divide en Hidrógeno y Oxígeno. La electrólisis consiste en pasar corriente eléctrica
ELECTROLISIS DEL AGUA POR TEORIA: La electrólisis del agua consiste en un proceso electroquímico en el cual el agua se divide en Hidrógeno y Oxígeno. La electrólisis consiste en pasar corriente eléctrica
LA ELECTRÓLISIS DEL AGUA
 LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
Dar a conocer la capacidad de disolución del agua frente a otras sustancias.
 MINISTERIO DE EDUCACION Actividad 1: Agua en la vida II. Laboratorio: Solubilidad del agua 1. Tema: AGUA DISOLVENTE UNIVERSAL 2. Objetivo: Dar a conocer la capacidad de disolución del agua frente a otras
MINISTERIO DE EDUCACION Actividad 1: Agua en la vida II. Laboratorio: Solubilidad del agua 1. Tema: AGUA DISOLVENTE UNIVERSAL 2. Objetivo: Dar a conocer la capacidad de disolución del agua frente a otras
Seminario de Química 2º Bachillerato LOGSE Unidad 0: Repaso Química 1º Bachillerato
 A) Composición Centesimal y Fórmulas químicas 1.- Determina la composición centesimal del Ca3(PO4)2. Datos: Masas atómicas (g/mol): Ca=40; P=31; O=16 S: Ca= 38,7%; P=20%; O=41,3% 2.- Determina la composición
A) Composición Centesimal y Fórmulas químicas 1.- Determina la composición centesimal del Ca3(PO4)2. Datos: Masas atómicas (g/mol): Ca=40; P=31; O=16 S: Ca= 38,7%; P=20%; O=41,3% 2.- Determina la composición
Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base. Disoluciones reguladoras del ph
 Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base IES La Magdalena. Avilés. Asturias Disoluciones reguladoras del ph Si añadimos una pequeña cantidad de ácido o base a agua pura, el
Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base IES La Magdalena. Avilés. Asturias Disoluciones reguladoras del ph Si añadimos una pequeña cantidad de ácido o base a agua pura, el
De cualquier manera, solo estudiaremos en esta unidad los compuestos inorgánicos.
 Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
OBTENCIÓN DE CARBONATO DE SODIO (P 5)
 OBTENCIÓN DE CARBONATO DE SODIO (P 5) Objetivos - Estudio descriptivo del carbonato de sodio y de sus usos industriales - Realización de la síntesis de carbonato de sodio y su comparación con el método
OBTENCIÓN DE CARBONATO DE SODIO (P 5) Objetivos - Estudio descriptivo del carbonato de sodio y de sus usos industriales - Realización de la síntesis de carbonato de sodio y su comparación con el método
Estequiometría PAU- Ejercicios resueltos
 Estequiometría PAU- Ejercicios resueltos 2012-Septiembre Pregunta B4. Una muestra de 15 g de calcita, que contiene un 98% en peso de carbonato de calcio puro, se hace reaccionar con ácido sulfúrico del
Estequiometría PAU- Ejercicios resueltos 2012-Septiembre Pregunta B4. Una muestra de 15 g de calcita, que contiene un 98% en peso de carbonato de calcio puro, se hace reaccionar con ácido sulfúrico del
XXIII OLIMPIADA NACIONAL DE QUÍMICA SEVILLA, 1 Y 2 DE MAYO 2010 EXAMEN DE PROBLEMAS
 EXAMEN DE PROBLEMAS PROBLEMA 1. LOS ÓXIDOS DE NITRÓGENO. IMPACTO AMBIENTAL El oxígeno y el nitrógeno se combinan formando varios compuestos químicos gaseosos que reciben el nombre genérico de "óxidos de
EXAMEN DE PROBLEMAS PROBLEMA 1. LOS ÓXIDOS DE NITRÓGENO. IMPACTO AMBIENTAL El oxígeno y el nitrógeno se combinan formando varios compuestos químicos gaseosos que reciben el nombre genérico de "óxidos de
ESTEQUIOMETRÍA. 3.- LEYES VOLUMÉTRICAS: 3.1. Ley de los volúmenes de combinación de gases o de Gay-Lussac. 3.2. Ley de Avogadro.
 ESTEQUIOMETRÍA 1.- ECUACIONES. SÍMBOLOS Y FÓRMULAS QUÍMICAS. 2.- LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS: 2.1. Ley de la conservación de la masa o de Lavoisier. 2.2. Ley de las proporciones constantes
ESTEQUIOMETRÍA 1.- ECUACIONES. SÍMBOLOS Y FÓRMULAS QUÍMICAS. 2.- LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS: 2.1. Ley de la conservación de la masa o de Lavoisier. 2.2. Ley de las proporciones constantes
PRUEBA ACCESO A CICLOS FORMATIVOS DE GRADO SUPERIOR OPCIÓN C QUÍMICA
 PRUEBA ACCESO A CICLOS FORMATIVOS DE GRADO SUPERIOR OPCIÓN C QUÍMICA DATOS DEL ASPIRANTE Apellidos: CALIFICACIÓN PRUEBA Nombre: D.N.I. o Pasaporte: Fecha de nacimiento: / / Instrucciones: Lee atentamente
PRUEBA ACCESO A CICLOS FORMATIVOS DE GRADO SUPERIOR OPCIÓN C QUÍMICA DATOS DEL ASPIRANTE Apellidos: CALIFICACIÓN PRUEBA Nombre: D.N.I. o Pasaporte: Fecha de nacimiento: / / Instrucciones: Lee atentamente
10.8. Balances de carga y materia
 10.8. Balances de carga y materia La determinación de la concentración de todas las especies en equilibrio de la disolución acuosa diluida de ácidos y bases se resume a un problema de N ecuaciones no lineales
10.8. Balances de carga y materia La determinación de la concentración de todas las especies en equilibrio de la disolución acuosa diluida de ácidos y bases se resume a un problema de N ecuaciones no lineales
Si el agua que llega a la superficie terrestre entra en contacto con minerales de caliza (carbonato de calcio) ocurre la disolución del mineral.
 COMPOSICIÓN QUÍMICA DE LAS AGUAS POTABLES Ingeniería de Tratamiento y Acondicionamiento de Aguas 2.0 INTERPRETACIÓN DE LOS ANÁLISIS DE AGUA Un análisis químico del agua nos indica que sustancias se encuentran
COMPOSICIÓN QUÍMICA DE LAS AGUAS POTABLES Ingeniería de Tratamiento y Acondicionamiento de Aguas 2.0 INTERPRETACIÓN DE LOS ANÁLISIS DE AGUA Un análisis químico del agua nos indica que sustancias se encuentran
REACCIONES DE OXIDACIÓN-REDUCCIÓN
 10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS CUESTINES DE INICIACIÓN 1. Cuáles de los siguientes procesos implican una reacción de oxidación?: a) la combustión de una hoja de papel; b) la oxidación
10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS CUESTINES DE INICIACIÓN 1. Cuáles de los siguientes procesos implican una reacción de oxidación?: a) la combustión de una hoja de papel; b) la oxidación
OPCIÓN A. moléculas 1 mol. moléculas 2 átomos. moléculas. = 0,166 10 22 moles.
 OPCIÓN A CUESTIÓN 4.- Se tienen tres depósitos cerrados A, B y C de igual olumen y que se encuentran a la misma temperatura. En ellos se introducen, respectiamente, 0 g de H (g), 7 moles de O (g) y 0 3
OPCIÓN A CUESTIÓN 4.- Se tienen tres depósitos cerrados A, B y C de igual olumen y que se encuentran a la misma temperatura. En ellos se introducen, respectiamente, 0 g de H (g), 7 moles de O (g) y 0 3
ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO
 ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO 1 Puede formarse un enlace iónico entre átomos de un mismo elemento químico? Por qué? No. El enlace químico se produce entre átomos con valores muy diferentes
ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO 1 Puede formarse un enlace iónico entre átomos de un mismo elemento químico? Por qué? No. El enlace químico se produce entre átomos con valores muy diferentes
Tema 7: Solubilidad. (Fundamentos de Química, Grado en Física) Equilibrio químico Enero Mayo, 2011 1 / 24
 Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
Física y química 1º bachillerato ESTEQUIOMETRÍA
 1.- Reacción química. Ecuación química. 2.- Tipos de reacciones. 3.- Cálculos estequiométricos. ESTEQUIOMETRÍA 1.- REACCIÓN QUÍMICA. ECUACIÓN QUÍMICA Una reacción química es cualquier proceso en el que
1.- Reacción química. Ecuación química. 2.- Tipos de reacciones. 3.- Cálculos estequiométricos. ESTEQUIOMETRÍA 1.- REACCIÓN QUÍMICA. ECUACIÓN QUÍMICA Una reacción química es cualquier proceso en el que
FÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación GAS LÍQUIDO SÓLIDO
 Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
Cómo se unen los átomos
 Nivel: 2.º Medio Subsector: Ciencias químicas Unidad temática: Los cuerpos presentan aspectos y propiedades diferentes según el tipo de átomos que los componen y según la forma en que estos se unen. Pensemos
Nivel: 2.º Medio Subsector: Ciencias químicas Unidad temática: Los cuerpos presentan aspectos y propiedades diferentes según el tipo de átomos que los componen y según la forma en que estos se unen. Pensemos
Reacciones Químicas: Estequiometría
 Una reacción química es un proceso en el que una o más sustancias se transforman en una o más sustancias nuevas Reacciones Químicas: Estequiometría Una ecuación química usa símbolos químicos para mostrar
Una reacción química es un proceso en el que una o más sustancias se transforman en una o más sustancias nuevas Reacciones Químicas: Estequiometría Una ecuación química usa símbolos químicos para mostrar
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10
 CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
KI K + + I. El K + y el I no se hidrolizan porque proceden de base y ácido muy fuertes, respectivamente. El ph de la disolución es neutro.
 1 PAU Química. Junio 2011. OPCIÓN A Pregunta 1A. Indique si las siguientes afirmaciones son verdaderas o falsas, justificando en cada caso su respuesta: a) La configuración electrónica ls 2 2s 2 2p 6 3s
1 PAU Química. Junio 2011. OPCIÓN A Pregunta 1A. Indique si las siguientes afirmaciones son verdaderas o falsas, justificando en cada caso su respuesta: a) La configuración electrónica ls 2 2s 2 2p 6 3s
CICLO CERRADO DEL MOTOR DE HIDRÓGENO
 CICLO CERRADO DEL MOTOR DE HIDRÓGENO 19 de abril 2013 Antonio Arenas Vargas Rafael González López Marta Navas Camacho Coordinado por Ángel Hernando García Colegio Colón Huelva Lise Meitner ESCUELA TÉCNICA
CICLO CERRADO DEL MOTOR DE HIDRÓGENO 19 de abril 2013 Antonio Arenas Vargas Rafael González López Marta Navas Camacho Coordinado por Ángel Hernando García Colegio Colón Huelva Lise Meitner ESCUELA TÉCNICA
10 Reacciones de oxidación-reducción
 10 Reacciones de oxidación-reducción Actividades del interior de la unidad 1. En las siguientes reacciones, señala el agente oxidante y el agente reductor: a) Mg(s) Cl 2 (aq) Mg (aq) 2 Cl (aq) b) F 2 (g)
10 Reacciones de oxidación-reducción Actividades del interior de la unidad 1. En las siguientes reacciones, señala el agente oxidante y el agente reductor: a) Mg(s) Cl 2 (aq) Mg (aq) 2 Cl (aq) b) F 2 (g)
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO
 QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS
 TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS Las celdas galvánicas (pilas) son dispositivos armados de tal forma que, usando reacciones redox espontáneas, generan energía eléctrica Ejemplo: Pila de Daniel:
TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS Las celdas galvánicas (pilas) son dispositivos armados de tal forma que, usando reacciones redox espontáneas, generan energía eléctrica Ejemplo: Pila de Daniel:
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2013 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 013 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción B Reserva 3, Ejercicio 6,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 013 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción B Reserva 3, Ejercicio 6,
UTN-FRRo CATEDRA DE PROCESOS INDUSTRIALES PAG. 1
 UTN-FRRo CATEDRA DE PROCESOS INDUSTRIALES PAG. 1 COQUIZACIÓN RETARDADA Objetivos: el procedimiento de coquización retardada se desarrolló para obtener por craqueo térmico (es decir, sin utilización de
UTN-FRRo CATEDRA DE PROCESOS INDUSTRIALES PAG. 1 COQUIZACIÓN RETARDADA Objetivos: el procedimiento de coquización retardada se desarrolló para obtener por craqueo térmico (es decir, sin utilización de
PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS
 PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS 1. A través de una cuba electrolítica que contiene una disolución de nitrato de cobalto (II) pasa una corriente eléctrica durante 30 minutos, depositándose
PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS 1. A través de una cuba electrolítica que contiene una disolución de nitrato de cobalto (II) pasa una corriente eléctrica durante 30 minutos, depositándose
Generadores de cloro por electrólisis de salmuera con tecnología de célula con membrana
 Generadores de cloro por electrólisis de salmuera con tecnología de célula con membrana Jorge Marcó Gratacós director general de Aquatracta 1. Introducción Para el tratamiento y desinfección del agua de
Generadores de cloro por electrólisis de salmuera con tecnología de célula con membrana Jorge Marcó Gratacós director general de Aquatracta 1. Introducción Para el tratamiento y desinfección del agua de
BATERIA AUTOMOTRIZ. HECTOR CISTERNA MARTINEZ Profesor Técnico. Duoc UC, Ingenería Mecánica Automotriz y Autotrónica 16/11/2006
 BATERIA AUTOMOTRIZ HECTOR CISTERNA MARTINEZ Profesor Técnico 1 Introducción La batería es un acumulador de energía que cuando se le alimenta de corriente continua, transforma energía eléctrica en energía
BATERIA AUTOMOTRIZ HECTOR CISTERNA MARTINEZ Profesor Técnico 1 Introducción La batería es un acumulador de energía que cuando se le alimenta de corriente continua, transforma energía eléctrica en energía
PARTE ESPECIFICA-OPCIÓN C MATERIA: QUÍMICA
 CALIFICACIÓN: Consejería de Educación, Cultura y Deportes. PRUEBAS DE ACCESO A CICLOS FORMATIVOS DE GRADO SUPERIOR DE FORMACIÓN PROFESIONAL JUNIO 2012 Resolución de 27 de abril de 2012 (DOCM de 30 de abril)
CALIFICACIÓN: Consejería de Educación, Cultura y Deportes. PRUEBAS DE ACCESO A CICLOS FORMATIVOS DE GRADO SUPERIOR DE FORMACIÓN PROFESIONAL JUNIO 2012 Resolución de 27 de abril de 2012 (DOCM de 30 de abril)
EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller
 2010 Reacciones de intercambio de Protones EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller Recopilación de ejercicios preguntados en exámenes de cursos anteriores Mª Teresa Gómez Ruiz IES Politécnico Cartagena.
2010 Reacciones de intercambio de Protones EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller Recopilación de ejercicios preguntados en exámenes de cursos anteriores Mª Teresa Gómez Ruiz IES Politécnico Cartagena.
OXIDACIÓN-REDUCCIÓN. PAU-tipos de problemas
 OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
TEMA 3 GENERADORES DE CORRIENTE CONTINUA
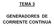 TEMA 3 GENERADORES DE CORRIENTE CONTINUA En todo circuito eléctrico es necesaria una fuente de energía que sea capaz de poner en movimiento a los electrones, a la cual llamamos generador. Si existen dos
TEMA 3 GENERADORES DE CORRIENTE CONTINUA En todo circuito eléctrico es necesaria una fuente de energía que sea capaz de poner en movimiento a los electrones, a la cual llamamos generador. Si existen dos
LA MATERIA Materia sustancias. Propiedades Propiedades generales. Propiedades características. Densidad
 LA MATERIA La materia son todos los sólidos, líquidos, gases que nos rodean (los árboles, los perros, el agua, una mesa de madera, aire, las personas, una silla de hierro, el refresco de una botella, las
LA MATERIA La materia son todos los sólidos, líquidos, gases que nos rodean (los árboles, los perros, el agua, una mesa de madera, aire, las personas, una silla de hierro, el refresco de una botella, las
Primer nombre Segundo nombre Primer apellido Segundo apellido
 ESCUELA SUPERIOR POLITECNICA DEL LITORAL INSTITUTO DE CIENCIAS QUIMICAS Y AMBIENTALES EXAMEN DE UBICACIÓN DE QUÍMICA PARA INGENIERIAS Primer Examen - Versión 0 Diciembre 2009 Primer nombre Segundo nombre
ESCUELA SUPERIOR POLITECNICA DEL LITORAL INSTITUTO DE CIENCIAS QUIMICAS Y AMBIENTALES EXAMEN DE UBICACIÓN DE QUÍMICA PARA INGENIERIAS Primer Examen - Versión 0 Diciembre 2009 Primer nombre Segundo nombre
Reacciones de oxido reducción
 Reacciones de oxido reducción Oxidación pérdida de electrones Reducción ganancia de electrones Las reacciones de oxido reducción tienen lugar mediante intercambio de electrones Ej.: Zn(s) + 2 H + (ac)
Reacciones de oxido reducción Oxidación pérdida de electrones Reducción ganancia de electrones Las reacciones de oxido reducción tienen lugar mediante intercambio de electrones Ej.: Zn(s) + 2 H + (ac)
REACCIONES DE PRECIPITACIÓN
 TEMA 12 REACCIONES DE PRECIPITACIÓN Las reacciones de disolución/precipitación en las que un sólido pasa a la disolución o viceversa afectan profundamente la ecología de ríos, lagos y océanos ya que controlan
TEMA 12 REACCIONES DE PRECIPITACIÓN Las reacciones de disolución/precipitación en las que un sólido pasa a la disolución o viceversa afectan profundamente la ecología de ríos, lagos y océanos ya que controlan
Los refractarios están compuestos principalmente de óxidos o compuestos como carburo de silicio que son estables a temperaturas elevadas.
 ASTM: define a los refractarios como materiales, generalmente no metálicos, utilizados para permanecer a altas temperaturas que proporcionan el revestimiento de hornos y reactores de alta temperatura.
ASTM: define a los refractarios como materiales, generalmente no metálicos, utilizados para permanecer a altas temperaturas que proporcionan el revestimiento de hornos y reactores de alta temperatura.
Ejercicios de acceso a la Universidad Problemas de Electroquímica
 Ejercicios de acceso a la Universidad Problemas de Electroquímica 57 Dada la reacción en la que el ión permanganato [tetraoxomanganato(vii)] oxida, en medio ácido, al dióxido de azufre, obteniéndose ión
Ejercicios de acceso a la Universidad Problemas de Electroquímica 57 Dada la reacción en la que el ión permanganato [tetraoxomanganato(vii)] oxida, en medio ácido, al dióxido de azufre, obteniéndose ión
1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %.
 Problemas 1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %. (septiembre 95) 2. Cuál es la concentración molar de una disolución de ácido
Problemas 1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %. (septiembre 95) 2. Cuál es la concentración molar de una disolución de ácido
Ca 2+ + 2OH - + CO 2 CaCO 3 + H 2 O
 DUREZA DEL AGUA Un agua dura requiere de grandes cantidades de jabón para producir espuma. La dureza de las aguas naturales es producida sobre todo por las sales de calcio y magnesio. La dureza corresponde
DUREZA DEL AGUA Un agua dura requiere de grandes cantidades de jabón para producir espuma. La dureza de las aguas naturales es producida sobre todo por las sales de calcio y magnesio. La dureza corresponde
TRANSFORMACIONES QUÍMICAS. ESTEQUIOMETRÍA.
 Tema 3 Estequiometría 1 TEMA 3. TRANSFORMACIONES QUÍMICAS. ESTEQUIOMETRÍA. 2. LAS REACCIONES QUÍMICAS. 1.- Señala justificándolas, las respuestas correctas: Se produce un cambio químico: a) Cuando las
Tema 3 Estequiometría 1 TEMA 3. TRANSFORMACIONES QUÍMICAS. ESTEQUIOMETRÍA. 2. LAS REACCIONES QUÍMICAS. 1.- Señala justificándolas, las respuestas correctas: Se produce un cambio químico: a) Cuando las
Tabla 4.1. Reglas de solubilidad para compuestos iónicos a 25ºC
 La disolución y la precipitación de compuestos son fenómenos que se presentan corrientemente en la naturaleza. Por ejemplo la preparación de muchos productos químicos industriales, como el Na 2 CO 3, está
La disolución y la precipitación de compuestos son fenómenos que se presentan corrientemente en la naturaleza. Por ejemplo la preparación de muchos productos químicos industriales, como el Na 2 CO 3, está
Resultado: a) K ps = 6,81 10 11 M 4 ; b) No hay precipitado.
 PRUEBA GENERAL OPCIÓN A PROBLEMA.- La solubilidad del Cr(OH) 3 es 0,13 mg ml 1 : a) Determina la constante de solubilidad K ps del hidróxido de cromo (III). b) Se tiene una disolución de CrCl 3 de concentración
PRUEBA GENERAL OPCIÓN A PROBLEMA.- La solubilidad del Cr(OH) 3 es 0,13 mg ml 1 : a) Determina la constante de solubilidad K ps del hidróxido de cromo (III). b) Se tiene una disolución de CrCl 3 de concentración
Taller de Balances de Masa y Energía Ingeniería de Minas y Metalurgia Pirometalurgia
 Taller de Balances de Masa y Energía Ingeniería de Minas y Metalurgia Pirometalurgia 1. Un mineral cuya composición es 55,0% FeCuS2, 30,0% FeS2 Y 15,0% de ganga, se trata por tostación a muerte ( combustión
Taller de Balances de Masa y Energía Ingeniería de Minas y Metalurgia Pirometalurgia 1. Un mineral cuya composición es 55,0% FeCuS2, 30,0% FeS2 Y 15,0% de ganga, se trata por tostación a muerte ( combustión
Trihidróxido de niquel
 HIDRÓXIDOS Los hidróxidos, aunque son combinaciones ternarias (tres elementos), se formulan y nombran como si fueran combinaciones binarias del ión (OH) - (que funciona como un no metal monovalente) con
HIDRÓXIDOS Los hidróxidos, aunque son combinaciones ternarias (tres elementos), se formulan y nombran como si fueran combinaciones binarias del ión (OH) - (que funciona como un no metal monovalente) con
TECNOLOGÍA. Tema 1. Materiales metálicos.
 TECNOLOGÍA Tema 1. Materiales metálicos. 1. LOS METALES. Debido a que es un material que se puede encontrar como tal en la naturaleza (solo unos pocos) o que son fáciles de obtener a partir del mineral
TECNOLOGÍA Tema 1. Materiales metálicos. 1. LOS METALES. Debido a que es un material que se puede encontrar como tal en la naturaleza (solo unos pocos) o que son fáciles de obtener a partir del mineral
UNIDAD III. METODOS CULOMBIMETRICOS, VOLTAMETRIA Y TRATAMIENTOS ESTADISTICOS
 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD ESCUELA DE CIENCIAS BÁSICAS, TECNOLOGÍA E INGENIERÍA 401538 Modulo Electroquímica UNIDAD III. METODOS CULOMBIMETRICOS, VOLTAMETRIA Y TRATAMIENTOS ESTADISTICOS
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD ESCUELA DE CIENCIAS BÁSICAS, TECNOLOGÍA E INGENIERÍA 401538 Modulo Electroquímica UNIDAD III. METODOS CULOMBIMETRICOS, VOLTAMETRIA Y TRATAMIENTOS ESTADISTICOS
Solubilidad. y se representa por.
 Solubilidad Solubilidad. La solubilidad mide la cantidad máxima de soluto capaz de disolverse en una cantidad definida de disolvente, a una temperatura determinada, y formar un sistema estable que se denomina
Solubilidad Solubilidad. La solubilidad mide la cantidad máxima de soluto capaz de disolverse en una cantidad definida de disolvente, a una temperatura determinada, y formar un sistema estable que se denomina
1) Agrupar las siguientes propiedades según sean extensivas o intensivas:
 Sistemas Materiales Guía de Ejercitación 1) Agrupar las siguientes propiedades según sean extensivas o intensivas: a) Volumen b) Densidad c) Olor d) Pto. de fusión e) Presión f) Sabor g) Pto. de ebullición
Sistemas Materiales Guía de Ejercitación 1) Agrupar las siguientes propiedades según sean extensivas o intensivas: a) Volumen b) Densidad c) Olor d) Pto. de fusión e) Presión f) Sabor g) Pto. de ebullición
Instalaciones de tratamiento de agua de alimentación de caldera
 Instalaciones de tratamiento de agua de alimentación de caldera Introducción La calidad del agua de alimentación a la caldera repercute directamente sobre el buen funcionamiento de la misma así como sobre
Instalaciones de tratamiento de agua de alimentación de caldera Introducción La calidad del agua de alimentación a la caldera repercute directamente sobre el buen funcionamiento de la misma así como sobre
