CORROSIÓN CORROSIÓN: DEFINICIÓN & EJEMPLOS
|
|
|
- Isabel Felisa Espinoza Aranda
- hace 8 años
- Vistas:
Transcripción
1 CORROSIÓN 1 CORROSIÓN: DEFINICIÓN & EJEMPLOS - Corrosión es el ataque destructivo de un metal por reacción química o electroquímica con su medio ambiente - Es la transformación indeseable de un material como consecuencia del medio que lo rodea Ejemplos cotidianos de corrosión: - Las cañerías de agua - El automóvil - El lavarropas - La corrosión de envases metálicos para conservas Agentes agresivos, producen la corrosión: - La atmósfera - El agua de mar - El aire húmedo - Los vapores ácidos La corrosión: un problema económico y de seguridad Se extiende a todos los materiales; pero solamente se tendrá en cuenta la corrosión metálica. Por lo tanto estudiaremos la velocidad con que se deterioran los metales y las formas en que dicha velocidad puede ser controlada. 2
2 CLASIFICACIÓN DE LOS PROCESOS DE CORROSION SEGUN LA FORMA UNIFORME Disolución uniforme de la superficie LOCALIZADA Por placas, Por grietas, Por picado, Intergranular, Fisurante SEGUN EL MEDIO QUIMICA En no electrolitos En interfases metal/gas ELECTROQUÍMICA Existe un medio conductor: a) en atmósfera. b) en suelos c) en soluciones electrolíticas d) en medios iónicos fundidos e) en medios contaminados por microorganismos. 3 CORROSIÓN SEGÚN LA FORMA Factores que favorecen la corrosión * Esfuerzo * Erosión * Cavitación * Frotamiento * Disolución selectiva * Celdas galvánicas * Celdas de concentración (aireación diferencial, diferencias de ph) * Presencia de microorganismos * Daño por hidrógeno Características de la corrosión uniforme * Microestructura homogénea y ambiente de composición uniforme. * Toda la superficie se corroe a igual velocidad y podemos predecir la pérdida de material en un cierto tiempo (g.cm -2.año -1 o mm.año -1 ) con las leyes de Faraday. w jatm nf w = masa del metal corroído (g); j = densidad de corriente (amp/cm 2 ) t = tiempo (segundos); A = área del material que se corroe (cm 2 ) M = masa del átomo gramo del metal (g/mol) n = nº de electrones/átomo producido o consumido en el proceso F = Constante de Faraday (96500 coulombs/mol) 4
3 CORROSIÓN SEGÚN EL MEDIO: CORRSIÓN QUÍMICA El metal reacciona con un medio no-iónico y la oxidación se produce por transferencia directa de e - al oxidante sin formación de una micropila. Por ej. una pieza de Fe calentada al aire seco, por encima de 500ºC se oxida a apreciable velocidad formando una película con la siguiente estructura: Etapa Inicial 2 Fe + O 2 2 FeO Se han producido reacciones redox sin la intervención de iones en solución CORROSIÓN SEGÚN EL MEDIO: CORROSIÓN ELECTROQUÍMICA Implica un transporte de cargas a través de un electrolito, hay una circulación de corrientes eléctricas y se cumplen las leyes de Faraday. Estas corrientes se producen porque el material presenta zonas con diferente reactividad (centros anódicos y "catódicos ); existe un paso conductor que conecta las zonas anódica y catódica (el metal conduce los electrones) y ambos microelectrodos estan inmersos en un mismo electrolito. 5 CONDICIONES PARA LA CORROSIÓN ELECTROQUÍMICA Causas frecuentes de la circulación de cargas: * El contacto de dos materiales diferentes * Presencia de fases diferentes de una misma aleación * Diferentes grados de aireación de una pieza metálica. * Corrientes inducidas por circuitos eléctricos mal aislados * Impurezas, tensiones en el metal, etc. Estos factores hacen que en el metal existan diferentes zonas (microelectrodos) que convierten al cuerpo metálico junto con el medio agresivo en un gran conjunto de micropilas electroquímicas. REACCIONES EN LA CORROSIÓN ELECTROQUÍMICA Reacciones anódicas: Pasaje de iones de la red metálica al medio corrosivo. Reacciones catódicas: Dependiendo de la presión de O 2 y del ph se puede observar reducción de oxígeno y/o desprendimiento de hidrógeno. Metal Metal +n + ne - Fe Fe e - Zn Zn e - O 2 + 4H + + 4e - 2H 2 O 2H + + 2e - H 2 O 2 + 2H 2 O + 4e - 4HO - 2H 2 O + 2e - H 2 + 2HO - 6
4 CORROSIÓN ELECTROQUÍMICA DE METALES Cada metal tiene una tendencia diferente frente a la corrosión por el ambiente circundante. Una reacción electroquímica es espontánea si: G < 0 E Pila = E Cat. - E Anod. > 0 Serie Electroquímica 7 Zn Fe CUPLA Fe/Zn Esta imagen muestra una placa que contiene la cupla Fe/Zn en un medio compuesto por agar-agar (similar a la gelatina) disuelto en una solución que posee una sustancia que me permite evidenciar la presencia de ión Zn ++ y fenolftaleína. Antes de comenzar la experiencia el color del agar-agar es similar al observado en el borde superior e inferior de la placa. Luego de unos días de colocar la cupla Fe/Zn se obtiene lo que observás en la figura. Puedes explicar los cambios? Porqué no se corroe el Fe? Los potenciales normales son: E 0 (Fe +2 / Fe 0 ) = V E 0 (Zn +2 / Zn 0 ) = V. Reacción catódica 2H 2 O + 2 e - H 2 + 2OH - Reacción anódica Zn 0 Zn e - La fenolftaleína toma color fucsia cuando en el medio se generan OH - Zn ++ + Compuesto de color blanco Sustancia (incolora) que permite identificar Zn ++ 3 Zn Fe(CN) -3 6 [Fe(CN) 6 ] 2 Zn 3 El ión Zn ++ se pone en evidencia al reaccionar con una sustancia que contiene el medio ( actúa como indicador del mismo) formando un compuesto de color blanco 8
5 Fe Cu CUPLA Fe/Cu Esta imagen muestra una placa que contiene la cupla Fe/Cu en un medio compuesto por agar-agar (similar a la gelatina) disuelto en una solución que posee una sustancia que me permite evidenciar la presencia de ión Fe ++ y fenolftaleína. Antes de comenzar la experiencia el color del agar-agar es similar al observado en el borde superior e inferior de la placa. Luego de unos días de colocar la cupla Fe/Cu se obtiene lo que observás en la figura. Puedes explicar los cambios? Los potenciales normales son: E 0 (Fe +2 / Fe 0 ) = V E 0 (Cu +2 /Cu 0 ) = V Ferroxil: Ferricianuro de potasio: K 3 Fe (CN) 6 Agar-agar Fenolftaleína NaOH para que el medio tenga un ph ~ 8 Reacción catódica 2H 2 O + 2 e - H 2 + 2OH - Reacción anódica Fe 0 Fe e - La fenolftaleína toma color fucsia cuando en el medio se generan OH - El ión Fe ++ se pone en evidencia al reaccionar con una sustancia que contiene el medio ( actúa como indicador del mismo) formando un compuesto de color azul Fe ++ + Sustancia (incolora) que permite identificar Fe ++ Compuesto de color azul 3 Fe Fe(CN) -3 6 [Fe(CN) 6 ] 2 Fe 3 9 Reacción del cátodo que acompaña a la oxidación del hierro Deposición metálica del cobre Desprendimiento de hidrógeno Reducción del oxígeno (solución ácida) O H e - 2 H 2 O Reducción del oxígeno (solución alcalina o neutra) O H 2 O + 4 e - 4 OH - Electrolito Contiene iones Cu +2 No contiene iones Cu +2 ni oxígeno Solución ácida con oxígeno Solución alcalina o neutra sin la presencia de iones cobre. Las celdas galvánicas pueden formarse también a nivel microscópico en metales y aleaciones por diferencias en su composición, estructura y concentración de tensiones. Observar y Completar: Identifica las zonas catódica y anódica Escribir las ecuaciones correspondientes Dar una explicación para el comportamiento CORROSIÓN EN EL CONTACTO ENTRE DOS METALES La corrosión de una tubería de hierro o acero puede acelerarse notablemente si está unida a una tubería de Cu. 10
6 color azul CORROSIÓN POR AIREACIÓN DIFERENCIAL En un tubo con agar-agar se colocó una solución con un indicador para Fe ++ y fenolftaleína y se agregó un clavo. Comparar y completar: Dónde hay mayor concentración de oxígeno? Identificar la zona catódica y la zona anódica Escribir las ecuaciones correspondientes Dar una explicación para este comportamiento CELDA DE CONCENTRACIÓN DE OXIGENO FORMACIÓN N DE HERRUMBRE Y PROTECCIÓN Esta foto muestra un clavo sumergido en agua, junto con otro que está unido a una placa de Zn. Observa con atención: Escribe las ecuaciones anódicas y catódicas en cada caso, y la formación de herrumbre Explica las diferencias observadas en cada caso Zn e - Zn (s) E o = -0,76V Fe e - Fe (s) E o =-0,44 V 11 ESPESORES DE ÓXIDO Y CRECIMIENTO (Corrosión Química) A) Capas delgadas (espesor <10-7 m). 1 ro La superficie del metal aparece limpia y brillante por cierto tiempo. 2 do Aparición de núcleos de óxido que se extienden sobre la superficie del metal. 3 ro Engrosamiento del óxido resultante de este conglomerado de núcleos B) Capas gruesas (espesor >10-7 m). * Continuas: Formación de una capa protectora. * Porosas: La corrosión se propaga en el tiempo. En 1923 Pilling y Bedworth propusieron un modo de diferenciar los metales que pueden formar capas protectoras de óxido de los que no las forman: V PB V Relación de Pilling y Bedworth o m w w o m m o w o = peso molecular del óxido w m = peso molecular del metal o = densidad del óxido m = densidad del metal. Si la relación es menor que 1 se tiene un óxido poroso, si es mayor que 1 el óxido es continuo. Aluminio Bario Cadmio Calcio Cesio Cinc Zirconio Cobalto Cobre Cromo Estaño Estroncio 1,28 0,78 1,32 0,78 0,42 1,59 1,55 2,10 1,70 3,92 1,33 0,69 Hierro Litio Magnesio Manganeso Niquel Plomo Potasio Silicio Sodio Torio Wolframio 2,06 0,60 0,84 2,07 1,68 1,31 0,51 2,04 0,32 1,36 3,30 12
7 CONTROL DE LA CORROSIÓN Selección de materiales Recubrimientos Diseño Protección anódica y catódica Control del medio Metálicos Metálicos (cinc, estaño, cobreníquel-cromo) Evitar excesos de tensiones Catódica (Corriente impresa) Temperatura No metálicos Inorgánicos (cerámicos y vidrio) Orgánicos (lacas barnices, pinturas, materiales poliméricos) Evitar contacto de distintos metales Evitar grietas Eliminar el aire Ánodos de sacrificio Anódica (corriente impresa) Oxígeno Concentración de iones Inhibidores, Biocidas, etc. 13 PROTECCIÓN DE METALES CONTRA LA CORROSIÓN Hierro Galvanizado Fe recubierto con Zn Hojalata Fe recubierto con Sn Estaño (cátodo) Hierro (ánodo) Zn : sirve como ánodo de sacrificio y protege al Fe aún cuando el recubrimiento presente algún orificio. El estaño expuesto al aire se pasiva y es estable frente a la corrosión 14
8 PROTECCIÓN CATÓDICA Consiste en suministrar electrones a la estructura protegida. Por ejemplo en el caso del acero la corrosión se detiene y la velocidad del proceso catódico aumentará. Los electrones para la protección catódica pueden provenir de: a) una fuente de corriente continua externa b) un ánodo de sacrificio, metal más susceptible a la corrosión como Mg 15 INHIBIDORES DE CORROSIÓN Son sustancias que reducen la disolución del metal ya sea actuando sobre el proceso de oxidación (inhibidores anódicos) o sobre la reacción de reducción (inhibidores catódicos). A) Inhibidores Anódicos: i) pueden formar películas con los cationes metálicos ii) pueden promover la estabilización de óxidos pasivos iii) pueden reaccionar con las sustancias potencialmente agresivas B) Inhibidores Catódicos: * Son menos eficaces pero más seguros. * Si se usan en dosis insuficientes no incrementan los riesgos de corrosión * Se utilizan polifosfatos, fosfonatos, Zn. * Son más estables, forman una película polarizante que dificulta la reacción de reducción de oxígeno. * También se utilizan compuestos orgánicos con grupos polares que tienen átomos de oxígeno, azufre, nitrógeno, con pares disponibles para formar enlaces con el metal 16
9 17
La corrosión: un problema económico y de seguridad
 CORROSIÓN CORROSIÓN: DEFINICIÓN & EJEMPLOS - Corrosión es el ataque destructivo de un metal por reacción química o electroquímica con su medio ambiente - Es la transformación indeseable de un material
CORROSIÓN CORROSIÓN: DEFINICIÓN & EJEMPLOS - Corrosión es el ataque destructivo de un metal por reacción química o electroquímica con su medio ambiente - Es la transformación indeseable de un material
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
ELECTROQUÍMICA. químicas que se producen por acción de una corriente eléctrica.
 ELECTROQUÍMICA La electroquímica estudia los cambios químicos que producen una corriente eléctrica y la generación de electricidad mediante reacciones químicas. Es por ello, que el campo de la electroquímica
ELECTROQUÍMICA La electroquímica estudia los cambios químicos que producen una corriente eléctrica y la generación de electricidad mediante reacciones químicas. Es por ello, que el campo de la electroquímica
LA ELECTRÓLISIS DEL AGUA
 LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
CORROSIÓN EN CONTACTO CON MEDIOS NATURALES
 EN CONTACTO CON MEDIOS NATURALES Índice 1.- Corrosión Atmosférica 2.- Corrosión en Agua Dulce 3.- Corrosión Marina 4.- Corrosión Mat. Enterrados 2 1.- Corrosión Atmosférica Deterioro de los materiales
EN CONTACTO CON MEDIOS NATURALES Índice 1.- Corrosión Atmosférica 2.- Corrosión en Agua Dulce 3.- Corrosión Marina 4.- Corrosión Mat. Enterrados 2 1.- Corrosión Atmosférica Deterioro de los materiales
Realizando una pequeña investigación
 Realizando una pequeña investigación 1. Introducción: Investigación realizada 1.1 Objetivo El Objetivo de esta investigación ha sido estudiar de qué factores depende la corrosión del hierro. 1.2 Hipótesis
Realizando una pequeña investigación 1. Introducción: Investigación realizada 1.1 Objetivo El Objetivo de esta investigación ha sido estudiar de qué factores depende la corrosión del hierro. 1.2 Hipótesis
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016
 REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
Capítulo V. Prueba de Corrosión
 Capítulo V Prueba de Corrosión La corrosión se puede definir como un proceso destructivo que ocasiona un deterioro en el material como resultado de un ataque químico provocado por el medio ambiente [ 9
Capítulo V Prueba de Corrosión La corrosión se puede definir como un proceso destructivo que ocasiona un deterioro en el material como resultado de un ataque químico provocado por el medio ambiente [ 9
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
RECUBRIMIENTO ELECTROLITICO
 Cómo motivar a los estudiantes mediante actividades científicas atractivas RECUBRIMIENTO ELECTROLITICO Introducción: Esther Pérez Real COLEGIO ESCLAVAS DE MARIA Valencia Los procesos de recubrimientos
Cómo motivar a los estudiantes mediante actividades científicas atractivas RECUBRIMIENTO ELECTROLITICO Introducción: Esther Pérez Real COLEGIO ESCLAVAS DE MARIA Valencia Los procesos de recubrimientos
DURABILIDAD DE LAS ESTRUCTURAS: CORROSIÓN POR CARBONATACIÓN. INFLUENCIA DEL ESPESOR Y CALIDAD DEL RECUBRIMIENTO
 DURABILIDAD DE LAS ESTRUCTURAS: CORROSIÓN POR CARBONATACIÓN. INFLUENCIA DEL ESPESOR Y CALIDAD DEL RECUBRIMIENTO Revista Cemento Año 6, Nº 25 Con frecuencia se comenta que el acero y el hormigón pueden
DURABILIDAD DE LAS ESTRUCTURAS: CORROSIÓN POR CARBONATACIÓN. INFLUENCIA DEL ESPESOR Y CALIDAD DEL RECUBRIMIENTO Revista Cemento Año 6, Nº 25 Con frecuencia se comenta que el acero y el hormigón pueden
- Temple bainítico o austempering. En aceros hipoeutectoides. Se obtiene bainita y no hace falta realizar revenido después.
 TRATAMIENTOS DEL ACERO PARA MEJORAR SUS PROPIEDADES TÉRMICOS TERMOQUÍMICOS MECÁNICOS SUPERFICIALES Recocido Normalizado Revenido escalonado bainítico Patentado Disminución gradual de la temperatura Tratamientos
TRATAMIENTOS DEL ACERO PARA MEJORAR SUS PROPIEDADES TÉRMICOS TERMOQUÍMICOS MECÁNICOS SUPERFICIALES Recocido Normalizado Revenido escalonado bainítico Patentado Disminución gradual de la temperatura Tratamientos
reactividad Abundancia (nucleogénesis) HIDRÓGENO Propiedades Propiedades iones y estructura Propiedades nucleares Aplicaciones: Síntesis
 HIDRÓGENO Atómico reactividad Molecular Propiedades iones Efectos isotópicos Propiedades nucleares RMN / IR o-h 2 y p-h 2 OM Propiedades y estructura Síntesis Laboratorio industrial Compuestos más importantes
HIDRÓGENO Atómico reactividad Molecular Propiedades iones Efectos isotópicos Propiedades nucleares RMN / IR o-h 2 y p-h 2 OM Propiedades y estructura Síntesis Laboratorio industrial Compuestos más importantes
Bloque IV: Electrolisis. Prof. Dr. Mª del Carmen Clemente Jul
 Bloque IV: Electrolisis Prof. Dr. Mª del Carmen Clemente Jul ELECTROLISIS PROCESO EN EL QUE SE UTILIZA LA ENERGÍA ELÉCTRICA PARA PROVOCAR UNA REACCIÓN QUÍMICA (REDOX) NO ESPONTÁNEA ELECTROLISIS DEL NaCl
Bloque IV: Electrolisis Prof. Dr. Mª del Carmen Clemente Jul ELECTROLISIS PROCESO EN EL QUE SE UTILIZA LA ENERGÍA ELÉCTRICA PARA PROVOCAR UNA REACCIÓN QUÍMICA (REDOX) NO ESPONTÁNEA ELECTROLISIS DEL NaCl
1El fuego y el calor. S u m a r i o. 1.1. El tetraedro del fuego. 1.2. Reacciones químicas. 1.3. Transmisión del calor
 1El fuego y el calor S u m a r i o 1.1. El tetraedro del fuego 1.2. Reacciones químicas 1.3. Transmisión del calor INVESTIGACIÓN DE INCENDIOS EN VEHÍCULOS 5 Capítulo 1 Desde el punto de vista de la investigación
1El fuego y el calor S u m a r i o 1.1. El tetraedro del fuego 1.2. Reacciones químicas 1.3. Transmisión del calor INVESTIGACIÓN DE INCENDIOS EN VEHÍCULOS 5 Capítulo 1 Desde el punto de vista de la investigación
Primer nombre Segundo nombre Primer apellido Segundo apellido
 ESCUELA SUPERIOR POLITECNICA DEL LITORAL INSTITUTO DE CIENCIAS QUIMICAS Y AMBIENTALES EXAMEN DE UBICACIÓN DE QUÍMICA PARA INGENIERIAS Primer Examen - Versión 0 Diciembre 2009 Primer nombre Segundo nombre
ESCUELA SUPERIOR POLITECNICA DEL LITORAL INSTITUTO DE CIENCIAS QUIMICAS Y AMBIENTALES EXAMEN DE UBICACIÓN DE QUÍMICA PARA INGENIERIAS Primer Examen - Versión 0 Diciembre 2009 Primer nombre Segundo nombre
RESISTENCIA A LA CORROSIÓN DE LOS ACEROS INOXIDABLES
 RESISTENCIA A LA CORROSIÓN DE LOS ACEROS INOXIDABLES La principal característica del acero inoxidable es: La resistencia a la corrosión, propiedad que le infiere el contener cuando menos 10.5% de cromo
RESISTENCIA A LA CORROSIÓN DE LOS ACEROS INOXIDABLES La principal característica del acero inoxidable es: La resistencia a la corrosión, propiedad que le infiere el contener cuando menos 10.5% de cromo
ELECTROLISIS. Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción:
 ELECTROLISIS Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción: + + Zn + Cu Zn + Cu se aplica una diferencia de potencial progresivamente creciente que se oponga
ELECTROLISIS Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción: + + Zn + Cu Zn + Cu se aplica una diferencia de potencial progresivamente creciente que se oponga
ELECTROQUÍMICA. 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday.
 ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción. Ajuste de reacciones de oxidación-reducción.
 Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
ELECTRÓLISIS. Electrólisis de sales fundidas
 El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
De qué estoy hecho? Comparando la química del cuerpo humano con la del resto de la Tierra
 De qué estoy hecho? Comparando la química del cuerpo humano con la del resto de la Tierra Introduzca los nombres y las características de las cuatro esferas que interactúan en la Tierra (esquema opuesto):
De qué estoy hecho? Comparando la química del cuerpo humano con la del resto de la Tierra Introduzca los nombres y las características de las cuatro esferas que interactúan en la Tierra (esquema opuesto):
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO. Modelo Curso 2010-2011
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA
 ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
ÍNDICE (del tema del libro) CLASIFICACIÓN DE LOS METALES NO FERROSOS. Metales pesados ESTAÑO COBRE PLOMO CINC OTROS METALES PESADOS. .
 ÍNDICE (del tema del libro) CLASIFICACIÓN DE LOS METALES NO FERROSOS Metales pesados ESTAÑO COBRE PLOMO CINC OTROS METALES PESADOS.- Cromo.- Níquel.- Wolframio.- Cobalto Metales ligeros ALUMINIO TITANIO
ÍNDICE (del tema del libro) CLASIFICACIÓN DE LOS METALES NO FERROSOS Metales pesados ESTAÑO COBRE PLOMO CINC OTROS METALES PESADOS.- Cromo.- Níquel.- Wolframio.- Cobalto Metales ligeros ALUMINIO TITANIO
Hidróxido Sódico Resumen de Seguridad GPS
 Hidróxido Sódico Resumen de Seguridad GPS Este Resumen de Seguridad del Producto está destinado a proporcionar una visión general de esta sustancia química en el marco de la Estrategia Global de Productos
Hidróxido Sódico Resumen de Seguridad GPS Este Resumen de Seguridad del Producto está destinado a proporcionar una visión general de esta sustancia química en el marco de la Estrategia Global de Productos
CONDUCTIVIDAD Y ph PRACTICA Nº 7
 CONDUCTIVIDAD Y ph PRACTICA Nº 7 OBJETO DE LA PRÁCTICA: MEDIDA DE CONDUCTIVIDAD Y MANEJO DE SUS UNIDADES RELACIÓN CONDUCTIVIDAD-SALINIDAD- Nº DE PURGAS RELACIÓN CONDUCTIVIDAD-EROSIÓN/CORROSIÓN MANEJO DEL
CONDUCTIVIDAD Y ph PRACTICA Nº 7 OBJETO DE LA PRÁCTICA: MEDIDA DE CONDUCTIVIDAD Y MANEJO DE SUS UNIDADES RELACIÓN CONDUCTIVIDAD-SALINIDAD- Nº DE PURGAS RELACIÓN CONDUCTIVIDAD-EROSIÓN/CORROSIÓN MANEJO DEL
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 REACCIONES DE TRANSFERENCIA DE ELECTRONES REACCIONES REDOX son aquellas en las que cambian el número de oxidación de algún elemento. En estas reacciones hay intercambio de electrones por lo que no se pueden
REACCIONES DE TRANSFERENCIA DE ELECTRONES REACCIONES REDOX son aquellas en las que cambian el número de oxidación de algún elemento. En estas reacciones hay intercambio de electrones por lo que no se pueden
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS
 EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
2. Escribir las reacciones de disolución de cada una de las especies siguientes en agua: a) HClO b) HC 3 H 5 O 3 c) H 2 PO 4
 OpenCourseWare Universidad Carlos III de Madrid 11/1 UNIDAD 4 PROCESOS DE EQUILIBRIO EJERCICIOS RESUELTOS 1. Calcule: a) El ph de una disolución de zumo de pomelo en la cual la [H + ] vale 5,1 3 M. b)
OpenCourseWare Universidad Carlos III de Madrid 11/1 UNIDAD 4 PROCESOS DE EQUILIBRIO EJERCICIOS RESUELTOS 1. Calcule: a) El ph de una disolución de zumo de pomelo en la cual la [H + ] vale 5,1 3 M. b)
TÉCNICAS METALOGRAFÍA - PREPARACIÓN DE PROBETAS TÉCNICA METALOGRÁFICA EXTRACCIÓN DE PROBETAS
 1 TÉCNICAS METALOGRAFÍA - PREPARACIÓN DE PROBETAS La metalografía microscópica (o micrografía de metales) estudia los productos metalúrgicos, con el auxilio del microscopio, objetivando determinar sus
1 TÉCNICAS METALOGRAFÍA - PREPARACIÓN DE PROBETAS La metalografía microscópica (o micrografía de metales) estudia los productos metalúrgicos, con el auxilio del microscopio, objetivando determinar sus
Características KOH sólido (90%) KOH solución acuosa (50%) Estado físico Sólido Liquido Color Blanco Incoloro 2.044 g/cm 3 (20 C) (sólido 1.
 Hidróxido potásico Resumen de Seguridad GPS Este Resumen de Seguridad del Producto está destinado a proporcionar una visión general de esta sustancia química en el marco de la Estrategia Global de Productos
Hidróxido potásico Resumen de Seguridad GPS Este Resumen de Seguridad del Producto está destinado a proporcionar una visión general de esta sustancia química en el marco de la Estrategia Global de Productos
UNIDAD 12 Fundamentos de corrosión y protección
 UNIDAD 1 Fundamentos de corrosión y protección 1.1 CUESTIONES DE AUTOEVALUACIÓN 1. Que ventajas presenta desde el punto de vista de la corrosión en la protección del acero un recubrimiento de Zn (galvanizado)
UNIDAD 1 Fundamentos de corrosión y protección 1.1 CUESTIONES DE AUTOEVALUACIÓN 1. Que ventajas presenta desde el punto de vista de la corrosión en la protección del acero un recubrimiento de Zn (galvanizado)
REACCIONES DE IONES METÁLICOS
 Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
TRABAJO PRÁCTICO N 6: ELECTRÓLISIS
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
Actividad: Qué es la anomalía del agua?
 Nivel: 1º Medio Subsector: Ciencias químicas Unidad temática: El agua Actividad: Seguramente ya has escuchado sobre la anomalía del agua. Sabes en qué consiste y qué es algo anómalo? Se dice que algo es
Nivel: 1º Medio Subsector: Ciencias químicas Unidad temática: El agua Actividad: Seguramente ya has escuchado sobre la anomalía del agua. Sabes en qué consiste y qué es algo anómalo? Se dice que algo es
TREN DE FILTRACIÓN DE AGUA
 TREN DE FILTRACIÓN DE AGUA Fluj 4 1 2 3 5 DESCRIPCIÓN DEL SISTEMA 1. FILTRO DE SEDIMENTOS 1 El Primer paso en el proceso de filtración de agua. El filtro de sedimentos elimina las partículas suspendidas
TREN DE FILTRACIÓN DE AGUA Fluj 4 1 2 3 5 DESCRIPCIÓN DEL SISTEMA 1. FILTRO DE SEDIMENTOS 1 El Primer paso en el proceso de filtración de agua. El filtro de sedimentos elimina las partículas suspendidas
PROBLEMAS QUÍMICA 2º BACHILLERATO
 PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS 1. A través de una cuba electrolítica que contiene una disolución de nitrato de cobalto (II) pasa una corriente eléctrica durante 30 minutos, depositándose
PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS 1. A través de una cuba electrolítica que contiene una disolución de nitrato de cobalto (II) pasa una corriente eléctrica durante 30 minutos, depositándose
CAPITULO I FUNDAMENTOS BÁSICOS SOBRE CORROSION.
 CAPITULO I FUNDAMENTOS BÁSICOS SOBRE CORROSION. I.1.- ASPECTOS GENERALES DE LA CORROSIÓN. (*1) La vida útil del equipo de la industria petrolera se acorta a menudo como un resultado de la corrosión y en
CAPITULO I FUNDAMENTOS BÁSICOS SOBRE CORROSION. I.1.- ASPECTOS GENERALES DE LA CORROSIÓN. (*1) La vida útil del equipo de la industria petrolera se acorta a menudo como un resultado de la corrosión y en
Introducción a la Química. Sistemas Materiales y Conceptos Fundamentales. Seminario de Problemas N 1
 Sistemas Materiales Introducción a la Química Seminario de Problemas N 1 1. Dibuja un esquema con los tres estados de la materia (sólido, líquido y gas) indicando el nombre de los cambios de estado. 2.
Sistemas Materiales Introducción a la Química Seminario de Problemas N 1 1. Dibuja un esquema con los tres estados de la materia (sólido, líquido y gas) indicando el nombre de los cambios de estado. 2.
El agua como disolvente
 hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
Tema 3: Materiales metálicos siderúrgicos.
 Tema 3: Materiales metálicos siderúrgicos. 1. Materiales metálicos y Aleaciones. 2. Aceros y fundiciones: el sistema hierrocarbono. 3. Tipos de aceros. 4. Tratamientos térmicos de los aceros 5. Fabricación
Tema 3: Materiales metálicos siderúrgicos. 1. Materiales metálicos y Aleaciones. 2. Aceros y fundiciones: el sistema hierrocarbono. 3. Tipos de aceros. 4. Tratamientos térmicos de los aceros 5. Fabricación
Galvanizado Continuo por Inmersión en Caliente comparado con el Galvanizado General (por Lotes) Rev. 0 Jan-07
 2. Procesos de Recubrimiento y Tratamiento de Superficies GalvInfoNote 2.3 Introducción Galvanizado Continuo por Inmersión en Caliente comparado con el Galvanizado General (por Lotes) Rev. 0 Jan-07 Hay
2. Procesos de Recubrimiento y Tratamiento de Superficies GalvInfoNote 2.3 Introducción Galvanizado Continuo por Inmersión en Caliente comparado con el Galvanizado General (por Lotes) Rev. 0 Jan-07 Hay
MANUAL TÉCNICO FILTRO DE POTENCIALES
 MANUAL TÉCNICO FILTRO DE POTENCIALES 1 Introducción a la Protección Catódica p. 2 2 Perjucios de la electrolisis p. 2 3 Filtro de Potenciales p. 4 4 Conexión del Filtro de Potenciales p. 5-1 - 1 Introducción
MANUAL TÉCNICO FILTRO DE POTENCIALES 1 Introducción a la Protección Catódica p. 2 2 Perjucios de la electrolisis p. 2 3 Filtro de Potenciales p. 4 4 Conexión del Filtro de Potenciales p. 5-1 - 1 Introducción
4.5. REACCIONES ÁCIDO-BASE.
 4.5. REACCIONES ÁCIDO-BASE. 4.5.1. ÁCIDOS, BASES Y SALES. Algunas sustancias tienen propiedades comunes y se pueden clasificar como del mismo tipo. El zumo de limón, el vinagre o la aspirina tienen un
4.5. REACCIONES ÁCIDO-BASE. 4.5.1. ÁCIDOS, BASES Y SALES. Algunas sustancias tienen propiedades comunes y se pueden clasificar como del mismo tipo. El zumo de limón, el vinagre o la aspirina tienen un
IES Real Instituto Jovellanos 1º BACHILLERATO. SERIE 17
 1.- Ajustar las siguientes reacciones: a) Propano + oxígeno === dióxido de carbono + agua b) Carbonato de sodio + ácido clorhídrico === cloruro de sodio + agua c) Tribromuro de fósforo + agua === ácido
1.- Ajustar las siguientes reacciones: a) Propano + oxígeno === dióxido de carbono + agua b) Carbonato de sodio + ácido clorhídrico === cloruro de sodio + agua c) Tribromuro de fósforo + agua === ácido
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10
 CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
Estequiometría PAU- Ejercicios resueltos
 Estequiometría PAU- Ejercicios resueltos 2012-Septiembre Pregunta B4. Una muestra de 15 g de calcita, que contiene un 98% en peso de carbonato de calcio puro, se hace reaccionar con ácido sulfúrico del
Estequiometría PAU- Ejercicios resueltos 2012-Septiembre Pregunta B4. Una muestra de 15 g de calcita, que contiene un 98% en peso de carbonato de calcio puro, se hace reaccionar con ácido sulfúrico del
FÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación GAS LÍQUIDO SÓLIDO
 Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
TEMA 2: Oxidación y corrosión
 Esquema: TEMA 2: Oxidación y corrosión TEMA 2: Oxidación y corrosión...1 1.- Introducción...1 2.- Fundamentos de los procesos de oxidación...2 3.- Corrosión y efectos de la misma...3 3.1. La pila de corrosión
Esquema: TEMA 2: Oxidación y corrosión TEMA 2: Oxidación y corrosión...1 1.- Introducción...1 2.- Fundamentos de los procesos de oxidación...2 3.- Corrosión y efectos de la misma...3 3.1. La pila de corrosión
BLOQUE I. CUÁL ES LA COMPOSICIÓN DE LOS SERES VIVOS? LAS MOLÉCULAS DE LA VIDA
 I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
EL OZONO EN FÁBRICAS DE HIELO Y HELADERAS
 EL OZONO EN FÁBRICAS DE HIELO Y HELADERAS Hielo líquido y Agua fría El hielo, producido mediante el agua, es uno de los medios más utilizados en la conservación y refresco de alimentos y/o bebidas. La
EL OZONO EN FÁBRICAS DE HIELO Y HELADERAS Hielo líquido y Agua fría El hielo, producido mediante el agua, es uno de los medios más utilizados en la conservación y refresco de alimentos y/o bebidas. La
Es un sulfato de cobre pentahidratado en polvo o cristales seco, es producido especialmente y bajo un proceso controlado por VPSA.
 1. IDENTIFICACIÓN Es un sulfato de cobre pentahidratado en polvo o cristales seco, es producido especialmente y bajo un proceso controlado por. 2. FABRICACIÓN Y ORIGEN NOMBRE: Vapor Proceso S.A. ORIGEN:
1. IDENTIFICACIÓN Es un sulfato de cobre pentahidratado en polvo o cristales seco, es producido especialmente y bajo un proceso controlado por. 2. FABRICACIÓN Y ORIGEN NOMBRE: Vapor Proceso S.A. ORIGEN:
TEMA 6 La reacción química
 TEMA 6 La reacción química 37. Cuando se calienta el carbonato de bario se desprende dióxido de carbono y queda un residuo de óxido de bario. Calcula: a) La cantidad de carbonato que se calentó si el dióxido
TEMA 6 La reacción química 37. Cuando se calienta el carbonato de bario se desprende dióxido de carbono y queda un residuo de óxido de bario. Calcula: a) La cantidad de carbonato que se calentó si el dióxido
EL GALVANIZADO EN CALIENTE EN LA INGENIERIA MECANICA Dictada por el Ing. Adriano Barboline
 EL GALVANIZADO EN CALIENTE EN LA INGENIERIA MECANICA Dictada por el Ing. Adriano Barboline Sumario: Protección del acero contra la corrosión Características, propiedades y ventajas del galvanizado en caliente
EL GALVANIZADO EN CALIENTE EN LA INGENIERIA MECANICA Dictada por el Ing. Adriano Barboline Sumario: Protección del acero contra la corrosión Características, propiedades y ventajas del galvanizado en caliente
1. La magnitud 0,0000024mm expresada en notación científica es: a) 2,4 10 6 mm b) 2,4 10 5 mm c) 24 10 5 mm d) 24 10 6 mm
 Se responderá escribiendo un aspa en el recuadro correspondiente a la respuesta correcta o a la que con carácter más general suponga la contestación cierta más completa en la HOJA DE RESPUESTAS. Se facilitan
Se responderá escribiendo un aspa en el recuadro correspondiente a la respuesta correcta o a la que con carácter más general suponga la contestación cierta más completa en la HOJA DE RESPUESTAS. Se facilitan
Lo esencial sobre el agua
 Lo esencial sobre el agua Prefacio Contenido El agua potable es el alimento más importante y la base de un buen nivel de higiene. Se utiliza en las áreas más diversas de la vida: como bebida, para preparar
Lo esencial sobre el agua Prefacio Contenido El agua potable es el alimento más importante y la base de un buen nivel de higiene. Se utiliza en las áreas más diversas de la vida: como bebida, para preparar
SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO
 Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
DISOLUCIONES Y ESTEQUIOMETRÍA
 DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
ELECTRÓLISIS DEL AGUA FRANCISCO MORENO HUESO. 18 de noviembre de 2013
 18 de noviembre de 2013 Índice General 1 FUNDAMENTO TEÓRICO Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS 3 PROCEDIMIENTO EXPERIMENTAL
18 de noviembre de 2013 Índice General 1 FUNDAMENTO TEÓRICO Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS 3 PROCEDIMIENTO EXPERIMENTAL
b) Para el último electrón del átomo de magnesio, los números cuánticos posibles son: n = 3; l = 1 ±.
 PRUEBA GENERAL OPCIÓN A CUESTIÓN 1.- Considerando el elemento alcalinotérreo del tercer período y el segundo elemento del grupo de los halógenos: a) Escribe sus configuraciones electrónicas. b) Escribe
PRUEBA GENERAL OPCIÓN A CUESTIÓN 1.- Considerando el elemento alcalinotérreo del tercer período y el segundo elemento del grupo de los halógenos: a) Escribe sus configuraciones electrónicas. b) Escribe
ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO
 ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO 1 Puede formarse un enlace iónico entre átomos de un mismo elemento químico? Por qué? No. El enlace químico se produce entre átomos con valores muy diferentes
ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO 1 Puede formarse un enlace iónico entre átomos de un mismo elemento químico? Por qué? No. El enlace químico se produce entre átomos con valores muy diferentes
1) Agrupar las siguientes propiedades según sean extensivas o intensivas:
 Sistemas Materiales Guía de Ejercitación 1) Agrupar las siguientes propiedades según sean extensivas o intensivas: a) Volumen b) Densidad c) Olor d) Pto. de fusión e) Presión f) Sabor g) Pto. de ebullición
Sistemas Materiales Guía de Ejercitación 1) Agrupar las siguientes propiedades según sean extensivas o intensivas: a) Volumen b) Densidad c) Olor d) Pto. de fusión e) Presión f) Sabor g) Pto. de ebullición
ESTEQUIOMETRÍA. 3.- LEYES VOLUMÉTRICAS: 3.1. Ley de los volúmenes de combinación de gases o de Gay-Lussac. 3.2. Ley de Avogadro.
 ESTEQUIOMETRÍA 1.- ECUACIONES. SÍMBOLOS Y FÓRMULAS QUÍMICAS. 2.- LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS: 2.1. Ley de la conservación de la masa o de Lavoisier. 2.2. Ley de las proporciones constantes
ESTEQUIOMETRÍA 1.- ECUACIONES. SÍMBOLOS Y FÓRMULAS QUÍMICAS. 2.- LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS: 2.1. Ley de la conservación de la masa o de Lavoisier. 2.2. Ley de las proporciones constantes
ALTIX S.A. Mantenimiento del Acero Inoxidable
 ALTIX S.A. Mantenimiento del Acero Inoxidable MANTENIMIENTO DEL ACERO INOXIDABLE LOS ACEROS INOXIDABLES Los aceros inoxidables son aleaciones capaces de presentar un amplio rango de resistencia a la corrosión,
ALTIX S.A. Mantenimiento del Acero Inoxidable MANTENIMIENTO DEL ACERO INOXIDABLE LOS ACEROS INOXIDABLES Los aceros inoxidables son aleaciones capaces de presentar un amplio rango de resistencia a la corrosión,
COMENTARIO DE TEXTO Los tests de alcoholemia GUÍA DE LECTURA:
 Los tests de alcoholemia Las pruebas que realiza la policía de tráfico para detectar el posible consumo de alcohol etílico (etanol, CH 3 -CH 2 OH) por parte de los conductores, y en las que éstos deben
Los tests de alcoholemia Las pruebas que realiza la policía de tráfico para detectar el posible consumo de alcohol etílico (etanol, CH 3 -CH 2 OH) por parte de los conductores, y en las que éstos deben
CROMO ELEMENTO QUIMICO MATERIALES DE INGENIERÍA MARCO ANDRÉS LÓPEZ FRANCO PRESENTADO POR: ING. OSCAR PRIETO PRESENTADO A:
 1 CROMO ELEMENTO QUIMICO MATERIALES DE INGENIERÍA MARCO ANDRÉS LÓPEZ FRANCO PRESENTADO POR: ING. OSCAR PRIETO PRESENTADO A: FUNDACION UNIVERSITARIA LOS LIBERTADORES INGENIERIA INDUSTRIAL SEMESRE I - NOCTURNO
1 CROMO ELEMENTO QUIMICO MATERIALES DE INGENIERÍA MARCO ANDRÉS LÓPEZ FRANCO PRESENTADO POR: ING. OSCAR PRIETO PRESENTADO A: FUNDACION UNIVERSITARIA LOS LIBERTADORES INGENIERIA INDUSTRIAL SEMESRE I - NOCTURNO
De cualquier manera, solo estudiaremos en esta unidad los compuestos inorgánicos.
 Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
Materiales de construcción M E T A L E S. 2ª parte
 UNIVERSIDAD DE LA REPUBLICA ORIENTAL DEL URUGUAY Facultad de Arquitectura OCTUBRE 2005 Materiales de construcción M E T A L E S 2ª parte SOLUCIONES DE UNION SOLDADURA AUTOGENA Union de las dos partes obteniendo
UNIVERSIDAD DE LA REPUBLICA ORIENTAL DEL URUGUAY Facultad de Arquitectura OCTUBRE 2005 Materiales de construcción M E T A L E S 2ª parte SOLUCIONES DE UNION SOLDADURA AUTOGENA Union de las dos partes obteniendo
Manchas de Color Oscuro en Planchas Galvannealed
 3. Corrosión Mecanismos, Prevención, y Ensayos GalvInfoNote 3.3 Manchas de Color Oscuro en Planchas Galvannealed Rev. 0 Jan-07 Introduccion Normalmente, la plancha de acero galvannealed tiene una apariencia
3. Corrosión Mecanismos, Prevención, y Ensayos GalvInfoNote 3.3 Manchas de Color Oscuro en Planchas Galvannealed Rev. 0 Jan-07 Introduccion Normalmente, la plancha de acero galvannealed tiene una apariencia
LOS METALES. Propiedades de los metales
 LOS METALES Propiedades de los metales Los metales son unos materiales de enorme interés. Se usan muchísimo en la industria, pues sus excelentes propiedades de resistencia y conductividad son de gran utilidad
LOS METALES Propiedades de los metales Los metales son unos materiales de enorme interés. Se usan muchísimo en la industria, pues sus excelentes propiedades de resistencia y conductividad son de gran utilidad
Tema 7. MOTORES ELÉCTRICOS DE CORRIENTE CONTINUA
 Tema 7. MOTORES ELÉCTRICOS DE CORRIENTE CONTINUA 1. MAGNETISMO Y ELECTRICIDAD...2 Fuerza electromotriz inducida (Ley de inducción de Faraday)...2 Fuerza electromagnética (2ª Ley de Laplace)...2 2. LAS
Tema 7. MOTORES ELÉCTRICOS DE CORRIENTE CONTINUA 1. MAGNETISMO Y ELECTRICIDAD...2 Fuerza electromotriz inducida (Ley de inducción de Faraday)...2 Fuerza electromagnética (2ª Ley de Laplace)...2 2. LAS
Tema 6 Diagramas de fase.
 Tema 6 Diagramas de fase. Los materiales en estado sólido pueden estar formados por varias fases. La combinación de estas fases define muchas de las propiedades que tendrá el material. Por esa razón, se
Tema 6 Diagramas de fase. Los materiales en estado sólido pueden estar formados por varias fases. La combinación de estas fases define muchas de las propiedades que tendrá el material. Por esa razón, se
Curso de hidrógeno y pilas de combustible. 11ª edición TEST Modulo 3
 TEST MODULO 3 1. Qué componente de las pilas de polímeros es polimérico? a) La membrana que actúa como electrolito. b) Los catalizadores que favorecen la reacción. c) Todos los que forman la MEA de 5 capas.
TEST MODULO 3 1. Qué componente de las pilas de polímeros es polimérico? a) La membrana que actúa como electrolito. b) Los catalizadores que favorecen la reacción. c) Todos los que forman la MEA de 5 capas.
OXIDACIÓN CORROSIÓN TECNOLOGÍA INDUSTRIAL II
 OXIDACIÓN CORROSIÓN TECNOLOGÍA INDUSTRIAL II OXIDACIÓN (CORROSIÓN SECA) El oxígeno acompañado de humedad, produce la CORROSIÓN. El oxígeno con el calor, produce OXIDACIÓN (corrosión seca). Como la atmósfera
OXIDACIÓN CORROSIÓN TECNOLOGÍA INDUSTRIAL II OXIDACIÓN (CORROSIÓN SECA) El oxígeno acompañado de humedad, produce la CORROSIÓN. El oxígeno con el calor, produce OXIDACIÓN (corrosión seca). Como la atmósfera
Reacciones de transferencia de electrones
 Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
Mecanismos de daño que afectan Equipos en la Industria de Refinación
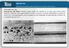 Corrosión por CO 2. Descripción del daño: Resulta cuando existe CO 2 disuelto en el agua para formar ácido carbónico (H2CO3), que puede disminuir el ph y promover corrosión generalizada o picado en aceros
Corrosión por CO 2. Descripción del daño: Resulta cuando existe CO 2 disuelto en el agua para formar ácido carbónico (H2CO3), que puede disminuir el ph y promover corrosión generalizada o picado en aceros
Medios de Transmisión
 Medios de Transmisión Se denomina medio de transmisión al soporte físico mediante el cual el emisor y el receptor establecen la comunicación. Los medios de transmisión se clasifican en guiados y no guiados.
Medios de Transmisión Se denomina medio de transmisión al soporte físico mediante el cual el emisor y el receptor establecen la comunicación. Los medios de transmisión se clasifican en guiados y no guiados.
1.- La masa atómica de la plata es de 107'9 u. Cuántos gramos pesan 0'25 mol de plata?
 Unidad 6 1.- La masa atómica de la plata es de 107'9 u. Cuántos gramos pesan 0'25 mol de plata? Como la masa atómica de la plata es de 107'9 u, la masa de 1 mol de plata es de 107'9 g (la misma cifra pero
Unidad 6 1.- La masa atómica de la plata es de 107'9 u. Cuántos gramos pesan 0'25 mol de plata? Como la masa atómica de la plata es de 107'9 u, la masa de 1 mol de plata es de 107'9 g (la misma cifra pero
a) Igualamos las unidades de los dos miembros de la ecuación:
 1 PAU Química. Junio 2010. Fase específica OPCIÓN A Cuestión 1A. Una reacción química del tipo A (g) B (g) + C (g) tiene a 25 C una constante cinética k = 5 l0 12 L mol 1 s 1. Conteste razonadamente a
1 PAU Química. Junio 2010. Fase específica OPCIÓN A Cuestión 1A. Una reacción química del tipo A (g) B (g) + C (g) tiene a 25 C una constante cinética k = 5 l0 12 L mol 1 s 1. Conteste razonadamente a
La Tecnología de los Selladores
 La Tecnología de los Selladores 1 Que son selladores? Maderas Tejidos Sustancia capaz de unir dos superficies o sustratos con el propósito de: Impermeabilizar Detener la filtración de fluidos: agua, aceites,
La Tecnología de los Selladores 1 Que son selladores? Maderas Tejidos Sustancia capaz de unir dos superficies o sustratos con el propósito de: Impermeabilizar Detener la filtración de fluidos: agua, aceites,
La microestructura se puede relacionar con:
 Metalografía Metalografía es la rama de la ciencia relativa al estudio de la constitución y estructura de los metales y aleaciones. A través de los estudios metalográficos se establece la relación que
Metalografía Metalografía es la rama de la ciencia relativa al estudio de la constitución y estructura de los metales y aleaciones. A través de los estudios metalográficos se establece la relación que
Actividad V.53 Transiciones de fases Calor latente de transformación
 Actividad V.53 Transiciones de fases Calor latente de transformación Objetivo Estudio de transiciones de fase líquido vapor y sólido líquido. Medición de los calores latentes de evaporación y de fusión
Actividad V.53 Transiciones de fases Calor latente de transformación Objetivo Estudio de transiciones de fase líquido vapor y sólido líquido. Medición de los calores latentes de evaporación y de fusión
Obtención y prueba de corazones y vigas extraídos de concreto endurecido
 el concreto en la obra editado por el instituto mexicano del cemento y del concreto, A.C. Abril 2009 Obtención y prueba de corazones y vigas extraídos de concreto endurecido Primera parte 20 Problemas,
el concreto en la obra editado por el instituto mexicano del cemento y del concreto, A.C. Abril 2009 Obtención y prueba de corazones y vigas extraídos de concreto endurecido Primera parte 20 Problemas,
LA IMPORTANCIA DEL USO DE UN BUEN REFRIGERANTE PARA AUTOMÓVILES
 LA IMPORTANCIA DEL USO DE UN BUEN REFRIGERANTE PARA AUTOMÓVILES DEPARTAMENTO TÉCNICO - VOLCKMANN S.A. Este apunte es ofrecido como una fuente de información sobre el uso del líquido refrigerante- anticongelante
LA IMPORTANCIA DEL USO DE UN BUEN REFRIGERANTE PARA AUTOMÓVILES DEPARTAMENTO TÉCNICO - VOLCKMANN S.A. Este apunte es ofrecido como una fuente de información sobre el uso del líquido refrigerante- anticongelante
EQUILIBRIO ÁCIDO-BASE
 EQUIIBRIO ÁCIDO-BASE Electrolito y no electrolito os electrolitos son sustancias (ácidos, bases y sales) que al disolverse en agua o fundidos, pueden conducir la corriente eléctrica. os electrolitos pueden
EQUIIBRIO ÁCIDO-BASE Electrolito y no electrolito os electrolitos son sustancias (ácidos, bases y sales) que al disolverse en agua o fundidos, pueden conducir la corriente eléctrica. os electrolitos pueden
FAMILIAS BÁSICAS DE ACERO INOXIDABLE:
 GENERALIDADES SOBRE ACEROS INOXIDABLES FAMILIAS BÁSICAS DE ACERO INOXIDABLE: MARTENSÍTICOS FERRÍTICOS AUSTENÍTICOS ACEROS INOXIDABLES MARTENSÍTICOS ALEACIONES HIERRO, CROMO Y CARBONO C 0.10 % Cr: 12-14
GENERALIDADES SOBRE ACEROS INOXIDABLES FAMILIAS BÁSICAS DE ACERO INOXIDABLE: MARTENSÍTICOS FERRÍTICOS AUSTENÍTICOS ACEROS INOXIDABLES MARTENSÍTICOS ALEACIONES HIERRO, CROMO Y CARBONO C 0.10 % Cr: 12-14
LOGRO: Identifica y nombra las diferentes funciones inorgánicas aplicando las reglas de la nomenclatura, común, stock y IUPAC.
 LOGRO: Identifica y nombra las diferentes funciones inorgánicas aplicando las reglas de la nomenclatura, común, stock y IUPAC. METODOLOGÍA DE TRABAJO: 1) Lea y repase la nomenclatura inorgánica. 2) Copie
LOGRO: Identifica y nombra las diferentes funciones inorgánicas aplicando las reglas de la nomenclatura, común, stock y IUPAC. METODOLOGÍA DE TRABAJO: 1) Lea y repase la nomenclatura inorgánica. 2) Copie
UNIVERSIDAD CARLOS III DE MADRID
 UNIVERSIDAD CARLOS III DE MADRID MODELO PRUEBA DE ACCESO A LA UNIVERSIDAD PARA MAYORES DE 25 AÑOS MATERIA: QUÍMICA Curso 2011-2012 INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consta de dos partes. En
UNIVERSIDAD CARLOS III DE MADRID MODELO PRUEBA DE ACCESO A LA UNIVERSIDAD PARA MAYORES DE 25 AÑOS MATERIA: QUÍMICA Curso 2011-2012 INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consta de dos partes. En
Figura Nº 4.1 (a) Circuito MOS de canal n con Carga de Deplexion (b) Disposición como Circuito Integrado CI
 Tecnología Microelectrónica Pagina 1 4- FABRICACIÓN DEL FET Describiendo el proceso secuencia de la elaboración del NMOS de acumulación y de dispositivos de deplexion, queda explicada la fabricación de
Tecnología Microelectrónica Pagina 1 4- FABRICACIÓN DEL FET Describiendo el proceso secuencia de la elaboración del NMOS de acumulación y de dispositivos de deplexion, queda explicada la fabricación de
TRABAJO PRÁCTICO N 2: TÉCNICAS DE ESTERILIZACIÓN Y CULTIVO DE MICROORGANISMOS Objetivos:
 TRABAJO PRÁCTICO N 2: TÉCNICAS DE ESTERILIZACIÓN Y CULTIVO DE MICROORGANISMOS Objetivos: -Conocer las metodologías actuales de control y eliminación de microorganismos. -Obtener dominio de los métodos
TRABAJO PRÁCTICO N 2: TÉCNICAS DE ESTERILIZACIÓN Y CULTIVO DE MICROORGANISMOS Objetivos: -Conocer las metodologías actuales de control y eliminación de microorganismos. -Obtener dominio de los métodos
ELECTRODOS ESPECIALES Y PLACAS. Electrodo de Grafito Rígido ELECTRODOS DE GRAFITO RIGIDO
 ELECTRODOS ESPECIALES Y PLACAS Electrodo de Grafito Rígido ELECTRODOS DE GRAFITO RIGIDO Nuestro Proveedor, ha diseñado nuevos electrodos fabricados a partir de grafito para ser utilizados en sistemas de
ELECTRODOS ESPECIALES Y PLACAS Electrodo de Grafito Rígido ELECTRODOS DE GRAFITO RIGIDO Nuestro Proveedor, ha diseñado nuevos electrodos fabricados a partir de grafito para ser utilizados en sistemas de
PROCESOS ENERGÉTICOS
 PROCESOS ENERGÉTICOS Tubería de salida del vapor vapor Nivel del agua Tubos de humo TUBO DE FUEGO Lodos Purga Tubería de entrada de agua de alimentación CIRCULACIÓN DE AGUA EN UNA CALDERA DE TUBOS DE
PROCESOS ENERGÉTICOS Tubería de salida del vapor vapor Nivel del agua Tubos de humo TUBO DE FUEGO Lodos Purga Tubería de entrada de agua de alimentación CIRCULACIÓN DE AGUA EN UNA CALDERA DE TUBOS DE
El futuro de la Galvanización:
 El futuro de la Galvanización: Innovando en busca de la competitividad Agenda 1. 2. 3. 4. 5. 6. 7. Votorantim Metais; Evolución del proceso de galvanización; Utilización de aleaciones en la tina de zinc;
El futuro de la Galvanización: Innovando en busca de la competitividad Agenda 1. 2. 3. 4. 5. 6. 7. Votorantim Metais; Evolución del proceso de galvanización; Utilización de aleaciones en la tina de zinc;
ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA
 VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
Manual de instrucciones Regulador de presión PR500 Watts Industries
 Manual de instrucciones Regulador de presión PR500 Watts Industries 1 Funcionamiento: El regulador de presión PR500 se controla mediante un piloto de control regulador de presión graduable, provisto de
Manual de instrucciones Regulador de presión PR500 Watts Industries 1 Funcionamiento: El regulador de presión PR500 se controla mediante un piloto de control regulador de presión graduable, provisto de
1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %.
 Problemas 1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %. (septiembre 95) 2. Cuál es la concentración molar de una disolución de ácido
Problemas 1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %. (septiembre 95) 2. Cuál es la concentración molar de una disolución de ácido
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva, Ejercicio 2, Opción A Reserva, Ejercicio, Opción B
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva, Ejercicio 2, Opción A Reserva, Ejercicio, Opción B
Química, desarrollo histórico y relación con otras ciencias
 Química, desarrollo histórico y relación con otras ciencias La definición de química hace una división entre la época antigua y la moderna; en la primera los procesos químicos eran realizados por artesanos
Química, desarrollo histórico y relación con otras ciencias La definición de química hace una división entre la época antigua y la moderna; en la primera los procesos químicos eran realizados por artesanos
TEMA 3. PROPIEDADES QUÍMICAS DEL SUELO. Los elementos químicos en el suelo Capacidad de intercambio catiónico El ph suelo Conductividad eléctrica
 TEMA 3. PROPIEDADES QUÍMICAS DEL SUELO Los elementos químicos en el suelo Capacidad de intercambio catiónico El ph suelo Conductividad eléctrica 1. Los elementos químicos en el suelo. 1.1. Situación de
TEMA 3. PROPIEDADES QUÍMICAS DEL SUELO Los elementos químicos en el suelo Capacidad de intercambio catiónico El ph suelo Conductividad eléctrica 1. Los elementos químicos en el suelo. 1.1. Situación de
