EQUILIBRIO QUIMICO. Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico
|
|
|
- Josefina Claudia Alarcón Herrero
- hace 7 años
- Vistas:
Transcripción
1 Química General e Inorgánica Licenciatura en Ciencias Biológicas rofesorado en Biología Analista Biológico EQUILIBRIO QUIMICO En general las reacciones químicas no se completan, es decir que no siempre la totalidad de los reactantes se convierten en productos, sino que se llega a un estado final de equilibrio, el cual es un equilibrio dinámico (las reacciones se siguen produciendo entre los reactantes que permanecen sin reaccionar y los productos de la reacción. Estas reacciones se denominan reacciones reversibles; en sistemas cerrados, todas las reacciones son reversibles. Sin embargo por ejemplo en el caso de sistemas abiertos: CaCO 3 (s CaO(s + CO (g en este sistemas abierto se desprende CO como gas, llega un momento en que se agota el CaCO 3, en ese caso se completa la reacción ya que uno de los productos es eliminado del medio de reacción; en ese caso se coloca una flecha en el sentido de los productos. Sin embargo, si la misma reacción la hacemos en un recipiente cerrado el dióxido de carbono queda en el medio y ejerce una presión sobre el sólido, esto hace que la reacción comience a transcurrir en sentido contrario hasta que se alcanza un estado final de equilibrio CaCO 3 (s = CaO(s + CO (g (sistema cerrado (El signo igual indicado (= puede además estar representado por dos flechas, una en un sentido ( y la otra en sentido contrario (, una sobre la otra. Este criterio se mantendrá en todo el texto. Se debe distinguir y poder diferenciar la reversibilidad de una reacción química; de lo considerado como proceso termodinámico cíclico, proceso termodinámico reversible o proceso termodinámico irreversible donde se esta considerando distintos caminos de cambio de estado de un sistema termodinámico. Todo estudio de equilibrio químico se realiza en sistemas cerrados donde tendremos reacciones químicas reversibles. El tratamiento del equilibrio químico se hace mediante consideraciones termodinámicas; que es el tratamiento estricto del equilibrio químico. Este tratamiento puede ser aplicado a sistemas homogéneos en el cual todos los integrantes de la reacción se encuentran en la misma fase, por ejemplo: todos gases o todos líquidos. También puede ser en un sistema heterogéneo cuando algunos reactantes o productos se encuentran en distintas fases, por ejemplo sólidos y gases, líquidos y gases. SO (g + ½ O (g = SO 3 (g homogéneo CaCO 3 (s = CaO(s + CO (g heterogéneo Tratamiento termodinámico
2 De manera empírica, se observa que las condiciones de equilibrio para un proceso químico dependen únicamente de la estequiometría y no de el mecanismo por el cual se verifica el proceso. Mediante el uso de la energía de gibbs, deduciremos la expresión correspondiente al equilibrio químico. La energía de gibbs de formación de un mol de gas en una mezcla de gases ideales es: G A = G A + R T ln A donde A es la presión parcial del gas A en la mezcla gaseosa expresada en atmósferas. G, es la energía de gibbs estándar, es decir definida para una atmósfera de presión; de esta manera G es solamente función de la temperatura. G A depende de la presión y la temperatura. Dada la reacción: N O (g = NO (g la variación de energía de gibbs para la reacción esta dado por: ΔG = n G ( n G (R ΔG = G ( NO + R T ln (G ( NO ( N + R T ln ΔG = G ( NO G ( N + R T ln O ΔG = ΔG + R T ln (NO (N O O (NO (N O ( N O ΔG es el cambio de energía de gibbs estándar de la reacción, es una constante para la reacción, la cual depende exclusivamente de la temperatura y esta definida para una atmósfera de presión. ΔG es el cambio de energía de gibbs de la reacción para cualquier condición de presión (distinta a una atmósfera y de temperatura. A esta expresión se le denomina isoterma de van t Hoff (T=cte Del cociente entre las presiones parciales surge el valor de ΔG, el cual debe ser al comienzo negativo (proceso espontáneo y llegar a un valor de cero. Cuando ΔG = 0 el sistema está en equilibrio. 0 = ΔG + R T ln (NO (N O en el equilibrio, la relación entre las presiones parciales se mantiene constante mientras no cambie la temperatura. A esta relación entre las presiones parciales se le denomina constante termodinámica de equilibrio (NO (N O
3 0 = ΔG + R T ln Kp La constante termodinámica de equilibrio Kp, es un número que no tiene unidades, es decir es adimensional; y es función exclusiva de la temperatura ( f(t, porque ΔG es función exclusiva de la temperatura. De la ecuación anterior queda ΔG = R T ln Kp Es una expresión muy importante para la química, es un caso especial de la isoterma de Van t Hoff ya que permite determinar la constante de equilibrio para una reacción química (Kp a partir del valor de ΔG de la reacción que se obtienen de las energías de gibbs de formación estándar de los integrantes de la reacción de valores de bibliografía ΔG = n pg f, nrg f, R además conociendo Kp puedo saber la cantidad de reactantes y productos que hay en el equilibrio, esto es conocer la conversión de sustancias reaccionantes en productos de reacción, o sea el rendimiento de la reacción. En forma general para una reacción química: a. A + b. B = c. C + d. D c C. ΔG = ΔG + R T ln a. A d D b B La constante de equilibrio termodinámica se puede expresar como c C a A d D b B considerar que Kp tiene valides solamente en el equilibrio, es decir cuando ΔG = 0. Distintas expresiones de la constante de equilibrio La constante de equilibrio puede tener diferentes expresiones de acuerdo a como se exprese la cantidad de productos y reactantes. Si la cantidad de reactantes y productos se indica en función de las concentraciones molares la constante de equilibrio se expresa como Kc. 3
4 Kc = [NO [N O en forma general para una reacción química tipo: Kc = c [C.[D a [A [B d b ara gases es común trabajar con las presiones parciales de la forma ya vista, que en general: c d C D a b A B Se puede expresar en función de las fracciones molares ; donde A = n A / n t en forma general: Kx = NO NO Kx = c C a A d D b B Relación entre Kp y Kc ara la reacción química antes considerada: N O (g = NO (g podemos expresar la constante de equilibrio en función de las presiones parciales NO ara gases ideales: V = n R T NO se puede escribir como = (n/v R T sabemos que la relación (n/v es una expresión de concentración molar que se podría representar como [ = [ R T
5 que especificado para un gas A de una mezcla de gases ideales A = [A R T Aplicado para el caso de la reacción considerada = [NO NO (R T N = [N O O R T reemplazando en la expresión de Kp [NO (R T [N O R T la relación entre las concentraciones molares ya la definimos como Kc = entonces queda expresado de otra manera agrupando Kc Kc (R T (- (R T R T Kc (R T (R T - [NO [N O donde el exponente "" es el número de moles del producto de la reacción y el exponente "" es el número de moles del reactante. Lo expresamos en forma general como Δn (gas donde Kc (R T Δn(gas Δn (gas = ( Σ n p Σ n r gases Aplicando esta expresión general para la reacción química que estamos considerando Δn (gas = moles mol = mol remplazando en la expresión queda Kc (R T Kc R T que permite relacionar Kp con Kc conociendo la constante de los gases y la temperatura para la reacción química considerada. En forma general Kc (R T Δn(gas 5
6 donde Kp y Kc dependen exclusivamente de la temperatura. Relación entre Kp y Kx También podemos calcular Kx si conocemos Kp o viceversa. or la ley de Dalton de las presiones parciales que establece que la presión parcial de un gas en una mezcla de gases es igual a la presión total multiplicada por la fracción molar de ese gas. De la ley de Dalton: A = t A Aplicado a los componentes de la reacción química que estamos considerando = NO t NO O N = t N O Reemplazando en la expresión de Kp NO NO = t t NO N O Agrupando términos como hicimos anteriormente NO NO t (- La relación entre las fracciones molares es Kx; El exponente de la presión total es la diferencia entre el número de moles de los productos y los reactantes al estado gaseoso. Kx t Δn(gas Es muy importante considerar la dependencia de cada una de las constantes de equilibrio y esta dependencia se debe relacionar con las expresiones de las constantes anteriormente vistas. Kp depende de la temperatura f(t Kc depende de la temperatura Kc = f(t Kx depende de la temperatura y de la presión total Kx = f(t, porque en la expresión está Kp y también la presión total. 6
7 Equilibrio Heterogéneo El equilibrio en sistemas heterogéneo se produce cuando los integrantes de una reacción química están en distintas fases CaCO 3 (s = CaO (s + CO (g Escribiendo la constante en función de las presiones Kp CO CaCO3 CaO odemos considerar que a temperatura constante (T=cte la presión parcial de los sólidos puros, es una constante, y a su vez es muy pequeña debido a que la presión parcial que ejerce un sólido puro, no es mas que su presión de vapor, por ello en el equilibrio la presión parcial que aportan los sólidos a la fase gaseosa es despreciable; esta aproximación se hace también para el caso de líquidos debido a que su presión de vapor también es baja. De esta forma la expresión de Kp para la reacción química considerada se puede escribir como: CO La misma aproximación podemos hacer cuando consideramos las constantes de equilibrio expresadas en función de las concentraciones y las fracciones molares: Kc = [CO Kx = CO osición y desplazamiento del equilibrio Consideremos el significado de la constante de equilibrio. or ejemplo para la reacción: H (g + Cl (g = HCl (g para el equilibrio a 5ºC. Kc =, = [ HCl [ H [ Cl como el valor de la constante es grande, hay gran cantidad de productos formados en relación a los reactantes que no han reaccionado. Esto significa que la posición de equilibrio se encuentra desplazada hacia los productos por lo tanto se dice que la reacción tiene alto rendimiento. ara la reacción: N (g + O (g = NO(g para el equilibrio a 5ºC. Kc =, [ NO = [ N [ O la posición de equilibrio está desplazada hacia los reactantes, por ello es de bajo rendimiento. 7
8 rincipio de Le Chatelier-Braun Si se tiene un sistema en equilibrio y se alteran las condiciones impuestas al mismo (concentración, presión, temperatura, etc. el sistema se desplaza hacia una nueva posición de equilibrio de acuerdo a las nuevas condiciones impuestas. or ejemplo para la reacción: N O (g = NO (g Hay tres factores que pueden alterar la posición de equilibrio de una reacción química y son: Variación de la concentración de alguno de los integrantes de la reacción. A temperatura constante constante, al igual que Kc o Kx [NO Kc = [N O si agregamos mayor cantidad de reactante tendrá que aumentar la cantidad de producto para mantener el valor de Kc y la reacción se desplazara hacia los productos hasta que se vuelva a establecer el equilibrio. Si agregamos mas productos la reacción se desplazara hacia los reactantes. Variación de la presión total del sistema. Recordemos que la relación con la presión total del sistema es: NO t ; Kx t ; Kx = NO en el ejemplo planteado hay aumento de volumen, el sistema pasa de un mol a dos moles, (Δn gas = el sistema pasa de un volumen a dos volúmenes, se expande cuando se forman el producto, entonces la reacción se verá favorecida por una disminución de la presión. Es decir para esta reacción a menor presión mayor volumen. ara la reacción: N (g + 3 H (g = NH 3 (g el sistema pasa de cuatro moles a dos moles (Δn gas =, pasa de cuatro volúmenes a dos volúmenes y se favorece la formación de producto con un aumento de presión. NH 3 Kx 3 t ; ; Kx = Kp t N H t al aumentar la presión total, aumenta Kx. ara un sistema donde no hay variación de volumen: I (g + H (g = IH(g Δn gas = 0; entonces Kx la presión total no cambiará la posición del equilibrio. Kp t 8
9 La presión exterior cambiará la posición de equilibrio solamente en aquellas reacciones gaseosas donde el volumen total de reactante sea distinto al volumen total de producto. 3 Variación de la Temperatura. a- Las constantes de equilibrio vistas Kp, Kc, Kx son función de la temperatura, por ello, una variación de temperatura hará variar el valor de la constante considerada. b- Si tenemos una reacción del tipo: a.a(g + b.b(g = c.c(g; ΔH = ( exotérmica la reacción naturalmente tiende a desprender calor, por lo tanto tenemos que disminuir la temperatura para favorecerla. ara el caso de reacciones endotérmica: d.d(g + f.f(g = l.l(g; ΔH = (+ las reacciones que absorben calor, se ven favorecidas por un aumento de la temperatura. c- Como la temperatura afecta la velocidad de reacción, una disminución de la temperatura puede hacer además disminuir la velocidad de reacción, y ésto afecta su rendimiento. Efecto de la temperatura sobre Kp La variación de la constante termodinámica de equilibrio (Kp con la temperatura, lo da la ecuación de van t Hoff d ln Kp dt = RT esta expresión se denomina isobara de van t Hoff. (=cte. ara poder usarla debemos resolver los términos diferenciales (d... odemos poner la expresión como: dln RT dln R dt; donde T d T dt = d( T Integrando en forma definida. La ecuación de van t Hoff se puede integrar en forma definida para dos constantes de equilibrio Kp a una temperatura T y Kp a una temperatura T. Con estos límites y suponiendo la entalpía constante en ese ámbito de temperatura: Kp Kp d ln R T T d ( T cuya solución es 9
10 ln Kp ln Kp = ( R T T despejando y colocando el signo negativo dentro del paréntesis ln Kp = ln Kp + R ( T T Con esta expresión se puede calcular por ejemplo el valor de Kp a una temperatura distinta al conocido. Integrando en forma indefinida. ln R + constante T en esta expresión se supone que la variación de entalpía estándar (ΔH no cambia con la variación de temperatura. Se debe tomar un pequeño intervalo de temperatura para que haya muy poco cambio en la entalpía y se pueda considerar aproximadamente constante. La expresión ultima representa una recta, y es del tipo Y = a x + b. Si graficamos ln Kp vs tendremos una recta cuya pendiente es T R Donde T > T y la reacción es endotérmica ΔH (+ ara hacer la gráfica debemos tener una serie de valores de Kp cada uno de ellos correspondientes a una temperatura (T distinta. De la pendiente de la gráfica se obtiene la entalpía de la reacción, y del signo se determina si la reacción es endotérmica (+ΔH pendiente negativa (no olvidar que en la expresión matemática la pendiente tiene un signo negativo, pero la entalpía es positiva o si la reacción es exotérmica ( ΔH pendiente positiva (el signo negativo de la expresión con el signo negativo de la entalpía, se hace positivo. Se puede ver que cuando la temperatura aumenta (/T disminuye la constante (Kp aumenta; y cuando la temperatura disminuye (/T aumenta la constante también disminuye. 0
TEMA 6 EQUILIBRIO QUÍMICO
 TEMA 6 EQUILIBRIO QUÍMICO ÍNDICE 1. Equilibrio químico homogéneo y heterogéneo 2. Concentraciones en equilibrio 3. Constante de equilibrio K c 4. Constantes de equilibrio K p y K c 5. Cociente de reacción
TEMA 6 EQUILIBRIO QUÍMICO ÍNDICE 1. Equilibrio químico homogéneo y heterogéneo 2. Concentraciones en equilibrio 3. Constante de equilibrio K c 4. Constantes de equilibrio K p y K c 5. Cociente de reacción
JMLC - Chena IES Aguilar y Cano - Estepa
 Termodinámica es la parte de la física que estudia los intercambios de calor y trabajo que acompañan a los procesos fisicoquímicos. Si estos son reacciones químicas, la parte de ciencia que los estudia
Termodinámica es la parte de la física que estudia los intercambios de calor y trabajo que acompañan a los procesos fisicoquímicos. Si estos son reacciones químicas, la parte de ciencia que los estudia
Tema 3: Ecuaciones químicas y concentraciones
 Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
UD 6. Equilibrio químico
 UD 6. Equilibrio químico 1- Equilibrio químico. Constante de equilibrio. 2- Equilibrios gaseosos. 3- Factores que modifican el equilibrio. 4- Termodinámica y constante de equilibrio. 1- Equilibrio químico.
UD 6. Equilibrio químico 1- Equilibrio químico. Constante de equilibrio. 2- Equilibrios gaseosos. 3- Factores que modifican el equilibrio. 4- Termodinámica y constante de equilibrio. 1- Equilibrio químico.
UD 6. Equilibrio químico
 UD 6. Equilibrio químico 1- Equilibrio químico. Constante de equilibrio. 2- Equilibrios gaseosos. 3- Factores que modifican el equilibrio. 4- Termodinámica y constante de equilibrio. 1- Equilibrio químico.
UD 6. Equilibrio químico 1- Equilibrio químico. Constante de equilibrio. 2- Equilibrios gaseosos. 3- Factores que modifican el equilibrio. 4- Termodinámica y constante de equilibrio. 1- Equilibrio químico.
de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC;
 Entalpía a estándar de la reacción Es el incremento entálpico de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC; conc.. = 1 M).
Entalpía a estándar de la reacción Es el incremento entálpico de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC; conc.. = 1 M).
1. Dado el equilibrio de disociación del cloruro nitrosilo.
 http://www.educa.aragob.es/iesfgcza/depart/depfiqui.htm 0/07/009 Química ªBachiller. Dado el equilibrio de disociación del cloruro nitrosilo. NOCl(g) NO + Cl ΔΗ 8KJ / mol Razone que efecto producirán en
http://www.educa.aragob.es/iesfgcza/depart/depfiqui.htm 0/07/009 Química ªBachiller. Dado el equilibrio de disociación del cloruro nitrosilo. NOCl(g) NO + Cl ΔΗ 8KJ / mol Razone que efecto producirán en
UNIDAD 8: EQUILIBRIO QUÍMICO EQUILIBRIO ÁCIDO-BASE
 UNIDAD 8: EQUILIBRIO QUÍMICO EQUILIBRIO ÁCIDO-BASE 1 Equilibrio Químico En la unidad 4 desarrollamos el tema de estequiometría de las reacciones químicas En esa unidad relacionábamos los reactivos con
UNIDAD 8: EQUILIBRIO QUÍMICO EQUILIBRIO ÁCIDO-BASE 1 Equilibrio Químico En la unidad 4 desarrollamos el tema de estequiometría de las reacciones químicas En esa unidad relacionábamos los reactivos con
Química 2º Bacharelato
 Química 2º Bacharelato DEPARTAMENTO DE FÍSICA E QUÍMICA Termodinámica química 13/12/07 Nombre: Problemas 1. a) Calcula qué calor se desprende en la combustión de 20,0 cm 3 de etanol líquido a presión atmosférica
Química 2º Bacharelato DEPARTAMENTO DE FÍSICA E QUÍMICA Termodinámica química 13/12/07 Nombre: Problemas 1. a) Calcula qué calor se desprende en la combustión de 20,0 cm 3 de etanol líquido a presión atmosférica
1. Termodinámica del Equilibrio Químico
 . Termodinámica del Equilibrio Químico Ya se ha explicado que la evolución de un proceso químico depende de la variación de energía libre. Así en la reacción A + B C + D, para que se efectúe en el sentido
. Termodinámica del Equilibrio Químico Ya se ha explicado que la evolución de un proceso químico depende de la variación de energía libre. Así en la reacción A + B C + D, para que se efectúe en el sentido
Unidad 5- Cinética Química
 La termodinámica nos permite conocer la espontaneidad ó no espontaneidad de las reacciones, pero no nos informa de la rapidez con que tendrá lugar el proceso de transformación de los reactivos en productos:
La termodinámica nos permite conocer la espontaneidad ó no espontaneidad de las reacciones, pero no nos informa de la rapidez con que tendrá lugar el proceso de transformación de los reactivos en productos:
Cinética química. Cinética Química Química 2º. Velocidad de reacción
 Cinética química Velocidad de reacción La velocidad de una reacción es la derivada de la concentración de un reactivo o producto con respecto al tiempo tomada siempre como valor positivo. Expresión de
Cinética química Velocidad de reacción La velocidad de una reacción es la derivada de la concentración de un reactivo o producto con respecto al tiempo tomada siempre como valor positivo. Expresión de
Reacciones Reversibles Equilibrio químico
 Reacciones Reversibles Equilibrio químico Introducción El concepto de equilibrio es fundamental para conocer y entender la química y el comportamiento de las sustancias. En la constante de equilibrio se
Reacciones Reversibles Equilibrio químico Introducción El concepto de equilibrio es fundamental para conocer y entender la química y el comportamiento de las sustancias. En la constante de equilibrio se
TEMA 5 CINÉTICA QUÍMICA
 TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
TERMOQUÍMICA. Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico
 Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico TERMOQUÍMICA La termoquímica es la aplicación de la Primera Ley de la Termodinámica al estudio
Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico TERMOQUÍMICA La termoquímica es la aplicación de la Primera Ley de la Termodinámica al estudio
Tema 7: EQUILIBRIO QUÍMICO
 Tema 7: EQUILIBRIO QUÍMICO 1) Qué es un equilibrio químico? En los problemas de estequiometría del tema 1 supusimos que las reacciones químicas se detienen cuando uno o más reactivos se agotan. Estas reacciones
Tema 7: EQUILIBRIO QUÍMICO 1) Qué es un equilibrio químico? En los problemas de estequiometría del tema 1 supusimos que las reacciones químicas se detienen cuando uno o más reactivos se agotan. Estas reacciones
EJERCICIO DE EXAMEN DE FISICOQUÍMICA
 EJERCICIO DE EXAMEN DE FISICOQUÍMICA 1) En un recipiente de volumen fijo, se tienen los gases ideales 1 y 2 a una presión total P. Si en estas condiciones se introduce un gas ideal manteniendo la presión
EJERCICIO DE EXAMEN DE FISICOQUÍMICA 1) En un recipiente de volumen fijo, se tienen los gases ideales 1 y 2 a una presión total P. Si en estas condiciones se introduce un gas ideal manteniendo la presión
Tecnólogo en Minería. Equilibrio Químico. Química I
 Tecnólogo en Minería Equilibrio Químico Química I Concepto de equilibrio y constante Pocas reacciones químicas se dan en un sentido Muchas veces las reacciones químicas no se completan, sino que llegan
Tecnólogo en Minería Equilibrio Químico Química I Concepto de equilibrio y constante Pocas reacciones químicas se dan en un sentido Muchas veces las reacciones químicas no se completan, sino que llegan
Equilibrio químico. 1.- Concepto de equilibrio químico. Características. Aspecto dinámico de las reacciones químicas. 2.- Ley de acción de masas.
 Equilibrio químico Tema 4 3 1.- Concepto de equilibrio químico. Características. Aspecto dinámico de las reacciones químicas. 2.- Ley de acción de masas. K C. Cociente de reacción. 3.- K p Relación con
Equilibrio químico Tema 4 3 1.- Concepto de equilibrio químico. Características. Aspecto dinámico de las reacciones químicas. 2.- Ley de acción de masas. K C. Cociente de reacción. 3.- K p Relación con
Equilibrio químico QUÍMICA III MEDIO 2018
 Equilibrio químico QUÍMICA III MEDIO 2018 Equilibrio químico con respecto a la velocidad Equilibrio químico con respecto a la concentración Equilibrio químico En una reacción química, generalmente los
Equilibrio químico QUÍMICA III MEDIO 2018 Equilibrio químico con respecto a la velocidad Equilibrio químico con respecto a la concentración Equilibrio químico En una reacción química, generalmente los
Unidad Equilibrio químico IIIº Medios º Parte.
 Unidad Equilibrio químico IIIº Medios 2018 1º Parte. Muchas de las reacciones que se producen en la naturaleza son irreversibles. Una reacción irreversible es aquella en que los reactantes se transforman
Unidad Equilibrio químico IIIº Medios 2018 1º Parte. Muchas de las reacciones que se producen en la naturaleza son irreversibles. Una reacción irreversible es aquella en que los reactantes se transforman
CINÉTICA QUÍMICA - PREGUNTAS DE TEST (2015)
 CINÉTICA QUÍMICA - PREGUNTAS DE TEST (2015) A- CONCEPTOS GENERALES DE CINÉTICA. ENERGÍA DE ACTIVACIÓN B- VELOCIDAD DE REACCIÓN C- CATALIZADORES D- ORDEN DE REACCIÓN - ECUACIÓN DE VELOCIDAD A - CONCEPTOS
CINÉTICA QUÍMICA - PREGUNTAS DE TEST (2015) A- CONCEPTOS GENERALES DE CINÉTICA. ENERGÍA DE ACTIVACIÓN B- VELOCIDAD DE REACCIÓN C- CATALIZADORES D- ORDEN DE REACCIÓN - ECUACIÓN DE VELOCIDAD A - CONCEPTOS
CURSO Bases moleculares, celulares y genéticas de la organización de los sistemas vivos
 KINESIOLOGIA UNIVERSIDAD DE CHILE 2011 CURSO Bases moleculares, celulares y genéticas de la organización de los sistemas vivos UNIDAD DE QUIMICA REMEDIAL Prof. Asoc. LUIS QUIÑONES SEPULVEDA, BQ., PhD Capítulo
KINESIOLOGIA UNIVERSIDAD DE CHILE 2011 CURSO Bases moleculares, celulares y genéticas de la organización de los sistemas vivos UNIDAD DE QUIMICA REMEDIAL Prof. Asoc. LUIS QUIÑONES SEPULVEDA, BQ., PhD Capítulo
2º Bachillerato EQUILIBRIO QUÍMICO
 º Bachillerato EQUILIBRIO QUÍMICO 1. Concepto de equilibrio químico.. ΔG en un proceso isotermo. 3. Constante de equilibrio Kp. 4. Constante de equilibrio Kc. 5. Constante de equilibrio Kx. 6. Equilibrio
º Bachillerato EQUILIBRIO QUÍMICO 1. Concepto de equilibrio químico.. ΔG en un proceso isotermo. 3. Constante de equilibrio Kp. 4. Constante de equilibrio Kc. 5. Constante de equilibrio Kx. 6. Equilibrio
Química general II Equilibrio químico
 Química general II Equilibrio químico capitulo 14, Chang El equilibrio es un estado en el que no se observan cambios conforme el tiempo transcurre. Cuando una reacción química alcanza el equilibrio, las
Química general II Equilibrio químico capitulo 14, Chang El equilibrio es un estado en el que no se observan cambios conforme el tiempo transcurre. Cuando una reacción química alcanza el equilibrio, las
REACCIONES EN EQUILIBRIO
 Equilibrio químico REACCIONES EN EQUILIBRIO El Equilibrio es un estado en el cual no se observan variaciones a lo largo del tiempo. Se alcanza el Equilibrio químico cuando: las velocidades de reacción,
Equilibrio químico REACCIONES EN EQUILIBRIO El Equilibrio es un estado en el cual no se observan variaciones a lo largo del tiempo. Se alcanza el Equilibrio químico cuando: las velocidades de reacción,
Las ecuaciones químicas
 Las reacciones químicas se representan escribiendo las fórmulas de los reactivos en el primer miembro de una ecuación y las de los productos en el segundo. El signo igual se sustituye por una flecha (
Las reacciones químicas se representan escribiendo las fórmulas de los reactivos en el primer miembro de una ecuación y las de los productos en el segundo. El signo igual se sustituye por una flecha (
1010 DEPARTAMENTO DE FÍSICA Y QUÍMICA 2º Bachillerato QUÍMICA
 1.- La constante de equilibrio, K p, para la siguiente reacción química: C 2 H 4 (g) + H 2 (g) C 2 H 6 (g), vale 5 x 10 17, a 25º C. Calcula, a la misma temperatura, el valor de K c. Solución: K c = 1,22
1.- La constante de equilibrio, K p, para la siguiente reacción química: C 2 H 4 (g) + H 2 (g) C 2 H 6 (g), vale 5 x 10 17, a 25º C. Calcula, a la misma temperatura, el valor de K c. Solución: K c = 1,22
Supongamos la reacción de formación de yoduro de hidrógeno a partir de sus componentes. I (g) + H (g) 2HI(g)
 TEMA 6: EQUILIBRIO QUÍMICO. 1.- Ley de equilibrio. En una reacción química, los reactivos se combinan entre sí para dar productos. Puede ocurrir, si el sistema de estudio es cerrado, que los productos
TEMA 6: EQUILIBRIO QUÍMICO. 1.- Ley de equilibrio. En una reacción química, los reactivos se combinan entre sí para dar productos. Puede ocurrir, si el sistema de estudio es cerrado, que los productos
Química general II Equilibrio químico
 Química general II Equilibrio químico capitulo 14, Chang El equilibrio es un estado en el que no se observan cambios conforme el tiempo transcurre. Cuando una reacción química alcanza el equilibrio, las
Química general II Equilibrio químico capitulo 14, Chang El equilibrio es un estado en el que no se observan cambios conforme el tiempo transcurre. Cuando una reacción química alcanza el equilibrio, las
EQUILIBRIO QUÍMICO. 1. Equilibrio químico. 2. La constante de equilibrio. 3. EL principio de LeChatelier. Química 2º bachillerato Equilibrio químico 1
 EQUILIBRIO QUÍMICO 1. Equilibrio químico. 2. La constante de equilibrio. 3. EL principio de LeChatelier. Química 2º bachillerato Equilibrio químico 1 0. CONOCIMIENTOS Los conocimientos previos que son
EQUILIBRIO QUÍMICO 1. Equilibrio químico. 2. La constante de equilibrio. 3. EL principio de LeChatelier. Química 2º bachillerato Equilibrio químico 1 0. CONOCIMIENTOS Los conocimientos previos que son
Equilibrio químico. Tema 5
 Equilibrio químico Tema 5 2 1.- Concepto de equilibrio químico. Características. Aspecto dinámico de las reacciones químicas. 2.- Ley de acción de masas. K C. Cociente de reacción. 3.- K p Relación con
Equilibrio químico Tema 5 2 1.- Concepto de equilibrio químico. Características. Aspecto dinámico de las reacciones químicas. 2.- Ley de acción de masas. K C. Cociente de reacción. 3.- K p Relación con
Equilibrio químico Dra. Patricia Satti, UNRN EQUILIBRIO QUÍMICO
 Equilibrio químico EQUILIBRIO QUÍMICO El estudio de las reacciones químicas debe permitir responder, entre otras, tres preguntas esenciales, de las cuáles hemos respondido dos: 1) Qué cantidad de energía
Equilibrio químico EQUILIBRIO QUÍMICO El estudio de las reacciones químicas debe permitir responder, entre otras, tres preguntas esenciales, de las cuáles hemos respondido dos: 1) Qué cantidad de energía
Equilibrio químico. El estudio del equilibrio químico trabaja básicamente con la siguiente pregunta: Reactantes Productos. Equilibrio Químico
 El estudio de las reacciones químicas debe permitir responder, entre otras, tres preguntas esenciales, de las cuáles hemos respondido dos: Equilibrio químico 1) Qué cantidad de energía está involucrada
El estudio de las reacciones químicas debe permitir responder, entre otras, tres preguntas esenciales, de las cuáles hemos respondido dos: Equilibrio químico 1) Qué cantidad de energía está involucrada
Ejercicios resueltos sobre Cinética de Reacción
 Ejercicios resueltos sobre Cinética de Reacción CUESTIÓN RESUELTA Señalar las proposiciones correctas referentes a la velocidad de una reacción química: a) Se puede expresar en mol -1. s -1 b) Se puede
Ejercicios resueltos sobre Cinética de Reacción CUESTIÓN RESUELTA Señalar las proposiciones correctas referentes a la velocidad de una reacción química: a) Se puede expresar en mol -1. s -1 b) Se puede
Mezclas ( G, S, H) ) Equilibrio y energía libre de Gibbs. Química Física I QUIM 4041 6/17/2014. Ileana Nieves Martínez. 17 de Junio de 2014
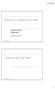 Equilibrio y energía libre de Gibbs Química Física I QUIM 441 Ileana Nieves Martínez 1 Mezclas (G, S, H) ) 2 1 Energía Libre molar parcial: i a T y constantes. dg dn dn 1 1 2 2... dg SdT Vd dn G total
Equilibrio y energía libre de Gibbs Química Física I QUIM 441 Ileana Nieves Martínez 1 Mezclas (G, S, H) ) 2 1 Energía Libre molar parcial: i a T y constantes. dg dn dn 1 1 2 2... dg SdT Vd dn G total
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2012 QUÍMICA TEMA 5: EQUILIBRIO QUÍMICO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 01 QUÍMICA TEMA 5: EQUILIBRIO QUÍMICO Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 6, Opción A Reserva, Ejercicio 3, Opción A Reserva, Ejercicio 6, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 01 QUÍMICA TEMA 5: EQUILIBRIO QUÍMICO Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 6, Opción A Reserva, Ejercicio 3, Opción A Reserva, Ejercicio 6, Opción
Química 2º Bachillerato. Dº de Física y Química. IES Atenea. S. S. Reyes 1. Equilibrio químico
 Química 2º Bachillerato. Dº de Física y Química. IES Atenea. S. S. Reyes 1 Equilibrio químico 1. En un matraz de 1 L se introducen 0,1 moles de PCl 5 y se calienta hasta 300 C, disociándose según: PCl
Química 2º Bachillerato. Dº de Física y Química. IES Atenea. S. S. Reyes 1 Equilibrio químico 1. En un matraz de 1 L se introducen 0,1 moles de PCl 5 y se calienta hasta 300 C, disociándose según: PCl
TERMODINÁMICA DEL EQUILIBRIO CAPÍTULO II. SOLUCIONES QUÍMICAS
 Ing. Federico G. Salazar Termodinámica del Equilibrio TERMODINÁMICA DEL EQUILIBRIO CAPÍTULO II. SOLUCIONES QUÍMICAS Contenido 1. Propiedades Parciales Molares 2. Entalpía de Mezcla 3. Efectos caloríficos
Ing. Federico G. Salazar Termodinámica del Equilibrio TERMODINÁMICA DEL EQUILIBRIO CAPÍTULO II. SOLUCIONES QUÍMICAS Contenido 1. Propiedades Parciales Molares 2. Entalpía de Mezcla 3. Efectos caloríficos
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 15 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio 6, Opción A Reserva 3,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 15 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio 6, Opción A Reserva 3,
El equilibrio químico es un equilibrio dinámico
 Equilibrio Químico 1. Conceptos básicos. Constante de equilibrio 3. Cociente de reacción 4. Usos de la constante de equilibrio 5. Alteración de un sistema de equilibrio 6. Presiones parciales y constante
Equilibrio Químico 1. Conceptos básicos. Constante de equilibrio 3. Cociente de reacción 4. Usos de la constante de equilibrio 5. Alteración de un sistema de equilibrio 6. Presiones parciales y constante
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 9 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio 4, Opción A Reserva, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 9 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio 4, Opción A Reserva, Ejercicio
EJERCICIOS DE TERMODINÁMICA
 EJERCICIOS DE TERMODINÁMICA. La descomposición del tetraóxido de nitrógeno ( N O 4 NO4( NO( ocurre espontáneamente a temperaturas altas. Los datos termodinámicos a 98ºK se incluyen en la tabla adjunta.
EJERCICIOS DE TERMODINÁMICA. La descomposición del tetraóxido de nitrógeno ( N O 4 NO4( NO( ocurre espontáneamente a temperaturas altas. Los datos termodinámicos a 98ºK se incluyen en la tabla adjunta.
TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1]
![TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1] TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1]](/thumbs/40/22050892.jpg) TEMA 4: BALANCES DE ENERGÍA IngQui-4 [1] OBJETIVOS! Aplicar la ecuación de conservación al análisis de la energía involucrada en un sistema.! Recordar las componentes de la energía (cinética, potencial
TEMA 4: BALANCES DE ENERGÍA IngQui-4 [1] OBJETIVOS! Aplicar la ecuación de conservación al análisis de la energía involucrada en un sistema.! Recordar las componentes de la energía (cinética, potencial
TEORICO-PRÁCTICO N 5: LEYES DE LOS GASES IDEALES
 TEORICO-PRÁCTICO N 5: LEYES DE LOS GASES IDEALES FUNDAMENTO TEÓRICO: La materia puede estar en tres estados: sólido, líquido y gaseoso. Los gases, no tienen forma ni volumen fijo, las fuerzas que mantienen
TEORICO-PRÁCTICO N 5: LEYES DE LOS GASES IDEALES FUNDAMENTO TEÓRICO: La materia puede estar en tres estados: sólido, líquido y gaseoso. Los gases, no tienen forma ni volumen fijo, las fuerzas que mantienen
CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara
 CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara OBJETIVOS 1.- Estudiar la cinética de la reacción de hidrólisis ácida del acetato de metilo en disolución
CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara OBJETIVOS 1.- Estudiar la cinética de la reacción de hidrólisis ácida del acetato de metilo en disolución
Universidad Tecnológica Nacional Facultad Regional Rosario Cátedra de Ing. De las Reacciones
 Universidad Tecnológica acional Facultad Regional Rosario Cátedra de Ing. e las Reacciones PRCTIC UI RECTORES IELES 01 Ing. Roque Masciarelli - Ing Silvia Stancich - Ing. Stoppani Fernando 1. Un reactor
Universidad Tecnológica acional Facultad Regional Rosario Cátedra de Ing. e las Reacciones PRCTIC UI RECTORES IELES 01 Ing. Roque Masciarelli - Ing Silvia Stancich - Ing. Stoppani Fernando 1. Un reactor
FÍSICA APLICADA Y FISICOQUÍMICA I. Tema 10. Equilibrio químico
 María del Pilar García Santos GRADO EN FARMACIA FÍSICA APLICADA Y FISICOQUÍMICA I Tema 10 Equilibrio químico Esquema Tema 10. Equilibrio químico 10.1 Condición de equilibrio químico y espontaneidad en
María del Pilar García Santos GRADO EN FARMACIA FÍSICA APLICADA Y FISICOQUÍMICA I Tema 10 Equilibrio químico Esquema Tema 10. Equilibrio químico 10.1 Condición de equilibrio químico y espontaneidad en
HOJA Nº 6. REACCIONES QUÍMICAS (II)
 HOJA Nº 6. REACCIONES QUÍMICAS (II) 1. El cobre reacciona con el ácido sulfúrico para producir sulfato de cobre (II), dióxido de azufre y agua. Si se tienen 30 g de cobre y 200 g de H2SO4, calcular: a.
HOJA Nº 6. REACCIONES QUÍMICAS (II) 1. El cobre reacciona con el ácido sulfúrico para producir sulfato de cobre (II), dióxido de azufre y agua. Si se tienen 30 g de cobre y 200 g de H2SO4, calcular: a.
( kj / mol) -1268 0-393,5-285,8
 Apellidos y Nombre Grupo 1. (1 punto) En un experimento se disuelve una barra de aluminio (sólido) en 100,00 ml de una disolución de HCl 1,50 M. 2 Al(s) + 6 HCl(ac) 2 AlCl 3 (ac) + 3 H 2 (g) Cuando termina
Apellidos y Nombre Grupo 1. (1 punto) En un experimento se disuelve una barra de aluminio (sólido) en 100,00 ml de una disolución de HCl 1,50 M. 2 Al(s) + 6 HCl(ac) 2 AlCl 3 (ac) + 3 H 2 (g) Cuando termina
DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA 2º DE BACHILLERATO. Equilibrio químico
 DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA º DE BACHILLERATO Actividades tema 6 Equilibrio químico Reacciones reversibles y equilibrio químico.-formula la expresión de K C para
DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA º DE BACHILLERATO Actividades tema 6 Equilibrio químico Reacciones reversibles y equilibrio químico.-formula la expresión de K C para
DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS
 DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS Se le llama fluido a toda aquella sustancia continua que puede fluir. Los fluidos pueden ser gaseosos y líquidos. Esta es la diferencia fundamental entre un sólido, cuya
DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS Se le llama fluido a toda aquella sustancia continua que puede fluir. Los fluidos pueden ser gaseosos y líquidos. Esta es la diferencia fundamental entre un sólido, cuya
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA GUÍA N 3: CINÉTICA QUÍMICA
 UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 3: CINÉTICA QUÍMICA 1.- Escriba las expresiones de las velocidades de
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 3: CINÉTICA QUÍMICA 1.- Escriba las expresiones de las velocidades de
UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A
 UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A CUESTIÓN.- Cuál de las siguientes reacciones nunca será espontánea independientemente del valor de la temperatura?, cuál será
UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A CUESTIÓN.- Cuál de las siguientes reacciones nunca será espontánea independientemente del valor de la temperatura?, cuál será
I 2 (s) I 2 (g) Los cambios de fase son reversibles y ambas fases coexisten en equilibrio en unas determinadas condiciones de presión y temperatura.
 El yodo molecular es un sólido de color violeta oscuro. Si en un recipiente de vidrio, en el que previamente se ha extraído el aire de su interior; se introduce yodo sólido, puede observarse cómo rápidamente
El yodo molecular es un sólido de color violeta oscuro. Si en un recipiente de vidrio, en el que previamente se ha extraído el aire de su interior; se introduce yodo sólido, puede observarse cómo rápidamente
Problemas resueltos = =
 Química General. Curso º Problemas resueltos. Sabiendo que la constante de equilibrio para la reacción entre el ácido acético y el etanol es 4, calcular las composiciones del equilibrio cuando se parte
Química General. Curso º Problemas resueltos. Sabiendo que la constante de equilibrio para la reacción entre el ácido acético y el etanol es 4, calcular las composiciones del equilibrio cuando se parte
Conceptos fundamentales en Termodinámica
 Conceptos fundamentales en Termodinámica Física II Grado en Ingeniería de Organización Industrial Primer Curso Joaquín Bernal Méndez Curso 2011-2012 Departamento de Física Aplicada III Universidad de Sevilla
Conceptos fundamentales en Termodinámica Física II Grado en Ingeniería de Organización Industrial Primer Curso Joaquín Bernal Méndez Curso 2011-2012 Departamento de Física Aplicada III Universidad de Sevilla
EL EQUILIBRIO QUÍMICO - PREGUNTAS TIPO TEST (2015)
 EL EQUILIBRIO QUÍMICO - PREGUNTAS TIPO TEST (2015) Grupo A - DEFINICIONES GENERALES: Grupo B - CONSTANTES DE EQUILIBRIO: Grupo C - PRINCIPIO DE LE CHATELIER: Grupo D- CONDICIONES TERMODINÁMICAS DE EQUILIBRIO
EL EQUILIBRIO QUÍMICO - PREGUNTAS TIPO TEST (2015) Grupo A - DEFINICIONES GENERALES: Grupo B - CONSTANTES DE EQUILIBRIO: Grupo C - PRINCIPIO DE LE CHATELIER: Grupo D- CONDICIONES TERMODINÁMICAS DE EQUILIBRIO
GUÍA N 3: Equilibrio Químico y Cinética Química
 1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Reacción irreversible b) Reacción reversible c) Equilibrio químico d) Constante de equilibrio e) Principio de Le Chatelier
1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Reacción irreversible b) Reacción reversible c) Equilibrio químico d) Constante de equilibrio e) Principio de Le Chatelier
EJERCICIOS RESUELTOS DE EQUILIBRIO QUIMICO
 EJERIIOS RESUELTOS DE EQUILIBRIO QUIMIO 1. uando el cloruro amónico se calienta a 75º en un recipiente cerrado de 1,0 litro, se descompone dando lugar a cloruro de hidrógeno gaseoso y amoniaco gaseoso
EJERIIOS RESUELTOS DE EQUILIBRIO QUIMIO 1. uando el cloruro amónico se calienta a 75º en un recipiente cerrado de 1,0 litro, se descompone dando lugar a cloruro de hidrógeno gaseoso y amoniaco gaseoso
Tema 12 Termoquímica. Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad En qué dirección se produce? Reacciones Químicas
 Tema 1 Estequiometría Cuánto se produce? Cuánto reacciona? Tema 15 Equilibrio Cuándo se alcanza? Cómo modificarlo? Tema 12 Termoquímica Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad
Tema 1 Estequiometría Cuánto se produce? Cuánto reacciona? Tema 15 Equilibrio Cuándo se alcanza? Cómo modificarlo? Tema 12 Termoquímica Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad
EQUILIBRIO QUÍMICO 1.- QUÉ ES UN EQUILIBRIO QUÍMICO? dinámico. EQUILIBRIO QUÍMICO. Equilibrio [I 2 ] [H 2 ] Tiempo QUÍMICA 2º BACHILLERATO
![EQUILIBRIO QUÍMICO 1.- QUÉ ES UN EQUILIBRIO QUÍMICO? dinámico. EQUILIBRIO QUÍMICO. Equilibrio [I 2 ] [H 2 ] Tiempo QUÍMICA 2º BACHILLERATO EQUILIBRIO QUÍMICO 1.- QUÉ ES UN EQUILIBRIO QUÍMICO? dinámico. EQUILIBRIO QUÍMICO. Equilibrio [I 2 ] [H 2 ] Tiempo QUÍMICA 2º BACHILLERATO](/thumbs/40/21650071.jpg) EQUILIBRIO QUÍMIO QUÍMIA º BAHILLERATO 1.- oncepto de equilibrio químico..- Ley de acción de masas. La constante de equilibrio..1. Generalizaión de la expresión de c.- P. Relación con..1. Magnitud de las
EQUILIBRIO QUÍMIO QUÍMIA º BAHILLERATO 1.- oncepto de equilibrio químico..- Ley de acción de masas. La constante de equilibrio..1. Generalizaión de la expresión de c.- P. Relación con..1. Magnitud de las
Unidad 7: Equilibrio químico
 Unidad 7: Equilibrio químico 1. INTRODUCCIÓN Una reacción reversible es aquella en la cual los productos vuelven a combinarse para generar los reactivos. En estos procesos ocurren simultáneamente dos reacciones:
Unidad 7: Equilibrio químico 1. INTRODUCCIÓN Una reacción reversible es aquella en la cual los productos vuelven a combinarse para generar los reactivos. En estos procesos ocurren simultáneamente dos reacciones:
Estequiometría. En química, la estequiometría (del griego "στοιχειον"
 Estequiometría En química, la estequiometría (del griego "στοιχειον" = stoicheion (elemento) y "μετρον"=métron, (medida) es el cálculo de las relaciones cuantitativas entre reactivos y productos en el
Estequiometría En química, la estequiometría (del griego "στοιχειον" = stoicheion (elemento) y "μετρον"=métron, (medida) es el cálculo de las relaciones cuantitativas entre reactivos y productos en el
ENERGÍA DE LAS REACCIONES QUÍMICAS. TERMOQUÍMICA
 ENERGÍA DE LAS REACCIONES QUÍMICAS. TERMOQUÍMICA Problemas 1. El calor de combustión del ácido acético(l) es 874 kj/mol. Sabiendo que las entalpías de formación estándar del CO 2 (g), H 2 O(l) son respectivamente:
ENERGÍA DE LAS REACCIONES QUÍMICAS. TERMOQUÍMICA Problemas 1. El calor de combustión del ácido acético(l) es 874 kj/mol. Sabiendo que las entalpías de formación estándar del CO 2 (g), H 2 O(l) son respectivamente:
Tema 2. Estequiometría
 Tema 2. Estequiometría Masas Atómicas Escala del carbono 12 Masas atómicas relativas Concepto de mol Relaciones de masa de las fórmulas químicas Composición centesimal Fórmula empírica. Fórmula molecular
Tema 2. Estequiometría Masas Atómicas Escala del carbono 12 Masas atómicas relativas Concepto de mol Relaciones de masa de las fórmulas químicas Composición centesimal Fórmula empírica. Fórmula molecular
Tema 6. Cinética de las Reacciones Químicas
 Tema 6 Cinética de las Reacciones Químicas 1 TEMA 6 CINÉTICA DE LAS REACCIONES QUÍMICAS 1. DEFINICIONES BÁSICAS CINÉTICA QUÍMICA VELOCIDAD DE REACCIÓN LEY DE VELOCIDADES Y ÓRDENES DE REACCIÓN ECUACIÓN
Tema 6 Cinética de las Reacciones Químicas 1 TEMA 6 CINÉTICA DE LAS REACCIONES QUÍMICAS 1. DEFINICIONES BÁSICAS CINÉTICA QUÍMICA VELOCIDAD DE REACCIÓN LEY DE VELOCIDADES Y ÓRDENES DE REACCIÓN ECUACIÓN
Solución: Método 1: Se calcula primero cuanto PCl 5 se disocia a partir de la cantidad dada: 6 g 208,25 g mol. = 0,0288 mol.
 00 Capítulo.En un matraz de L de capacidad se colocan 6 g de PCl 5 sólido. Se hace el vacío, se cierra el matraz y se calienta a 50 C. El PCl 5 pasa al estado de vapor y se disocia parcialmente. La presión
00 Capítulo.En un matraz de L de capacidad se colocan 6 g de PCl 5 sólido. Se hace el vacío, se cierra el matraz y se calienta a 50 C. El PCl 5 pasa al estado de vapor y se disocia parcialmente. La presión
TERMODINÁMICA 1. En la fermentación de la glucosa (C6H12O6) se obtiene etanol (C2H5OH) y CO2. Si la entalpía de combustión de la glucosa es de 15.
 TERMODINÁMICA 1. En la fermentación de la glucosa (C6H12O6) se obtiene etanol (C2H5OH) y CO2. Si la entalpía de combustión de la glucosa es de 15.63 kj/g y la del etanol es de 29.72 kj/g, a) Calcular la
TERMODINÁMICA 1. En la fermentación de la glucosa (C6H12O6) se obtiene etanol (C2H5OH) y CO2. Si la entalpía de combustión de la glucosa es de 15.63 kj/g y la del etanol es de 29.72 kj/g, a) Calcular la
GUIA DE EJERCICIOS (Equilibrio Químico y Cinética Química Empírica)
 Universidad de Santiago de Chile Departamento de Ingeniería Química GUIA DE EJERCICIOS (Equilibrio Químico y Cinética Química Empírica) Autor: Prof. Julio Romero 1. Describa aplicando el principio de Le
Universidad de Santiago de Chile Departamento de Ingeniería Química GUIA DE EJERCICIOS (Equilibrio Químico y Cinética Química Empírica) Autor: Prof. Julio Romero 1. Describa aplicando el principio de Le
Análisis esquemático simplificado de una torre de enfriamiento.
 Análisis esquemático simplificado de una torre de enfriamiento. En el diagrama el aire con una humedad Y 2 y temperatura t 2 entra por el fondo de la torre y la abandona por la parte superior con una humedad
Análisis esquemático simplificado de una torre de enfriamiento. En el diagrama el aire con una humedad Y 2 y temperatura t 2 entra por el fondo de la torre y la abandona por la parte superior con una humedad
Equilibrio químico 9/23/2010. Copyright The McGraw-Hill Companies, Inc. / Provisto por Dr. Hernández-Castillo 1. Capítulo 14
 Equilibrio es un estado en el que no hay cambios observables con el pasar del tiempo. Equilibrio químico Capítulo 14 Equilibrio químico es logrado cuando: La rapidez de la reacción en una dirección y en
Equilibrio es un estado en el que no hay cambios observables con el pasar del tiempo. Equilibrio químico Capítulo 14 Equilibrio químico es logrado cuando: La rapidez de la reacción en una dirección y en
TEMA 6: CINÉTICA HETEROGÉNEA FLUIDO - FLUIDO CQA-6/1
 TEMA 6: CINÉTICA HETEROGÉNEA FLUIDO - FLUIDO CQA-6/1 PLANTEAMIENTO DEL MODELO CINÉTICO Objetivos de las reacciones heterogéneas fluido-fluido:! Obtener productos valiosos mediante reacciones gas-líquido!
TEMA 6: CINÉTICA HETEROGÉNEA FLUIDO - FLUIDO CQA-6/1 PLANTEAMIENTO DEL MODELO CINÉTICO Objetivos de las reacciones heterogéneas fluido-fluido:! Obtener productos valiosos mediante reacciones gas-líquido!
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre 2010. Fase general OPCIÓN A
 1 PAU Química. Septiembre 2010. Fase general OPCIÓN A Cuestión 1A. Considerando el elemento alcalinotérreo del tercer periodo y el segundo elemento del grupo de los halógenos: a) Escriba sus configuraciones
1 PAU Química. Septiembre 2010. Fase general OPCIÓN A Cuestión 1A. Considerando el elemento alcalinotérreo del tercer periodo y el segundo elemento del grupo de los halógenos: a) Escriba sus configuraciones
EJERCICIOS RESUELTOS DE CINÉTICA
 UNIVERSIDAD DEL ZULIA FACULTAD DE INGENIERÍA CICLO BÁSICO DEPARTAMENTO DE QUÍMICA CÁTEDRA: QUÍMICA II EJERCICIOS RESUELTOS DE CINÉTICA Profesora Neida Núñez Maracaibo, Agosto 2015 Ejercicios de Cinética
UNIVERSIDAD DEL ZULIA FACULTAD DE INGENIERÍA CICLO BÁSICO DEPARTAMENTO DE QUÍMICA CÁTEDRA: QUÍMICA II EJERCICIOS RESUELTOS DE CINÉTICA Profesora Neida Núñez Maracaibo, Agosto 2015 Ejercicios de Cinética
TERMODINÁMICA QUÍMICA
 TERMODINÁMICA QUÍMICA GBZA 1. INTRODUCCIÓN. CONCEPTOS ELEMENTALES. 2. PRIMER PRINCIPIO DE LA TERMODINÁMICA. 3. ECUACIONES TERMODINÁMICAS. 4. ENTALPÍA DE REACCIÓN. LEY DE HESS. 5. DIAGRAMAS DE ENTALPÍA.
TERMODINÁMICA QUÍMICA GBZA 1. INTRODUCCIÓN. CONCEPTOS ELEMENTALES. 2. PRIMER PRINCIPIO DE LA TERMODINÁMICA. 3. ECUACIONES TERMODINÁMICAS. 4. ENTALPÍA DE REACCIÓN. LEY DE HESS. 5. DIAGRAMAS DE ENTALPÍA.
EQUILIBRIO QUIMICO QUIMICA-CPAM. FCM 2016
 EQUILIBRIO QUIMICO QUIMICA-CPAM. FCM 2016 Qué es equilibrio? Equilibrio: es un estado en el cual no se observan cambios a medida que transcurre el tiempo. Copyright The McGraw-Hill Companies, Inc. Permission
EQUILIBRIO QUIMICO QUIMICA-CPAM. FCM 2016 Qué es equilibrio? Equilibrio: es un estado en el cual no se observan cambios a medida que transcurre el tiempo. Copyright The McGraw-Hill Companies, Inc. Permission
La velocidad de una reacción describe qué tan rápido se consumen los reactivos y se forman los productos. CH 4. (g) + 2 O 2.
 Cinética Química 1. Velocidad de reacción. 2. Factores que afectan la velocidad de reacción. 3. Expresión de la ley de velocidad. 4. Teoría de las colisiones moleculares 5. Estado de transición. 6. Catalizadores.
Cinética Química 1. Velocidad de reacción. 2. Factores que afectan la velocidad de reacción. 3. Expresión de la ley de velocidad. 4. Teoría de las colisiones moleculares 5. Estado de transición. 6. Catalizadores.
Ejercicios Equilibrio Químico
 Ejercicios Equilibrio Químico 1. En un recipiente de 10,0 L a 800K, se encierran 1,00 mol de CO(g) y 1,00 mol de H 2 O(g). Cuando se alcanza el equilibrio: CO(g) + H 2 O(g) CO 2 (g) + H 2 (g) se hallan
Ejercicios Equilibrio Químico 1. En un recipiente de 10,0 L a 800K, se encierran 1,00 mol de CO(g) y 1,00 mol de H 2 O(g). Cuando se alcanza el equilibrio: CO(g) + H 2 O(g) CO 2 (g) + H 2 (g) se hallan
El grado de avance de las reacciones
 Facultad de Química Cátedra de Química Inorgánica DEPARTAMENTO ESTRELLA CAMPOS QUÍMICA GENERAL II 2006 Semana 7 El grado de avance de las reacciones Bibliografía: - Química, La Ciencia Central, T.L.Brown,
Facultad de Química Cátedra de Química Inorgánica DEPARTAMENTO ESTRELLA CAMPOS QUÍMICA GENERAL II 2006 Semana 7 El grado de avance de las reacciones Bibliografía: - Química, La Ciencia Central, T.L.Brown,
F o r m a n d o P e r s o n a s Í n t e g r a s. Guía de Contenido Unidad Equilibrio químico
 Departamento de Ciencias y Tecnología. Profesora Ana María González. O Saint Gaspar College Misio nero s de la Precio sa Sangre Guía de Contenido Unidad Equilibrio químico Muchas de las reacciones que
Departamento de Ciencias y Tecnología. Profesora Ana María González. O Saint Gaspar College Misio nero s de la Precio sa Sangre Guía de Contenido Unidad Equilibrio químico Muchas de las reacciones que
Reacciones químicas. Equilibrio. Cinética. Tipos. Equilibrios ácido-base. Equilibrios de solubilidad Disoluciones Equilibrios redox. Eq.
 Estequiometría Termoquímica Espontaneidad Cuánto se produce? Cuánto reacciona? Desprende o absorbe calor? Cuánto calor? Por qué se produce? En qué dirección? Equilibrio Cuándo se alcanza? Cómo modificarlo?
Estequiometría Termoquímica Espontaneidad Cuánto se produce? Cuánto reacciona? Desprende o absorbe calor? Cuánto calor? Por qué se produce? En qué dirección? Equilibrio Cuándo se alcanza? Cómo modificarlo?
UNIDAD 3. EQULIBRIO QUÍMICO
 UNIDAD 3. EQULIBRIO QUÍMICO Equilibrio químico y características Constantes de equilibrio: K c y K p Grado de disociación Cociente de reacción Factores que afectan al equilibrio químico. Principio de Le
UNIDAD 3. EQULIBRIO QUÍMICO Equilibrio químico y características Constantes de equilibrio: K c y K p Grado de disociación Cociente de reacción Factores que afectan al equilibrio químico. Principio de Le
RELACIÓN DE PROBLEMAS. DISOLUCIONES Y PROPIEDADES COLIGATIVAS.
 RELACIÓN DE PROBLEMAS. Y PROPIEDADES COLIGATIVAS. 1.- Se disuelven 150 gramos de etanol (CH 3 CH 2 OH), de densidad 0,8 g /cm 3, en agua hasta completar 0,5 litros de disolución. Calcular el porcentaje
RELACIÓN DE PROBLEMAS. Y PROPIEDADES COLIGATIVAS. 1.- Se disuelven 150 gramos de etanol (CH 3 CH 2 OH), de densidad 0,8 g /cm 3, en agua hasta completar 0,5 litros de disolución. Calcular el porcentaje
Guía de repaso 5: Gases-Transformación isotérmica
 Guía de repaso 5: Gases-Transformación isotérmica 1- a) Cuáles son las cantidades que determinan el estado de un gas? b) Qué significa decir que un gas sufrió una transformación? 2- a) Qué son los gases
Guía de repaso 5: Gases-Transformación isotérmica 1- a) Cuáles son las cantidades que determinan el estado de un gas? b) Qué significa decir que un gas sufrió una transformación? 2- a) Qué son los gases
QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS
 UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://www.uprh.edu/~quimgen) QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS Ejemplo #1 PRESIÓN DE VAPOR DE UNA DISOLUCIÓN DE COMPONENTES
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://www.uprh.edu/~quimgen) QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS Ejemplo #1 PRESIÓN DE VAPOR DE UNA DISOLUCIÓN DE COMPONENTES
CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA EQUILIBRIO QUÍMICO EQUILIBRIO QUÍMICO
 CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA EQUILIBRIO QUÍMICO EQUILIBRIO QUÍMICO Desde un punto de vista termodinámico, la condición de equilibrio químico se establece a partir de la variación de la
CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA EQUILIBRIO QUÍMICO EQUILIBRIO QUÍMICO Desde un punto de vista termodinámico, la condición de equilibrio químico se establece a partir de la variación de la
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 Equilibrio Químico Programa de Acceso Inclusivo, Equidad y Permanencia RECUERDA QUE: el Equilibrio Químico, se presenta cuando reacciones opuestas ocurren a velocidades iguales. La velocidad a la que se
Equilibrio Químico Programa de Acceso Inclusivo, Equidad y Permanencia RECUERDA QUE: el Equilibrio Químico, se presenta cuando reacciones opuestas ocurren a velocidades iguales. La velocidad a la que se
EQUILIBRIO QUÍMICO. Cuando ocurre una reacción química, termina agotándose siempre, al menos, uno de los reactivos?
 EQUILIBRIO QUÍMICO Cuando ocurre una reacción química, termina agotándose siempre, al menos, uno de los reactivos? DEFINICIÓN DE EQUILIBRIO QUÍMICO Las reacciones que ocurren en un único sentido se llaman
EQUILIBRIO QUÍMICO Cuando ocurre una reacción química, termina agotándose siempre, al menos, uno de los reactivos? DEFINICIÓN DE EQUILIBRIO QUÍMICO Las reacciones que ocurren en un único sentido se llaman
CINÉTICA QUÍMICA. Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico
 Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico CINÉTICA QUÍMICA La cinética química estudia la variación de la concentración de reactantes o
Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico CINÉTICA QUÍMICA La cinética química estudia la variación de la concentración de reactantes o
GUÍA 2 DE EJERCICIOS EQUÍLIBRIO QUÍMICO
 GUÍA 2 DE EJERCICIOS EQUÍLIBRIO QUÍMICO Área Química Resultados de aprendizaje Conocer y analizar las características de un sistema en equilibrio y en base a condiciones iniciales de esté, determinar concentraciones
GUÍA 2 DE EJERCICIOS EQUÍLIBRIO QUÍMICO Área Química Resultados de aprendizaje Conocer y analizar las características de un sistema en equilibrio y en base a condiciones iniciales de esté, determinar concentraciones
Equilibrio químico EQUILIBRIO QUÍMICO QUÍMICA 2º
 Equilibrio químico Qué es un equilibrio químico? En una reacción química reversible como: a A + b B c C + d D se dan dos reacciones al mismo tiempo, por un lado A y B reaccionan para dar C y D y, conforme
Equilibrio químico Qué es un equilibrio químico? En una reacción química reversible como: a A + b B c C + d D se dan dos reacciones al mismo tiempo, por un lado A y B reaccionan para dar C y D y, conforme
TEMA V: EQUILIBRIO QUIMICO
 EMA V: EQUILIBRIO QUIMICO 1.- El CO gaseoso se disocia a 1000K según la reacción: CO (g) CO (g) + (g) Calcule el valor de Kp cuando la presión de equilibrio es 1 atm y el grado de disociación del CO es
EMA V: EQUILIBRIO QUIMICO 1.- El CO gaseoso se disocia a 1000K según la reacción: CO (g) CO (g) + (g) Calcule el valor de Kp cuando la presión de equilibrio es 1 atm y el grado de disociación del CO es
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo.
 Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
T(K) 298 400 600 800 1000 Kp 2,82 10-25 1,78 10-16 1,98 10-8 1,29 10-3 2,642 10 1
 EQUILIBRIO QUÍMICO : ACTIVIDADES DE SELECTIVIDAD Curso 13-14 1.- En un matraz de 2 l se introducen 12 g de PCl 5 y se calienta hasta 300 º C. En el equilibrio de disociación; PCl 5 (g) PCl 3 (g) + Cl 2
EQUILIBRIO QUÍMICO : ACTIVIDADES DE SELECTIVIDAD Curso 13-14 1.- En un matraz de 2 l se introducen 12 g de PCl 5 y se calienta hasta 300 º C. En el equilibrio de disociación; PCl 5 (g) PCl 3 (g) + Cl 2
Equilibrio Químico. 2º Bachillerato IES Fuerte de Cortadura (Cádiz)
 Equilibrio Químico 2º Bachillerato IES Fuerte de Cortadura (Cádiz) 1 INTRODUCCIÓN Existen muchas reacciones en las que los productos obtenidos son capaces de reaccionar mutuamente entre sí, o descomponerse,
Equilibrio Químico 2º Bachillerato IES Fuerte de Cortadura (Cádiz) 1 INTRODUCCIÓN Existen muchas reacciones en las que los productos obtenidos son capaces de reaccionar mutuamente entre sí, o descomponerse,
Qué son los diagramas Ternarios?
 Diagramas Ternarios Qué son los diagramas Ternarios? Diagramas que representan el equilibrio entre las distintas fases que se forman mediante tres componentes, como una función de la temperatura. Normalmente,
Diagramas Ternarios Qué son los diagramas Ternarios? Diagramas que representan el equilibrio entre las distintas fases que se forman mediante tres componentes, como una función de la temperatura. Normalmente,
Resolución de un problema básico de Cinética Química: hallar n y k
 Resolución de un problema básico de Cinética Química: hallar n y k Apellidos, nombre Departamento Centro Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento de Tecnología de Alimentos ETSIA (Universidad
Resolución de un problema básico de Cinética Química: hallar n y k Apellidos, nombre Departamento Centro Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento de Tecnología de Alimentos ETSIA (Universidad
EQUILIBRIO EN SISTEMAS
 UNIVERSIDAD AUTÓNOMA DEL ESTADO DE MÉXICO FACULTAD DE INGENIERÍA EQUILIBRIO EN SISTEMAS TERMODINÁMICOS (PARTE I) Unidad de aprendizaje: Fisicoquímica Dra. MERCEDES LUCERO CHÁVEZ Semestre 2015B CONTENIDO
UNIVERSIDAD AUTÓNOMA DEL ESTADO DE MÉXICO FACULTAD DE INGENIERÍA EQUILIBRIO EN SISTEMAS TERMODINÁMICOS (PARTE I) Unidad de aprendizaje: Fisicoquímica Dra. MERCEDES LUCERO CHÁVEZ Semestre 2015B CONTENIDO
Termodinámica: Gases Ideales y Sustancia Pura
 Termodinámica: Gases Ideales y Sustancia Pura Presenta: M. I. Ruiz Gasca Marco Antonio Instituto Tecnológico de Tláhuac II Septiembre, 2015 Marco Antonio (ITT II) México D.F., Tláhuac Agosto, 2015 1 /
Termodinámica: Gases Ideales y Sustancia Pura Presenta: M. I. Ruiz Gasca Marco Antonio Instituto Tecnológico de Tláhuac II Septiembre, 2015 Marco Antonio (ITT II) México D.F., Tláhuac Agosto, 2015 1 /
