LICENCIATURA EN FARMACIA ÁREA: MICROBIOLOGÍA ASIGNATURA: LABORATORIO DE INMUNOLOGÍA FARMACÉUTICA CÓDIGO: FARM-018 L
|
|
|
- Elena Herrero Zúñiga
- hace 7 años
- Vistas:
Transcripción
1 BENÉMERITA UNIVERSIDAD AUTÓNOMA DE PUEBLA VICERRECTORÍA DE DOCENCIA DIRECCIÓN GENERALDE EDUCACIÓN SUPERIOR FACULTAD DE CIENCIAS QUÍMICAS LICENCIATURA EN FARMACIA ÁREA: MICROBIOLOGÍA ASIGNATURA: LABORATORIO DE INMUNOLOGÍA FARMACÉUTICA ELABORADO POR: CÓDIGO: FARM-018 L M.S.P. Carlos Cabrera Maldonado M. C. Gloria León Tello M.S.P. Jesús Luzuriaga Galicia. M.C. Nidia Gary, Pazos Salazar M.C. Ana Berta Escobedo López. M.S.P. María de la Cruz Meneses Sánchez Dr. Juan Manuel Álvarez López FEBRERO 2009
2 ÍNDICE NÚMERO DE LA PRÁCTICA PRACTICA N 1 PRACTICA N 2 PRACTICA N 3 PRACTICA N 4 PRACTICA N 5 PRACTICA N 6 TITULO DE LA PRÁCTICA SEGURIDAD EN EL LABORATORIO PÁGINA TOMA DE MUESTRAS 7 DILUCIONES OBSERVACION DE LEUCOCITOS DETERMINACIÓN DEL GRUPO SANGUÍNEO 11 SEMINARIO: HERENCIA DE LOS GRUPOS SANGUÍNEOS PRACTICA N 7 PRACTICA N 8 PRACTICA N 9 PRACTICA N 10 PRACTICA N 11 PRACTICA N 12 PRACTICA N 13 DETERMINACIÓN DEL TITULO DE ANTICUERPOS ABO DEL SUERO PRUEBAS CRUZADAS REACCIONES FEBRILES SEMINARIO: DIAGNÓSTICO SEROLÓGICO DE INFECCIONES MICROBIANAS FACTOR REUMATOIDE Y PROTEINA C REACTIVA DETERMINACIÓN DE ANTIESTREPTOLISINAS O (ASO) SEMINARIO: INMUNIZACIÓN PRACTICA N 14 PRACTICA N 15 PRACTICA N 16 DETERMINACIÓN DE LA GONADOTROPINA CORIONICA HUMANA SEMINARIO: DETECCIÓN DE ANTICUERPOS CONTRA EL VIH (ELISA/WESTERN BLOT) SEMINARIO: INMUNOELECTROFORESIS 23
3 INTRODUCCIÓN Desde el descubrimiento de la alta especificidad de las reacciones antígeno-anticuerpo (Ag-Ac), muchos investigadores han buscado su aplicación con propósitos de diagnóstico (inmunodiagnóstico). Inicialmente los investigadores se dedicaron a la detección de anticuerpos en el suero del paciente como un signo de infección y así a la identificación serológica del microorganismo. Sin embargo, hoy en día la sensibilidad y especificidad de los inmunoensayos permiten no solo la detección de anticuerpos contra una amplia variedad de organismos infecciosos incluyendo bacterias, parásitos, hongos y virus sino a la identificación del propio microorganismo. Aún más, proporcionan un medio para la detección y cuantificación de antígenos no infecciosos y anticuerpos de importancia clínica tales como la determinación del grupo sanguíneo, el VDRL, la determinación de la proteína C-reactiva, una prueba que señala un proceso inflamatorio agudo, la detección de antígenos asociados a tumores y la demostración de la hormona gonadotropina coriónica, una prueba diagnóstica del embarazo. Independientemente de la variedad de reacciones Ag-Ac usadas in vitro con propósito diagnóstico, hay dos principios que deben ser establecidos: un anticuerpo con especificidad conocida sirve como reactivo para la identificación del antígeno correspondiente y de igual manera un antígeno conocido sirve como reactivo para la identificación del anticuerpo correspondiente. Se ha desarrollado una gran variedad de métodos para demostrar y medir las reacciones antígeno-anticuerpo in vitro. Sin embargo de manera general las técnicas de inmunoensayo pueden dividirse en dos grupos: las que se ven afectadas por la concentración de Ag y Ac en la reacción y las que no se afectan por la concentración. Dentro del primer grupo se encuentran las reacciones de aglutinación y de precipitación. En el segundo se incluyen los ensayos que emplean al complemento, las pruebas de neutralización en las cuales se inhibe alguna propiedad del antígeno o del anticuerpo y especialmente los ensayos que dependen de antígenos o anticuerpos marcados con radioisótopos, con colorantes fluorescentes o con enzimas. Aunque existen técnicas modernas más sensibles las pruebas de aglutinación son muy usadas en muchas disciplinas del laboratorio clínico. La aglutinación es una manifestación secundaria de la reacción antígeno-anticuerpo. En la aglutinación el antígeno y el anticuerpo se unen para formar un agregado macroscópico fácilmente visible. La principal diferencia entre una prueba de precipitación y una de aglutinación es que en precipitación el antígeno es soluble (molecular) mientras que la aglutinación es agregación de partículas o una células. Por esta razón se necesita mucho menos antígeno para obtener una reacción de aglutinación visible que en la precipitación. La aglutinación se puede observar
4 sobre un portaobjetos a simple vista o con el microscopio, otro método es en un tubo de ensaye se puede detectar por la formación de grumos en la suspensión o viendo el patrón de sedimentación en el fondo del tubo. La reacción de aglutinación ocurre en dos etapas, combinación y agregación. La combinación o unión es extremadamente rápida, mientras que la agregación es mucho más lenta, sin embargo la velocidad puede incrementarse por incubación en baño serológico. También es la razón por la cual muchos ensayos incluyen instrucciones de agitar, centrifugar o mezclar frecuentemente. Como se comentó al inicio, el exceso de antígeno o anticuerpo pueden afectar las reacciones de aglutinación al inhibir la formación del agregado, esto se conoce como fenómeno de zona. La formación del agregado es máxima a una concentración óptima de antígenos y anticuerpos, mientras que un exceso de anticuerpos (prozona) o un exceso de antígenos (postzona) pueden causar la inhibición del agregado y por los tanto dar un resultado falsamente negativo a la prueba.
5 PRACTICA N 1 SEGURIDAD EN EL LABORATORIO El conocimiento de las propiedades fisicoquímicas y de la infecto-contagiosidad de los viriones, permite definir las normas que en materia de seguridad, son necesarias para no correr ningún riesgo de adquirir aún en forma accidental, una infección por este tipo de partículas. Con base en lo anterior, se enlistan a continuación los reglamentos y normas que habrán de seguirse en el Laboratorio de Virología, con la finalidad de asegurar la integridad física de los alumnos, así como para mantener una organización adecuada para el desarrollo de las prácticas correspondientes. La hora de entrada tiene 10 minutos de tolerancia, pasado este tiempo, no se permitirá el acceso al laboratorio. Entrar al laboratorio con la bata puesta y abotonada. Colocar todo los artículos personales en la zona lateral o en los cajones de las mesa de trabajo. Al iniciar y finalizar las prácticas, lavarse las manos con agua y jabón desinfectante. Queda estrictamente prohibido comer, beber o fumar en el laboratorio, así como introducir algún objeto en la boca. La puerta del laboratorio debe mantenerse cerrada. Limpiar y desinfectar el área de trabajo antes y después de utilizarla. Permanecer en la zona de trabajo asignada para cada equipo. Comunicarse con sus compañeros solo en la medida indispensable. Antes de iniciar la práctica, leer y recordar la metodología a seguir de acuerdo con las indicaciones del profesor. Si se tienen dudas, es el momento para aclararlas. Informe al profesor de cualquier accidente que ocurra (rotura de material, derramamiento de suspensiones virales, etc.). Todo el material que se va a incubar o desechar, deberá colocarse en el sitio indicado por el profesor. Sea cuidadoso con el material y equipo que se le proporciona; el material de desecho no contaminado deberá depositarse en los contenedores correspondientes. En forma previa a su lavado, siempre se deberá desinfectar el material que se le proporcione en el laboratorio. Rotule todo el material que se va a incubar, con los siguientes datos: grupo, sección, equipo, nombre del alumno, así como fecha de entrada y salida. En general, las disposiciones anteriores tienden al cumplimiento de la Norma Oficial Mexicana NOM-087-ECOL-1995, en la cual se establecen los requisitos para la separación, envasado, almacenamiento, recolección, transporte, tratamiento y disposición final de los Residuos Peligrosos biológico-infecciosos que se generan en establecimientos e instituciones relacionadas con el sector salud. En la NOM referida, se establecen además definiciones de interés para los laboratorios y áreas de microbiología, tales como:
6 Desinfección: Destrucción de microorganismos patógenos en todos los ambientes, materias o partes que pueden ser nocivos, por los distintos medios mecánicos, físicos o químicos contrarios a su vida o desarrollo, con el fin de reducir el riesgo de transmisión de enfermedades. Residuo peligroso biológico-infeccioso: El que contiene bacterias, virus u otros microorganismos con capacidad de causar infección o que contiene o puede contener toxinas producidas por microorganismos que causan efectos nocivos a seres vivos y al ambiente, que se generan en hospitales y establecimientos de atención médica. En adición, se consideran residuos peligrosos biológico-infecciosos los siguientes: La sangre Los cultivos y cepas almacenadas de agentes infecciosos Los cultivos generados en los procedimientos de diagnóstico e investigación, así como los generados en la producción de biológicos Los instrumentos y aparatos para transferir, inocular y mezclar cultivos Las muestras biológicas para análisis químico, microbiológico, citológico e histológico Los residuos anatómicos derivados de la atención a pacientes de los laboratorios Los equipos y dispositivos desechables utilizados para la exploración y toma de muestras Los objetos punzo cortantes usados o sin usar Los que han estado en contacto con pacientes o sus muestras clínicas durante el diagnóstico y tratamiento, incluyendo navajas, lancetas, jeringas, pipetas Pasteur, agujas hipodérmicas, de acupuntura y para tatuaje, bisturíes, cajas de Petri, cristalería entera o rota, porta y cubreobjetos, tubos de ensayo y similares. Con base en lo anterior, los residuos peligrosos infecto-contagiosos, deberán ser tratados por métodos físicos o químicos, los cuales: Deberán garantizar la eliminación de microorganismos patógenos Deberán volver irreconocibles a los residuos peligrosos biológico-infecciosos Deberán ser cremados, si se trata de residuos patológicos. El cumplimiento de las consideraciones señaladas con anterioridad, garantiza la seguridad que deberá observarse tanto para alcanzar los objetivos de las prácticas, como para su desarrollo en condiciones asépticas. Finalmente y dada la especificidad de especie que presentan los virus, en esta primera sesión de laboratorio se hará énfasis en que a través de las diferentes prácticas, se utilizarán únicamente suspensiones virales de tipo vacunal destinadas para uso veterinario, con la finalidad de evitar el más mínimo riesgo de infección hacia los estudiantes. CUESTIONARIO 1. Con ayuda de un esquema especifique, cuál sería el manejo que se la daría a materiales como jeringas, portaobjetos, pipetas, tubos y material con residuos de tejidos, desde que han sido utilizados para el análisis de la sangre hasta su destino final.
7 PRACTICA N 2 TOMA DE MUESTRA Obtención de Muestra de Sangre. Para efectuar análisis serológicos, las muestras de sangre pueden ser de sangre capilar o periférica y de sangre venosa. Sangre capilar o periférica. La sangre capilar o periférica es la que fluye después de aplicar una punción superficial cutánea. Se puede obtener de la yema del dedo. Algunas pruebas pueden realizarse con sangre capilar o periférica y se aconseja cuando no es posible obtener una muestra de sangre venosa o no se desea puncionar la vena. Sangre venosa. Esta muestra se obtiene por punción de una de las tres venas del pliegue del codo: la basílica, la cefálica o la mediana cubital. Se emplean jeringas desechables con agujas de tipo 21x32, 20x32 o el sistema para la extracción de sangre intravenosa al vacío Vacuntainer. Previamente se realiza la limpieza del área elegida con torunda y alcohol. Antes de puncionar se coloca el torniquete aproximadamente a 8 cm de distancia arriba del pliegue del codo. No debe olvidar soltarlo tan pronto empiece a obtenerse la muestra. La cantidad máxima de sangre a extraer será estrictamente la necesaria para las pruebas. Anticoagulantes. Los anticoagulantes más usados son el citrato de sodio, oxalato de sodio y EDTA. El citrato de sodio se emplea al 3.8% y el oxalato de sodio al 1.4%. Se usan en relación de una parte de anticoagulante por cada nueve partes de sangre, habitualmente se usan 0.25ml de la solución para completar a 2.5ml de volumen total con la muestra de sangre. El EDTA (ácido etilen-diamino-tetra-acético) se utiliza al 10% y es uno de los anticoagulantes de elección para el trabajo de rutina. Manejo y conservación de la muestra. La muestra debe rotularse correctamente y separase según el caso en plasma o suero, y dependiendo del tipo de análisis debe analizarse inmediatamente o puede conservarse adecuadamente refrigerada entre 4 y 8ºC para el análisis posterior.
8 PRACTICA N 3 DILUCIONES Se les llama diluciones a las soluciones con concentración menor obtenidas al agregar volúmenes conocidos de diluyente a una solución de concentración conocida. Las diluciones se expresan en forma de una proporción, por ejemplo 1/10 (1:10) donde la primera cifra o numerador (1) corresponde al volumen de lo que se está diluyendo y la segunda cifra o denominador (10) al volumen total en que se encuentra. Así, una dilución 1/10 indica que se tiene un volumen de la solución original contenido o diluido en 10 volúmenes totales, de los cuales 9 corresponden al diluyente. Dado que en una dilución lo que se indica es la relación entre el volumen de la solución original y el volumen total en que se encuentra, una dilución 1/10 puede prepararse de diferentes maneras: Por ejemplo: 1 ml de muestra en 9 ml de diluyente 0.1 ml de muestra en 0.9 ml de diluyente 0.5 ml de muestra en 4.5 ml de diluyente En la práctica el cálculo de las diluciones se puede efectuar de dos maneras diferentes que cumplen ciertas expectativas, la dilución directa y la dilución en serie. Dilución directa. Para realizar una dilución directa se puede hacer uso de la siguiente expresión: 1/d=Vm/Vt donde 1/d= dilución Vm= volumen de muestra Vt= volumen total (volumen de diluyente + volumen de muestra) Ejemplo N 1 Lleve 5 ml de muestra a una dilución 1/10. Sustituyendo los valores conocidos tenemos: 1/d=1/10 Vm=5 ml Vt=? Así: 1/10=5 ml/vt despejando Vt tenemos que Vt=10 x 5/1=50 ml volumen de diluyente = volumen total-volumen de muestra volumen de muestra = 50-5 = 45 ml Ejemplo N 2 Prepare exactamente 200 ml de una dilución 1/50.
9 Sustituyendo los valores conocidos tenemos: 1/d=1/50 Vm=? Vt= 200 ml Así: 1/50=Vm/200 despejando Vm tenemos que Vm=200 x 1/50=4 ml volumen de diluyente = volumen total-volumen de muestra volumen de diluyente = 200-4=196 ml Sin embargo, las diluciones directas tienen el inconveniente de que cuando es necesario hacer una dilución alta por ejemplo 1/ , se desperdicia mucho reactivo o se incurre en un error de medición. Así, una dilución 1/ se prepararía con 1 ml de muestra y ml de diluyente o bien ml de diluyente y ml de muestra. Dilución seriada Este tipo de dilución soluciona los inconvenientes que presenta el calculo directo de las diluciones altas. Además, en microbiología permite el calculo de la población microbiana en la muestra de estudio, de la cual se toma una alícuota que se diluye en varios tubos y se siembra por vertido en placa. La diferencia entre la dilución de dos tubos consecutivo se conoce como factor de dilución, siendo 2, 4 y 10 los más usados. En el ejemplo de la dilución 1/ , la muestra se puede diluir 1/ 100 ( Vm= 0.1 ml + Vt= 10 ml) en un primer tubo y colocar 0.1 ml de esta dilución en un segundo tubo con 9.9 de diluyente. El segundo tubo tendrá una dilución 1/ 100, sin embargo como la muestra ya se encuentra diluída previamente 1/ 100, multiplicando sus denominadores tenemos: 1/ 100 x 1/ 100= 1/ En este caso el factor de dilución es de 100. Debe insistirse en que solo el primer tubo lleva la alícuota de la muestra sin diluir, los demás tubos toman la alícuota ya diluida del tubo previo. El número de tubos y las diluciones intermedias se plantean considerando el volumen de los tubos así como el volumen mínimo que se puede medir fácil y exactamente con las pipetas disponibles. Cómo lograr exactamente 30 ml de una dilución 1:2000?
10 PRACTICA N 4 OBSERVACION DE LEUCOCITOS (CUENTA DIFERENCIAL) Los cinco principales tipos de leucocitos son los neutrófilos (50-70%), los eosinófilos (1-5%), basófilos ( %), linfocitos (20-30%), y monocitos (2 6%). Por cuenta diferencial se entiende la determinación del porcentaje relativo de cada tipo de leucocito en una muestra de sangre. Se realiza en extendidos (frotis) preparados cuidadosamente y teñidos con colorantes tales como Wright, el cual tiñe el núcleo de los leucocitos de un color púrpura que facilita la diferenciación. MATERIAL Y EQUIPO Portaobjetos Lancetas desechables Algodón Colorante de Wright Solución reguladora ph 6.4 Microscopio PROCEDIMIENTO 1. A partir de la muestra de sangre preparar 2 extendidos (frotis) siguiendo las indicaciones del instructor. 2. Dejar secar completamente los frotis, colocar en un puente de tinción y cubrirlos (contar el número de gotas) con colorante de Wright. Dejar el colorante 1 minuto y añadir el mismo número de gotas de solución reguladora ph 6.4 durante 8 minutos. 3. Lavar suavemente la preparación por 30 segundos y secar el exceso de agua. 4. Cuando la preparación esté completamente seca, colocar una gota de aceite de inmersión y observar al microscopio. 5. Para facilitar la identificación consultar las láminas a color que ilustran los diferentes leucocitos.
11 PRACTICA N 5 DETERMINACIÓN DEL GRUPO SANGUÍNEO Alrededor de 1900 Karl Landsteiner descubrió que en el humano existen cuatro tipos de sangres con respecto a la presencia o ausencia de dos antígenos específicos denominados A y B. Estos cuatro grupos se conocen actualmente como tipos A, B, AB y O. Este último se caracteriza por la ausencia de los antígenos A y B. En 1940 Landsteiner y Wiener reportaron que el suero de conejo producido contra eritrocitos de mono Rhesus podía aglutinar los eritrocitos del 85% de una población caucásica. Este antígeno se designó inicialmente como factor Rh, posteriormente se encontró que existe como seis antígenos a los cuales Fisher y Race designaron con letras C, D, E, c, d, e. Uno de estos antígenos, el D es responsable de la condición Rh positivo. La tipificación de eritrocitos en el laboratorio se realiza con antisueros específicos contra los antígenos A, B y D, y puede realizarse por métodos en tubo o en portaobjetos. OBJETIVO Demostrar por medio de una reacción de aglutinación la presencia de los Ag eritrocitarios A, B y D. MATERIALES Y EQUIPO 1. Muestras de sangre con anticoagulante 2. Pipetas graduadas de 1 y 5 ml 3. Tubos de ensayo de 10 X 75 mm 4. Solución salina isotónica 5. Lancetas desechable 6. Aplicadores de madera o palillos 7. Sueros tipificadores anti-a anti-b anti-d (Rh) 8. Placa oscilatoria PROCEDIMIENTO Método en tubo 1. Se obtiene aproximadamente 5 ml de sangre venosa y se colocan en un tubo con EDTA (0.1 ml de EDTA al 1% por cada ml de sangre). Se centrífuga por 2 min. a 2000 r.p.m. para separar el plasma del paquete celular. 2. Se toman 0.1 ml del paquete celular y se resuspenden en 1.9 ml de solución salina para una suspensión aproximada del 5%. 3. Se marcan tres tubos de la siguiente manera: anti-a, anti-b y anti-d, y se agrega una gota del suero tipificador según corresponda. 4. Se agregan 4 gotas de la suspensión de eritrocitos a cada tubo y se agitan suavemente. 5. Los tubos se centrifugan 1 min a 2000 r.p.m.
12 6. Se busca la presencia de aglutinación agitando suavemente los tubos. La aglutinación se reconoce por la formación de grumos. 7. Si la prueba en el tubo anti-d es negativa se realiza el siguiente procedimiento. 8. Se incuba a 37 C por 30 minutos, se centrífuga y se busca la aglutinación. 9. Si persiste la negatividad se lavan los eritrocitos 3 veces con 0.5 ml de solución salina y se elimina perfectamente el sobrenadante. 10. Se agrega una gota del suero de Coombs y se agita suavemente, se centrífuga y se busca la aglutinación Interpretación: Si aglutina en el paso 6 es Rh positivo Si aglutina en el paso 10 es D u Si persiste la negatividad es Rh negativo. Método en portaobjetos 1. Depositar 2 gotas de sangre en tres diferentes divisiones de un portaobjetos. 2. Agregar de izquierda a derecha una gota del antisuero anti-a, una gota de anti-b y una gota de anti-d respectivamente. 3. Mezclar los reactivos con un aplicador de madera diferente para cada gota. 4. Agitar suavemente en la placa oscilatoria. 5. Buscar la presencia de aglutinación. CUESTIONARIO 1. Cuál es la estructura química de los Ag A y B? 2. Elabore una tabla que muestre los Ag, Ac, fenotipo y genotipo de los grupos sanguíneos del sistema ABO y Rh. 3. Puede una persona de grupo A y una B tener como descendencia a un hijo de grupo O? Explique
13 PRACTICA N 7 DETERMINACIÓN DEL TITULO DE ANTICUERPOS ABO DEL SUERO. El sistema de grupo sanguíneo ABO posee una característica única; la presencia de anticuerpos fuertemente reactivos en el suero de los que carecen de los antígenos correspondientes. Estos anticuerpos pertenecen a la clase IgM y son producidos en respuesta a una inmunización. Se dice que estos anticuerpos se producen de manera natural en base a que los inmunógenos son probablemente de origen bacteriano, dado que algunas bacterias presentan sustancias similares a los antígenos A o B. El título es una medida relativa de anticuerpos o antígenos en una reacción serológica. Se determina realizando a partir del suero problema diluciones seriadas. El título del anticuerpos A o B del suero se reporta como el recíproco de la máxima dilución en la cual es posible observar eritrocitos aglutinados. OBJETIVO Establecer a través de diluciones seriadas el concepto de título aplicado en las reacciones serológicas MATERIAL Suspensión de eritrocitos de grupo A o B al 5 % en SSI Suero (plasma) de grupo O Pipetas graduadas de 1 y 5 ml Tubos de ensayo de 10 X 75 mm Solución salina isotónica Lancetas desechable Aplicadores de madera o palillos Sueros tipificadores anti-a anti-b PROCEDIMIENTO 1. Colocar en una gradilla una serie de 6 tubos rotulados del 1 al 6 y se agregar 0.1 ml de solución salina cada uno de ellos. 2. Agregar 0.1 ml del suero problema al tubo n 1, mezclar bien y transferir 0.1 ml al tubo n 2 y así sucesivamente hasta el tubo n 6 del cual se desechan 0.1 ml. 3. Agregar 4 gotas de la suspensión de eritrocitos a cada tubo y mezclar. 4. Incubar a 37 C por 15 minutos, mezclan suavemente y centrifugar a 1000 r.p.m. durante 1 minuto. 5. Desprender el botón suavemente y buscar la presencia de aglutinación.
14 INTERPRETACIÓN 1. El título de anticuerpos en el suero problema se determina como el recíproco de la dilución máxima en la que se observa aglutinación. 2. Además de la aglutinación se puede observar hemólisis, por lo que se debe comprobar la presencia de hemoglobina libre CUESTIONARIO 1. Cuál es la dilución en cada uno de los tubos? 2. Explique porqué puede variar el título de Ac. en la muestra para cada equipo 3. Existen los Ac anti-o naturales
15 PRACTICA N 8 PRUEBAS CRUZADAS El objetivo de una transfusión es el proporcionar al paciente (receptor) el tipo preciso de sangre. Por supuesto este objetivo es difícil de lograr, pero es posible aproximarse mucho si se realizan las pruebas correctas de hemaglutinación. En primer lugar, deben determinarse con exactitud los anfígenos de los grupos sanguíneos principales: el grupo ABO y el Rh del paciente, sobre la base de estos grupos se selecciona la unidad de sangre de grupo ABO y Rh compatible y se procede a efectuar las denominadas pruebas cruzadas mayor y menor. La prueba cruzada mayor, denominada prueba de compatibilidad, se realiza mezclando el suero del receptor con los eritrocitos del donador. Si se produce hemaglutinación, esta sangre no puede darse al receptor porque tiene anticuerpos capaces de reaccionar y destruir la sangre administrada. En la prueba cruzada menor, los eritrocitos del receptor son incubados con suero del donador y se observa si hay aglutinación. Si se produce hemaglutinación, la sangre del donador no debe administrase. En ambas pruebas una suspensión de los eritrocitos respectivos se mezclan con el suero y la mezcla se incuba a 37 C durante unos minutos. Después del periodo de incubación los eritrocitos se lavan para eliminar los anticuerpos que no se han fijado a los eritrocitos, y se añade el reactivo de Coombs (anti-globulina). MATERIAL Y EQUIPO Muestras de sangre con y sin anticoagulante Pipetas graduadas de 1 ml y 5 ml 8 tubos de ensaye de 10 X 75 mm solución salina isotónica. Baño serológico Centrífuga Solución de albúmina bovina al 10% PROCEDIMIENTO 1. Se obtiene una muestra de sangre del donador y receptor y se procede igual a lo descrito en los incisos 1 y 2 de la práctica anterior. 2. Se disponen 4 tubos etiquetados como sigue: PM/S =Prueba Mayor en solución salina pm/s =Prueba Menor en solución salina PM/A =Prueba Mayor en albúmina pm/a =Prueba Menor en albúmina 3. Se agregan a cada tubo los siguientes reactivos en el orden indicado: PM/S. pm/s. 2 gotas del suero del receptor + 4 gotas de eritrocitos (al 5%) del donador 2 gotas del suero del donador + 4 gotas de eritrocitos (al 5%) del receptor
16 PM/A. 2 gotas del suero del receptor + 4 gotas de albúmina + 1 gota de eritrocitos (al 5%) del donador pm/a. 2 gotas del suero del donador + 4 gotas de albúmina + 1 gota de eritrocitos (al 5%) del receptor 4. Se mezclan bien y se incuban a 37 C por 30 minutos. 5. Se centrifugan 1 minuto a 2000 r.p.m. y se busca la presencia de aglutinación. 6. En caso de que no se presente la aglutinación, los tubos se centrifugan nuevamente y se descarta el sobrenadante. Se lava el paquete celular de cada tubo con 1 ml de solución salina y se centrifuga nuevamente descartando el sobrenadante. Repetir el lavado 2 veces. 7. Al paquete celular se le agrega un agota del suero de Coombs y se busca la presencia de hemaglutinación. Interpretación: Si hay aglutinación en cualquiera de los tubos, será indicativo de que hay incompatibilidad entre el posible donador y el receptor (paciente). Si no la hay, las sangres son compatibles. CUESTIONARIO. 1.- Qué significa una prueba cruzada positiva y una negativa? 2.- Qué nos indica la prueba mayor y menor? 3.- Qué factores pueden interferir en los resultados de una prueba cruzada? 4.- Qué características debe tener un donador sanguíneo ideal?
17 PRACTICA N 9 REACCIONES FEBRILES (DIAGNÓSTICO SEROLÓGICO DE INFECCIÓNES BACTERIANAS) La aglutinación de células bacterianas con antisueros es una de las pruebas serológicas mas antiguas de la inmunología práctica. Se inició como un método para el diagnóstico de la infecciones bacterianas y fue propuesta por Widal en La pruebas de aglutinación bacteriana tienen dos aplicaciones principales en el diagnóstico ; las células bacterianas desconocidas pueden identificarse por medio de anticuerpos conocidos, o bien utilizando bacterias conocidas pueden identificarse los anticuerpos en el suero del paciente. La identificación bacteriológica completa del agente patógeno es un proceso que lleva tiempo (3 o más días), mientras se intenta el reconocimiento del agente es posible la identificación serológica. En la aglutinación de los antígenos bacterianos con sus anticuerpos portaobjetos produce un agregado macroscópico. MATERIAL Y EQUIPO 1. Muestras de sueros 2. Placa de vidrio marcada en 6 cuadros 3. Pipetas graduadas de 1 y 0.2 ml 4. Pipeta Pasteur 5. Placa oscilatoria 6. Equipo con antígenos: O de Salmonella typhi H de Salmonella typhi H de Salmonella enteritidis paratyphi A H de Salmonella enteritidis paratyphi B Brucella abortus Proteus OX-19 PROCEDIMIENTO 1. En una placa de vidrio perfectamente limpia se depositan 0.08 ml del suero problema en cada una de las seis divisiones. 2. Se agrega una gota de cada antígeno comenzando por la izquierda arriba, respetando el orden establecido. 3. Se mezclan las gotas con palillos diferentes y se agita suavemente en la placa de rotación durante dos minutos. 4. La lectura se hace observando la aglutinación macroscópica. 5. Si aparece aglutinación con alguno de los antígenos, continuar con el siguiente paso. 6. Se toma otra placa y se depositan 0.08, 0.04, 0.02, 0.01, y ml del suero problema. 7. Se agrega una gota del antígeno seleccionado, se mezclan con un palillo y se revisa la presencia de aglutinación.
18 INTERPRETACIÓN: 1. Los volúmenes de suero empleados corresponden respectivamente a diluciones 1/20, 1/40, 1/80, 1/160 y 1/ El titulo de anticuerpos del suero problema se reporta como el recíproco de la máxima dilución que muestra aglutinación. 3. La mayoría de los títulos mayores de 160 son presuntivos de infección. 4. La mejor indicación de una infección activa es un aumento en el título de dos determinaciones sucesivas con una diferencia de 5-7 días concomitantes a la infección. CUESTIONARIO 1. Qué enfermedades producen los agentes microbianos revisados? 2. Qué significado tiene el demostrar la presencia de Ac en el suero del paciente 3. Cuál es la razón de utilizar una suspensión de Proteus OX-19 para el diagnóstico de tifo?
19 PRACTICA N 11 FACTOR REUMATOIDE Y PROTEINA C REACTIVA Los factores reumatoides son anticuerpos dirigidos contra los determinantes antigénicos de la región Fc de las IgG. En personas sanas, estos anticuerpos pueden hallarse en baja concentración, sin embargo se encuentra aumentado en la mayoría de los pacientes con artritis reumatoide. La determinación del factor reumatoide se lleva a cabo con partículas de latex cubiertas de IgG. La Proteína C Reactiva forma parte de las proteínas de fase aguda, un conjunto de proteínas del suero cuya concentración aumenta de manera drástica durante el daño tisular, la infección o el estrés. No es específica de una enfermedad sino que es un indicador del proceso inflamatorio. MATERIAL Y EQUIPO 1. Muestras de sueros 2. Placa de vidrio oscuro marcada 3. Pipetas graduadas de 1 y 0.2 ml 4. Aplicadores de madera o palillos 5. Pipeta Pasteur 6. Reactivo de latex-fr 7. Reactivo de latex- Proteína C Reactiva 8. Solución amortiguadora de glicina-cloruro de sodio ph Solución salina isotónica 10. Placa rotatoria PROCEDIMIENTO Factor Reumatoiden (FR). Por el método de aglutinación en latex en placa, utiliza una suspensión estabilizada de partículas de latex sensibilizadas con IgG humana. 1. El suero se inactiva previamente calentando en baño serológico a 56 C por 15 min o 60 C por 1 min. Ya inactivado se diluye 1:20 con amortiguador de glicina-cloruro de sodio colocando 0.1 ml de suero y 1.9 ml del amortiguador. 2. Se coloca una gota de la dilución en la placa de vidrio oscura y se añade una gota del reactivo latex-fr. 3. Se mezcla y se agita suavemente en la placa rotatoria durante dos minutos. 4. Se busca la aglutinación macroscópica. 5. La prueba semicuantitativa utiliza diluciones del suero 1/20, 1/40, 1/80, 1/160, 1/320 y 1/640, las cuales se preparan con 0.5 ml de la dilución 1/20 en 0.5 ml del amortiguador para una dilución 1/40 y así consecutivamente. Proteína C Reactiva (PCR). Por el método de aglutinación en latex en placa. Utiliza una suspensión acuosa de partículas de latex recubiertas de anticuerpos específicos anti- Proteína C Reactiva.
20 1. El suero problema se diluye 1/5, 1/40 con solución salina isotónica y se coloca una gota de la dilución en una placa de vidrio oscuro. 2. Se añade una gota del reactivo latex-pcr se mezcla bien y se agita suavemente en la placa rotatoria por 3 min. 3. Se busca la aglutinación macroscópica. 4. La prueba semicuantitativa utiliza diluciones del suero a partir de 1/80. CUESTIONARIO 1. Por qué se inactiva el suero? 2. Explique el fundamento de cada una de las pruebas 3. Explique el significado clínico de una prueba FR positiva y el de una PCR positiva
21 PRACTICA N 12 DETERMINACIÓN DE ANTIESTREPTOLISINAS O (ASO) Las estreptolisinas son enzimas hemolíticas producidas por la mayoría de los estreptococos del grupo A, destruyen la membrana de los eritrocitos ocasionando la hemólisis. Este producto bacteriano es una de las muchas toxinas extracelulares y enzimas producidas por los estreptococos. En particular, la estreptolisina O recibe este nombre debido a que sensible al oxígeno, solo posee actividad en estado reducido, razón por la cual se le incorpora un reductor (el hidrosulfito de sodio) inmediatamente antes de usarla. En el laboratorio las ASO pueden determinarse por una reacción serológica de neutralización, en la cual si el suero del paciente contiene anticuerpos contra la enzima (antiestreptolisinas) neutralizarán su capacidad hemolítica y ocurrirá inhibición de la hemólisis. MATERIAL Y EQUIPO Muestras de suero Suspensión de eritrocitos al 5% Amortiguador para ASO (fosfatos ph 6.5) Estreptolisina O Baño serológico Centrífuga Pipetas graduadas de 1 ml y 5 ml 15 tubos de ensaye de 10 X 75 mm PROCEDIMIENTO 1. Preparar a partir del suero problema las siguientes diluciones iniciales: a) 1:10 con 0.2 ml del suero problema ml de solución amortiguadora b) 1:100 con 0.3 ml de la dilución 1: ml de solución amortiguadora c) 1:500 con 0.6 ml de la dilución 1: ml de solución amortiguadora 2. Rotular los tubos de ensaye con números del 1 al 12 y dos más como control (+) y control (-). 3. Preparar diluciones secundarias añadiendo primero el volumen de solución amortiguadora y posteriormente el volumen del suero diluido según se indica a continuación: Tubos N (+) (-) ml amortiguador Dilución 1:10 1:100 1:500 ml suero diluido Unidades Todd
22 4. Mezclar suavemente y añadir a cada tubo 0.25 ml de estreptolisina, EXCEPTO al tubo control (-). 5. Mezclar por agitación e incubar a 37 C por 15 min. 6. Añadir a cada tubo 0.25 ml de una suspensión de eritrocitos al 5%., mezclar e incubar a 37 C por 30 min. 7. Centrifugar los tubos a 2500 rpm por 2 min. 8. Comprobar la presencia de hemólisis completa en el tubo control (+) y la ausencia de hemólisis en el tubo control (-) 9. Determinar el título de antiestreptolisinas (unidades Todd) como el de la máxima dilución que no presenta hemólisis.
23 PRACTICA N 14 DETERMINACIÓN DE LA GONADOTROPINA CORIONICA HUMANA Las pruebas de laboratorio para el diagnóstico del embarazo se basan en la determinación de la gonadotropina coriónica humana (hgc), hormona producida por la placenta y que puede detectarse tanto en el suero como en la orina. La excreción de hgc alcanza su máximo durante la duodécima a decimocuarta semana de gestación y a partir de entonces desciende de nivel. Hasta los años 60, las pruebas de embarazo eran bioensayos en los cuales la presencia de la hgc en el suero o en la orina se demostraba por su efecto en animales. Las primeras pruebas utilizaban ratones y conejos, las pruebas ulteriores ratas hembra o ranas. Actualmente estas pruebas han sido sustituidas por pruebas inmunológicas. Las pruebas inmunológicas dependen del anticuerpo anti-hgc. La presencia de hgc en el suero u orina se demuestra por un sistema indicador. Los ensayo de aglutinación denominadas de inhibición de la aglutinación consisten de eritrocitos de conejo o partículas de látex recubiertas con hgc. Cuando se realiza la prueba, el suero u orina de la paciente se incuban con el anticuerpo. Si existe hgc en la muestra, el anticuerpo es inactivado y los eritrocitos o partículas de látex no aglutinan. Si la muestra no contiene hgc, el anticuerpo permanece activo y se produce la aglutinación. Además de la aglutinación, existen otras técnicas inmunológicas para la determinación de la hgc, tales como los inmunoensayos enzimáticos (ELISA) y el radioinmunoanálisis (RIA), el cual requiere de equipo especial para su realización. Esta técnicas varían en su sensibilidad, esto es las pruebas inmunológicas son, más sensibles al detectar concentraciones menores de hgc, por ejemplo las pruebas con eritrocitos tienden a ser más sensibles que la que emplean partículas de látex. MATERIAL Orina del Paciente (10 ml) Solución salina isotónica (SSI) Equipo de diagnostico de hgc Pipetas serológicas de 1 ml PROCEDIMIENTO 1. Se filtran unos 5 ml de orina o se centrifuga a 3000 r.p.m. 5 minutos para precipitar el material insoluble. Se usa el filtrado o el liquido sobrenadante 2. Se diluye un volumen de orina en dos volúmenes de solución salina, por ejemplo 0.5 ml de orina y 1.0 ml de solución salina. 3. Se colocan en el tubo apropiado 0.25 ml de antisuero anti-hgc, se agregan 0.25 ml de la orina diluida y se agita suavemente. 4. Se agrega una gota de la suspensión de eritrocitos sensibilizados y se agita suavemente hasta lograr una suspensión homogénea.
24 5. Se coloca en una superficie libre de vibraciones o del calor. De preferencia en una gradilla con el espejo adecuado. 6. Efectuar la lectura 2 horas después. RECOMENDACIONES 1. Los residuos de orinas anteriores falsearan la prueba. 2. Tubos diferentes a los apropiados distorsionan la lectura 3. No deben mezclarse los goteros o tocar con ellos los tubos de ensayo. 4. Los reactivos deben agregarse en el orden establecido. INTERPRETACION Para la lectura se interpretan los esquemas celulares en el fondo del tubo de ensayo Prueba positiva = un botón claramente definido Prueba negativa = un tapiz difuso de células PRUEBA NEGATIVA PRUEBA POSITIVA
25 BIBLIOGRAFÍA 1. REGUEIRO JOSE R. Y LOPEZ LARREA CARLOS INMUNOLOGIA BIOLOGÍA Y PATOLOGÍA DEL SISTEMA INMUNE. 2ª EDICIÓN. EDITORIAL MÉDICA PANAMERICANA. 2. JANEWAY, CHARLES A. Y TRAVERS PAUL IMMUNOBIOLOGY THE IMMUNE SYSTEM IN HEALTH AND DISEASE. 2ª EDICIÓN. CURRENT BIOLOGY-GARLAND. 3. ROITT, IVAN ESSENTIAL IMMUNOLOGY. 8ª EDICIÓN. BLACKWELL SCIENTIFIC PUBLICATIONS. 4. ROITT, IVAN IMUNOLOGIA FUNDAMENTOS. 9ª EDICIÓN. PANAMERICANA. 5. ROITT, IVAN. BROSTOFF JONATHAN Y MALE DAVID IMMUNOLOGY 4ª EDICIÓN. MOSBY. 6. ROITT, IVAN. BROSTOFF JONATHAN Y MALE DAVID INMUNOLOGIA 5ª EDICIÓN. EDICIONES HARCOURT. ESPAÑA 7. ABBAS, A. K. LICHTMAN A. H. Y POBER J. S INMUNOLOGÍA CELULAR Y MOLECULAR. 3ª EDICIÓN. INTERAMERICANA- McGRAW- HILL.
Inmunohematología. Dra. Ana Cecilia Haro
 Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO
 PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
Tipificación de Grupos Sanguineos e Isohemaglutininas
 Tipificación de Grupos Sanguineos e Isohemaglutininas Introducción Los eritrocitos expresan antígenos de membrana. Dichos antígenos se encuentran determinados genéticamente y pueden ser identificados mediante
Tipificación de Grupos Sanguineos e Isohemaglutininas Introducción Los eritrocitos expresan antígenos de membrana. Dichos antígenos se encuentran determinados genéticamente y pueden ser identificados mediante
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS
 PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS
 Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS La prueba a realizar depende de las características del Ag SOLUBLE PRECIPITACIÓN PARTICULADO AGLUTINACIÓN SUPERFICIE + COMPLEMENTO FIJACIÓN
Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS La prueba a realizar depende de las características del Ag SOLUBLE PRECIPITACIÓN PARTICULADO AGLUTINACIÓN SUPERFICIE + COMPLEMENTO FIJACIÓN
CONTROL DE CALIDAD PREANALITICO
 CONTROL DE CALIDAD PREANALITICO TOMA DE MUESTRA LAS FASES DE CONTROL DE CALIDAD SON; PREANALITICO ANALITICO POST ANALITICO CONTROL PREANALITICO *SON TODAS LAS ESPECIFICACIONES QUE SE DEBEN CONSIDERAR,
CONTROL DE CALIDAD PREANALITICO TOMA DE MUESTRA LAS FASES DE CONTROL DE CALIDAD SON; PREANALITICO ANALITICO POST ANALITICO CONTROL PREANALITICO *SON TODAS LAS ESPECIFICACIONES QUE SE DEBEN CONSIDERAR,
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente
 Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
LIMPIEZA Y DESINFECCION
 PAGINA: 1 de 7 1. DEFINICION: Es el procedimiento, mediante el cual son eliminados los diferentes desechos generados en los procesos de recolección y procesamiento de muestras; y además se describe el
PAGINA: 1 de 7 1. DEFINICION: Es el procedimiento, mediante el cual son eliminados los diferentes desechos generados en los procesos de recolección y procesamiento de muestras; y además se describe el
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Trabajo Práctico N 3. Reconocimiento de sustancias ácidas, básicas y neutras. mediante el empleo de indicadores químicos.
 Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
DETECCIÓN, CARACTERIZACIÓN Y TITULACIÓN DE ISOHEMAGLUTININAS
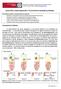 Área de Inmunología. Prácticas de Inmunología Clínica Autor: Gonzalo Rubio Pedraza grubio@um.es DETECCIÓN, CARACTERIZACIÓN Y TITULACIÓN DE ISOHEMAGLUTININAS Al finalizar la práctica, el alumno debe ser
Área de Inmunología. Prácticas de Inmunología Clínica Autor: Gonzalo Rubio Pedraza grubio@um.es DETECCIÓN, CARACTERIZACIÓN Y TITULACIÓN DE ISOHEMAGLUTININAS Al finalizar la práctica, el alumno debe ser
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL
 UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO FACULTAD DE MEDICINA Y NUTRICIÓN Unidad Médica de Simulación Clínica "Dr. José Jorge Talamas Márquez"
 LICENCIATURA EN NUTRICIÓN Practica #10 TOMA DE MUESTRA DE GLUCOSA CAPILAR OBJETIVOS: Al concluir la práctica el alumno será capaz de: 1. Definir y conocer la técnica de toma de muestra de glucosa capilar
LICENCIATURA EN NUTRICIÓN Practica #10 TOMA DE MUESTRA DE GLUCOSA CAPILAR OBJETIVOS: Al concluir la práctica el alumno será capaz de: 1. Definir y conocer la técnica de toma de muestra de glucosa capilar
Residuos Peligrosos Generados en el consultorio médico del TESCHI se utilizará la clasificación RPBI s siguiente:
 Página 1 de 6 1. Propósito Establecer los conocimientos necesarios para establecer los lineamientos acerca del manejo de los residuos peligrosos biológicos infecciosos en el consultorio médico, con el
Página 1 de 6 1. Propósito Establecer los conocimientos necesarios para establecer los lineamientos acerca del manejo de los residuos peligrosos biológicos infecciosos en el consultorio médico, con el
RESIDUOS CITOTOXICOS. Farm. Andrea Imhoff Hospital Dr. O. Alassia
 RESIDUOS CITOTOXICOS Farm. Andrea Imhoff Hospital Dr. O. Alassia RESIDUOS CITOTOXICOS Son aquellos que por sus características y grado de contaminación química o biológica requieren un tratamiento específico
RESIDUOS CITOTOXICOS Farm. Andrea Imhoff Hospital Dr. O. Alassia RESIDUOS CITOTOXICOS Son aquellos que por sus características y grado de contaminación química o biológica requieren un tratamiento específico
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA
 PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS PROGRAMAS DE DEPORTE Y FISIOTERAPIA GUIA PRÁCTICA N 6
 Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
Asignatura: Procesamiento De Lácteos AG Ing. Elvis Cruz
 Universidad Nacional Autónoma De Honduras Centro Universitario Regional Del Centro UNAH-CURC Departamento De Agroindustria Ingeniería Agroindustrial Asignatura: Procesamiento De Lácteos AG - 422 Ing. Elvis
Universidad Nacional Autónoma De Honduras Centro Universitario Regional Del Centro UNAH-CURC Departamento De Agroindustria Ingeniería Agroindustrial Asignatura: Procesamiento De Lácteos AG - 422 Ing. Elvis
Grupo sanguíneo Antígenos en glóbulos rojos Anticuerpos en el plasma. A A anti-b B B anti-a AB A + B O anti-a y anti-b
 TEMA 6.- LOS GRUPOS SANGUÍNEOS. PROBLEMAS DE GENÉTICA. LOS GRUPOS SANGUÍNEOS Los grupos sanguíneos fueron descubiertos en 1900 por el doctor austriaco Karl Landsteiner. Las transfusiones sanguíneas se
TEMA 6.- LOS GRUPOS SANGUÍNEOS. PROBLEMAS DE GENÉTICA. LOS GRUPOS SANGUÍNEOS Los grupos sanguíneos fueron descubiertos en 1900 por el doctor austriaco Karl Landsteiner. Las transfusiones sanguíneas se
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
GenPE: estudio Internacional de Genética en Preeclampsia
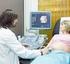 GenPE: estudio Internacional de Genética en Preeclampsia INSTRUCTIVO Toma de muestra proyecto GenPE PAQUETE PARA CAPTACIÓN DE PACIENTE Y TOMA DE MUESTRA. Cuando llegue a su institución la caja del proyecto
GenPE: estudio Internacional de Genética en Preeclampsia INSTRUCTIVO Toma de muestra proyecto GenPE PAQUETE PARA CAPTACIÓN DE PACIENTE Y TOMA DE MUESTRA. Cuando llegue a su institución la caja del proyecto
PRÁCTICO N 3. Técnicas para la observación, aislamiento y conservación de microorganismos
 PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
MANEJO DE RESIDUOS PELIGROSOS BIOLOGICO INFECCIOSOS
 MANEJO DE RESIDUOS PELIGROSOS BIOLOGICO INFECCIOSOS Laboratorio de Análisis Clínicos QFB. MARCO ANTONIO URTIS GARCÍA. En un laboratorio clínico así como en una consultorio médico, la manipulación de substancias
MANEJO DE RESIDUOS PELIGROSOS BIOLOGICO INFECCIOSOS Laboratorio de Análisis Clínicos QFB. MARCO ANTONIO URTIS GARCÍA. En un laboratorio clínico así como en una consultorio médico, la manipulación de substancias
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt
 Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico.
 FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA
 UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA I. TÍTULO Dilución II. OBJETIVOS Repasar el concepto de dilución
UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA I. TÍTULO Dilución II. OBJETIVOS Repasar el concepto de dilución
MANEJO DE SOLUCIONES DESINFECTANTES
 PAGINA: 1 de 8 REVISADO: ELABORADO: COORDINADOR DE CALIDAD 1. DEFINICION ENFERMERO JEFE COORDINADOR CIRUGIA Las soluciones desinfectantes son sustancias que actúan sobre los microorganismos inactivándolos
PAGINA: 1 de 8 REVISADO: ELABORADO: COORDINADOR DE CALIDAD 1. DEFINICION ENFERMERO JEFE COORDINADOR CIRUGIA Las soluciones desinfectantes son sustancias que actúan sobre los microorganismos inactivándolos
REACCIONES ANTÍGENO ANTICUERPO
 REACCIONES ANTÍGENO ANTICUERPO CONCEPTO DE ANTÍGENO Características de los determinantes antigénicos Concepto Inmunopotencia Inmunodominancia Determinantes inmunogénicos y hapténicos Inmunogenicidad: Carácter
REACCIONES ANTÍGENO ANTICUERPO CONCEPTO DE ANTÍGENO Características de los determinantes antigénicos Concepto Inmunopotencia Inmunodominancia Determinantes inmunogénicos y hapténicos Inmunogenicidad: Carácter
TEST RESIDUOS SANITARIOS
 1) LOS RESIDUOS SANITARIOS SE CLASIFICAN, EN FUNCIÓN DE LOS RIESGOS, EN: a) 4 grupos: 0I, II, III y IV. b) 3 grupos: 0I, II y III. c) 2 grupos: 0I y II. d) Ninguna es correcta. 2) NO SE INCLUYE EN EL GRUPO
1) LOS RESIDUOS SANITARIOS SE CLASIFICAN, EN FUNCIÓN DE LOS RIESGOS, EN: a) 4 grupos: 0I, II, III y IV. b) 3 grupos: 0I, II y III. c) 2 grupos: 0I y II. d) Ninguna es correcta. 2) NO SE INCLUYE EN EL GRUPO
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS
 HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
Guía para el docente
 Guía para el docente Descripción curricular: - Nivel: 4.º Medio - Subsector: Biología - Unidad temática: Biología humana y salud Rechazo inmune - Palabras clave: grupos sanguíneos ABO, factor Rh, transfusión
Guía para el docente Descripción curricular: - Nivel: 4.º Medio - Subsector: Biología - Unidad temática: Biología humana y salud Rechazo inmune - Palabras clave: grupos sanguíneos ABO, factor Rh, transfusión
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA
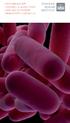 SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
MEDICIÓN DEL VOLUMEN
 MEDICIÓN DEL VOLUMEN CONCEPTOS BÁSICOS Volumen: porción de espacio que ocupa un cuerpo ya sea sólido, líquido o gaseoso. Capacidad: es el volumen de un fluido que puede contener o suministrar un instrumento
MEDICIÓN DEL VOLUMEN CONCEPTOS BÁSICOS Volumen: porción de espacio que ocupa un cuerpo ya sea sólido, líquido o gaseoso. Capacidad: es el volumen de un fluido que puede contener o suministrar un instrumento
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS
 DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
Instructivo Tratamiento de Sustancias y Residuos Peligrosos
 Página 1 de 6 1. Objetivo y alcance El objeto del presente instructivo es establecer la metodología para el tratamiento ambiental de las sustancias y residuos peligrosos generados en las actividades de
Página 1 de 6 1. Objetivo y alcance El objeto del presente instructivo es establecer la metodología para el tratamiento ambiental de las sustancias y residuos peligrosos generados en las actividades de
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
ENFERMEDADES TRANSMITIDAS POR ALIMENTOS
 ENFERMEDADES TRANSMITIDAS POR ALIMENTOS Melany Aguirre Diana Rivera Christopher Delbrey INTRODUCCIÓN En esta presentación estaremos presentando las siguientes enfermedades transmitidas por alimentos: Salmonelosis,
ENFERMEDADES TRANSMITIDAS POR ALIMENTOS Melany Aguirre Diana Rivera Christopher Delbrey INTRODUCCIÓN En esta presentación estaremos presentando las siguientes enfermedades transmitidas por alimentos: Salmonelosis,
2. ESTRATEGIA PARA EFECTUAR LA CLONACION Y EXPRESION DEL GEN
 1. CONTROL FINAL Nombre Internacional y nombre de la vacuna Nombre del propietario Nombre y dirección del fabricante Número de Lote Fecha de fabricación Fecha de caducidad Temperatura de almacenamiento
1. CONTROL FINAL Nombre Internacional y nombre de la vacuna Nombre del propietario Nombre y dirección del fabricante Número de Lote Fecha de fabricación Fecha de caducidad Temperatura de almacenamiento
50 kits de recolección de muestras con torunda multitest Aptima (N.º de catálogo PRD-03546) Cada kit contiene:
 Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
3.- Higiene de manos y Antisepsia cutánea
 Higiene de manos La medida más sencilla y eficaz para reducir la infección asociada a la asistencia sanitaria Transmisión cruzada de microorganismos a través de las manos: Las manos de los profesionales
Higiene de manos La medida más sencilla y eficaz para reducir la infección asociada a la asistencia sanitaria Transmisión cruzada de microorganismos a través de las manos: Las manos de los profesionales
3.9 Imprime los resultados obtenidos y los entrega al personal del área de recepción.
 Código: I-FMED-LAC-10 Revisión: 02 Página: 1 de 5 1.- OBJETIVO Proporcionar información para realizar la Citometría Hemática (BH) 2.- ALCANCE Aplica para todas las muestras referenciadas al laboratorio
Código: I-FMED-LAC-10 Revisión: 02 Página: 1 de 5 1.- OBJETIVO Proporcionar información para realizar la Citometría Hemática (BH) 2.- ALCANCE Aplica para todas las muestras referenciadas al laboratorio
CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E
 CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E 221 07 1. OBJETO 1.1 Esta norma tiene por objeto establecer el método para determinar el porcentaje de partículas livianas en los agregados
CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E 221 07 1. OBJETO 1.1 Esta norma tiene por objeto establecer el método para determinar el porcentaje de partículas livianas en los agregados
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
El término de tejido sanguíneo es un tejido conectivo altamente especializado, cuya matriz extracelular es liquida y se denomina plasma
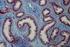 Trabajo Práctico N o 10: Tejido sanguíneo Nombre... Comisión... Objetivos 1. Identificar en microscopio óptico los elementos del tejido sanguíneo 2. Observar cristales de hemoglobina 3. Comprender los
Trabajo Práctico N o 10: Tejido sanguíneo Nombre... Comisión... Objetivos 1. Identificar en microscopio óptico los elementos del tejido sanguíneo 2. Observar cristales de hemoglobina 3. Comprender los
Agentes Biológicos. Médico Carlos A. Contreras Quevedo Mestría en ciencias especialidad en salud ocupacional.
 Agentes Biológicos Médico Carlos A. Contreras Quevedo Mestría en ciencias especialidad en salud ocupacional. Introducción. En el medio sanitario el riesgo biológico es el que más frecuentemente encontramos,
Agentes Biológicos Médico Carlos A. Contreras Quevedo Mestría en ciencias especialidad en salud ocupacional. Introducción. En el medio sanitario el riesgo biológico es el que más frecuentemente encontramos,
Fortel PROSTATE (PSA)
 Fortel PROSTATE (PSA) Test para Screening Simple, realizable y confidencial [Seleccione la fecha] Un test visual fácil, para detectar niveles anormales del Antígeno Prostático Específico (PSA), sobre rango
Fortel PROSTATE (PSA) Test para Screening Simple, realizable y confidencial [Seleccione la fecha] Un test visual fácil, para detectar niveles anormales del Antígeno Prostático Específico (PSA), sobre rango
Composición Líquido Elementos formes
 Composición Líquido Elementos formes Plasma Glóbulos blancos Glóbulos rojos Plaquetas Transporte de sustancias Homeostasis de los líquidos l corporales Protección TRANSPORTE O 2 desde los pulmones a los
Composición Líquido Elementos formes Plasma Glóbulos blancos Glóbulos rojos Plaquetas Transporte de sustancias Homeostasis de los líquidos l corporales Protección TRANSPORTE O 2 desde los pulmones a los
LABORATORIO: MICROBIOLOGÍA BIOQUÍMICA Y HEMATOLOGÍA.
 LABORATORIO: MICROBIOLOGÍA BIOQUÍMICA Y HEMATOLOGÍA. CS Illes Columbretes Página 1 En el laboratorio de microbiología se realizan investigaciones microbiológicas (diagnóstico bacteriológico, micológico,
LABORATORIO: MICROBIOLOGÍA BIOQUÍMICA Y HEMATOLOGÍA. CS Illes Columbretes Página 1 En el laboratorio de microbiología se realizan investigaciones microbiológicas (diagnóstico bacteriológico, micológico,
PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013
 PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013 Este programa de control externo permite verificar el desempeño de los procesos en el área de Inmunohematología, evalúa los reactivos utilizados
PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013 Este programa de control externo permite verificar el desempeño de los procesos en el área de Inmunohematología, evalúa los reactivos utilizados
Capítulo II: Aspectos clínicos y Organización de los servicios para la atención del dengue
 Capítulo II: Aspectos clínicos y Organización de los servicios para la atención del dengue Tema 3 : Organización de los servicios para la atención del dengue Contenido: La Organización de los servicios
Capítulo II: Aspectos clínicos y Organización de los servicios para la atención del dengue Tema 3 : Organización de los servicios para la atención del dengue Contenido: La Organización de los servicios
SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor
 CAJA DE SALUD DE LA BANCA PRIVADA www.csbp.com.bo REGIONAL Cochabamba SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor N RL-06/13 N RL-06/13 Cochabamba 5 de Agosto de
CAJA DE SALUD DE LA BANCA PRIVADA www.csbp.com.bo REGIONAL Cochabamba SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor N RL-06/13 N RL-06/13 Cochabamba 5 de Agosto de
Aplicación a escala de laboratorio
 Aplicación a escala de laboratorio Índice de contenidos Velcorin Aplicación a escala de laboratorio págs. 3 5 Introducción pág. 3 Medidas de precaución pág. 3 Método de trabajo (sensorial) pág. 4 Método
Aplicación a escala de laboratorio Índice de contenidos Velcorin Aplicación a escala de laboratorio págs. 3 5 Introducción pág. 3 Medidas de precaución pág. 3 Método de trabajo (sensorial) pág. 4 Método
Sistema Integrado de Gestión. Titulación ácido-base. Determinación del contenido de ácido acético en el vinagre
 Sistema Integrado de Gestión Titulación ácido-base. Determinación del contenido de ácido acético en el vinagre Versión 3 Proceso: Investigación IV Febrero de 2016 Página 2 de 9 1. OBJETIVOS Ilustrar los
Sistema Integrado de Gestión Titulación ácido-base. Determinación del contenido de ácido acético en el vinagre Versión 3 Proceso: Investigación IV Febrero de 2016 Página 2 de 9 1. OBJETIVOS Ilustrar los
PRACTICA No.9 REACCIONES QUIMICAS I
 PRACTICA No.9 REACCIONES QUIMICAS I INTRODUCCION: Las transformaciones de la materia se conocen como REACCIONES QUIMICAS. En ellas se opera un cambio en la estructura íntima de las sustancias reaccionantes
PRACTICA No.9 REACCIONES QUIMICAS I INTRODUCCION: Las transformaciones de la materia se conocen como REACCIONES QUIMICAS. En ellas se opera un cambio en la estructura íntima de las sustancias reaccionantes
PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL
 PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL Determinación del contenido de humedad Determinación gravimétrica del contenido de sólidos insolubles en agua Conductividad eléctrica Determinación del
PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL Determinación del contenido de humedad Determinación gravimétrica del contenido de sólidos insolubles en agua Conductividad eléctrica Determinación del
Seguridad en Laboratorios. Valeria Matamala Avila Prevencionista de Riesgos
 Seguridad en Laboratorios Valeria Matamala Avila Prevencionista de Riesgos Riesgos en Laboratorios Incendio Derrame Contacto con sustancias peligrosas Inhalación Intoxicación Como disminuir estos riesgos?
Seguridad en Laboratorios Valeria Matamala Avila Prevencionista de Riesgos Riesgos en Laboratorios Incendio Derrame Contacto con sustancias peligrosas Inhalación Intoxicación Como disminuir estos riesgos?
Determinación de Sólidos Disueltos Totales en Aguas
 QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Sólidos Disueltos en Aguas Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 22/09/2013 Método Gravimétrico Página 2 de 7
QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Sólidos Disueltos en Aguas Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 22/09/2013 Método Gravimétrico Página 2 de 7
FACULTAD DE MEDICINA DE SEVILLA. PRACTICAS DE MICROBIOLOGÍA MÉDICA. SEGUNDO CICLO.
 FACULTAD DE MEDICINA DE SEVILLA. PRACTICAS DE MICROBIOLOGÍA MÉDICA. SEGUNDO CICLO. - DIAGNÓSTICO DIRECTO DE LAS ENFERMEDADES INFECCIOSAS DE ETIOLOGÍA FÚNGICA. - DIAGNOSTICO INDIRECTO DE LAS ENFERMEDADES
FACULTAD DE MEDICINA DE SEVILLA. PRACTICAS DE MICROBIOLOGÍA MÉDICA. SEGUNDO CICLO. - DIAGNÓSTICO DIRECTO DE LAS ENFERMEDADES INFECCIOSAS DE ETIOLOGÍA FÚNGICA. - DIAGNOSTICO INDIRECTO DE LAS ENFERMEDADES
Erradicación de la Tuberculosis Bovina en España Santander, 29 y 30 de junio de 2010
 Jornadas de Debate: MINISTERIO DE MEDIO AMBIENTE Y MEDIO RURAL Y MARINO Erradicación de la Tuberculosis Bovina en España Santander, 29 y 30 de junio de 2010 El diagnóstico de laboratorio y las nuevas herramientas
Jornadas de Debate: MINISTERIO DE MEDIO AMBIENTE Y MEDIO RURAL Y MARINO Erradicación de la Tuberculosis Bovina en España Santander, 29 y 30 de junio de 2010 El diagnóstico de laboratorio y las nuevas herramientas
INTERPRETACIÓN NORMA OHSAS 18001:2007 MÓDULO 1 SESIÓN 1 INTERPRETACIÓN DE LA NORMA OHSAS 18001:2007 DOCENTE: Ing. Dª. Ana I.
 INTERPRETACIÓN NORMA OHSAS 18001:2007 MÓDULO 1 SESIÓN 1 INTERPRETACIÓN DE LA NORMA OHSAS 18001:2007 DOCENTE: Ing. Dª. Ana I. Menac Lumbreras Especializados 1 TEMA 1 Contenidos INTRODUCCIÓN A LA NORMA OHSAS
INTERPRETACIÓN NORMA OHSAS 18001:2007 MÓDULO 1 SESIÓN 1 INTERPRETACIÓN DE LA NORMA OHSAS 18001:2007 DOCENTE: Ing. Dª. Ana I. Menac Lumbreras Especializados 1 TEMA 1 Contenidos INTRODUCCIÓN A LA NORMA OHSAS
Con esta pregunta se desea conocer la cantidad y tipo de residuos peligrosos, que son recolectados en los establecimientos de salud.
 BLOQUE 15 RESIDUOS PELIGROSOS EN ESTABLECIMIENTOS DE SALUD RESIDUOS PELIGROSOS EN ESTABLECIMIENTOS DE SALUD.- Son los residuos generados en establecimientos de salud que tienen propiedades peligrosas y
BLOQUE 15 RESIDUOS PELIGROSOS EN ESTABLECIMIENTOS DE SALUD RESIDUOS PELIGROSOS EN ESTABLECIMIENTOS DE SALUD.- Son los residuos generados en establecimientos de salud que tienen propiedades peligrosas y
PET-RPLA KIT para DETECCIÓN de TOXINAS. Código: TD0930
 PET-RPLA KIT para DETECCIÓN de TOXINAS Código: TD0930 Kit para detección de enterotoxina tipo A de Clostridium perfringens en muestras fecales o en filtrados de cultivos por aglutinación pasiva de látex
PET-RPLA KIT para DETECCIÓN de TOXINAS Código: TD0930 Kit para detección de enterotoxina tipo A de Clostridium perfringens en muestras fecales o en filtrados de cultivos por aglutinación pasiva de látex
TÍTULO: Determinación colorimétrica de fenoles en agua por el método de la 4- aminoantipirina
 Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Manual para la disposición final de desechos o material bio-infeccioso. Servicios Médicos
 Manual para la disposición final de desechos o material bio-infeccioso Servicios Médicos Los desechos peligrosos generados en centros de salud requieren de un manejo especial para evitar la transmisión
Manual para la disposición final de desechos o material bio-infeccioso Servicios Médicos Los desechos peligrosos generados en centros de salud requieren de un manejo especial para evitar la transmisión
Mat. Natalia Torres D.Educadora Roche Diabetes Care
 Mat. Natalia Torres D.Educadora Roche Diabetes Care Objetivos Definir Glicemia capilar Identificar los objetivos del control de glicemia capilar Conocer la historia toma de muestra de glicemia capilar
Mat. Natalia Torres D.Educadora Roche Diabetes Care Objetivos Definir Glicemia capilar Identificar los objetivos del control de glicemia capilar Conocer la historia toma de muestra de glicemia capilar
Anemias en Pediatría Diagnóstico, interpretación del hemograma
 Anemias en Pediatría Diagnóstico, interpretación del hemograma Dra. Marcela Gutiérrez Médica Pediatra Hematóloga Hospital de Niños Ricardo Gutiérrez Buenos Aires Técnica de recolección: recursos para su
Anemias en Pediatría Diagnóstico, interpretación del hemograma Dra. Marcela Gutiérrez Médica Pediatra Hematóloga Hospital de Niños Ricardo Gutiérrez Buenos Aires Técnica de recolección: recursos para su
Conservantes y técnicas de Bioconservación como alternativas más saludables
 Conservantes y técnicas de Bioconservación como alternativas más saludables Dra. María José Grande Burgos Área de Microbiología Dpto. de Ciencias de la Salud Universidad de Jaén Qué es un alimento? Es
Conservantes y técnicas de Bioconservación como alternativas más saludables Dra. María José Grande Burgos Área de Microbiología Dpto. de Ciencias de la Salud Universidad de Jaén Qué es un alimento? Es
Protocolo de toma de muestra arterial MANUAL DE CALIDAD LABORATORIO CLÍNICO. PRO 08 D Ed 01 Protocolo extracción arterial
 MANUAL DE CALIDAD LABORATORIO CLÍNICO Protocolo de toma de muestra arterial Código Fecha emisión/última revisión Revisado Aprobado PRO 08 D Ed 01 18/11/09 Spsor. Rafael Infantes Viano Dr. Vidal Pérez Valero.
MANUAL DE CALIDAD LABORATORIO CLÍNICO Protocolo de toma de muestra arterial Código Fecha emisión/última revisión Revisado Aprobado PRO 08 D Ed 01 18/11/09 Spsor. Rafael Infantes Viano Dr. Vidal Pérez Valero.
INDICACIONES PARA LA HIGIENE DE MANOS
 Medicina Preventiva y Salud Pública H.C.U.V. Actualizado 2010 INDICACIONES PARA LA HIGIENE DE MANOS Debe realizarse higiene de las manos por parte del personal sanitario en las siguientes situaciones A.
Medicina Preventiva y Salud Pública H.C.U.V. Actualizado 2010 INDICACIONES PARA LA HIGIENE DE MANOS Debe realizarse higiene de las manos por parte del personal sanitario en las siguientes situaciones A.
Métodos para la determinación de grasas
 Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
Propuesta de un programa de gestión de la información y comunicación del riesgo químico
 Propuesta de un programa de gestión de la información y comunicación del riesgo químico Póster. XII Congreso Nacional de Seguridad y Salud en el Trabajo. Valencia 20-23 de noviembre de 2001. Mª José Berenguer
Propuesta de un programa de gestión de la información y comunicación del riesgo químico Póster. XII Congreso Nacional de Seguridad y Salud en el Trabajo. Valencia 20-23 de noviembre de 2001. Mª José Berenguer
CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS
 CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS DIAGNOSTICO POR LABORATORIO DEL VIRUS DEL OESTE DEL NILO Participantes José Carmen Gudiño Rita Flores
CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS DIAGNOSTICO POR LABORATORIO DEL VIRUS DEL OESTE DEL NILO Participantes José Carmen Gudiño Rita Flores
Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia
 Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia LABORATORIO NACIONAL DE BACTERIOLOGIA DIAGNOSTICO DE LABORATORIO EN LA VIGILANCIA DE LEPTOSPIROSIS EN LA RED NACIONAL DE LABORATORIOS
Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia LABORATORIO NACIONAL DE BACTERIOLOGIA DIAGNOSTICO DE LABORATORIO EN LA VIGILANCIA DE LEPTOSPIROSIS EN LA RED NACIONAL DE LABORATORIOS
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA. Gotas Óticas. Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g.
 DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
Métodos para la cuantificación de nitrógeno y proteína
 Practica 5 Métodos para la cuantificación de nitrógeno y proteína Antecedentes Para la determinación de proteínas en muestras de alimentos se cuenta con una gran variedad de métodos, basados en diferentes
Practica 5 Métodos para la cuantificación de nitrógeno y proteína Antecedentes Para la determinación de proteínas en muestras de alimentos se cuenta con una gran variedad de métodos, basados en diferentes
RIESGOS DERIVADOS DE LA INCORRECTA CLASIFICACIÓN
 1. Riesgo de pinchazo o corte Situación 1: Deshacer elementos punzantes y cortantes en contenedores no destinados a tal fin. Ejemplo: Desechar un elemento cortante o punzante en contenedores de 30 y 60
1. Riesgo de pinchazo o corte Situación 1: Deshacer elementos punzantes y cortantes en contenedores no destinados a tal fin. Ejemplo: Desechar un elemento cortante o punzante en contenedores de 30 y 60
CAPÍTULO III CRITERIOS, PROCESOS SERVICIOS Y RESULTADOS
 23 CAPÍTULO III CRITERIOS, PROCESOS SERVICIOS Y RESULTADOS A. Criterios de inclusión de donadores Los donadores deben cumplir con los requisitos establecidos en el anexo 2 formato 2, también deben cumplir
23 CAPÍTULO III CRITERIOS, PROCESOS SERVICIOS Y RESULTADOS A. Criterios de inclusión de donadores Los donadores deben cumplir con los requisitos establecidos en el anexo 2 formato 2, también deben cumplir
Pruebas de compatibilidad, qué técnica emplear?
 Pruebas de compatibilidad, qué técnica emplear? XIV Jornadas de Medicina Transfusional Dra. Carmen Buesa García Sº Hematología y Hemoterapia Hospital Universitario Central de Asturias Pruebas pretransfusionales
Pruebas de compatibilidad, qué técnica emplear? XIV Jornadas de Medicina Transfusional Dra. Carmen Buesa García Sº Hematología y Hemoterapia Hospital Universitario Central de Asturias Pruebas pretransfusionales
PRÁCTICA 1: Funcionamiento laboratorio. Normas y material
 PRÁCTICA 1: Funcionamiento laboratorio. Normas y material OBJETIVO: 1. Familiarizarse con el uso y manejo de todo el material del laboratorio, así como con las normas para un buen funcionamiento del mismo.
PRÁCTICA 1: Funcionamiento laboratorio. Normas y material OBJETIVO: 1. Familiarizarse con el uso y manejo de todo el material del laboratorio, así como con las normas para un buen funcionamiento del mismo.
ESPECIFICACIÓN DE LOS ÍTEMES DE PRUEBA
 Técnicas de Panadería Alimentación Química ESPECIFICACIÓN DE LOS ÍTEMES DE PRUEBA Aprendizaje Esperado Establecer relaciones cuantitativas en diversas reacciones químicas 1. Juan, debe diseñar un programa
Técnicas de Panadería Alimentación Química ESPECIFICACIÓN DE LOS ÍTEMES DE PRUEBA Aprendizaje Esperado Establecer relaciones cuantitativas en diversas reacciones químicas 1. Juan, debe diseñar un programa
PREPARACIÓN DE MEDIOS DE CULTIVO
 Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
ANALISIS DE COMUNIDAD: EXTRACCION Y DERIVATIZACION DE ACIDOS GRASOS TOTALES
 CUARTA PARTE ANALISIS DE CMUNIDAD: EXTRACCIN Y DERIVATIZACIN DE ACIDS GRASS TTALES PERFILES DE ACIDS GRASS derivados de los fosfolípidos de membranas celulares de microorganismos pueden ser utilizados
CUARTA PARTE ANALISIS DE CMUNIDAD: EXTRACCIN Y DERIVATIZACIN DE ACIDS GRASS TTALES PERFILES DE ACIDS GRASS derivados de los fosfolípidos de membranas celulares de microorganismos pueden ser utilizados
Influencia de la evaluación de los efectos de residuos en flora intestinal sobre el IDA de una droga
 Influencia de la evaluación de los efectos de residuos en flora intestinal sobre el IDA de una droga A. Haydée Fernández, DVM, MS, DABT 25 de Septiembre de 2010 Cartagena de Indias, Colombia Como se calcula
Influencia de la evaluación de los efectos de residuos en flora intestinal sobre el IDA de una droga A. Haydée Fernández, DVM, MS, DABT 25 de Septiembre de 2010 Cartagena de Indias, Colombia Como se calcula
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS PROGRAMAS DE DEPORTE Y FISIOTERAPIA GUIA PRÁCTICA N 6
 Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROGRAMAS DE DEPORTE Y Versión 5 Proceso: Investigación - IV Febrero de 2016 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROGRAMAS DE DEPORTE Y Versión 5 Proceso: Investigación - IV Febrero de 2016 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de
Prestación de Servicio Laboratorio de Microbiología
 1 Prestación de Servicio de Página 1 de 7 1. Objetivo y Alcance: Prestar el servicio en los laboratorios de microbiología y apoyo a la docencia, que contribuya a la formación académica de los estudiantes
1 Prestación de Servicio de Página 1 de 7 1. Objetivo y Alcance: Prestar el servicio en los laboratorios de microbiología y apoyo a la docencia, que contribuya a la formación académica de los estudiantes
DETERMINACIÓN DE LA DEMANDA QUÍMICA DE OXÍGENO, DQO, TOTAL EN UNA MUESTRA DE AGUA RESIDUAL DOMÉSTICA
 EXPERIMENTO 4 DETERMINACIÓN DE LA DEMANDA QUÍMICA DE OXÍGENO, DQO, TOTAL EN UNA MUESTRA DE AGUA RESIDUAL DOMÉSTICA Objetivo general Determinación de Demanda Química de Oxígeno total (DQO) en una muestra
EXPERIMENTO 4 DETERMINACIÓN DE LA DEMANDA QUÍMICA DE OXÍGENO, DQO, TOTAL EN UNA MUESTRA DE AGUA RESIDUAL DOMÉSTICA Objetivo general Determinación de Demanda Química de Oxígeno total (DQO) en una muestra
3. REQUERIMIENTOS. El estudiante debe tener conocimientos básicos de: - Química General - Laboratorio de Química General 4. OBJETIVOS.
 1. IDENTIFICACIÓN Materia: LABORATORIO DE QUIMICA ANALITICA Códigos: SIRE: 6102 EIQ: IQ-5064 Prelación: IQ-5023 - IQ-5032 Ubicación: Cuarto Semestre TPLU: 0-0-3-1 Condición: Obligatoria Departamento: Química
1. IDENTIFICACIÓN Materia: LABORATORIO DE QUIMICA ANALITICA Códigos: SIRE: 6102 EIQ: IQ-5064 Prelación: IQ-5023 - IQ-5032 Ubicación: Cuarto Semestre TPLU: 0-0-3-1 Condición: Obligatoria Departamento: Química
El sistema inmune y las vacunas
 SESIÓN DE INFORMACIÓN SOBRE VACUNAS, Santiago, Chile 7 de mayo 9 mayo, 2014 El sistema inmune y las vacunas Dra. Juanita Zamorano R Pediatra- Infectóloga jzamorano@uandes.cl 1 Jenner: En 1796 inicia la
SESIÓN DE INFORMACIÓN SOBRE VACUNAS, Santiago, Chile 7 de mayo 9 mayo, 2014 El sistema inmune y las vacunas Dra. Juanita Zamorano R Pediatra- Infectóloga jzamorano@uandes.cl 1 Jenner: En 1796 inicia la
PRÁCTICA Nº 7 SOLUCIONES AMORTIGUADORAS Y CURVAS DE TITULACIÓN
 PRÁCTICA Nº 7 SOLUCIONES AMORTIGUADORAS Y CURVAS DE TITULACIÓN OBJETIVOS Demostrar que el ph de una solución amortiguadora no depende de la concentración de sus componentes. Comprobar las propiedades de
PRÁCTICA Nº 7 SOLUCIONES AMORTIGUADORAS Y CURVAS DE TITULACIÓN OBJETIVOS Demostrar que el ph de una solución amortiguadora no depende de la concentración de sus componentes. Comprobar las propiedades de
Procedimiento RETIRO DE RESIDUOS PELIGROSOS
 Nombre archivo:.doc 1 de 7 Procedimiento RETIRO DE RESIDUOS PELIGROSOS UNIDAD DE PREVENCIÓN DE RIESGOS Diciembre de 2012. Preparado por: Revisado y aprobado por: UPR Mauricio Larco A. 2 de 7 Tabla de contenido
Nombre archivo:.doc 1 de 7 Procedimiento RETIRO DE RESIDUOS PELIGROSOS UNIDAD DE PREVENCIÓN DE RIESGOS Diciembre de 2012. Preparado por: Revisado y aprobado por: UPR Mauricio Larco A. 2 de 7 Tabla de contenido
UNIVERSIDAD JUÁREZ AUTÓNOMA DE TABASCO
 UNIVERSIDAD JUÁREZ AUTÓNOMA DE TABASCO DIVISIÓN ACADÉMICA DE CIENCIAS BIOLÓGICAS LICENCIATURA EN BIOLOGÍA ASIGNATURA: LABORATORIO DE HISTOLOGÍA ANIMAL ÁREA DE FORMACION: SUSTANTIVA PROFESIONAL HORAS TEÓRICAS:
UNIVERSIDAD JUÁREZ AUTÓNOMA DE TABASCO DIVISIÓN ACADÉMICA DE CIENCIAS BIOLÓGICAS LICENCIATURA EN BIOLOGÍA ASIGNATURA: LABORATORIO DE HISTOLOGÍA ANIMAL ÁREA DE FORMACION: SUSTANTIVA PROFESIONAL HORAS TEÓRICAS:
CUIDADOS DE HERIDAS QUIRÚRGICAS
 DIRECCION DE CUIDADOS DE HERIDAS QUIRÚRGICAS AUTORES Ultima actualización Alba Mª Álvarez González Enero 2011 REVISORES Comisión Cuidados Enfermería Mayo 2012 AUTORIZADO Dirección de Enfermería Mayo 2012
DIRECCION DE CUIDADOS DE HERIDAS QUIRÚRGICAS AUTORES Ultima actualización Alba Mª Álvarez González Enero 2011 REVISORES Comisión Cuidados Enfermería Mayo 2012 AUTORIZADO Dirección de Enfermería Mayo 2012
DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4
 Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
URGENCIAS. Servicio de Microbiología
 URGENCIAS Servicio de Microbiología Peticiones urgentes al Servicio de Microbiología 1 I. Consideraciones generales La guardia para las urgencias microbiológicas tiene varios objetivos: 1) Asistencial
URGENCIAS Servicio de Microbiología Peticiones urgentes al Servicio de Microbiología 1 I. Consideraciones generales La guardia para las urgencias microbiológicas tiene varios objetivos: 1) Asistencial
Capítulo 30. Productos farmacéuticos
 Capítulo 30 Productos farmacéuticos Notas. 1. Este Capítulo no comprende: a) los alimentos dietéticos, alimentos enriquecidos, alimentos para diabéticos, complementos alimenticios, bebidas tónicas y el
Capítulo 30 Productos farmacéuticos Notas. 1. Este Capítulo no comprende: a) los alimentos dietéticos, alimentos enriquecidos, alimentos para diabéticos, complementos alimenticios, bebidas tónicas y el
