Estereoisomerismo en los alfaaminoácidos.
|
|
|
- Mario Murillo Aguilera
- hace 8 años
- Vistas:
Transcripción
1 Estructura general de un aminoácido. Esta estructura es común a todos los alfaaminoácidos, con una única excepción. (La excepción es la prolina, un aminoácido cíclico). El grupo R o cadenal lateral (en rojo) unido al carbono α (alfa) (en azul) es diferente para cada aminoácido. Se usan dos convenciones para identificar a los carbonos dentro de un aminoácido. Los carbonos adicionales de un grupo R se designan comúnmente β (beta), γ (gamma), δ (delta), ε (epsilon), empezando a partir del carbono α (alfa). Para la mayoría de las demás moléculas orgánicas, los átomos de carbono se numeran simplemente a partir de un extremo, dando la máxima prioridad a los carbonos con sustituciones que contengan átomos de mayor número atómico. Siguiendo esta última convención, el grupo carboxilo de un aminoácido sería el C-1 y el carbono alfa sería el C-2. Estereoisomerismo en los alfaaminoácidos. a)los dos estereoisómeros de la alanina, la L- y la D-alanina, son imágenes especulares no superponibles entre sí (enantiómeros). b) Los enlaces con forma de cuña se proyectan fuera del plano del papel; los enlaces a trazos lo hacen por detrás. c) Se supone que los enlaces horizontales se proyectan fuera del plano del papel, los enlaces verticales por detrás. No obstante, se utilizan a menudo las fórmulas de proyección de una forma descuidada sin pretender representar una configuración estereoquímica específica.
2 Asimetría Molecular: moléculas quirales y aquérales. a) Cuando un átomo de carbono tiene cuatro sustituyentes diferentes (A,B,X,Y), éstos pueden disponerse de dos maneras diferentes, que dan lugar a dos moléculas no superponibles, siendo cada una de ellas la imagen especular de la otra (enantiómeros). Estos átomos de carbono son asimétricos y se denominan átomos quirales o centros quirales. b) Cuando alrededor del átomo de carbono tetraédrico se disponen únicamente tres sustituyentes diferentes (es decir, hay dos sustituyentes iguales), solamente es posible una configuración espacial y la molécula es simétrica o aquiral. En este caso la molécula puede superimponerse a su imagen especular: aquí, la molécula de la izquierda, rotando en sentido contrario a las agujas del reloj (cuando se mira hacia abajo por el eje vertical que une A y C), da lugar a la molécula del espejo. Relación estérica de los estereoisómeros de la alanina con la configuración absoluta del L- y D-gliceraldehído. En estas fórmulas de perspectiva los carbonos están alineados verticalmente con el átomo quiral en el centro. Los carbonos de estas moléculas están numerados empezando con los carbonos aldehído o carboxilo en el extremo (en rojo), 1 a 3 de arriba abajo tal como se muestra. Cuando se presentan de esta forma, el grupo R del aminoácido (en este caso el grupo metilo de la alanina) está siempre debajo del carbono alfa. Los L-aminoácidos son los que tienen el grupo alfa-amino a la izquierda y los D-aminoácidos los que tienen el grupo alfa-amino a la derecha.
3 Aminoácidos APOLARES, con cadenas laterales alifáticas. (También Phe y Trp.) Aminoácidos POLARES, sin carga. MUY IMPORTANTE, existe un error!. El aminoácido PROLINA que aparece en este última clasificación dentro de los aminoácidos polares sin carga, tiene como cadena lateral una cadena alifática (sombreada en rosa) y es por tanto apolar, por lo que debería aparecer en el recuadro de arriba.
4 Aminoácidos AROMÁTICOS con cadenas laterales (o grupos R) aromáticos. Aminoácidos BÁSICOS con cadenas laterales cargadas positivamente. Aminoácidos ÁCIDOS con cadenas laterales cargadas negativamente.
5 Los 20 aminoácidos estándar de las proteínas. Las fórmulas estructurales muestran el estado de ionización que predomina a ph 7.0 Las partes no sombreadas son comunes para todos los aminoácidos; las partes sombreadas en color son los grupos R. Aunque el grupo R de la histidina se muestra sin carga, su pka es tal que una fracción pequeña pero significativa de estos grupos está cargada positivamente a ph 7.0
6 Absorbancia de la luz ultravioleta por los aminoácidos aromáticos. Espectros de absorción de luz de los aminoácidos aromáticos triptófano y tirosina a ph 6,0. Los aminoácidos están presentes en cantidades equimolares (10-3 M) en idénticas condiciones. La absorción de la luz por el triptófano es cuatro veces mayor que la de la tirosina. El máximo de absorbancia para ambos está cercano a 280 nm (nanómetros). La absorción de la luz del tercer aminoácido aromático, la fenilalanina (no mostrado), generalmente contribuye poco a las propiedades de absorbancia de las proteínas. Formación reversible de un puente disulfuro por oxidación de dos moléculas de cisteína. Los puentes disulfuro entre residuos de Cys estabilizan las estructuras de muchas proteínas.
7 Aminoácidos no estándar a) Algunos aminoácidos no estándar encontrados en proteínas. Todos ellos provienen de aminoácidos estándar. Los grupos funcionales extra añadidos a través de reacciones de modificación se muestran en rojo. La desmosina se forma a partir de cuatro residuos de Lys. b) La ornitina y la citrulina, que no se encuentran en las proteínas, son intermediarios en la biosíntesis de arginina y en el ciclo de la urea.
8 Propiedades y convenciones asociadas a los aminoácidos estándar. Nombres abreviados: Normalmente, aunque no en todos los casos, las tres primeras letras del nombre en inglés de cada aminoácido. pk 1 indica el valor de pka del grupo alfa carboxilo. pk 2 indica el valor de pka del grupo alfa amino. pk R indica el valor de pka de la cadena lateral de los aminoácidos cuya cadenal lateral sea ionizable. pi indica el valor del punto isoeléctrico o ph isoeléctrico. Índice hidropático: escala que combina la hidrofobicidad y la hidrofilicidad de las cadenas laterales, se usa para predecir la tendencia de los aminoácidos a buscar un ambiente acuoso (valores negativos) o un ambiente hidrófobo (valores positivos). Presencia en las proteínas (%): Presencia media en unas proteínas estudiadas.
9
10 Curvas de valoración del glutamato (izquierda) y de la lisina (derecha). Glutamato: El valor de pk 1 se corresponde con el pka del grupo alfa-carboxilo (2.19), El valor de pk 2 se corresponde con el pka del grupo carboxilo de la cadena lateral (4.25), El valor de pk 3 se corresponde con el pka del grupo alfa-amino (9.67). El ph isoeléctrico o punto isoeléctrico (pi) será la media aritmética de los valores de pka de los grupos alfa-carboxilo y carboxilo de la cadena lateral (porque en este caso se trata de un aminoácido ácido): pi = ( ) / 2 = 3.22 Lisina: El valor de pk 1 se corresponde con el pka del grupo alfa-carboxilo (2.18), El valor de pk 2 se corresponde con el pka del grupo alfa-amino (8.95), El valor de pk 3 se corresponde con el pka del grupo amino de la cadena lateral (10.53). El ph isoeléctrico o punto isoeléctrico (pi) será la media aritmética de los valores de pka de los grupos alfa-amino y amino de la cadena lateral (porque en este caso de trata de un aminoácido básico): pi = ( ) / 2 = 9.74 Los aminoácidos con un grupo R ionizable (Lys, Arg, His, Asp, Glu, Tyr y Cys), tienen curvas de valoración más complejas que la de la glicina, con tres etapas correspondientes a los tres pasos de ionización posibles; tienen por tanto tres valores de pka. La etapa adicional debida a la valoración del grupo R ionizable se fusiona en cierto grado con las otras dos, tal y como observamos en los aminoácidos aquí expuestos.
11 Formación de un enlace peptídico por condensación. El grupo alfa-amino de un aminoácido (el que tiene el R 2 ), actúa como nucleófilo desplazando el grupo hidroxilo de otro aminoácido (el que tiene el R 1 ) para formar un enlace covalente denominado enlace peptídico (sombreado en gris). Al ser esta reacción energéticamente desfavorable los aminoácidos deben ser activados previamente. Estructura del pentapéptido seril-glicil-tirosinil-alanil-leucina o Ser-Gly-Tyr-Ala-Leu. Los péptidos se nombran empezando por el residuo amino-terminal que, por convención, se sitúa a la izquierda y terminan con el residuo carboxilo-terminal, a la derecha. Los enlaces peptídicos se muestran sombreados en gris y las cadenas laterales en rojo.
12 Ionización y carga eléctrica del péptido Alanil-glutamil-glicil-lisina. Este tetrapéptido tiene un grupo alfa-amino libre, un grupo alfa carboxilo libre y dos cadenas laterales (o grupos R) ionizables. Los grupos ionizados a ph 7.0 se muestran en rojo. Algunos péptidos naturales con intensa actividad biológica. Los residuos amino-terminales están a la izquierda. (a) La bradiquinina es un péptido de tipo hormonal que inhibe las reacciones inflamatorias. (b) Oxitocina, formada por la hipófisis posterior, estimula las contracciones uterinas. (c) factor liberador de la tirotropina (o TSH), formado por el hipotálamo. (d) Dos encefalinas (Metencefalina y Leu-encefalina), péptidos cerebrales que afectan a la percepción del dolor. (e) Gramicidina S, antibiótico producido por la bacteria Bacillus brevis. Las flechas indican la dirección desde el extremo amino al carboxilo de cada residuo. El péptido no tiene final porque es circular. Orn es el símbolo de la ornitina, aminoácido que generalmente no se presenta en las proteínas. Obsérvese que la gramicidina S contiene dos residuos de un D-aminoácido (D-fenilalanina).
13 Propiedades ácido-base
14 Estructura química. a) Modificación de los extremos NH 2 terminal: acetilaciones, aa cíclicos COOH terminal: en forma amida b) Por proteolisis de precursores mayores c) En hongos y bacterias: presencia de estructuras cíclicas y D-aminoácidos a) Ejemplos Ac-NH-SYSMEHFRWGKPV-CONH 2 α-msh (hormona estimulante de los melanocitos) TRH (hormona liberadora de tirotropina) b) PROOPIOMELANOCORTINA SYSMEHFRWGKPVGKKRRPVKVYPDAGEDQSAEAFPLEF (ACTH) SYSMEHFRWGKPV (α-msh) c) γ- MSH β-lipotropina γ-lipotropina β- endorf.
15 Actividad biológica 1) Péptidos vasoactivos A) Vasoconstrictores RENINA ANGIOTENSINASA B) Vasodilatadores ANGIOTENSINOGENO ANGIOTENSINA I ANGIOTENSINA II DRVYIHPFHL DRVYIHPF + HL KALIKREÍNAS QUININÓGENO BRADIQUININA Y KALIDINA RPPGFSPFR KRPPGFSPFR 2) Hormonas OXITOCINA CYIQNCPLG-CO-NH 2 ARGININ-VASOPRESINA (ADH) CYFQNCPRG-CO-NH 2 LISIN-VASOPRESINA (ADH) CYFQNCPKG-CO-NH 2 Otras hormonas: a) hipotlámicas b) hipofisarias c) pancreáticas: insulina, glugagón d) gastrointestinales: gastrina, secretina, colecistoquinina, VIP (péptido intestinal vasoactivo, etc 3) neurotransmisores ENDORFINAS PROTEOLISIS ESPECÍFICA Leu-encefalina Met-encefalina YGGFL YGGFM 4) Antioxidante GLUTATION (γ-glutamil-l-cistenil-glicina) 2GSH + H 2 O 2 GSSG + 2H 2 O
16 Proteínas conjugadas: proteínas que contienen componentes químicos diferentes a los aminoácidos. La parte no aminoácido de una proteína conjugada se denomina frecuentemente grupo prostético.
17 Antes de comenzar la secuenciación se purifica la proteína, y una vez en su estado puro, se rompen los puentes disulfuro si se trata de una proteína que los contiene, de esta forma se obtienen las cadenas polipeptídicas separadas. La secuenciación se lleva a cabo con cada polipéptido por separado. Rotura enzimática del enlace peptídico mediante tripsina, enzima proteolítico.
18 Secuenciación indirecta. Hoy en día la estructura primaria de muchas proteínas se conoce a partir de las secuencias de nucleótidos de los genes que las codifican. Las primeras bases de datos de secuencias de aminoácidos proteicos fueron reunidas basándose en el uso de los métodos de secuenciación química. Hoy en día, la enorme preponderancia de información de las secuencias de proteínas derivan de la traducción de las secuencias de los genes codificadas en los codones y desde ésta la obtención de las secuencias de los aminoácidos proteicos. Secuenciar el orden de los nucléotidos en los genes clonados es un proceso más rápido, eficiente e informativo que la determinación de las secuencias de los aminoácidos proteicos por métodos químicos. El desarrollo de métodos rápidos para la secuenciación del DNA, el descubrimiento del código genético, y el desarrollo de técnicas para el aislamiento de genes, permiten deducir la secuencia de un polipéptido mediante la determinación de la secuencia de nucleótidos del gen que lo codifica. De esta manera se ha llegado a conocer secuencias de muchas proteínas antes de su aislamiento o mera caracterización.
19 Separación de aminoácidos Poliestireno sulfonado ph
20 Mismo genoma Ciclo Vital de la Mariposa Distintas proteínas El huevo La mariposa crisálida La oruga Proteómica Conocer el proteóma de un organismo es tener una imagen dinámica de todas las proteínas expresadas por ese organismo, en un momento dado y bajo determinadas condiciones concretas de tiempo y ambiente Qué función tienen las proteínas?, Qué tipo de modificaciones postraduccionales sufren las proteínas y cuál es su función?, Cómo varían las proteínas de una célula enfrentada a distintas condiciones ambientales?. También es posible entender la proteómica como el conjunto de técnicas que permiten analizar el conjunto de proteínas presentes en la célula en determinado momento, o sea, el proteoma. Estas técnicas incluyen el 2D- PAGE (electroforesis de poliacrilamida de dos dimensiones) y la MS (espectrometría de masas). La manera más fácil de hacer un estudio proteómico es comparar los proteomas de dos condiciones y observar sus diferencias.
21 Electroforésis en dos dimensiones
 Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO
 ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS AMINOÁCIDOS
 ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de
 Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Estructura y propiedades de las proteínas
 Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Isomería estructural o constitucional
 TEMA 7.- Estereoisomería. Isomería: constitucional y estereoisomería. Isomería óptica. Quiralidad y enantiomería. Configuraciones absoluta y relativa. Moléculas con dos o más estereocentros: diastereoisomería
TEMA 7.- Estereoisomería. Isomería: constitucional y estereoisomería. Isomería óptica. Quiralidad y enantiomería. Configuraciones absoluta y relativa. Moléculas con dos o más estereocentros: diastereoisomería
AMINOÁCIDOS Y PÉPTIDOS
 TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
AMINOÁCIDOS y proteínas
 AMINOÁCIDOS y proteínas La Luciferina es una proteína Marijose Artolozaga Sustacha, MSc Las proteínas son las macromoléculas biológicas más abundantes y variadas. Diferentes estructuras y funciones Las
AMINOÁCIDOS y proteínas La Luciferina es una proteína Marijose Artolozaga Sustacha, MSc Las proteínas son las macromoléculas biológicas más abundantes y variadas. Diferentes estructuras y funciones Las
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Glucosa-6-fosfato. La estructura de la derecha es la forma predominante a ph 7.0
 Glucosa-6-fosfato. La estructura de la derecha es la forma predominante a ph 7.0 ph óptimos de algunos enzimas: pepsina, enzima digestivo secretado en el jugo gástrico (negro); tripsina, enzima digestivo
Glucosa-6-fosfato. La estructura de la derecha es la forma predominante a ph 7.0 ph óptimos de algunos enzimas: pepsina, enzima digestivo secretado en el jugo gástrico (negro); tripsina, enzima digestivo
Tema 3. Tema 3. Péptidos.. Enlace Peptídico. Péptidos naturales de interés Biológico. Péptidos. Péptidos
 Tema 3 Tema 3 Péptidos.. Enlace Peptídico. Péptidos naturales de interés Biológico. Péptidos Enlace Peptídico Nomenclatura de péptidos Características estructurales del enlace peptídico Estéreoespecificidad
Tema 3 Tema 3 Péptidos.. Enlace Peptídico. Péptidos naturales de interés Biológico. Péptidos Enlace Peptídico Nomenclatura de péptidos Características estructurales del enlace peptídico Estéreoespecificidad
3. AMINOACIDOS. PROPIEDADES ACIDO-BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
AMINOÁCIDOS SE PUEDEN UNIR POR ENLACES PEPTÍDICOS
 Tema 4. Proteínas: funciones biológicas y estructura primaria. Enlace peptídico. Péptidos y proteínas. Diversidad de funciones biológicas. Niveles de organización estructural de las proteínas. Separación
Tema 4. Proteínas: funciones biológicas y estructura primaria. Enlace peptídico. Péptidos y proteínas. Diversidad de funciones biológicas. Niveles de organización estructural de las proteínas. Separación
AMINOÁCIDOS 3B EXPLIQUE EL COMPORTAMIENTO DEL ACIDO ASPARTICO A UNA SOLUCION CON PH DE 8
 AMINOÁCIDOS 1A EXPLIQUE LOS AMINOACIDOS GLUCOCETOGENICOS Los aminoácidos glucocetogénicos son aquellos que producen acetil-coenzima A que posteriormente ayudara en la formación de lípidos, y los intermediarios
AMINOÁCIDOS 1A EXPLIQUE LOS AMINOACIDOS GLUCOCETOGENICOS Los aminoácidos glucocetogénicos son aquellos que producen acetil-coenzima A que posteriormente ayudara en la formación de lípidos, y los intermediarios
Aminoácidos, péptidos y proteinas
 Aminoácidos, péptidos y proteinas Generalidades sobre los aminoácidos Compuestos que contienen un grupo -NH 2 y un grupo -CO 2 H esos grupos en realidad están presentes como -NH 3+ and -CO 2 respectivamente.
Aminoácidos, péptidos y proteinas Generalidades sobre los aminoácidos Compuestos que contienen un grupo -NH 2 y un grupo -CO 2 H esos grupos en realidad están presentes como -NH 3+ and -CO 2 respectivamente.
Aminoácidos Pi Primera Parte
 Proteínas Aminoácidos Pi Primera Parte 1 Introducción a proteínas Las proteínas están constituidas básicamente por unidades elementales (monómeros) denominadas aminoácidos. Hay 20 aminoácidos diferentes,
Proteínas Aminoácidos Pi Primera Parte 1 Introducción a proteínas Las proteínas están constituidas básicamente por unidades elementales (monómeros) denominadas aminoácidos. Hay 20 aminoácidos diferentes,
2.2- FENOLES. Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH.
 2.2- FENOLES Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH. Si se sustituye un solo átomo de hidrógeno, se obtienen los fenoles; si se sustituyen
2.2- FENOLES Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH. Si se sustituye un solo átomo de hidrógeno, se obtienen los fenoles; si se sustituyen
TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR
 Tema 5 Simetría Molecular 1 TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR La simetría de una molécula determina muchas de sus propiedades e incluso determina cómo se producen algunas reacciones. El estudio
Tema 5 Simetría Molecular 1 TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR La simetría de una molécula determina muchas de sus propiedades e incluso determina cómo se producen algunas reacciones. El estudio
Clasificación de los isómeros:
 ISOMERÍA onsiste en que dos o más compuestos tienen la misma fórmula molecular, pero diferente estructura molecular. En consecuencia poseen diferentes propiedades físicas y químicas. Se denominan isómeros
ISOMERÍA onsiste en que dos o más compuestos tienen la misma fórmula molecular, pero diferente estructura molecular. En consecuencia poseen diferentes propiedades físicas y químicas. Se denominan isómeros
Proteínas. Características generales
 Proteínas Características generales Son las macromoléculas más abundantes en las células. Constituyen hasta el 50% del peso. Forman moléculas específicas en cada especie, incluso entre individuos. Además,
Proteínas Características generales Son las macromoléculas más abundantes en las células. Constituyen hasta el 50% del peso. Forman moléculas específicas en cada especie, incluso entre individuos. Además,
PROTEINAS AMINOACIDOS
 PROTEINAS AMINOACIDOS 1 2 PROTEINAS Las proteínas son las moléculas constituyentes de los seres vivos que, además de ocupar el 50% del peso seco de los tejidos, tienen la máxima importancia por las funciones
PROTEINAS AMINOACIDOS 1 2 PROTEINAS Las proteínas son las moléculas constituyentes de los seres vivos que, además de ocupar el 50% del peso seco de los tejidos, tienen la máxima importancia por las funciones
Clase No.11: Estereoquímica, Isomería óptica y Rotación específica
 Clase No.11: Estereoquímica, Isomería óptica y Rotación específica Departamento de Química Orgánica Facultad de Ciencias Químicas y Farmacia Universidad de San Carlos de Guatemala Quiralidad Porqué no
Clase No.11: Estereoquímica, Isomería óptica y Rotación específica Departamento de Química Orgánica Facultad de Ciencias Químicas y Farmacia Universidad de San Carlos de Guatemala Quiralidad Porqué no
TEMA 5. LAS PROTEÍNAS.
 TEMA 5. LAS PROTEÍNAS. 1.- CARACTERÍSTICAS GENERALES. Son macromoléculas formadas por C, H, O y N. (en algunas ocasiones S). Son importantes porque son las biomoléculas más abundantes en peso seco (50%)
TEMA 5. LAS PROTEÍNAS. 1.- CARACTERÍSTICAS GENERALES. Son macromoléculas formadas por C, H, O y N. (en algunas ocasiones S). Son importantes porque son las biomoléculas más abundantes en peso seco (50%)
MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN
 MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN Propiedades de una proteína que son útiles para su purificación por cromatografía Peso molecular Carga iónica Hidrofobicidad
MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN Propiedades de una proteína que son útiles para su purificación por cromatografía Peso molecular Carga iónica Hidrofobicidad
XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA
 Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 09 Semestre: 16-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 09 Semestre: 16-I Este material es exclusivamente para uso
Contenidos. Introducción general
 Contenidos Introducción general Test Uno: Razonamiento Test Dos: Velocidad de percepción Test Tres: Velocidad y precisión numérica Test Cuatro: Significación verbal Test Cinco: Razonamiento espacial Esta
Contenidos Introducción general Test Uno: Razonamiento Test Dos: Velocidad de percepción Test Tres: Velocidad y precisión numérica Test Cuatro: Significación verbal Test Cinco: Razonamiento espacial Esta
7.012 Serie de ejercicios 1
 ombre Grupo 7.01 Serie de ejercicios 1 Pregunta 1 a) uáles son los 4 tipos principales de moléculas biológicas mencionadas en clase? ite una función importante de cada tipo de molécula biológica celular.
ombre Grupo 7.01 Serie de ejercicios 1 Pregunta 1 a) uáles son los 4 tipos principales de moléculas biológicas mencionadas en clase? ite una función importante de cada tipo de molécula biológica celular.
Qué es un gen? EXPRESION GÉNICA 01/05/2013
 Qué es un gen? Es una secuencia de nucleótidos en la molécula de ADN, equivalente a una unidad de transcripción. Contiene la información, a partir de la cual se sintetiza un polipéptido, una enzima, un
Qué es un gen? Es una secuencia de nucleótidos en la molécula de ADN, equivalente a una unidad de transcripción. Contiene la información, a partir de la cual se sintetiza un polipéptido, una enzima, un
III. Material genético. b. Composición y estructura del RNA.
 III. Material genético b. Composición y estructura del RNA. RNA (ácido ribonucléico) Polímero de nucleótidos La pentosa de los nucleótidos es la Ribosa: en la posición 2' del anillo del azúcar hay un grupo
III. Material genético b. Composición y estructura del RNA. RNA (ácido ribonucléico) Polímero de nucleótidos La pentosa de los nucleótidos es la Ribosa: en la posición 2' del anillo del azúcar hay un grupo
Clasificación de los AA en familias, según su biosíntesis
 Tema 15: : Aspectos generales de la biosíntesis de aminoácidos. Fijación n del nitrógeno a cadenas carbonadas. Algunos ejemplos de interés s biológico. T 15 síntesis AA Los AA se clasifican en esenciales
Tema 15: : Aspectos generales de la biosíntesis de aminoácidos. Fijación n del nitrógeno a cadenas carbonadas. Algunos ejemplos de interés s biológico. T 15 síntesis AA Los AA se clasifican en esenciales
PROTEÍNAS. Largas cadenas de aminoácidos que se pliegan con una estructura definida Son responsables de la mayoría de las funciones bioquímicas:
 PROTEÍNAS Largas cadenas de aminoácidos que se pliegan con una estructura definida Son responsables de la mayoría de las funciones bioquímicas: Tipos de Proteínas ESTRUCTURA DE LAS PROTEÍNAS Estructura
PROTEÍNAS Largas cadenas de aminoácidos que se pliegan con una estructura definida Son responsables de la mayoría de las funciones bioquímicas: Tipos de Proteínas ESTRUCTURA DE LAS PROTEÍNAS Estructura
SEMANA 29 AMINOACIDOS Y PÉPTIDOS Elaborado por: Lic. Fernando Andrade
 +UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 29 AMINOACIDOS Y PÉPTIDOS Elaborado por: Lic. Fernando Andrade Lea
+UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 29 AMINOACIDOS Y PÉPTIDOS Elaborado por: Lic. Fernando Andrade Lea
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 09 Semestre: 14-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 09 Semestre: 14-I Este material es exclusivamente para uso
ácidos orgánicos con un grupo amino en posición alfa
 AMINOÁIDOS ASPETOS GENERALES Desde el punto de vista químico, los aminoácidos (AA) son ácidos orgánicos con un grupo amino en posición alfa. Según esta definición, los cuatro sustituyentes del carbono
AMINOÁIDOS ASPETOS GENERALES Desde el punto de vista químico, los aminoácidos (AA) son ácidos orgánicos con un grupo amino en posición alfa. Según esta definición, los cuatro sustituyentes del carbono
TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS. A.- Concepto de prótidos y clasificación B.-Los aminoácidos
 TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS A.- Concepto de prótidos y clasificación B.-Los aminoácidos Estructura química y funciones Propiedades químicas. El enlace peptídico C.- Estructura tridimensional
TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS A.- Concepto de prótidos y clasificación B.-Los aminoácidos Estructura química y funciones Propiedades químicas. El enlace peptídico C.- Estructura tridimensional
Preguntas de selectividad en Andalucía. Ácidos nucleicos. Análisis e interpretación de imágenes, esquemas, figuras...
 Año 2001 Describa las funciones más relevantes de los nucleótidos. Cite un ejemplo de nucleótido que participe en cada una de ellas [1,5]. Explique las funciones de los distintos tipos de RNA que participan
Año 2001 Describa las funciones más relevantes de los nucleótidos. Cite un ejemplo de nucleótido que participe en cada una de ellas [1,5]. Explique las funciones de los distintos tipos de RNA que participan
AMINOÁCIDOS, PÉPTIDOS Y PROTEINAS. M.Sc. GABY MÓNICA FELIPE BRAVO
 AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
Capítulo 2. LOS AMINOÁCIDOS, EL ENLACE PEPTÍDICO Y LA ESTRUCTURA SECUNDARIA
 Capítulo 2. LOS AMINOÁCIDOS, EL ENLACE PEPTÍDICO Y LA ESTRUCTURA SECUNDARIA Javier Sancho jsancho@unizar.es Departamento de Bioquímica y Biología Molecular y Celular & Instituto de Biocomputación y Física
Capítulo 2. LOS AMINOÁCIDOS, EL ENLACE PEPTÍDICO Y LA ESTRUCTURA SECUNDARIA Javier Sancho jsancho@unizar.es Departamento de Bioquímica y Biología Molecular y Celular & Instituto de Biocomputación y Física
La práctica del análisis de correspondencias
 La práctica del análisis de correspondencias MICHAEL GREENACRE Catedrático de Estadística en la Universidad Pompeu Fabra Separata del capítulo 18 Análisis de correspondencias múltiples Primera edición:
La práctica del análisis de correspondencias MICHAEL GREENACRE Catedrático de Estadística en la Universidad Pompeu Fabra Separata del capítulo 18 Análisis de correspondencias múltiples Primera edición:
Biomoléculas. Se clasifican básicamente en 4 grandes grupos: Hidratos de carbono Proteínas Lípidos Ácidos nucleicos
 Biomoléculas Se clasifican básicamente en 4 grandes grupos: Hidratos de carbono Proteínas Lípidos Ácidos nucleicos Aminoácidos, péptidos y proteínas Las proteínas cumplen importantes funciones biológicas:
Biomoléculas Se clasifican básicamente en 4 grandes grupos: Hidratos de carbono Proteínas Lípidos Ácidos nucleicos Aminoácidos, péptidos y proteínas Las proteínas cumplen importantes funciones biológicas:
IV. B. 3. 8. DETERMINACIÓN DE LOS PUENTES DISULFURO DEL QUINTO INTERMEDIARIO DE PLEGAMIENTO DEL PCI, Xe.
 IV. B. 3. 8. DETERMINACIÓN DE LOS PUENTES DISULFURO DEL QUINTO INTERMEDIARIO DE PLEGAMIENTO DEL PCI, Xe. La caracterización estructural por digestión con proteasas de la especie scrambled Xe no se realizó
IV. B. 3. 8. DETERMINACIÓN DE LOS PUENTES DISULFURO DEL QUINTO INTERMEDIARIO DE PLEGAMIENTO DEL PCI, Xe. La caracterización estructural por digestión con proteasas de la especie scrambled Xe no se realizó
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Biología. Proteínas.
 Proteínas. Los monómeros de las proteínas son veinte aminoácidos, donde 9 de estoss aminoácidos son esenciales, ya que no son producidos por nuestro organismo, por lo tanto deben ser adquiridos a través
Proteínas. Los monómeros de las proteínas son veinte aminoácidos, donde 9 de estoss aminoácidos son esenciales, ya que no son producidos por nuestro organismo, por lo tanto deben ser adquiridos a través
PROTEÍNAS. Las proteínas están constituidas por la unión de numerosas moléculas sencillas (monómeros) denominados aminoácidos.
 PROTEÍNAS 1. INTRODUCCIÓN Las proteínas son los constituyentes químicos fundamentales de la materia viva. Constituyen alrededor del 50% en peso seco del cuerpo. Los glúcidos y lípidos se encuentran en
PROTEÍNAS 1. INTRODUCCIÓN Las proteínas son los constituyentes químicos fundamentales de la materia viva. Constituyen alrededor del 50% en peso seco del cuerpo. Los glúcidos y lípidos se encuentran en
AMINOACIDOS Y PEPTIDOS. SEMANA 29 Licda. Lilian Judith Guzmán Melgar
 AMINOACIDOS Y PEPTIDOS SEMANA 29 Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los mas importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS SEMANA 29 Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los mas importantes en el mundo biológico son los α-aminoácidos,
Tema 4: METABOLISMO DE PROTEINAS
 Tema 4: METABOLISMO DE PROTEINAS Introducción Generalidades sobre el metabolismo de proteínas Recambio proteico Fuentes de proteína en AA Calidad proteica Digestión. Metabolismo de aminoácidos Ciclo de
Tema 4: METABOLISMO DE PROTEINAS Introducción Generalidades sobre el metabolismo de proteínas Recambio proteico Fuentes de proteína en AA Calidad proteica Digestión. Metabolismo de aminoácidos Ciclo de
7.012 Serie de ejercicios 5
 Nombre Grupo 7.012 Serie de ejercicios 5 Pregunta 1 Al estudiar los problemas de esterilidad, usted intenta aislar un hipotético gen de conejo que explique la prolífica reproducción de estos animales.
Nombre Grupo 7.012 Serie de ejercicios 5 Pregunta 1 Al estudiar los problemas de esterilidad, usted intenta aislar un hipotético gen de conejo que explique la prolífica reproducción de estos animales.
Capítulo 10. Gráficos y diagramas
 Capítulo 10. Gráficos y diagramas 1. Introducción Los gráficos y diagramas que se acostumbran a ver en libros e informes para visualizar datos estadísticos también se utilizan con propósitos cartográficos,
Capítulo 10. Gráficos y diagramas 1. Introducción Los gráficos y diagramas que se acostumbran a ver en libros e informes para visualizar datos estadísticos también se utilizan con propósitos cartográficos,
TUTORIAL: USO DE LA BASE DE DATOS RCSB PDB Y VISUALIZACIÓN DE MOLÉCULAS BIOLÓGICAS USANDO EL PROGRAMA AVOGADRO
 TUTORIAL: USO DE LA BASE DE DATOS RCSB PDB Y VISUALIZACIÓN DE MOLÉCULAS BIOLÓGICAS USANDO EL PROGRAMA AVOGADRO En este tutorial aprenderemos a buscar estructuras en la base de datos RCSB PDB y a visualizar
TUTORIAL: USO DE LA BASE DE DATOS RCSB PDB Y VISUALIZACIÓN DE MOLÉCULAS BIOLÓGICAS USANDO EL PROGRAMA AVOGADRO En este tutorial aprenderemos a buscar estructuras en la base de datos RCSB PDB y a visualizar
ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS
 ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS La espectrometría de masas es una técnica experimental que permite la medición de iones derivados de moléculas. El espectrómetro de masas es un instrumento que permite
ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS La espectrometría de masas es una técnica experimental que permite la medición de iones derivados de moléculas. El espectrómetro de masas es un instrumento que permite
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
CÓDIGO GENÉTICO Y SÍNTESIS DE PROTEÍNAS
 CÓDIGO GENÉTICO Y SÍNTESIS DE PROTEÍNAS Sumario Mitosis y meiosis Código genético y síntesis de proteínas: 1. Concepto de gen 2. Estructura del ADN 3. La replicación del ADN 4. La transcripción 5. La traducción
CÓDIGO GENÉTICO Y SÍNTESIS DE PROTEÍNAS Sumario Mitosis y meiosis Código genético y síntesis de proteínas: 1. Concepto de gen 2. Estructura del ADN 3. La replicación del ADN 4. La transcripción 5. La traducción
MENSAJEROS QUÍMICOS HIDROFÓBICOS
 TRANSDUCCIÓN DE SEÑALES EN EUCARIOTAS: MENSAJEROS QUÍMICOS HIDROFÓBICOS Vamos a ver en esta clase como se biosintetizan algunos de estos mensajeros químicos hidrofóbicos y después veremos cómo se biosintetizan
TRANSDUCCIÓN DE SEÑALES EN EUCARIOTAS: MENSAJEROS QUÍMICOS HIDROFÓBICOS Vamos a ver en esta clase como se biosintetizan algunos de estos mensajeros químicos hidrofóbicos y después veremos cómo se biosintetizan
DISEÑO, SÍNTESIS Y ESTRUCTURA DE DOMINIOS HELICOIDALES INFLUENCIA DE LA INTRODUCCIÓN DE AMINOÁCIDOS D
 Tesis Doctoral DISEÑO, SÍNTESIS Y ESTRUCTURA DE DOMINIOS HELICOIDALES INFLUENCIA DE LA INTRODUCCIÓN DE AMINOÁCIDOS D Carmen Giovana Granados Ramírez Departamento de Química Orgánica Facultad de Química
Tesis Doctoral DISEÑO, SÍNTESIS Y ESTRUCTURA DE DOMINIOS HELICOIDALES INFLUENCIA DE LA INTRODUCCIÓN DE AMINOÁCIDOS D Carmen Giovana Granados Ramírez Departamento de Química Orgánica Facultad de Química
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS
 UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
Capítulo 9. Archivos de sintaxis
 Capítulo 9 Archivos de sintaxis El SPSS permite generar y editar archivos de texto con sintaxis SPSS, es decir, archivos de texto con instrucciones de programación en un lenguaje propio del SPSS. Esta
Capítulo 9 Archivos de sintaxis El SPSS permite generar y editar archivos de texto con sintaxis SPSS, es decir, archivos de texto con instrucciones de programación en un lenguaje propio del SPSS. Esta
Química orgánica. Cuarto Medio 25/06
 Química orgánica Cuarto Medio 25/06 CARBONO Es el elemento principal de las moléculas orgánicas. Debido a que este átomo, presenta una gran estabilidad. Dado que, tiene una baja tendencia a donar y quitar
Química orgánica Cuarto Medio 25/06 CARBONO Es el elemento principal de las moléculas orgánicas. Debido a que este átomo, presenta una gran estabilidad. Dado que, tiene una baja tendencia a donar y quitar
(Estudios in vivo y estudios in vitro)
 (Estudios in vivo y estudios in vitro) IN VIVO: es la experimentación con un todo, que viven organismos en comparación. Ensayos con animales y ensayos clínicos son dos formas de investigación in vivo.
(Estudios in vivo y estudios in vitro) IN VIVO: es la experimentación con un todo, que viven organismos en comparación. Ensayos con animales y ensayos clínicos son dos formas de investigación in vivo.
1) a) En la figura señale, englobando con un trazo continuo, lo siguiente:
 CÁTEDRA: BIOQUÍMICA Carreras: Farmacia Profesorado en Química Licenciatura en Química Licenciatura en Alimentos ÁCIDOS NUCLEICOS 1) a) En la figura señale, englobando con un trazo continuo, lo siguiente:
CÁTEDRA: BIOQUÍMICA Carreras: Farmacia Profesorado en Química Licenciatura en Química Licenciatura en Alimentos ÁCIDOS NUCLEICOS 1) a) En la figura señale, englobando con un trazo continuo, lo siguiente:
Presentación organizada por José Antonio Pascual Trillo
 Presentación organizada por José Antonio Pascual Trillo La fotosíntesis es un proceso que se desarrolla en dos etapas: Reacciones lumínicas: es un proceso dependiente de la luz (etapa clara), requiere
Presentación organizada por José Antonio Pascual Trillo La fotosíntesis es un proceso que se desarrolla en dos etapas: Reacciones lumínicas: es un proceso dependiente de la luz (etapa clara), requiere
QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Agua (o humedad, si se conoce)*
 QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Entregar el 21 de Mayo. Selecciona un alimento, de preferencia de los que consumes con regularidad, que contenga proteínas. 1. De acuerdo
QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Entregar el 21 de Mayo. Selecciona un alimento, de preferencia de los que consumes con regularidad, que contenga proteínas. 1. De acuerdo
Unidad I. 1.1 Sistemas numéricos (Binario, Octal, Decimal, Hexadecimal)
 Unidad I Sistemas numéricos 1.1 Sistemas numéricos (Binario, Octal, Decimal, Hexadecimal) Los computadores manipulan y almacenan los datos usando interruptores electrónicos que están ENCENDIDOS o APAGADOS.
Unidad I Sistemas numéricos 1.1 Sistemas numéricos (Binario, Octal, Decimal, Hexadecimal) Los computadores manipulan y almacenan los datos usando interruptores electrónicos que están ENCENDIDOS o APAGADOS.
Estructura y función de proteínas
 Estructura y función de proteínas Luciferina y uciferasa. Producción de luz. Hemoglobina. Transporte de oxígeno. Queratina: Principal componente estructural de pelo, escamas, cuernos, lana, uñas y plumas.
Estructura y función de proteínas Luciferina y uciferasa. Producción de luz. Hemoglobina. Transporte de oxígeno. Queratina: Principal componente estructural de pelo, escamas, cuernos, lana, uñas y plumas.
Proteínas y su Papel Biológico
 Proteínas Proteínas y su Papel Biológico Las proteínas son macromoléculas de gran diversidad de formas y versatilidad de funciones. Pueden servir como componentes estructurales de células y tejidos (pelo,
Proteínas Proteínas y su Papel Biológico Las proteínas son macromoléculas de gran diversidad de formas y versatilidad de funciones. Pueden servir como componentes estructurales de células y tejidos (pelo,
En el APOENZIMA se distinguen tres tipos de aminoácidos:
 1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
Movimiento Rectilíneo Uniforme
 Movimiento Rectilíneo Uniforme 1. Teoría La mecánica es la parte de la física encargada de estudiar el movimiento y el reposo de los cuerpos, haciendo un análisis de sus propiedades y causas. La mecánica
Movimiento Rectilíneo Uniforme 1. Teoría La mecánica es la parte de la física encargada de estudiar el movimiento y el reposo de los cuerpos, haciendo un análisis de sus propiedades y causas. La mecánica
DOMINIO Y RANGO página 89. Cuando se grafica una función existen las siguientes posibilidades:
 DOMINIO Y RANGO página 89 3. CONCEPTOS Y DEFINICIONES Cuando se grafica una función eisten las siguientes posibilidades: a) Que la gráfica ocupe todo el plano horizontalmente (sobre el eje de las ). b)
DOMINIO Y RANGO página 89 3. CONCEPTOS Y DEFINICIONES Cuando se grafica una función eisten las siguientes posibilidades: a) Que la gráfica ocupe todo el plano horizontalmente (sobre el eje de las ). b)
En la actualidad ASCII es un código de 8 bits, también conocido como ASCII extendido, que aumenta su capacidad con 128 caracteres adicionales
 Definición(1) Sistemas numéricos MIA José Rafael Rojano Cáceres Arquitectura de Computadoras I Un sistema de representación numérica es un sistema de lenguaje que consiste en: un conjunto ordenado de símbolos
Definición(1) Sistemas numéricos MIA José Rafael Rojano Cáceres Arquitectura de Computadoras I Un sistema de representación numérica es un sistema de lenguaje que consiste en: un conjunto ordenado de símbolos
Singularidad del carbono
 Singularidad del carbono Su configuración electrónica y su tamaño determinan que sea el único elemento químico que puede: Formar enlaces covalentes sencillos, dobles o triples con otros átomos de carbono.
Singularidad del carbono Su configuración electrónica y su tamaño determinan que sea el único elemento químico que puede: Formar enlaces covalentes sencillos, dobles o triples con otros átomos de carbono.
MICROECONOMÍA II. PRÁCTICA TEMA II: Equilibrio parcial
 MICROECONOMÍA II PRÁCTICA TEMA II: Equilibrio parcial EJERCICIO 1 A) En equilibrio, la cantidad demandada coincide con la cantidad ofrecida, así como el precio de oferta y demanda. Por lo tanto, para hallar
MICROECONOMÍA II PRÁCTICA TEMA II: Equilibrio parcial EJERCICIO 1 A) En equilibrio, la cantidad demandada coincide con la cantidad ofrecida, así como el precio de oferta y demanda. Por lo tanto, para hallar
TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO)
 TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO) Existen 2 clases de electrización, la positiva (que se representa con + ), y la negativa (que se representa con - ). Hay una partícula
TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO) Existen 2 clases de electrización, la positiva (que se representa con + ), y la negativa (que se representa con - ). Hay una partícula
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
Aminoácidos y proteínas. Cintia Mendez Vedia
 Aminoácidos y proteínas Cintia Mendez Vedia Aminoácidos Grupo amino (protonado) Grupo carboxilo (disociado) H 3 N + C H Cadena lateral R Carbono Aminoácidos Funciones + H 3 N C H + H 3 N C H H C OH H
Aminoácidos y proteínas Cintia Mendez Vedia Aminoácidos Grupo amino (protonado) Grupo carboxilo (disociado) H 3 N + C H Cadena lateral R Carbono Aminoácidos Funciones + H 3 N C H + H 3 N C H H C OH H
El agua como disolvente
 hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
Química Orgánica. por átomos de carbono. A diferencia de otros
 Química Orgánica La definición moderna de la química orgánica es el estudio de los compuestos que se componen por átomos de carbono. A diferencia de otros elementos, el carbono crea enlaces muy fuertes
Química Orgánica La definición moderna de la química orgánica es el estudio de los compuestos que se componen por átomos de carbono. A diferencia de otros elementos, el carbono crea enlaces muy fuertes
Proteínas fibrosas. Alfa Queratinas Beta-Queratinas Fibroína Colágeno Elastina
 Proteínas Fibrosas La mayor parte o casi toda la proteína está organizada de manera paralela a un sólo eje Las proteínas fibrosas son generalmente fuertes mecánicamente Son generalmente insolubles Generalmente
Proteínas Fibrosas La mayor parte o casi toda la proteína está organizada de manera paralela a un sólo eje Las proteínas fibrosas son generalmente fuertes mecánicamente Son generalmente insolubles Generalmente
INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS
 INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS Lic. Claudio Vidos Departamento de investigación de DEMIK Electromedicina Director del INSTITUTO CAV Rehabilitación Departamento de investigación
INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS Lic. Claudio Vidos Departamento de investigación de DEMIK Electromedicina Director del INSTITUTO CAV Rehabilitación Departamento de investigación
Enunciado unidades fraccionarias fracción fracciones equivalentes comparar operaciones aritméticas fracciones propias Qué hacer deslizador vertical
 Enunciado Si la unidad la dividimos en varias partes iguales, podemos tomar como nueva unidad de medida una de estas partes más pequeñas. Las unidades fraccionarias son necesarias cuando lo que queremos
Enunciado Si la unidad la dividimos en varias partes iguales, podemos tomar como nueva unidad de medida una de estas partes más pequeñas. Las unidades fraccionarias son necesarias cuando lo que queremos
METABOLISMO CELULAR. Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio
 METABOLISMO CELULAR Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio Reacciones Celulares Básicas. Los sistemas vivos convierten la energía
METABOLISMO CELULAR Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio Reacciones Celulares Básicas. Los sistemas vivos convierten la energía
Características de funciones que son inversas de otras
 Características de funciones que son inversas de otras Si f es una función inyectiva, llamamos función inversa de f y se representa por f 1 al conjunto. f 1 = a, b b, a f} Es decir, f 1 (x, y) = { x =
Características de funciones que son inversas de otras Si f es una función inyectiva, llamamos función inversa de f y se representa por f 1 al conjunto. f 1 = a, b b, a f} Es decir, f 1 (x, y) = { x =
Decisión: Indican puntos en que se toman decisiones: sí o no, o se verifica una actividad del flujo grama.
 Diagrama de Flujo La presentación gráfica de un sistema es una forma ampliamente utilizada como herramienta de análisis, ya que permite identificar aspectos relevantes de una manera rápida y simple. El
Diagrama de Flujo La presentación gráfica de un sistema es una forma ampliamente utilizada como herramienta de análisis, ya que permite identificar aspectos relevantes de una manera rápida y simple. El
a) Aminoácidos b) Estructura primaria
 Estructura y función de proteínas a) Aminoácidos b) Estructura primaria Luciferina y luciferasa. Producción de luz. Hemoglobina. Transporte de oxígeno. Queratina: Principal componente estructural de pelo,
Estructura y función de proteínas a) Aminoácidos b) Estructura primaria Luciferina y luciferasa. Producción de luz. Hemoglobina. Transporte de oxígeno. Queratina: Principal componente estructural de pelo,
4 1 fuerzas eléctricas responsables de la activación auricular. Un segundo vector (2) correspondiente. con la despolarización ventricular central y
 5 el eje eléctrico cardiaco Vectores Un vector es la forma de representar una magnitud que tiene una dirección y un sentido determinados. Se representa un vector como una flecha cuyo tamaño sería su magnitud,
5 el eje eléctrico cardiaco Vectores Un vector es la forma de representar una magnitud que tiene una dirección y un sentido determinados. Se representa un vector como una flecha cuyo tamaño sería su magnitud,
Para crear una lista como la anterior, primero escribe la información, y después selecciona el texto y aplícale el formato de viñetas.
 Módulo 3 Herramientas de Cómputo Listas, tabulaciones, columnas y cuadros de texto Listas En muchas ocasiones es necesario que enumeres diferentes elementos en tus documentos. Word no sólo reconoce números
Módulo 3 Herramientas de Cómputo Listas, tabulaciones, columnas y cuadros de texto Listas En muchas ocasiones es necesario que enumeres diferentes elementos en tus documentos. Word no sólo reconoce números
SISTEMA DIÉDRICO PARA INGENIEROS. David Peribáñez Martínez DEMO
 SISTEMA DIÉDRICO PARA INGENIEROS David Peribáñez Martínez SISTEMA DIÉDRICO PARA INGENIEROS David Peribáñez Martínez Valderrebollo 20, 1 A 28031 MADRID 1ª Edición Ninguna parte de esta publicación, incluido
SISTEMA DIÉDRICO PARA INGENIEROS David Peribáñez Martínez SISTEMA DIÉDRICO PARA INGENIEROS David Peribáñez Martínez Valderrebollo 20, 1 A 28031 MADRID 1ª Edición Ninguna parte de esta publicación, incluido
SISTEMAS DE COORDENADAS SISTEMA COORDENADO UNIDIMENSIONAL
 SISTEMAS DE COORDENADAS En la vida diaria, nos encontramos con el problema de ordenar algunos objetos; de tal manera que es necesario agruparlos, identificarlos, seleccionarlos, estereotiparlos, etc.,
SISTEMAS DE COORDENADAS En la vida diaria, nos encontramos con el problema de ordenar algunos objetos; de tal manera que es necesario agruparlos, identificarlos, seleccionarlos, estereotiparlos, etc.,
AMINOACIDOS Y PEPTIDOS. SEMANA 29 Licda. Lilian Judith Guzmán Melgar
 AMINOACIDOS Y PEPTIDOS SEMANA 29 Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los mas importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS SEMANA 29 Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los mas importantes en el mundo biológico son los α-aminoácidos,
FLUJO DE LA INFORMACIÓN GENÉTICA REPRODUCCIÓN CELULAR Biología General
 FLUJO DE LA INFORMACIÓN GENÉTICA REPRODUCCIÓN CELULAR Biología General 1- Diga si son falsas o verdaderas las siguientes afirmaciones con respecto al núcleo celular: I. La envoltura nuclear presenta dos
FLUJO DE LA INFORMACIÓN GENÉTICA REPRODUCCIÓN CELULAR Biología General 1- Diga si son falsas o verdaderas las siguientes afirmaciones con respecto al núcleo celular: I. La envoltura nuclear presenta dos
Manual de Microsoft Power Point 2007 Parte 2 Universidad Politécnica de San Luis Potosí
 Contenido: Manual de Microsoft Power Point 2007 Parte 2 1. Insertar y dar formato a los cuadros de texto.... 2 2. Insertar cuadros de texto.... 2 3. Estilos de forma - Contornos y colores.... 3 4. Estilos
Contenido: Manual de Microsoft Power Point 2007 Parte 2 1. Insertar y dar formato a los cuadros de texto.... 2 2. Insertar cuadros de texto.... 2 3. Estilos de forma - Contornos y colores.... 3 4. Estilos
Operación de Microsoft Excel. Guía del Usuario Página 79. Centro de Capacitación en Informática
 Manejo básico de base de datos Unas de las capacidades de Excel es la de trabajar con listas o tablas de información: nombres, direcciones, teléfonos, etc. Excel puede trabajar con tablas de información
Manejo básico de base de datos Unas de las capacidades de Excel es la de trabajar con listas o tablas de información: nombres, direcciones, teléfonos, etc. Excel puede trabajar con tablas de información
METABOLISMO DEL NITRÓGENO
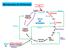 METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
Lehninger Principles of Biochemistry Fourth Edition
 David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
Roberto Quejido Cañamero
 Crear un documento de texto con todas las preguntas y respuestas del tema. Tiene que aparecer en él todos los contenidos del tema. 1. Explica qué son los modos de presentación en Writer, cuáles hay y cómo
Crear un documento de texto con todas las preguntas y respuestas del tema. Tiene que aparecer en él todos los contenidos del tema. 1. Explica qué son los modos de presentación en Writer, cuáles hay y cómo
Proteínas fibrosas. α-queratinas
 Hélices α entrecruzadas por puentes disulfuro Proteínas fibrosas α-queratinas Estructura Características Localización Estructuras resistentes e insolubles de dureza y flexibilidad variables Estructura
Hélices α entrecruzadas por puentes disulfuro Proteínas fibrosas α-queratinas Estructura Características Localización Estructuras resistentes e insolubles de dureza y flexibilidad variables Estructura
REPASANDO CONCEPTOS : LAS PROTEÍNAS
 REPASANDO CONCEPTOS : LAS PROTEÍNAS Drqf. Manuel Fontboté A. Consultor en Ciencias Cosméticas CHILE El uso de materias activas de naturaleza proteica en los cosméticos no es un hecho reciente, antes bien,
REPASANDO CONCEPTOS : LAS PROTEÍNAS Drqf. Manuel Fontboté A. Consultor en Ciencias Cosméticas CHILE El uso de materias activas de naturaleza proteica en los cosméticos no es un hecho reciente, antes bien,
Aminoácidos y péptidos
 Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
CLASIFICACION POR LA CADENA LATERAL POR SU REQUERIMIENTO POR SU POLARIDAD. Esenciales No esenciales CADENA LATERAL CON GRUPO
 29 2018 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
29 2018 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
