GENUTEN CITOSTÁTICO-ANTITUMORAL
|
|
|
- Joaquín Carrizo Benítez
- hace 7 años
- Vistas:
Transcripción
1 GENUTEN CITOSTÁTICO-ANTITUMORAL COMPOSICIÓN GENUTEN 200 mg. Cada frasco-ampolla contiene: Gemcitabina (como clorhidrato) 200 mg. Excipientes: Manitol, Acetato de sodio trihidrato, Hidróxido de sodio, Ácido clorhídrico, Nitrógeno, en c.s. GENUTEN 1 g. Cada frasco-ampolla contiene: Gemcitabina (como clorhidrato) 1,0 g. Excipientes: Manitol, Acetato de sodio trihidrato, Hidróxido de sodio, Ácido clorhídrico, Nitrógeno, en c.s. ACCIÓN TERAPÉUTICA GENUTEN es un análogo nucleósido (2',2'-difluorodesoxicitidina) con actividad antitumoral que exhibe especificidad en la fase celular, interviniendo en la síntesis del DNA (fase S) y también bloqueando la progresión de las células a través de la fase terminal G1/S. La acción citotóxica in vitro de la gemcitabina es concentración y tiempo dependiente. Se metaboliza intracelularmente por las nucleósidos cinasas a los nucleósidos activos difosfato y trifosfato. Su efecto citotóxico es atribuido a la combinación de dos acciones de los nucleósidos difosfato y trifosfato, los cuales producen la inhibición de la síntesis del DNA. Primero, la gemcitabina difosfato inhibe la ribonucleótido reductasa, la cual es responsable de catalizar las reacciones que generan la desoxinucleósido trifosfato para la síntesis del DNA. Esta inhibición causa una reducción en las concentraciones de desoxinucleótidos, incluyendo dctp. En segundo lugar, la gemcitabina trifosfato compite con la dctp para la incorporación en el DNA. La reducción en la concentración intracelular de dctp (por la acción de la difosfato) aumenta la incorporación de gemcitabina trifosfato en el DNA (autopotenciación). Después que el nucleótido gemcitabina es incorporado al DNA, sólo otro nucleótido se adiciona a la hebra en crecimiento del DNA, por lo cual hay una inhibición de la síntesis posterior de DNA. La DNA polimerasa epsilon es incapaz de remover el nucleótido gemcitabina y reparar la cadena en crecimiento del DNA (terminación enmascarada de la cadena). La gemcitabina (<10%) y su principal metabolito inactivo (2'-desoxi-2',2'-difluorouridina) se excretan por orina. La depuración se ve afectada por la edad y el sexo, por lo que existe una diferencia en la vida media y en las concentraciones plasmáticas de esta droga, siendo más altas en las mujeres y en los ancianos. INDICACIONES Cáncer pulmonar de células no pequeñas: GENUTEN está indicado solo o en combinación con cisplatino como tratamiento de primera línea en pacientes con cáncer pulmonar de células no pequeñas localmente avanzado (estado llla o lllb) o metastásico (estado IV). Cáncer de páncreas: GENUTEN está indicado como tratamiento de primera línea en pacientes con adenocarcinoma pancreático localmente avanzado o metastásico. GENUTEN también está indicado para pacientes con cáncer pancreático refractario a 5-FU. GENUTEN también ha demostrado utilidad para el tratamiento de cáncer de vejiga. GENUTEN está indicado, en combinación, para el tratamiento de pacientes con cáncer de mama con recurrencia local o metastásico, no resecable, que han recaído después de quimioterapia adyuvante/neoadyuvante o como monoterapia luego de otra quimioterapia para enfermedad metastásica. La quimioterapia previa debe haber incluido una antraciclina a menos que esté clínicamente contraindicado. GENUTEN está indicado para el tratamiento
2 combinado con carboplatino para el cáncer de ovario epitelial en pacientes que han recaído como mínimo 6 meses de finalizada una terapia basada en platinos. Gemcitabina está indicada para el tratamiento de cáncer biliar. GENUTEN está indicado como tratamiento de primera línea, en combinación con cisplatino para el tratamiento de cáncer cérvico-uterino localmente avanzado y metastásico. CONTRAINDICACIONES GENUTEN está contraindicado en pacientes con hipersensibilidad conocida a la gemcitabina. Embara-zo. Lactancia. Niños. El riesgo beneficio debe ser evaluado en pacientes con depresión de la médula ósea, viruela, herpes zoster o que estén afectados por infección. ADVERTENCIAS Y PRECAUCIONES Advertencias: La prolongación del tiempo de infusión y el aumento en la frecuencia de administración han demostrado incrementar la toxicidad. La gemcitabina puede suprimir la función medular que se manifiesta por leucopenia, trombocitopenia Y anemia. Sin embargo, la mielosupresión es de corta duración, generalmente no obliga a reducir la posología y raramente demanda la suspensión de la administración. Hipersensibilidad: Se ha reportado un caso aislado de anafilaxis. Precauciones: Los pacientes deben ser monitoreados cuidadosamente. Se deberá disponer de instalaciones adecuadas para monitorear el estado del paciente y de recursos terapéuticos para los pacientes comprometidos por la toxicidad. Pruebas de laboratorio: El tratamiento se iniciará con precaución en pacientes con una función medular comprometida. Como con otros oncológicos, cuando se use quimioterapia combinada o secuencial deberá considerarse la posibilidad de mielosupresión acumulativa. Los pacientes que reciban gemcitabina deberán ser monitoreados antes de cada dosis en relación a los valores de plaquetas, leucocitos y granulocitos, y en caso de detectarse mielosupresión inducida por el fármaco se considerará la suspensión o modificación de la terapia (ver Posología). Los recuentos hematológicos pueden continuar bajando luego de haberse interrumpido el tratamiento. Embarazo y lactancia: Embarazo - Teratogénesis: La seguridad de este medicamento para su empleo en el embarazo no ha sido establecida. La evaluación de estudios en animales de experimentación ha evidenciado toxicidad reproductiva, esto es, defectos congénitos u otros efectos sobre el desarrollo del feto, el curso de la gestación o el desarrollo peri y postnatal (ver Precauciones). Lactancia: Se debe evitar el empleo de gemcitabina en la mujer que amamanta debido a los posibles riesgos potenciales para el niño. Carcinogénesis, mutagénesis, fertilidad: En estudios in-vitro gemcitabina produjo daños cromosómicos, incluyendo ruptura de cromátides. En ratas machos, gemcitabina indujo hipospermatogénesis reversible y dependiente del esquema y la dosis. Si bien los estudios en animales han demostrado un efecto de la gemcitabina sobre la fertilidad masculina, no se ha observado efecto alguno sobre la fertilidad de la mujer. No se han realizado estudios a largo plazo en animales para evaluar el potencial carcinogénico de gemcitabina. EFECTOS ADVERSOS Hematológicas: Dado que gemcitabina es un mielosupresor, como resultado de su administración pueden observarse anemia, leucopenia y trombocitopenia. La mielosupresión es en general, leve a moderada, y más pronunciada respecto a los valores de granulocitos. También han sido comunes las comunicaciones de trombocitemia.
3 Gastrointestinales: En aproximadamente dos tercios de los pacientes se verifican anomalías de las transaminasas hepáticas, pero en general son leves, no progresivas y raramente obligan a suspender el tratamiento. No obstante, gemcitabina debe ser usada con precaución en pacientes con disfunción hepática (ver Posología y FORMA de administración). Un tercio de los pacientes reporta náuseas, y otro tercio reporta náuseas acompañadas de vómitos. Este efecto adverso requiere tratamiento en aproximadamente el 20% de los pacientes, raramente limita la dosificación y es fácilmente tratable con antieméticos. Renales: Casi la mitad de los pacientes presenta proteinuria y hematuria leves, pero raramente revisten significancia clínica y por lo general no están asociadas con cambio alguno en los valores de creatinina sérica o nitrógeno ureico en sangre. No obstante, se han señalado unos pocos casos de insuficiencia renal de etiología incierta, por lo que gemcitabina deberá ser empleada con precaución en pacientes con disfunción renal (ver Posología y FORMA de administración). Alérgicas: En aproximadamente el 25% de los pacientes se observa una erupción, asociada con prurito en el 10% de los casos. En general la erupción es leve, no limita la posología y responde a las terapias locales. Raramente se ha comunicado descamación, vesiculación y ulceración. En menos del 1 % de los pacientes se reporta bronco espasmo luego de la infusión de gemcitabina, el cual habitualmente es leve y transitorio, pero que puede requerir tratamiento parenteral. Gemcitabina no debe ser administrada a pacientes con hipersensibilidad conocida a esta droga. Alrededor del 10% de los pacientes experimenta disnea pocas horas después de la inyección de gemcitabina. Este efecto es usualmente leve, breve, raramente limita la posología y habitualmente desaparece sin tratamiento específico. Se desconoce el mecanismo de este evento y no está dilucidada la relación con gemcitabina. Otras reacciones: En aproximadamente el 20% de los pacientes se observa un síndrome que se asemeja a la gripe. Usualmente es leve, breve y raramente limita la posología, y sólo en el 15% de los pacientes es severo. Fiebre, cefalea, dolor de espalda, escalofríos, mialgia, astenia y anorexia son los síntomas reportados más frecuentemente. También son comunes tos, rinitis, malestar, sudoración e insomnio. Fiebre y astenia también son comunicados frecuentemente como síntomas aislados. Se desconoce el mecanismo de esta toxicidad. Alrededor del 30% de los pacientes comunica edema I edema periférico. También se han incluido algunos casos de edema facial. El edema pulmonar ha sido infrecuente (1 %). Generalmente el edema es leve a moderado, raramente limita la dosificación, algunas veces ha sido calificado como doloroso y normalmente revierte luego de suspendido el tratamiento con gemcitabina. Se desconoce el mecanismo de esta toxicidad que no está asociada con evidencia alguna de insuficiencia cardíaca, hepática o renal. Los siguientes efectos adversos también han sido comunicados frecuentemente: alopecia (en general pérdida mínima de cabello) 13% de los pacientes, somnolencia 10%, diarrea 8%, toxicidad oral (básicamente inflamación y eritema) 7%, y constipación 6%. Se han informado muy infrecuentemente casos de insuficiencia cardíaca. Se han reportado arritmias. Se han señalado unos pocos casos de hipotensión. POSOLOGÍA Y FORMA DE ADMINISTRACIÓN Cáncer de pulmón a células no pequeñas: Adultos: La dosis recomendada de gemcitabina es de 1000 mg/m 2, administrada en infusión endovenosa de 30 minutos. Esta dosis debe repetirse una vez por semana durante tres semanas, seguidas de un período de descanso de una semana. Luego se repite este ciclo de cuatro semanas. La reducción de la dosis se aplica en base a la magnitud de la toxicidad experimentada por el paciente.
4 Cáncer de páncreas: Adultos: La dosis recomendada de gemcitabina es de 1000 mg/m 2, administrada en infusión endovenosa de 30 minutos. Esta dosis debe repetirse una vez a la semana durante un período de hasta 7 semanas, seguidas de una semana de descanso. Los ciclos subsiguientes consistirán de una infusión por semana durante 3 semanas consecutivas, cada 4 semanas. La reducción de la dosis se aplica en base a la magnitud de los efectos colaterales evidenciados por el paciente. Cáncer de vejiga: Adultos: La dosis recomendada de gemcitabina es de 1250 mg/m 2, administrada mediante infusión I.V. de 30 minutos. Esta dosis debe darse los días 1, 8 Y 15 de un ciclo de 28 días. Este ciclo de 4 semanas debe luego repetirse. La reducción de la dosificación en cada ciclo o dentro del ciclo se aplica basándose en el grado de toxicidad experimentada por el paciente. En combinación con cisplatino: Adultos: La dosis recomendada es de 1000 mg/m 2, administrada mediante infusión I.V. de 30 minutos. Esta dosis debe darse los días 1, 8 y 15 de un ciclo de 28 días en combinación con cisplatino. La dosis recomendada de cisplatino es de 70 mg/m 2 en el día 1, seguido de gemcitabina, o en el día 2 de un ciclo de 28 días. Este ciclo de 4 semanas debe luego repetirse. La reducción de la dosificación en cada ciclo o dentro del ciclo se aplica basándose en el grado de toxicidad experimentada por el paciente. Cáncer de mama: Adultos: La dosis recomendada de gemcitabina es de 1000 a 1200 mg/m 2, administrada mediante infusión I.V. de 30 minutos. Esta dosis debe darse los días 1, 8 y 15 de un ciclo de 28 días. Este ciclo de 4 semanas debe luego repetirse. La reducción de la dosificación en cada ciclo o dentro del ciclo se aplica basándose en el grado de toxicidad experimentado por el paciente. En el caso de combinación con paclitaxel la dosis recomendada es: Paclitaxel (175 mg/m 2 ) administrado en el día 1 como infusión I.V. en aproximadamente 3 horas, seguida de GENUTEN (1250 mg/m 2 ) administrada como una infusión I.V. de 30 minutos en los días 1 y 8 de cada ciclo de 21 días. La dosis en cada ciclo o dentro de un mismo ciclo se puede reducir en función de la toxicidad experimentada por el paciente. Cáncer de ovario: Adultos: Se recomienda administrar la siguiente combinación de gemcitabina y carboplatino: gemcitabina 1000 mg/m 2 mediante infusión I.V. de 30 minutos, en los días 1 y 8 de cada ciclo de 21 días. El carboplatino será administrado en el día 1, después de la administración de gemcitabina, en una dosis consistente con el objetivo del área bajo la curva (ABC) de 4,0 mg/ml-min. La reducción de la dosificación en cada ciclo o dentro del ciclo se aplica basándose en el grado de toxicidad experimentado por el paciente. Cáncer de tracto biliar: Adultos: La dosis recomendada es de 1000 mg/m 2, administrada mediante infusión I.V. de 30 minutos. Esto debe repetirse 1 vez a la semana durante 3 semanas, seguido por un período de descanso de 1 semana. Luego se repite este ciclo de 4 semanas. La reducción de la dosificación en cada ciclo o dentro del ciclo puede aplicar basándose en el grado de toxicidad experimentada por el paciente. En combinación con cisplatino la dosis recomendada es: Cisplatino (70 mg/m 2 ) administrado en el día 1 como infusión I.V., seguida de GENUTEN (1250 mg/m 2 ) administrada como una infusión I.V. de 30 minutos en los días 1 y 8 de cada ciclo de 21 días. Este ciclo de 3 semanas debe luego repetirse. La reducción de la dosificación en cada ciclo o dentro del ciclo puede aplicar basándose en el grado de toxicidad experimentada por el paciente. Cáncer cérvico-uterino: Tratamiento neoadyuvante en adultos y enfermedad metastásica: En el caso de combinación con cisplatino, la dosis recomendada es: Cisplatino 70 mg/m 2 administrado en el día 1, seguido de gemcitabina 1250 mg/m 2 administrado en los días 1 y 8 cada 21 días. Este ciclo de 3 semanas debe luego repetirse.
5 La reducción de la dosis en cada ciclo o dentro del ciclo se aplica basándose en el grado de toxicidad experimentado por el paciente. Los pacientes que reciben gemcitabina deben ser monitoreados, antes de cada aplicación, en cuanto a los recuentos de plaquetas, leucocitos y granulocitos y, de ser necesario, se reducirá o bien se suspenderá la dosis en presencia de toxicidad hematológica, de acuerdo al siguiente cuadro: Recuento absoluto de granulocitos/mm 3 Recuento de plaquetas/mm 3 > y > o < o < suspender Porcentaje de la dosis total Pacientes ancianos: Gemcitabina ha sido bien tolerada por pacientes de más de 65 años de edad. No hay evidencias que sugieran la necesidad de un ajuste posológico en los ancianos, aunque la eliminación y la vida media de gemcitabina se ven afectadas por la edad. Insuficiencia hepática y renal: Gemcitabina debe ser usada con precaución en pacientes con disfunción hepática o renal. No se han realizado estudios en pacientes con insuficiencia hepática o renal significativa. Niños: Gemcitabina no ha sido estudiada en niños. SOBREDOSIFICACIÓN No se conoce antídoto para la sobredosificación de gemcitabina. Se han administrado dosis elevadas de 5,7 g/m 2 por infusión endovenosa de 30 minutos cada dos semanas con una toxicidad clínicamente aceptable. En el caso de sospechar sobredosificación, el paciente deberá ser monitoreado mediante recuentos sanguíneos apropiados y recibir tratamiento de apoyo, de ser necesario. Ante la eventualidad de una sobredosificación, concurrir al hospital más cercano o comunicarse con el médico tratante. PRESENTACIONES GENUTEN 200 mg. Se presenta en un frasco-ampolla que contiene gemcitabina 200 mg, polvo liofilizado para solución inyectable vía intravenosa. GENUTEN 1 g. Se presenta en un frasco-ampolla que contiene gemcitabina 1 g, polvo liofilizado para solución inyectable vía intravenosa.
Principio Activo: Gemcitabina clorhidrato Forma Farmacéutica: Polvo liofilizado estéril para Solución Inyectable
 Gemcitabina 1000 mg Guarde este folleto, puede necesitar leerlo nuevamente. Si tiene cualquier duda o no está seguro de algo, pregunte a su médico o químico farmacéutico. Principio Activo: Gemcitabina
Gemcitabina 1000 mg Guarde este folleto, puede necesitar leerlo nuevamente. Si tiene cualquier duda o no está seguro de algo, pregunte a su médico o químico farmacéutico. Principio Activo: Gemcitabina
Polvo para solución inyectable para su reconstitución y administración por vía intravenosa.
 FT200899+3-B 1. DENOMINACIÓN DEL MEDICAMENTO GEMZAR Gemcitabina 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA GEMZAR 200 mg polvo para solución inyectable : cada vial contiene 200 mg de gemcitabina (DCI) (hidrocloruro).
FT200899+3-B 1. DENOMINACIÓN DEL MEDICAMENTO GEMZAR Gemcitabina 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA GEMZAR 200 mg polvo para solución inyectable : cada vial contiene 200 mg de gemcitabina (DCI) (hidrocloruro).
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: PAMIGEN 2. Nombre Genérico: GEMCITABINA 3. Forma Farmacéutica y Formulación: Solución Cada frasco ámpula con liofilizado contiene: Clorhidrato de
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: PAMIGEN 2. Nombre Genérico: GEMCITABINA 3. Forma Farmacéutica y Formulación: Solución Cada frasco ámpula con liofilizado contiene: Clorhidrato de
GEMCITABINA. 1000,0 mg. 24 meses
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: GEMCITABINA Polvo liofilizado para
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: GEMCITABINA Polvo liofilizado para
FOLLETO DE INFORMACION AL PACIENTE. ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg
 FOLLETO INFORMACION AL PACIENTE ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg NANOPARTICULAS DE PACLITAXEL LIGADO A ALBÚMINA Leer esta Información para el paciente antes de empezar a recibir ABRAXANE
FOLLETO INFORMACION AL PACIENTE ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg NANOPARTICULAS DE PACLITAXEL LIGADO A ALBÚMINA Leer esta Información para el paciente antes de empezar a recibir ABRAXANE
ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg. COMPOSICIÓN Cada comprimido recubierto contiene: Excipientes: Según lo aprobado en Registro
 ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg COMPOSICIÓN Cada comprimido recubierto contiene: Anastrozol 1 mg Excipientes: Según lo aprobado en Registro CLASIFICACION TERAPEUTICA Antineoplásico INDICACIONES
ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg COMPOSICIÓN Cada comprimido recubierto contiene: Anastrozol 1 mg Excipientes: Según lo aprobado en Registro CLASIFICACION TERAPEUTICA Antineoplásico INDICACIONES
1. NOMBRE DEL PRINCIPIO ACTIVO ACICLOVIR 2. VIA DE ADMINISTRACION INFUSION INTRAVENOSA
 1. NOMBRE DEL PRINCIPIO ACTIVO ACICLOVIR 2. VIA DE ADMINISTRACION INFUSION INTRAVENOSA 3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Antivirales de acción directa, nucleósidos y nucleótidos excluyendo
1. NOMBRE DEL PRINCIPIO ACTIVO ACICLOVIR 2. VIA DE ADMINISTRACION INFUSION INTRAVENOSA 3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Antivirales de acción directa, nucleósidos y nucleótidos excluyendo
INFORMACION PARA PRESCRIBIR AMPLIA:
 INFORMACION PARA PRESCRIBIR AMPLIA: 1. Nombre Comercial: CARBOPLAT 2. Nombre Genérico: CARBOPLATINO 3. Forma Farmacéutica y Formulación: Solución Inyectable. Cada frasco ámpula con liofilizado contiene:
INFORMACION PARA PRESCRIBIR AMPLIA: 1. Nombre Comercial: CARBOPLAT 2. Nombre Genérico: CARBOPLATINO 3. Forma Farmacéutica y Formulación: Solución Inyectable. Cada frasco ámpula con liofilizado contiene:
3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Antineoplásicos, análogos de pirimidina. Código ATC: L01BC05
 1. NOMBRE DEL PRINCIPIO ACTIVO (DCI) GEMCITABINA 2. VIA DE ADMINISTRACION INTRAVENOSA 3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Antineoplásicos, análogos de pirimidina. Código ATC: L01BC05
1. NOMBRE DEL PRINCIPIO ACTIVO (DCI) GEMCITABINA 2. VIA DE ADMINISTRACION INTRAVENOSA 3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Antineoplásicos, análogos de pirimidina. Código ATC: L01BC05
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: CALUTOL 2. Nombre Genérico: BICALUTAMIDA 3. Forma Farmacéutica y Formulación: Tabletas Cada tableta contiene: Bicalutamida.. 50 mg y 150 mg Excipiente
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: CALUTOL 2. Nombre Genérico: BICALUTAMIDA 3. Forma Farmacéutica y Formulación: Tabletas Cada tableta contiene: Bicalutamida.. 50 mg y 150 mg Excipiente
Docetoxel solución concentrado inyectable 80 mg
 Docetoxel solución concentrado inyectable 80 mg Guarde este folleto, puede necesitar leerlo nuevamente. Si tiene cualquier duda o no está seguro de algo, pregunte a su médico o químico farmacéutico. Composición
Docetoxel solución concentrado inyectable 80 mg Guarde este folleto, puede necesitar leerlo nuevamente. Si tiene cualquier duda o no está seguro de algo, pregunte a su médico o químico farmacéutico. Composición
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
FOLLETO DE INFORMACIÓN AL PROFESIONAL GEMCIMIRA SOLUCIÓN INYECTABLE 1g/26,3 ml GEMCIMIRA SOLUCION INYECTABLE 200 mg/5,3 ml (Gemcitabina clorhidrato)
 FOLLETO DE INFORMACIÓN AL PROFESIONAL GEMCIMIRA SOLUCIÓN INYECTABLE 1g/26,3 ml GEMCIMIRA SOLUCION INYECTABLE 200 mg/5,3 ml (Gemcitabina clorhidrato) 1. NOMBRE DEL MEDICAMENTO GEMCIMIRA Solución Inyectable
FOLLETO DE INFORMACIÓN AL PROFESIONAL GEMCIMIRA SOLUCIÓN INYECTABLE 1g/26,3 ml GEMCIMIRA SOLUCION INYECTABLE 200 mg/5,3 ml (Gemcitabina clorhidrato) 1. NOMBRE DEL MEDICAMENTO GEMCIMIRA Solución Inyectable
Estadíos tumor maligno de cuello uterino
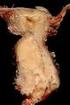 TUMOR MALIGNO DE CUELLO UTERINO Codificación CIE10 C53 tumor maligno del cuello del útero Problema: El cáncer cervical usualmente es un carcinoma de células escamosas (70% de todos los cánceres cervicales),
TUMOR MALIGNO DE CUELLO UTERINO Codificación CIE10 C53 tumor maligno del cuello del útero Problema: El cáncer cervical usualmente es un carcinoma de células escamosas (70% de todos los cánceres cervicales),
INFORMACIÓN PARA PRESCRIBIR AMPLIA DE ZOLSTRO
 INFORMACIÓN PARA PRESCRIBIR AMPLIA DE ZOLSTRO LETROZOL 1.- DENOMINACIÓN DISTINTIVA: ZOLSTRO 2.- DENOMINACIÓN GENÉRICA: LETROZOL 3.- FORMA FARMACEUTICA Y FORMULACION: F.F. TABLETAS Cada tableta recubierta
INFORMACIÓN PARA PRESCRIBIR AMPLIA DE ZOLSTRO LETROZOL 1.- DENOMINACIÓN DISTINTIVA: ZOLSTRO 2.- DENOMINACIÓN GENÉRICA: LETROZOL 3.- FORMA FARMACEUTICA Y FORMULACION: F.F. TABLETAS Cada tableta recubierta
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina ratiopharm 200 mg polvo para solución para perfusión EFG Gemcitabina ratiopharm 1 g polvo para solución
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina ratiopharm 200 mg polvo para solución para perfusión EFG Gemcitabina ratiopharm 1 g polvo para solución
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO MONTEVIDEO, URUGUAY.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: OXALIPLATINO 100 mg Liofilizado para
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: OXALIPLATINO 100 mg Liofilizado para
FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL
 FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL DOLGENAL Ketorolaco Trometamol 30 mg/1 ml Solución inyectable Vía de Administración: I.M. - I.V. Venta bajo receta médica en establecimientos
FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL DOLGENAL Ketorolaco Trometamol 30 mg/1 ml Solución inyectable Vía de Administración: I.M. - I.V. Venta bajo receta médica en establecimientos
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg Polvo para solución para perfusión EFG Gemcitabina Hospira 1 g Polvo para solución para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg Polvo para solución para perfusión EFG Gemcitabina Hospira 1 g Polvo para solución para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg Polvo para solución para perfusión EFG Gemcitabina Hospira 1 g Polvo para solución para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg Polvo para solución para perfusión EFG Gemcitabina Hospira 1 g Polvo para solución para
SODIOFOLIN 50 mg/ml solución para inyección o perfusión intravenosa
 L e a t o d o e l p r o s p e c t o d e t e n i d a m e n t e a n t e s d e e m p e z a r En este prospecto 1. Qué es Sodiofolin 50 mg/ml solución para inyección o perfusión intravenosa y para qué se utiliza
L e a t o d o e l p r o s p e c t o d e t e n i d a m e n t e a n t e s d e e m p e z a r En este prospecto 1. Qué es Sodiofolin 50 mg/ml solución para inyección o perfusión intravenosa y para qué se utiliza
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
FICHA TÉCNICA. La cantidad de principios activos presentes en 1 ml de ADDAMEL es de:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ADDAMEL concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de ADDAMEL contiene: Principio activo Cantidad Cloruro de cromo,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ADDAMEL concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de ADDAMEL contiene: Principio activo Cantidad Cloruro de cromo,
FICHA TECNICA DE ZOVIRAX INTRAVENOSO. Aciclovir (D.C.I) (sódico) mg
 FICHA TECNICA DE ZOVIRAX INTRAVENOSO NOMBRE DEL MEDICAMENTO ZOVIRAX INTRAVENOSO COMPOSICION CUALITATIVA Y CUANTITATIVA Cada vial contiene:: Aciclovir (D.C.I) (sódico)...250 mg FORMA FARMACEUTICA Vial liofilizado
FICHA TECNICA DE ZOVIRAX INTRAVENOSO NOMBRE DEL MEDICAMENTO ZOVIRAX INTRAVENOSO COMPOSICION CUALITATIVA Y CUANTITATIVA Cada vial contiene:: Aciclovir (D.C.I) (sódico)...250 mg FORMA FARMACEUTICA Vial liofilizado
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION
 SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Gemcitabina Pharm V Solutions 1000 mg polvo para solución para perfusión EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemcitabina Pharm V Solutions 1000 mg polvo para solución para perfusión EFG Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemcitabina Pharm V Solutions 1000 mg polvo para solución para perfusión EFG Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
FOLLETO DE INFORMACIÓN AL PROFESIONAL. CIMAherrr SOLUCIÓN INYECTABLE PARA PERFUSIÓN 50 mg/10 ml (NIMOTUZUMAB)
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: CIMAher (Nimotuzumab) Forma farmacéutica: Presentación: Inyección IV. Estuche con x frascos ampolla. Composición: Cada frasco ampolla contiene:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: CIMAher (Nimotuzumab) Forma farmacéutica: Presentación: Inyección IV. Estuche con x frascos ampolla. Composición: Cada frasco ampolla contiene:
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Gemcitabina Kewl 1000 mg polvo para solución para perfusión EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto, ya que puede tener que volver a leerlo. - Si tiene alguna duda,
PROSPECTO: INFORMACIÓN PARA EL USUARIO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto, ya que puede tener que volver a leerlo. - Si tiene alguna duda,
La citarabina, ARA-C o arabinósido de citocina es un antimetabolito específico de la fase S del ciclo celular; impide la síntesis de ADN.
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: MEDSARA 2. Nombre Genérico: CITARABINA 3. Forma Farmacéutica y Formulación: SOLUCIÓN INYECTABLE Cada frasco ámpula contiene: Citarabina.. 500 mg
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: MEDSARA 2. Nombre Genérico: CITARABINA 3. Forma Farmacéutica y Formulación: SOLUCIÓN INYECTABLE Cada frasco ámpula contiene: Citarabina.. 500 mg
UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C.
 UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C. I CONGRESO INTERNACIONAL DE ONCOLOGÍA: Avances y Retos AVANCES RECIENTES EN LA ADMINISTRACION DE QUIMIOTERAPIA EN CANCER DE MAMA
UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C. I CONGRESO INTERNACIONAL DE ONCOLOGÍA: Avances y Retos AVANCES RECIENTES EN LA ADMINISTRACION DE QUIMIOTERAPIA EN CANCER DE MAMA
FICHA TÉCNICA. Un ml de la solución para perfusión reconstituida contiene 38 mg de gemcitabina (como hidrocloruro).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina SUN 200 mg polvo para solución para perfusión EFG. Gemcitabina SUN 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina SUN 200 mg polvo para solución para perfusión EFG. Gemcitabina SUN 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION
 SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TOLFEDINE 4% 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. INGREDIENTES ACTIVOS: Ácido tolfenámico... 4,00 g EXCIPIENTES:
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TOLFEDINE 4% 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. INGREDIENTES ACTIVOS: Ácido tolfenámico... 4,00 g EXCIPIENTES:
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina medac 200 mg polvo para solución para perfusión EFG Gemcitabina medac 1000 mg polvo para solución para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina medac 200 mg polvo para solución para perfusión EFG Gemcitabina medac 1000 mg polvo para solución para
ambroxol cinfa 15 mg / 5 ml jarabe EFG
 FICHA TÉCNICA ambroxol cinfa 15 mg / 5 ml jarabe EFG 1. NOMBRE DEL MEDICAMENTO ambroxol cinfa 15 mg/5 ml jarabe EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA 5 ml de jarabe contienen 15 mg de clorhidrato
FICHA TÉCNICA ambroxol cinfa 15 mg / 5 ml jarabe EFG 1. NOMBRE DEL MEDICAMENTO ambroxol cinfa 15 mg/5 ml jarabe EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA 5 ml de jarabe contienen 15 mg de clorhidrato
COMPOSICIÓN CUALITATIVA Y CUANTITATIVA DE LA SUSTANCIA ACTIVA Y OTRAS SUSTANCIAS
 PROSPECTO NOMBRE O RAZON SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Y DEL FABRICANTE RESPONSABLE DE LA LIBERACIÓN DE LOS LOTES, EN CASO DE QUE SEAN DIFERENTES Titular
PROSPECTO NOMBRE O RAZON SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Y DEL FABRICANTE RESPONSABLE DE LA LIBERACIÓN DE LOS LOTES, EN CASO DE QUE SEAN DIFERENTES Titular
FICHA TÉCNICA. Cada ml de concentrado para solución para perfusión contiene 40 mg de gemcitabina (como hidrocloruro de gemcitabina).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Aurovitas 200 mg concentrado para solución para perfusión Gemcitabina Aurovitas 1.000 mg concentrado para solución para perfusión Gemcitabina Aurovitas
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Aurovitas 200 mg concentrado para solución para perfusión Gemcitabina Aurovitas 1.000 mg concentrado para solución para perfusión Gemcitabina Aurovitas
CARBOPLATINO IVAX 150
 CARBOPLATINO IVAX 150 CARBOPLATINO Inyectable Industria Argentina Venta bajo receta archivada FORMULA: CARBOPLATINO IVAX 150: Cada frasco ampolla contiene: Carboplatino 150 mg Excipiente: manitol c.s.
CARBOPLATINO IVAX 150 CARBOPLATINO Inyectable Industria Argentina Venta bajo receta archivada FORMULA: CARBOPLATINO IVAX 150: Cada frasco ampolla contiene: Carboplatino 150 mg Excipiente: manitol c.s.
NOROCARP COMPRIMIDOS 20 mg PARA PERROS NOROCARP COMPRIMIDOS 50 mg PARA PERROS PROSPECTO
 NOROCARP COMPRIMIDOS 20 mg PARA PERROS PROSPECTO CORREO ELECTRÓNICO Sugerencias_ft@aemps.es C/ CAMPEZO, 1 EDIFICIO 8 28022 MADRID PROSPECTO NOROCARP COMPRIMIDOS 20 mg PARA PERROS 1. NOMBRE O RAZÓN SOCIAL
NOROCARP COMPRIMIDOS 20 mg PARA PERROS PROSPECTO CORREO ELECTRÓNICO Sugerencias_ft@aemps.es C/ CAMPEZO, 1 EDIFICIO 8 28022 MADRID PROSPECTO NOROCARP COMPRIMIDOS 20 mg PARA PERROS 1. NOMBRE O RAZÓN SOCIAL
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. ACICLOVIR ACCORD INYECTABLE EFG Infusión intravenosa 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR ACCORD INYECTABLE EFG Infusión intravenosa 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene: Aciclovir (D.C.I.) (sódico) 250 mg 3. FORMA FARMACÉUTICA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR ACCORD INYECTABLE EFG Infusión intravenosa 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene: Aciclovir (D.C.I.) (sódico) 250 mg 3. FORMA FARMACÉUTICA
FICHA TÉCNICA. Gemcitabina Kewl mg: cada vial contiene hidrocloruro de gemcitabina equivalente a
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kewl 200 mg polvo para solución para perfusión EFG Gemcitabina Kewl 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kewl 200 mg polvo para solución para perfusión EFG Gemcitabina Kewl 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
Tratamiento del herpes genital inicial y recurrente, herpes labial y de infecciones mucocutáneas localizadas, producidas por virus de herpes simple
 1. NOMBRE DEL MEDICAMENTO ACICLOVIR DEXTER Crema E.F.G. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA ACICLOVIR DEXTER Crema E.F.G. Cada gramo contiene: Aciclovir (DCI)... 50 mg Excipientes, c.s. 3. FORMA
1. NOMBRE DEL MEDICAMENTO ACICLOVIR DEXTER Crema E.F.G. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA ACICLOVIR DEXTER Crema E.F.G. Cada gramo contiene: Aciclovir (DCI)... 50 mg Excipientes, c.s. 3. FORMA
DOCUMENTO LOCAL DE PRODUCTO
 DOCUMENTO LOCAL DE PRODUCTO Título del documento de producto: Pamoato de oxantel, Pamoato de pirantel Documento de producto No: 35 Fecha: 29 de agosto de 2008 Reemplaza a: 1 de agosto de 2003 1. NOMBRE(S)
DOCUMENTO LOCAL DE PRODUCTO Título del documento de producto: Pamoato de oxantel, Pamoato de pirantel Documento de producto No: 35 Fecha: 29 de agosto de 2008 Reemplaza a: 1 de agosto de 2003 1. NOMBRE(S)
FICHA TÉCNICA. Cada vial contiene hidrocloruro de gemcitabina equivalentes a 200 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemzar 200 mg polvo para solución para perfusión. Gemzar 1.000 mg polvo para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemzar 200 mg polvo para solución para perfusión. Gemzar 1.000 mg polvo para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene
FICHA TÉCNICA. Cada vial contiene hidrocloruro de gemcitabina equivalentes a 200 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemzar 200 mg polvo para solución para perfusión. Gemzar 1.000 mg polvo para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemzar 200 mg polvo para solución para perfusión. Gemzar 1.000 mg polvo para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene
FICHA TÉCNICA. Concentración Cantidad de gemcitabina (como hidrocloruro)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg concentrado para solución para perfusión Gemcitabina Hospira 1000 mg concentrado para solución para perfusión Gemcitabina Hospira 2000
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg concentrado para solución para perfusión Gemcitabina Hospira 1000 mg concentrado para solución para perfusión Gemcitabina Hospira 2000
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. ARGENTINA. 40,0 mg. 4000,0 mg 5,0 mg. 10,0 ml
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Nombre del producto: Ulcozol 40 (omeprazol) Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: Polvo liofilizado
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Nombre del producto: Ulcozol 40 (omeprazol) Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: Polvo liofilizado
FICHA TÉCNICA. Normoreum 400 mg comprimidos recubiertos con película
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada película bucodispersable contiene 16 mg de extracto (como extracto seco) de hoja
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada película bucodispersable contiene 16 mg de extracto (como extracto seco) de hoja
No es necesario modificar el régimen terapéutico en pacientes con insuficiencia renal, hepática o en ancianos.
 1. NOMBRE DEL MEDICAMENTO Troxerutina Pensa 100 mg/ml solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución oral contiene 100 mg de Troxerutina. Excipientes: Cada ml de solución
1. NOMBRE DEL MEDICAMENTO Troxerutina Pensa 100 mg/ml solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución oral contiene 100 mg de Troxerutina. Excipientes: Cada ml de solución
Se recomiendan las siguientes modificaciones en caso de disfunción renal. (ml/min) mg/kg cada 8 horas 10 mg/kg cada 8 horas
 1. NOMBRE DEL MEDICAMENTO ACICLOVIR SALA 250 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITITATIVA Y CUANTITATIVA Cada vial contiene: Aciclovir (D.O.E.) (sódico) 250 mg Para excipientes,
1. NOMBRE DEL MEDICAMENTO ACICLOVIR SALA 250 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITITATIVA Y CUANTITATIVA Cada vial contiene: Aciclovir (D.O.E.) (sódico) 250 mg Para excipientes,
CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG
 CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG COMPOSICIÓN Por ml: Principio activo: Carboplatino (D.C.I.) 10 mg Excipientes: Agua para inyección c.s. FORMA FARMACÉUTICA Y
CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG COMPOSICIÓN Por ml: Principio activo: Carboplatino (D.C.I.) 10 mg Excipientes: Agua para inyección c.s. FORMA FARMACÉUTICA Y
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METOCLOPRAMIDA 10 mg COMPRIMIDOS RECUBIERTOS ANTIHEMÉTICO Página 1 METOCLOPRAMIDA 10 mg Comprimidos Recubiertos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METOCLOPRAMIDA 10 mg COMPRIMIDOS RECUBIERTOS ANTIHEMÉTICO Página 1 METOCLOPRAMIDA 10 mg Comprimidos Recubiertos
FICHA TÉCNICA. Un mililitro de la solución reconstituida contiene 38 mg de gemcitabina (como hidrocloruro)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina GP-Pharm 200 mg polvo para solución para perfusión EFG Gemcitabina GP-Pharm 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina GP-Pharm 200 mg polvo para solución para perfusión EFG Gemcitabina GP-Pharm 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
Venoruton 1000, Sobres Sabor naranja Venoruton 500, Sobres Sabor naranja Venoruton 300, Cápsulas Troxerutina
 FICHA TÉCNICA Troxerutina 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUANTITATIVA Y CUALITATIVA : Cada sobre contiene: Troxerutina (DOE) 1000 mg : Cada sobre contiene: Troxerutina (DOE) 500 mg Cada cápsula
FICHA TÉCNICA Troxerutina 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUANTITATIVA Y CUALITATIVA : Cada sobre contiene: Troxerutina (DOE) 1000 mg : Cada sobre contiene: Troxerutina (DOE) 500 mg Cada cápsula
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
ESTAVUDINA 40 mg Cápsulas
 ESTAVUDINA 40 mg Cápsulas ESTAVUDINA 40 mg Cápsulas COMPOSICIÓN Cada cápsula contiene: Estavudina 40 mg Excipientes c.s.p INDICACIONES Estavudina está indicada para el tratamiento de pacientes con infección
ESTAVUDINA 40 mg Cápsulas ESTAVUDINA 40 mg Cápsulas COMPOSICIÓN Cada cápsula contiene: Estavudina 40 mg Excipientes c.s.p INDICACIONES Estavudina está indicada para el tratamiento de pacientes con infección
Ácido cítrico anhidro mg
 DIFENHIDRAMINA CLORHIDRATO Solución (Jarabe) Control Médico Recomendado Industria Argentina Cada 100 ml de jarabe contiene: DIFENHIDRAMINA CLORHIDRATO.. 250 mg Ácido cítrico anhidro... 400 mg 1 / 9 Benzoato
DIFENHIDRAMINA CLORHIDRATO Solución (Jarabe) Control Médico Recomendado Industria Argentina Cada 100 ml de jarabe contiene: DIFENHIDRAMINA CLORHIDRATO.. 250 mg Ácido cítrico anhidro... 400 mg 1 / 9 Benzoato
FICHA TÉCNICA. Alivio a corto plazo (de dos o tres meses) del edema y síntomas relacionados con la insuficiencia venosa crónica.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Troxerutina NORMON 1000 mg granulado para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 1000 mg de troxerutina. Excipientes: Isomaltosa,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Troxerutina NORMON 1000 mg granulado para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 1000 mg de troxerutina. Excipientes: Isomaltosa,
Se recomiendan las siguientes modificaciones en caso de disfunción renal.
 1. NOMBRE DEL MEDICAMENTO ACICLOVIR TEDEC 25 mg/ml solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla contiene: Aciclovir (D.O.E.) 250 mg Para excipientes, ver 6.1. 3. FORMA
1. NOMBRE DEL MEDICAMENTO ACICLOVIR TEDEC 25 mg/ml solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla contiene: Aciclovir (D.O.E.) 250 mg Para excipientes, ver 6.1. 3. FORMA
Cada ampolleta contiene: Clorhidrato dihidratado de ondansetrón equivalente a 4 mg 8 mg de Ondansetron. Excipiente, c.b.p... 2.
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: MODIFICAL 2. Nombre Genérico: ONDANSETRÓN 3. Forma Farmacéutica y Formulación: Solución Inyectable Cada ampolleta contiene: Clorhidrato dihidratado
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: MODIFICAL 2. Nombre Genérico: ONDANSETRÓN 3. Forma Farmacéutica y Formulación: Solución Inyectable Cada ampolleta contiene: Clorhidrato dihidratado
FICHA TÉCNICA. Gemcitabina Accord 200 mg: un vial contiene hidrocloruro de gemcitabina equivalentes a 200 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Accord 200 mg polvo para solución para perfusión EFG Gemcitabina Accord 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Accord 200 mg polvo para solución para perfusión EFG Gemcitabina Accord 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. Gemcitabina Accord 200 mg: un vial contiene hidrocloruro de gemcitabina equivalentes a 200 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Accord 200 mg polvo para solución para perfusión EFG Gemcitabina Accord 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Accord 200 mg polvo para solución para perfusión EFG Gemcitabina Accord 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
INFORMACIÓN PARA PRESCRIBIR AMPLIA
 INFORMACIÓN PARA PRESCRIBIR AMPLIA IFADEX MR Ifosfamida Laboratorios Cryopharma, S.A. de C.V INFORMACIÓN PARA PRESCRIBIR AMPLIA 1.- NOMBRE COMERCIAL Y GENÉRICO: 1.1 Nombre comercial: IFADEX MR 1.2 Nombre
INFORMACIÓN PARA PRESCRIBIR AMPLIA IFADEX MR Ifosfamida Laboratorios Cryopharma, S.A. de C.V INFORMACIÓN PARA PRESCRIBIR AMPLIA 1.- NOMBRE COMERCIAL Y GENÉRICO: 1.1 Nombre comercial: IFADEX MR 1.2 Nombre
PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica
 ÁCIDOS ENÓLICOS PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica MECANISMO DE ACCIÓN de prostaglandinas. INHIBICIÓN DE LA COX Inhibe la migración de PMN y monocitos a lugar de
ÁCIDOS ENÓLICOS PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica MECANISMO DE ACCIÓN de prostaglandinas. INHIBICIÓN DE LA COX Inhibe la migración de PMN y monocitos a lugar de
Prospecto: información para el usuario. Gemcitabina Hospira 1000 mg concentrado para solución para perfusión
 Prospecto: información para el usuario Gemcitabina Hospira 1000 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: información para el usuario Gemcitabina Hospira 1000 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CLORANFENICOL 500 mg CÁPSULA ANTIINFECCIOSO Página 1 CLORANFENICOL 500 mg Cápsula Principio Activo Cloranfenicol
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CLORANFENICOL 500 mg CÁPSULA ANTIINFECCIOSO Página 1 CLORANFENICOL 500 mg Cápsula Principio Activo Cloranfenicol
FICHA TÉCNICA. Un ml de la solución para perfusión reconstituida contiene 38 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kabi 200 mg polvo para solución para perfusion EFG Gemcitabina Kabi 1000 mg polvo para solución para perfusion EFG Gemcitabina Kabi 2000 mg polvo para
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kabi 200 mg polvo para solución para perfusion EFG Gemcitabina Kabi 1000 mg polvo para solución para perfusion EFG Gemcitabina Kabi 2000 mg polvo para
SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS
 SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante
SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante
FICHA TÉCNICA. Una vez reconstituida, 1 ml de la solución contiene 38 mg/ml de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hetero 200 mg polvo para solución para perfusión EFG Gemcitabina Hetero 1.000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hetero 200 mg polvo para solución para perfusión EFG Gemcitabina Hetero 1.000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y
Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol.
 1. NOMBRE DEL MEDICAMENTO TROSID 280 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol. Para consultar la
1. NOMBRE DEL MEDICAMENTO TROSID 280 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol. Para consultar la
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 250 mg/5 ml SUSPENSIÓN ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 250 mg/5 ml Suspensión
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 250 mg/5 ml SUSPENSIÓN ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 250 mg/5 ml Suspensión
MUCOSEC Ambroxol clorhidrato 300 mg Jarabe
 MUCOSEC Ambroxol clorhidrato 300 mg Jarabe MUCOSEC PEDIÁTRICO 15 mg / 5 ml JARABE Ambroxol clorhidrato EXPECTORANTE MUCOLÍTICO COMPOSICIÓN: Cada 100 ml contiene: Ambroxol clorhidrato...300 mg Excipientes...c.s.p.
MUCOSEC Ambroxol clorhidrato 300 mg Jarabe MUCOSEC PEDIÁTRICO 15 mg / 5 ml JARABE Ambroxol clorhidrato EXPECTORANTE MUCOLÍTICO COMPOSICIÓN: Cada 100 ml contiene: Ambroxol clorhidrato...300 mg Excipientes...c.s.p.
MANEJO DE RAM JOSÉ CORNEJO GARCÍA NEUMÓLOGO HOSPITAL NACIONAL ARZOBISPO LOAYZA
 MANEJO DE RAM JOSÉ CORNEJO GARCÍA NEUMÓLOGO HOSPITAL NACIONAL ARZOBISPO LOAYZA QUE ES UNA RAM? Es una reacción adversa, no deseada ni intencionada, de un paciente a un fármaco adecuadamente administrado,
MANEJO DE RAM JOSÉ CORNEJO GARCÍA NEUMÓLOGO HOSPITAL NACIONAL ARZOBISPO LOAYZA QUE ES UNA RAM? Es una reacción adversa, no deseada ni intencionada, de un paciente a un fármaco adecuadamente administrado,
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea
 FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FARMIBLASTINA SOLUCION 50 mg (doxorubicina) Solución inyectable VIA INTRAVENOSA
 FARMIBLASTINA SOLUCION 50 mg (doxorubicina) Solución inyectable VIA INTRAVENOSA COMPOSICIÓN FARMIBLASTINA SOLUCION 50 mg: Vial conteniendo en solución 50 mg de doxorubicina (DCI) (clorhidrato) y excipientes:
FARMIBLASTINA SOLUCION 50 mg (doxorubicina) Solución inyectable VIA INTRAVENOSA COMPOSICIÓN FARMIBLASTINA SOLUCION 50 mg: Vial conteniendo en solución 50 mg de doxorubicina (DCI) (clorhidrato) y excipientes:
Comprimidos de 300 mg: Úlcera duodenal. Úlcera gástrica benigna. Esofagitis por reflujos. Síndrome de Zollinger-Ellison.
 FICHA TECNICA 1.-NOMBRE DE LA ESPECIALIDAD FARMACEUTICA Ranitidina Bexal 150 mg EFG Ranitidina Bexal 300 mg EFG 2.-COMPOSICION CUALITATIVA Y CUANTITATIVA Ranitidina 150 mg y 300 mg como clorhidrato de
FICHA TECNICA 1.-NOMBRE DE LA ESPECIALIDAD FARMACEUTICA Ranitidina Bexal 150 mg EFG Ranitidina Bexal 300 mg EFG 2.-COMPOSICION CUALITATIVA Y CUANTITATIVA Ranitidina 150 mg y 300 mg como clorhidrato de
FICHA TÉCNICA. La composición cuantitativa de cada presentación se proporciona en la tabla siguiente:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kabi 200 mg concentrado para solución para perfusión Gemcitabina Kabi 1000 mg concentrado para solución para perfusión Gemcitabina Kabi 2000 mg concentrado
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kabi 200 mg concentrado para solución para perfusión Gemcitabina Kabi 1000 mg concentrado para solución para perfusión Gemcitabina Kabi 2000 mg concentrado
Cada mililitro de concentrado para solución para perfusión contiene 45,6 mg de hidrocloruro de gemcitabina equivalentes a 40 mg de gemcitabina.
 1. NOMBRE DEL MEDICAMENTO Gemcitabina Sandoz 200 mg concentrado para solución para perfusión Gemcitabina Sandoz 1000 mg concentrado para solución para perfusión Gemcitabina Sandoz 2000 mg concentrado para
1. NOMBRE DEL MEDICAMENTO Gemcitabina Sandoz 200 mg concentrado para solución para perfusión Gemcitabina Sandoz 1000 mg concentrado para solución para perfusión Gemcitabina Sandoz 2000 mg concentrado para
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERITROMICINA 500 mg COMPRIMIDOS RECUBIERTOS ANTIBIÓTICO Página 1 ERITROMICINA 500 mg Comprimidos Recubiertos Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERITROMICINA 500 mg COMPRIMIDOS RECUBIERTOS ANTIBIÓTICO Página 1 ERITROMICINA 500 mg Comprimidos Recubiertos Principio
Alivio de la inflamación y el dolor en trastornos músculo-esqueléticos agudos y crónicos en perros.
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Meloxoral 1,5 mg/ml suspensión oral para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam 1,5 mg. Excipiente: Benzoato
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Meloxoral 1,5 mg/ml suspensión oral para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam 1,5 mg. Excipiente: Benzoato
VILTAR LOPERAMIDA. Comprimidos - Gotas FORMULA. Comprimidos. Cada comprimido contiene: Loperamida Clorhidrato
 VILTAR LOPERAMIDA Comprimidos - Gotas Industria Argentina Venta bajo receta FORMULA Comprimidos Cada comprimido contiene: Loperamida Clorhidrato 2 mg. Excipientes : Lactosa - Almidón de maiz - Almidón
VILTAR LOPERAMIDA Comprimidos - Gotas Industria Argentina Venta bajo receta FORMULA Comprimidos Cada comprimido contiene: Loperamida Clorhidrato 2 mg. Excipientes : Lactosa - Almidón de maiz - Almidón
Tableta recubierta. 8 mg. 88,0 mg. 24 meses
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: ONDANSETRÓN Forma farmacéutica: Tableta recubierta Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: 8 mg
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: ONDANSETRÓN Forma farmacéutica: Tableta recubierta Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: 8 mg
Resumen de las características del producto. 1 ml. Para consultar la lista completa de excipientes, ver sección 6.1.
 Resumen de las características del producto 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables B.Braun Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio Activo
Resumen de las características del producto 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables B.Braun Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio Activo
Prospecto: información para el usuario. Gemcitabina Hospira 200 mg concentrado para solución para perfusión
 Prospecto: información para el usuario Gemcitabina Hospira 200 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: información para el usuario Gemcitabina Hospira 200 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION
 SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
PP060912_2+1A (II28) PROSPECTO: INFORMACIÓN PARA EL USUARIO. Gemzar 200 mg polvo para solución para perfusión Gemcitabina
 PP060912_2+1A (II28) PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemzar 200 mg polvo para solución para perfusión Gemcitabina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
PP060912_2+1A (II28) PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemzar 200 mg polvo para solución para perfusión Gemcitabina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
DRAGOXILO Suspensión Oral
 DRAGOXILO Suspensión Oral ANTIMICROBIANO DE AMPLIO ESPECTRO. Dragoxilo polvo para reconstituir suspensión oral, está indicado en el tratamiento de infecciones de la piel y tejidos blandos provocadas por
DRAGOXILO Suspensión Oral ANTIMICROBIANO DE AMPLIO ESPECTRO. Dragoxilo polvo para reconstituir suspensión oral, está indicado en el tratamiento de infecciones de la piel y tejidos blandos provocadas por
