JANUMET (Merck Sharp & Dohme) VELMETIA (Ferrer Grupo) EFFICIB (Almirall) 50 mg/1.000 mg 56 comprimidos recubiertos (61,19 )
|
|
|
- Alberto Ramos González
- hace 7 años
- Vistas:
Transcripción
1 - COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN NUEVA ASOCIACIÓN SITAGLIPTINA/METFORMINA NO SUPONE UN AVANCE TERAPÉUTICO Nombre Comercial y presentaciones: JANUMET (Merck Sharp & Dohme) VELMETIA (Ferrer Grupo) EFFICIB (Almirall) 50 mg/1.000 mg 56 comprimidos recubiertos (61,19 ) Condiciones de dispensación: Con receta médica Fecha de evaluación: Marzo 2009 Fecha de autorización: Julio 2008 Procedimiento de autorización: Centralizado Grupo Terapéutico: A10BD07. Combinaciones de fármacos hipoglucemiantes orales. INDICACIONES APROBADAS 1 La asociación a dosis fijas de sitagliptina/metformina (SI/ME) está indicada, como adyuvante a la dieta y el ejercicio, en pacientes ya tratados con la combinación de sitagliptina y metformina y en pacientes que no controlan su glucemia adecuadamente con: i) la dosis máxima tolerada de metformina en monoterapia, ii) la dosis máxima tolerada de metformina y una sulfonilurea, iii) la dosis máxima tolerada de metformina y una glitazona, iv) una dosis estable de insulina y metformina. Contraindicaciones - Insuficiencia renal o hepática. MECANISMO DE ACCIÓN La SI es un inhibidor de la enzima dipeptidil-peptidasa 4 (DPP-4) que inactiva las hormonas incretinas, entre las que se incluyen el péptido-1 similar al glucagón (GLP-1) y el péptido insulinotrópico dependiente de la glucosa (GIP). Tanto GLP-1 como GIP aumentan la síntesis y liberación de insulina por las células beta pancreáticas, incrementando la captación tisular de glucosa, y disminuyendo la secreción de glucagón de las celulas alfa pancreáticas. Estas hormonas son liberadas por el intestino y sus niveles aumentan en respuesta al contenido en glucosa de las comidas. La SI, al inhibir la DPP-4, produce un incremento de las concentraciones de las formas activas de GLP-1 y GIP, lo que conlleva un aumento en la liberación de insulina y reducción en los niveles de glucagón 3. Por su parte, la ME actúa principalmente sobre la producción hepática de glucosa, inhibiendo de gluconeogénesis y glucogenolisis; asimismo, también reduce la absorción intestinal de glucosa y aumenta la sensibilidad del músculo a la insulina, mejorando la captación y utilización de la glucosa periférica. Su acción produce reducción de la glucosa plasmática, tanto basal como postprandrial 1,2. FARMACOCINÉTICA Se ha demostrado la bioequivalencia de la asociación a dosis fijas SI/ME con la administración conjunta de SI+ME 1,2. 1
2 POSOLOGÍA Y FORMA DE ADMINISTRACIÓN Vía oral. La asociación a dosis fijas de SI/ME debe administrarse dos veces al día con las comidas para reducir las reacciones adversas gastrointestinales asociadas a la ME 1. La posología debe ser individualizada en cada paciente, sin superar la dosis máxima recomendada de SI (100 mg/d). Así: - en pacientes previamente tratados con ME, se recomienda administrar una dosis diaria de ME similar a la utilizada por el paciente y 50 mg de SI dos veces al día (dosis total diaria de 100 mg), - en los pacientes tratados con la combinación SI+ME (administrados por separado), deben mantenerse las mismas dosis que se venían empleando, - en los pacientes tratados con la combinación de ME (dosis máxima tolerada)+su, se recomienda iniciar el tratamiento con la asociación SI/ME utilizando dosis de 50 mg de SI, e igual dosis de ME a la que utilizaba previamente el paciente; no obstante, puede ser necesario reducir la dosis de SU a fin de evitar hipoglucemias, - en pacientes que no controlen adecuadamente su glucemia con la terapia de combinación doble con ME a la dosis máxima tolerada y una glitazona, la dosis de SI/ME consistirá en 50 mg de SI dos veces al día (dosis total diaria de 100 mg) y dosis de ME similar a la que ya se estaba tomando el paciente 1,2. EFICACIA CLÍNICA Los estudios publicados han evaluado variables intermedias por lo que no se dispone de datos sobre los efectos a largo plazo del tratamiento con SI/ME sobre las complicaciones de la diabetes mellitus (DM). Se dispone de un estudio clínico realizado en pacientes con DM2, que no controlan su glucemia con dieta y ejercicio, comparándose la terapia inicial con SI/ME (indicación no autorizada) frente a placebo, y frente a cada uno de los componentes en monoterapia, pero no frente a la administración conjunta de SI y ME administrados por separado. Se trata de un ensayo aleatorizado doble ciego, de 24 semanas de duración, en el que se incluyeron pacientes con DM2 que fueron distribuidos en seis grupos de tratamiento: placebo, ME mg, ME 2000 mg, SI 100 mg, SI 100 mg/me mg y SI 100 mg/me mg. Los cambios en la HbA1c respecto a placebo fueron estadísticamente significativos (p<0,001) para todos los grupos, si bien las mayores reducciones se observaron en los grupos tratados con la terapia combinada, SI 100 mg/me 1000 mg: -1,57% (IC 95%: de -1,80 a -1,34) y SI 100 mg/me mg: -2,07% (IC 95%: de -2,30 a -1,84) 4. Recientemente se ha publicado la continuación de este estudio durante 30 semanas más, destinado a evaluar la eficacia y seguridad a largo plazo del tratamiento combinado (54 semanas). Un total de 885 pacientes continuaron la segunda fase de 30 semanas. Los pacientes se aleatorizaron en 5 grupos: placebo+me mg, ME mg, ME mg, SI 100 mg, SI 100 mg+me mg y SI 100 mg+me mg. A las 54 semanas, la reducción en la HbA1c respecto al valor basal en los grupos tratados con la combinación fue de: -1,4% (IC 95%: de -1,6 a -1,3) y -1,8% (IC 95%: de -2,0 a -1,7), respectivamente. Al incluir en el análisis sólo los datos de los pacientes que completaron el estudio, la reducción en la HbA1 fue algo mayor: -1,7% (IC 95%: de -1,8 a -1,5) y -1,9% (IC 95%: de -2,1 a -1,8) 5. Se han publicado dos ensayos clínicos destinados a evaluar los efectos de la adición de SI al tratamiento previo con ME mg/d, en pacientes en los que éste resulta insuficiente para controlar la glucemia. En los dos estudios se compara la adición de SI 100 mg/d frente a placebo 6,7. En el primero de ellos, de 24 semanas de duración, y en el que participaron 701 pacientes, se observó en el grupo SI+ME una disminución significativa de la HbA1c de 7,96% a 7,26%, siendo la diferencia frente a placebo de -0,65% (IC 95%: de -0,77 a -0,53) (p<0,001), mientras que en el grupo placebo la reducción no fue significativa 6. El otro estudio controlado frente a placebo, de 30 semanas de duración, incluyó 190 pacientes con DM2 en los que se observó una diferencia en la disminución de la HbA1c respecto al grupo control de -1,0% (IC 95%: de - 1,40 a -0,7) en la semana 18 (variable principal) y de -1,0% (IC 95%: de -1,40 a -0,6) en la semana 30 (variable secundaria), siendo la diferencia significativa en ambos casos (p<0,001) 7. Se dispone de dos estudios comparativos frente a otros antidiabéticos 8,9. Así, en un ensayo de no-inferioridad realizado en pacientes no controlados adecuadamente con ME (dosis media mg/d), se comparó el efecto de la adición de SI (100 mg/d) frente a la adición de glipizida, a dosis media de 10,3 mg, posología que es inferior a la dosis máxima autorizada (40 mg/d). Tras 52 semanas, los cambios en HbA1c con respecto al valor 2
3 basal (7,5 %) fueron de -0,67% en ambos grupos (SI+ME y glipizida+me), alcanzándose el criterio de no-inferioridad preestablecido (cambio medio HbA1c 0,3%). El porcentaje de abandonos fue del 34% en los pacientes tratados con SI y 29 % en los tratados con glipizida. En el grupo de la SI+ME hubo más pacientes que abandonaron el tratamiento por falta de eficacia comparado con los pacientes tratados con glipizida+me (15% frente al 10%). Los tratados con SI+ME dejaron el tratamiento principalmente al comienzo del estudio, mientras que los tratados con glipizida+me lo hicieron al final 8. También se ha comparado la combinación SI 100 mg/d+me mg/d frente a rosiglitazona 8 mg/d+me mg/d y frente a placebo+me mg/d en 273 pacientes con DM2 no controlados adecuadamente tras recibir tratamiento con ME. A las 18 semanas del inicio del estudio no se observaron diferencias significativas en los niveles plasmáticos de HbA1c entre la doble terapia SI+ME y rosiglitazona+me 9. La terapia triple SI+glimepirida+ME se ha ensayado en un estudio de 24 semanas de duración que incluyó 441 pacientes con DM2. En este estudio se comparó, frente a placebo, la adición de SI 100 mg/d al tratamiento con glimepirida 4-8 mg/d, con o sin ME mg/d, observándose una disminución en los niveles de HbA1c a las 24 semanas de -0,59% con la terapia triple SI+glimepirida+ME, mientras que en el grupo placebo+glimepirida+me, dichos niveles se incrementaron un 0,3%. La diferencia entre los grupos fue de -0,89% (IC 95%: de -1,10 a -0,68) (p 0,001) 10. SEGURIDAD Reacciones adversas El mecanismo de acción de SI permite reducir la glucemia sin estimular la secreción de insulina y, por lo tanto, se asocia a una baja incidencia de hipoglucemias, siendo neutro su efecto sobre el peso 1,2. El tratamiento con SI se ha asociado con un incremento en la incidencia de infecciones, infestaciones y alteraciones gastrointestinales; asimismo también puede asociarse a trastornos musculoesqueléticos, neurotoxicidad y alteraciones de la piel y tejidos subcutáneos, incluyendo urticaria 2. Se desconoce la repercusión a largo plazo de la inhibición de la enzima DPP-4 sobre el sistema inmunitario 3. Los efectos adversos más comúnmente asociados al tratamiento con ME son: dolor abdominal, diarrea y anorexia; que se presentan con una tasa de incidencia en torno al 20%, que no parece incrementarse al añadir SI. De forma poco frecuente también se ha asociado al tratamiento con ME reducción de los niveles plasmáticos de vitamina B12, acidosis láctica, urticaria, eritema, prurito y trastornos hepáticos y renales, así como sabor metálico 1,2. En los ensayos clínicos con SI+ME, las náuseas se han comunicado frecuentemente ( 1/100 a <1/10); mientras que la somnolencia, diarrea y dolor abdominal fueron poco frecuentes ( 1/1.000 a <1/100). La incidencia de hipoglucemia fue muy frecuente ( 1/10) en los pacientes tratados con SI+ME+SU. En los pacientes tratados con SI+ME fue inferior a la observada con glipizida+me, y similar a la de placebo+me 1. Tras la comercialización de SI/ME y de SI, se han notificado 88 casos de pancreatitis aguda en pacientes tratados con SI o SI/ME, de los que un 66% requirió hospitalización 11. También se han notificado reacciones de hipersensibilidad (anafilaxia, angioedema, erupción, urticaria y casos de síndrome de Stevens-Johnson) 1. Precauciones especiales de uso, interacciones, utilización en grupos especiales 1 - Evitar el consumo de alcohol. - Antes de la administración de contrastes radiológicos iodados, debe suspenderse el tratamiento con SI/ME. - En pacientes tratados con corticosteroides, IECA y digoxina, se requieren precauciones adicionales, como el seguimiento de la glucemia y el ajuste de la dosis. 3
4 RESUMEN ANÁLISIS COMPARATIVO Fármaco comparador: SI+ME (administrados por separado), vildagliptina/me, SU+ME como combinación más recomendada y glitazona+me en pacientes con intolerancia a SU. 1. Eficacia: la eficacia de la asociación SI+ME (en preparados diferentes) fue superior a ME en monoterapia, no-inferior a glipizida+me y similar a rosiglitazona+me; no se ha comparado frente a pioglitazona+me. La asociación de SI+glimepirida+ME (en preparados diferentes) se mostró más eficaz que placebo+glimepirida+me. 2. Seguridad: la asociación SI+ME (en preparados diferentes) se asoció a menor incidencia de hipoglucemias y menos incremento de peso que glipizida+me. Se desconoce la repercusión a largo plazo de la inhibición del enzima DPP-4 sobre el sistema inmunitario. 3. Pauta: la nueva asociación SI/ME presenta la ventaja potencial de administrar menos formas orales en cada toma. 4. Coste: superior a la combinación SI+ME administrados por separado. Similar al de las asociaciones a dosis fijas de vildagliptina/me, pioglitazona/me y rosiglitazona/me. Superior a otras combinaciones de antidiabéticos orales con ME en preparados diferentes (glipizida+me y glimepirida+me). COSTE TRATAMIENTO ( )/DÍA Sitagliptina/Metformina (100/2000mg) Sitagliptina (100mg) + Metformina (1700mg) Vildagliptina/Metformina (100/1700mg) Vildagliptina/Metformina (100/2000mg) Metformina (1700mg) + Glipizida (20mg) 0,26 2,19 2,09 2,19 2,19 Metformina (1700mg) + Glimepirida (2mg) Rosiglitazona/Metformina (4/2000mg) 0,21 1,44 Rosiglitazona/Metformina (8/2000mg) Metformina/Pioglitazona (1700/30mg) 2,14 2,14 0,00 0,50 1,00 1,50 2,00 2,50 LUGAR EN TERAPÉUTICA Cuando las medidas no farmacológicas dieta y ejercicio son insuficientes para conseguir un control glucémico adecuado, la mayoría de las guías sobre DM2 recomiendan el tratamiento con ME en monoterapia. Cuando ésta resulta insuficiente, proponen la adición de una sulfonilurea (ME+SU) En España, el Grupo de Estudio para la Diabetes en Atención Primaria (GEDAPS) recomienda la adición de un inhibidor de la DPP-4 (gliptina) al tratamiento con ME como una alternativa a las SU a igual nivel que una glitazona, glinida o un inhibidor de α- glucosidasas 15. El National Institute for Health and Clinical Excellence (NICE) británico considera las gliptinas (sitagliptina, vildagliptina) o las glitazonas (pioglitazona, rosiglitazona), como alternativa a las SU si éstas están contraindicadas, no se toleran o hay riesgo significativo de hipoglucemia; siendo preferible una gliptina a una glitazona si el aumento de peso supone un problema grave 12. La eficacia y seguridad de la administración a dosis fija SI/ME no se ha evaluado frente a la de ambos principios activos en preparados diferentes. Considerando los estudios realizados con SI+ME administrados por separado, su eficacia en la reducción de los niveles de HbA1c fue similar a la de rosiglitazona+me 9 y no-inferior a la de glipizida+me 8. Se desconocen las consecuencias sobre el sistema inmunitario de la inhibición de la DPP-4 a largo plazo. 4
5 A la vista de las evidencias disponibles, la comercialización de la nueva asociación a dosis fijas SI/ME no parece aportar ventajas frente a las alternativas disponibles, no suponiendo un avance terapéutico en el tratamiento de la DM2. CONCLUSIONES: La asociación a dosis fijas de sitagliptina/metformina ha sido autorizada, como tratamiento adyuvante a la dieta y el ejercicio, en pacientes ya tratados con la combinación de sitagliptina y metformina y en pacientes que no controlan su glucemia adecuadamente con: i) la dosis máxima tolerada de metformina en monoterapia, ii) la dosis máxima tolerada de metformina y una sulfonilurea, iii) la dosis máxima tolerada de metformina y una glitazona, iv) una dosis estable de insulina y metformina. EFICACIA: los estudios realizados con la combinación sitagliptina+metformina administrados por separado muestran eficacia no-inferior a glipizida+metformina y similar a rosiglitazona+metformina en cuanto a la reducción de la hemoglobina glicosilada. SEGURIDAD: el tratamiento con sitagliptina+metformina se ha asociado a una menor incidencia de hipoglucemias que la observada con glipizida+metformina. Los estudios clínicos han mostrado un incremento de la frecuencia de infecciones en los pacientes tratados con sitagliptina, desconociéndose las repercusiones del tratamiento a largo plazo sobre el sistema inmunitario. A la vista de las evidencias disponibles, no parece que la asociación sitagliptina/metformina aporte ventajas frente a las alternativas disponibles, por lo que no supone un avance terapéutico. FRASE RESUMEN: continuar utilizando los tratamientos actualmente recomendados cuando se precise la terapia combinada con dos fármacos, en pacientes con diabetes mellitus 2 que no alcanzan el control glucémico suficiente con la dosis óptima de metformina en monoterapia. CALIFICACIÓN: NO SUPONE UN AVANCE TERAPÉUTICO Esta evaluación ha sido realizada de acuerdo con el Procedimiento Normalizado de Trabajo de los Comités de Evaluación de Nuevos Medicamentos de Andalucía, Aragón, Cataluña, Euskadi y Navarra. La evaluación de novedades terapéuticas en el momento de su comercialización se apoya en información cuya validez puede verse limitada con el paso del tiempo, por lo que debe ser empleada con precaución. Queda totalmente prohibido el uso de este documento con fines promocionales. 5
6 COMITÉ DE REDACCIÓN - Iñigo Aizpurua Imaz. Farmacéutico de CEVIME. Departamento de Sanidad. - Susana Fernández Gallastegui. Farmacéutica de Atención Primaria; Comarca Uribe. Osakidetza. - Julia Fernández Uria. Farmacéutica de Atención Primaria; Comarca Bilbao. Osakidetza. - Juan José García Albás. Farmacéutico de Farmacia Hospitalaria; Hospital de Txagorritxu. Osakidetza. - Josu Ibarra Amarica. Médico de Atención Primaria; Comarca Araba. Osakidetza. - Nekane Jaio Atela. Farmacéutica de Atención Primaria; Comarca Interior. Osakidetza. - Itxasne Lekue Alkorta. Farmacéutica de Atención Primaria; Comarca Ezkerraldea-Enkarterri. Osakidetza. - Eulali Mariñelarena Mañeru. Médica de Atención Primaria; Comarca Gipuzkoa Este. Osakidetza. - Carmela Mozo Avellaned. Farmacéutica de Atención Primaria; Comarca Gipuzkoa Este. Osakidetza. - Justo Mugica Campos. Médico de Atención Primaria; Comarca Gipuzkoa Oeste. Osakidetza. - Margarita Odriozola Altuna. Médica de Atención Primaria; Comarca Interior. Osakidetza. - Isabel Porras Arregui. Farmacéutica de CEVIME. Departamento de Sanidad. - María Teresa Santamarta Lozano. Farmacéutica de BIOEF. Fundación Vasca de Innovación e Investigación Sanitarias. - Luisa Ugedo Urruela. Farmacóloga; Facultad de Medicina y Odontología. Universidad del País Vasco. - Elena Valverde Bilbao. Farmacéutica de Atención Primaria; Comarca Gipuzkoa Oeste. Osakidetza. BIBLIOGRAFÍA 1. Ficha técnica de Janumet (sitagliptina/metformina). Laboratorios Merck Sharp & Dohme Ltd. Disponible en URL: [consultado ]. 2. Comité de Medicamentos de Uso Humano (CHMP). Informe Público Europeo de Evaluación (EPAR). Janumet. DCI: sitagliptina/metformina. EMEA H/C/ ; (Rev. 6), Disponible en URL: [consultado ]. 3. CADIME-Grupo de Expertos en Uso Racional de Medicamentos del SAS. Sitagliptina (DCI). Informe de Novedad Terapéutica 2008; (18150). 4. Goldstein BJ, Feinglos MN, Lunceford JK, Johnson J, Williams-Herman DE. Effect of initial combination therapy with sitagliptin, a dipeptidyl petptidase-4-inhibitor and metformin on glycemic control in patients with 2 diabetes. Diabetes Care. 2007;30(8): Williams-Herman D, Johnson J, Teng R, Luo E, Davies MJ, Kaufman KD, et al. Efficacy and safety of initial combination therapy with sitagliptin and metformin in patients with type 2 diabetes: a 54-week study. Curr Med Res Opin. 2009;25(3): Charbonnel B, Karasik A, Wu M, Meininger G. Efficacy and safety of the dipeptidyl peptidase-4 inhibitor sitagliptin added to ongoing metformin therapy in patients with type 2 diabetes inadequately controlled with metformin alone. Diabetes Care. 2006;29(12): Raz I, Chen Y, Wu M, Hussain S, Kaufman KD, Amatruda JM, et al. Efficacy and safety of sitagliptin added to ongoing metformin therapy in patients with type 2 diabetes. Curr Med Res. 2008;24(2): Nauck MA, Meininger G, Sheng D, Terranella L, Stein PP. Efficacy and safety of the dipetidyl peptidase-4 inhibitor, sitagliptin, compared with the sulfonylurea, glipizide, in patients with type 2 diabetes inadequately controlled in metformin alone: a randomized, double-blind, non-inferiority trial. Diabetes Obes Metab.2007;9(2): Scott R, Loeys T, Davies MJ, Engel SS. Efficacy and safety of sitagliptin when added to ongoing metformin therapy in patients with type 2 diabetes. Diabetes Obes Metab.2008;10(10): Hermansen K, Kipnes M, Luo E, Fanurik D, Khatami H, Stein P. Efficacy and safety of the dipeptidyl peptidase-4 inhibitor, sitagliptin, in patients with type 2 diabetes mellitus inadequately controlled on glimepiride alone or on glimepiride and metformin. Diab Obes Metab 2007; 9(5): Information for healthcare professionals. Acute pancreatitis and sitagliptin (marketed as Januvia and Janumet). Disponible en URL: [consultado ]. 12. National Institute for Health and Clinical Excellence. Type 2 diabetes: newer agents. NICE short clinical guideline 87. May Disponible en URL: [consultado ]. 13. Ministerio de Sanidad y Consumo. Guía de Práctica Clínica sobre Diabetes tipo 2. Guía rápida. Disponible en URL: [consultado marzo 2009]. 14. Nathan DM, Buse JB, Davidson MB, Ferrannini E, Holman RR, Sherwin R, et al. Medical management of hyperglycaemia in type 2 diabetes mellitus: a consensus algorithm for the initiation and adjustment of therapy. A consensus statement from the American Diabetes Association and the European Association for the Study of Diabetes. Diabetologia 2009;52(1): Algoritmo de tratamiento de la DM2. GEDAPS Disponible en URL: [consultado ]. 6
7 INFORME DE SITAGLIPTINA/METFORMINA: TABLA RESUMEN DE ENSAYOS CLÍNICOS Referencia (Autor, publicación) Charbonnel B et al. Diabetes Care 2006; 29(12): Tipo de estudio y objetivo EC aleatorizado, multicéntrico, doble ciego controlado con placebo. Duración: 24 semanas Objetivo: Evaluar eficacia y seguridad de la adición de SI al tratamiento con ME en pacientes con DM2 e inadecuado control glucémico (HbA 1c 7-10%). SI y ME en preparaciones separadas. Población estudiada (criterios de inclusión y exclusión) N=701 pacientes con DM2, años, inadecuado control glucémico con dieta, ejercicio y ME mg/día (HbA 1c : 6,4-11,0%, media 8,0%). Distribución de pacientes: HbA 1c < 8%: 54,6% HbA 1c : 8 < 9%:31,1 % HbA 1c 9%: 14,3% Uso de ADO previo al inicio del estudio: -Sin tratamiento: 5,8% -Monoterapia: 61,5% -Terapia combinada: 32,7% Criterios de exclusión: pacientes con DM1, pacientes con insulina en las 2 grupos: Pauta de tratamiento -SI+ME = SI 100 mg/día + ME 1500 mg/día (n=464) -Placebo+ME = Placebo + ME 1500 mg/día (n=237) Variables de medida (endpoint) Eficacia Variable principal: Cambio en HbA 1c respecto al basal Diferencia SI+ME frente a Placebo+ME Variables secundarias: Cambio en niveles de GPA. Diferencia entre grupos: % Pacientes con Hb<7% -% Pacientes con terapia de rescate Seguridad % Abandonos por EA % Pacientes con EA relacionada con el fármaco EA más frecuentes en el grupo de SI Resultados (tamaño / valores p / intervalos de confianza) -SI+ME: de 7,96 a 7,26= -0.67% (IC 95%:-0,77-0,57) (p<0,001) -Placebo+ME:de 8,03 a 7,95 = % (IC 95%: -0,15, 0,10) -0,65% (IC95%: -0,77, -0,53) (p<0,001) -SI+ME: -16,2 mg/dl -Placebo+ME: 9 mg/dl -25,4 mg/dl (-31,0 a -19,8) p< SI+ME: 47,0% -Placebo+ME: 18,3% -SI+ME: 4,5% Placebo+ME: 13,5% -SI+ME: 2,4% -Placebo+ME: 3% -SI+ME: 9,7% -Placebo+ME: 10,5% nasofaringitis, infección urinaria, Comentarios -Análisis por ITT, incluyendo todos los pacientes que tomaron una dosis del fármaco y tenían una medida basal y otra posterior (677 pacientes). -Terapia de rescate con PI si: GPA>270 mg/dl en las primeras 6 semanas. GPA>240 mg/dl de las semanas 6 a la 12. GPA>200 mg/dl a partir de la semana 12. -En los pacientes que recibieron tratamiento de rescate con PI se consideró la última observación antes de dicho tratamiento. Calidad del estudio (escala Jadad) (*) Total: 3 puntos -Aleatorizado: 1 -Doble ciego: 1 -Pérdidas: 1 -Aleat. apropiada: 0 -Ciego apropiado: 0 7
8 Goldstein BJ et al. Diabetes Care 2007; 30(8): EC aleatorizado, multicéntrico, doble ciego controlado con placebo. Duración: 24 semanas Objetivo: Evaluar eficacia y seguridad de SI/ME (preparación dosis fijas) en pacientes con DM2 e inadecuado control glucémico (HbA 1c 7,5-11%) con dieta y ejercicio. Se diseñó para evaluar la asociación a dosis fijas frente a placebo, frente a SI en monoterapia y frente a ME en monoterapia. 8 semanas previas, con deterioro de la función renal o con concentraciones de GPA> 260 mg/dl N=1091 pacientes con DM2, de 18 a 78 años con inadecuado control glucémico (HbA 1c : 6,3-11,9%; media 8,8%). Distriibución de los valores de HbA 1c basales era similar entre los diferentes grupos. Grupo SI 100 mg+me 2000 mg HbA 1c < 8%: 20,9% HbA 1c 8 < 9%: 39,6 % HbA 1c : 9% < 10%:26,9% HbA 1c 10%: 12,6% Uso de ADO previo al inicio del estudio: 50% Criterios de exclusión: pacientes con DM1, enfermedad cardiaca inestable, deterioro de la 6 grupos: -Placebo (n=165) -SI= SI 100 mg/día (n=175) -ME 1000= Metformina 1000 mg/día (n=178) -ME 2000= Metformina 2000 mg/día (n=177) -SI/ME1000= SI 100 mg/día + ME 1000 mg/día (n=183) -SI/ME2000= SI 100 mg/día + ME 2000 mg/día (n=178) % Hipoglucemia Diferencia en el peso Eficacia Variable principal: Diferencia en HbA 1c a las 24 semanas respecto a placebo. Variables secundarias: Cambio GPA con respecto a placebo. % Pacientes con Hb<7% y <6,5% Seguridad % EA asociados al fármaco % Hipoglucemias Cambio de peso artralgia, dolor de espalda, tos. -SI+ME: 1,3% -Placebo+ME: 2,1% Diferencia entre grupos NS -SI 100: -0,83% (IC 95%:-1,06-0,60) p 0,001 -ME1000: -0,99% (IC 95%:-1,22, - 0,66) p 0,001 -ME2000: -1,30% (IC 95%:-1,53-1,06) p 0,001 -SI/ME1000: -1,57% (IC 5%:-1,80, - 1,34) p 0,001 -SI/ME2000: -2,07% (IC 95%:-2,30, -1,84) p SI: -23,3 mg/dl -ME1000: -33,1 mg/dl -ME2000: -35,1 mg/dl -SI/ME1000: -52,9mg/dl -SI/ME2000: -69,7 mg/dl -Placebo: 9%; 2% -SI100: 20%; 10% -ME1000: 23%; 9% -ME2000: 3 8%; 20% -SI/ME1000: 43%; 22% -SI/ME2000: 66%; 44% p<0,001; p<0,.005 -Placebo: 9,7%; 0,6% -SI: 6,7%; 0,6% -ME1000: 11,5%; 0,5% -ME2000: 16,5%; 1,1% -SI/ME1000:12,6%; 1,1% -SI/ME2000:15,4%; 2,2% Se produjeron reducciones de peso No se compara SI/ME frente al tratamiento combinado con SI+ME administrado en preparaciones separadas. Total: 3 puntos -Aleatorizado: 1 -Doble ciego: 1 -Pérdidas: 1 -Aleat. apropiada: 0 -Ciego apropiado: 0 8
9 función renal o elevación de enzimas hepáticas. respecto al basal: en todos los grupos de 0,6 a 1,3 kg, excepto en el grupo de SI donde no se observó ningún cambio. Williams-Herman D et al. Curr Med Res Opin 2009; 25(3): Estudio aleatorizado, multicéntrico, doble ciego. Continuación de 30 semanas del estudio de Goldstein (24 semanas). Objetivo: Evaluar la eficacia y seguridad a largo plazo del tratamiento con SI y ME coadministrados. N=885 que completaron la fase anterior Criterios de inclusión y exclusión: Los mismos del ensayo de Goldstein 6 grupos: -Placebo+ME2000 mg/d (n=123) - SI 100mg/d (n=141) -ME 1000= ME 1000 mg/día (n=147) -ME 2000= ME 2000 mg/día (n=153) -SI+ME1000= SI 100 mg/día + ME 1000 mg/día (n=160) -SI+ME2000= SI 100 mg/día + ME 2000 mg/día (n=161) Eficacia Reducción en HbA 1c a las 54 semanas respecto al nivel basal -Análisis de datos de todos los pacientes que inician fase de continuación (ITT) -Análisis de datos de todos los pacientes que completan fase de continuación (PP) SI 100mg/d: -0,8% (IC 95%: -1,0, - 0,6) p NE ME 1000mg: -1% (IC 95%: -1,2, - 0,8) ME 2000mg: -1,3 (IC 95%: -1,5, - 1,2), p NE SI+ME1000: -1,4% (IC95%: -1,6; - 1,3) p NE SI+ME2000: -1,8% (IC95%: -2; - 1,7) p NE SI 100mg/d: -1,4% (IC 95%: -1,6, - 1,2) p NE ME 1000 mg: -1,2% (IC 95%: -1,4, - 1,1) ME 2000mg: -1,6 (IC 95%: -1,7, - 1,4), p NE SI+ME1000: -1,7% (IC95%: -1,8; - 1,5) p NE SI+ME2000: -1,9% (IC95%: -2,1; - 1,8) p NE No especifica que SI y ME se administran en una combinación a dosis fijas como en la 1ª fase, se habla de coadministración. El análisis de seguridad se realiza en todos los pacientes que han recibido una dosis de la medicación desde el inicio del estudio. Total: 3 puntos -Aleatorizado: 1 -Doble ciego: 1 -Pérdidas: 1 -Aleat. apropiada: 0 -Ciego apropiado: 0 % Pacientes con Hb<7% a las 54 semanas: todos los pacientes que iniciaron fase de continuación, y sólo los que la completaron. SI 100: 68 %, 41% ME1000: 55 %, 35% ME2000: 77 %, 57% SI100+ME1000: 80 %,63% SI100+ME2000: 86%, 77% Cambios en GPA (mg/dl) con respecto a valor basal: todos los pacientes que iniciaron fase continuación, sólo los SI100: -16,0 (-23,2, -8,7) -26,0 (-34,0, -18,1) ME1000: -29,0 (-35,9, -22,2), -35,6 (-42,5, -28.7) 9
10 que la completaron. ME2000: -39,6 (-46,00, -32,2), -43,8 (-49,8, -37,8) SI100+ME1000: -42,5 (-48,6, -36,3), -49,8 (-55,7, -44,0) SI100+ME2000: -55,6 (-61,6, -49,6), -59,4 (-64,8, -53,9) Seguridad % Hipoglucemia -Placebo/ME: 2% -SI: 1% -ME1000: 1% -ME2000: 1% -SI/ME1000: 2% -SI/ME2000: 3% Raz I et al. Curr Med Res Opin 2008; 24(2): EC aleatorizado, multicéntrico, doble ciego, controlado con placebo. Duración: 30 semanas Objetivo: Evaluar eficacia y tolerabilidad de SI en combinación con ME en pacientes con DM2 tratados con ME, que no controlan su glucemia (HbA1c 8-11%). N=190 pacientes con DM2, de 18 a 78 años, tratados con ME ( 1500mg/día, máximo 2550 mg/día) e inadecuado control glucémico: HbA1c: 8-11% Distribución de pacientes: HbA1c < 9%: 42,1 % HbA1c: 9-10%: 40,5 % HbA1c > 10%: 2 grupos: -SI+ME = SI100 mg/día + ME 1500 mg/día (n=96) - Placebo+ME= Placebo + ME 1500 mg/día (n=94) Efectos gastrointestinales Eficacia Variable principal: Reducción en % HbA1c respecto al valor basal a las 18 semanas. Diferencia frente a placebo Diferencia frente a placebo en la reducción en % HbA1c respecto al valor basal a las 30 semanas. Reducción en GPA -Placebo/ME: 16% -SI: 20% -ME1000: 20% -ME2000: 31% -SI/ME1000: 26% -SI/ME2000: 29% -SI+ME= -1,0% (-1,2 a -0,80) -Placebo+ME = 0% (-0,2 a 0,3) -1,0% (IC95%:-1,40 a -0,7) p< ,0% (IC95%:-1,40 a -0,6) p< ,4 95% CI (-2,1 0.7) -Análisis por ITT, incluyendo todos los pacientes que tomaron una dosis del fármaco y tenían una medida basal y otra posterior. -No especifica la dosis media de ME. -Terapia de rescate con GLIP -% Pacientes con terapia de rescate: - ME+ SI: 6,8% - ME+Placebo: 26,9% Total: 3 puntos -Aleatorizado: 1 -Doble ciego: 1 -Pérdidas: 1 -Aleat. apropiada: 0 -Ciego apropiado: 0 10
11 17,4 % Uso de ADO previo al inicio del estudio: -Sin tratamiento: 0 % -Monoterapia con ME: 52,1% -Monoterapia con otro ADO: 3,2% -Terapia combinada: 44,7 % Diferencia entre grupos a las 18 y 30 semanas % Pacientes con Hb<7%: Seguridad % Abandonos: p<0.001en ambos casos. -SI+ME: 13,7% en la semana 18 y 22,1% en la semana 30 -Placebo+ME: 3,3% en la semana 18 (p=0,012) y 3,3% en la semana 30 (p<0.001) -SI+ME:17,7% -Placebo+ME: 14,9% Nauck MA et al. Obes Metab 2007; 9(2): EC aleatorizado, multicéntrico, doble ciego, de no-inferioridad. Duración: 52 semanas Objetivo: Evaluar en términos de no inferioridad, la eficacia y seguridad, de la adición de SI frente a la adición Criterios de exclusión: pacientes con DM1, que hubieran utilizado insulina en las 8 semanas previas, con tratamiento con glitazonas o incretin miméticos en las 12 semanas previas, con IMC<20 kg/m2 o >43 kg/m2, GPA<135 mg/dl o >270 mg/dl N=1172 pacientes con DM2, de 18 a 78 años, tratados con ME 1500mg/día (HbA 1c : 5,8-11%, media 7,5) Niveles de HbA1c basales en el 2 grupos: -SI+ME= SI 100 mg/día + ME 1500 mg/día (n=588) -GLIP+ME= GLIP (5-20) mg/día + ME 1500 mg/día (n=584) % EA relacionados con el tratamiento % Hipoglucemia Efectos gastrointestinales Cambio de peso respecto al basal en la semana 30 Eficacia Variable principal: Cambio en HbA 1c respecto al basal: Diferencia SI+ME frente a GLIP+ME: Variables -SI+ME: 5,2% -Placebo+ME. 4,3% -SI+ME: 1% -Placebo+ME: 0 % -SI+ME: 10,4% -Placebo+ME: 7,4 % -Disminución de 0,5 kg en ambos grupos. -Análisis por protocolo -SI+ME: -0,67% (IC95%: - 0,75 a -0,59) -GLIP+ME: -0,67% (IC95%: - 0,75 a -0,59) -0,01% (IC95%: - 0,09 a 0,08) -Análisis por protocolo (n=793) El porcentaje de pacientes excluidos es 32,3% (379): 86 pacientes (15%) en el grupo de SI+ME y 58 (10%) en el de GLIP+ME fueron excluidos por falta de eficacia. Total: 3 puntos -Aleatorizado: 1 -Doble ciego: 1 -Pérdidas: 1 -Aleat. apropiada: 0 - Ciego apropiado: 0 11
12 Scott R et al. Diabetes Obes Metab 2008; 10(10): de GLIP, al tratamiento con ME en pacientes con DM2 e inadecuado control glucémico con ME. Margen de no inferioridad predefinido: 0,3% EC aleatorizado, multicéntrico, doble ciego controlado con placebo. Duración: 18 semanas Objetivo: Evaluar eficacia y tolerabilidad de SI en combinación con ME comparada con RO o grupo SI+ME y GLIP+ME HbA 1c < 8%: 64,0%; 65,5% HbA 1c : 8 <9%: 25,8%; 24,2% HbA 1c 9%: 10,2%; 10,3% Uso de ADO previo al inicio del estudio grupo SI+ME y GLIP+ME Sin tratamiento: 4,3%; 4,8% Monoterapia: 65,6%; 68,0% Terapia doble: 30,1%; 27,2% Criterios de exclusión: pacientes con DM1, pacientes que hubieran utilizado insulina en las 8 semanas previas, deterioro de la función renal no relacionada con el uso de ME, GPA>270 mg/dl. N=273 pacientes con DM2, de 18 a 75 años, tratados con ME ( 1500mg/día) e inadecuado control glucémico (HbA1c: 7-11%). Distribución de 3 grupos: -Placebo+ME 1500 mg/día (n=92) -SI+ME= SI 100 mg/día + ME 1500mg/día (n=94) -RO+ME= RO 8 secundarias: Reducción en niveles de glucosa en ayunas, dif. entre grupos: % Pacientes con Hb<7%: Cambio en HbA 1c respecto al basal: Diferencia SI+ME frente a GLIP+ME: Seguridad: % EA relacionados con el tratamiento: % Hipoglucemia: % abandonos por falta de eficacia Cambio de peso respecto al basal: Diferencia en el peso entre ambos grupos: Eficacia Variable principal: Cambio en % HbA1c respecto al basal: Diferencia frente a placebo -2,52 mg/dl (IC 95%: -6,84 a 1,98 ) -SI+ME: 63% -GLIP+ME: 59% -Analisis por ITT -SI+ME: -0,51% (IC95%: - 0,60 a -0,43) -GLIP+ME: -0,56% (IC95%: - 0,64 a -0,47) 0,04% (IC95%: - 0,04 a 0,13) -SI+ME: 14,5% -GLIP+ME 30,3% -SI+ME: 4,9% - GLIP+ME: 32% -SI+ME: 15% - GLIP+ME: 10% -SI+ME: -1,5 kg (IC 95%: -2,0 a 0,9) -GLIP+ME: 1,1 kg (IC 95%: 0,5 a 1,6) -2,5 kg (IC95% -3,1 a -2,0) p< Placebo+ME= -0.22% (IC 95%: -0,36 a -0,08) -SI+ME= -0.73% (IC 95%: -0,87 a -0,60) -RO+ME= -0.79% (IC 95%: -0,92 a -0,65) -SI+ME:-0,51% Análisis por ITT (n=1135): en todos los pacientes que tomaron una dosis del fármaco y tenían una medida basal y otra posterior. La dosis media de GLIP fue 10,3 mg/día, (sólo el 22% de los pacientes llegaron a los 20 mg/día). Esto puede limitar su eficacia, pero dosis mayores pueden aumentar el riesgo de hipoglucemia que ya es alto. Está en desarrollo una extensión del estudio durante 52 semanas más. -Análisis por ITT, incluyendo todos los pacientes que tomaron una dosis del fármaco y tenían una medida basal y otra posterior. -No existe terapia de rescate Total: 3 puntos -Aleatorizado: 1 -Doble ciego: 1 -Pérdidas: 1 -Aleat. apropiada: 0 -Ciego adecuado: 0 12
13 placebo en pacientes con DM2 e inadecuado control glucémico (HbA1c 7-11%) con ME. pacientes: HbA1c < 8%: 71,1 % HbA1c: 8-9%: 18,7 % HbA1c > 9%: 10,2 % Criterios de exclusión: pacientes con DM1, que hubieran utilizado insulina en las 8 semanas previas, con deterioro de la función renal o con niveles de enzimas hepáticas doble del valor normal, o con un valor de GPA>270 mg/dl o con intolerancia o contraindicación al uso de tiazolidindionas o ME. mg/día + ME 1500mg/día (n=87) Diferencia SI+ME frente a RO+ME % Pacientes con Hb<7%: Seguridad % Abandonos % Abandonos por EA relacionados con el fármaco % EA relacionados con el tratamiento % Hipoglucemia (IC 95%:-0,70 a -0,32 -RO+ME: -0.57% (IC 95%: -0,76 a -0,37) 0,06% (IC 95%: -0,14 a 0,25) -Placebo+ME: 38% -SI+ME: 55% -RO+ME: 63% -Placebo+ME: 9,7 % -SI+ME: 9,6%. -RO+ME: 2,3% -Placebo+ME: 0 % -SI+ME: 1% -RO+ME:0% -Placebo+ME: 9 % -SI+ME: 11%. -ROS+ME: 10% -Placebo+ME: 2 % -SI+ME: 1% -RO+ME: 1% -No especifica la dosis media de ME. -Respecto al perfil lipídico, tanto placebo como SI y RO aumentaron el nivel de LDL y colesterol total. En el grupo de SI, el incremento fue menor pero no se considera relevante para incluirlo en el análisis de resultados. % Edema -Placebo+ME: 1 % -SI+ME: 1% -RO+ME: 5% Efectos gastrointestinales: -Placebo+ME: 9 % -SI+ME: 9% -RO+ME: 7% Cambio de peso -Placebo: -0,8 kg -SI: -0,4 kg -RO: 1,5 kg 13
14 Hermansen K et al. Diab Obes Metab 2007; 9(5): EC aleatorizado, multicéntrico, doble ciego controlado con placebo. Duración: 24 semanas Objetivo: Evaluar eficacia y tolerabilidad de la adición de SI al tratamiento con GLIM sola o la combinación GLIME+ME en pacientes con DM2 e inadecuado control glucémico N=441 pacientes con DM2, de 18 a 75 años en tratamiento con GLIM sola o GLIM +ME Distribución de pacientes: HbA 1c < 8%: 35,15 % HbA 1c : 8 < 9%: 44,80 % HbA 1c 9%: 20,05 % Uso de ADO previo al inicio del estudio: -Sin tratamiento: 5,0 % -Monoterapia: 32,4 % -Terapia combinada 62,6 % Criterios de exclusión: pacientes con DM1 o que hubieran utilizado insulina en las 8 semanas previas, con deterioro de la función renal o con intolerancia o contraindicación al uso de GLIM, sulfonilureas, ME o PI. 2 Cohortes y 4 Grupos: COHORTE SI (n=222) -SI + GLIM+ ME= SI 100 mg/día + GLIM (4-8 mg/día) + ME mg/día) (n=116) -SI + GLIM= SI 100 mg/día + Glimepirida (4-8 mg/día) (n=106) COHORTE PLACEBO (n=219) -Placebo + GLIM+ ME= GLIM (4-8 mg/día) + ME mg/día) (n=113) -Placebo + GLIM= GLIM (4-8 mg/día) (n=106) Eficacia Variable principal: Reducción en % HbA 1c respecto al valor basal en la cohorte. Diferencia SI frente a placebo: Diferencia SI+GLIM+ME frente a Placebo+GLIM+ ME: Variables secundarias: % pacientes con Hb<7% en la cohorte SI % % pacientes que precisan tratamiento de rescate. Seguridad % abandonos por EA en la cohorte de SI % EA relacionados con el fármaco en la cohorte de SI % Hipoglucemia en la cohorte de SI EA gastrointestinales en la cohorte de SI Cambio de peso en la -SI: -0,45% (IC 95 % : -0,57 a -0,34) -Placebo: 0,28% (IC 95% : -0,17 a -0,40) -0,74% (IC95:-0,90 a -0,57) -0,89% (IC 95%: -1,10 a -0,68) -SI: 17,1% -Placebo: 4,8 % p<0,001 -SI: 11,3% -Placebo: 24,7% -SI: 2,3% -Placebo: 1,4% -SI: 14,9% -Placebo: 6,8% -SI: 12,2% -Placebo: 1,8% -SI: 5% -Placebo: 4,6% -Análisis por ITT (N=425) incluyendo todos los pacientes que tomaron una dosis del fármaco y tenían una medida basal y otra posterior. Terapia de rescate con PI si: GPA>270 mg/dl en las primeras 6 semanas. GPA>240 mg/dl de las semanas 6 a la 12. GPA>200 mg/dl a partir de la semana 12. -Los pacientes con PI se consideraban pérdidas y se medía la última observación recogida antes de iniciar la terapia de rescate. -El estudio fue diseñado para evaluar la eficacia y seguridad de la adición de SI comparado con la adición de placebo para toda la cohorte de población. Total: 4 puntos -Aleatorizado: 1 -Doble ciego: 1 -Pérdidas: 1 -Aleat. apropiada: 1 -Ciego apropiado: 0 14
15 cohorte de SI -SI: 0,8 kg -Placebo: -0,4 kg (IC 95%: -0,8 a 0,1) ADO: antidiabéticos orales. DM1: diabetes mellitus tipo 1, DM2: diabetes mellitus tipo 2, EA: efecto adverso, GPA: glucosa plasmática en ayunas; GLIM: glimepirida, GLIP: glipizida, HbA 1c : hemoglobina glicosilada, ITT: análisis por intención de tratar, ME: metformina, NE: no se especifica el dato en el estudio, NS: no significativo, PI: pioglitazona, RO: rrosiglitazona, SI: sitagliptina, SI/ME: asociación a dosis fijas de SI y ME. (*) Rango de puntuación: 0-5. Estudio de baja calidad: puntuación < 3. 15
INFORME DE EVALUACIÓN SITAGLIPTINA
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI Principio activo Nombre Comercial y presentaciones INFORME DE EVALUACIÓN SITAGLIPTINA JANUVIA (Merck Sharp & Dohme ) Comprimido recubierto (55,95
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI Principio activo Nombre Comercial y presentaciones INFORME DE EVALUACIÓN SITAGLIPTINA JANUVIA (Merck Sharp & Dohme ) Comprimido recubierto (55,95
Que hacer cuando fracasa la terapia oral combinada?
 Que hacer cuando fracasa la terapia oral combinada? 1. Añadir Insulina basal (nocturna) 2. Añadir un tercer fármaco oral 3. Añadir un análogo GLP1 4. Derivar al endocrino NICE 2008 ADA/EASD 2009 AACE 2009
Que hacer cuando fracasa la terapia oral combinada? 1. Añadir Insulina basal (nocturna) 2. Añadir un tercer fármaco oral 3. Añadir un análogo GLP1 4. Derivar al endocrino NICE 2008 ADA/EASD 2009 AACE 2009
6.1. Control glucémico con antidiabéticos orales (ADO) En el estudio observacional UKPDS 35, cada reducción del 1% de HbA 1
 6. Control glucémico Preguntas para responder Cuáles son las cifras objetivo de Hb 1 c? Cuál es el tratamiento farmacológico inicial de pacientes con diabetes que no alcanzan criterios de control glucémico
6. Control glucémico Preguntas para responder Cuáles son las cifras objetivo de Hb 1 c? Cuál es el tratamiento farmacológico inicial de pacientes con diabetes que no alcanzan criterios de control glucémico
INFORME DE EVALUACIÓN SAXAGLIPTINA
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN Principio activo: Nombre comercial y presentaciones: SAXAGLIPTINA ONGLYZA (Bristol-Myers Squibb Pharmaceuticals) 5 mg 28 comprimidos
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN Principio activo: Nombre comercial y presentaciones: SAXAGLIPTINA ONGLYZA (Bristol-Myers Squibb Pharmaceuticals) 5 mg 28 comprimidos
SITAGLIPTINA Diabetes mellitus tipo 2
 Comisión de Evaluación de Medicamentos SITAGLIPTINA Diabetes mellitus tipo 2 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Sitagliptina Indicación clínica: En pacientes con diabetes mellitus
Comisión de Evaluación de Medicamentos SITAGLIPTINA Diabetes mellitus tipo 2 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Sitagliptina Indicación clínica: En pacientes con diabetes mellitus
Programa RIO Rimonabant en Obesidad Estudios clínicos
 Programa RIO Rimonabant en Obesidad Estudios clínicos Evaluación de eficacia y seguridad de Acomplia en más de 6.600 pacientes Buenos Aires, 25 de Agosto de 2005.- El Programa RIO (Rimonabant in Obesity,
Programa RIO Rimonabant en Obesidad Estudios clínicos Evaluación de eficacia y seguridad de Acomplia en más de 6.600 pacientes Buenos Aires, 25 de Agosto de 2005.- El Programa RIO (Rimonabant in Obesity,
Estudio BASAL LIXI Presentación de Resultados
 Estudio observacional para evaluar el impacto de la intensificación de la terapia con insulina propuesta por la ADA/EASD 2012 (estrategia insulina basal + GLP-1 RA) sobre el control glucémico en pacientes
Estudio observacional para evaluar el impacto de la intensificación de la terapia con insulina propuesta por la ADA/EASD 2012 (estrategia insulina basal + GLP-1 RA) sobre el control glucémico en pacientes
Escarlata Angullo CS Escola Graduada Palma de Mallorca. Grupo DM semfyc
 Escarlata Angullo CS Escola Graduada Palma de Mallorca Grupo DM semfyc Declaración de actividades: Actividades formativas para AstraZeneca, Boehringer-Ingelheim, Janssen, Lilly, Merck Sharp & Dohme y Novartis.
Escarlata Angullo CS Escola Graduada Palma de Mallorca Grupo DM semfyc Declaración de actividades: Actividades formativas para AstraZeneca, Boehringer-Ingelheim, Janssen, Lilly, Merck Sharp & Dohme y Novartis.
Fecha autorización (procedimiento): noviembre, 2006 (centralizado)
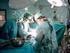 EXENATIDA (DCI) Calificación: NO SUPONE AVANCE TERAPÉUTICO Fecha de evaluación: Octubre, 2008 Nuevo principio activo Marca registrada (Laboratorio): Byetta (Eli Lilly Nederland B.V.) Fecha autorización
EXENATIDA (DCI) Calificación: NO SUPONE AVANCE TERAPÉUTICO Fecha de evaluación: Octubre, 2008 Nuevo principio activo Marca registrada (Laboratorio): Byetta (Eli Lilly Nederland B.V.) Fecha autorización
Juan Manuel Guardia Baena MIR Endocrinología - Nutrición
 SESIONES DE ACTUALIZACIÓN EN DIABETES Juan Manuel Guardia Baena MIR Endocrinología - Nutrición seguro????? Hoy en diase dispone para el tratamiento DM tipo 2 de nuevas terapias que son de administracion
SESIONES DE ACTUALIZACIÓN EN DIABETES Juan Manuel Guardia Baena MIR Endocrinología - Nutrición seguro????? Hoy en diase dispone para el tratamiento DM tipo 2 de nuevas terapias que son de administracion
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN VILDAGLIPTINA
 Principio activo COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN VILDAGLIPTINA GALVUS 50 mg 28 comprimidos (34,37 ) () Nombre Comercial y presentaciones GALVUS 50 mg 56 comprimidos
Principio activo COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN VILDAGLIPTINA GALVUS 50 mg 28 comprimidos (34,37 ) () Nombre Comercial y presentaciones GALVUS 50 mg 56 comprimidos
Guías ADA ta Parte. Objetivos y tratamiento
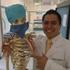 Guías ADA 2016 4ta Parte Objetivos y tratamiento El objetivo principal del tratamiento es el control glucémico. El control de la glucemia reduce a largo plazo complicaciones microvasculares como: nefropatía,
Guías ADA 2016 4ta Parte Objetivos y tratamiento El objetivo principal del tratamiento es el control glucémico. El control de la glucemia reduce a largo plazo complicaciones microvasculares como: nefropatía,
Alternativas Terapéuticas en la DM tipo 2. Dr. Angel Merchante Alfaro Consorcio Hospital General Universitario de Valencia
 Alternativas Terapéuticas en la DM tipo 2 Dr. Angel Merchante Alfaro Consorcio Hospital General Universitario de Valencia Alternativas Terapéuticas en la DM tipo 2 Agenda Revisión algoritmos terapéuticos
Alternativas Terapéuticas en la DM tipo 2 Dr. Angel Merchante Alfaro Consorcio Hospital General Universitario de Valencia Alternativas Terapéuticas en la DM tipo 2 Agenda Revisión algoritmos terapéuticos
DIABETES TIPO 2 : HIPOGLUCEMIANTES ORALES CURSO DE ENFERMERIA SAD CAP. CORDOBA 2014
 DIABETES TIPO 2 : HIPOGLUCEMIANTES ORALES CURSO DE ENFERMERIA SAD CAP. CORDOBA 2014 DR ALEJANDRO MORERO MP 25208-1 MEDICINA INTERNA ME 10558 DIABETOLOGIA ME 14002 DIABETES MELLITUS La Diabetes Mellitus,
DIABETES TIPO 2 : HIPOGLUCEMIANTES ORALES CURSO DE ENFERMERIA SAD CAP. CORDOBA 2014 DR ALEJANDRO MORERO MP 25208-1 MEDICINA INTERNA ME 10558 DIABETOLOGIA ME 14002 DIABETES MELLITUS La Diabetes Mellitus,
LAS SULFONILUREAS A DEBATE. Sara Artola CS Hereza. Leganés Madrid
 LAS SULFONILUREAS A DEBATE Sara Artola CS Hereza. Leganés Madrid A FAVOR DE LAS SULFONILUREAS Posición de las SU en las Guías de Tratamiento Ventajas de las SU Problemas atribuidos a las SU Conclusiones
LAS SULFONILUREAS A DEBATE Sara Artola CS Hereza. Leganés Madrid A FAVOR DE LAS SULFONILUREAS Posición de las SU en las Guías de Tratamiento Ventajas de las SU Problemas atribuidos a las SU Conclusiones
INFORME DE EVALUACIÓN LINAGLIPTINA/METFORMINA
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ATENCIÓN PRIMARIA DE EUSKADI INFORME DE EVALUACIÓN LINAGLIPTINA/METFORMINA Nombre comercial y presentaciones JENTADUETO (Boehringer Ingelheim Internacional
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ATENCIÓN PRIMARIA DE EUSKADI INFORME DE EVALUACIÓN LINAGLIPTINA/METFORMINA Nombre comercial y presentaciones JENTADUETO (Boehringer Ingelheim Internacional
Cuál es la eficacia y seguridad de los análogos de insulina frente a las insulinas convencionales en pacientes con DM 2 que requieren insulina?
 8. Control glucémico Las preguntas que se van a responder son: Cuáles son las cifras objetivo de HbA 1 c? Cuál es el tratamiento farmacológico inicial de pacientes con diabetes que no alcanzan criterios
8. Control glucémico Las preguntas que se van a responder son: Cuáles son las cifras objetivo de HbA 1 c? Cuál es el tratamiento farmacológico inicial de pacientes con diabetes que no alcanzan criterios
Rol de Inhibidores de DPP 4 en el Tratamiento de la Diabetes
 Rol de Inhibidores de DPP 4 en el Tratamiento de la Diabetes Dr. Rodolfo Lahsen M. IX JORNADAS ACHINUMET Santiago, viernes 27 de abril de 2012 Visión Actual de la Diabetes tipo 2 Pérdida de Capacidad Compensatoria
Rol de Inhibidores de DPP 4 en el Tratamiento de la Diabetes Dr. Rodolfo Lahsen M. IX JORNADAS ACHINUMET Santiago, viernes 27 de abril de 2012 Visión Actual de la Diabetes tipo 2 Pérdida de Capacidad Compensatoria
ACTUALIDADES EN EL DIAGNÓSTICO Y TRATAMIENTO DEL PACIENTE DIABETICO. Dra. Karla Patricia Martínez Rocha. Medicina Interna Endocrinología.
 ACTUALIDADES EN EL DIAGNÓSTICO Y TRATAMIENTO DEL PACIENTE DIABETICO Dra. Karla Patricia Martínez Rocha. Medicina Interna Endocrinología. Aspectos Histórico del diagnóstico La descripción diagnóstica inicial
ACTUALIDADES EN EL DIAGNÓSTICO Y TRATAMIENTO DEL PACIENTE DIABETICO Dra. Karla Patricia Martínez Rocha. Medicina Interna Endocrinología. Aspectos Histórico del diagnóstico La descripción diagnóstica inicial
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox
 TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
Anexo II. Modificaciones a las secciones pertinentes de la ficha técnica y el prospecto
 Anexo II Modificaciones a las secciones pertinentes de la ficha técnica y el prospecto 6 Para los medicamentos que contienen los inhibidores de la enzima convertidora de angiotensina (IECA) benazepril,
Anexo II Modificaciones a las secciones pertinentes de la ficha técnica y el prospecto 6 Para los medicamentos que contienen los inhibidores de la enzima convertidora de angiotensina (IECA) benazepril,
Objetivos del tratamiento
 Diapositiva 2 de 41 Objetivos del tratamiento Reducir los síntomas de hiperglucemia Limitar los efectos adversos del tratamiento Mantener la calidad de vida y el bienestar psicológico Prevenir o retrasar
Diapositiva 2 de 41 Objetivos del tratamiento Reducir los síntomas de hiperglucemia Limitar los efectos adversos del tratamiento Mantener la calidad de vida y el bienestar psicológico Prevenir o retrasar
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
Grupo Terapéutico: A10AB Antidiabéticos: insulina y análogos de acción rápida.
 INSULINA GLULISINA (DCI) Calificación: NO SUPONE AVANCE TERAPÉUTICO Fecha de evaluación: enero 2007 Nuevo principio activo Marca registrada (Laboratorio): Apidra Optiset (Sanofi Aventis ) Fecha autorización
INSULINA GLULISINA (DCI) Calificación: NO SUPONE AVANCE TERAPÉUTICO Fecha de evaluación: enero 2007 Nuevo principio activo Marca registrada (Laboratorio): Apidra Optiset (Sanofi Aventis ) Fecha autorización
VILDAGLIPTINA, INHIBIDOR DE LA DPP-4 un nuevo potenciador del islote pancreático
 VILDAGLIPTINA, INHIBIDOR DE LA DPP-4 un nuevo potenciador del islote pancreático Directrices de la ADA y la IDF: objetivos terapéuticos de HbA 1C, GA y GPP Parámetro Valor normal Obj. ADA Obj. IDF GA,
VILDAGLIPTINA, INHIBIDOR DE LA DPP-4 un nuevo potenciador del islote pancreático Directrices de la ADA y la IDF: objetivos terapéuticos de HbA 1C, GA y GPP Parámetro Valor normal Obj. ADA Obj. IDF GA,
GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos
 GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos Industria Alemana EXPENDIO BAJO RECETA Nota importante: Antes de recetar este medicamento, consulte toda la información relativa a su prescripción.
GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos Industria Alemana EXPENDIO BAJO RECETA Nota importante: Antes de recetar este medicamento, consulte toda la información relativa a su prescripción.
No. el alcohol no altera el mecanismo de acción o los efectos del Andanza.
 GUÍA SOBRE 1 1. Qué es Es un fármaco aprobado para su uso como adyuvante, del plan alimentario hipocalórico y la práctica de ejercicio, en el manejo del sobrepeso y la obesidad en adolescentes y adultos.
GUÍA SOBRE 1 1. Qué es Es un fármaco aprobado para su uso como adyuvante, del plan alimentario hipocalórico y la práctica de ejercicio, en el manejo del sobrepeso y la obesidad en adolescentes y adultos.
Publicación de la Dirección General de Farmacia y Productos Sanitarios
 Noviembre 20 - Volumen I Ficha Vildagliptina nº 42 Publicación de la Dirección General de Farmacia y Productos Sanitarios Eficacia La vildagliptina es un inhibidor de la DPP-4, enzima que inactiva las
Noviembre 20 - Volumen I Ficha Vildagliptina nº 42 Publicación de la Dirección General de Farmacia y Productos Sanitarios Eficacia La vildagliptina es un inhibidor de la DPP-4, enzima que inactiva las
Acude a consulta porque en el análisis para el examen de salud de la empresa le han sacado "azúcar".
 ESCENARIO 3 Se trata de un hombre, de 52 años. No antecedentes personales de interés. No antecedentes familiares de enfermedad cardiovascular precoz ni de diabetes. Es conductor de autobus. Estudios primarios
ESCENARIO 3 Se trata de un hombre, de 52 años. No antecedentes personales de interés. No antecedentes familiares de enfermedad cardiovascular precoz ni de diabetes. Es conductor de autobus. Estudios primarios
Durante los últimos años se han desarrollado
 Incretinas: nueva opción terapéutica para la diabetes mellitus tipo 2 P. Nogales Aguado a y F. Arrieta Blanco b a Centro de Salud Las Águilas. Área 7. Grupo de DM de la SoMaMFyc. Madrid. b Unidad de Nutrición
Incretinas: nueva opción terapéutica para la diabetes mellitus tipo 2 P. Nogales Aguado a y F. Arrieta Blanco b a Centro de Salud Las Águilas. Área 7. Grupo de DM de la SoMaMFyc. Madrid. b Unidad de Nutrición
Selección Antidiabético oral: Evidencia actual.
 Selección Antidiabético oral: Evidencia actual. Alejandro Pinzón Tovar MD, Médico Internista - Endocrinólogo. Hospital Universitario Hernando Moncaleano Perdomo Docente Universidad Surcolombiana Presidente
Selección Antidiabético oral: Evidencia actual. Alejandro Pinzón Tovar MD, Médico Internista - Endocrinólogo. Hospital Universitario Hernando Moncaleano Perdomo Docente Universidad Surcolombiana Presidente
4.3) Caso clínico: paciente con cardiopatía isquémica crónica y
 obesidad 4.3) Caso clínico: paciente con cardiopatía isquémica crónica y Título Varón de 60 años con diabetes tipo 2, obesidad, HTA y cardiopatía isquémica Filiación Arturo Lisbona Gil. Servicio de Endocrinología
obesidad 4.3) Caso clínico: paciente con cardiopatía isquémica crónica y Título Varón de 60 años con diabetes tipo 2, obesidad, HTA y cardiopatía isquémica Filiación Arturo Lisbona Gil. Servicio de Endocrinología
Es ú&l el control intensivo de la glicemia en los ancianos?
 Es ú&l el control intensivo de la glicemia en los ancianos? Tutor: Dr. Roberto Loureço XI Curso ALMA 1 al 4 de Abril de 2012 Salamanca, España El Anciano con Diabetes José Ricardo Jáuregui Marco Antonio
Es ú&l el control intensivo de la glicemia en los ancianos? Tutor: Dr. Roberto Loureço XI Curso ALMA 1 al 4 de Abril de 2012 Salamanca, España El Anciano con Diabetes José Ricardo Jáuregui Marco Antonio
Taula Rodona Actualització en el tractament farmacològic de la DM2. Triple teràpia
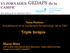 Taula Rodona Actualització en el tractament farmacològic de la DM2 Triple teràpia Manel Mata CAP La Mina. Sant Adrià de Besòs (Barcelona). Institut català de la Salut GedapS de la CAMFiC. RedGDPS Declaración
Taula Rodona Actualització en el tractament farmacològic de la DM2 Triple teràpia Manel Mata CAP La Mina. Sant Adrià de Besòs (Barcelona). Institut català de la Salut GedapS de la CAMFiC. RedGDPS Declaración
Manejo de la hipoglucemia en el anciano. Trinidad Soriano Llora J. Carlos Aguirre Rodríguez
 Manejo de la hipoglucemia en el anciano Trinidad Soriano Llora J. Carlos Aguirre Rodríguez Hace tiempo que me dan mareos!!! Trini tiene 76 años Acude a urgencias por caída en su domicilio Diagnóstico:
Manejo de la hipoglucemia en el anciano Trinidad Soriano Llora J. Carlos Aguirre Rodríguez Hace tiempo que me dan mareos!!! Trini tiene 76 años Acude a urgencias por caída en su domicilio Diagnóstico:
Utilidad de los nuevos tratamientos para DM2 en PPP y EA. E. Sacanella U. Geriatría - Servicio Med. Interna Hospital Clínic Barcelona
 Utilidad de los nuevos tratamientos para DM2 en PPP y EA E. Sacanella U. Geriatría - Servicio Med. Interna Hospital Clínic Barcelona DM2 en MI. Estudio DICAMI. Edad avanzada Variable tiempo de evolución
Utilidad de los nuevos tratamientos para DM2 en PPP y EA E. Sacanella U. Geriatría - Servicio Med. Interna Hospital Clínic Barcelona DM2 en MI. Estudio DICAMI. Edad avanzada Variable tiempo de evolución
Caso clínico. II Reunión de Obesidad y Diabetes
 Caso clínico. II Reunión de Obesidad y Diabetes Inmaculada Fernández Galante Servicio de Medicina Interna Hospital Clínico Universitario de Valladolid Antecedentes personales Hombre de 53 años. HTA. Hipercolesterolemia.
Caso clínico. II Reunión de Obesidad y Diabetes Inmaculada Fernández Galante Servicio de Medicina Interna Hospital Clínico Universitario de Valladolid Antecedentes personales Hombre de 53 años. HTA. Hipercolesterolemia.
UNIDAD VIII: Hormonas y farmacología del sistema endocrino. 2013
 UNIDAD VIII: Hormonas y farmacología del sistema endocrino. 2013 Objetivos de la unidad Conocer el mecanismo de acción de los fármacos del sistema endocrino y las normas que rigen su uso en la terapéutica.
UNIDAD VIII: Hormonas y farmacología del sistema endocrino. 2013 Objetivos de la unidad Conocer el mecanismo de acción de los fármacos del sistema endocrino y las normas que rigen su uso en la terapéutica.
JANUMET (sitagliptina/metformina HCl) comprimidos Aprobación inicial en Estados Unidos: 2007
 ASPECTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN Estos aspectos destacados no incluyen toda la información necesaria para usar JANUMET de forma segura y eficaz. Consulte la información de prescripción
ASPECTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN Estos aspectos destacados no incluyen toda la información necesaria para usar JANUMET de forma segura y eficaz. Consulte la información de prescripción
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN EBERCONAZOL NO APORTA NADA NUEVO Nombre Comercial y presentación: EBERNET EBERTOP (Salvat) EBESUPOL (Chiesi España) 1% crema
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN EBERCONAZOL NO APORTA NADA NUEVO Nombre Comercial y presentación: EBERNET EBERTOP (Salvat) EBESUPOL (Chiesi España) 1% crema
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Januvia 25 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Januvia 25 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
METFORMINA, SULFONILUREAS Y TIAZOLIDINEDIONAS EN EL TRATAMIENTO DE DM TIPO 2. Dra. Marcela Alfaro Rodríguez. Residente de endocrinología 2014
 METFORMINA, SULFONILUREAS Y TIAZOLIDINEDIONAS EN EL TRATAMIENTO DE DM TIPO 2 Dra. Marcela Alfaro Rodríguez. Residente de endocrinología 2014 INTRODUCCIÓN No siempre es posible alcanzar un optimo control
METFORMINA, SULFONILUREAS Y TIAZOLIDINEDIONAS EN EL TRATAMIENTO DE DM TIPO 2 Dra. Marcela Alfaro Rodríguez. Residente de endocrinología 2014 INTRODUCCIÓN No siempre es posible alcanzar un optimo control
Diagnóstico positivo y enfoque de Laboratorio.
 Diagnóstico positivo y enfoque de Laboratorio. Lic. Celia A. Alonso Rodríguez J.Sección de Endocrinología Servicio de Laboratorio Clínico HCQ Hermanos Ameijeiras e-mail: celialon@infomed.sld.cu Diagnóstico
Diagnóstico positivo y enfoque de Laboratorio. Lic. Celia A. Alonso Rodríguez J.Sección de Endocrinología Servicio de Laboratorio Clínico HCQ Hermanos Ameijeiras e-mail: celialon@infomed.sld.cu Diagnóstico
APIDRA (Sanofi Aventis) SoloStar 100 UI/ml 5 plumas precargadas 3 ml (46,97 ) OptiSet 100 UI/ml 5 plumas precargadas 3 ml (46,97 )
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN INSULINA GLULISINA Nombre Comercial y presentación: NO SUPONE UN AVANCE TERAPÉUTICO APIDRA (Sanofi Aventis) SoloStar 100 UI/ml
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN INSULINA GLULISINA Nombre Comercial y presentación: NO SUPONE UN AVANCE TERAPÉUTICO APIDRA (Sanofi Aventis) SoloStar 100 UI/ml
Las tablas de la ley según la ADA 2014. Fernando Álvarez Guisasola
 Las tablas de la ley según la ADA 2014 Fernando Álvarez Guisasola Perfil de paciente Elena, 53 años, Diabetes tipo 2 desde hace 2 años IMC 29,5 kg/m 2 En tratamiento con ISRS Secretaria de dirección a
Las tablas de la ley según la ADA 2014 Fernando Álvarez Guisasola Perfil de paciente Elena, 53 años, Diabetes tipo 2 desde hace 2 años IMC 29,5 kg/m 2 En tratamiento con ISRS Secretaria de dirección a
Actividad de formación: ACTUALIZACIÓN DE CONCEPTOS EN DIABETES MELLITUS
 Actividad de formación: ACTUALIZACIÓN DE CONCEPTOS EN DIABETES MELLITUS Título Introducción Objetivos Metodología Dirigido a Programa Ficha ACTUALIZACIÓN DE CONCEPTOS EN DIABETES MELLITUS Este curso pretende
Actividad de formación: ACTUALIZACIÓN DE CONCEPTOS EN DIABETES MELLITUS Título Introducción Objetivos Metodología Dirigido a Programa Ficha ACTUALIZACIÓN DE CONCEPTOS EN DIABETES MELLITUS Este curso pretende
Número de preguntas correctas Aprobó Sí No VALOR DEL EXAMEN 20 PUNTOS, MÍNIMO PUNTAJE PARA ACREDITACION 14 PUNTOS
 COD. o Cédula Nombre del participante: Nombre de la actividad: Seminario de Actualización en Diabetes Mellitus I y II Fecha: 13 de setiembre 2014 Número de preguntas correctas Aprobó Sí No VALOR DEL EXAMEN
COD. o Cédula Nombre del participante: Nombre de la actividad: Seminario de Actualización en Diabetes Mellitus I y II Fecha: 13 de setiembre 2014 Número de preguntas correctas Aprobó Sí No VALOR DEL EXAMEN
Aportando valor al tratamiento de niños y adolescentes Farmacocinética, Eficacia y Seguridad de DEGLUDEC
 Aportando valor al tratamiento de niños y adolescentes Farmacocinética, Eficacia y Seguridad de DEGLUDEC Gema Mira-Perceval Juan. R3 Tutor: Andrés Mingorance Delgado Endocrinología y Diabetes Pediátrica
Aportando valor al tratamiento de niños y adolescentes Farmacocinética, Eficacia y Seguridad de DEGLUDEC Gema Mira-Perceval Juan. R3 Tutor: Andrés Mingorance Delgado Endocrinología y Diabetes Pediátrica
Nuevos fármacos para la diabetes tipo 2 Jorge Navarro
 Nuevos fármacos para la diabetes tipo 2 Jorge Navarro Gdt Diabetes SEMFYC The 5 P s PATOPHYS POTENCY PRECAUTIO NS PRACTICALI TIES PLUSES ADA 75th Scientific Sessions 2015 The 6 P s PATOPHYS POTENCY PRICE
Nuevos fármacos para la diabetes tipo 2 Jorge Navarro Gdt Diabetes SEMFYC The 5 P s PATOPHYS POTENCY PRECAUTIO NS PRACTICALI TIES PLUSES ADA 75th Scientific Sessions 2015 The 6 P s PATOPHYS POTENCY PRICE
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Icandra 50 mg/850 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Icandra 50 mg/850 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
4 Diabetes Práctica 2014;05(Supl Extr 7):1-24.
 El nuevo algoritmo de la redgdps para el tratamiento individualizado de la diabetes mellitus tipo 2: abordaje según grado de control glucémico José Juan Alemán Sánchez Médico de familia. Centro de Salud
El nuevo algoritmo de la redgdps para el tratamiento individualizado de la diabetes mellitus tipo 2: abordaje según grado de control glucémico José Juan Alemán Sánchez Médico de familia. Centro de Salud
INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) INSULINAS
 Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) Datos del solicitante INSULINAS Dr. Pedro José Pines Corrales, FEA del servicio
Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) Datos del solicitante INSULINAS Dr. Pedro José Pines Corrales, FEA del servicio
ROSIGLITAZONA (MALEATO) / METFORMINA CLORHIDRATO COMPRIMIDOS RECUBIERTOS 2/500mg,4/500mg-2/1000mg-4/1000mg
 ROSIGLITAZONA (MALEATO) / METFORMINA CLORHIDRATO COMPRIMIDOS RECUBIERTOS 2/500mg,4/500mg-2/1000mg-4/1000mg Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto.
ROSIGLITAZONA (MALEATO) / METFORMINA CLORHIDRATO COMPRIMIDOS RECUBIERTOS 2/500mg,4/500mg-2/1000mg-4/1000mg Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto.
REVISIÓN DE LOS ESTÁNDARES EN LA ATENCIÓN MÉDICA EN DIABETES 2013 POR LA ADA EN RELACIÓN A LAS 2012.
 REVISIÓN DE LOS ESTÁNDARES EN LA ATENCIÓN MÉDICA EN DIABETES 2013 POR LA ADA EN RELACIÓN A LAS 2012. Además de pequeños cambios relacionados a las nuevas evidencias, y para aclarar las recomendaciones,
REVISIÓN DE LOS ESTÁNDARES EN LA ATENCIÓN MÉDICA EN DIABETES 2013 POR LA ADA EN RELACIÓN A LAS 2012. Además de pequeños cambios relacionados a las nuevas evidencias, y para aclarar las recomendaciones,
Generalidades Tiazolinedionas (glitazonas) Terapia efecto incretina : Agonistas del GLP-1 Inhibidores de DPP-4 Meglitinidas (glinidas) Conclusiones
 Antidiabéticos ticos orales Cuáles son las novedades? Laura Castelo Corral (MIR 4 Medicina Interna) Generalidades Tiazolinedionas (glitazonas) Terapia efecto incretina : Agonistas del GLP-1 Inhibidores
Antidiabéticos ticos orales Cuáles son las novedades? Laura Castelo Corral (MIR 4 Medicina Interna) Generalidades Tiazolinedionas (glitazonas) Terapia efecto incretina : Agonistas del GLP-1 Inhibidores
Taller 6. Insulinizacion B. Inicio de la Insulinizacion Casos Prácticos Dosier previo al Taller Dr. Alberto Goday
 Taller 6. Insulinizacion B. Inicio de la Insulinizacion Casos Prácticos Dosier previo al Taller Dr. Alberto Goday 01 Paciente en tratamiento con 2 antidiabéticos orales a dosis máximas y mal control metabólico
Taller 6. Insulinizacion B. Inicio de la Insulinizacion Casos Prácticos Dosier previo al Taller Dr. Alberto Goday 01 Paciente en tratamiento con 2 antidiabéticos orales a dosis máximas y mal control metabólico
LINAGLIPTINA DIABETES MELLITUS TIPO 2 VOLUMEN ; Nº. 2013 HOJA DE EVALUACIÓN DE MEDICAMENTOS. Índice: 1. INTRODUCCIÓN
 VOLUMEN ; Nº. 2013 HOJA DE EVALUACIÓN DE MEDICAMENTOS LINAGLITINA N N O N O N N N N CH 3 H NH 2 DIABETES MELLITUS TIO 2 CH 3 CH 3 Autor: Revisores: Almudena Mancebo González. Área IV. Montserrat Llopis
VOLUMEN ; Nº. 2013 HOJA DE EVALUACIÓN DE MEDICAMENTOS LINAGLITINA N N O N O N N N N CH 3 H NH 2 DIABETES MELLITUS TIO 2 CH 3 CH 3 Autor: Revisores: Almudena Mancebo González. Área IV. Montserrat Llopis
Cada comprimido contiene sitagliptina fosfato monohidrato equivalente a 25 mg de sitagliptina.
 1. NOMBRE DEL MEDICAMENTO Januvia 25 mg comprimidos recubiertos con película Januvia 50 mg comprimidos recubiertos con película Januvia 100 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA
1. NOMBRE DEL MEDICAMENTO Januvia 25 mg comprimidos recubiertos con película Januvia 50 mg comprimidos recubiertos con película Januvia 100 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA
Tratamiento con antidiabéticos orales
 120 Guías ALAD de diagnóstico, control y tratamiento de la Diabetes Mellitus Tipo 2 Capítulo 7 Tratamiento con antidiabéticos orales Recomendaciones generales para iniciar tratamiento farmacológico R7.1:
120 Guías ALAD de diagnóstico, control y tratamiento de la Diabetes Mellitus Tipo 2 Capítulo 7 Tratamiento con antidiabéticos orales Recomendaciones generales para iniciar tratamiento farmacológico R7.1:
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN ZONISAMIDA Nombre Comercial y presentaciones: ZONEGRAN (Eisai Farmacéutica) 25 mg 14 cápsulas duras (11,80 ) 50 mg 28 cápsulas
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN ZONISAMIDA Nombre Comercial y presentaciones: ZONEGRAN (Eisai Farmacéutica) 25 mg 14 cápsulas duras (11,80 ) 50 mg 28 cápsulas
CIRUGÍA METABÓLICA EN LA DM 2: CURACIÓN, O REMISIÓN Y RECAÍDA? análogos de GLP-1, una opción terapéutica en la recaída
 CIRUGÍA METABÓLICA EN LA DM 2: CURACIÓN, O REMISIÓN Y RECAÍDA? análogos de GLP-1, una opción terapéutica en la recaída Marco Fernández Blest (1), JC. Ferrer García (2) (1) Servicio de Medicina Interna.
CIRUGÍA METABÓLICA EN LA DM 2: CURACIÓN, O REMISIÓN Y RECAÍDA? análogos de GLP-1, una opción terapéutica en la recaída Marco Fernández Blest (1), JC. Ferrer García (2) (1) Servicio de Medicina Interna.
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
9. Tratamiento farmacológico de la DM2
 9. Tratamiento farmacológico de la DM2 47 Dr. William Kattah Calderón Médico Internista. Endocrinólogo. Expresidente y Miembro Honorario de la Asociación Colombiana de Endocrinología. Bogotá. Desde el
9. Tratamiento farmacológico de la DM2 47 Dr. William Kattah Calderón Médico Internista. Endocrinólogo. Expresidente y Miembro Honorario de la Asociación Colombiana de Endocrinología. Bogotá. Desde el
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
Manejo del Paciente diabético hospitalizado. Yineth Agudelo Zapata Especialista en Medicina Interna Universidad de Antioquia
 Manejo del Paciente diabético hospitalizado Yineth Agudelo Zapata Especialista en Medicina Interna Universidad de Antioquia EN DIABETES ES TAN GRAVE LA FALTA DE EDUCACIÓN COMO LA FALTA DE INSULINA Objetivos
Manejo del Paciente diabético hospitalizado Yineth Agudelo Zapata Especialista en Medicina Interna Universidad de Antioquia EN DIABETES ES TAN GRAVE LA FALTA DE EDUCACIÓN COMO LA FALTA DE INSULINA Objetivos
Incidencia episodios severos de hipoglucemia en pacientes con diabetes tipo 2 en el País Vasco: impacto en el coste sanitario
 Incidencia episodios severos de hipoglucemia en pacientes con diabetes tipo 2 en el País Vasco: impacto en el coste sanitario Edurne Alonso-Morán. Juan F. Orueta y Roberto Nuño-Solinis Introducción En
Incidencia episodios severos de hipoglucemia en pacientes con diabetes tipo 2 en el País Vasco: impacto en el coste sanitario Edurne Alonso-Morán. Juan F. Orueta y Roberto Nuño-Solinis Introducción En
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN Principio activo LINAGLIPTINA / METFORMINA Nombre comercial y presentaciones JENTADUETO 2,5mg/1000mg 60 comprimidos recubiertos
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN Principio activo LINAGLIPTINA / METFORMINA Nombre comercial y presentaciones JENTADUETO 2,5mg/1000mg 60 comprimidos recubiertos
Dra. Karen Valenzuela Landaeta
 Dra. Karen Valenzuela Landaeta Tratamiento farmacológico COMPLEMENTARIO QUE NO SUPLEMENTA EL TRATAMIENTO NO FARMACOLOGICO. Objetivos del tratamiento Alcanzar un control metabólico normal. Prevenir y tratar
Dra. Karen Valenzuela Landaeta Tratamiento farmacológico COMPLEMENTARIO QUE NO SUPLEMENTA EL TRATAMIENTO NO FARMACOLOGICO. Objetivos del tratamiento Alcanzar un control metabólico normal. Prevenir y tratar
Introducción. Papel de la obesidad en la patogenia y en el tratamiento de la DBT2
 Obesidad y riesgo metabólico Revisión sobre el empleo de la metformina para el control de peso Se registraron beneficios en términos de reducción del riesgo de diabetes en sujetos con intolerancia a la
Obesidad y riesgo metabólico Revisión sobre el empleo de la metformina para el control de peso Se registraron beneficios en términos de reducción del riesgo de diabetes en sujetos con intolerancia a la
Diabesil hoy. Introducción. Ventajas de la utilización de metformina
 Diabesil hoy Introducción Cualquier estrategia para reducir la obesidad, la grasa visceral y la resistencia a la insulina disminuye la incidencia del síndrome metabólico. Esto fue demostrado con cambios
Diabesil hoy Introducción Cualquier estrategia para reducir la obesidad, la grasa visceral y la resistencia a la insulina disminuye la incidencia del síndrome metabólico. Esto fue demostrado con cambios
Grupo Terapéutico: A10AE Insulinas y análogos de acción prolongada. Coste tratamiento/día comparativo: Principio activo...coste diario en euros
 INSULINA DETEMIR (DCI) NO APORTA NADA NUEVO Fecha de evaluación: Junio 2006 Nuevo principio activo Marca registrada (Laboratorio): Levemir (Novo Nordisk A/S) Fecha autorización (procedimiento): Junio 2004
INSULINA DETEMIR (DCI) NO APORTA NADA NUEVO Fecha de evaluación: Junio 2006 Nuevo principio activo Marca registrada (Laboratorio): Levemir (Novo Nordisk A/S) Fecha autorización (procedimiento): Junio 2004
INTRODUCCIÓN. Otras investigaciones mostraron que el incremento de la glicemia basal en ayunas en hipertiroideos fue más alta que en normales (4,5,6).
 INTRODUCCIÓN La alteración en el metabolismo de la glucosa ha sido descrita en pacientes con hipertiroidismo; muchas investigaciones se han realizado al respecto, siendo sus resultados controversiales.
INTRODUCCIÓN La alteración en el metabolismo de la glucosa ha sido descrita en pacientes con hipertiroidismo; muchas investigaciones se han realizado al respecto, siendo sus resultados controversiales.
METFORMINA CLORHIDRATO 850 mg Tabletas
 METFORMINA CLORHIDRATO 850 mg Tabletas METFORMINA CLORHIDRATO 850 mg Tabletas Recubiertas Antihiperglicémico COMPOSICIÓN: Cada tableta recubierta contiene: Metformina clorhidrato 850 mg Excipientes c.s.p.
METFORMINA CLORHIDRATO 850 mg Tabletas METFORMINA CLORHIDRATO 850 mg Tabletas Recubiertas Antihiperglicémico COMPOSICIÓN: Cada tableta recubierta contiene: Metformina clorhidrato 850 mg Excipientes c.s.p.
FENOTIPOS EN DIABETES TIPO 2. NUEVOS TRATAMIENTOS. HIPOGLUCEMIAS.
 FENOTIPOS EN DIABETES TIPO 2. NUEVOS TRATAMIENTOS. HIPOGLUCEMIAS. Bienvenidos a la tercera jornada del 49º Congreso anual de la EASD que se celebra estos días en Barcelona. Hoy el programa científico del
FENOTIPOS EN DIABETES TIPO 2. NUEVOS TRATAMIENTOS. HIPOGLUCEMIAS. Bienvenidos a la tercera jornada del 49º Congreso anual de la EASD que se celebra estos días en Barcelona. Hoy el programa científico del
INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS
 INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: Nombre Comercial y presentación: LEVOCETIRIZINA XAZAL (lab. UCB Pharma) 5 mg 20 comprimidos con cubierta pelicular (11,17
INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: Nombre Comercial y presentación: LEVOCETIRIZINA XAZAL (lab. UCB Pharma) 5 mg 20 comprimidos con cubierta pelicular (11,17
GLITAZONAS. CONTROVERSIAS EN EL TRATAMIENTO DE LA DM TIPO 2: y después de la Metformina, qué asociar..?
 CONTROVERSIAS EN EL TRATAMIENTO DE LA DM TIPO 2: y después de la Metformina, qué asociar..? GLITAZONAS Arturo Lisbona Gil Servicio de Endocrinología y Nutrición Hospital U. Central de la Defensa. Madrid
CONTROVERSIAS EN EL TRATAMIENTO DE LA DM TIPO 2: y después de la Metformina, qué asociar..? GLITAZONAS Arturo Lisbona Gil Servicio de Endocrinología y Nutrición Hospital U. Central de la Defensa. Madrid
INDIVIDUALIZANDO EL TRATAMIENTO EN DIABETES TIPO 2:
 INDIVIDUALIZANDO EL TRATAMIENTO EN DIABETES TIPO 2: ALIADOS DESPUES DE LA METFORMINA Dr. Daniel Abouganem M., FACP, FACE Centro de Tratamiento de Diabetes-HPP Seminario de Actualización SPMI Santiago de
INDIVIDUALIZANDO EL TRATAMIENTO EN DIABETES TIPO 2: ALIADOS DESPUES DE LA METFORMINA Dr. Daniel Abouganem M., FACP, FACE Centro de Tratamiento de Diabetes-HPP Seminario de Actualización SPMI Santiago de
THERAPEUTIC DECISIONS IN T 2 DM: Add-on Agents DPP4/SGLT 2 Inhibitors. Jorge Navarro Gdt Diabetes semfyc
 THERAPEUTIC DECISIONS IN T 2 DM: Add-on Agents DPP4/SGLT 2 Inhibitors Jorge Navarro Gdt Diabetes semfyc DIABETES Una enfermedad compleja que requiere un tratamiento complejo Enfermedades asociadas (como
THERAPEUTIC DECISIONS IN T 2 DM: Add-on Agents DPP4/SGLT 2 Inhibitors Jorge Navarro Gdt Diabetes semfyc DIABETES Una enfermedad compleja que requiere un tratamiento complejo Enfermedades asociadas (como
ARIPIPRAZOL En adolescentes contrastorno Bipolar I
 ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
HIPERGLUCEMIA CORTICOIDES.
 HIPERGLUCEMIA INDUCIDA POR CORTICOIDES. María Luisa Fernández López, Residente 4ºaño MFYC. Introducción. 1. Problema frecuente. Alta prevalencia de la diabetes y el elevado uso de corticoides. Provoca
HIPERGLUCEMIA INDUCIDA POR CORTICOIDES. María Luisa Fernández López, Residente 4ºaño MFYC. Introducción. 1. Problema frecuente. Alta prevalencia de la diabetes y el elevado uso de corticoides. Provoca
TRATAMI ENTO DE LA HI P ERGLUCEMI A EN DI ABETES MELLI TUS TI P O 2. Con. Especialista en Endocrinología y Nutrición
 TRATAMI ENTO DE LA HI P ERGLUCEMI A EN DI ABETES MELLI TUS TI P O 2. Con Antidiabéticos Orales Dra. Rutila Castañeda Especialista en Endocrinología y Nutrición Paciente masculino 52 años de edad Antecedentes:
TRATAMI ENTO DE LA HI P ERGLUCEMI A EN DI ABETES MELLI TUS TI P O 2. Con Antidiabéticos Orales Dra. Rutila Castañeda Especialista en Endocrinología y Nutrición Paciente masculino 52 años de edad Antecedentes:
HDL y diabetes. Nuevas formulaciones de insulina. Metformina. Riesgo y beneficio de los nuevos tratamientos.
 HDL y diabetes. Nuevas formulaciones de insulina. Metformina. Riesgo y beneficio de los nuevos tratamientos. A primera hora hubo tres charlas sobre HDL. En la primera la Dra. Rye explicó cómo la molécula
HDL y diabetes. Nuevas formulaciones de insulina. Metformina. Riesgo y beneficio de los nuevos tratamientos. A primera hora hubo tres charlas sobre HDL. En la primera la Dra. Rye explicó cómo la molécula
Cada comprimido contiene sitagliptina fosfato monohidrato equivalente a 50 mg de sitagliptina y 1.000 mg de metformina clorhidrato.
 1. NOMBRE DEL MEDICAMENTO Janumet 50 mg/1.000 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene sitagliptina fosfato monohidrato equivalente a 50
1. NOMBRE DEL MEDICAMENTO Janumet 50 mg/1.000 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene sitagliptina fosfato monohidrato equivalente a 50
POSE REINO A UNIDAD DE PLURIPATOLOXÍA E IDADE AVANZADA COMPLEXO HOSPITALARIO UNIVERSITARIO SANTIAGO DE COMPOSTELA
 ESTRATEGIAS TERAPÉUTICAS PARA EL USO DE LA INSULINA EN LA DM 2 Y SUS POSIBLES PROBLEMAS POSE REINO A UNIDAD DE PLURIPATOLOXÍA E IDADE AVANZADA COMPLEXO HOSPITALARIO UNIVERSITARIO SANTIAGO DE COMPOSTELA
ESTRATEGIAS TERAPÉUTICAS PARA EL USO DE LA INSULINA EN LA DM 2 Y SUS POSIBLES PROBLEMAS POSE REINO A UNIDAD DE PLURIPATOLOXÍA E IDADE AVANZADA COMPLEXO HOSPITALARIO UNIVERSITARIO SANTIAGO DE COMPOSTELA
TRATAMIENTO FARMACOLOGICO EN DIABETES MELLITUS 2. Dra. Graciela Fajardo Astudillo Diabetóloga Hospital Regional de Rancagua Diciembre 2016
 TRATAMIENTO FARMACOLOGICO EN DIABETES MELLITUS 2 Dra. Graciela Fajardo Astudillo Diabetóloga Hospital Regional de Rancagua Diciembre 2016 TEMARIO 1. Introducción 2. Objetivos de tratamiento 3. Factores
TRATAMIENTO FARMACOLOGICO EN DIABETES MELLITUS 2 Dra. Graciela Fajardo Astudillo Diabetóloga Hospital Regional de Rancagua Diciembre 2016 TEMARIO 1. Introducción 2. Objetivos de tratamiento 3. Factores
Tratamiento del Paciente Diabético Hospitalizado y tras el Alta Hospitalaria
 Tratamiento del Paciente Diabético Hospitalizado y tras el Alta Hospitalaria Dr Javier Ena Hospital Marina Baixa. Villajoyosa. Alicante 24 y 25 de Mayo de 2013 Parador Nacional de La Granja. Caso Clínico
Tratamiento del Paciente Diabético Hospitalizado y tras el Alta Hospitalaria Dr Javier Ena Hospital Marina Baixa. Villajoyosa. Alicante 24 y 25 de Mayo de 2013 Parador Nacional de La Granja. Caso Clínico
Actualización en el tratamiento de la Diabetes Mellitus 2
 Actualización en el tratamiento de la Diabetes Mellitus 2 Francisco Javier Ortega Ríos Médico de Familia C. S. Campos-Lampreana (Zamora) SED / redgdps Colegio Médicos Zamora, 28 octubre 2015 Esquema de
Actualización en el tratamiento de la Diabetes Mellitus 2 Francisco Javier Ortega Ríos Médico de Familia C. S. Campos-Lampreana (Zamora) SED / redgdps Colegio Médicos Zamora, 28 octubre 2015 Esquema de
ANÁLOGOS DE GLP-1. Dr. Álvaro Sillero Servicio de Endocrinología Complejo Hospitalario de Mérida
 ANÁLOGOS DE GLP-1 Dr. Álvaro Sillero Servicio de Endocrinología Complejo Hospitalario de Mérida TRATAMIENTOS DM-2 METFORMINA AGLP1 SGLT2 IDPP4 PIOGLITAZONA SU/GLINIDAS ACARBOSA HIPOGLUCEMIA NO NO NO NO
ANÁLOGOS DE GLP-1 Dr. Álvaro Sillero Servicio de Endocrinología Complejo Hospitalario de Mérida TRATAMIENTOS DM-2 METFORMINA AGLP1 SGLT2 IDPP4 PIOGLITAZONA SU/GLINIDAS ACARBOSA HIPOGLUCEMIA NO NO NO NO
Paciente varón de 71 años.
 C aso clínico Paciente diabético tipo 2 con antecedente de hipoglucemias e insuficiencia renal Rafael Julián Colás Chacartegui Médico de familia. Centro de Salud de Santoña. Gerencia de Atención Primaria
C aso clínico Paciente diabético tipo 2 con antecedente de hipoglucemias e insuficiencia renal Rafael Julián Colás Chacartegui Médico de familia. Centro de Salud de Santoña. Gerencia de Atención Primaria
ESTATINAS EN PERSONAS MAYORES
 ESTATINAS EN PERSONAS MAYORES Farmacia Atención Primaria Sevilla Servicios de Farmacia de las Áreas y Distritos Sanitarios Aljarafe Norte, Sevilla, Sur y Osuna Consideraciones previas Principalmente prescritas
ESTATINAS EN PERSONAS MAYORES Farmacia Atención Primaria Sevilla Servicios de Farmacia de las Áreas y Distritos Sanitarios Aljarafe Norte, Sevilla, Sur y Osuna Consideraciones previas Principalmente prescritas
INHIBIDORES DE ALFA-GLUCOSIDADAS INTESTINALES
 INHIBIDORES DE ALFA-GLUCOSIDADAS INTESTINALES Los inhibidores de la alfa glucosidasa funcionan inhibiendo las enzimas del borde en cepillo del enterocito (maltasas, sacarasas, dextrinasas,glucoamilasas)
INHIBIDORES DE ALFA-GLUCOSIDADAS INTESTINALES Los inhibidores de la alfa glucosidasa funcionan inhibiendo las enzimas del borde en cepillo del enterocito (maltasas, sacarasas, dextrinasas,glucoamilasas)
TIMOLOL/BRINZOLAMIDA
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI Nueva asociación: TIMOLOL/BRINZOLAMIDA Nombre comercial y presentaciones: AZARGA (Alcon) timolol 5 mg/ml + brinzolamida 10 mg/ml colirio en suspensión
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI Nueva asociación: TIMOLOL/BRINZOLAMIDA Nombre comercial y presentaciones: AZARGA (Alcon) timolol 5 mg/ml + brinzolamida 10 mg/ml colirio en suspensión
INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS
 INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: ROSIGLITAZONA EN MONOTERAPIA Nº86-2004 evaluación de nueva indicación Nombre Comercial y presentación: AVANDIA (Lab.
INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: ROSIGLITAZONA EN MONOTERAPIA Nº86-2004 evaluación de nueva indicación Nombre Comercial y presentación: AVANDIA (Lab.
Factores de riesgo Qué hay de nuevo en el último año?
 Vicente Bertomeu Martínez Servicio de Cardiología Hospital Universitario San Juan de Alicante Alicante (España) Factores de riesgo Qué hay de nuevo en el último año? VBM 2012 Reducción de mortalidad coronaria
Vicente Bertomeu Martínez Servicio de Cardiología Hospital Universitario San Juan de Alicante Alicante (España) Factores de riesgo Qué hay de nuevo en el último año? VBM 2012 Reducción de mortalidad coronaria
EXENATIDA de administración semanal
 Principio activo COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN EXENATIDA de administración semanal Nombre comercial y presentaciones BYDUREON. (Bristol Myers Squibb / Astrazeneca
Principio activo COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN EXENATIDA de administración semanal Nombre comercial y presentaciones BYDUREON. (Bristol Myers Squibb / Astrazeneca
La dura realidad de la Diabetes y las personas de edad
 La dura realidad de la Diabetes y las personas de edad Himara Davila Arroyo, MD Qué es la Diabetes? Diabetes tipo 1 se desarrolla cuando el sistema inmunológico del cuerpo destruye las células beta pancreáticas.
La dura realidad de la Diabetes y las personas de edad Himara Davila Arroyo, MD Qué es la Diabetes? Diabetes tipo 1 se desarrolla cuando el sistema inmunológico del cuerpo destruye las células beta pancreáticas.
Equivalentes terapéuticos
 Versión 1 10 Oct 2006 Equivalentes terapéuticos Por qué surge el concepto de equivalentes terapéuticos? El sistema de autorización de medicamentos por parte de las Agencias Reguladoras provoca que en el
Versión 1 10 Oct 2006 Equivalentes terapéuticos Por qué surge el concepto de equivalentes terapéuticos? El sistema de autorización de medicamentos por parte de las Agencias Reguladoras provoca que en el
CASO CLÍNICO: INSULINIZACIÓN HOSPITALARIA
 CASO CLÍNICO: INSULINIZACIÓN HOSPITALARIA Moderador: Dr. Javier García Alegría Rubén Díez Bandera Residente Medicina Interna Hospital Clínico Universitario de Salamanca Mujer de 72 años con antecedentes
CASO CLÍNICO: INSULINIZACIÓN HOSPITALARIA Moderador: Dr. Javier García Alegría Rubén Díez Bandera Residente Medicina Interna Hospital Clínico Universitario de Salamanca Mujer de 72 años con antecedentes
SÍNDROME METABÓLICO DIABETES TIPO II. Dra. Carmen Alfonso. Especialista en Endocrinología
 SÍNDROME METABÓLICO DIABETES TIPO II Dra. Carmen Alfonso. Especialista en Endocrinología SINDROME METABOLICO Es el conjunto de rasgos clínicos que traducen la RESISTENCIA A LA INSULINA Trastorno de lípidos
SÍNDROME METABÓLICO DIABETES TIPO II Dra. Carmen Alfonso. Especialista en Endocrinología SINDROME METABOLICO Es el conjunto de rasgos clínicos que traducen la RESISTENCIA A LA INSULINA Trastorno de lípidos
Inicio de la insulinización Francisco Javier García Soidán Médico de Familia. Centro de Salud de Porriño (Pontevedra)
 C ASO CLÍNICO Inicio de la insulinización Francisco Javier García Soidán Médico de Familia. Centro de Salud de Porriño (Pontevedra) INTRODUCCIÓN Según las actuales guías clínicas 1,2,el tratamiento de
C ASO CLÍNICO Inicio de la insulinización Francisco Javier García Soidán Médico de Familia. Centro de Salud de Porriño (Pontevedra) INTRODUCCIÓN Según las actuales guías clínicas 1,2,el tratamiento de
