Reacciones comunes en el metabolismo.
|
|
|
- Adolfo Cano Giménez
- hace 6 años
- Vistas:
Transcripción
1 eacciones comunes en el metabolismo. 1. Deshidrogenasas a. Dependientes de niacina Existen dos coenzimas derivadas de la vitamina niacina, El AD y el AD, Ambas son importantes transportadores de electrones, el AD generalmente asociado a reacciones degradativas mientras que el AD generalmente asociado a reacciones biosintéticas. de alcohol a ceto AD AD AD AD En la oxidación de alcohol a ceto, en general la coenzima interviniente es el AD. Ejemplo: Lactato deshidrogenasa, alcohol deshidrogenasa de aldehido a ácido i i AD AD AD AD AD AD AT AT La oxidación de aldehídos a ácidos carboxílicos se realiza utilizando un par de etapas que incluyen la conservación de parte de la energía asociada con la oxidación en la forma de un enlace fosfoanhidro en el AT. Ejemplo: gliceraldehido-- deshidrogenasa. desaminación oxidativa del glutamato: AD AD glutamato α-cetoglutarato
2 Isomerizaciones asociadas a deshidrogenasas La isomería del carbono que se oxida pasa de tetraédrica o sp4 en el alcohol a planar o sp2, en el aldehido. or ello, algunas reacciones de isomerización (por ejemplo en la reacción clave de AD AD UD-Glucosa 4-epimerasa UD-Glucosa AD AD 2 2 Intermediario oxidado 2 2 UD-Galactosa la epimerización entre glucosa y galactosa) utilizan un mecanismo en el cual se obtiene un intermediario de reacción oxidado (y planar) que puede ser convertido en alguno de los dos epímeros dependiendo del plano desde donde se porduzca el ataque para regenerar el grupo alcohólico. b. Dependientes de ivoflavina Dos derivados de esta vitamina (B2) actúan como cofactores, el flavin mononucleótido (FM) y el flavin adenin dinucleótido (FAD). Ambas coenzimas contienen un anillo de isoaloxacina que funciona como sitio funcional. En realidad el FM, no es un verdadero nucleótido, sino un derivado reducido de estos, ya que el anillo de isoloxacina no está unido a un azúcar sino al polialcohol ribitol (obtenido por reducción del 1 de la ribosa). En general las coenzimas se encuentran unidas por enlaces no covalentes a las enzimas aunque hay algunos casos donde se encuentran enlazadas covalentes. La importancia bioquímica de estas coenzimas reside en su versatilidad redox, incluyendo transferencias electrónicas y la activación del 2 molecular para reacciones de oxigenación. Una manifestación especialmente importante de su versatilidad redox es su capacidad de servir como punto de enlace entre las transferencias electrónicas de a dos electrones por vez (como usualmente ocurren en el metabolismo citosólico) y las transferencias electrónicas de a un electrón por vez (que predominan en los transportadores asociados a membranas). Así, las flavinas son utilizadas en una variedad de reacciones redox en las células, entre ellas: Deshidrogenasas Estas enzimas no usan 2 como aceptor electrónico, los ejemplos más clásicos son la succinato deshidrogenasa que transfiere los e- a las quinonas y la acil-oa deshidrogenasa que transfiere electrones al AD. En general estas son reacciones asociadas a enzimas de membrana y el aceptor de los electrones de las flavinas es la oenzima Q como por ejemplo en la succinato deshidrogenasa.
3 Q 2 Q E-FAD E-FAD 2 E-FAD E-FAD 2 sp sp 2 Q Q 2 xidasas Estas enzimas tienen como aceptor final al 2, y lo convierten en 2 o 2 2. Esta última es finalmente descompuesta en 2 y ½ 2 por acción de otra enzima asociada con la función oxidasa, la catalasa. Una característica general de las oxidasas es que, cuando un sustrato orgánico se oxida, el oxígeno agregado no proviene del 2 sino del 2. Muchas de las oxidasas son flavoproteinas, asociadas al FAD o al FM. La reacción de la citocromo oxidasa dentro del complejo IV de la cadena de transporte mitocondrial, es un ejemplo del primer tipo, mientras que las aminoácido oxidasas, enzimas que catalizan la desaminación oxidativa de los L- y D- aminoácidos, catalizan reacciones del segundo tipo. 2 2 E-FM E-FM 2 E-FM 2 2 E-FM 2 2 xigenasas Estas enzimas también producen la reacción del sustrato con 2. Sin embargo, a diferencia de las oxidasas, en este caso uno o los dos átomos del 2 terminan incorporados en el sustrato que se oxida. De acuerdo a cuantos átomos de oxígeno incorporan, se clasifican en monooxigenasas o dioxigenasas. Monooxigenasas En estas enzimas el 2 puede actuar como aceptor final. Uno de sus átomos queda unido al sustrato mientras que el otro se transforma en 2. or ejemplo la lactato oxidasa cataliza la reacción: E-FM lactato E-FM AD 2 AD 2 2 salicilato
4 La salicilato oxidasa es una enzima múltiple en la que el oxígeno, además de oxidar al substrato, también oxida al AD. Dioxigenasas El oxígeno molecular también sirve como aceptor final de la transferencia electrónica de las dioxigenasas. Estas enzimas catalizan reacciones redox más complejas en las que están involucradas, además de los nucleótidos de flavina y el 2, varios componentes redox como iones metálicos y centros de Fe-S. or ejemplo, la triptofano-2,-dioxigenasa, una enzima que participa en la ruta de catabolismo del triptofano, permite la apertura del anillo de cinco átomos del aminoácido 2 Triptofano 2 2 Triptofano-2,-dioxigenasa 2 2 -formilkinureina 2. Transferasas a. Transferasas de grupos de un carbono Que utilizan Folato La vitamina ácido fólico es el precursor de la familia de las coenzimas del tetrahidrofolato. Estas moléculas sirven como cosubstratos más que como grupos prost'éticos fuertemente unidos, en reacciones que implican la transferencia de unidades de un carbono.las unidades de un carbono son en generla derivados de formaldehido o del formiato. El formaldehido es altamente reactivo y potencialmente tóxico. or el contrario, en comparación el formiato es prácticamente no reactivo. Estas coenzimas mantienen a estos sustratos en una forma en la que ellos se encuentran suficientemente activados para ser utilizados en reacciones metabólicas pero no tanto como para que llegaran a ser tóxicos. La lista siguiente indica los miembros de esta familia de coenzimas junto con la actividad asociada a cada uno de ellos: 1. Tetrahidrofolato es activado por la reacción con formiato y AT para convertirlo en 10 - formiltetrahidrofolato. En esta molécula el elemento de un carbono activado posee un estado de oxidación de 2, idéntico al que poseía como formiato, ya que lo único que se produjo es el intercambio de una unión - (en el formiato) por una unión - (en la coenzima). tra reacción importante por la que se 2. El 10 -formiltetrahidrofolato actúa como un donor de grupos formilo. Esta molécula es interconvertible con el metenil-tetrahidrofolato por medio de la acción de la ciclohidrolasa.. El metilen-tetrahidrofolato es un donor de grupos hidroximetilos en una gran variedad de reacciones pero también actúa como donor de grupos metilo para la timidilato sintasa que cataliza la metilación del dum para obtener el dtm ( en esta reacción el folato es oxidado a dihiro folato el cual debe ser reducido por AD para obtener la coenzima en su estado activo). El metilen-tetrahidrofolato puede ser obtenido ya sea por la reducción del metenil-tetrahidrofolato utilizando AD o por la reacción de la serina hidroximetil transferasa : serina tetrahidrofolato glicina metilen-tetrahidrofolato.
5 4. el 5 -metil-tetrahidrofolato, puede ser obtenido por reducción del metilentetrahidrofolato y es utilizado como donor de grupos metilo para la reacción de metilación del sulfidrilo de la homocisteína para sintetizar metionina formimino-tetrahidrofolato Estado de oxidación de la unidad de un carbono formil-tetrahidrofolato 2 iclohidrolasa , 10 -metenil-tetrahidrofolato ácido fórmico 2 5 Tetrahidrofolato Serina-hidroximetil Transferasa Serina (Glu) n 5, 10 -metilen-tetrahidrofolato deshidrogenasa Glicina 2 AD AD , 10 -metilen-tetrahidrofolato AD formaldehido 5, 10 -metilen-tetrahidrofolato reductasa AD metil-tetrahidrofolato metanol b. que transfieren grupos aldehido o cetona a. Dependientes de Tiamina pirofosfato (T) El T es un derivado fosforilado de la vitamina B1 o tiamina. Las reacciones en las que interviene la tiamina pirofosfato como cofactor involucran la ruptura o la formación de enlaces - de uno de estos dos tipos: a. 1 1 b
6 Si 1 es un, la molécula señalada en a es un α-cetoácido y la reacción involucrada es una descarboxilación, como por ejemplo la del piruvato (2 = ). omo regla general en la descarboxilación de α-cetoácidos la coenzima asociada a la enzima es la tiamina pirofosfato. El carbono carboxílico se oxida a 2 y el carbono carbonílico se reduce a aldehido. En todo caso, siempre es necesario la presencia de un carbono unido a un oxhidrilo, adyascente a un carbono carnonílico. El mecanismo de reacción involucra la formación y la estabilización de un carbanión sobre el grupo que se une a la coenzima, según el siguiente esquema: E 1 -B : S 1 E 1 -B- S 2 1 E 1 -B : 2 S S S En la transcetolasa se transfiere entre dos moléculas el grupo - 2. El al que estaba unido el grupo normalmente es un y queda oxidado a aldehido. El carbono receptor, normalmente es un aldehido y queda convertido en un b. on mecanismo de catálisis ácido-base Las Aldolasas o transaldolasas pertenecen a este grupo. El mecansimo de catálisis no requiere de ningún cofactor y los aminoácidos del sitio activo que particpan de la reacción corresponden a aquellos que pueden poseer ácidos o bases conjugados. Estas enzimas son muy específicas para sustratos cuya estructura es equivalente a la estructura de los tres o cuatro primeros átomos de la fructosa.
7 Transaldolasa 2 -X Transaldolasa X :B 2 X _ 2-2 gliceraldehido--fosfato B 2-2 Eritrosa-4-fosfato 2 X :B Fructosa-6-fosfato 2-2 Sedoheptulosa-7-fosfato Aldolasa Esta enzima reconoce el extremo de una molécula de azúcar (o similar) que cotenga un derivado de la hidroxiacetona. ompen o forman un enlace - entre un resto de (hidroxiacetona fosfato) y liberan (o unen) el resto de la molécula en la que el 1 (que antes tenía un oxhidrilo) será un aldehido por medio de una catálisis ácido-base similar a la anteriormente mostrada. 2 2 Aldolasa c. Acil transferasas a. que utilizan oenzima A (oas). La mayoría de las acil transferasas son de este tipo. Un ejemplo es la enzima glutamato-acetil transferasa que permite incorporar un grupo acilo sobre el nitrógeno alfa del glutamato para protegerlo de la ciclación en etapas posteriores en la ruta de síntesis de arginina. La oas es el derivado más importante de la vitamina pantotenato. Esta coenzima activa los
8 sustratos para las reacciones de transferencia de grupos acilos o de enolización a través de su esterificación con el grupo sulfidrilo terminal de la coenzima. En la figura se ve la imagen de la oa obtenida del programa ASML. El código de color es el siguiente: -gris, -rojo, -azul, -naranja, S-amarillo. El único átomo de S que contiene la coenzima A es el sulfhidrilo reactivo donde se unen a los acilos. Un ejemplo de la acción de la oas es la reacción de condensación entre dos moléculas de acetil-oa 2 --SoA ----SoA oas La coenzima activa la enolización de una de las moléculas de acetil-oa, de modo que pueda actuar como nucleófilo, y activa el carbonil del segundo acetato, de manera que actue como electrófilo, de manera que: 1. La carga que se desarrolla en el recientemente formado enolato, es más estable que la que podría establecerse en una molécula de acetato, la cual tendría otra carga negativa adyacente. 2. or la misma razón, el ataque nucleofílico sobre el segundo carbonilo, es mas favorable que si se realizara sobre el correspondiente carboxilato.. El anion oas- es un grupo saliente más estable, comparado con el hidroxilato. 4. La reacción tiene dos reactivos y dos productos, por lo que está entrópicamente favorecida si se la compara con la condensación de dos acetatos libres que implican dos reactivos pero solo un producto. El tioester sirve a este propósito aún mejor que el correspondiente oxoéster, debido a que el átomo de S dona una menor densidad electrónica sobre el carbonilo adyacente que lo que lo haría el más electronegativo átomo de. Estas actividades se supone que pueden llegar a aumentar la actividad catalítica en el orden de veces. Además, el resto de la oas podría ayudar a estabilizar los estados de transición de otras maneras. b. Que utilizan ácido lipoico. Esta coenzima posee un anillo de 5 miembros, dos de los cuales son átomos de S unidos por un enlace tioéter. Es capáz de transferir tanto electrones como grupos acilo activados a otra molécula conteniedo tioles, como la oas. En el proceso de transferencia esta coenzima es reducida transitoriamente a ácido dihidrolipoico (conteniendo los dos átomos de S en la forma de tioles) el cual es reoxidado por medio de la utilización de coenzimas de niacina o de flavina.
9 d. Transaminasas Las podemos clasificar según el grupo dador del nitrógeno y también en base a la conformación del átomo de carbono que funciona como aceptor. En la tabla siguiente se puede observar esta clasificación. Además, los cambios en el estado redox de los productos con respecto a los sustratos son diferentes para los tres tipos de transaminasas. DAD AET DUT- DAD DUT AET EAIÓ MUMETE ALADA glutamato ceto 1 2 α-cetoglutarato 2 2 amino-derivado aspartato 2 2 ceto 1 2 fumarato imino-derivado 1 2 AT AD i o AT AM i glutamina enol 1 2 glutamato enamino-derivado AT AD i a. Transaminasas del tipo I o del glutamato orresponden a las transaminaciones más comunes e implican el intercambio de grupos ceto por amino entre dos sustratos orgánicos. Desde el punto de vista de la biosíntesis de aminoácidos, el dador de grupos amino más general es el glutamato que se convierte en la reacción en α-cetoglutarato, y por lo tanto su carbono α se oxida. or el contrario el sustrato es un α-oxoácido que se convierte en un compuesto más reducido, el correspondiente α- aminoácido. El mecanismo de reacción está explicado más adelante junto con las liasas dependientes de fosfato de piridoxal. El glutamato puede ceder su grupo amino a otros compuestos con un ceto, además de a los α-cetoácidos. En este tipo de transaminaciónes tanto el dador como el aceptor del grupo amino cambian de estado de oxidación. El balance redox global es nulo. b. Transaminasas de tipo II o del aspartato En este tipo de transaminaciones el aceptor es también un ceto, pero en este caso es convertido a una imina, sin cambiar su estado de oxidación. or su parte el compuesto dador de nitrógeno, el aspartato, es convertido en fumarato, también sin cambiar su estado de oxidación global. Sin embargo si existe un cambio de estado de oxidación en los dos átomos de carbono centrales de la molécula de aspartato, el 2 se reduce una unidad, mientras que el se oxida en la misma proporción. or lo mismo, en este tipo de transaminaciónes aunque ni el dador ni el aceptor del grupo amino cambian de estado de oxidación, si existe un cambio en la estructura redox del dador de nitrógenos. El balance redox global es nulo. uando el aspartato es el dador de nitrógeno, como en la síntesis de arginina o en la síntesis de AM, se produce una reacción de intercambio en el que el dador se convierte en fumarato mientras que el aceptor (un ceto) se convierte en primera instancia en un imino. Tomando como ejemplo este último caso:
10 AD AD α-cetoglutarato glutamato 2 xalacetato 2 Malato IM 2 2 Aspartato GT GD i 2 2 Fumarato AM 2 Vemos que debido a la necesidad de regeneración del aspartato a partir del fumarato, se genera poder reductor en el proceso de transaminación como si estuviéramos en una ruta de oxidación de los sustratos. Ese poder reductor proviene de una molécula de glutamato que se oxida a α-cetoglutarato, en forma neta por cada vuelta del ciclo que mostramos. En algunos casos (como en la síntesis de arginina) estas reacciones están acopladas a la hidrólisis de enlaces de alta energía, a veces a uno y otras a dos de estos enlaces. c. Transaminasas de tipo III o de la glutamina uando el dador de grupos amino es la glutamina, no cambia el estado de oxidación ni del dador ni del aceptor del grupo amino. En general estas reacciones están acopladas a la hidrólisis del AT. La glutamina se convierte en glutamato (igual estado redox) y el sustrato puede modificarse por medio del intercambio de una unión - por otra - 2 o en menor proporción de casos de una unión = por otra =, conservando también su estado redox. d. Aminaciones reductivas La incorporación de 4 inorgánico en el oxalacetato es una reacción redox que requiere del gasto de una molécula de AD. e. Kinasas a. Intercambiadoras de fosfoanhidros Ejemplo: fosfogliceratoquinasa. b. Tiokinasas Ejemplo: succinil-oa tiokinasa. c. Fosforilación de Ejemplo: hexoquinasa en 6 o fructoquinasa en 1
11 . idrolasas iclasas Ejemplo: dihidroorotato sintasa. Generadoras de un enlace de alta energía Ejemplo: enolasa. Isomerasas Ejemplo: aconitasa. xidación de un metileno. Ejemplo: succinato deshidrogenasa fumarasa. 4. Liasas/Descarboxilasas Las descarboxilasas eliminan un grupo ácido carboxílico de un compuesto reemplazando la unión - por una -. Muchas descarboxilasas/carboxilasas tienen como cofactor a la biotina (ejemplo M descarboxilasa) o no tienen ningun cofactor. a. Liasas Dependientes de Fosfato de iridoxal Esta coenzima es derivada de la vitamina B6. El grupo activo es el aldehido, que forma una 4 b 2 1 base de Schiff con el grupo amino de los α-aminoácidos. Esta base de Schiff permite estabilizar la formación de un carbanión en los átomos de α o β del aminoácido. Esto facilita la ruptura y el consiguiente intercambio de cualquiera de los enlaces marcados por las flechas azules o rojas de esta figura: Los tipos de actividades que son catalizadas por enzimas que utilizan al fosfato de piridoxal como cofactor son las siguientes: a Tipo de Enzima Transaminasas: acemasas: Liasas (tipo aldolasa): β-descarboxilasa: ejemplo oxalacetato glutamato ---> L-aspartato α-cetoglutarato L-alanina ---> D-alanina glicina formil-tf ---> L-serina L-aspartato ---> 2 L-alanina El mecanismo general de estas reacciones es el que se muestra más abajo. Todos los mecanismos comienzan por la reacción señalada como 1, que implica la formación de la base de Schiff.
12 El resto del mecanismo es utilizada solo en parte por cada uno de los tipos de reacción que individualizamos en la tabla más arriba. β α 2 Sustratos β α 2 Base de Schiff - β α β 2 2 e β β 4 α f α α β 2 - α β α 2 β α 2.. a b c β 2 α d or ejemplo las transaminasas utilizan solo las reacciones 1, 2 y. En estas enzimas, la hidrólisis del compuesto señalado como d. produce la amina derivada del piridoxal (piridoxamina) y libera un α-cetoácido. La piridoxamina puede a su vez reaccionar con otro α- cetoácido para regenerar un compuesto del tipo d. Este compuesto puede ahora revertir las reacciones, perdiendo un protón del carbono aldehídico del piridoxal, luego tautomerizándose (para formar un carbanión en el α, un compuesto del tipo a.) y captando un protón para regenerar una base de Schiff, que contiene el esqueleto carbonado del α-cetoácido que fue incorporado en último término. La hidrólisis de esta base de Schiff regenerará el fosfato de piridoxal y liberará un α-aminoácido. En las reacciones de racemización el tipo de reacciones utilizadas es solamente la 1 y la 2. En el compuesto marcado como b., el α inicialmente tetraédrico está convertido en un carbono planar (sp 2 ). De esta manera el de la reacción 2. puede ser reincorporado de cualquiera de los dos lados del plano para regenerar la base de Schiff. La hidrólisis de esta base generará entonces cualquiera de los dos compuestos racémicos. b. que utilizan Biotina Esta vitamina está normalmente unida a la enzima a través de una larga cadena hidrocarbonada. El grupo funcional para la carboxilación es el átomo de nitrógeno 1 de un grupo imidazol. La biotina sirve como agente carboxilante que utiliza el bicarbonato como sustrato y fuente del grupo carboxilo. En la primera etapa el bicarbonato es activado: AT bicarbonato carbonil-fosfato AD
13 Después el grupo carboxilo activado se une a la biotina a través del 1 recién mencionado, y desde allí es transferido a otra molécula orgánica como por ejemplo en la carboxilación del piruvato a oxalacetato: Enz 1 Enz i carbonil-fosfato S biotina S 2 S Enz 2 2 S biotina Enz La biotina se encuentra unida a la enzima en forma covalente, a travéz de una unión amida con el resto amino de una lisina de la proteína. De esta manera el centro activo de la biotina (el sitio de unión al 2 ) esta ligado a la enzima a través de un largo brazo que contiene en forma mayoritaria metilenos (8 en total, 4 de la lisina y 4 de la biotina) y que por lo mismo posee una gran flexibilidad y posibilidad de movimientos. En general los sitios catalíticos de estas dos actividades (reacciones 1 y 2 en la figura) están bien separados, de manera que la biotina se encuentra particularmente bien localizada (con su largo brazo de unión a la enzima) para hacer de puente entre ambos. 5. Transferencia electrónica a. De a un electrón por vez Las proteínas que contienen iones metálicos, como hierro, u, Mg o Mn, transfieren en general los electrones de a uno por vez a su aceptor. Entre estas tenemos a los citocromos, las proteínas de los clusters de Fe-S, las clorofilas (y sus derivados no asociados a iones las feofitinas), y los componentes de la rueda de Mn. En general estas trasportadores de a un electron por vez están asociados a membranas. b. De a dos electrones por vez Estas transferencias se dan en general en el metabolismo en solución. La mayoría de las deshidrogenasas celulares que utilizan derivados de la niacina o de la riboflavina como coenzimas intervienen en este tipo de procesos.
14 c. De a uno o dos electrones por vez Los nucleótidos de flavina (FM o FAD) así como la coenzima Q, son capaces de intervenir en transferencias electrónicas de a dos electrones al mismo tiempo o de sólo un electrón por vez. En este último caso se genera un intermediario (que incluso puede tener una carga negativa como en el caso de la oq) que contiene un electrón desapareado. Estos intermediarios del FAD, FM o de la oq, son semiquinonas que, a diferencia de las formas totalmente oxidadas o totalmente reducidas de las coenzimas, son normalmente incapaces de moverse libremente a - A FM (en negro) o FAD (en negro y azul) los átomos reactivos están en rojo 2 través de la membrana. Generalmente, estas semiquinonas tienen sitios de anclaje a una proteína, perteneciente a alguno de los complejos donde actúan, siempre en un sitio adyascente a una de las soluciones acuosas en contacto con la membrana, ya sea la matriz o el espacio intermembrana. 5 1 Flavoquinona (FM o FAD) 5 1 Flavohidroquinona (FM 2 o FAD 2 ) B 5 1 Flavosemiquinona (FM. o FAD. ) e - e Ubiquinona (oenzima Q) lastoquinona e - e - 2 e - 2 e - ambios en los estados de oxidación de la Ubiquinona De esta manera estas coenzimas están adaptadas para hacer de nexo entre las reacciones redox que ocurren en el citosol (de a dos electrones) y las que ocurren en las membranas (de a un electrón).
Ciclo del ácido cítrico (Krebs o Ciclo de los ácidos tricarboxílicos
 Ciclo del ácido cítrico (Krebs o Ciclo de los ácidos tricarboxílicos Oxidación de los derivados de la glucosa para dar CO 2 Dentro de la mitocondria (eucariotas) Eje central del metabolismo celular Vía
Ciclo del ácido cítrico (Krebs o Ciclo de los ácidos tricarboxílicos Oxidación de los derivados de la glucosa para dar CO 2 Dentro de la mitocondria (eucariotas) Eje central del metabolismo celular Vía
RESULTADO DE APRENDIZAJE:
 Explicar las reacciones químicas del ciclo de Krebs y su regulación RESULTADO DE APRENDIZAJE: Relacionar el metabolismo de las distintas macromoléculas alrededor del Ciclo de Krebs Las reacciones se llevan
Explicar las reacciones químicas del ciclo de Krebs y su regulación RESULTADO DE APRENDIZAJE: Relacionar el metabolismo de las distintas macromoléculas alrededor del Ciclo de Krebs Las reacciones se llevan
Fosforilación a nivel de sustrato. Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria).
 Fosforilación a nivel de sustrato Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria). La Fosforilación a nivel de sustrato es un mecanismo poco habitual de formación de ATP FOSFOGLICERATO
Fosforilación a nivel de sustrato Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria). La Fosforilación a nivel de sustrato es un mecanismo poco habitual de formación de ATP FOSFOGLICERATO
CADENA RESPIRATORIA O CADENA DE TRANSPORTE DE ELECTRONES
 CADENA RESPIRATORIA O CADENA DE TRANSPORTE DE ELECTRONES El NADH y FADH2 obtenidos contienen un par de electrones que se transfieren al O2 con liberación de energía. La cadena respiratoria transporta los
CADENA RESPIRATORIA O CADENA DE TRANSPORTE DE ELECTRONES El NADH y FADH2 obtenidos contienen un par de electrones que se transfieren al O2 con liberación de energía. La cadena respiratoria transporta los
Clase 4 Metabolismo bacteriano
 Clase 4 Metabolismo bacteriano Composición química de las bacterias. Fuentes de carbono y energía. Categorías nutricionales. Catabolismo y anabolismo. Reacciones de óxido-reducción, torre de electrones,
Clase 4 Metabolismo bacteriano Composición química de las bacterias. Fuentes de carbono y energía. Categorías nutricionales. Catabolismo y anabolismo. Reacciones de óxido-reducción, torre de electrones,
TEMA 11 Metabolismo de lípidos y de aminoácidos
 TEMA 11 Metabolismo de lípidos y de aminoácidos 1. Movilización de lípidos de reserva 2. Degradación y biosíntesis de ácidos grasos 3. Formación de cuerpos cetónicos 4. Degradación de aminoácidos y eliminación
TEMA 11 Metabolismo de lípidos y de aminoácidos 1. Movilización de lípidos de reserva 2. Degradación y biosíntesis de ácidos grasos 3. Formación de cuerpos cetónicos 4. Degradación de aminoácidos y eliminación
METABOLISMO DE PROTEINAS Y AMINOACIDOS
 sección III, metabolismo de proteínas y aminoácidos. Harper, bioquímica, 28a edición. ALFREDO ABADIA G. RESIDENTE III AÑO MD DE LA ACTIVIDAD FISICA Y EL DEPORTE FUCS-HISJ. METABOLISMO DE PROTEINAS Y AMINOACIDOS
sección III, metabolismo de proteínas y aminoácidos. Harper, bioquímica, 28a edición. ALFREDO ABADIA G. RESIDENTE III AÑO MD DE LA ACTIVIDAD FISICA Y EL DEPORTE FUCS-HISJ. METABOLISMO DE PROTEINAS Y AMINOACIDOS
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO
 UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
FOSFORILACIÓN OXIDATIVA
 FOSFORILACIÓN OXIDATIVA a) Reacciones de transferencia de electrones en las mitocondrias b) Síntesis de ATP LOCALIZACIÓN Y ESTRUCTURA DE LAS MITOCONDRIAS LA FOSFORILACIÓN OXIDATIVA SE LLEVA A CABO EN LA
FOSFORILACIÓN OXIDATIVA a) Reacciones de transferencia de electrones en las mitocondrias b) Síntesis de ATP LOCALIZACIÓN Y ESTRUCTURA DE LAS MITOCONDRIAS LA FOSFORILACIÓN OXIDATIVA SE LLEVA A CABO EN LA
Ciclo de Krebs Destino del piruvato. Descarboxilación oxidativa. Aspectos estructurales y mecanismos de la piruvato deshidrogenasa.
 Ciclo de Krebs Destino del piruvato. Descarboxilación oxidativa. Aspectos estructurales y mecanismos de la piruvato deshidrogenasa. Relevancia del ciclo de Krebs dentro del metabolismo en general. Descripción
Ciclo de Krebs Destino del piruvato. Descarboxilación oxidativa. Aspectos estructurales y mecanismos de la piruvato deshidrogenasa. Relevancia del ciclo de Krebs dentro del metabolismo en general. Descripción
La Fosforilación Oxidativa Mitocondrial. Parte 1. Javier Corzo Departamento de Bioquímica y Biología Molecular Universidad de La Laguna
 La Fosforilación xidativa Mitocondrial. Parte 1. Javier orzo Departamento de Bioquímica y Biología Molecular Universidad de La Laguna 1 oncepto básico 2 Potenciales redox 3 Transportadores de electrones
La Fosforilación xidativa Mitocondrial. Parte 1. Javier orzo Departamento de Bioquímica y Biología Molecular Universidad de La Laguna 1 oncepto básico 2 Potenciales redox 3 Transportadores de electrones
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA
 BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
El catabolismo es la fase degradativa del metabolismo. El catabolismo es semejante en organismos autótrofos y heterótrofos.
 PROCESOS CATABÓLICOS El catabolismo es la fase degradativa del metabolismo El catabolismo es semejante en organismos autótrofos y heterótrofos. Son reacciones de oxidación y reducción acopladas En estas
PROCESOS CATABÓLICOS El catabolismo es la fase degradativa del metabolismo El catabolismo es semejante en organismos autótrofos y heterótrofos. Son reacciones de oxidación y reducción acopladas En estas
Metabolismo II. Anabolismo
 Metabolismo II. Anabolismo I. Definición II. Tipos de anabolismo III. Anabolismo Heterótrofo A. Gluconeogénesis B. Glucogenogénesis C. Amilogénesis D. Anabolismo de lípidos E. Anabolismo de proteínas F.
Metabolismo II. Anabolismo I. Definición II. Tipos de anabolismo III. Anabolismo Heterótrofo A. Gluconeogénesis B. Glucogenogénesis C. Amilogénesis D. Anabolismo de lípidos E. Anabolismo de proteínas F.
Catabolismo de los glúcidos
 atabolismo de los glúcidos (un ejemplo del uso de LYX/L A TEX en Biología) Luque Resumen Práctica final del curso Software Libre y Educación: Guadalinex (Thales-ica 2004-05). Estudio de la degradación
atabolismo de los glúcidos (un ejemplo del uso de LYX/L A TEX en Biología) Luque Resumen Práctica final del curso Software Libre y Educación: Guadalinex (Thales-ica 2004-05). Estudio de la degradación
Tema 7. Actividad enzimática
 Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
RESPIRACIÓN CELULAR. C 6 H 12 O 6 + O 2 + 6H 2 O CO H 2 O + Energía
 RESPIRACIÓN CELULAR Es el proceso por el cual la energía química de las moléculas de "alimento" es liberada y parcialmente capturada en forma de ATP. Los carbohidratos, grasas y proteínas pueden ser usados
RESPIRACIÓN CELULAR Es el proceso por el cual la energía química de las moléculas de "alimento" es liberada y parcialmente capturada en forma de ATP. Los carbohidratos, grasas y proteínas pueden ser usados
Mitocondrial. Potencial de transferencia de electrones
 TEMA 7.a Cadena de Transporte Electrónico 1. Introducción y repaso: La mitocondria Mitocondrial Potencial de transferencia de electrones 2. Transportadores electrónicos 3. Organización y funcionamiento
TEMA 7.a Cadena de Transporte Electrónico 1. Introducción y repaso: La mitocondria Mitocondrial Potencial de transferencia de electrones 2. Transportadores electrónicos 3. Organización y funcionamiento
CATABOLISMO DE GLÚCIDOS.
 CATABOLISMO DE GLÚCIDOS. El Catabolismo de glúcidos consiste en reacciones de oxidación de monosacáridos y consta de los siguientes procesos: 1. Glucólisis. 2. Respiración celular. Respiración aerobia.
CATABOLISMO DE GLÚCIDOS. El Catabolismo de glúcidos consiste en reacciones de oxidación de monosacáridos y consta de los siguientes procesos: 1. Glucólisis. 2. Respiración celular. Respiración aerobia.
INTRODUCCIÓN A LA BIOQUÍMICA. La bioquímica se puede definir como el estudio de las bases moleculares de la vida.
 INTRODUCCIÓN A LA BIOQUÍMICA La bioquímica se puede definir como el estudio de las bases moleculares de la vida. BIOMOLECULAS + Los seres vivos están formados por miles de clases diferentes de moléculas
INTRODUCCIÓN A LA BIOQUÍMICA La bioquímica se puede definir como el estudio de las bases moleculares de la vida. BIOMOLECULAS + Los seres vivos están formados por miles de clases diferentes de moléculas
-La molécula glucídica utilizada por las células como combustible es la glucosa, que puede proceder de:
 BIOLOGÍA CATABOLISMO DE LOS GLÚCIDOS CARACTERES GENERALES -La molécula glucídica utilizada por las células como combustible es la glucosa, que puede proceder de: a)la digestión de los nutrientes. b)las
BIOLOGÍA CATABOLISMO DE LOS GLÚCIDOS CARACTERES GENERALES -La molécula glucídica utilizada por las células como combustible es la glucosa, que puede proceder de: a)la digestión de los nutrientes. b)las
TRANSPORTE ELECTRONICO Y FOSFORILACION OXIDATIVA
 TRANSPORTE ELECTRONICO Y FOSFORILACION OXIDATIVA 1.- CADENA TRANSPORTADORA O DE ELECTRONES La glucólisis y el ciclo del ácido cítrico generan una cantidad relativamente baja de energía en forma de ATP.
TRANSPORTE ELECTRONICO Y FOSFORILACION OXIDATIVA 1.- CADENA TRANSPORTADORA O DE ELECTRONES La glucólisis y el ciclo del ácido cítrico generan una cantidad relativamente baja de energía en forma de ATP.
Biología 2º Bachiller. Tema 13: Respiración y fotosíntesis
 Biología 2º Bachiller Tema 13: Respiración y fotosíntesis Qué vamos a ver en este tema?: Respiración aerobia: Oxidación de moléculas orgánicas para la obtención de energía Catabolismo de glúcidos: Oxidación
Biología 2º Bachiller Tema 13: Respiración y fotosíntesis Qué vamos a ver en este tema?: Respiración aerobia: Oxidación de moléculas orgánicas para la obtención de energía Catabolismo de glúcidos: Oxidación
METABOLISMO ENERGETICO. Dra. Carmen Aída Martínez
 METABOLISMO ENERGETICO Dra. Carmen Aída Martínez CICLO DE KREBS Ciclo de los Ácidos Tricarboxílicos (ATC) Vía común del metabolismo de todos los combustibles (grasas, Carbohidratos y proteínas) Localizado
METABOLISMO ENERGETICO Dra. Carmen Aída Martínez CICLO DE KREBS Ciclo de los Ácidos Tricarboxílicos (ATC) Vía común del metabolismo de todos los combustibles (grasas, Carbohidratos y proteínas) Localizado
Respiracion Celular Prof. Nerybelle Perez-Rosas 2011
 Respiracion Celular Prof. Nerybelle Perez-Rosas 2011 2 Respiracion Celular Podemos clasificar organismos basandonos en la forma en que obtienen energia. autotrofos: son capaces de producir sus propias
Respiracion Celular Prof. Nerybelle Perez-Rosas 2011 2 Respiracion Celular Podemos clasificar organismos basandonos en la forma en que obtienen energia. autotrofos: son capaces de producir sus propias
Biopolímero s (4831)
 Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
CATABOLISMO ESQUEMA METABOLISMO
 ESQUEMA METABOLISMO 1.- ENERGÉTICA CELULAR 1.1 Concepto de reacción espontánea y no espontánea Energía libre Reacciones espontáneas exoergónicas Reacciones no espontáneas endoergónicas Sistemas en equilibrio
ESQUEMA METABOLISMO 1.- ENERGÉTICA CELULAR 1.1 Concepto de reacción espontánea y no espontánea Energía libre Reacciones espontáneas exoergónicas Reacciones no espontáneas endoergónicas Sistemas en equilibrio
1- DESCARBOXILACIÓN OXIDATIVA DEL PIRUVATO. 2- CICLO DE KREBS. Dr. Mynor A. Leiva Enríquez
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO, 2011 1- DESCARBOXILACIÓN OXIDATIVA DEL PIRUVATO. 2- CICLO DE KREBS. Dr. Mynor A.
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO, 2011 1- DESCARBOXILACIÓN OXIDATIVA DEL PIRUVATO. 2- CICLO DE KREBS. Dr. Mynor A.
Metabolismo. Forma de obtención de carbono. Corresponde a la actividad. participan sistemas multienzimáticos (rutas metabólicas) RUTAS METABÓLICAS
 Facultad de Ciencias de la Salud BIO160 Bioquímica i General Metabolismo METABOLISMO Corresponde a la actividad coordinada que ocurre dentro de una célula, en la cual participan sistemas multienzimáticos
Facultad de Ciencias de la Salud BIO160 Bioquímica i General Metabolismo METABOLISMO Corresponde a la actividad coordinada que ocurre dentro de una célula, en la cual participan sistemas multienzimáticos
Respiración Aeróbica y Anaeróbica, y Control
 Fisiología Vegetal Respiración Aeróbica y Anaeróbica, y Control Dra. Karen Peña R Respiración: Oxido-Reducción Organelos Glicólisis, Formación de acetil CoA, Ciclo de Krebs, Cadena Transportadora de Electrones,
Fisiología Vegetal Respiración Aeróbica y Anaeróbica, y Control Dra. Karen Peña R Respiración: Oxido-Reducción Organelos Glicólisis, Formación de acetil CoA, Ciclo de Krebs, Cadena Transportadora de Electrones,
VÍA DE PENTOSA FOSFATO
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, UNIDAD DIDÁCTICA: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,013 VÍA DE PENTOSA FOSFATO DR. MYNOR A. LEIVA ENRÍQUEZ Fuente: Bioquímica,
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, UNIDAD DIDÁCTICA: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,013 VÍA DE PENTOSA FOSFATO DR. MYNOR A. LEIVA ENRÍQUEZ Fuente: Bioquímica,
Una visión detallada. Clase 13. Energética celular Glucólisis y oxidación aeróbica II. 1. NADH deshidrogenasa 26/10/2009
 Clase 13. Energética celular Glucólisis y oxidación aeróbica II Una visión detallada 1. Rutas metabólicas, niveles de complejidad y mapas metabólicos. 2. Glucólisis: principal ruta de nivel 2. 3. Respiración
Clase 13. Energética celular Glucólisis y oxidación aeróbica II Una visión detallada 1. Rutas metabólicas, niveles de complejidad y mapas metabólicos. 2. Glucólisis: principal ruta de nivel 2. 3. Respiración
Metabolismo. Conjunto de reacciones bioquímicas de una célula. El metabolismo comprende dos grandes tipos de reacciones:
 Metabolismo Conjunto de reacciones bioquímicas de una célula El metabolismo comprende dos grandes tipos de reacciones: 1) reacciones de mantenimiento, que suministran a) energía b) poder reductor c) precursores
Metabolismo Conjunto de reacciones bioquímicas de una célula El metabolismo comprende dos grandes tipos de reacciones: 1) reacciones de mantenimiento, que suministran a) energía b) poder reductor c) precursores
ATP. Catabolismo. Anabolismo ATP
 CAITUL 2: METABLISM Conceptos generales Comprende el conjunto de reacciones bioquímicas que ocurren en los tejidos de los seres vivos. Específicamente, a las transformaciones que ocurren dentro de las
CAITUL 2: METABLISM Conceptos generales Comprende el conjunto de reacciones bioquímicas que ocurren en los tejidos de los seres vivos. Específicamente, a las transformaciones que ocurren dentro de las
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR
 INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
Mitocondrias. Son los organoides encargados de proveer de energía a la célula, mediante la síntesis de ATP
 Mitocondrias Mitocondrias Son los organoides encargados de proveer de energía a la célula, mediante la síntesis de ATP Se cree que derivan de antiguas células procariotas endocitadas por precursoras de
Mitocondrias Mitocondrias Son los organoides encargados de proveer de energía a la célula, mediante la síntesis de ATP Se cree que derivan de antiguas células procariotas endocitadas por precursoras de
Los mecanismos de las reacciones de la glucólisis son, en general, sustituciones nucleofílicas. Veamos algunos ejemplos:
 METABLISM DE AZÚAES III. Mecanismos de reacción Los mecanismos de las reacciones de la glucólisis son, en general, sustituciones nucleofílicas. Veamos algunos ejemplos:. Transferencia de grupo fosforilo
METABLISM DE AZÚAES III. Mecanismos de reacción Los mecanismos de las reacciones de la glucólisis son, en general, sustituciones nucleofílicas. Veamos algunos ejemplos:. Transferencia de grupo fosforilo
EL CONTROL DE LAS ACTIVIDADES CELULARES
 EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
Transaminasa. Piridoxal-fosfato. α-cetoácido O C. Glutamato deshidrogenasa CH 2 C O
 XVII. Degradación de aminoácidos Eliminación del amonio. El catabolismo de los aminoácidos se inicia con frecuencia con la pérdida del (o los) átomo(s) de nitrógeno, seguida de la degradación de las cadenas
XVII. Degradación de aminoácidos Eliminación del amonio. El catabolismo de los aminoácidos se inicia con frecuencia con la pérdida del (o los) átomo(s) de nitrógeno, seguida de la degradación de las cadenas
Planta en desarrollo. Energía
 Respiración Planta en desarrollo Energía Respiración La característica más importante de la respiración es la liberación de energía susceptible de ser utilizada en cualquier ruta metabólica Ruta metabólica
Respiración Planta en desarrollo Energía Respiración La característica más importante de la respiración es la liberación de energía susceptible de ser utilizada en cualquier ruta metabólica Ruta metabólica
CADENA RESPIRATORIA I. Dra. María Uxúa Alonso Fresán
 Universidad Autónoma del Estado de México Facultad de Medicina Veterinaria y Zootecnia Licenciatura en Medicina Veterinaria y Zootecnia Unidad de Aprendizaje de Bioquímica CADENA RESPIRATORIA I Dra. María
Universidad Autónoma del Estado de México Facultad de Medicina Veterinaria y Zootecnia Licenciatura en Medicina Veterinaria y Zootecnia Unidad de Aprendizaje de Bioquímica CADENA RESPIRATORIA I Dra. María
En las células aerobias distintas vías catabólicas convergen en el ciclo de Krebs
 CICLO DE KREBS Material elaborado por: J. Monza, S. Doldán y S. Signorelli. En las células aerobias distintas vías catabólicas convergen en el ciclo de Krebs El ciclo de Krebs (de los ácidos tricarboxílicos
CICLO DE KREBS Material elaborado por: J. Monza, S. Doldán y S. Signorelli. En las células aerobias distintas vías catabólicas convergen en el ciclo de Krebs El ciclo de Krebs (de los ácidos tricarboxílicos
Ejercicios de Repaso. Fermentación y Respiración Celular
 1. Llena los espacios en blanco a. se refiere al conjunto de reacciones metabólicas que tienen que ver con la degradación de moléculas complejas. Estas reacciones energía por lo tanto se definen como.
1. Llena los espacios en blanco a. se refiere al conjunto de reacciones metabólicas que tienen que ver con la degradación de moléculas complejas. Estas reacciones energía por lo tanto se definen como.
Iván Ferrer Rodríguez, Ph.D. Catedrático
 Iván Ferrer Rodríguez, Ph.D. Catedrático Respiración celular y fermentación Capítulo 9, Reece, Urry, Cain, Wasserman, Minorsky, Jackson, 2009 Campbell Biology 9 th Edition Respiración celular Respiración
Iván Ferrer Rodríguez, Ph.D. Catedrático Respiración celular y fermentación Capítulo 9, Reece, Urry, Cain, Wasserman, Minorsky, Jackson, 2009 Campbell Biology 9 th Edition Respiración celular Respiración
RESPIRACIÓN CELULAR (I): CICLO DE KREBS
 Mediante la respiración celular, el acido pirúvico formado durante la glucólisis se oxida completamente a CO 2 y H 2 O en presencia de oxígeno, Este proceso de respiración se desarrolla en dos etapas sucesivas:
Mediante la respiración celular, el acido pirúvico formado durante la glucólisis se oxida completamente a CO 2 y H 2 O en presencia de oxígeno, Este proceso de respiración se desarrolla en dos etapas sucesivas:
 www.paestarporaqui.com PRINCIPALES RUTAS DEL CATABOLISMO Catabolismo de los glúcidos PRINCIPALES RUTAS DEL CATABOLISMO DE LA GLUCOSA Ácido pirúvico Según el destino del piruvato y de la naturaleza del
www.paestarporaqui.com PRINCIPALES RUTAS DEL CATABOLISMO Catabolismo de los glúcidos PRINCIPALES RUTAS DEL CATABOLISMO DE LA GLUCOSA Ácido pirúvico Según el destino del piruvato y de la naturaleza del
Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato.
 Introducción Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato. Origen de los átomos que componen: Las bases púricas Base Nucleósido Nucleótido monofosfato
Introducción Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato. Origen de los átomos que componen: Las bases púricas Base Nucleósido Nucleótido monofosfato
L(Leucina)- K(lisina) F(fenilalanina) Y(Tirosina) I(isoleucina) W(triptófano) T(treonina)
 L(Leucina)- K(lisina) F(fenilalanina) Y(Tirosina) I(isoleucina) W(triptófano) T(treonina) Para que el ciclo de krebs pueda iniciar es necesario que exista Acetil CoA, la formación de acetil
L(Leucina)- K(lisina) F(fenilalanina) Y(Tirosina) I(isoleucina) W(triptófano) T(treonina) Para que el ciclo de krebs pueda iniciar es necesario que exista Acetil CoA, la formación de acetil
METABOLISMO DE AMINOACIDOS. Kinesiología 2011
 METABOLISMO DE AMINOACIDOS Kinesiología 2011 BALANCE NITROGENADO BN=Nitrógeno total ingerido Nitrógeno total excretado BN=0 existe equilibrio nitrogenado BN es negativo, cuando hay condiciones de síntesis
METABOLISMO DE AMINOACIDOS Kinesiología 2011 BALANCE NITROGENADO BN=Nitrógeno total ingerido Nitrógeno total excretado BN=0 existe equilibrio nitrogenado BN es negativo, cuando hay condiciones de síntesis
1- LANZADERAS 2- CADENA RESPIRATORIA Dr. Mynor A. Leiva Enríquez
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, BIOQUÍMICA MÉDICA 2º AÑO - 2012 1- LANZADERAS 2- CADENA RESPIRATORIA Dr. Mynor A. Leiva Enríquez Lanzaderas de sustrato. El
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, BIOQUÍMICA MÉDICA 2º AÑO - 2012 1- LANZADERAS 2- CADENA RESPIRATORIA Dr. Mynor A. Leiva Enríquez Lanzaderas de sustrato. El
GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL
 GLICÓLISIS GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL GLICÓLISIS (GLYCOS = AZÚCAR + LÍSIS = RUPTURA) FASE PREPARATORIA O FASE DE GASTO DE ENERGÍA (ATP) Inversión de ATP aumenta el contenido de
GLICÓLISIS GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL GLICÓLISIS (GLYCOS = AZÚCAR + LÍSIS = RUPTURA) FASE PREPARATORIA O FASE DE GASTO DE ENERGÍA (ATP) Inversión de ATP aumenta el contenido de
TEMA IV. GLUCÓLISIS. 1.Generalidades 2.Reacciones de la glucólisis 3.Control de la glucólisis
 TEMA IV. GLUCÓLISIS 1.Generalidades 2.Reacciones de la glucólisis 3.Control de la glucólisis PRINCIPALES DESTINOS DE LA GLUCOSA SÍNTESIS DE GLUCÓGENO, ALMIDÓN, SACAROSA Reserva GLUCOSA Oxidación vía Pentosas
TEMA IV. GLUCÓLISIS 1.Generalidades 2.Reacciones de la glucólisis 3.Control de la glucólisis PRINCIPALES DESTINOS DE LA GLUCOSA SÍNTESIS DE GLUCÓGENO, ALMIDÓN, SACAROSA Reserva GLUCOSA Oxidación vía Pentosas
Catabolismo de la glucosa: respiración celular
 El Catabolismo 1 Catabolismo Obje/vo: obtención de energía (y almacenamiento en forma de ATP) Fuentes principales de E: glúcidos y lípidos Energía ATP para llevar a cabo ac/vidad celular o para sinte/zar
El Catabolismo 1 Catabolismo Obje/vo: obtención de energía (y almacenamiento en forma de ATP) Fuentes principales de E: glúcidos y lípidos Energía ATP para llevar a cabo ac/vidad celular o para sinte/zar
Respiración. Taiz Lincoln y Eduardo Zeiger Tercera o cuarta Edición
 Respiración es un proceso catabólico en el que se oxida una molécula combustible, la glucosa (sacarosa), cuya energía es atrapada en forma de ATP (fuente universal de energía). http://www.forest.ula.ve/~rubenhg
Respiración es un proceso catabólico en el que se oxida una molécula combustible, la glucosa (sacarosa), cuya energía es atrapada en forma de ATP (fuente universal de energía). http://www.forest.ula.ve/~rubenhg
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 FOSFORILACIÓN OXIDATIVA INTRODUCCIÓN A través de las distintas rutas catabólicas analizadas hasta este punto, se ha ido produciendo una liberación de energía neta, en forma de ATP, y un segundo tipo de
FOSFORILACIÓN OXIDATIVA INTRODUCCIÓN A través de las distintas rutas catabólicas analizadas hasta este punto, se ha ido produciendo una liberación de energía neta, en forma de ATP, y un segundo tipo de
Metabolismo de hidratos de carbono
 Introducción a la Botánica 2016 10ma. clase teórica: 13/4/2016 Metabolismo de hidratos de carbono La fotosíntesis y la respiración 1 La fotosíntesis y la respiración Azúcares + ATP + nutrientes del suelo
Introducción a la Botánica 2016 10ma. clase teórica: 13/4/2016 Metabolismo de hidratos de carbono La fotosíntesis y la respiración 1 La fotosíntesis y la respiración Azúcares + ATP + nutrientes del suelo
Vias alternativas de oxidación de Glucosa: Ruta de las pentosas fosfato
 Vias alternativas de oxidación de Glucosa: Ruta de las pentosas fosfato Ruta alternativa de oxidación de glucosa: Ruta de las Pentosas Fosfato Productos primarios: NADPH: agente reductor en biosíntesis.
Vias alternativas de oxidación de Glucosa: Ruta de las pentosas fosfato Ruta alternativa de oxidación de glucosa: Ruta de las Pentosas Fosfato Productos primarios: NADPH: agente reductor en biosíntesis.
FOSFORILACIÓN OXIDATIVA
 FOSFORILACIÓN OXIDATIVA El NADH y el FADH 2 formados en la glicólisis, en la oxidación de los ácidos grasos y en el ciclo del ácido cítrico, son moléculas ricas en energía porque poseen un par de electrones
FOSFORILACIÓN OXIDATIVA El NADH y el FADH 2 formados en la glicólisis, en la oxidación de los ácidos grasos y en el ciclo del ácido cítrico, son moléculas ricas en energía porque poseen un par de electrones
OXIDACIÓN DEL PIRUVATO Y CICLO DE KREBS (o ciclo del ácido cítrico, o ciclo de los ácidos tricarboxílicos)
 OXIDACIÓN DEL IRUVATO Y CICLO DE KREBS (o ciclo del ácido cítrico, o ciclo de los ácidos tricarboxílicos) Estos procesos oxidan completamente el piruvato hasta CO 2, es decir completan la oxidación total
OXIDACIÓN DEL IRUVATO Y CICLO DE KREBS (o ciclo del ácido cítrico, o ciclo de los ácidos tricarboxílicos) Estos procesos oxidan completamente el piruvato hasta CO 2, es decir completan la oxidación total
Estructura del grupo carbonilo
 TEMA 19.- Compuestos carbonílicos. Clasificación y propiedades generales. Reacciones de adición. Características generales y factores con influencia en la velocidad de la adición. Adiciones de Michael.
TEMA 19.- Compuestos carbonílicos. Clasificación y propiedades generales. Reacciones de adición. Características generales y factores con influencia en la velocidad de la adición. Adiciones de Michael.
LAS ENZIMAS ENZIMAS CLASIFICACIÓN ESTRUCTURA FUNCIÓN. Biocatalizadores. proteica. velocidad reacción. Energía activación. Inorgánica.
 LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
Unidad 7: Respiración Celular
 1 La energía lumínica es capturada por las plantas verdes y otros organismos fotosintéticos, que la transforman en energía química fijada en moléculas como la glucosa. Estas moléculas son luego degradadas
1 La energía lumínica es capturada por las plantas verdes y otros organismos fotosintéticos, que la transforman en energía química fijada en moléculas como la glucosa. Estas moléculas son luego degradadas
OXIDACIÓN DE LA GLUCOSA GLUCÓLISIS DECARBOXILACIÓN OXIDATIVA CICLO DE KREBS CADENA TRANSPORTADORA DE ELECTRONES
 OXIDACIÓN DE LA GLUCOSA GLUCÓLISIS DECARBOXILACIÓN OXIDATIVA CICLO DE KREBS CADENA TRANSPORTADORA DE ELECTRONES Reacciones de oxido-reducción Energía celular El ATP es el principal transportador de energía
OXIDACIÓN DE LA GLUCOSA GLUCÓLISIS DECARBOXILACIÓN OXIDATIVA CICLO DE KREBS CADENA TRANSPORTADORA DE ELECTRONES Reacciones de oxido-reducción Energía celular El ATP es el principal transportador de energía
OXIDACIÓN DEL PIRUVATO Y CICLO DE KREBS. Dra. Carmen Aída Martínez
 OXIDACIÓN DEL PIRUVATO Y CICLO DE KREBS Dra. Carmen Aída Martínez CICLO DE KREBS Ciclo de los Ácidos Tricarboxílicos (ATC) Vía común del metabolismo de todos los combustibles (grasas, Carbohidratos y
OXIDACIÓN DEL PIRUVATO Y CICLO DE KREBS Dra. Carmen Aída Martínez CICLO DE KREBS Ciclo de los Ácidos Tricarboxílicos (ATC) Vía común del metabolismo de todos los combustibles (grasas, Carbohidratos y
1- LANZADERAS 2- CADENA RESPIRATORIA Dr. Mynor A. Leiva Enríquez
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO-2011 1- LANZADERAS 2- CADENA RESPIRATORIA Dr. Mynor A. Leiva Enríquez Lanzaderas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO-2011 1- LANZADERAS 2- CADENA RESPIRATORIA Dr. Mynor A. Leiva Enríquez Lanzaderas
Metabolismo metabolismo rutas metabólicas. dos fases anabolismo ATP NADPH catabolismo ATP NADH NADPH convergente interconectados
 Metabolismo El metabolismo es el conjunto de procesos, intercambios y transformaciones que tienen lugar en el interior de la célula, catalizados por enzimas. Estos procesos se organizan en rutas metabólicas.
Metabolismo El metabolismo es el conjunto de procesos, intercambios y transformaciones que tienen lugar en el interior de la célula, catalizados por enzimas. Estos procesos se organizan en rutas metabólicas.
Revisión- Opción Múltiple Procesamiento de energía
 Revisión- Opción Múltiple Procesamiento de energía 1. El mmetabolismo es considerado como las "reacciones químicas totales que ocurren dentro de un organismo". Estas reacciones químicas pueden estar vinculados
Revisión- Opción Múltiple Procesamiento de energía 1. El mmetabolismo es considerado como las "reacciones químicas totales que ocurren dentro de un organismo". Estas reacciones químicas pueden estar vinculados
TEMA 9 EL METABOLISMO CELULAR. CATABOLISMO 1ª parte
 TEMA 9 EL METABOLISMO CELULAR. CATABOLISMO 1ª parte Características del metabolismo celular. Llamamos metabolismo al conjunto de todas las reacciones químicas que suceden en el interior de las células
TEMA 9 EL METABOLISMO CELULAR. CATABOLISMO 1ª parte Características del metabolismo celular. Llamamos metabolismo al conjunto de todas las reacciones químicas que suceden en el interior de las células
GLUCO-NEO. NEO-GÉNESIS: NESIS: esquema general Ruta anabólica que se produce en hígado y riñón
 T 6-gluconeogénesis GLUCO-NEO NEO-GÉNESIS: NESIS: esquema general Ruta anabólica que se produce en hígado y riñón Glucosa6- fosfatasa La gluconeogénesis convierte dos moléculas de piruvato en una de glucosa
T 6-gluconeogénesis GLUCO-NEO NEO-GÉNESIS: NESIS: esquema general Ruta anabólica que se produce en hígado y riñón Glucosa6- fosfatasa La gluconeogénesis convierte dos moléculas de piruvato en una de glucosa
Cloroplastos y Fotosíntesis
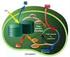 Cloroplastos y Fotosíntesis Víctor Hugo Casco 2012 Labor Improbus Omnia Vincit (El Trabajo Tenaz Todo lo Puede) Funciones Los plástidos son los sitios donde se produce la fotosíntesis, allí se depositan
Cloroplastos y Fotosíntesis Víctor Hugo Casco 2012 Labor Improbus Omnia Vincit (El Trabajo Tenaz Todo lo Puede) Funciones Los plástidos son los sitios donde se produce la fotosíntesis, allí se depositan
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS.
 REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
CADENA RESPIRATORIA MITOCONDRIAL FOSFORILACIÓN OXIDATIVA. Dr. Mynor Leiva
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS ÁREA DE BIOQUÍMICA, 2º. AÑO. CADENA RESPIRATORIA MITOCONDRIAL FOSFORILACIÓN OXIDATIVA Dr. Mynor Leiva Cadena Respiratoria y Fosforilación
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS ÁREA DE BIOQUÍMICA, 2º. AÑO. CADENA RESPIRATORIA MITOCONDRIAL FOSFORILACIÓN OXIDATIVA Dr. Mynor Leiva Cadena Respiratoria y Fosforilación
Colegio San Ignacio de Loyola María Eugenia Ochoa B Ciencias Naturales Noveno 2014
 Colegio San Ignacio de Loyola María Eugenia Ochoa B Ciencias Naturales Noveno 2014 Fotosíntesis QCA- BIOLOGÍA PHOTO SYNTHESIS LUZ FORMAR COMPUESTOS FORMAR MOLECULAS COMPLEJAS A PARTIR DE MOLECULAS SIMPLES
Colegio San Ignacio de Loyola María Eugenia Ochoa B Ciencias Naturales Noveno 2014 Fotosíntesis QCA- BIOLOGÍA PHOTO SYNTHESIS LUZ FORMAR COMPUESTOS FORMAR MOLECULAS COMPLEJAS A PARTIR DE MOLECULAS SIMPLES
Metabolismo de aminoácidos
 Metabolismo de aminoácidos El nitrógeno, presente en la biosfera como nitrato (NO 3- ) o dinitrógeno (N 2 ), debe ser reducido a amonio (NH 4+ ) para su incorporación a proteínas. El hombre adquiere el
Metabolismo de aminoácidos El nitrógeno, presente en la biosfera como nitrato (NO 3- ) o dinitrógeno (N 2 ), debe ser reducido a amonio (NH 4+ ) para su incorporación a proteínas. El hombre adquiere el
La fosforilación oxidativa
 La fosforilación oxidativa arriba ) Bioenergética del transporte de electrones Transportadores de electrones en la mitocondria 4. Hierro. La reacción redox es la siguiente: Fe 2+ Fe 3+ + e - El átomo
La fosforilación oxidativa arriba ) Bioenergética del transporte de electrones Transportadores de electrones en la mitocondria 4. Hierro. La reacción redox es la siguiente: Fe 2+ Fe 3+ + e - El átomo
Composición química de los seres vivos
 Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Conversión del glucoso 6 fosfato en otras hexosas
 BIOSINTESIS DE LOS CARBOHIDRATOS TABLA DE CONTENIDO Introducción Justificación Objetivos Síntesis del glucoso fosfato a partir del ácido pirúvico Regulación de la ruta que va desde el piruvato al glucoso
BIOSINTESIS DE LOS CARBOHIDRATOS TABLA DE CONTENIDO Introducción Justificación Objetivos Síntesis del glucoso fosfato a partir del ácido pirúvico Regulación de la ruta que va desde el piruvato al glucoso
RESPIRACIÓN AEROBIA Y ANAEROBIA
 RESPIRACIÓN AEROBIA Y ANAEROBIA Las células llevan a cabo diversos procesos para mantener su funcionamiento normal, muchos de los cuales requieren energía. La respiración celular es una serie de reacciones
RESPIRACIÓN AEROBIA Y ANAEROBIA Las células llevan a cabo diversos procesos para mantener su funcionamiento normal, muchos de los cuales requieren energía. La respiración celular es una serie de reacciones
Generalidades de ENZIMAS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
HSCoA. CH 3 CO-SCoA COO HO C COO. Citrato. Sintasa. Aconitasa COO COO. Citrato NADH + H + + CO 2 COO І І І І. S-CoA Succinil-CoA
 IL DE KREBS HSoA AD + Malato H 2 ADH + H + Malato deshidrogenasa H H HH Fumarato hidratasa xalacetato H 2 H 3 -SoA itrato Sintasa H itrato H 2 Aconitasa H is-aconitato H 2 Aconitasa Fumarato FADH 2 H H
IL DE KREBS HSoA AD + Malato H 2 ADH + H + Malato deshidrogenasa H H HH Fumarato hidratasa xalacetato H 2 H 3 -SoA itrato Sintasa H itrato H 2 Aconitasa H is-aconitato H 2 Aconitasa Fumarato FADH 2 H H
La fotosíntesis es uno de los procesos metabólicos de los que se valen las células para obtener energía.
 La fotosíntesis es uno de los procesos metabólicos de los que se valen las células para obtener energía. Es un proceso complejo, mediante el cual los seres vivos poseedores de clorofila y otros pigmentos,
La fotosíntesis es uno de los procesos metabólicos de los que se valen las células para obtener energía. Es un proceso complejo, mediante el cual los seres vivos poseedores de clorofila y otros pigmentos,
METABOLISMO DEL NITRÓGENO
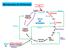 METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
PROTEINAS COMO CATALIZADORES ENZIMAS
 PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
UNIDAD 18: ANABOLISMO
 UNIDAD 18: ANABOLISMO ORGANISMOS SEGÚN EL TIPO DE NUTRICIÓN. Tipos de organismos Fuente de carbono Fuente de energía Ejemplos Fotoautótrofos CO 2 Luz Bacterias fotosintéticas, algas y plantas Quimioautótrofos
UNIDAD 18: ANABOLISMO ORGANISMOS SEGÚN EL TIPO DE NUTRICIÓN. Tipos de organismos Fuente de carbono Fuente de energía Ejemplos Fotoautótrofos CO 2 Luz Bacterias fotosintéticas, algas y plantas Quimioautótrofos
Universidad Católica Agropecuaria del Trópico Seco Pbro. Francisco Luis Espinoza Pineda Fundación Bioquímica Oxidaciones Biológicas
 Universidad Católica Agropecuaria del Trópico Seco Pbro. Francisco Luis Espinoza Pineda Fundación 1968-2012 Bioquímica Oxidaciones Biológicas Ingeniería Agropecuaria Contenido Introducción... 2 Reacciones
Universidad Católica Agropecuaria del Trópico Seco Pbro. Francisco Luis Espinoza Pineda Fundación 1968-2012 Bioquímica Oxidaciones Biológicas Ingeniería Agropecuaria Contenido Introducción... 2 Reacciones
Universidad Católica Agropecuaria del Trópico Seco Pbro. Francisco Luis Espinoza Pineda Fundación 1968-2011
 Universidad Católica Agropecuaria del Trópico Seco Pbro. Francisco Luis Espinoza Pineda Fundación 1968-2011 Carrera: Medicina Veterinaria y Zootecnia Asignatura: Bioquímica Oxidaciones Biológicas Introducción
Universidad Católica Agropecuaria del Trópico Seco Pbro. Francisco Luis Espinoza Pineda Fundación 1968-2011 Carrera: Medicina Veterinaria y Zootecnia Asignatura: Bioquímica Oxidaciones Biológicas Introducción
Potencial de oxido-reducci. Cadena respiratoria: composición n y localización n subcelular. y fosforilación n oxidativa
 Oxidoreducción Tema 2: Oxidoreducción biológica y fosforilación n oxidativa Oxidorreducción n biológica Potencial de oxido-reducci reducción n y de energía a libre. Cadena respiratoria: composición n y
Oxidoreducción Tema 2: Oxidoreducción biológica y fosforilación n oxidativa Oxidorreducción n biológica Potencial de oxido-reducci reducción n y de energía a libre. Cadena respiratoria: composición n y
1.- CONCEPTO DE ENZIMA
 ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
Figura: las reacciones del ciclo de Krebs.
 El ciclo del ácido cítrico oxida acetil-coa, producto común de la degradación de la glucosa, ácidos grasos y aminoácidos cetogénicos, a CO 2 y H 2 0 con la producción de NADH y FADH 2. Muchos aminoácidos
El ciclo del ácido cítrico oxida acetil-coa, producto común de la degradación de la glucosa, ácidos grasos y aminoácidos cetogénicos, a CO 2 y H 2 0 con la producción de NADH y FADH 2. Muchos aminoácidos
TEMA 1: CÉLULA. ACTIVIDAD ORIENTADORA 13. TÍTULO: METABOLISMO Y RESPIRACIÓN CELULAR
 TEMA 1: CÉLULA. ACTIVIDAD ORIENTADORA 13. TÍTULO: COMPONENTES MOLECULARES METABOLISMO Y RESPIRACIÓN CELULAR Autor: Dr. Daniel Sánchez Serrano Parte II TRANSPORTADORES DE LA CADENA DE HIDRÓGENO Coenzima
TEMA 1: CÉLULA. ACTIVIDAD ORIENTADORA 13. TÍTULO: COMPONENTES MOLECULARES METABOLISMO Y RESPIRACIÓN CELULAR Autor: Dr. Daniel Sánchez Serrano Parte II TRANSPORTADORES DE LA CADENA DE HIDRÓGENO Coenzima
Metabolismo de AMINOÁCIDOS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
Glucolisis y gluconeogénesis. Algunos aspectos puntuales Dr. Alfredo Rigalli
 Glucolisis y gluconeogénesis. Algunos aspectos puntuales Dr. Alfredo Rigalli Tabla de contenidos 1.Aspectos generales de glucólisis...1 2.Algunos aspectos particulares de la glucólisis...4 2.1.Glucokinase
Glucolisis y gluconeogénesis. Algunos aspectos puntuales Dr. Alfredo Rigalli Tabla de contenidos 1.Aspectos generales de glucólisis...1 2.Algunos aspectos particulares de la glucólisis...4 2.1.Glucokinase
Profesor(a): C.D. María Isabel Pérez Aguilar
 Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS
 REATIVIDAD DE LS MPUESTS RGÁNIS 1. Reacciones inorgánicas / Reacciones orgánicas 2. Representación general de una reacción orgánica 3. Algunos aspectos a tener en cuenta en las reacciones orgánicas 4.
REATIVIDAD DE LS MPUESTS RGÁNIS 1. Reacciones inorgánicas / Reacciones orgánicas 2. Representación general de una reacción orgánica 3. Algunos aspectos a tener en cuenta en las reacciones orgánicas 4.
Energía y metabolismo
 Energía y metabolismo Sesión 17 Introducción a la Biología Prof. Nelson A. Lagos Los sistemas vivos son abiertos y requieren energía para mantenerse La energía es la capacidad de hacer trabajo. Cinético
Energía y metabolismo Sesión 17 Introducción a la Biología Prof. Nelson A. Lagos Los sistemas vivos son abiertos y requieren energía para mantenerse La energía es la capacidad de hacer trabajo. Cinético
FUNCIONES DE LA RUTA DE LAS PENTOSAS FOSFATO
 FUNCIONES DE LA RUTA DE LAS La ruta de las pentosas fosfato es una vía de oxidación de la G6P, cuyas funciones son: Generar poder reductor en forma de NADPH. Suministrar esqueletos carbonados de 3, 4,
FUNCIONES DE LA RUTA DE LAS La ruta de las pentosas fosfato es una vía de oxidación de la G6P, cuyas funciones son: Generar poder reductor en forma de NADPH. Suministrar esqueletos carbonados de 3, 4,
Ruta de las pentosas fosfato
 Ruta de las pentosas fosfato La ruta predominante del catabolismo de la glucosa es la glucólisis para dar piruvato, seguida por la oxidación a CO 2 en el ciclo del ácido cítrico. Un proceso alternativo,
Ruta de las pentosas fosfato La ruta predominante del catabolismo de la glucosa es la glucólisis para dar piruvato, seguida por la oxidación a CO 2 en el ciclo del ácido cítrico. Un proceso alternativo,
IX. Transporte electrónico
 IX. Transporte electrónico Los electrones generados a partir de la oxidación de los sustratos orgánicos en la rutas de glucólisis y ciclo de Krebs, son canalizados hacia un aceptor final a través de una
IX. Transporte electrónico Los electrones generados a partir de la oxidación de los sustratos orgánicos en la rutas de glucólisis y ciclo de Krebs, son canalizados hacia un aceptor final a través de una
Reacciones de adición
 erramientas de la Química rgánica erramientas de la Química rgánica eacciones de adición en los alquenos : adición polar (I) eacciones de adición + + - δ+ δ- - 1 2 erramientas de la Química rgánica eacciones
erramientas de la Química rgánica erramientas de la Química rgánica eacciones de adición en los alquenos : adición polar (I) eacciones de adición + + - δ+ δ- - 1 2 erramientas de la Química rgánica eacciones
Es el inicio de un proceso que puede continuar con la respiración celular (si existe oxígeno) o con la fermentación (en ausencia del oxígeno).
 Glucólisis Del griego glycos: azúcar y lysis: ruptura. Es el primer paso de la respiración, es una secuencia compleja de reacciones que se realizan en el citosol de la célula y por el cual la molécula
Glucólisis Del griego glycos: azúcar y lysis: ruptura. Es el primer paso de la respiración, es una secuencia compleja de reacciones que se realizan en el citosol de la célula y por el cual la molécula
