REALPURE SPIN DNA/RNA KIT
|
|
|
- Alba Salazar Lozano
- hace 6 años
- Vistas:
Transcripción
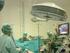
1 REALPURE SPIN DNA/RNA KIT Ref. 50 Preps. 1. INTRODUCCIÓN 1. INTRODUCTION La extracción de ADN y ARN a partir de una única muestra es una necesidad para un numero creciente de aplicaciones. En muchas ocasiones no es fácil obtener réplicas de una misma muestra, como muestras de biopsia, focos únicos en células en cultivo o individuos de pequeños organismos. REALPURE SPIN DNA/RNA Kit provee un método rápido para la extracción y purificación simultánea de ADN genómico y ARN total a partir de una única muestra de células en cultivo y pequeñas muestras de tejidos, sangre, bacterias, levaduras, hongos y plantas. El proceso implica primero la lisis de las células o tejido de interés en un Tampón de guanidine isotiocianato, que rápidamente inactiva las RNasas y DNasas para asegurar una extracción de ADN y ARN intacto. El lisado se pasa a través de una DNA Spin columna, esta columna permite la unión selectiva del ADN genómico. La columna es lavada y el ADN es posteriormente eluido. Se añade etanol al líquido que ha pasado a través de la DNA Spin columna para crear las condiciones favorables para que el ARN se una, y la muestra es pasada por la RNA Spin columna, donde el ARN total se une a la membrana y los contaminantes son eliminados mediante lavados y luego el ARN total es eluido con agua libre de nucleasas. El kit permite purificar todas las especies de ARN, desde el ARN ribosomal y ARNm hasta el microarn (miarn) y el ARN de interferencia (ARNi). El ARN purificado puede ser utilizado en diversas aplicaciones incluidas real time PCR, RT-PCR, Northern blotting, ensayos de protección de la RNasa, primer extension y ensayos en arrays de expresión. El ADN genómico es de alta calidad y puede ser utilizado en reacciones de PCR, secuenciación, Southern blotting y análisis de SNP. Selective isolation of DNA and RNA from unique, precious samples is a demand for an increasing number of applications. Splitting is unfavourable if not impossible for a number of samples like biopsy samples, single foci from cell cultures or single individuals of small organisms. REALPURE SPIN DNA/RNA Kit provides a rapid method for the isolation and purification genomic DNA and total RNA simultaneously from a single sample of cultured animal cells, small tissues samples, blood, bacteria, yeast, fungi or plants. The process involves first the cells or tissue lysis in a highly denaturing guanidine-isothiocyanatecontaining buffer, that will rapidly inactive RNases and DNases to ensure isolation of intact DNA and RNA. The lysate is then passed through a DNA spin column; this column allows selective binding of genomic DNA. The column is washed and pure, ready-to-use DNA is the eluted. Ethanol is added to the flow-through from the DNA spin column to provide appropriate binding conditions for RNA, and the sample is the applied to a RNA spin column, where total RNA binds to the membrane and contaminants are efficiently washed away, high-quality RNA is then eluted. The kit purifies all sizes of RNA, from large mrna and ribosomal RNA down to microrna (mirna) and small interfering RNA (RNAi). The purified RNA can be used in a number of downstream applications including real time PCR, RT-PCR, Northern blotting, RNase protection and primer extension and expression array assays. The genomic DNA is of the highest quality and can be used in PCR reactions, sequencing, Southern blotting and SNP analysis. 1/19
2 2. COMPONENTES DEL KIT KIT COMPONENTS Solución de Lisis ARN RNA Lysis Buffer Tampón de Lavado ARN RNA Washing Buffer Tampón de Elución ARN RNA Elution Buffer Tampón de Desinhibición Desinhibition Buffer Tampón de Lavado ADN DNA Washing Buffer Tampón de Elución ADN DNA Elution Buffer REAL DNA Spin Columnas REAL DNA Spin Columns REAL RNA Spin Columnas REAL RNA Spin Columns Tubos de Recogida Collection Tubes Equipos y reactivos necesarios no incluidos en el kit: * Etanol 100%. * Etanol 70% * Microtubos de 1.5 o 2 ml libres de RNasas * Microcentrifuga * Homogeneizadores generales para tejidos animales y de plantas * Nitrógeno líquido, mortero y maza * -mercaptoetanol. Ref. Ref. 50 preps Equipment and additional reagents required Tª ERS01 25 ml RT ERS02 22 ml RT ERS03 6 ml RT REA03 18 ml RT REA04 10 ml RT REA05 6 ml RT RSC01 50 unid. RT RSCR01 50 unid. RT R unid. RT * 100 % Ethanol * 70% Ethanol * Rnase-free 1.5 or 2 ml microtubes * Microcentrifuge * Mechanical homogenizator for animal and plants tissues * Liquid Nitrogen, mortar and pestle. -mercaptoethanol. 3. PROTOCOLO GENERAL GENERAL PROCEDURE 3.1 Consideraciones preliminares 3.1 Preliminary conditions OPCIONAL: El uso de -mercaptoetanol en la lisis es altamente recomendado para tejidos animales, particularmente en aquellos que se sabe que tienen un alto contenido en RNAsas (ejem. páncreas), al igual que en tejidos de plantas. También se recomienda para aquellos usuarios que quieren aislar RNA para aplicaciones muy sensibles o enriquecimiento de microrna. Preparar una cantidad apropiada de Tampón de Lisis RNA añadiendo 10 l de - mercaptoetanol por 1 ml de Tampón de Lisis RNA. Alternativamente, la Solución de Lisis RNA puede ser utilizada tal y como es suministrada. OPTIONAL: The use of -mercaptoethanol in lysis is highly recommended for most animal tissues, particularly those know to have a high RNAse content (ex. pancreas), as well as for most plant tissues. It is also recommended for uses who whish to isolate RNA for sensitive downstream applications or microrna enrichment. Add 10 l of -mercaptoethanol (provided by the user) to each 1 ml of Lysis Buffer required. Alternatively, the Lysis Buffer can be used as provided. 2/19
3 NO utilizar más muestra que la indicada en la DNA Spin columna, ya que esto llevará a co-purificar ADN con ARN. Tampoco sobrecargar la RNA Spin columna ya que esto reducirá el rendimiento y pureza del ARN total obtenido. Algunos tejidos o muestras pueden contener cantidades altas de ADN lo que sobrecargará la DNA Spin columna, para estas muestras, se recomienda realizar una digestión de DNasa si el eluido de ARN total va a ser utilizado posteriormente en aplicaciones sensibles a la presencia de pequeñas cantidades de ADN. ATENCION: El Tampón de Lisis RNA contiene Guanidine isothiocianato y el tampón de desinhibición contienen Guanidine hydrochloride, ambos son agentes irritantes, por lo que es conveniente la utilización de guantes y gafas para su manejo Do not overload the DNA Spin column, as this will lead to co purification of DNA with RNA. Do not overload the RNA Spin column, as this will significantly reduce RNA yield and purity. Some tissues or samples can contain very high amounts of DNA will overload the DNA Spin column, for these samples, we recommended performing DNase digestion if the eluted RNA will be used in downstream applications sensitive to very small amounts of DNA. ATTENTION: The Lysis Solution contains Guanidine thiocyanate and the Desinhibition Buffer contains Guanidine hydrochloride which is an irritant agent, for this reason we recommend to use gloves and glasses for its manipulation. 3.2 Preparaciones preliminares 3.2 Preliminary Preparations Añadir 50 ml de Etanol 100 % al Tampón de Lavado RNA, con lo que el volumen final será de 72 ml.mantener el envase bien cerrado para evitar la evaporación del etanol. Añadir 10 ml de Etanol 100 % al Tampón de Desinhibición. Mantener el envase bien cerrado para evitar la evaporación del etanol. Añadir 40 ml de Etanol 100 % al Tampón de Lavado DNA. Mantener el envase bien cerrado para evitar la evaporación del etanol. Precalentar el Tampón de Elución DNA a 70ºC. El resto de soluciones deben estar a temperatura ambiente. Add 50 ml of 100% Ethanol to the RNA Wash Buffer. This will give a final volume of 72 ml. Keep the container closed to avoid ethanol evaporation. Add 10 ml of 100 % Ethanol to the Desinhibition Buffer. Keep the container closed to avoid the ethanol evaporation Add 40 ml of 100% Ethanol to the DNA Wash Buffer. Keep the container closed to avoid the ethanol evaporation. Pre-heat the Elution Buffer DNA at 70ºC. Ensure that all the rest of solutions are at room temperature prior use. 3.3 Protocolo de extracción de ADN/ARN a partir de células en cultivo monocapa Protocol of DNA/RNA isolation from cultured animal cells growing in a monolayer Nota: La máxima cantidad recomendada de células es 1 x Los pellets de células pueden ser conservados a -70ºC para un uso posterior (determinar el número de células antes de congelar). Los pellets congelados no deberán ser conservados más de 2 semanas para asegurar que la integridad del ARN no se verá comprometida. El Tampón de lisis RNA se añadirá directamente sobre los pellets congelados sin dejar que alcancen la temperatura ambiente. Note: The maximum recommended input of cells is 1 x 10 6.Cell pellets can be stored at -70ºC for later use or used directly in the procedure. Determine the number of cell present before freezing. Frozen pellets should be stored no longer than 2 weeks to ensure that the integrity of the RNA is not compromised. Frozen pellets should not be thawed to beginning the protocol. Add the Lysis buffer directly to the frozen cell pellet. 3/19
4 Protocolo para la extracción de ARN total de células creciendo en monocapa 1. Aspirar el medio y lavar las células con una cantidad apropiada de PBS. Aspirar el PBS. 2. Añadir 400l de Tampón de Lisis RNA directamente a la placa de cultivo. 3. Lisar las células, tapar la placa y agitar el tampón alrededor de la superficie de la placa durante 5 minutos. 4. Pasar el lisado a un microtubo. IMPORTANTE: Anotar la cantidad de lisado. 5. Añadir 15 l de etanol 100 % por cada 100 l de lisado. Mezclar mediante 10 segundos. 6. Ensamblar una DNA Spin columna con un tubo de recogida que se suministra. 7. Añadir el lisado + etanol a la columna. Centrifugar durante 1 minuto. 8. Retener el líquido que ha pasado a través de la columna y que se encuentra en el tubo de recogida y que contiene el ARN total. Pasar el líquido retenido a un microtubo nuevo de 1.5 ml (no suministrado con el kit). 9. Ensamblar la DNA Spin columna con un tubo de recogida y conservar a temperatura ambiente (15-25ºC) o a 4ºC para purificación del ADN más tarde. 10. Añadir 450 l de Etanol % al líquido retenido que contiene el ARN total. Mezcla por vortex 10 segundos. Después de la adición del etanol se podrá apreciar un precipitado, asegurarse de que todo el precipitado se añade a la RNA Spin columna. 11. Ensamblar una RNA Spin columna con un tubo de recogida que se suministra. 12. Aplicar la mitad del liquido + etanol en la RNA Spin columna y centrifugar durante 1 minuto. Descartar el líquido y reensamblar la columna con su tubo de recogida. 13. Repetir el punto 12 hasta completar la captura de todo el ARN total. 14. Añadir 400 l de Tampón de Lavado RNA a la Asegurarse que todo el tampón de lavado ha pasado a través de la columna, sino fuera así centrifugar otro minuto adicional. 15. Eliminar el líquido y ensamblar la columna con el tubo de recogida. Añadir 400 l de Tampón de Lavado RNA a la columna y centrifugar durante 1 minuto. 16. Realizar un tercer lavado. Añadir 400 l de Tampón de Lavado RNA a la columna y centrifugar durante 1 minuto. Eliminar el líquido del tubo de recogida y centrifugar durante 2 minutos adicionales para eliminar todo el etanol residual. Eliminar el tubo de recogida. 17. Colocar la columna en un microtubo nuevo de 1.5 ml (no suministrado con el kit) para eluir el ARN total. 18. Añadir l de Tampón de Elución RNA a la columna. 19. Centrifugar durante 2 minutos a 200xg (aprox rpm), seguido de 1 minuto a xg (aprox rpm). Ver la cantidad de eluido de la columna, sino se han eluido los 50 l centrifugar por 1 minuto adicional a x g (aprox rpm). 20. El ARN purificado puede ser conservado a - 20ºC durante algunos días. Se recomienda que las muestras se conserven a -70ºC para almacenamientos largos Protocolo para la extracción de ADN genómico de células creciendo en monocapa 1. Añadir 500 l de Tampón de Desinhibición a la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 2. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 3. 2º Lavado. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido 4. Centrifugar a máxima velocidad durante 2 minutos para eliminar todo el etanol residual. 5. Eliminar el tubo de recolección y insertar la DNA Spin columna en un microtubo de 1.5 ml. Añadir l Tampón de Elución DNA (precalentado a 70ºC) en el reservorio de la DNA Spin columna. Incubar durante 1 minuto. 6. Centrifugar a máxima velocidad durante 1 minuto. El microtubo contiene ahora el ADN genómico. 4/19
5 Protocol for total RNA extraction from cultured animal cells growing in a monolayer 1. Aspirate media and wash cell monolayer with an appropriate amount of PBS. Aspirate PBS 2. Add 400 l of Lysis Buffer directly to culture plate. 3. Lyse cells by gently tapping culture dish and swirling buffer around plate surface for five minutes. 4. Transfer lysate to a microcentrifuge tube. IMPORTANT: Note the volume of the lysate. 5. Add 15 l of 100 % ethanol every 100 l of lysate. Mix by vortexing for 10 seconds. 6. Assemble a DNA Spin column with one 7. Apply the clarified lysate with ethanol onto the columns. Centrifuge for 1 minute. 8. Retains the flowthrough, which contains the total RNA. Use the flowthrough for RNA purification. Transfer the flowthrough to a new RNase-free microcentrifuge tube (not provided). 9. Place the DNA Spin column in a new collection tube and store at room temperature (15-25ºC) or a 4ºC for later DNA purification. 10. Add 450 l of % Ethanol to the flowthrough. Mix by vortexing for 10 seconds. After addition of ethanol a stringy precipitate may become visible, be sure to load all of the precipitate on the RNA Spin column. 11. Assemble a RNA Spin column with one 12. Apply half of the flowthrough with ethanol onto the columns and centrifuge for 1 minute. Discard the flowthrough and reassemble the spin column with the collection tube. 13. Repeat step 12 to complete the capture of the total RNA. 14. Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Ensure the entire wash buffer has passed through into the collection tube by inspecting the column. If the entire wash volume has not passed, spin for an additional minute. 15. Discard the flowthrough and reassemble the spin column with its collection tube. Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute 16. Wash column a third time by adding another 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Discard the flowthrough and centrifuge for 2 minutes to eliminate the residual ethanol. En sure that the column is dry and discard the collection tube with the flowthrough. 17. Place the column into a fresh 1.5 ml microfuge tube (not provided in the kit) 18. Add 50 l-100 of Elution Buffer RNA to the column. 19. Centrifuge for 2 minutes at 200x g (aprox rpm), followed by 1 minute at xg (aprox rpm). Note the volume eluted from the column. If the entire 50 l has not been eluted, spin the column at x g (aprox rpm) for 1 additional minute. 20. The purified microrna sample may be stored at -20ºC for a few days. It is recommended that samples be placed at - 70ºC for long term storage Protocol for Genomic DNA isolation from cultured animal cells growing in a monolayer 1. Add 500 l of Desinhibition Buffer to the DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 2. Add 500 l of Wash Buffer DNA into reservoir of DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 3. 2º Wash. Add 500 l of Wash Buffer DNA into reservoir of DNA Spin column Centrifuge for 1 minute. Remove the liquid. 4. Centrifuge at maximum speed for 120 seconds to remove the residual ethanol. 5. Remove the collection tube and insert the DNA Spin Column in a 1.5 ml microtube. Add 100l of elution buffer (preheated at 70ºC) into reservoir of DNA Spin column. Incubate 1 minute. 6. Centrifuge at maximum speed for 60 seconds. The microtube contains now the genomic DNA. 5/19
6 3.4. Protocolo de extracción de ADN/ARN a partir de células creciendo en suspensión Protocol of DNA/RNA isolation from cells growing in suspension Protocolo de extracción de ARN total de células creciendo en suspensión 1. Transferir la suspensión celular a un tubo libre de RNAsas (no suministrado) y centrifugar a no más de 200x g (aprox rpm) durante 10 minutos para obtener el pellet de las células. 2. Cuidadosamente eliminar el sobrenadante. 3. Añadir 400 l de Tampón de Lisis RNA al pellet. Lisar las células por vortex durante 15 segundos. Asegurarse que todo el pellet está disuelto antes de proceder con el siguiente paso. 4. Pasar el lisado a un microtubo. IMPORTANTE: Anotar la cantidad de lisado. 5. Añadir 15 l de etanol 100 % por cada 100 l de lisado. Mezcla por vortex 10 segundos. 6. Ensamblar una DNA Spin columna con 7. Añadir el lisado + etanol a la columna. Centrifugar durante 1 minuto. 8. Retener el líquido que ha pasado a través de la columna y que se encuentra en el tubo de recogida y que contiene el ARN total. Pasar el líquido retenido a un microtubo nuevo de 1.5 ml ( no suministrado con el kit). 9. Ensamblar la DNA Spin columna con un tubo de recogida y conservar a temperatura ambiente (15-25ºC) o a 4ºC para purificación del ADN más tarde. 10. Añadir 450 l de Etanol % al líquido retenido que contiene el ARN total. Mezcla por vortex 10 segundos. Después de la adición del etanol se podrá apreciar un precipitado, asegurarse de que todo el precipitado se añade a la RNA Spin columna. 11. Ensamblar una RNA Spin columna con 12. Aplicar la mitad del liquido + etanol en la RNA Spin columna y centrifugar durante 1 minuto. Descartar el líquido y reensamblar la columna con su tubo de recogida. 13. Repetir el punto 12 hasta completar la captura de todo el ARN total. 14. Añadir 400 l de Tampón de Lavado RNA a la columna y centrifugar durante 1 minuto. Asegurarse que todo el tampón de lavado ha pasado a través de la columna, sino fuera así centrifugar otro minuto adicional. 15. Eliminar el líquido y ensamblar la columna con el tubo de recogida. Añadir 400 l de Tampón de Lavado RNA a la 16. Realizar un tercer lavado. Añadir 400 l de Tampón de Lavado RNA a la Eliminar el líquido del tubo de recogida y centrifugar durante 2 minutos adicionales para eliminar todo el etanol residual. Eliminar el tubo de recogida. 17. Colocar la columna en un microtubo nuevo de 1.5 ml ( no suministrado con el kit) para eluir el ARN total. 18. Añadir l de Tampón de Elución RNA a la columna. 19. Centrifugar durante 2 minutos a 200xg (aprox rpm), seguido de 1 minuto a xg (aprox rpm). Ver la cantidad de eluido de la columna, sino se han eluido los 50 l centrifugar por 1 minuto adicional a x g (aprox rpm). 20. El ARN purificado puede ser conservado a -20ºC durante algunos días. Se recomienda que las muestras se conserven a -70ºC para almacenamientos largos Protocolo de extracción de ADN genómico de células creciendo en suspensión 1. Añadir 500 l de Tampón de Desinhibición a la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 2. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 3. 2º Lavado. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido 4. Centrifugar a máxima velocidad durante 2 minutos para eliminar todo el etanol residual. 5. Eliminar el tubo de recolección y insertar la DNA Spin columna en un microtubo de 1.5 ml. Añadir l Tampón de Elución DNA (precalentado a 70ºC) en el reservorio de la DNA Spin columna. Incubar durante 1 minuto. 6. Centrifugar a máxima velocidad durante 1 minuto. El microtubo contiene ahora el ADN genómico. 6/19
7 Protocol for total RNA isolation from cells growing in suspension 1. Transfer cell suspension to an RNase-free tube (not provided) and centrifuge at no more than 200x g (aprox rpm) for 10 minutes to pellet cells. 2. Carefully decant the supernatant. 3. Add 400 l of Lysis Buffer RNA to the pellet. Lyse cells by vortexing for 15 seconds. Ensure that the entire pellet is completely dissolved before proceeding to the next step. IMPORTANT: Note the volume of the lysate. 4. Transfer lysate to a microcentrifuge tube. IMPORTANT: Note the volume of the lysate. 5. Add 15 l of 100 % ethanol to every 100l of lysate. Mix by vortexing for 10 seconds. 6. Assemble a DNA Spin column with one 7. Apply the clarified lysate with ethanol onto the columns. Centrifuge for 1 minute. 8. Retains the flowthrough, which contains the total RNA. Use the flowthrough for RNA purification. Transfer the flowthrough to a new RNase-free microcentrifuge tube (not provided). 9. Place the DNA Spin column in a new collection tube and store at room temperature (15-25ºC) or a 4ºC for later DNA purification. 10. Add 450 l of % Ethanol to the flowthrough. Mix by vortexing for 10 seconds. After addition of ethanol a stringy precipitate may become visible, be sure to load all of the precipitate on the RNA Spin column. 11. Assemble a RNA Spin column with one 12. Apply half of the flowthrough with ethanol onto the columns and centrifuge for 1 minute. Discard the flowthrough and reassemble the spin column with the collection tube. 13. Repeat step 12 to complete the capture of the total RNA. 14. Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Ensure the entire wash buffer has passed through into the collection tube by inspecting the column. If the entire wash volume has not passed, spin for an additional minute. 15. Discard the flowthrough and reassemble the spin column with its collection tube. Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute 16. Wash column a third time by adding another 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Discard the flowthrough and centrifuge for 2 minutes to eliminate the residual ethanol. En sure that the column is dry and discard the collection tube with the flowthrough. 17. Place the column into a fresh 1.5 ml microfuge tube (not provided in the kit) 18. Add 50 l-100 of Elution Buffer RNA to the column. 19. Centrifuge for 2 minutes at 200xg (aprox rpm), followed by 1 minute at xg (aprox rpm). Note the volume eluted from the column. If the entire 50 l has not been eluted, spin the column at xg (aprox rpm) for 1 additional minute. 20. The purified microrna sample may be stored at -20ºC for a few days. It is recommended that samples be placed at - 70ºC for long term storage Protocol for Genomic DNA isolation from cells growing in suspension 1. Add 500 l of Desinhibition Buffer to the DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 2. Add 500 l of Wash Buffer DNA into reservoir of DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 3. 2º Wash. Add 500 l of Wash Buffer DNA into reservoir of DNA Spin column Centrifuge for 1 minute. Remove the liquid. 4. Centrifuge at maximum speed for 120 seconds to remove the residual ethanol. 5. Remove the collection tube and insert the DNA Spin Column in a 1.5 ml microtube. Add 100l of elution buffer (preheated at 70ºC) into reservoir of DNA Spin column. Incubate 1 minute. 6. Centrifuge at maximum speed for 60 seconds. The microtube contains now the genomic DNA. 7/19
8 3.5. Protocolo de extracción de ADN/ARN a partir de tejidos animales Protocol of DNA/RNA isolation from animal tissues Nota: El ARN en tejidos animales no se encuentra protegido hasta que después de su recolección es roto y homogenizado en la Solución de Lisis. Para este procedimiento se pueden utilizar tanto tejidos frescos como congelados. Los tejidos deberían congelarse en nitrógeno líquido y transferidos inmediatamente a -70ºC para almacenamientos largos. Cuando aislamos ARN total de tejidos congelados asegurase que no asciende mucho su temperatura durante el pesaje y la pulverización con una mano de mortero. Note: RNA in animal tissues is not protected after harvesting until it is disrupted and homogenized into Lysis solution. Fresh or frozen tissues may be used for the procedure. Tissues should be flashfrozen in liquid nitrogen and transfer immediately to a -70ºC freezer for long term storage. When isolating total RNA from frozen tissues, you need to ensure that the tissue does not thaw during weighing or prior to grinding with the mortar and pestle Protocolo de extracción de ARN total a partir de tejidos animales 1. Determinar la cantidad de tejido a pesar, se recomienda no utilizar más de 10 mg de tejido. 2. Colocar el tejido en un mortero que contenga una cantidad apropiada de nitrógeno líquido para cubrir la muestra. Pulverizar el tejido utilizando una mano de mortero. Permitir que el nitrógeno líquido se evapore, sin que se descongele la muestra. 3. Pasar la muestra a un microtubo libre de RNAsas (no suministrado) y añadir 400 l de Tampón de Lisis RNA. Homogenizar pasando el lisado 5 o 10 veces a través de una jeringa con una aguja de 25 o con un homogenizador eléctrico de mano. 4. Centrifugar durante 2 minutos para obtener el pellet de algún desecho celular que pueda quedar. Pasar el sobrenadante a un microtubo libre RNAsas nuevo (no suministrado).importante: Anotar la cantidad de sobrenadante/lisado. 5. Añadir 15 l de etanol 100 % por cada 100 l de lisado. Mezclar por vortex 10 segundos. 6. Ensamblar una DNA Spin columna con 7. Añadir el lisado + etanol a la columna. Centrifugar durante 1 minuto. 8. Retener el líquido que ha pasado a través de la columna y que se encuentra en el tubo de recogida y que contiene el ARN total. Pasar el líquido retenido a un microtubo nuevo de 1.5 ml ( no suministrado con el kit). 9. Ensamblar la DNA Spin columna con un tubo de recogida y conservar a temperatura ambiente (15-25ºC) o a 4ºC para purificación del ADN más tarde. 10. Añadir 450 l de Etanol % al líquido retenido que contiene el ARN total. Mezcla por vortex 10 segundos. Después de la adición del etanol se podrá apreciar un precipitado, asegurarse de que todo el precipitado se añade a la RNA Spin columna. 11. Ensamblar una RNA Spin columna con 12. Aplicar la mitad del liquido + etanol en la RNA Spin columna y centrifugar durante 1 minuto. Descartar el líquido y reensamblar la columna con su tubo de recogida. 13. Repetir el punto 12 hasta completar la captura de todo el ARN total. 14. Añadir 400 l de Tampón de Lavado RNA a la columna y centrifugar durante 1 minuto. Asegurarse que todo el tampón de lavado ha pasado a través de la columna, sino fuera así centrifugar otro minuto adicional. 15. Eliminar el líquido y ensamblar la columna con el tubo de recogida. Añadir 400 l de Tampón de Lavado RNA a la 16. Realizar un tercer lavado. Añadir 400 l de Tampón de Lavado RNA a la Eliminar el líquido del tubo de recogida y centrifugar durante 2 minutos adicionales para eliminar todo el etanol residual. Eliminar el tubo de recogida. 17. Colocar la columna en un microtubo nuevo de 1.5 ml ( no suministrado con el kit) para eluir el ARN total. 18. Añadir l de Tampón de Elución RNA a la columna. 19. Centrifugar durante 2 minutos a 200x g (aprox rpm), seguido de 1 minuto a xg (aprox rpm). Ver la cantidad de eluido de la columna, sino se han eluido los 50 l centrifugar por 1 minuto adicional a x g (aprox rpm). 20. El ARN purificado puede ser conservado a -20ºC durante algunos días. Se recomienda que las muestras se conserven a -70ºC para almacenamientos largos. 8/19
9 Protocolo de extracción de ADN genómico a partir de tejidos animales 1. Añadir 500 l de Tampón de Desinhibición a la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 2. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 3. 2º Lavado. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido 4. Centrifugar a máxima velocidad durante 2 minutos para eliminar todo el etanol residual. 5. Eliminar el tubo de recolección y insertar la DNA Spin columna en un microtubo de 1.5 ml. Añadir l Tampón de Elución DNA (precalentado a 70ºC) en el reservorio de la DNA Spin columna. Incubar durante 1 minuto. 6. Centrifugar a máxima velocidad durante 1 minuto. El microtubo contiene ahora el ADN genómico Protocol for Total RNA isolation from animal tissues 1. Determine the amount of tissue by weighing. It is recommended that no more than 10 mg of tissue be used for the protocol. 2. Transfer the tissue into a mortar that contains an appropriate amount of liquid nitrogen to cover the sample. Grind the tissue thoroughly using a pestle. Allow the liquid nitrogen to evaporate, without allowing the tissue to thaw. 3. Transfer the sample to an RNase-free tube (not provided)) and add 400 l de Lysis Buffer. Homogenize by passing the lysate 5-10 times through a 25 gauge needle attached to a syringe or an electrical homogenizator. 4. Spin the lysate for 2 minutes to pellet any cell debris. Transfer de supernatant to another RNase-free microcentrifuge tube. IMPORTANT: Note the volume of the supernatant/lysate. 5. Add 15 l of 100 % ethanol to every 100l of lysate.. Mix by vortexing for 10 seconds. 6. Assemble a DNA Spin column with one 7. Apply the clarified lysate with ethanol onto the columns. Centrifuge for 1 minute. 8. Retains the flowthrough, which contains the total RNA. Use the flowthrough for RNA purification. Transfer the flowthrough to a new RNase-free microcentrifuge tube (not provided). 9. Place the DNA Spin column in a new collection tube and store at room temperature (15-25ºC) or a 4ºC for later DNA purification. 10. Add 450 l of % Ethanol to the flowthrough. Mix by vortexing for 10 seconds. After addition of ethanol a stringy precipitate may become visible, be sure to load all of the precipitate on the RNA Spin column. 11. Assemble a RNA Spin column with one 12. Apply half of the flowthrough with ethanol onto the columns and centrifuge for 1 minute. Discard the flowthrough and reassemble the spin column with the collection tube. 13. Repeat step 12 to complete the capture of the total RNA. 14. Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Ensure the entire wash buffer has passed through into the collection tube by inspecting the column. If the entire wash volume has not passed, spin for an additional minute. 15. Discard the flowthrough and reassemble the spin column with its collection tube. Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute 16. Wash column a third time by adding another 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Discard the flowthrough and centrifuge for 2 minutes to eliminate the residual ethanol. En sure that the column is dry and discard the collection tube with the flowthrough. 17. Place the column into a fresh 1.5 ml microfuge tube (not provided in the kit) 18. Add 50 l -100 of Elution Buffer RNA to the column. 9/19
10 19. Centrifuge for 2 minutes at 200xg (aprox rpm), followed by 1 minute at x g (aprox rpm). Note the volume eluted from the column. If the entire 50 l has not been eluted, spin the column at xg (aprox rpm) for 1 additional minute. 20. The purified microrna sample may be stored at -20ºC for a few days. It is recommended that samples be placed at - 70ºC for long term storage Protocol for Genomic DNA isolation from animal tissues 1. Add 500 l of Desinhibition Buffer to the DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 2. Add 500 l of Wash Buffer DNA in to reservoir of DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 3. 2º Wash. Add 500 l of Wash Buffer DNA into reservoir of DNA Spin column Centrifuge for 1 minute. Remove the liquid. 4. Centrifuge at maximum speed for 120 seconds to remove the residual ethanol. 5. Remove the collection tube and insert the DNA Spin Column in a 1.5 ml microtube. Add 100l of elution buffer (preheated at 70ºC) into reservoir of DNA Spin column. Incubate 1 minute. 6. Centrifuge at maximum speed for 60 seconds. The microtube contains now the genomic DNA Protocolo de extracción de ADN/ARN a partir de sangre. Protocol of DNA/RNA isolation from blood Nota: Se recomienda no utilizar más de 100 l de sangre total con el fin de prevenir el colapsado de la membrana. Recomendamos el uso de este kit para la extracción de ARN a partir de sangre fresca no coagulada, utilizando EDTA como anticoagulante Note: It is recommended that no more than 100 l of blood be used in order to prevent clogging of the column. We recommend the use of this kit to isolate RNA from non coagulating fresh blood using EDTA as the anti-coagulant Protocolo de extracción de ARN total a partir de sangre 1. Transferir 100 l de sangre no coagulada a un microtubo libre RNAsas (no suministrado). 2. Añadir 300 l de Tampón de Lisis RNA a la sangre. Lisar las células por vortex durante 15 segundos. Asegurarse que la mezcla está transparente antes de proceder con el siguiente paso. IMPORTANTE: Anotar la cantidad de lisado. 3. Añadir 15 l de etanol 100 % por cada 100 l de lisado. Mezcla por vortex 10 segundos. 4. Ensamblar una DNA Spin columna con 5. Añadir el lisado + etanol a la columna. Centrifugar durante 1 minuto. 6. Retener el líquido que ha pasado a través de la columna y que se encuentra en el tubo de recogida y que contiene el ARN total. Pasar el líquido retenido a un microtubo nuevo de 1.5 ml ( no suministrado con el kit). 7. Ensamblar la DNA Spin columna con un tubo de recogida y conservar a temperatura ambiente (15-25ºC) o a 4ºC para purificación del ADN más tarde. 8. Añadir 450 l de Etanol % al líquido retenido que contiene el ARN 10/19 total. Mezcla por vortex 10 segundos. Después de la adición del etanol se podrá apreciar un precipitado, asegurarse de que todo el precipitado se añade a la RNA Spin columna. 9. Ensamblar una RNA Spin columna con 10. Aplicar la mitad del liquido + etanol en la RNA Spin columna y centrifugar durante 1 minuto. Descartar el líquido y reensamblar la columna con su tubo de recogida. 11. Repetir el punto 12 hasta completar la captura de todo el ARN total. 12. Añadir 400 l de Tampón de Lavado RNA a la columna y centrifugar durante 1 minuto. Asegurarse que todo el tampón de lavado ha pasado a través de la columna, sino fuera así centrifugar otro minuto adicional. 13. Eliminar el líquido y ensamblar la columna con el tubo de recogida. Añadir 400 l de Tampón de Lavado RNA a la 14. Realizar un tercer lavado. Añadir 400 l de Tampón de Lavado RNA a la
11 Eliminar el líquido del tubo de recogida y centrifugar durante 2 minutos adicionales para eliminar todo el etanol residual. Eliminar el tubo de recogida. 15. Colocar la columna en un microtubo nuevo de 1.5 ml ( no suministrado con el kit) para eluir el ARN total. 16. Añadir l de Tampón de Elución RNA a la columna. 17. Centrifugar durante 2 minutos a 200xg (aprox rpm), seguido de 1 minuto a xg (aprox rpm). Ver la cantidad de eluido de la columna, sino se han eluido los 50 l centrifugar por 1 minuto adicional a x g (aprox rpm). 18. El ARN purificado puede ser conservado a -20ºC durante algunos días. Se recomienda que las muestras se conserven a -70ºC para almacenamientos largos Protocolo de extracción de ADN genómico de sangre 1. Añadir 500 l de Tampón de Desinhibición a la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 2. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 3. 2º Lavado. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido 4. Centrifugar a máxima velocidad durante 2 minutos para eliminar todo el etanol residual. 5. Eliminar el tubo de recolección y insertar la DNA Spin columna en un microtubo de 1.5 ml. Añadir l Tampón de Elución DNA (precalentado a 70ºC) en el reservorio de la DNA Spin columna. Incubar durante 1 minuto. 6. Centrifugar a máxima velocidad durante 1 minuto. El microtubo contiene ahora el ADN genómico Protocol for Total RNA isolation from blood 1. Transfer up to 100 f non coagulating blood to an RNase free microcentrifuge tube (not provided). 2. Add 300 l of Lysis Buffer to the blood. Lyse cells by vortexing for 15 seconds. Ensure that the mix become transparent before proceeding to the next step. IMPORTANT: Note the volume of the supernatant/lysate. 3. Add 15 l of 100 % ethanol every 100 l of lysate. Mix by vortexing for 10 seconds. 4. Assemble a DNA Spin column with one 5. Apply the clarified lysate with ethanol onto the columns. Centrifuge for 1 minute. 6. Retains the flowthrough, which contains the total RNA. Use the flowthrough for RNA purification. Transfer the flowthrough to a new RNase-free microcentrifuge tube (not provided). 7. Place the DNA Spin column in a new collection tube and store at room temperature (15-25ºC) or a 4ºC for later DNA purification. 8. Add 450 l of % Ethanol to the flowthrough. Mix by vortexing for 10 seconds. After addition of ethanol a stringy precipitate may become visible, be sure to load all of the precipitate on the RNA Spin column. 9. Assemble a RNA Spin column with one 10. Apply half of the flowthrough with ethanol onto the columns and centrifuge for 1 minute. Discard the flowthrough and reassemble the spin column with the collection tube. 11. Repeat step 12 to complete the capture of the total RNA. 12. Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Ensure the entire wash buffer has passed through into the collection tube by inspecting the column. If the entire wash volume has not passed, spin for an additional minute. 13. Discard the flowthrough and reassemble the spin column with its collection tube. 11/19
12 Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute 14. Wash column a third time by adding another 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Discard the flowthrough and centrifuge for 2 minutes to eliminate the residual ethanol. En sure that the column is dry and discard the collection tube with the flowthrough. 15. Place the column into a fresh 1.5 ml microfuge tube (not provided in the kit) 16. Add 50 l -100 of Elution Buffer RNA to the column. 17. Centrifuge for 2 minutes at 200xg (aprox rpm), followed by 1 minute at xg (aprox rpm). Note the volume eluted from the column. If the entire 50 l has not been eluted, spin the column at x g (aprox rpm) for 1 additional minute. 18. The purified microrna sample may be stored at -20ºC for a few days. It is recommended that samples be placed at - 70ºC for long term storage Protocol for Genomic DNA isolation from blood 1. Add 500 l of Desinhibition Buffer to the DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 2. Add 500 l of Wash Buffer DNA into reservoir of DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 3. 2º Wash. Add 500 l of Wash Buffer DNA into reservoir of DNA Spin column Centrifuge for 1 minute. Remove the liquid. 4. Centrifuge at maximum speed for 120 seconds to remove the residual ethanol. 5. Remove the collection tube and insert the DNA Spin Column in a 1.5 ml microtube. Add 100l of elution buffer (preheated at 70ºC) into reservoir of DNA Spin column. Incubate 1 minute. 6. Centrifuge at maximum speed for 60 seconds. The microtube contains now the genomic DNA Protocolo de extracción de ADN/ARN a partir de bacterias Protocol of DNA/RNA isolation from bacteria Nota: Se recomienda no utilizar más de 1 x 10 9 células /ml, el crecimiento bacteriano puede ser medido por un espectrofotómetro, como regla general, un cultivo de E.coli de 1 x 10 9 células /ml tiene una DO 600 de 1.0. Preparar una cantidad apropiada de TE conteniendo lisozima, esta solución se preparará con TE libre de RNAsas y conservado en hielo hasta su uso. Para Gram negativos la concentración de lisozima será de 1 mg/ml y Gram-positivos la concentración de lisozima será de 3 mg/ml. Note: It is recommended that no more than 1 x 10 9 bacteria cells be used. Bacterial growth can be measured using a spectrophotometer, as a general rule, an E.coli culture containing 1 x 10 9 bacteria cells has an OD 600 of 1.0. Prepare the appropriate lysozyme-containing TE buffer, this solution should be prepared with sterile, Rnase free TE buffer, and kept on ice until needed. For Gram-negative the concentration of lysozyme will be of 1 mg/ml and for Gram-positive the concentration of lysozyme will be of 3 mg/ml Protocolo de extracción de ARN total a partir de bacterias 1. Obtener el pellet de las células por centrifugación a x g (aprox rpm) durante 1 minuto. 2. Eliminar el sobrenadante y resuspender por vortex el pellet en 100 l del TE con la cantidad apropiada de lisozima. Incubar a temperatura ambiente durante 10 minutos. 3. Añadir 200 l de Tampón de Lisis RNA y vortex durante 15 segundos. 4. Añadir 50 l de Etanol % al lisado. Mezcla por vortex 10 segundos. Asegurarse que el pellet es completamente disuelto antes de proceder con el siguiente paso. 5. Ensamblar una DNA Spin columna con 6. Añadir el lisado + etanol a la columna. Centrifugar durante 1 minuto. 7. Retener el líquido que ha pasado a través de la columna y que se encuentra en el tubo de recogida y que contiene el ARN total. Pasar el líquido retenido a un microtubo nuevo de 1.5 ml ( no suministrado con el kit). 8. Ensamblar la DNA Spin columna con un tubo de recogida y conservar a temperatura ambiente (15-25ºC) o a 4ºC para purificación del ADN más tarde. 9. Añadir 450 l de Etanol % al líquido retenido que contiene el ARN total. Mezcla por vortex 10 segundos. Después de la adición del etanol se podrá apreciar un precipitado, asegurarse de 12/19
13 que todo el precipitado se añade a la RNA Spin columna. 10. Ensamblar una RNA Spin columna con 11. Aplicar la mitad del liquido + etanol en la RNA Spin columna y centrifugar durante 1 minuto. Descartar el líquido y reensamblar la columna con su tubo de recogida. 12. Repetir el punto 12 hasta completar la captura de todo el ARN total. 13. Añadir 400 l de Tampón de Lavado RNA a la columna y centrifugar durante 1 minuto. Asegurarse que todo el tampón de lavado ha pasado a través de la columna, sino fuera así centrifugar otro minuto adicional. 14. Eliminar el líquido y ensamblar la columna con el tubo de recogida. Añadir 400 l de Tampón de Lavado RNA a la 15. Realizar un tercer lavado. Añadir 400 l de Tampón de Lavado RNA a la Eliminar el líquido del tubo de recogida y centrifugar durante 2 minutos adicionales para eliminar todo el etanol residual. Eliminar el tubo de recogida. 16. Colocar la columna en un microtubo nuevo de 1.5 ml ( no suministrado con el kit) para eluir el ARN total. 17. Añadir l de Tampón de Elución RNA a la columna. 18. Centrifugar durante 2 minutos a 200xg (aprox rpm), seguido de 1 minuto a xg (aprox rpm). Ver la cantidad de eluido de la columna, sino se han eluido los 50 l centrifugar por 1 minuto adicional a x g (aprox rpm). 19. El ARN purificado puede ser conservado a -20ºC durante algunos días. Se recomienda que las muestras se conserven a -70ºC para almacenamientos largos Protocolo de extracción de ADN genómico a partir de bacterias 1. Añadir 500 l de Tampón de Desinhibición a la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 2. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 3. 2º Lavado. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido 4. Centrifugar a máxima velocidad durante 2 minutos para eliminar todo el etanol residual. 5. Eliminar el tubo de recolección y insertar la DNA Spin columna en un microtubo de 1.5 ml. Añadir l Tampón de Elución DNA (precalentado a 70ºC) en el reservorio de la DNA Spin columna. Incubar durante 1 minuto. 6. Centrifugar a máxima velocidad durante 1 minuto. El microtubo contiene ahora el ADN genómico Protocol for Total RNA isolation from bacteria 1. Pellet bacteria by centrifugation at x g (aprox rpm) for 1 minute. 2. Decant supernatant, and carefully remove any remaining media by aspiration. Resuspend the bacteria in 100 l of appropriate lysozyme-containing TE by vortexing. Incubate at room temperature for 10 minutes 3. Add 200 l of Lysis Buffer. Lyse cells by vortexing for 15 seconds 4. Add 50 l of ethanol % to lysate. Mix by vortexing for 10 seconds. Ensure that the entire pellet is completely 13/19 dissolved before proceeding to the next step. 5. Assemble a DNA Spin column with one 6. Apply the clarified lysate with ethanol onto the columns. Centrifuge for 1 minute. 7. Retains the flowthrough, which contains the total RNA. Use the flowthrough for RNA purification. Transfer the flowthrough to a new RNase-free microcentrifuge tube (not provided).
14 8. Place the DNA Spin column in a new collection tube and store at room temperature (15-25ºC) or a 4ºC for later DNA purification. 9. Add 450 l of % Ethanol to the flowthrough. Mix by vortexing for 10 seconds. After addition of ethanol a stringy precipitate may become visible, be sure to load all of the precipitate on the RNA Spin column. 10. Assemble a RNA Spin column with one 11. Apply half of the flowthrough with ethanol onto the columns and centrifuge for 1 minute. Discard the flowthrough and reassemble the spin column with the collection tube. 12. Repeat step 12 to complete the capture of the total RNA. 13. Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Ensure the entire wash buffer has passed through into the collection tube by inspecting the column. If the entire wash volume has not passed, spin for an additional minute. 14. Discard the flowthrough and reassemble the spin column with its collection tube Protocol for Genomic DNA isolation from bacteria Add 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute 15. Wash column a third time by adding another 400 l of Wash Buffer RNA to the column and centrifuge for 1 minute. Discard the flowthrough and centrifuge for 2 minutes to eliminate the residual ethanol. En sure that the column is dry and discard the collection tube with the flowthrough. 16. Place the column into a fresh 1.5 ml microfuge tube (not provided in the kit) 17. Add 50 l -100 of Elution Buffer RNA to the column. 18. Centrifuge for 2 minutes at 200xg (aprox rpm), followed by 1 minute at xg (aprox rpm). Note the volume eluted from the column. If the entire 50 l has not been eluted, spin the column at xg (aprox rpm) for 1 additional minute. 19. The purified microrna sample may be stored at -20ºC for a few days. It is recommended that samples be placed at - 70ºC for long term storage. 1. Add 500 l of Desinhibition Buffer to the DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 2. Add 500 l of Wash Buffer DNA in to reservoir of DNA Spin column. Centrifuge for 1 minute. Remove the liquid. 3. 2º Wash. Add 500 l of Wash Buffer DNA into reservoir of DNA Spin column Centrifuge for 1 minute. Remove the liquid. 4. Centrifuge at maximum speed for 120 seconds to remove the residual ethanol. 5. Remove the collection tube and insert the DNA Spin Column in a 1.5 ml microtube. Add 100l of elution buffer (preheated at 70ºC) into reservoir of DNA Spin column. Incubate 1 minute. 6. Centrifuge at maximum speed for 60 seconds. The microtube contains now the genomic DNA Protocolo de extracción de ADN/ARN a partir de levaduras Protocol of DNA/RNA isolation from yeast Nota: Se recomienda no utilizar más de 10 7 células de levadura o 1ml de cultivo. Preparar una cantidad apropiada de Tampón de Resuspensión que contenga liticasa : 50mM tris, ph 7.5, 10 mm EDTA, 1M Sorbitol, 0.10 % - mercaptoetanol y 1 unidad / l de liticasa. Esta solución debería prepararse con reactivos estériles y libres de RNAsas y mantenida en hielo hasta ser utilizada Protocolo de extracción de ARN total a partir de levaduras Note: It is recommended that no more than 10 7 yeast cells or 1 ml of culture be used for this procedure. Prepare the appropriate amount of lyticase resuspension buffer: 50mM Tris, ph 7.5, 10 mm EDTA, 1M Sorbital, 0.10 % -mercaptoethanol and 1 unit / l of lyticase. This solution should be prepared with sterile, Rnase free reagents, and kept on ice until needed. 1. Obtener el pellet de las levaduras por centrifugación a xg (aprox rpm) durante 1 minuto. 2. Eliminar el sobrenadante y resuspender por vortex el pellet en 100 l del Tampón de Resuspensión con la cantidad apropiada de liticasa. Incubar a 37ºC durante 10 minutos. 3. Añadir 300 l de Tampón de Lisis RNA al pellet. Lisar las células por vortex durante 15 segundos. Asegurarse que todo 14/19
15 el pellet está disuelto antes de proceder con el siguiente paso. 4. Pasar el lisado a un microtubo. IMPORTANTE: Anotar la cantidad de lisado. 5. Añadir 15 l de etanol 100 % por cada 100 l de lisado). Mezcla por vortex 10 segundos. 6. Ensamblar una DNA Spin columna con 7. Añadir el lisado + etanol a la columna. Centrifugar durante 1 minuto. 8. Retener el líquido que ha pasado a través de la columna y que se encuentra en el tubo de recogida y que contiene el ARN total. Pasar el líquido retenido a un microtubo nuevo de 1.5 ml ( no suministrado con el kit). 9. Ensamblar la DNA Spin columna con un tubo de recogida y conservar a temperatura ambiente (15-25ºC) o a 4ºC para purificación del ADN más tarde. 10. Añadir 450 l de Etanol % al líquido retenido que contiene el ARN total. Mezcla por vortex 10 segundos. Después de la adición del etanol se podrá apreciar un precipitado, asegurarse de que todo el precipitado se añade a la RNA Spin columna. 11. Ensamblar una RNA Spin columna con 12. Aplicar la mitad del liquido + etanol en la RNA Spin columna y centrifugar durante 1 minuto. Descartar el líquido y reensamblar la columna con su tubo de recogida. 13. Repetir el punto 12 hasta completar la captura de todo el ARN total. 14. Añadir 400 l de Tampón de Lavado RNA a la columna y centrifugar durante 1 minuto. Asegurarse que todo el tampón de lavado ha pasado a través de la columna, sino fuera así centrifugar otro minuto adicional. 15. Eliminar el líquido y ensamblar la columna con el tubo de recogida. Añadir 400 l de Tampón de Lavado RNA a la 16. Realizar un tercer lavado. Añadir 400 l de Tampón de Lavado RNA a la Eliminar el líquido del tubo de recogida y centrifugar durante 2 minutos adicionales para eliminar todo el etanol residual. Eliminar el tubo de recogida. 17. Colocar la columna en un microtubo nuevo de 1.5 ml ( no suministrado con el kit) para eluir el ARN total. 18. Añadir l de Tampón de Elución RNA a la columna. 19. Centrifugar durante 2 minutos a 200xg (aprox rpm), seguido de 1 minuto a xg (aprox rpm). Ver la cantidad de eluido de la columna, sino se han eluido los 50 l centrifugar por 1 minuto adicional a x g (aprox rpm). 20. El ARN purificado puede ser conservado a -20ºC durante algunos días. Se recomienda que las muestras se conserven a -70ºC para almacenamientos largos Protocolo de extracción de ADN genómico a partir de levaduras 1. Añadir 500 l de Tampón de Desinhibición a la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 2. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido. 3. 2º Lavado. Añadir 500 l de Tampón de Lavado DNA en el reservorio de la DNA Spin columna. Centrifugar durante 1 minuto. Eliminar el líquido 4. Centrifugar a máxima velocidad durante 2 minutos para eliminar todo el etanol residual. 5. Eliminar el tubo de recolección y insertar la DNA Spin columna en un microtubo de 1.5 ml. Añadir l Tampón de Elución DNA (precalentado a 70ºC) en el reservorio de la DNA Spin columna. Incubar durante 1 minuto. 6. Centrifugar a máxima velocidad durante 1 minuto. El microtubo contiene ahora el ADN genómico. 15/19
DANAGENE RNA PURIFICATION KIT
 DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
REALPLASMID SPIN MIDI/MAXI PREP KIT
 05/10 RBMEPS02 REALPLASMID SPIN MIDI/MAXI PREP KIT Ref. RBMEPS02 20 Preps. 1. INTRODUCCIÓN 1. INTRODUCTION REALPLASMID Spin Midi/Maxiprep Kit provee de un método simple y rápido para aislar ADN plasmídico
05/10 RBMEPS02 REALPLASMID SPIN MIDI/MAXI PREP KIT Ref. RBMEPS02 20 Preps. 1. INTRODUCCIÓN 1. INTRODUCTION REALPLASMID Spin Midi/Maxiprep Kit provee de un método simple y rápido para aislar ADN plasmídico
REAL TOTAL RNA FROM BACTERIA AND YEAST KIT
 REAL TOTAL RNA FROM BACTERIA AND YEAST KIT Ref. 1. INTRODUCCIÓN 1. INTRODUCTION Este kit permite la obtención de ARN total a partir de diferentes cultivos de bacterias y levaduras, sin la utilización de
REAL TOTAL RNA FROM BACTERIA AND YEAST KIT Ref. 1. INTRODUCCIÓN 1. INTRODUCTION Este kit permite la obtención de ARN total a partir de diferentes cultivos de bacterias y levaduras, sin la utilización de
DANAGENE PLASMID MIDI/MAXI KIT
 REF.0702.4 25 Midis REF.0702.5 10 Maxis DANAGENE PLASMID MIDI/MAXI KIT 1. INTRODUCCION DANAGENE PLASMID Midi/Maxiprep Kit proporciona un método simple para purificar ADN plasmídico a partir de cultivos
REF.0702.4 25 Midis REF.0702.5 10 Maxis DANAGENE PLASMID MIDI/MAXI KIT 1. INTRODUCCION DANAGENE PLASMID Midi/Maxiprep Kit proporciona un método simple para purificar ADN plasmídico a partir de cultivos
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
REAL TOTAL RNA SPIN BLOOD KIT
 REAL TOTAL RNA SPIN BLOOD KIT Ref. 50 Preps. 1. INTRODUCCIÓN 1. INTRODUCTION Sistema de producción certificado bajo norma ISO Este kit permite la obtención de ARN total libre de ADN directamente de sangre
REAL TOTAL RNA SPIN BLOOD KIT Ref. 50 Preps. 1. INTRODUCCIÓN 1. INTRODUCTION Sistema de producción certificado bajo norma ISO Este kit permite la obtención de ARN total libre de ADN directamente de sangre
DANAGENE SALIVA KIT. Ref Extracciones / Ref Extracciones
 DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION Este kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras de saliva
DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION Este kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras de saliva
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS
 1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
DANAGENE GENOMIC DNA KIT
 Ref. 0603.1 Ref. 0603.2 Ref. 0603.3 DANAGENE GENOMIC DNA KIT 1.INTRODUCCION 1.1 Descripción del producto Este kit está designado para la extracción de ADN genómico de alta calidad a partir de una amplia
Ref. 0603.1 Ref. 0603.2 Ref. 0603.3 DANAGENE GENOMIC DNA KIT 1.INTRODUCCION 1.1 Descripción del producto Este kit está designado para la extracción de ADN genómico de alta calidad a partir de una amplia
Protocolo de iniciación PCR. a tiempo real
 Protocolo de iniciación PCR a tiempo real CERTEST Biotec, S.L. Pol. Industrial Río Gállego II, Calle J, Nº 1, 50840, San Mateo de Gállego, Zaragoza (SPAIN) www.certest.es Protocolo de iniciación PCR a
Protocolo de iniciación PCR a tiempo real CERTEST Biotec, S.L. Pol. Industrial Río Gállego II, Calle J, Nº 1, 50840, San Mateo de Gállego, Zaragoza (SPAIN) www.certest.es Protocolo de iniciación PCR a
REAL MINIPREP TURBO KIT
 REAL MINIPREP TURBO KIT Ref. 500 Preps. 1. INTRODUCCIÓN 1. INTRODUCTION Este kit provee un método para una rápida, sencilla y eficiente extracción de DNA plasmídico a partir de cultivos de E.coli de 1.5-3.0
REAL MINIPREP TURBO KIT Ref. 500 Preps. 1. INTRODUCCIÓN 1. INTRODUCTION Este kit provee un método para una rápida, sencilla y eficiente extracción de DNA plasmídico a partir de cultivos de E.coli de 1.5-3.0
SPEEDTOOLS DNA EXTRACTION KIT
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu SPEEDTOOLS DNA EXTRACTION
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu SPEEDTOOLS DNA EXTRACTION
SPEEDTOOLS RNA VIRUS EXTRACTION KIT
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid Spain Tel. (34) 91 710 00 74 Fax (34) 91 505 31 18 e-mail: info@biotools.eu www.biotools.eu SPEEDTOOLS RNA VIRUS EXTRACTION
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid Spain Tel. (34) 91 710 00 74 Fax (34) 91 505 31 18 e-mail: info@biotools.eu www.biotools.eu SPEEDTOOLS RNA VIRUS EXTRACTION
PROCEDIMIENTO PARA REALIZAR CONCENTRACION DE VIRUS ENTERICOS EN MUESTRAS DE AGUA. PRT Página 1 de 5
 PRT-712.07.01-104 Página 1 de 5 1. OBJETIVO Realizar concentración viral desde muestras de agua para su posterior análisis de presencia de virus entéricos. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento
PRT-712.07.01-104 Página 1 de 5 1. OBJETIVO Realizar concentración viral desde muestras de agua para su posterior análisis de presencia de virus entéricos. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento
REAL CLEAN SPIN KIT. Ref. RBMCS01 50 Preps. Ref. RBMCS02 250 Preps 1. INTRODUCCIÓN 1. INTRODUCTION
 REAL CLEAN SPIN KIT Ref. RBMCS01 50 Preps. Ref. RBMCS02 250 Preps 1. INTRODUCCIÓN 1. INTRODUCTION Sistema de producción certificado bajo norma ISO Real Clean Spin Kit es un método versátil y efectivo para
REAL CLEAN SPIN KIT Ref. RBMCS01 50 Preps. Ref. RBMCS02 250 Preps 1. INTRODUCCIÓN 1. INTRODUCTION Sistema de producción certificado bajo norma ISO Real Clean Spin Kit es un método versátil y efectivo para
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
REAL TOTAL RNA FROM TISSUES AND CELLS STAR KIT
 10/10 RBMER02 REAL TOTAL RNA FROM TISSUES AND CELLS STAR KIT Ref. RBMER02 1. INTRODUCCIÓN 1. INTRODUCTION Este kit permite la obtención de ARN total a partir de muestras de tejidos y células, sin la utilización
10/10 RBMER02 REAL TOTAL RNA FROM TISSUES AND CELLS STAR KIT Ref. RBMER02 1. INTRODUCCIÓN 1. INTRODUCTION Este kit permite la obtención de ARN total a partir de muestras de tejidos y células, sin la utilización
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar
 4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA
 DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA MÓDULO DE GENÉTICA TÉCNICAS MOLECULARES DE ANÁLISIS GENÉTICO AISLAMIENTO Y CLONACIÓN DE ADN SATÉLITE
DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA MÓDULO DE GENÉTICA TÉCNICAS MOLECULARES DE ANÁLISIS GENÉTICO AISLAMIENTO Y CLONACIÓN DE ADN SATÉLITE
ADN PuriPrep-T kit K Extracción y purificación rápida de ADN a partir de tejidos sólidos:
 K 1208 ADN PuriPrep-T kit Extracción y purificación rápida de ADN a partir de tejidos sólidos: Hueso disgregado, Bulbo capilar Cola de ratón, Tejidos fijados Biopsias, Hígado, Bazo Indice Presentación...
K 1208 ADN PuriPrep-T kit Extracción y purificación rápida de ADN a partir de tejidos sólidos: Hueso disgregado, Bulbo capilar Cola de ratón, Tejidos fijados Biopsias, Hígado, Bazo Indice Presentación...
EXTRACCIÓN Y PURIFICACIÓN DE ÁCIDOS NUCLEICOS
 EXTRACCIÓN Y PURIFICACIÓN DE ÁCIDOS NUCLEICOS Consideraciones iniciales - Condiciones de limpieza y esterilidad - Peligrosidad de algunos reactivos usados en la purificación Fases - Rotura-homogeneización:
EXTRACCIÓN Y PURIFICACIÓN DE ÁCIDOS NUCLEICOS Consideraciones iniciales - Condiciones de limpieza y esterilidad - Peligrosidad de algunos reactivos usados en la purificación Fases - Rotura-homogeneización:
SPEEDTOOLS FOOD DNA EXTRACTION KIT
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 91 505 31 18 e-mail: info@biotools.eu www.biotools.eu SPEEDTOOLS FOOD DNA EXTRACTION
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 91 505 31 18 e-mail: info@biotools.eu www.biotools.eu SPEEDTOOLS FOOD DNA EXTRACTION
K ADN PuriPrep-GP kit. Extracción y purificación rápida de ADN a partir de: Gel de agarosa y Productos de PCR en solución
 K 1206 ADN PuriPrep-GP kit Extracción y purificación rápida de ADN a partir de: Gel de agarosa y Productos de PCR en solución Indice Presentación... 6 Importante... 6 Componentes del kit... 6 Condiciones
K 1206 ADN PuriPrep-GP kit Extracción y purificación rápida de ADN a partir de: Gel de agarosa y Productos de PCR en solución Indice Presentación... 6 Importante... 6 Componentes del kit... 6 Condiciones
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987)
 EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497.
 Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497. Extracción de DNA genómico El DNA de A. brasilense CBG 497 se extrajo siguiendo el método descrito por la casa comercial distribuidora
Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497. Extracción de DNA genómico El DNA de A. brasilense CBG 497 se extrajo siguiendo el método descrito por la casa comercial distribuidora
SPEEDTOOLS TISSUE DNA EXTRACTION KIT
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel: (34) 91 710 00 74 Fax : (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu SPEEDTOOLS TISSUE DNA
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel: (34) 91 710 00 74 Fax : (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu SPEEDTOOLS TISSUE DNA
BASE & WALL EASY REACH CABINET 170º Hinge Replacement
 These instructions should only be printed using Adobe Acrobat and should not be faxed or reproduced on a digital copier. American Woodmark Corporation provides these instructions on an AS IS basis and
These instructions should only be printed using Adobe Acrobat and should not be faxed or reproduced on a digital copier. American Woodmark Corporation provides these instructions on an AS IS basis and
PCR gen 16S ARNr bacteriano
 PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
Greetings. Lists and TPR Sheets The Enlightened Elephant
 Greetings Lists and TPR Sheets Total Physical Response Vocabulary Practice The set of pages with images are the TPR (Total Physical Response) picture pages. They are available with or without words and
Greetings Lists and TPR Sheets Total Physical Response Vocabulary Practice The set of pages with images are the TPR (Total Physical Response) picture pages. They are available with or without words and
Kit de purificación de ARN sanguíneo RNAgard Manual de usuario
 Kit de purificación de ARN sanguíneo RNAgard Manual de usuario CE-12000-001 Para usar en el diagnóstico in vitro. Biomatrica, Inc. 5627 Oberlin Drive, Suite 120 San Diego, CA 92121, EE.UU 00 1 858 550
Kit de purificación de ARN sanguíneo RNAgard Manual de usuario CE-12000-001 Para usar en el diagnóstico in vitro. Biomatrica, Inc. 5627 Oberlin Drive, Suite 120 San Diego, CA 92121, EE.UU 00 1 858 550
Anexo Conservar a 4 o C.
 Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Flashcards Series 5 El Agua
 Flashcards Series 5 El Agua Flashcards are one of the quickest and easiest ways to test yourself on Spanish vocabulary, no matter where you are! Test yourself on just these flashcards at first. Then, as
Flashcards Series 5 El Agua Flashcards are one of the quickest and easiest ways to test yourself on Spanish vocabulary, no matter where you are! Test yourself on just these flashcards at first. Then, as
TP2: Extracción y cuantificación de proteínas
 Objetivo TP2: Extracción y cuantificación de proteínas Comparar métodos de extracción de proteínas a partir de distintos organismos. Cuantificar las proteínas resultantes de cada extracto. Introducción
Objetivo TP2: Extracción y cuantificación de proteínas Comparar métodos de extracción de proteínas a partir de distintos organismos. Cuantificar las proteínas resultantes de cada extracto. Introducción
TRABAJO PRÁCTICO No. 2 EXTRACION DE ACIDO NUCLEICO VIRAL
 Unidad Curricular: Virología y Micología Veterinaria TRABAJO PRÁCTICO No. 2 EXTRACION DE ACIDO NUCLEICO VIRAL Las pruebas para el diagnostico específico de una infección viral se clasifican en dos tipos:
Unidad Curricular: Virología y Micología Veterinaria TRABAJO PRÁCTICO No. 2 EXTRACION DE ACIDO NUCLEICO VIRAL Las pruebas para el diagnostico específico de una infección viral se clasifican en dos tipos:
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
Anexo 1: Enfermedades monogénicas diagnosticadas hasta la fecha, en España, mediante DGP (Fuente: datos propios del grupo de interés en DGP de
 Anexo 1: Enfermedades monogénicas diagnosticadas hasta la fecha, en España, mediante DGP (Fuente: datos propios del grupo de interés en DGP de ASEBIR). 1 2 3 4 Anexo2: Ejemplo de protocolo para translocaciones
Anexo 1: Enfermedades monogénicas diagnosticadas hasta la fecha, en España, mediante DGP (Fuente: datos propios del grupo de interés en DGP de ASEBIR). 1 2 3 4 Anexo2: Ejemplo de protocolo para translocaciones
Manual de Uso (Ref /2)
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Buffy_Coat_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Buffy_Coat_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
RapidFinder STEC Detection Workflow
 QUICK REFERENCE RapidFinder STEC Detection Workflow Aislamiento automático de ADN y detección de la PCR en tiempo real de E. coli O157:H7 y cepas "Big 6" de STEC no O157 Número de catálogo 4480466, 4428176,
QUICK REFERENCE RapidFinder STEC Detection Workflow Aislamiento automático de ADN y detección de la PCR en tiempo real de E. coli O157:H7 y cepas "Big 6" de STEC no O157 Número de catálogo 4480466, 4428176,
Evaluate the effect of ProStart PLUS in the flowering response of Cherries plants cv. Bing
 Interpretando El Lenguaje de las Plantas Evaluate the effect of ProStart PLUS in the flowering response of Cherries plants cv. Bing Evaluate the effect of ProStart PLUS in the flowering response of Cherries
Interpretando El Lenguaje de las Plantas Evaluate the effect of ProStart PLUS in the flowering response of Cherries plants cv. Bing Evaluate the effect of ProStart PLUS in the flowering response of Cherries
New igenatal TM. New & Optimized Genomic DNA Extraction Kit
 New igenatal TM New & Optimized Genomic DNA Extraction Kit (FOR 50 EXTRACTIONS) ilab Tech SL, Gustavo Fernández Balbuena 11, 28002 Madrid Tel: +34 91 510 29 99 Fax: +34 91 51913 26 HIGH QUALITY GENOMIC
New igenatal TM New & Optimized Genomic DNA Extraction Kit (FOR 50 EXTRACTIONS) ilab Tech SL, Gustavo Fernández Balbuena 11, 28002 Madrid Tel: +34 91 510 29 99 Fax: +34 91 51913 26 HIGH QUALITY GENOMIC
ANEXOS. Anexo 1 Transformación mediante electroporación
 Anexo 1 Transformación mediante electroporación ANEXOS En este método de transformación de E. coli se requieren células electrocompetentes. La preparación de estas células consta de los siguientes pasos:
Anexo 1 Transformación mediante electroporación ANEXOS En este método de transformación de E. coli se requieren células electrocompetentes. La preparación de estas células consta de los siguientes pasos:
Manual de Uso (Ref /1/2)
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 91 505 31 18 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 91 505 31 18 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
DANAGENE SALIVA KIT. Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones
 DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION DANAGENE SALIVA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras
DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION DANAGENE SALIVA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras
 New! Solvent-free The new MiniSystem is here... New cap design for easier sample collection!! New! New! 1. Ready to Use 2. One Step 3. Disposable 4. Closed Process 5. Save space and reagents 6. Fast Protocol
New! Solvent-free The new MiniSystem is here... New cap design for easier sample collection!! New! New! 1. Ready to Use 2. One Step 3. Disposable 4. Closed Process 5. Save space and reagents 6. Fast Protocol
Level 1 Spanish, 2013
 90911 909110 1SUPERVISOR S Level 1 Spanish, 2013 90911 Demonstrate understanding of a variety of Spanish texts on areas of most immediate relevance 9.30 am Tuesday 3 December 2013 Credits: Five Achievement
90911 909110 1SUPERVISOR S Level 1 Spanish, 2013 90911 Demonstrate understanding of a variety of Spanish texts on areas of most immediate relevance 9.30 am Tuesday 3 December 2013 Credits: Five Achievement
Programación lineal Optimización de procesos químicos DIQUIMA-ETSII
 Programación lineal PROGRAMACIÓN LINEAL PROGRAMACIÓN LINEAL se formula siguiendo el planteamiento general: Función objetivo Restricciones de igualdad Restricciones de desigualdad Límite variables PROGRAMACIÓN
Programación lineal PROGRAMACIÓN LINEAL PROGRAMACIÓN LINEAL se formula siguiendo el planteamiento general: Función objetivo Restricciones de igualdad Restricciones de desigualdad Límite variables PROGRAMACIÓN
KILLS ON CONTACT MAKES 2 GALLONS
 131_BF_Extreme_HIC_Conc_16oz_F.ai K Cool Gray 7 Cool Gray 3 PMS 109 Matte Lam 9688-30_Black Flag Extreme Home Insect Control Concentrate _0170516_7_9688_.pdf KILLS ON CONTACT MAKES GALLONS GUARANTEED TO
131_BF_Extreme_HIC_Conc_16oz_F.ai K Cool Gray 7 Cool Gray 3 PMS 109 Matte Lam 9688-30_Black Flag Extreme Home Insect Control Concentrate _0170516_7_9688_.pdf KILLS ON CONTACT MAKES GALLONS GUARANTEED TO
SAMPLE EXAMINATION BOOKLET
 S SAMPLE EXAMINATION BOOKLET New Zealand Scholarship Spanish Time allowed: Three hours Total marks: 24 EXAMINATION BOOKLET Question ONE TWO Mark There are three questions. You should answer Question One
S SAMPLE EXAMINATION BOOKLET New Zealand Scholarship Spanish Time allowed: Three hours Total marks: 24 EXAMINATION BOOKLET Question ONE TWO Mark There are three questions. You should answer Question One
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo VirusBlood200_V5_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN viral a partir
Hoja de protocolo del instrumento QIAsymphony SP Protocolo VirusBlood200_V5_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN viral a partir
SIHI México, S. de R.L. de C.V. Pricing Guide
 Pricing Guide Rates effective as of: October 1, 2016 Note: Rates are subject to change without prior notice. Rates are stated in Mexican Pesos unless otherwise specified. page 1 of 5 Table Of Contents
Pricing Guide Rates effective as of: October 1, 2016 Note: Rates are subject to change without prior notice. Rates are stated in Mexican Pesos unless otherwise specified. page 1 of 5 Table Of Contents
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA
 PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
Instructivo de uso y cuidado del Aplicador de Implantes Lapisa. Productos Destacados
 Instructivo de uso y cuidado del Aplicador de Implantes Lapisa Productos Destacados Diseño ergonómico Producido con materiales de larga duración para asegurar una vidá útil prolongada Espacio para aguja
Instructivo de uso y cuidado del Aplicador de Implantes Lapisa Productos Destacados Diseño ergonómico Producido con materiales de larga duración para asegurar una vidá útil prolongada Espacio para aguja
SOLICITUD DEL SERVICIO DE SECUENCIACION CENTRO DE DETECCION BIOMOLECULAR EN ENFERMEDADES EMERGENTES/BUAP
 SOLICITUD DEL SERVICIO DE SECUENCIACION CENTRO DE DETECCION BIOMOLECULAR EN ENFERMEDADES EMERGENTES/BUAP Usuario: Institución: Fecha: Departamento: e-mail: Teléfono: Ext.: Investigador Principal: e-mail:
SOLICITUD DEL SERVICIO DE SECUENCIACION CENTRO DE DETECCION BIOMOLECULAR EN ENFERMEDADES EMERGENTES/BUAP Usuario: Institución: Fecha: Departamento: e-mail: Teléfono: Ext.: Investigador Principal: e-mail:
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
Tissue_LC_200_V7_DSP y. Tissue_HC_200_V7_DSP. Sample to Insight. Agosto 2015 Hoja de protocolo del instrumento QIAsymphony SP
 Agosto 2015 Hoja de protocolo del instrumento QIAsymphony SP Tissue_LC_200_V7_DSP y Tissue_HC_200_V7_DSP Este documento es Hoja de protocolo del instrumento QIAsymphony SP para los protocolos Tissue_LC_200_V7_DSP
Agosto 2015 Hoja de protocolo del instrumento QIAsymphony SP Tissue_LC_200_V7_DSP y Tissue_HC_200_V7_DSP Este documento es Hoja de protocolo del instrumento QIAsymphony SP para los protocolos Tissue_LC_200_V7_DSP
Technique For CADVEST. CAD RESIN PATTERN INVESTMENT Fine-Grained Investment Formulated Specifically For Partial Framework Printed Resin Patterns
 Technique For CADVEST CAD RESIN PATTERN INVESTMENT Fine-Grained Investment Formulated Specifically For Partial Framework Printed Resin Patterns 1 Sprue with the CAD software if possible or attach (6 ga)
Technique For CADVEST CAD RESIN PATTERN INVESTMENT Fine-Grained Investment Formulated Specifically For Partial Framework Printed Resin Patterns 1 Sprue with the CAD software if possible or attach (6 ga)
RESOLUCIÓN OIV-OENO
 RESOLUCIÓN OIV-OENO 574-2017 MONOGRAFÍA SOBRE LOS TANINOS: REVISIÓN DEL MÉTODO DE DETERMINACIÓN DE LOS POLIFENOLES LA ASAMBLEA GENERAL, Visto el artículo 2, párrafo 2 iv del Acuerdo del 3 de abril de 2001
RESOLUCIÓN OIV-OENO 574-2017 MONOGRAFÍA SOBRE LOS TANINOS: REVISIÓN DEL MÉTODO DE DETERMINACIÓN DE LOS POLIFENOLES LA ASAMBLEA GENERAL, Visto el artículo 2, párrafo 2 iv del Acuerdo del 3 de abril de 2001
Extração de DNA/RNA Viral
 Extração de DNA/RNA Viral Instruções de uso Instrucciones de uso Usage instructions K204 Revisão: Agosto/2016 ÍNDICE Finalidade... 3 Princípio de Ação... 3 Apresentação... 3 Reagentes... 4 Equipamentos
Extração de DNA/RNA Viral Instruções de uso Instrucciones de uso Usage instructions K204 Revisão: Agosto/2016 ÍNDICE Finalidade... 3 Princípio de Ação... 3 Apresentação... 3 Reagentes... 4 Equipamentos
Protocolo de laboratorio para purificación manual de ADN a partir de una muestra entera
 Protocolo de laboratorio para purificación manual de ADN a partir de una muestra entera Para la purificación de ADN genómico de todos los estuches de colección Oragene y ORAcollect. Visite nuestro sitio
Protocolo de laboratorio para purificación manual de ADN a partir de una muestra entera Para la purificación de ADN genómico de todos los estuches de colección Oragene y ORAcollect. Visite nuestro sitio
Aspira* Pleural Drainage System
 Patient Information on the Aspira* Pleural Drainage System Información para el paciente sobre el Sistema de drenado pleural Aspira* Aspira* Pleural Drainage Catheter The pain and difficult breathing you
Patient Information on the Aspira* Pleural Drainage System Información para el paciente sobre el Sistema de drenado pleural Aspira* Aspira* Pleural Drainage Catheter The pain and difficult breathing you
Installation Guide. Green momit
 Installation Guide Green momit 2015 www.momit.com momit Deviceses Gateway: Model 1 and 2 Wall option The momit Gateway allows your thermostat to be connected to the Internet. It s included in the Starter
Installation Guide Green momit 2015 www.momit.com momit Deviceses Gateway: Model 1 and 2 Wall option The momit Gateway allows your thermostat to be connected to the Internet. It s included in the Starter
IC BOVINO IC CAPRINO. Immunochromatrographic test for milk species identification. Test Inmunocromatográfico para la detección de mezclas de leche
 IC BOVINO IC CAPRINO ZE/ICB ZE/ICB100 ZE/ICC ZE/ICC100 Immunochromatrographic test for milk species identification Test Inmunocromatográfico para la detección de mezclas de leche ZEULAB, S.L. C/ Bari,
IC BOVINO IC CAPRINO ZE/ICB ZE/ICB100 ZE/ICC ZE/ICC100 Immunochromatrographic test for milk species identification Test Inmunocromatográfico para la detección de mezclas de leche ZEULAB, S.L. C/ Bari,
Indirect Object Pronouns
 Indirect Object Pronouns We ve seen three types of pronouns so far: Subject: yo, tú, él Reflexive: me, te, se Direct object: me, te, lo, la In this slide show, we are going to look at one more type: indirect
Indirect Object Pronouns We ve seen three types of pronouns so far: Subject: yo, tú, él Reflexive: me, te, se Direct object: me, te, lo, la In this slide show, we are going to look at one more type: indirect
How to use? Como se usa? Método de Cuatro Veces al día. Four Times a Day Method (after 2 weeks)
 Como se usa? Se comienza preparando el cuerpo por dos semanas ingiriendo una cuarta parte de las gotas totales por peso según la tabla a continuación. Por ejemplo para el peso de 190 el total de gotas
Como se usa? Se comienza preparando el cuerpo por dos semanas ingiriendo una cuarta parte de las gotas totales por peso según la tabla a continuación. Por ejemplo para el peso de 190 el total de gotas
NUEVO: tubo de 5,0 ml con tapa de rosca. El eslabón perdido. Eppendorf Tubes 5.0 ml sistema simple y seguro
 NUEVO: tubo de 5,0 ml con tapa de rosca El eslabón perdido 5.0 ml sistema simple y seguro 5mL_Tube_BRO_GB_2015.indd 1 27.11.15 14:04 2 En combinación con el amplio surtido de accesorios, los 5.0 ml son
NUEVO: tubo de 5,0 ml con tapa de rosca El eslabón perdido 5.0 ml sistema simple y seguro 5mL_Tube_BRO_GB_2015.indd 1 27.11.15 14:04 2 En combinación con el amplio surtido de accesorios, los 5.0 ml son
Protocolo del instrumento QIAsymphony SP
 Protocolo del instrumento QIAsymphony SP Tissue_LC_200_V7_DSP y Tissue_HC_200_V7_DSP Información general Para el diagnóstico in vitro. Estos protocolos sirven para la purificación del ADN total procedente
Protocolo del instrumento QIAsymphony SP Tissue_LC_200_V7_DSP y Tissue_HC_200_V7_DSP Información general Para el diagnóstico in vitro. Estos protocolos sirven para la purificación del ADN total procedente
Instructions For Use. STEP 1 Locate the area on your horse that you wish to patch.
 AcuLife Instructions Instrucciones Instructions For Use You don t need to be a veterinarian or a pain expert to use AcuLife. Simply follow these instructions for patching your horse and be sure to monitor
AcuLife Instructions Instrucciones Instructions For Use You don t need to be a veterinarian or a pain expert to use AcuLife. Simply follow these instructions for patching your horse and be sure to monitor
Creating your Single Sign-On Account for the PowerSchool Parent Portal
 Creating your Single Sign-On Account for the PowerSchool Parent Portal Welcome to the Parent Single Sign-On. What does that mean? Parent Single Sign-On offers a number of benefits, including access to
Creating your Single Sign-On Account for the PowerSchool Parent Portal Welcome to the Parent Single Sign-On. What does that mean? Parent Single Sign-On offers a number of benefits, including access to
AdnaTest BreastCancerSelect
 AdnaTest BreastCancerSelect Enriquecimiento de células tumorales provenientes de sangre de pacientes con cáncer de mama para el análisis de la expresión génica Para uso de diagnóstico in vitro Manual T-1-508
AdnaTest BreastCancerSelect Enriquecimiento de células tumorales provenientes de sangre de pacientes con cáncer de mama para el análisis de la expresión génica Para uso de diagnóstico in vitro Manual T-1-508
Cantemos Las Posadas - Contiene Villancicos, Cánticos para Pedir la Piñata, Letanía y todo para la Temporada Navideña. (Corazón Renovado)
 Cantemos Las Posadas - Contiene Villancicos, Cánticos para Pedir la Piñata, Letanía y todo para la Temporada Navideña. (Corazón Renovado) Tradiciones Mexicanas Click here if your download doesn"t start
Cantemos Las Posadas - Contiene Villancicos, Cánticos para Pedir la Piñata, Letanía y todo para la Temporada Navideña. (Corazón Renovado) Tradiciones Mexicanas Click here if your download doesn"t start
Pida un póster para su laboratorio ahora enviando un mail con sus datos a la dirección:
 Parasitology NUEVO! NEW! * SISTEMA MINI PARA RECOGIDA, TRANSPORTE Y FILTRACIÓN DE PARÁSITOS. MINI-SYSTEM FOR COLLECTING, TRANSPORT AND FILTRATION OF PARASITES. * Sistema patentado por Durviz S.L.U. * System
Parasitology NUEVO! NEW! * SISTEMA MINI PARA RECOGIDA, TRANSPORTE Y FILTRACIÓN DE PARÁSITOS. MINI-SYSTEM FOR COLLECTING, TRANSPORT AND FILTRATION OF PARASITES. * Sistema patentado por Durviz S.L.U. * System
UNA MUJER DE FE EXTRAORDINARIA: ENTREGA TODA TU VIDA A DIOS (SPANISH EDITION) BY JULIE CLINTON
 Read Online and Download Ebook UNA MUJER DE FE EXTRAORDINARIA: ENTREGA TODA TU VIDA A DIOS (SPANISH EDITION) BY JULIE CLINTON DOWNLOAD EBOOK : UNA MUJER DE FE EXTRAORDINARIA: ENTREGA TODA TU Click link
Read Online and Download Ebook UNA MUJER DE FE EXTRAORDINARIA: ENTREGA TODA TU VIDA A DIOS (SPANISH EDITION) BY JULIE CLINTON DOWNLOAD EBOOK : UNA MUJER DE FE EXTRAORDINARIA: ENTREGA TODA TU Click link
Instruction Manual. Safety Warning and Precautions
 Art# GAZ201490/5055 Instruction Manual Save this Manual for future reference. Your Gazebo requires assembly prior to use. It is important that you read the entire manual to become familiar with the unit
Art# GAZ201490/5055 Instruction Manual Save this Manual for future reference. Your Gazebo requires assembly prior to use. It is important that you read the entire manual to become familiar with the unit
IC-BOVINO. Immunocromatographic test to detect cow s milk in sheep or goat s milk
 Immunocromatographic test to detect cow s milk in sheep or goat s milk Test inmunocromatográfico para la detección de leche de vaca en leche de oveja o leche de cabra 100 tests ZEU-INMUNOTEC S.L. María
Immunocromatographic test to detect cow s milk in sheep or goat s milk Test inmunocromatográfico para la detección de leche de vaca en leche de oveja o leche de cabra 100 tests ZEU-INMUNOTEC S.L. María
centrífuga refrigerada
 centrífuga refrigerada 02 Centrífuga de sobremesa de alta velocidad con sistema de refrigeración integrado de gran utilidad en laboratorios de Biotecnología, Microbiología, Bioquímica, Biomedicina o Biología
centrífuga refrigerada 02 Centrífuga de sobremesa de alta velocidad con sistema de refrigeración integrado de gran utilidad en laboratorios de Biotecnología, Microbiología, Bioquímica, Biomedicina o Biología
Sabes cuanto deja tu negocio?: Completa guia Pymes y emprendedores (Spanish Edition)
 Sabes cuanto deja tu negocio?: Completa guia Pymes y emprendedores (Spanish Edition) Leo Socolovsky Click here if your download doesn"t start automatically Sabes cuanto deja tu negocio?: Completa guia
Sabes cuanto deja tu negocio?: Completa guia Pymes y emprendedores (Spanish Edition) Leo Socolovsky Click here if your download doesn"t start automatically Sabes cuanto deja tu negocio?: Completa guia
NO VACÍO SERIES DE GRAVEDAD MÉTODO GV-65 PARA EL ANALISIS DE PENCICLIDINA (PCP) EN ORINA POR GC/MS.
 NO VACÍO SERIES DE GRAVEDAD MÉTODO GV-65 PARA EL ANALISIS DE PENCICLIDINA (PCP) EN ORINA POR GC/MS. Aunque este método ha dado buenos resultados en nuestro laboratorio. Este tiene que ser validado por
NO VACÍO SERIES DE GRAVEDAD MÉTODO GV-65 PARA EL ANALISIS DE PENCICLIDINA (PCP) EN ORINA POR GC/MS. Aunque este método ha dado buenos resultados en nuestro laboratorio. Este tiene que ser validado por
All written implementation materials are provided in both English and Spanish. The Employee MPN Information packet includes the following documents:
 Dear Employer, Your company has elected to participate in the Medical Provider Network (MPN) Program, which is the MPN utilized by Hanover Insurance Company for workers compensation. This letter is designed
Dear Employer, Your company has elected to participate in the Medical Provider Network (MPN) Program, which is the MPN utilized by Hanover Insurance Company for workers compensation. This letter is designed
WOW SECOND SKIN INSTALLATION GUIDE. Steps and recommendations to install and enhance your Second Skin product. WOW SECOND SKIN GUÍA DE INSTALACIÓN
 WOW SECOND SKIN INSTALLATION GUIDE Steps and recommendations to install and enhance your Second Skin product. WOW SECOND SKIN GUÍA DE INSTALACIÓN Pasos y recomendaciones para instalar y ensalzar Second
WOW SECOND SKIN INSTALLATION GUIDE Steps and recommendations to install and enhance your Second Skin product. WOW SECOND SKIN GUÍA DE INSTALACIÓN Pasos y recomendaciones para instalar y ensalzar Second
PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR
 PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR FUNDAMENTO TEÓRICO Para estudiar la estructura y/o las funciones metabólicas de los distintos compartimentos celulares hay que aislarlos del resto de los orgánulos.
PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR FUNDAMENTO TEÓRICO Para estudiar la estructura y/o las funciones metabólicas de los distintos compartimentos celulares hay que aislarlos del resto de los orgánulos.
El Jardín de la Memoria (El adepto de la Reina nº 2) (Spanish Edition)
 El Jardín de la Memoria (El adepto de la Reina nº 2) (Spanish Edition) Rodolfo Martínez Click here if your download doesn"t start automatically Download and Read Free Online El Jardín de la Memoria (El
El Jardín de la Memoria (El adepto de la Reina nº 2) (Spanish Edition) Rodolfo Martínez Click here if your download doesn"t start automatically Download and Read Free Online El Jardín de la Memoria (El
MANUAL DE FARMACIA CLINICA Y ATENCION FARMACEUTICA. EL PRECIO ES EN DOLARES BY JOAQUIN HERRERA CARRANZA
 MANUAL DE FARMACIA CLINICA Y ATENCION FARMACEUTICA. EL PRECIO ES EN DOLARES BY JOAQUIN HERRERA CARRANZA DOWNLOAD EBOOK : MANUAL DE FARMACIA CLINICA Y ATENCION HERRERA CARRANZA PDF Click link bellow and
MANUAL DE FARMACIA CLINICA Y ATENCION FARMACEUTICA. EL PRECIO ES EN DOLARES BY JOAQUIN HERRERA CARRANZA DOWNLOAD EBOOK : MANUAL DE FARMACIA CLINICA Y ATENCION HERRERA CARRANZA PDF Click link bellow and
WebForms con LeadTools
 WebForms con LeadTools 21.01.2007 Danysoft Con la aparición de la version 15 de LEADTOOLS, LEAD ha incluido un control.net para la gestión de formularios en la Web. A continuación le incluimos unas instrucciones
WebForms con LeadTools 21.01.2007 Danysoft Con la aparición de la version 15 de LEADTOOLS, LEAD ha incluido un control.net para la gestión de formularios en la Web. A continuación le incluimos unas instrucciones
Michaelson Español 1
 Michaelson Español 1 English Grammar Connection: indicate Subject Pronouns who is being described or who does the action in a sentence. Yo = I Tú =You (familiar) Él = He Ella = She Usted =You (formal)
Michaelson Español 1 English Grammar Connection: indicate Subject Pronouns who is being described or who does the action in a sentence. Yo = I Tú =You (familiar) Él = He Ella = She Usted =You (formal)
Preparación y Caracterización de Ácidos Nucleicos
 Práctico Nº 5. Ácidos Nucleicos I Preparación y Caracterización de Ácidos Nucleicos Facultad de Ciencias Bioquímica (Licenciatura en Ciencias Biológicas) Objetivos Laboratorio Ácidos Nucleicos I: Extracción
Práctico Nº 5. Ácidos Nucleicos I Preparación y Caracterización de Ácidos Nucleicos Facultad de Ciencias Bioquímica (Licenciatura en Ciencias Biológicas) Objetivos Laboratorio Ácidos Nucleicos I: Extracción
Operaciones y procesos en los servicios de bar y cafeteria (Spanish Edition)
 Operaciones y procesos en los servicios de bar y cafeteria (Spanish Edition) Roser Vives Serra, Gonzalo Herrero Arroyo Click here if your download doesn"t start automatically Operaciones y procesos en
Operaciones y procesos en los servicios de bar y cafeteria (Spanish Edition) Roser Vives Serra, Gonzalo Herrero Arroyo Click here if your download doesn"t start automatically Operaciones y procesos en
Natural Sciences 3. Module 3: Matter (Materia.)
 Natural Sciences 3 Module 3: Matter (Materia.) Matter. (Materia.) Matter is everything that exists. (Materia es todo aquello que existe.) All living things and non-living things are made of matter. (Todos
Natural Sciences 3 Module 3: Matter (Materia.) Matter. (Materia.) Matter is everything that exists. (Materia es todo aquello que existe.) All living things and non-living things are made of matter. (Todos
Might. Área Lectura y Escritura. In order to understand the use of the modal verb might we will check some examples:
 Might Área Lectura y Escritura Resultados de aprendizaje Conocer el uso del verbo modal might. Aplicar el verbo modal might en ejercicios de escritura. Contenidos 1. Verbo modal might. Debo saber - Verbos
Might Área Lectura y Escritura Resultados de aprendizaje Conocer el uso del verbo modal might. Aplicar el verbo modal might en ejercicios de escritura. Contenidos 1. Verbo modal might. Debo saber - Verbos
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
Los nombres originales de los territorios, sitios y accidentes geograficos de Colombia (Spanish Edition)
 Los nombres originales de los territorios, sitios y accidentes geograficos de Colombia (Spanish Edition) Click here if your download doesn"t start automatically Los nombres originales de los territorios,
Los nombres originales de los territorios, sitios y accidentes geograficos de Colombia (Spanish Edition) Click here if your download doesn"t start automatically Los nombres originales de los territorios,
INSTALLATION INSTRUCTIONS
 Brix Ratio Check Instructions for ColdFusion and Flavor Overload Units INSTALLATION INSTRUCTIONS Brix Ratio Check Instructions For Coldfusion, Flavorfusion and Flavor Overload Units Kit P/N 629096865 SAFETY
Brix Ratio Check Instructions for ColdFusion and Flavor Overload Units INSTALLATION INSTRUCTIONS Brix Ratio Check Instructions For Coldfusion, Flavorfusion and Flavor Overload Units Kit P/N 629096865 SAFETY
Universal aftermarket speaker installation kit
 INSTALLATION INSTRUCTIONS FOR PART 82-4600 APPLICATIONS Universal aftermarket speaker installation kit 82-4600 KIT FEATURES Provides spacing for 6-1/2 aftermarket speaker installation. KIT COMPONENTS A)
INSTALLATION INSTRUCTIONS FOR PART 82-4600 APPLICATIONS Universal aftermarket speaker installation kit 82-4600 KIT FEATURES Provides spacing for 6-1/2 aftermarket speaker installation. KIT COMPONENTS A)
Most Wanted Products
 Most Wanted Products Purificación de ADN, ARN y proteínas MACHEREY-NAGEL Guía de productos destacados MN La solución perfecta para cada aplicación Kits de purificación en formato de columna Máxima calidad
Most Wanted Products Purificación de ADN, ARN y proteínas MACHEREY-NAGEL Guía de productos destacados MN La solución perfecta para cada aplicación Kits de purificación en formato de columna Máxima calidad
Flashcards Series 1 Saludos y Despedidas
 Flashcards Series 1 Saludos y Despedidas Flashcards are one of the quickest and easiest ways to test yourself on Spanish vocabulary, no matter where you are! Setting Up Print this file. (In Adobe Acrobat,
Flashcards Series 1 Saludos y Despedidas Flashcards are one of the quickest and easiest ways to test yourself on Spanish vocabulary, no matter where you are! Setting Up Print this file. (In Adobe Acrobat,
Level 1 Spanish, 2016
 90911 909110 1SUPERVISOR S Level 1 Spanish, 2016 90911 Demonstrate understanding of a variety of Spanish texts on areas of most immediate relevance 2.00 p.m. Thursday 24 November 2016 Credits: Five Achievement
90911 909110 1SUPERVISOR S Level 1 Spanish, 2016 90911 Demonstrate understanding of a variety of Spanish texts on areas of most immediate relevance 2.00 p.m. Thursday 24 November 2016 Credits: Five Achievement
Nuevas perspectivas en el diagnóstico de Clostridium difficile. Evelyn Rodríguez Cavallini
 Nuevas perspectivas en el diagnóstico de Clostridium difficile Evelyn Rodríguez Cavallini Pruebas diagnósticas Detectan productos de C. difficile Métodos de cultivo Detección de genes o deleciones GDH
Nuevas perspectivas en el diagnóstico de Clostridium difficile Evelyn Rodríguez Cavallini Pruebas diagnósticas Detectan productos de C. difficile Métodos de cultivo Detección de genes o deleciones GDH
Los números. 0 cero 1 uno / un 2 dos 3 tres 4 cuatro. 6 seis 7 siete 8 ocho 9 nueve 10 diez 5 cinco
 53 31 16 0 cero 1 uno / un 2 dos 3 tres 4 cuatro 6 seis 7 siete 8 ocho 9 nueve 10 diez 5 cinco 11 - once 12 - doce 13 - trece 14 - catorce 17 - diecisiete 18 - dieciocho 19 - diecinueve 20 - veinte 15
53 31 16 0 cero 1 uno / un 2 dos 3 tres 4 cuatro 6 seis 7 siete 8 ocho 9 nueve 10 diez 5 cinco 11 - once 12 - doce 13 - trece 14 - catorce 17 - diecisiete 18 - dieciocho 19 - diecinueve 20 - veinte 15
Pregunta 1 Suponga que una muestra de 35 observaciones es obtenida de una población con media y varianza. Entonces la se calcula como.
 Universidad de Costa Rica Programa de Posgrado en Computación e Informática Doctorado en Computación e Informática Curso Estadística 18 de febrero 2013 Nombre: Segundo examen corto de Probabilidad Pregunta
Universidad de Costa Rica Programa de Posgrado en Computación e Informática Doctorado en Computación e Informática Curso Estadística 18 de febrero 2013 Nombre: Segundo examen corto de Probabilidad Pregunta
Real Colegio Alfonso XII Padres Agustinos
 REVIEW ACTIVITIES (TECHNOLOGY; 3º ESO) A. Electricity 1. What is the force between two charges of 2 μc and 3 μc placed 5 mm apart. (K = 9 10 9 N m 2 C 2 ) 2. Two identical charges placed at a distance
REVIEW ACTIVITIES (TECHNOLOGY; 3º ESO) A. Electricity 1. What is the force between two charges of 2 μc and 3 μc placed 5 mm apart. (K = 9 10 9 N m 2 C 2 ) 2. Two identical charges placed at a distance
