PRESENTACIÓN DE LA ASIGNATURA:
|
|
|
- Celia Villalobos Correa
- hace 6 años
- Vistas:
Transcripción
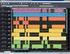
1 UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIOS NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL CUATRIMESTRAL Enfoque Educativo Basado en el Desarrollo de Competencias MODALIDAD ASIGNATURA TIPO DE CICLO ÁREA DISCIPLINAR ESCOLARIZADA QUÍMICA I CUATRIMESTRAL CICLO PRIMERO CIENCIAS EXPERIMENTALES COMPONENTE DE FORMACIÓN OPCIÓN EDUCATIVA TOTAL DE CRÉDITOS HORAS A LA SEMANA BÁSICO PRESENCIAL 10 5 HORAS TOTALES FECHA DE ELABORACIÓN 65 AGOSTO 2013 PRESENTACIÓN DE LA ASIGNATURA: A continuación se presenta el programa de estudios de la asignatura de Química I. Este campo de conocimiento, que forma parte del área de Ciencias Experimentales, tiene la finalidad de que el estudiante conozca y aplique los métodos y procedimientos de las ciencias experimentales para la resolución de problemas cotidianos y la compresión racional de su entorno, mediante procesos de razonamiento, argumentación y estructuración de ideas que conlleven el despliegue de distintos conocimientos, habilidades, actitudes y valores, en la resolución de problemas que trasciendan el ámbito escolar; para seguir lo anterior se establecieron las competencias disciplinares básicas del campo de las ciencias experimentales, mismas que han servido de guía para la actualización del presente programa. La asignatura de Química I es la primera de las dos que forman parte del campo de las ciencias experimentales, y su antecedente son las Ciencias (con énfasis en Química) de la educación básica (secundaria). Durante la secundaria, se buscó que los estudiantes consolidaran su formación en las ciencias básicas potenciando su desarrollo cognitivo, afectivo y de valores, invitándolos a la reflexión, la crítica, la investigación y la curiosidad. También contribuyó a ampliar su concepción de las ciencias y su interacción con otras áreas del conocimiento, valorar el impacto ambiental y social que generan las actividades humanas al aplicar las ciencias, pero a su vez valorar las contribuciones de la ciencia al mejoramiento de la calidad de vida, tanto de las personas como de la sociedad en su conjunto. En el bachillerato, se busca consolidar y diversificar los aprendizajes y desempeños adquiridos, ampliando y profundizando los conocimientos, habilidades, actitudes y valores relacionados con el campo de las ciencias experimentales, promoviendo en Química I, el reconocimiento de esta ciencia como parte importante de su vida diaria y como una herramienta para resolver problemas del mundo que nos rodea, implementando el método científico como un elemento indispensable en la resolución y exploración de éstos, con la finalidad de contribuir al desarrollo humano y científico. La relación de la Química con la tecnología y la sociedad, y el impacto que ésta genera en el medio ambiente, buscando generar en el estudiante una conciencia de cuidado y preservación del medio que lo rodea así como un accionar ético y responsable del manejo de los recursos naturales para su generación y las generaciones futuras. En la siguiente figura, se muestra la relación de Química I con otras asignaturas del 2013 por la Universidad del Valle de México. Este documento fue elaborado en la Dirección Académica de Preparatoria de la UVM. Página 1 de 35
2 bachillerato cuatrimestral. QUÍMICA II MATEMÁTICAS FÍSICA I Y II QUÍMICA I GEOGRAFÍA BIOLOGIA I Y II ECOLOGÍA Y MEDIOAMBIENTE Gráfico 1. Relación de la asignatura con otras del MCC que asegura el trabajo interdisciplinario. Se consideran todas las competencias disciplinares y genéricas señaladas en el programa de estudios oficial. En cada bloque se desarrollan las competencias disciplinares establecidas. En el caso de las competencias genéricas, se desarrollan todos los atributos correspondientes a cada bloque dándoles un tratamiento y peso diferenciado, de tal manera que los atributos con mayor frecuencia en todos los bloques de la asignatura, aparecen en la gráfica denominada Matriz de competencias disciplinares y genéricas por bloque y, el resto de atributos se desarrollan en las estrategias de enseñanza-aprendizaje propuestas para cada bloque. Cabe señalar que la UVM concibe como una institución que, de manera integral, educa con un equilibrio entre los enfoques científico-tecnológicos y ético-cultural, acordes con las necesidades sociales, la búsqueda de la verdad y el bien común, de ahí la importancia de que la presente asignatura coadyuve al logro del perfil de egreso de nuestros estudiantes de bachillerato. Definir el perfil del egresado en términos de desempeño terminales tiene la ventaja de que proporciona el marco común del bachillerato a partir de distintos desarrollos curriculares, sin forzar troncos comunes a asignaturas obligatorias, conciliando los propósitos de alcanzar lo común y al mismo tiempo respetar la necesaria diversidad. Los atributos del egresado de la Preparatoria UVM son: -Se comunica con confianza y eficiencia en español e inglés de manera escrita -Usa eficientemente la tecnología de la información y comunicación -Desarrolla un pensamiento lógico-matemático en la solución de problemas -Se identifica como un ciudadano global 2013 por la Universidad del Valle de México. Este documento fue elaborado en la Dirección Académica de Preparatoria de la UVM. Página 2 de 35
3 -Reconoce, y valora y respeta la diversidad -Favorece un estilo de vida saludable e integral de sí mismo y de su entorno -Cuenta con una formación como Asistente Administrativo. Nota: Se consideran las competencias genéricas y disciplinares señaladas en el programa de estudios oficial de la Dirección General de Bachillerato (SEP). En el caso de las competencias genéricas, se desarrollan los atributos correspondientes a cada bloque, dándoles un tratamiento y peso diferenciado, de tal manera que los atributos con mayor frecuencia (70%) en todos los bloques de la asignatura aparecen en la gráfica denominada matriz de competencias por bloque. En cada bloque se desarrollan las competencias disciplinares establecidas bajo los criterios de proximidad, frecuencia y complejidad. El resto de atributos se desarrollan en las estrategias de enseñanza-aprendizaje propuestas para cada bloque. BLOQUES CORRESPONDIENTES A LA ASIGNATURA: NÚMERO DE BLOQUE I II III IV V VI VII VIII NOMBRE DEL BLOQUE Reconoce a la Química como una herramienta para la vida. Comprende la interrelación de la materia y la energía. Explica el modelo atómico actual y sus aplicaciones. Interpreta la Tabla Periódica. Interpreta enlaces químicos e interacciones intermoleculares. Maneja la nomenclatura Química inorgánica. Representa y opera reacciones químicas. Comprende los procesos asociados con el calor y la velocidad de las reacciones químicas por la Universidad del Valle de México. Este documento fue elaborado en la Dirección Académica de Preparatoria de la UVM. Página 3 de 35
4 MATRIZ DE COMPETENCIAS GENÉRICAS Y DISCIPLINARES BÁSICAS (DE ACUERDO A SU PROXIMIDAD, FRECUENCIA Y COMPLEJIDAD) COMPETENCIAS GENÉRICAS (ATRIBUTOS) 3.2 Toma decisiones a partir de la valoración de las consecuencias de distintos hábitos de consumo y conductas de riesgo. COMPETENCIAS DISCIPLINARES BÁSICAS CE-1. Establece la interrelación entre la ciencia, la tecnología, la sociedad y el ambiente en contextos históricos y sociales específicos. I BLOQUES II III IV V VI VII VIII CE-2. Fundamenta opiniones sobre los impactos de la ciencia y la tecnología en su vida cotidiana, asumiendo consideraciones éticas. x x CE-12. Decide sobre el cuidado de su salud a partir del conocimiento de su cuerpo, sus procesos vitales y el entorno al que pertenece. CE-11. Analiza las leyes generales que rigen el funcionamiento del medio físico y valora las acciones humanas de riesgo e impacto ambiental. CE-10. Relaciona las expresiones simbólicas de un fenómeno de la naturaleza y los rasgos observables a simple vista o mediante instrumentos o modelos científicos. BLOQUES II III IV V VI VII VIII 5.6 Utiliza las tecnologías de la información y comunicación para procesar e interpretar información. x x 8.3 Asume una actitud constructiva, congruente con los conocimientos y habilidades con los que cuenta dentro de distintos equipos de trabajo. x x x x x x x x x x x x x CE-9. Diseña modelos o prototipos para resolver problemas, satisfacer necesidades. x x x x x I x x x x 5.2 Ordena información de acuerdo a categorías, jerarquías y relaciones. x x x 7.1 Define metas y da seguimiento a sus procesos de construcción de conocimientos. x x x 8.1 Propone manera de solucionar un problema y desarrolla un proyecto en equipo, definiendo un curso de acción con pasos específicos. x x x x 5.4 Construye hipótesis y diseña y aplica modelos para probar su validez. x x x x x 5.3 Identifica los sistemas y reglas o principios medulares que subyacen a una serie de fenómenos. x x x x x x 6.1 Elige las fuentes de información más relevantes para un propósito específico y discrimina entre ellas de acuerdo a su relevancia y confiabilidad. x x x x x x x 8.2 Aporta puntos de vista con apertura y considera los de otras personas de manera reflexiva. x x x x x x x 5.1 Sigue instrucciones y procedimientos de manera reflexiva, comprendiendo cómo cada uno de sus pasos contribuye al alcance de un objetivo. x x x x x x x x 2013 por la Universidad del Valle de México. Este documento fue elaborado en la Dirección Académica de Preparatoria de la UVM. Página 4 de 35
5 COMPETENCIAS DISCIPLINARES BÁSICAS CE-7. Explicita las nociones científicas que sustentan los procesos para la solución de problemas cotidianos. CE-5. Contrasta los resultados obtenidos en una investigación o experimento con hipótesis previas y comunica sus conclusiones. CE-4. Obtiene, registra y sistematiza la información para responder a preguntas de carácter científico, consultando fuentes relevantes y realizando experimentos pertinentes. CE-3. Identifica problemas, formula preguntas de carácter científico y plantea las hipótesis necesarias para responderlas. CE-14. Aplica normas de seguridad en el manejo de sustancias, instrumentos y equipo en la realización de actividades de su vida cotidiana. BLOQUES I II III IV V VI VII VIII x x x x x x x x x x x x x x x x x x x x x x x x x x x x x x x x x X Se Desarrolla O Se Fortalece 2013 por la Universidad del Valle de México. Este documento fue elaborado en la Dirección Académica de Preparatoria de la UVM. Página 5 de 35
6 Atributos de las Competencias Genéricas No. DE BLOQUE: I TÍTULO: Reconoce a la Química como una herramienta para la vida. NÚMERO DE HORAS: 10* RESULTADO DE APRENDIZAJE: El estudiante es competente cuando reconoce a la Química como parte de su vida cotidiana, tras conocer el progreso que ha tenido esta a través del tiempo y la forma en que ha empleado el método científico para resolver problemas del mundo que nos rodea, así como su relación con otras ciencias, que conjuntamente han contribuido al desarrollo de la humanidad. Competencias Disciplinares Básicas Bloque I CE-14 CE-3 CE-4 CE-5 CE-7 CE-9 CE-10 CE-11 CE-12 CE-2 CE *DISTRIBUCIÓN DE TIEMPO Apertura Desarrollo Cierre 1 h 8 h 1 h 2013 por la Universidad del Valle de México. Este documento fue elaborado en la Dirección Académica de Preparatoria de la UVM. Página 6 de 35
7 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** 1 1- Explica el concepto de Química y sus aplicaciones, utilizando ejemplos reales de su vida cotidiana. 2- Relata los momentos trascendentales que ha vivido el desarrollo de la Química, a través del tiempo. CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES 1. Comprende el concepto de Química. 1. Reconoce los grandes momentos del desarrollo de la Química. 1. Expresa la importancia que tiene la Química, ubicando las aplicaciones de ésta en sus actividades cotidianas. Da seguimiento a procesos de construcción de conocimientos 1.Valora las aplicaciones de la Química en su vida cotidiana y en el desarrollo de la humanidad. 1. Valora las aplicaciones de la Química en su vida cotidiana y en el desarrollo de la humanidad. 2. Desarrolla un sentido de responsabilidad y compromiso al reconocer que la Química se aplica de manera permanente en su vida diaria. Apertura: El docente realiza el encuadre de la asignatura. Desarrollo: 1. Situación didáctica: Analiza dibujos y discute quién hace química y en qué. 2. Situación didáctica: Análisis de la lectura Recorrido histórico de una página web indicada en el manual. EVIDENCIAS DEL LOGRO - Conclusión del análisis de imágenes y propuesta de 5 ejemplos - Línea de tiempo citando los eventos históricos trascendentales en el desarrollo de la química. CONOCIMIENTOS Oral Escrito Expositivo HABILIDADES Y ACTITUDES Rúbrica Guía de observación Lista de cotejo Portafolio Semana 2 3- Establece la relación de la Química con las Matemáticas, Física y Biología, utilizando ejemplos reales de su vida cotidiana. 4- Explica la forma *1. Definición de Física, definición de Matemáticas y definición de Biología. 1. Reconoce los pasos del método Científico. 1. Relaciona a la Química con otras ciencias, como las Matemáticas, la Física y la Biología, entre otras. 1. Aplica los 1. Valora las aplicaciones de la Química en su vida cotidiana y en el desarrollo de la humanidad. 1. Muestra interés por aplicar el método científico a los problemas que se 3. Análisis de la ficha técnica de una Aspirina. - Mapa conceptual - Propuesta de 2 ejemplos relacionando a la química con matemáticas, física y biología por la Universidad del Valle de México. Este documento fue elaborado en la Dirección Académica de Preparatoria de la UVM. Página 7 de 35
8 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** en que el método científico ha ayudado a la Química en la resolución de problemas. 5- En un nivel incipiente, observa y analiza un fenómeno, hecho o situación de la vida cotidiana; formula una hipótesis, experimenta y obtiene las conclusiones correspondientes. CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES 1.1 Identificación de problemas y formulación de preguntas de carácter científico. 1.2 Planteamiento de hipótesis 1.3Obtención y registro de información. 1.4 Experimentación. 1.5 Contrastación de resultados. 1.6 Comunicación de las conclusiones. *1. Identifica los sistemas y reglas o principios medulares que subyacen a una serie de fenómenos. *2. Construye hipótesis y diseña y aplica modelos para probar su validez. pasos del método científico en la resolución de problemas del campo de la Química. Aplica los pasos del método científico en la resolución de problemas del campo de la Química. Desarrolla actividades experimentales y/o de campo, siguiendo los pasos del método científico. le presenten y como herramienta para comprender diversos fenómenos y hechos de la naturaleza. Muestra interés por participar en actividades experimentales y/o de campo. Promueve el trabajo metódico y organizado. Cierre: 1. Propuesta de fenómeno o hecho natural. El estudiante lo explica utilizando los pasos del método científico. EVIDENCIAS DEL LOGRO Reporte de investigación. CONOCIMIENTOS HABILIDADES Y ACTITUDES **Los instrumentos de evaluación debo seleccionarlos de acuerdo a los criterios de la evaluación cualitativa que deseo observar en el desempeño de mis estudiantes a partir de la evidencias de logro por la Universidad del Valle de México. Este documento fue elaborado en la Dirección Académica de Preparatoria de la UVM. Página 8 de 35
9 Atributos de las Competencias Genéricas No. DE BLOQUE: II TÍTULO: Comprende las interacciones de la materia y la energía. NÚMERO DE HORAS: 10* RESULTADO DE APRENDIZAJE: El estudiante es competente cuando establece la relación que existe entre de las propiedades de la materia y los cambios que se dan en ella, por efectos de la energía. Asimismo, valora los beneficios y riesgos que tiene utilizar la energía en su vida cotidiana y el medio ambiente. Competencias Disciplinares Básicas Bloque II CE-14 CE-3 CE-4 CE-5 CE-7 CE-9 CE-10 CE-11 CE-12 CE-2 CE *DISTRIBUCIÓN DE TIEMPO Apertura Desarrollo Cierre 1 h 8 h 1 h Página 9 de 35
10 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES Semana 3 1.Explica las propiedades y estados de agregación de la materia de las sustancias que observa en su entorno cotidiano. 1.Reconoce las propiedades de la materia: extensivas e intensivas, Físicas y Químicas. 1.Explica el concepto de materia. 2.Caracteriza los estados de agregación y sus cambios en los fenómenos que observa en su entorno. Apertura: 1.Situación didáctica. Relación de los estados de agregación con sus características. - Relación correcta de las palabras con los estados de agregación. Oral Escrito Expositivo Rúbrica Guía de observación Lista de cotejo Semana 4 2.Reconoce en su entorno la presencia de diversos tipos de energía, identificando sus características e interrelación. 3.Explica la forma en que la energía provoca cambios en la materia. 1.Describe las características de los diferentes tipos de energía y su interrelación. Cinética. Potencial. Luminosa. Calorífica. Química. Eólica. 1.Describe las características de los cambios físicos, químicos y nucleares de la materia. 1.Expresa algunas aplicaciones de los cambios físicos, químicos y nucleares. 1.*Expresa algunas 1.Aprecia las distintas energías que existen en la naturaleza y que existen otras fuentes de energía. Desarrollo: 1.Situación didáctica. Análisis de imágenes y el tipo de energía que representan. - Conclusión del análisis de imágenes y propuesta de ejemplos. Portafolio 4.Aplicando el método científico, desarrolla 1.*Describe las características de los cambios físicos y aplicaciones que impliquen cambios físicos y químicos. 1. Manifiesta interés por el trabajo 1.Cátedra experimental de un cambio físico y un cambio químico. - Documento con la selección correcta del Página 10 de 35
11 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES experimentos sobre propiedades Físicas, estados de agregación y cambios que presenta la materia. 5.Valora los beneficios y riesgos en el consumo de la energía. 6.Argumenta los riesgos y beneficios del uso de la energía en su vida cotidiana y en especial en el medio ambiente. químicos de la materia. 1.Distingue entre las fuentes de energías limpias y las contaminantes. 1.Argumenta la importancia que tienen las energías limpias en el cuidado del medio ambiente. ordenado en el laboratorio y el cuidado con su persona y el material dado. 1. Promueve el uso responsable de la energía junto con el uso de energías limpias. 1.Promueve el uso responsable de la materia para el cuidado del medio ambiente. 2. Situación didáctica. Elegir el tipo de cambio de las actividades mostradas y fundamentar su respuesta. Cierre: 1.Situación didáctica. Fuentes alternativas de energía. Las otras opciones. tipo de cambio y su explicación. - Resolución de un cuestionario de opciones múltiples. **Los instrumentos de evaluación debo seleccionarlos de acuerdo a los criterios de la evaluación cualitativa que deseo observar en el desempeño de mis estudiantes a partir de la evidencias de logro. Página 11 de 35
12 Atributos de las Competencias Genéricas No. DE BLOQUE: III TÍTULO: Explica el modelo atómico actual y sus aplicaciones. NÚMERO DE HORAS: 10* RESULTADO DE APRENDIZAJE: El estudiante es competente cuando valora las aportaciones históricas de diversos modelos atómicos al describir la estructura del átomo, reconocer sus propiedades nucleares y electrónicas, así como las aplicaciones de elementos radiactivos en su vida personal y social. Competencias Disciplinares Básicas Bloque III CE-14 CE-3 CE-4 CE-5 CE-7 CE-9 CE-10 CE-11 CE-12 CE-2 CE-1 *DISTRIBUCIÓN DE TIEMPO Apertura Desarrollo Cierre 1 h 8 h 1 h Página 12 de 35
13 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES Semana 5 Semana 6 1.Relata las aportaciones de Dalton, Thomson, Rutherford, Chadwick, Goldstein, Bohr, Sommerfeld y Dirac- Jordan como parte de un proceso histórico que desemboca en el modelo atómico actual. 2.Describe la masa, carga y ubicación de las partículas subatómicas (electrón, protón y neutrón). 3.Diseña modelos con materiales diversos para representar la estructura del átomo. 4.Identifica el número atómico, masa atómica y número de masa de cualquier elemento de la Tabla Periódica. 5.Representa la configuración electrónica de un átomo y su 1.Describe las aportaciones al modelo atómico actual realizadas por Dalton, Thomson, Rutherford, Chadwick, Goldstein, Bohr, Sommerfeld y Dirac-Jordan. 1.Reconoce las partículas subatómicas y sus características más relevantes. 1.*Comprende la importancia de los diversos modelos y su evolución al modelo actual. 1.Define los conceptos de número atómico, masa atómica y número de masa. 1.Establece la relación entre número atómico, masa atómica y número de masa. 1.Realiza cálculos sencillos relacionados con partículas subatómicas, tomando como base el número atómico, la masa 1.Valora las aportaciones históricas de los modelos atómicos que nos llevan al modelo actual. 1.Muestra disposición al trabajo metódico y organizado. Apertura: 1.Situación didáctica. Las leyes y sus modelos atómicos y sus autores. - Relaciona correctamente los modelos atómicos con sus autores. Desarrollo: 1.Situación didáctica. Tabla que relaciona las partículas subatómicas con su carga, masa relativa y ubicación en el átomo. - Identifica las diferencias de masa y ubicación de las partículas subatómicas. 1. Situación didáctica. Cálculo del número de protones, neutrones y electrones mediante la fórmula N = A-Z. Cuadro sinóptico Tabla - Oral Escrito Expositivo Rúbrica Guía de observación Lista de cotejo Portafolio Página 13 de 35
14 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES diagrama energético, aplicando el principio de exclusión de Pauli, la regla de Hund y el principio de edificación progresiva. 6.Identifica los electrones de valencia en la configuración electrónica de los elementos, y su relación con las características de éstos. 7.Reflexiona sobre las aplicaciones de los isótopos en las actividades humanas. 1.Describe los significados y valores de los números cuánticos (n, l, m, s). 2.Explica las reglas para elaborar las configuraciones electrónicas: Principio de edificación progresiva, Principio de exclusión de Pauli y Regla de Hund. 1.Define el concepto de isótopo. 2.Conoce algunos isótopos radiactivos: Cobalto-60 Yodo-131 Carbono-11 Carbono-14 Plomo-212 atómica y el número de masa. 1.Desarrolla e interpreta configuraciones electrónicas considerando los números cuánticos y los electrones de valencia de los elementos, relacionándolos con las características de los mismos. 1.Explica la relación existente entre el número atómico y el número de masa de los isótopos. 2.Describe las aplicaciones de algunos isótopos radiactivos. 3.Reconoce la importancia y los riesgos del 1.Valora las aplicaciones de los isótopos en la vida cotidiana. Señala la cantidad de protones, neutrones y electrones con la fórmula E. Cierre: A Z 1.Situación didáctica. Representación de los electrones de un átomo mediante la configuración electrónica e identificación de los electrones de valencia. - Indica, de acuerdo con el Principio de construcción progresiva el número de electrones en una serie de átomos y señala a los electrones de valencia. 1. Situación didáctica. Relevancia de algunos isótopos y sus distintas aplicaciones. Para realizar este ejercicio revisar la página web indicada en el manual. Relaciona los siguientes isótopos con sus principales usos. Representación - Ejercicio web. Página 14 de 35
15 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES empleo de isótopos en diferentes campos. **Los instrumentos de evaluación debo seleccionarlos de acuerdo a los criterios de la evaluación cualitativa que deseo observar en el desempeño de mis estudiantes a partir de la evidencias de logro. Página 15 de 35
16 Atributos de las Competencias Genéricas No. DE BLOQUE: IV TÍTULO: Interpreta la Tabla Periódica. NÚMERO DE HORAS: 10* RESULTADO DE APRENDIZAJE: El estudiante es competente cuando explica las propiedades y características de los grupos de elementos, considerando su ubicación en la Tabla Periódica, y promueve el manejo sustentable de los recursos minerales del país. Competencias Disciplinares Básicas Bloque IV CE-14 CE-3 CE-4 CE-5 CE-7 CE-9 CE-10 CE-11 CE-12 CE-2 CE *DISTRIBUCIÓN DE TIEMPO Apertura Desarrollo Cierre 1 h 8 h 1 h Página 16 de 35
17 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES CONOCIMIENTOS HABILIDADES Y ACTITUDES Semana 7 Semana 8 1.Identifica las propuestas y personajes más relevantes relacionados con el desarrollo de la tabla Periódica. 2.Relaciona la información que brinda la configuración electrónica con la ubicación de los elementos en la tabla Periódica y algunas de sus propiedades. 3.Clasifica los elementos de la Tabla Periódica en grupos, periodos y bloques s, p, d y f. 4.Establece las diferencias entre metales, no metales y metaloides y los ubica en la Tabla Periódica. 1.Describe los antecedentes históricos de la clasificación de los elementos químicos. 1.Reconoce las nociones de grupo, período y bloque, aplicadas a los elementos químicos. 1. Describe las propiedades de metales, no metales y semimetales. 1.Maneja la tabla Periódica para obtener información sobre las características y propiedades de los elementos. 1.Clasifica los elementos en metales, no metales y semimetales destacando sus características.. 1.*Valora las aportaciones históricas de las propuestas que nos llevan al modelo actual de tabla periódica. 1. *Valora la información que la organización de la tabla periódica ofrece. Apertura: 1.Situación didáctica. Relación de columnas de diversos modelos de tabla periódica con sus autores. - Relaciona correctamente los modelos atómicos con sus autores. Desarrollo: 1.Situación didáctica. Cómo está organizada la tabla periódica? - Escriben nombre y símbolo de elementos que conforman el 3 periodo e identifican metales y no metales y grupos I A y II A. Tabla Ejercicios Ejercicios Oral Escrito Expositivo Rúbrica Guía de observación Lista de cotejo Portafolio 5.Relaciona las propiedades periódicas (electronegatividad, energía de ionización, afinidad electrónica, radio y volumen 1.Describe las propiedades Periódicas (electronegatividad, energía de ionización, 1.Desarrolla, siguiendo el método científico, una práctica experimental en la que observe las propiedades 1. Situación didáctica. Dónde ubico a los metales, no metales y metaloides en la tabla periódica? - Identifican correctamente los metales, no metales y metaloides. Ejercicios Página 17 de 35
18 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES CONOCIMIENTOS HABILIDADES Y ACTITUDES atómico) con respecto a la ubicación de los elementos en la tabla. 6.Expresa cuáles metales, no metales o minerales participan significativamente en las actividades económicas del país, en su vida cotidiana y en el desempeño de los seres orgánicos. afinidad electrónica, radio y volumen atómico) y su variación en la Tabla Periódica. 1.Caracteriza la utilidad e importancia de los metales y no metales para la vida socioeconómica del País. de algunos elementos químicos y las asocia con la información que le brinda la tabla Periódica. 1.Argumenta los beneficios del manejo racional y sustentable de algunos elementos de relevancia económica. 1.Promueve el uso racional de los recursos minerales. 2.Reconoce problemas comunitarios relacionados con la explotación, tanto racional como irracional de recursos minerales. 3.Asume el reciclaje, como forma de resolver una problemática social. 4.Promueve el cuidado ambiental con relación al uso racional de elementos químicos de relevancia económica. Identifican correctamente por familia y periodo el orden de las distintas propiedades periódicas. 1.Situación didáctica. En qué orden se encuentran los elementos más electronegativos? Cierre: 1. Situación didáctica. Los minerales de mayor importancia económica en México. Reconoce los principales metales que se extraen en el país y su importancia económica (Plata, Oro, Carbón, entre otros). Mapa de la Republica Mexicana y su asociación con minerales. **Los instrumentos de evaluación debo seleccionarlos de acuerdo a los criterios de la evaluación cualitativa que deseo observar en el desempeño de mis estudiantes a partir de la evidencias de logro. Página 18 de 35
19 Atributos de las Competencias Genéricas No. DE BLOQUE: V TÍTULO: Interpreta enlaces químicos e interacciones intermoleculares. NÚMERO DE HORAS: 10* RESULTADO DE APRENDIZAJE: El estudiante es competente cuando distingue los diferentes modelos de enlaces interatómicos e intermoleculares, relacionando las propiedades macroscópicas de las sustancias con el tipo de enlace que presentan. 3.2 Competencias Disciplinares Básicas Bloque V CE-14 CE-3 CE-4 CE-5 CE-7 CE-9 CE-10 CE-11 CE-12 CE-2 CE *DISTRIBUCIÓN DE TIEMPO Apertura Desarrollo Cierre 1 h 8 h 1 h Página 19 de 35
20 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES Semana 9 1.Elabora representaciones de Lewis para diversos elementos químicos mostrando los electrones de valencia. 2.Realiza ejercicios en los que demuestra la formación del enlace iónico utilizando estructuras de Lewis. 3.Explica las características que debe tener un enlace covalente. 4.Desarrolla ejercicios en los que muestra la 1.Define el concepto de enlace químico. 2.Enuncia la regla del octeto. 1.Describe la formación del enlace iónico y las propiedades que presentan los compuestos con este tipo de enlace. 1.Define el concepto de enlace covalente. 1.Conoce las características de los diferentes tipos 1.Emplea la representación de Lewis para mostrar los electrones de valencia de un elemento químico. 1.Demuestra la formación de enlaces iónicos utilizando representaciones de Lewis. 2.Relaciona las características del enlace iónico con las propiedades macroscópicas de los compuestos. 1.Clasifica los diversos tipos de enlace covalente de acuerdo al número de electrones compartidos entre átomos. 1.Asocia la diferencia de electronegatividades con el tipo de enlace covalente. 2.Dibuja la 1.Valora la utilidad de los modelos teóricos utilizados para explicar la estructura de la materia. 1.Valora la importancia de los modelos teóricos para explicar las propiedades de las sustancias. 1.Valora la importancia de los enlaces químicos en la formación de nuevos materiales y su impacto en la sociedad. Apertura: 1.Situación didáctica. La estructura de Lewis, regla del octeto y su relación con los electrones de valencia - Identifica por familia el número de electrones de valencia. Desarrollo: 1. Situación didáctica. Relación de algunas sales inorgánicas con sus propiedades periódicas y físicas. - Identifica la formación de sales entre metales y no metales con estructuras de Lewis. 1.Situación didáctica. El agua y los gases en la naturaleza. Distintos tipos de enlace covalente. Ejercicios Ejercicios Oral Escrito Expositivo Rúbrica Guía de observación Lista de cotejo Portafolio Página 20 de 35
21 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES Semana 10 estructura de Lewis y la geometría molecular de compuestos covalentes. de enlace covalente. 1.Explica las propiedades de los compuestos covalentes. geometría molecular de compuestos sencillos, partiendo de la estructura de Lewis. 1.Utiliza las estructuras de Lewis para representar compuestos covalentes. - Reconocen los distintos tipos de enlace calculando la diferencia de electronegatividad (Δχ). - Revisión de cuestionario de la práctica. 5.Desarrolla experimentos con compuestos iónicos y covalentes para distinguir sus propiedades. 6.Explica qué es un enlace metálico, mediante el modelo de electrones libres y la teoría de bandas. 7.Explica las propiedades de los metales, a partir de las teorías del enlace metálico. 8.Explica las propiedades macroscópicas de los líquidos y gases, a partir de las fuerzas intermoleculares 1.Describe las teorías que explican el enlace metálico (teoría del mar de electrones y la teoría de bandas). 2.Reconoce las características que se derivan del enlace metálico. 1.Refiere la formación de las fuerzas intermoleculares Fuerzas de dispersión o fuerzas de London. Dipolo-dipolo. Dipolo-dipolo inducido. 1.Explica la importancia que tienen los metales en la economía de México. 1.Asocia las fuerzas intermoleculares con las propiedades que presentan los gases y los líquidos. 1.Describe la importancia de los puentes de hidrógeno en las propiedades de compuestos que forman parte de los seres vivos. 1.Valora el uso apropiado de los metales y su reciclaje. 1.Situación didáctica. Desarrollo de práctica en el Aula. 1.Situación didáctica. Por qué un metal es un buen conductor de electricidad? - Conclusión del análisis de imágenes y propuesta de 2 ejemplos. - Elaboración de cuestionario. Página 21 de 35
22 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES que los constituyen. 9.Describe el comportamiento químico del agua al desarrollar actividades experimentales con ella. 1.Identifica las características de los compuestos que presentan un puente de hidrógeno, especialmente la del agua y moléculas de importancia biológica. 1. Situación didáctica. Relación de imágenes gráficas con las fuerzas intermoleculares representativas. Cierre: 1. Situación didáctica. El caso del ADN y sus puentes de hidrógeno que le confieren su forma de doble hélice. **Los instrumentos de evaluación debo seleccionarlos de acuerdo a los criterios de la evaluación cualitativa que deseo observar en el desempeño de mis estudiantes a partir de la evidencias de logro. Página 22 de 35
23 Atributos de las Competencias Genéricas No. DE BLOQUE: VI TÍTULO: Maneja la nomenclatura Química inorgánica. NÚMERO DE HORAS: 5* RESULTADO DE APRENDIZAJE: El estudiante es cuando maneja el lenguaje de la Química inorgánica, identifica los compuestos de uso cotidiano y aplica las normas de seguridad necesarias para el manejo de productos químicos. 3.2 Competencias Disciplinares Básicas Bloque VI CE-14 CE-3 CE-4 CE-5 CE-7 CE-9 CE-10 CE-11 CE-12 CE-2 CE *DISTRIBUCIÓN DE TIEMPO Apertura Desarrollo Cierre 30 m 4 h 30 m Página 23 de 35
24 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES Semana 11 1.Resuelve ejercicios de nomenclatura Química donde a partir del nombre escribe la fórmula y viceversa, siguiendo las reglas establecidas por la UIQPA. 2.Desarrolla una práctica experimental en la que conoce las características de diversas sustancias para ubicarlas en el tipo de compuesto que le corresponde siguiendo las normas de seguridad que apliquen. 3.Muestra su habilidad en el reconocimiento de compuestos inorgánicos presentes en productos de uso cotidiano. 1. Describe las reglas establecidas por la UIQPA para escribir fórmulas y nombres de los compuestos químicos inorgánicos: Óxidos metálicos. Óxidos no metálicos. Hidruros metálicos. Hidrácidos. Hidróxidos. Oxiácidos. Sales. 1. Reconoce las propiedades de las sustancias que le permite ubicarla en un tipo de compuesto y qué medidas de seguridad deberá tener. 1.Resuelve ejercicios de nomenclatura Química inorgánica siguiendo las reglas establecidas por la UIQPA. 1.Identifica las fórmulas Químicas en productos de uso común. 1.Clasifica por la función Química los diferentes tipos de compuestos inorgánicos (óxidos, ácidos, bases y sales) de mayor uso. 1.Valora la utilidad del manejo del lenguaje de la Química. 1. Disposición al trabajo metódico y organizado. 2.Previene riesgos al utilizar con cuidado las sustancias Químicas que utiliza cotidianamente. Apertura: 1.Situación didáctica. La aplicación de las reglas UIQPA en la nomenclatura de compuestos inorgánicos. Desarrollo: 1. Realización de práctica en el laboratorio. Cierre: 1.Situación didáctica. Aplicación de reglas de nomenclatura para óxidos, ácidos, bases y sales inorgánicas mediante ejercicios. - Adquiere capacidad para identificar y nombrar diversos compuestos inorgánicos. - Resuelve correctamente ejercicios de nomenclatura siguiendo las reglas indicadas por la UIQPA. - Reporte de práctica y cuestionario. Oral Escrito Expositivo Rúbrica Guía de observación Lista de cotejo Portafolio **Los instrumentos de evaluación debo seleccionarlos de acuerdo a los criterios de la evaluación cualitativa que deseo observar en el desempeño de mis estudiantes a partir de la evidencias de logro. Página 24 de 35
25 Atributos de las Competencias Genéricas No. DE BLOQUE: VII TÍTULO: Representa y opera reacciones químicas. NÚMERO DE HORAS: 5* RESULTADO DE APRENDIZAJE: El estudiante es competente cuando reconoce a los procesos químicos como fenómenos de su entorno y demuestra la validez de la ley de la conservación de la materia al balancear ecuaciones químicas. Competencias Disciplinares Básicas Bloque VII CE-14 CE-3 CE-4 CE-5 CE-7 CE-9 CE-10 CE-11 CE-12 CE-2 CE-1 *DISTRIBUCIÓN DE TIEMPO Apertura Desarrollo Cierre 30 m 4 h 30 m Página 25 de 35
26 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES Semana 12 1.Resuelve ejercicios de Identificación del tipo de reacción: síntesis, descomposición, simple sustitución y doble sustitución. 2.Resuelve cuestionario y/o una colección de ejercicios donde complete ecuaciones Químicas, efectuando el balanceo correspondiente. 3.Argumenta los resultados de la Experimentación sobre reacciones redox. 4.Explica las reacciones Químicas que observa 1.Distingue entre las reacciones de síntesis, descomposición, sustitución simple y sustitución doble. 1.Reconoce el significado de los símbolos utilizados en la escritura de ecuaciones Químicas. 2.Conoce los métodos de balanceo de ecuaciones Químicas por tanteo y por óxido-reducción. 1.Explica los conceptos de oxidación y reducción, agente reductor, agente oxidante y número de oxidación. 1.Explicar la transformación de las sustancias, empleando ecuaciones Químicas. 1.Predice los productos de diferentes reacciones Químicas. 2.Demuestra la Ley de la Conservación de la Materia a partir del balanceo de ecuaciones. 1.Calcula el número de oxidación de los elementos que participan en una reacción Química tipo redox, determinando que elementos se oxidan y cuales 1.Valora la observación e Identificación experimental de los cambios químicos. 1.Valora la Ley de la Conservación de la Materia como principio fundamental de la Química Moderna. Valora las repercusiones positivas o negativas sobre el medio ambiente y la sociedad, provocadas por los procesos químicos. Apertura: 1.Situación didáctica. Relación del tipo de reacción química con su modelo de ecuación característico. - Identifica el tipo de reacción con su modelo y ofrece un ejemplo. Desarrollo: 1. Situación didáctica. Representación de diversas reacciones e identificación de sus componentes. - Aplica correctamente los métodos de balanceo de ecuaciones y señala los componentes de una ecuación química. 2.Situación didáctica. Balanceo de ecuaciones por tanteo y óxido-reducción. 1.Situación didáctica. Balanceo de ecuaciones por tanteo y óxido-reducción. Ejercicios - Revisión de ejercicios de balance de ecuaciones a través de participaciones. - Reporte de práctica y cuestionario Oral Escrito Expositivo Rúbrica Guía de observación Lista de cotejo Portafolio Página 26 de 35
27 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES en su entorno identificando cuales generan productos nocivos. 1 *Reconoce la importancia y cuidado que se debe tener con el manejo de sustancias en el laboratorio y en el hogar. se reducen. 2.Aplica el balanceo por el método de tanteo y óxido-reducción. 1.Aprecia la importancia de las reacciones de óxidoreducción en su entorno y en su organismo. 2. Realización de práctica en el laboratorio. - Resalta las reacciones redox y sus efectos directos en el organismo. Cierre: 1.Situación didáctica. Casos de reacciones redox en nuestro organismo. Lectura de 2 artículos cortos. Ejercicios **Los instrumentos de evaluación debo seleccionarlos de acuerdo a los criterios de la evaluación cualitativa que deseo observar en el desempeño de mis estudiantes a partir de la evidencias de logro. Página 27 de 35
28 Atributos de las Competencias Genéricas No. DE BLOQUE: VIII TÍTULO: Comprende los procesos asociados con el calor y la velocidad de las reacciones químicas. NÚMERO DE HORAS: 5* RESULTADO DE APRENDIZAJE: El estudiante es competente cuando reconoce la influencia de los factores que intervienen en la rapidez con que se llevan a cabo las reacciones químicas y la cantidad de calor que se intercambia cuando se desarrollan. Asimismo, valora la importancia del desarrollo sostenible y adopta una postura crítica y responsable ante el cuidado del medio ambiente. Competencias Disciplinares Básicas Bloque VIII 3.2 CE-14 CE-3 CE-4 CE-5 CE-7 CE-9 CE-10 CE-11 CE-12 CE-2 CE-1 *DISTRIBUCIÓN DE TIEMPO Apertura Desarrollo Cierre 30 h 4 h 30 h Página 28 de 35
29 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES Semana 13 Semana 13 1.Describe el concepto de entalpía de reacción, utilizándolo como criterio para distinguir entre reacciones endotérmicas y exotérmicas. 2.Resuelve ejercicios relacionados con la variación de la entalpía de reacción, identificando aquellas reacciones que son exotérmicas o endotérmicas. 3.Explica la forma en que algunos factores (naturaleza de los reactivos, tamaño de partícula, temperatura, presión, concentración, catalizadores) modifican la velocidad de reacción. 1.Explica los conceptos de entalpía de reacción y entalpía de formación. 1.Distingue entre reacciones químicas endotérmicas y reacciones químicas exotérmicas partiendo de los datos de entalpía de reacción. 1.Explica el concepto de velocidad de reacción. 1.Utilizando datos de tablas calcula la entalpía de reacción a partir de la entalpía de formación. 1.Identifica los factores que intervienen en la velocidad de una reacción química: naturaleza de los reactivos, tamaño de partícula, temperatura, presión, concentración y catalizadores. Asimismo, explica 1.Muestra interés por comprender los cambios energéticos en las reacciones químicas que se dan en su entorno. 1.Valora la conveniencia de la lentitud o la rapidez de algunos procesos químicos que se presentan en su vida diaria. Apertura: 1.Situación didáctica. Cómo determinar si una reacción es exotérmica o endotérmica? Desarrollo: - Relaciona correctamente las entalpías de formación de reactivos y productos y comprende su importancia para calcular la entalpía de una reacción química. 1.Situación didáctica. Identificar cómo diversos factores pueden alterar la cinética de una reacción. - Identifica el efecto que tiene la temperatura, la concentración, la presión y el uso de catalizadores en la cinética de reacción. Oral Escrito Expositivo Rúbrica Guía de observación Lista de cotejo Portafolio Página 29 de 35
30 SEMANA INDICADORES DE DESEMPEÑO SABERES REQUERIDOS PARA EL LOGRO DE LOS RESULTADOS DEL APRENDIZAJE ESTRATEGIAS DE APRENDIZAJE INSTRUMENTOS DE EVALUACIÓN** CONOCIMIENTOS HABILIDADES ACTITUDES Y VALORES EVIDENCIAS DEL LOGRO CONOCIMIENTOS HABILIDADES Y ACTITUDES 4.Siguiendo el método científico, realiza una actividad experimental sobre velocidad de reacción y factores que la modifican. 5.Explica la noción de desarrollo sustentable y las acciones necesarias para promoverlo. 6.Participa en la discusión en equipo y plenaria sobre el consumismo e impacto ambiental, distando alternativas de solución. 1.Describe la noción de desarrollo sustentable. 1. *Identifica algunos de los factores que afectan el medio ambiente debido al consumismo. cómo afecta cada uno de ellos a la velocidad de reacción. 1.Desarrolla actividades experimentales donde observa alguno (s) de los factores que modifican la velocidad de reacción. 1.Argumenta los beneficios y riesgos relacionados al consumismo y su impacto en el medio ambiente. 1 *Valora la importancia y cuidado que se debe tener con el manejo de sustancias en el laboratorio y el manejo de residuos. 1.Considera el desarrollo sustentable como una medida para aminorar los problemas ambientales. 2.Colabora con sus compañeros de equipo para apoyar el desarrollo sustentable. 1.Situación didáctica. Desarrollo de la práctica. Cierre: 1.Situación didáctica. Situación del agua en México. (revisión de la página web: - Entrega de resultados y cuestionario relacionado a la práctica. - Discusión en equipo y cuestionario relacionado al tema. * **Los instrumentos de evaluación debo seleccionarlos de acuerdo a los criterios de la evaluación cualitativa que deseo observar en el desempeño de mis estudiantes a partir de la evidencias de logro. Página 30 de 35
31 RECURSOS DIDÁCTICOS BIBLIOGRAFÍA BÁSICA BIBLIOGRAFÍA COMPLEMENTARIA Temas preparados en Presentaciones Power Point. Páginas web de interés particular. Modelos moleculares. Videos Experimentales. Mapas mentales Química I. Landa Barrera, Manuel y Beristain Bonilla, Bladimir. México. Nueva Imagen Química 1. Martínez Márquez, Eduardo J. México. Cengage Learning Química 1: Bachillerato General. Ramírez Regalado, Víctor Manuel. México. Patria Química. Chang, Raymond. México. McGraw- Hill Fundamentos de Química Zumbdhal, Steven. México. McGraw-Hill Estructura atómica. Un enfoque químico. Cruz-Garritz Diana; Garrita, Andoni y Chamizo José. México. Addison-Wesley Iberoamericana Química. La ciencia central. Brown, T.; LeMay, H. y Bursten, B. México. Pearson Educación- Prentice Hall Estructura atómica y enlace químico. Casabó I Gispert, Jaume. España. Reverte Página 31 de 35
32 PROCESO DE EVALUACIÓN PARA EL APRENDIZAJE* Funciones Tipos Instrumentos Diagnóstica Formativa Sumativa Autoevaluación Coevaluación Heteroevaluación Rúbrica Lista de Cotejo Portafolio Guía de observación Examen Tipo de asignatura: Teórica- práctica. Si es solo con el apoyo de laboratorio experimental: Ponderación 35% evidencias de conocimiento (Evaluación escrita) 35% evaluación formativa 30% prácticas de laboratorio Si es con apoyo de laboratorio experimental y EDULAB: 50% evidencias de conocimiento (Evaluación escrita) 30% prácticas de laboratorio 20% practicas en Edulab 3 evaluaciones parciales Fuente: SEP (2011). Lineamientos de evaluación del aprendizaje. México: SEP. 82 p. *La evaluación para el aprendizaje. Bajo este enfoque se percibe que la evaluación es un medio para el aprendizaje y la educación y no el fin. Los criterios, instrumentos y procedimientos que se utilizan en la evaluación, están diseñados y aplicados para que el estudiante aprenda de manera natural, espontánea, fácil, motivado. Su objetivo primordial es hacer que los alumnos y alumnas observen su propio aprendizaje, con el fin de que mejoren su desempeño independientemente del nivel en que se encuentran. Evaluar para el Aprendizaje se logra cuando los estudiantes saben en qué consisten las metas del aprendizaje, cuando en forma anticipada saben con qué criterios se juzgará la calidad de sus trabajos, cuando tienen modelos de lo que constituye un buen trabajo y cuando reciben retroalimentación para que mejoren su desempeño a partir del trabajo realizado. Por su parte, el docente retroalimenta el aprendizaje considerando las fortalezas y debilidades observadas de los estudiantes. Dentro de la vertiente de la evaluación para el aprendizaje, las tareas propuestas por los docentes son variadas, de tal suerte que permiten demostrar el aprendizaje de distintas maneras (SEP, 2009). Página 32 de 35
QUÍMICA I ELABORACIÓN
 QUÍMICA I ELABORACIÓN 2011-2 BLOQUE I: RECONOCES A LA QUIMICA COMO UNA HERRAMIENTA PARA LA VIDA. 2 2 Comprende el concepto de Química, su desarrollo histórico y su relación con otras ciencias. La química
QUÍMICA I ELABORACIÓN 2011-2 BLOQUE I: RECONOCES A LA QUIMICA COMO UNA HERRAMIENTA PARA LA VIDA. 2 2 Comprende el concepto de Química, su desarrollo histórico y su relación con otras ciencias. La química
Química I. Contenido. Bloque I Reconoces a la Química como una herramienta para la vida 2
 Contenido Bloque I Reconoces a la Química como una herramienta para la vida 2 Sesión A. Qué es la Química? 5 Qué es la Química? 5 La Química en nuestro mundo cotidiano 6 Sesión B. Desarrollo histórico
Contenido Bloque I Reconoces a la Química como una herramienta para la vida 2 Sesión A. Qué es la Química? 5 Qué es la Química? 5 La Química en nuestro mundo cotidiano 6 Sesión B. Desarrollo histórico
Universidad Autónoma de Guadalajara Unidad Académica de Educación Secundaria y Media Superior Bachillerato General Guía de clases para el estudiante
 Universidad Autónoma de Guadalajara Unidad Académica de Educación Secundaria y Media Superior Bachillerato General Guía de clases para el estudiante Departamento Física y Química Materia Química I Clave:
Universidad Autónoma de Guadalajara Unidad Académica de Educación Secundaria y Media Superior Bachillerato General Guía de clases para el estudiante Departamento Física y Química Materia Química I Clave:
Nombre de la asignatura: Química. Créditos: Aportación al perfil
 Nombre de la asignatura: Química Créditos: 2 2-4 Aportación al perfil Conoce la composición de los materiales usados en la fabricación de productos y su comportamiento con otros materiales. Aplica procedimientos,
Nombre de la asignatura: Química Créditos: 2 2-4 Aportación al perfil Conoce la composición de los materiales usados en la fabricación de productos y su comportamiento con otros materiales. Aplica procedimientos,
DIRECCIÓN ACADÉMICA. Competencia Genérica:
 DIRECCIÓN ACADÉMICA SECUENCIA FORMATIVA Plantel: Clave: Asignatura: Química II Clave: QI2102 Docente: Semestre: Segundo Periodo: 2009 Fecha: Unidad IV: Estado gaseoso Tiempo Asignado: 12 sesiones Grupo:
DIRECCIÓN ACADÉMICA SECUENCIA FORMATIVA Plantel: Clave: Asignatura: Química II Clave: QI2102 Docente: Semestre: Segundo Periodo: 2009 Fecha: Unidad IV: Estado gaseoso Tiempo Asignado: 12 sesiones Grupo:
Identificar y desarrollar estructuras de compuestos químicos comunes y de los presentes en los problemas ambientales.
 Nombre de la asignatura: Química Ambiental I Créditos: 2 2-4 Aportación al perfil Ser analítico, ético, crítico y conciente de la importancia de su entorno para la vida y respetuoso de la misma, siendo
Nombre de la asignatura: Química Ambiental I Créditos: 2 2-4 Aportación al perfil Ser analítico, ético, crítico y conciente de la importancia de su entorno para la vida y respetuoso de la misma, siendo
Dirección de Desarrollo Curricular Secretaría Académica
 PLAN DE ESTUDIOS DE EDUCACIÓN MEDIA SUPERIOR CAMPO DISCIPLINAR Ciencias Experimentales PROGRAMA DE ASIGNATURA (UNIDADES DE APRENDIZAJE CURRICULAR) Ecología y Medio Ambiente PERIODO III CLAVE BCCE.03.03-05
PLAN DE ESTUDIOS DE EDUCACIÓN MEDIA SUPERIOR CAMPO DISCIPLINAR Ciencias Experimentales PROGRAMA DE ASIGNATURA (UNIDADES DE APRENDIZAJE CURRICULAR) Ecología y Medio Ambiente PERIODO III CLAVE BCCE.03.03-05
Guía Temática de Química
 Guía Temática de Química Introducción a la Química Definición de química y de ciencias afines a ella Diferenciación de las ciencias afines a la química 1 Conceptos básicos de química y el método científico
Guía Temática de Química Introducción a la Química Definición de química y de ciencias afines a ella Diferenciación de las ciencias afines a la química 1 Conceptos básicos de química y el método científico
Química inorgánica. Carrera: IAF Participantes. Representantes de las academias de Ingeniería Ambiental. Academia de Ingeniería
 1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Química inorgánica Ingeniería Ambiental IAF - 0427 4-2-10 2.- HISTORIA DEL PROGRAMA
1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Química inorgánica Ingeniería Ambiental IAF - 0427 4-2-10 2.- HISTORIA DEL PROGRAMA
UNIVERSIDAD DE SONORA DIRECCIÓN DE SERVICIOS ESCOLARES DEPARTAMENTO DE INCORPORACIÓN Y REVALIDACIÓN DE ESTUDIOS
 1 UNIVERSIDAD DE SONORA DIRECCIÓN DE SERVICIOS ESCOLARES DEPARTAMENTO DE INCORPORACIÓN Y REVALIDACIÓN DE ESTUDIOS PROGRAMAS SINTÉTICOS DEL BACHILLERATO GENERAL UNIVERSITARIO Asignatura: Química I Tipo:
1 UNIVERSIDAD DE SONORA DIRECCIÓN DE SERVICIOS ESCOLARES DEPARTAMENTO DE INCORPORACIÓN Y REVALIDACIÓN DE ESTUDIOS PROGRAMAS SINTÉTICOS DEL BACHILLERATO GENERAL UNIVERSITARIO Asignatura: Química I Tipo:
PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA
 PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA UNIDAD 1: MATERIA Y MEDICIÓN CLASE TEMAS SUBTEMAS JUSTIFICACIÓN 1 2 3 MATERIA Y MEDICIÓN La química. Ramas de la química. La materia. Estados de la Materia Clasificación
PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA UNIDAD 1: MATERIA Y MEDICIÓN CLASE TEMAS SUBTEMAS JUSTIFICACIÓN 1 2 3 MATERIA Y MEDICIÓN La química. Ramas de la química. La materia. Estados de la Materia Clasificación
AÑO: HORAS CÁTEDRA SEMANALES:...3 horas... CURSO: cuarto año bachiller Decreto 6680/56
 Escuela del caminante Instituto Privado Incorporado a la Enseñanza Oficial AÑO: 2014 ASIGNATURA:... QUIMICA HORAS CÁTEDRA SEMANALES:...3 horas... CURSO: cuarto año bachiller Decreto 6680/56 PROFESOR/A:...Guillermo
Escuela del caminante Instituto Privado Incorporado a la Enseñanza Oficial AÑO: 2014 ASIGNATURA:... QUIMICA HORAS CÁTEDRA SEMANALES:...3 horas... CURSO: cuarto año bachiller Decreto 6680/56 PROFESOR/A:...Guillermo
UNIVERSIDAD AUTÓNOMA DE NAYARIT
 UNIVERSIDAD AUTÓNOMA DE NAYARIT SECRETARÍA DE EDUCACIÓN MEDIA SUPERIOR C.P. Juan López Salazar Rector Lic. Ricardo Chávez González Secretario de Educación Media Superior 1 2 Identificación de la Asignatura
UNIVERSIDAD AUTÓNOMA DE NAYARIT SECRETARÍA DE EDUCACIÓN MEDIA SUPERIOR C.P. Juan López Salazar Rector Lic. Ricardo Chávez González Secretario de Educación Media Superior 1 2 Identificación de la Asignatura
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS INDUSTRIALES ÁREA SISTEMAS DE GESTIÓN DE LA CALIDAD EN COMPETENCIAS PROFESIONALES
 TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS INDUSTRIALES ÁREA SISTEMAS DE GESTIÓN DE LA CALIDAD EN COMPETENCIAS PROFESIONALES ASIGNATURA DE QUÍMICA BÁSICA 1. Competencias Plantear y solucionar problemas
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS INDUSTRIALES ÁREA SISTEMAS DE GESTIÓN DE LA CALIDAD EN COMPETENCIAS PROFESIONALES ASIGNATURA DE QUÍMICA BÁSICA 1. Competencias Plantear y solucionar problemas
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE QUÍMICA BÁSICA
 TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE QUÍMICA BÁSICA 1. Competencias Plantear y solucionar problemas con base en los principios y teorías de
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE QUÍMICA BÁSICA 1. Competencias Plantear y solucionar problemas con base en los principios y teorías de
QUÍMICA GENERAL. Introducción:
 QUÍMICA GENERAL Nombre de la asignatura: Química General Datos de identificación Clave: 7162 Semestre: Primer semestre Créditos: Créditos (4 horas teoría y 2 horas de laboratorio ) Total de horas: 64 Horas
QUÍMICA GENERAL Nombre de la asignatura: Química General Datos de identificación Clave: 7162 Semestre: Primer semestre Créditos: Créditos (4 horas teoría y 2 horas de laboratorio ) Total de horas: 64 Horas
Nombre de la asignatura: Química. Créditos: Aportación al perfil
 Nombre de la asignatura: Química Créditos: 4 2 6 Aportación al perfil Crear y transferir tecnología aplicando métodos y procedimientos en proyectos de ingeniería electrónica, tomando en cuenta el desarrollo
Nombre de la asignatura: Química Créditos: 4 2 6 Aportación al perfil Crear y transferir tecnología aplicando métodos y procedimientos en proyectos de ingeniería electrónica, tomando en cuenta el desarrollo
Preparatoria Centro Calmecac
 PREPARATORIA CENTRO CALMECAC MATERIA: QUÍMICA I SEMESTRE: PRIMERO CARGA HORARIA TEORÍA Y PRÁCTICA: 5 HRS. SEMANALES TITULAR DE LA MATERIA: Q. en A. MARICARMEN PÉREZ LÓPEZ BIENVENIDA Estimados estudiantes
PREPARATORIA CENTRO CALMECAC MATERIA: QUÍMICA I SEMESTRE: PRIMERO CARGA HORARIA TEORÍA Y PRÁCTICA: 5 HRS. SEMANALES TITULAR DE LA MATERIA: Q. en A. MARICARMEN PÉREZ LÓPEZ BIENVENIDA Estimados estudiantes
Dirección de Desarrollo Curricular Secretaría Académica
 PLAN DE ESTUDIOS DE EDUCACIÓN MEDIA SUPERIOR CAMPO DISCIPLINAR Ciencias Experimentales PROGRAMA DE ASIGNATURA (UNIDADES DE CURRICULAR) Física I PERIODO III CLAVE BCCE.07.05-09 HORAS/SEMANA 5 CRÉDITOS 9
PLAN DE ESTUDIOS DE EDUCACIÓN MEDIA SUPERIOR CAMPO DISCIPLINAR Ciencias Experimentales PROGRAMA DE ASIGNATURA (UNIDADES DE CURRICULAR) Física I PERIODO III CLAVE BCCE.07.05-09 HORAS/SEMANA 5 CRÉDITOS 9
Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial
 Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial Programa de la asignatura: (QUI-011) Química General Total de Créditos:
Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial Programa de la asignatura: (QUI-011) Química General Total de Créditos:
UNIVERSIDAD AUTÓNOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA AZTLÁN
 R-RS-01-25-03 UNIVERSIDAD AUTÓNOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA AZTLÁN NOMBRE DE LA CARRERA LICENCIADO EN NUTRICIÓN Y CIENCIA DE LOS ALIMENTOS NOMBRE DE LA ASIGNATURA QUÍMICA
R-RS-01-25-03 UNIVERSIDAD AUTÓNOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA AZTLÁN NOMBRE DE LA CARRERA LICENCIADO EN NUTRICIÓN Y CIENCIA DE LOS ALIMENTOS NOMBRE DE LA ASIGNATURA QUÍMICA
I.E.S. ADEJE 2. DEPARTAMENTO DE FÍSICA Y QUÍMICA CURSO 2012/2013 CONTENIDOS MÍNIMOS PARA 3º DE LA ESO
 I.E.S. ADEJE 2. DEPARTAMENTO DE FÍSICA Y QUÍMICA CURSO 2012/2013 CONTENIDOS MÍNIMOS PARA 3º DE LA ESO Unidad 1: La ciencia, la materia y su medida El Sistema Internacional de unidades. Magnitudes fundamentales
I.E.S. ADEJE 2. DEPARTAMENTO DE FÍSICA Y QUÍMICA CURSO 2012/2013 CONTENIDOS MÍNIMOS PARA 3º DE LA ESO Unidad 1: La ciencia, la materia y su medida El Sistema Internacional de unidades. Magnitudes fundamentales
Academia de Ingeniería Civil y Ciencias Básicas.
 1.-DATOS DE LA ASIGNATURA NOMBRE DE LA ASIGNATURA : Química CARRERA : Ingeniería Civil CLAVE DE LA ASIGNATURA : Horas Teoría Horas práctica Créditos 4 2-10 2.- HISTORIA DEL PROGRAMA Lugar y fecha de la
1.-DATOS DE LA ASIGNATURA NOMBRE DE LA ASIGNATURA : Química CARRERA : Ingeniería Civil CLAVE DE LA ASIGNATURA : Horas Teoría Horas práctica Créditos 4 2-10 2.- HISTORIA DEL PROGRAMA Lugar y fecha de la
Química. Carrera: Ingeniería Civil CIC 0532
 1.-DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos: Química Ingeniería Civil CIC 0532 4 2 10 2.- HISTORIA DEL PROGRAMA Lugar y fecha
1.-DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos: Química Ingeniería Civil CIC 0532 4 2 10 2.- HISTORIA DEL PROGRAMA Lugar y fecha
Universidad de Guanajuato Tronco Común de Ingenierías
 Universidad de Guanajuato Tronco Común de Ingenierías Objetivo del Área Proporcionar las bases teórico-prácticas de las materias de Química, Física y Matemáticas, que conforman el Tronco Común de las carreras
Universidad de Guanajuato Tronco Común de Ingenierías Objetivo del Área Proporcionar las bases teórico-prácticas de las materias de Química, Física y Matemáticas, que conforman el Tronco Común de las carreras
GUÍA DIDÁCTICA DE QUÍMICA I
 GUÍA DIDÁCTICA DE QUÍMICA I MAYO 2011. /COBATAB ÍNDICE Introducción Fundamentación Ubicación de la materia y asignatura en el Plan Estudios Distribución de bloques Competencias Genéricas del Bachillerato
GUÍA DIDÁCTICA DE QUÍMICA I MAYO 2011. /COBATAB ÍNDICE Introducción Fundamentación Ubicación de la materia y asignatura en el Plan Estudios Distribución de bloques Competencias Genéricas del Bachillerato
Ingeniería Ingeniería en Sistemas Programa(s) Educativo(s): Computacionales en Hardware. UNIVERSIDAD AUTÓNOMA DE CHIHUAHUA Clave: 08MSU0017H
 UNIVERSIDAD AUTÓNOMA DE CHIHUAHUA Clave: 08MSU007H Clave: 08USU4053W FACULTAD DE INGENIERÍA PROGRAMA DEL CURSO: QUIMICA GENERAL DES: Ingeniería Ingeniería en Sistemas Programa(s) Educativo(s): Computacionales
UNIVERSIDAD AUTÓNOMA DE CHIHUAHUA Clave: 08MSU007H Clave: 08USU4053W FACULTAD DE INGENIERÍA PROGRAMA DEL CURSO: QUIMICA GENERAL DES: Ingeniería Ingeniería en Sistemas Programa(s) Educativo(s): Computacionales
Dirección de Desarrollo Curricular Secretaría Académica
 PLAN DE ESTUDIOS DE EDUCACIÓN MEDIA SUPERIOR CAMPO DISCIPLINAR Comunicación PROGRAMA DE ASIGNATURA (UNIDADES DE APRENDIZAJE CURRICULAR) Comprensión y Análisis de Textos PERIODO III CLAVE BCCO.03.04-08
PLAN DE ESTUDIOS DE EDUCACIÓN MEDIA SUPERIOR CAMPO DISCIPLINAR Comunicación PROGRAMA DE ASIGNATURA (UNIDADES DE APRENDIZAJE CURRICULAR) Comprensión y Análisis de Textos PERIODO III CLAVE BCCO.03.04-08
Unidad I: INTRODUCCIÓN A LA QUÍMICA INORGÁNICA DESCRIPCIÓN DE LOS TEMAS Tema I Tema II Tema III. Tema IV. Tema V
 Unidad I: INTRODUCCIÓN A LA QUÍMICA INORGÁNICA I II V Tema V I II V Tema V Materia y medida. 1. Introducción: el alcance de la química. 2. El método científico. 3. Clasificaciones de la materia. 4. Propiedades
Unidad I: INTRODUCCIÓN A LA QUÍMICA INORGÁNICA I II V Tema V I II V Tema V Materia y medida. 1. Introducción: el alcance de la química. 2. El método científico. 3. Clasificaciones de la materia. 4. Propiedades
CALENDARIO DE PRÁCTICAS DE QUÍMICA GENERAL I SEMESTRE
 Semana Fecha Número y nombre de la práctica (*) prácticas que pueden omitirse por reducción de sesiones debido a días feriados 01 Presentación, seguridad y entrega de gavetas 1. LA MATERIA Y SUS CAMBIOS
Semana Fecha Número y nombre de la práctica (*) prácticas que pueden omitirse por reducción de sesiones debido a días feriados 01 Presentación, seguridad y entrega de gavetas 1. LA MATERIA Y SUS CAMBIOS
Asignaturas antecedentes y subsecuentes
 PROGRAMA DE ESTUDIOS Química General Área a la que ÁREA GENERAL pertenece: Horas teóricas: 4 Horas practicas: 0 Créditos: 8 Clave: F0150 Ninguna. Asignaturas antecedentes y subsecuentes PRESENTACIÓN La
PROGRAMA DE ESTUDIOS Química General Área a la que ÁREA GENERAL pertenece: Horas teóricas: 4 Horas practicas: 0 Créditos: 8 Clave: F0150 Ninguna. Asignaturas antecedentes y subsecuentes PRESENTACIÓN La
Nombre de la asignatura: Química General. Créditos: Aportación al perfil
 Nombre de la asignatura: Química General Créditos: 2-2- 4 Aportación al perfil Aplicar conocimientos de las ciencias básicas y ciencias de la Ingeniería en Sistemas Computacionales. Diseñar e implementar
Nombre de la asignatura: Química General Créditos: 2-2- 4 Aportación al perfil Aplicar conocimientos de las ciencias básicas y ciencias de la Ingeniería en Sistemas Computacionales. Diseñar e implementar
INSTITUTO TECNOLOGICO METROPOLITANO Establecimiento Público de Educación Superior, Adscrito a la Alcaldía de Medellín
 QUÍMICA BÁSICA QBX4 016-0 ORGANIZACIÓN SEMANA A SEMANA Presentación del curso: 1. 3 La química y su importancia La química y su importancia en la formación de las tecnologías e ingenierías. Surgimiento
QUÍMICA BÁSICA QBX4 016-0 ORGANIZACIÓN SEMANA A SEMANA Presentación del curso: 1. 3 La química y su importancia La química y su importancia en la formación de las tecnologías e ingenierías. Surgimiento
BACHILLERATO GENERAL SEMESTRAL
 UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIO NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL SEMESTRAL Enfoque educativo basado en el desarrollo de competencias ASIGNATURA TEMAS SELECTOS
UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIO NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL SEMESTRAL Enfoque educativo basado en el desarrollo de competencias ASIGNATURA TEMAS SELECTOS
EVALUACIÓN E XTRAO RDIN ARI A DE SEPTIEMBRE Curso 2015/2016
 EVALUACIÓN E XTRAO RDIN ARI A DE SEPTIEMBRE Curso 2015/2016 ASIGNATURA: Física y Química CURSO-NIVEL: 3º ESO Unidad 1. El trabajo científico: Su relación con la ciencia, la tecnología, la sociedad y el
EVALUACIÓN E XTRAO RDIN ARI A DE SEPTIEMBRE Curso 2015/2016 ASIGNATURA: Física y Química CURSO-NIVEL: 3º ESO Unidad 1. El trabajo científico: Su relación con la ciencia, la tecnología, la sociedad y el
Guía de estudio para presentar el examen de Química I Ciclo escolar B
 CENTRO DE ESTUDIOS DE BACHILLERATO 4/2 LIC. JESÚS REYES HEROLES Guía de estudio para presentar el examen de Química I Ciclo escolar 2014-15 B Recuerda que la guía sólo es un referente del contenido del
CENTRO DE ESTUDIOS DE BACHILLERATO 4/2 LIC. JESÚS REYES HEROLES Guía de estudio para presentar el examen de Química I Ciclo escolar 2014-15 B Recuerda que la guía sólo es un referente del contenido del
índice ~
 - ---------------- índice ~ Página CAPíTULO 1 CONCEPTOS FUNDAMENTALES 23 1. MATERIA 2. MASA Y PESO 3. VOLUMEN 4. MEDICIÓN 4.1 Unidades fundamentales o patrones de medición unidades SI 5. OPERACIONES MATEMÁTICAS
- ---------------- índice ~ Página CAPíTULO 1 CONCEPTOS FUNDAMENTALES 23 1. MATERIA 2. MASA Y PESO 3. VOLUMEN 4. MEDICIÓN 4.1 Unidades fundamentales o patrones de medición unidades SI 5. OPERACIONES MATEMÁTICAS
UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA INFORMATICA SÍLABO
 UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA INFORMATICA SÍLABO 1. DATOS ADMINISTRATIVOS. Asignatura : QUÍMICA GENERAL Código : II0106 Area Académica : Química
UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA INFORMATICA SÍLABO 1. DATOS ADMINISTRATIVOS. Asignatura : QUÍMICA GENERAL Código : II0106 Area Académica : Química
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
PROGRAMA DE ESTUDIO. Básico ( ) Profesional ( x ) Especializado ( ) Horas de Teórica ( ) Presencial ( x ) Teórica-práctica ( ) Híbrida ( )
 PROGRAMA DE ESTUDIO Nombre de la asignatura: LABORATORIO DE QUÍMICA INORGÁNICA 1 Clave: LQU02 Fecha de elaboración: marzo 2015 Horas Semestre Horas semana Horas de Ciclo Formativo: Básico ( ) Profesional
PROGRAMA DE ESTUDIO Nombre de la asignatura: LABORATORIO DE QUÍMICA INORGÁNICA 1 Clave: LQU02 Fecha de elaboración: marzo 2015 Horas Semestre Horas semana Horas de Ciclo Formativo: Básico ( ) Profesional
LISTA DE TEMAS UNIVERSIDAD MARIANO GALVEZ DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS Y DE LA SALUD TEMARIO QUIMICA. 1. Química:
 UNIVERSIDAD MARIANO GALVEZ DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS Y DE LA SALUD TEMARIO QUIMICA LISTA DE TEMAS 1. Química: 1.1.Introducción a la química 1.1.1. Mezclas homogéneas y heterogéneas 1.1.2.
UNIVERSIDAD MARIANO GALVEZ DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS Y DE LA SALUD TEMARIO QUIMICA LISTA DE TEMAS 1. Química: 1.1.Introducción a la química 1.1.1. Mezclas homogéneas y heterogéneas 1.1.2.
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS
 PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS MATERIA: Química General I CARRERA: Química Analítica NIVEL: Primero
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS MATERIA: Química General I CARRERA: Química Analítica NIVEL: Primero
ACADEMIA DE CIENCIAS EXPERIMENTALES
 CENTRO DE ESTUDIOS DE BACHILLERATO 4/2 LIC. JESÚS REYES HEROLES ACADEMIA DE CIENCIAS EXPERIMENTALES Nombre del alumno (a) Situación académica (X) Egresado ( ) Baja Temporal ( ) Inscrito ( ) GUÍA PARA EL
CENTRO DE ESTUDIOS DE BACHILLERATO 4/2 LIC. JESÚS REYES HEROLES ACADEMIA DE CIENCIAS EXPERIMENTALES Nombre del alumno (a) Situación académica (X) Egresado ( ) Baja Temporal ( ) Inscrito ( ) GUÍA PARA EL
Fecha de elaboración: Agosto de Fecha de última actualización: Julio de Presentación
 Programa elaborado por: PROGRAMA DE ESTUDIO QUÍMICA GENERAL Programa Educativo: Licenciatura en Física Área de Formación : Transversal Horas teóricas: 4 Horas prácticas: 0 Total de Horas: 4 Total de créditos:
Programa elaborado por: PROGRAMA DE ESTUDIO QUÍMICA GENERAL Programa Educativo: Licenciatura en Física Área de Formación : Transversal Horas teóricas: 4 Horas prácticas: 0 Total de Horas: 4 Total de créditos:
UNIVERSIDAD DEL CARIBE UNICARIBE ESCUELA DE EDUCACIÓN. Programa de Asignatura
 UNIVERSIDAD DEL CARIBE UNICARIBE ESCUELA DE EDUCACIÓN Programa de Asignatura Nombre de la asignatura : Química I Carga académica : 4 créditos Modalidad : Semipresencial Clave : QUI-101 Pre-requisito :
UNIVERSIDAD DEL CARIBE UNICARIBE ESCUELA DE EDUCACIÓN Programa de Asignatura Nombre de la asignatura : Química I Carga académica : 4 créditos Modalidad : Semipresencial Clave : QUI-101 Pre-requisito :
TÓPICOS GENERATIVOS UNIDAD 1. Todos los elementos químicos se comportan de la misma manera? Tendrán pautas de comportamiento?
 COLEGIO NACIONAL RAFAEL HERNÁNDEZ - U.N.L.P. PROGRAMA DE TERCER AÑO ASIGNATURA: QUÍMICA CICLO LECTIVO 2016 SECCIÓN: QUÍMICA HILOS CONDUCTORES La presencia de diferentes clases de sustancias en la naturaleza
COLEGIO NACIONAL RAFAEL HERNÁNDEZ - U.N.L.P. PROGRAMA DE TERCER AÑO ASIGNATURA: QUÍMICA CICLO LECTIVO 2016 SECCIÓN: QUÍMICA HILOS CONDUCTORES La presencia de diferentes clases de sustancias en la naturaleza
Contenidos mínimos Física y Química 3º ESO
 Contenidos mínimos Física y Química 3º ESO EL TRABAJO CIENTÍFICO Etapas del método científico. Magnitudes y unidades. Cambio de unidades. Sistema Internacional de Unidades (SI). Representación de gráficas
Contenidos mínimos Física y Química 3º ESO EL TRABAJO CIENTÍFICO Etapas del método científico. Magnitudes y unidades. Cambio de unidades. Sistema Internacional de Unidades (SI). Representación de gráficas
UNIVERSIDAD DE GUANAJUATO COLEGIO DEL NIVEL MEDIO SUPERIOR
 UNIVERSIDAD DE GUANAJUATO COLEGIO DEL NIVEL MEDIO SUPERIOR QUÍMICA II (PROGRAMA DE ESTUDIOS) DR. JOSÉ MANUEL CABRERA SIXTO RECTOR GENERAL Q. RICARDO GÓMEZ GOVEA DIRECTOR 1 UNIVERSIDAD DE GUANAJUATO NOMBRE
UNIVERSIDAD DE GUANAJUATO COLEGIO DEL NIVEL MEDIO SUPERIOR QUÍMICA II (PROGRAMA DE ESTUDIOS) DR. JOSÉ MANUEL CABRERA SIXTO RECTOR GENERAL Q. RICARDO GÓMEZ GOVEA DIRECTOR 1 UNIVERSIDAD DE GUANAJUATO NOMBRE
Contenidos 1. La medida: Magnitud y unidad. Sistema internacional de unidades. Múltiplos y submúltiplos. Notación científica.
 Objetivos La enseñanza de la Física y Química de 3º ESO tendrá como finalidad el desarrollo de las siguientes capacidades: 1. Reconocer y valorar las aportaciones de la ciencia para la mejora de las condiciones
Objetivos La enseñanza de la Física y Química de 3º ESO tendrá como finalidad el desarrollo de las siguientes capacidades: 1. Reconocer y valorar las aportaciones de la ciencia para la mejora de las condiciones
UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA ELECTRONICA SILABO PLAN DE ESTUDIOS
 1. DATOS GENERALES. ASIGNATURA CODIGO CONDICION UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA ELECTRONICA SILABO PLAN DE ESTUDIOS 2006-2 NIVEL : 1 CREDITOS
1. DATOS GENERALES. ASIGNATURA CODIGO CONDICION UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA ELECTRONICA SILABO PLAN DE ESTUDIOS 2006-2 NIVEL : 1 CREDITOS
INFORMACIÓN PARA LOS ALUMNOS DE 3º ESO
 INFORMACIÓN PARA LOS ALUMNOS DE 3º ESO DE FISICA Y QUIMICA Curso 2010-2011 1 OBJETIVOS Al finalizar el curso deberás ser capaz de: 1. Dominar la transformación de una unidad en otras. 2. Identificar magnitudes
INFORMACIÓN PARA LOS ALUMNOS DE 3º ESO DE FISICA Y QUIMICA Curso 2010-2011 1 OBJETIVOS Al finalizar el curso deberás ser capaz de: 1. Dominar la transformación de una unidad en otras. 2. Identificar magnitudes
FACULTAD DE MEDICINA FCS102 (FUNDAMENTOS DE QUIMICA GENERAL Y ORGANIC) MARZO - JUNIO 2014
 FACULTAD DE MEDICINA FCS102 (FUNDAMENTOS DE QUIMICA GENERAL Y ORGANIC) 2014-2 MARZO - JUNIO 2014 1. Identificación Número de sesiones: 3 Número de créditos: 4.5 Profesor(a): Jaime Gía. Correo electrónico
FACULTAD DE MEDICINA FCS102 (FUNDAMENTOS DE QUIMICA GENERAL Y ORGANIC) 2014-2 MARZO - JUNIO 2014 1. Identificación Número de sesiones: 3 Número de créditos: 4.5 Profesor(a): Jaime Gía. Correo electrónico
FÍSICA Y QUÍMICA 3º de ESO
 FÍSICA Y QUÍMICA 3º de ESO A) Contenidos (conceptos) UNIDAD 1: La medida. El método científico Fenómenos físicos. Física. Fenómenos químicos. Química. Magnitud física. Unidad de medida. Sistema Internacional
FÍSICA Y QUÍMICA 3º de ESO A) Contenidos (conceptos) UNIDAD 1: La medida. El método científico Fenómenos físicos. Física. Fenómenos químicos. Química. Magnitud física. Unidad de medida. Sistema Internacional
OPCIÓN EDUCATIVA TOTAL DE CRÉDITOS HORAS A LA SEMANA
 UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIOS NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL SEMESTRAL Enfoque Educativo Basado en el Desarrollo de Competencias MODALIDAD ASIGNATURA
UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIOS NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL SEMESTRAL Enfoque Educativo Basado en el Desarrollo de Competencias MODALIDAD ASIGNATURA
QUÍMICA BÁSICA. 4 horas a la semana 6 créditos. 2 horas teóricas y 2 horas de laboratorio
 QUÍMICA BÁSICA 4 horas a la semana 6 créditos 2 horas teóricas y 2 horas de laboratorio OBJETIVO: El alumno analizará los conceptos básicos de Química para identificar las propiedades de las sustancias
QUÍMICA BÁSICA 4 horas a la semana 6 créditos 2 horas teóricas y 2 horas de laboratorio OBJETIVO: El alumno analizará los conceptos básicos de Química para identificar las propiedades de las sustancias
FÍSICA Y QUÍMICA DE 3º DE ESO
 FÍSICA Y QUÍMICA DE 3º DE ESO CONTENIDOS. BLOQUE 1. Contenidos comunes. Utilización de estrategias propias del trabajo científico, como el planteamiento de problemas y discusión de su interés, la formulación
FÍSICA Y QUÍMICA DE 3º DE ESO CONTENIDOS. BLOQUE 1. Contenidos comunes. Utilización de estrategias propias del trabajo científico, como el planteamiento de problemas y discusión de su interés, la formulación
Licenciatura en Química PROGRAMA DE ESTUDIO. Obligatoria Abraham Gómez Rivera, Lorena Isabel Programa elaborado por:
 PROGRAMA DE ESTUDIO Química Básica Programa Educativo: Área de Formación: Licenciatura en Química General Horas teóricas: 2 Horas prácticas: 2 Total de horas: 4 Total de créditos: 6 Clave: F1407 Tipo:
PROGRAMA DE ESTUDIO Química Básica Programa Educativo: Área de Formación: Licenciatura en Química General Horas teóricas: 2 Horas prácticas: 2 Total de horas: 4 Total de créditos: 6 Clave: F1407 Tipo:
UNIVERSIDAD DEL VALLE DE MÉXICO
 UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIOS NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL SEMESTRAL Enfoque Educativo Basado en el Desarrollo de Competencias ASIGNATURA DESARROLLO
UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIOS NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL SEMESTRAL Enfoque Educativo Basado en el Desarrollo de Competencias ASIGNATURA DESARROLLO
Pontificia Universidad Católica del Ecuador
 Pontificia Universidad Católica del Ecuador Escuela de Ciencias Químicas 1.- DATOS INFORMATIVOS: MATERIA: Química General I (Teoría y Laboratorio) CODIGO: 12793 CARRERA: Ciencias Químicas, mención Química
Pontificia Universidad Católica del Ecuador Escuela de Ciencias Químicas 1.- DATOS INFORMATIVOS: MATERIA: Química General I (Teoría y Laboratorio) CODIGO: 12793 CARRERA: Ciencias Químicas, mención Química
DIRECCIÓN GENERAL DE BACHILLERATO SECUENCIA DIDÁCTICA NOMBRE DEL PLANTEL CLAVE LOCALIDAD ZONA EXPERIMENTAL DIURNA 30EBH0020U XALAPA XALAPA
 NOMBRE DEL PLANTEL CLAVE LOCALIDAD ZONA EXPERIMENTAL DIURNA 30EBH0020U XALAPA XALAPA ASIGNATURA DOCENTE (S) FISICA I I.E. OMAR DEL CASTILLO CALDERON Semestre Periodo escolar No. de secuencia No. de sesiones
NOMBRE DEL PLANTEL CLAVE LOCALIDAD ZONA EXPERIMENTAL DIURNA 30EBH0020U XALAPA XALAPA ASIGNATURA DOCENTE (S) FISICA I I.E. OMAR DEL CASTILLO CALDERON Semestre Periodo escolar No. de secuencia No. de sesiones
CONCRECIÓN CURRICULAR FÍSICA Y QUÍMICA CURSO: 4º DE LA ESO
 CONCRECIÓN CURRICULAR FÍSICA Y QUÍMICA CURSO: 4º DE LA ESO CRITERIOS DE EVALUACIÓN COMPETENCIAS BÁSICAS CONTENIDOS OBJETIVOS DE ÁREA /MATERIA OBJETIVOS DE ETAPA Aplicar algunos de los elementos básicos
CONCRECIÓN CURRICULAR FÍSICA Y QUÍMICA CURSO: 4º DE LA ESO CRITERIOS DE EVALUACIÓN COMPETENCIAS BÁSICAS CONTENIDOS OBJETIVOS DE ÁREA /MATERIA OBJETIVOS DE ETAPA Aplicar algunos de los elementos básicos
ESTRUCTURA, VALORACIÓN Y CONTENIDOS DEL EXAMEN DE QUÍMICA DE LAS PRUEBAS DE ACCESO A LA UNIVERSIDAD POLITÉCNICA DE CARTAGENA PARA MAYORES DE 25 AÑOS.
 ESTRUCTURA, VALORACIÓN Y CONTENIDOS DEL EXAMEN DE QUÍMICA DE LAS PRUEBAS DE ACCESO A LA UNIVERSIDAD POLITÉCNICA DE CARTAGENA PARA MAYORES DE 25 AÑOS. ESTRUCTURA La prueba constará de cuatro bloques, existiendo
ESTRUCTURA, VALORACIÓN Y CONTENIDOS DEL EXAMEN DE QUÍMICA DE LAS PRUEBAS DE ACCESO A LA UNIVERSIDAD POLITÉCNICA DE CARTAGENA PARA MAYORES DE 25 AÑOS. ESTRUCTURA La prueba constará de cuatro bloques, existiendo
Objetivos. Contenidos
 Objetivos La enseñanza de la Física y química en el bachillerato tendrá como finalidad contribuir al desarrollo de las siguientes capacidades: 1. Conocer los conceptos, leyes, teorías y modelos más importantes
Objetivos La enseñanza de la Física y química en el bachillerato tendrá como finalidad contribuir al desarrollo de las siguientes capacidades: 1. Conocer los conceptos, leyes, teorías y modelos más importantes
PLANEACIÓN DIDÁCTICA GENERAL TEMAS SELECTOS DE QUÍMICA
 PLANEACIÓN DIDÁCTICA GENERAL TEMAS SELECTOS DE QUÍMICA QUÍMICA SEMESTRE: QUINTO HORAS TEÓRICAS 2 CRÉDITOS 5 HORAS PRÁCTICAS 1 TIPO DE CURSO OPTATIVA TOTAL DE HORAS: 3 PLANTEL ELABORÓ M. en P.D. Sandra
PLANEACIÓN DIDÁCTICA GENERAL TEMAS SELECTOS DE QUÍMICA QUÍMICA SEMESTRE: QUINTO HORAS TEÓRICAS 2 CRÉDITOS 5 HORAS PRÁCTICAS 1 TIPO DE CURSO OPTATIVA TOTAL DE HORAS: 3 PLANTEL ELABORÓ M. en P.D. Sandra
Nombre de la materia Química General Departamento Nanotecnología Academia Química
 Nombre de la materia Química General Departamento Nanotecnología Academia Química Clave Horas-teoría Horas-práctica Horas-AI Total-horas Créditos I4225 4 4 9 Nivel Carrera Tipo Prerrequisitos 1 Nanotecnología
Nombre de la materia Química General Departamento Nanotecnología Academia Química Clave Horas-teoría Horas-práctica Horas-AI Total-horas Créditos I4225 4 4 9 Nivel Carrera Tipo Prerrequisitos 1 Nanotecnología
DEPARTAMENTO DE FÍSICA Y QUÍMICA IEES SEVERO OCHOA PRIMERO DE BACHILLERATO CONTENIDOS MÍNIMOS 3.1. Contenidos comunes. Utilización de estrategias
 DEPARTAMENTO DE FÍSICA Y QUÍMICA IEES SEVERO OCHOA PRIMERO DE BACHILLERATO CONTENIDOS MÍNIMOS 3.1. Contenidos comunes. Utilización de estrategias básicas de la actividad científica, tales como: el planteamiento
DEPARTAMENTO DE FÍSICA Y QUÍMICA IEES SEVERO OCHOA PRIMERO DE BACHILLERATO CONTENIDOS MÍNIMOS 3.1. Contenidos comunes. Utilización de estrategias básicas de la actividad científica, tales como: el planteamiento
PROGRAMA INSTRUCCIONAL
 UNIVERSIDAD FERMÍN TORO VICE RECTORADO ACADÉMICO FACULTAD DE INGENIERIA PROGRAMA AL DATOS BÁSICOS DE LA ASIGNATURA Nombre de la asignatura: Código Semestre U.C. Pre- Requisito QUÍMICA QUI-422 IV 2 S/P
UNIVERSIDAD FERMÍN TORO VICE RECTORADO ACADÉMICO FACULTAD DE INGENIERIA PROGRAMA AL DATOS BÁSICOS DE LA ASIGNATURA Nombre de la asignatura: Código Semestre U.C. Pre- Requisito QUÍMICA QUI-422 IV 2 S/P
Básico ( ) Profesional ( x ) Especializado ( ) Horas de. Práctica ( ) Teórica ( X ) Presencial ( X ) Teórica-práctica ( ) Híbrida ( X )
 Nombre de la asignatura: QUÍMICA ANALITICA 2 Clave: QUI07 Fecha de elaboración: Marzo 2015 Horas Semestre Horas semana Horas de Teoría PROGRAMA DE ESTUDIO Ciclo Formativo: Básico ( ) Profesional ( x )
Nombre de la asignatura: QUÍMICA ANALITICA 2 Clave: QUI07 Fecha de elaboración: Marzo 2015 Horas Semestre Horas semana Horas de Teoría PROGRAMA DE ESTUDIO Ciclo Formativo: Básico ( ) Profesional ( x )
SECUENCIA DIDÁCTICA. Nombre de curso: Química Clave de curso: QUI0702A21
 SECUENCIA DIDÁCTICA Nombre de curso: Química Clave de curso: QUI0702A21 Antecedente: Clave de antecedente: Módulo Competencia de Módulo: Aplicar los fundamentos y procesos biológicos, físicos y químicos
SECUENCIA DIDÁCTICA Nombre de curso: Química Clave de curso: QUI0702A21 Antecedente: Clave de antecedente: Módulo Competencia de Módulo: Aplicar los fundamentos y procesos biológicos, físicos y químicos
Ubicación de la asignatura. Propósito de la asignatura. Desarrollando proyectos. Asignaturas relacionadas. Una mirada hacia la optimización económica
 EL CÁLCULO EN MI VIDA DIARIA OPTATIVAS ÁREA: MATEMÁTICAS Ubicación de la asignatura La asignatura El cálculo en mi vida diaria, se encuentra dentro del bloque de las asignaturas optativas del Bachillerato
EL CÁLCULO EN MI VIDA DIARIA OPTATIVAS ÁREA: MATEMÁTICAS Ubicación de la asignatura La asignatura El cálculo en mi vida diaria, se encuentra dentro del bloque de las asignaturas optativas del Bachillerato
CENTRO UNIVERSITARIO MONTEJO A.C. Temario Ciencias 3 Énfasis en química. Bloque I. Las características de los materiales
 Bloque I. Las características de los materiales La ciencia y la tecnología en el mundo actual Identifica las aportaciones del conocimiento químico y tecnológico en la satisfacción de necesidades básicas,
Bloque I. Las características de los materiales La ciencia y la tecnología en el mundo actual Identifica las aportaciones del conocimiento químico y tecnológico en la satisfacción de necesidades básicas,
UNIVERSIDAD DEL VALLE DE MÉXICO
 UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIOS NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL SEMESTRAL Enfoque Educativo Basado en el Desarrollo de Competencias ASIGNATURA TIPO DE
UNIVERSIDAD DEL VALLE DE MÉXICO PROGRAMA DE ESTUDIOS NIVEL MEDIO SUPERIOR PLANEACIÓN DIDÁCTICA BACHILLERATO GENERAL SEMESTRAL Enfoque Educativo Basado en el Desarrollo de Competencias ASIGNATURA TIPO DE
UNIVERSIDAD AUTÓNOMA DE COAHUILA
 UNIVERSIDAD AUTÓNOMA DE COAHUILA DIRECCIÓN DE ASUNTOS ACADÉMICOS COORDINACIÓN DE BACHILLERATOS Nombre del módulo: QUÍMICA I Campo disciplinar: CIENCIAS EXPERIMENTALES PROPÓSITO DEL MÓDULO: Discute las
UNIVERSIDAD AUTÓNOMA DE COAHUILA DIRECCIÓN DE ASUNTOS ACADÉMICOS COORDINACIÓN DE BACHILLERATOS Nombre del módulo: QUÍMICA I Campo disciplinar: CIENCIAS EXPERIMENTALES PROPÓSITO DEL MÓDULO: Discute las
Pontificia Universidad Católica del Ecuador
 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: GEOQUÍMICA CÓDIGO: CARRERA: Ingeniería en Ciencias Geográficas NIVEL: III No. CRÉDITOS: CRÉDITOS TEORÍA: 2 CRÉDITOS PRÁCTICA: 3 SEMESTRE / AÑO ACADÉMICO: 2011-2012
1. DATOS INFORMATIVOS: MATERIA O MÓDULO: GEOQUÍMICA CÓDIGO: CARRERA: Ingeniería en Ciencias Geográficas NIVEL: III No. CRÉDITOS: CRÉDITOS TEORÍA: 2 CRÉDITOS PRÁCTICA: 3 SEMESTRE / AÑO ACADÉMICO: 2011-2012
Pontificia Universidad Católica del Ecuador
 1. DATOS INFORMATIVOS: MATERIA: QUÍMICA I CÓDIGO: CARRERA: CIENCIAS BIOLÓGICAS NIVEL: PRIMERO No. CREDITOS: 5 CRÉDITOS TEORÍA: 3 CREDITOS PRÁCTICA: 2 SEMESTRE/AÑO ACADÉMICO: Primer semestre 2010-2011.
1. DATOS INFORMATIVOS: MATERIA: QUÍMICA I CÓDIGO: CARRERA: CIENCIAS BIOLÓGICAS NIVEL: PRIMERO No. CREDITOS: 5 CRÉDITOS TEORÍA: 3 CREDITOS PRÁCTICA: 2 SEMESTRE/AÑO ACADÉMICO: Primer semestre 2010-2011.
UNIVERSIDAD EMILIANO ZAPATA
 UNIVERSIDAD EMILIANO ZAPATA OBJETIVO DE LA MATERIA El estudiante describirá la importancia de la química en la ciencia y tecnología, a través del conocimiento de sus principios básicos, con el fin de explicar
UNIVERSIDAD EMILIANO ZAPATA OBJETIVO DE LA MATERIA El estudiante describirá la importancia de la química en la ciencia y tecnología, a través del conocimiento de sus principios básicos, con el fin de explicar
PENDIENTES DE 3º ESO. DEPARTAMENTO DE FÍSICA Y QUÍMICA. CURSO 13-14
 PENDIENTES DE 3º ESO. DEPARTAMENTO DE FÍSICA Y QUÍMICA. CURSO 13-14 INFORMACIÓN Y CONTENIDOS MÍNIMOS PARA LA EVALUACIÓN Información Para que los alumnos puedan recuperar esta asignatura lo más pronto posible,
PENDIENTES DE 3º ESO. DEPARTAMENTO DE FÍSICA Y QUÍMICA. CURSO 13-14 INFORMACIÓN Y CONTENIDOS MÍNIMOS PARA LA EVALUACIÓN Información Para que los alumnos puedan recuperar esta asignatura lo más pronto posible,
QUÍMICA I QUIMICA I SERIE PROGRAMAS DE ESTUDIOS 1 DGB/DCA/
 QUIMICA I SERIE PROGRAMAS DE ESTUDIOS 1 DGB/DCA/07-2010 SERIE: PROGRAMAS DE ESTUDIO SECRETARÍA DE EDUCACIÓN PÚBLICA SUBSECRETARÍA DE EDUCACIÓN MEDIA SUPERIOR DIRECCIÓN GENERAL DEL BACHILLERATO SEMESTRE
QUIMICA I SERIE PROGRAMAS DE ESTUDIOS 1 DGB/DCA/07-2010 SERIE: PROGRAMAS DE ESTUDIO SECRETARÍA DE EDUCACIÓN PÚBLICA SUBSECRETARÍA DE EDUCACIÓN MEDIA SUPERIOR DIRECCIÓN GENERAL DEL BACHILLERATO SEMESTRE
UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO FACULTAD DE AGRONOMÍA Y AGROINDUSTRIAS DEPARTAMENTO FÍSICO-MATEMÁTICO
 UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO FACULTAD DE AGRONOMÍA Y AGROINDUSTRIAS DEPARTAMENTO FÍSICO-MATEMÁTICO ASIGNATURA: QUIMICA PARA EL CURSO DE INGRESO 2010 CARRERAS: INGENIERÍA EN ALIMENTOS INGENIERÍA
UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO FACULTAD DE AGRONOMÍA Y AGROINDUSTRIAS DEPARTAMENTO FÍSICO-MATEMÁTICO ASIGNATURA: QUIMICA PARA EL CURSO DE INGRESO 2010 CARRERAS: INGENIERÍA EN ALIMENTOS INGENIERÍA
Bloque 1. Las magnitudes físicas y su medida
 Bloque 1. Las magnitudes físicas y su medida El sistema métrico decimal El sistema internacional de unidades Conversiones de unidades con factores de conversión. Unidades compuestas Magnitudes escalares
Bloque 1. Las magnitudes físicas y su medida El sistema métrico decimal El sistema internacional de unidades Conversiones de unidades con factores de conversión. Unidades compuestas Magnitudes escalares
PLANEACIÓN Y SECUENCIA DIDÁCTICA Colegio de Bachilleres del Estado de Morelos
 PLANEACIÓN Y SECUENCIA DIDÁCTICA Colegio de Bachilleres del Estado de Morelos 1. DATOS GENERALES DE LA ASIGNATURA: Número: Grupo:202 1. Plantel /módulo EMSAD: PLANTEL 05 2. Turno: MATUTINO 3. Facilitador
PLANEACIÓN Y SECUENCIA DIDÁCTICA Colegio de Bachilleres del Estado de Morelos 1. DATOS GENERALES DE LA ASIGNATURA: Número: Grupo:202 1. Plantel /módulo EMSAD: PLANTEL 05 2. Turno: MATUTINO 3. Facilitador
CONTENIDOS MÍNIMOS septiembre
 DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
TAREA INTEGRADA DE LA TABLA PERÍODICA Asignatura: Química 3º ESO
 TAREA INTEGRADA DE LA TABLA PERÍODICA Asignatura: Química 3º ESO INFORME PRELIMINAR 5 de marzo de 2012 IES Virgen del Castillo Semana de los proyectos, Página 1 Introducción La importancia de la tabla
TAREA INTEGRADA DE LA TABLA PERÍODICA Asignatura: Química 3º ESO INFORME PRELIMINAR 5 de marzo de 2012 IES Virgen del Castillo Semana de los proyectos, Página 1 Introducción La importancia de la tabla
Colegio San Agustín de Atacama Copiapó TEMARIO QUÍMICA. Séptimo Básico:
 UNIDAD CERO: Sustancias puras y mezclas Séptimo Básico: Describir los estados de la materia a nivel macroscópico y molecular. Comprender que toda la materia está constituida por un número reducido de elementos
UNIDAD CERO: Sustancias puras y mezclas Séptimo Básico: Describir los estados de la materia a nivel macroscópico y molecular. Comprender que toda la materia está constituida por un número reducido de elementos
Temario: 1.- ESTRUCTURA ATÓMICA 14 hrs.
 QUÍMICA GENERAL CLAVE: SEMESTRE EN LA QUE SE IMPARTE: I CARÁCTER: OBLIGATORIO MODALIDAD: CURSO HRS. TEÓRICAS A LA SEMANA: 3 HRS. PRÁCTICAS A LA SEMANA:3 CRÉDITOS: 9 TOTAL DE HORAS AL SEMESTRE: 96 SERIACIÓN
QUÍMICA GENERAL CLAVE: SEMESTRE EN LA QUE SE IMPARTE: I CARÁCTER: OBLIGATORIO MODALIDAD: CURSO HRS. TEÓRICAS A LA SEMANA: 3 HRS. PRÁCTICAS A LA SEMANA:3 CRÉDITOS: 9 TOTAL DE HORAS AL SEMESTRE: 96 SERIACIÓN
DIRECCIÓN GENERAL DE BACHILLERATO SECUENCIA DIDÁCTICA NOMBRE DEL PLANTEL CLAVE LOCALIDAD ZONA EXPERIMENTAL DIURNA 30EBH0020U XALAPA XALAPA
 NOMBRE DEL PLANTEL CLAVE LOCALIDAD ZONA EXPERIMENTAL DIURNA 30EBH0020U XALAPA XALAPA ASIGNATURA DOCENTE (S) FISICA I I.E. OMAR DEL CASTILLO CALDERON Semestre Periodo escolar No. de secuencia No. de sesiones
NOMBRE DEL PLANTEL CLAVE LOCALIDAD ZONA EXPERIMENTAL DIURNA 30EBH0020U XALAPA XALAPA ASIGNATURA DOCENTE (S) FISICA I I.E. OMAR DEL CASTILLO CALDERON Semestre Periodo escolar No. de secuencia No. de sesiones
Universidad Autónoma de Sinaloa Escuela de Ciencias de la Tierra Tronco Común
 Universidad Autónoma de Sinaloa Escuela de Ciencias de la Tierra Tronco Común PROGRAMA DE ESTUDIOS 1. DATOS DE IDENTIFICACIÓN UNIDAD DE SEMINARIO DE INVESTIGACIÓN APRENDIZAJE Clave Semestre: IX Semestre
Universidad Autónoma de Sinaloa Escuela de Ciencias de la Tierra Tronco Común PROGRAMA DE ESTUDIOS 1. DATOS DE IDENTIFICACIÓN UNIDAD DE SEMINARIO DE INVESTIGACIÓN APRENDIZAJE Clave Semestre: IX Semestre
UNIVERSIDAD AUTÓNOMA DEL ESTADO DE MORELOS SECRETARÍA ACADÉMICA DIRECCIÓN GENERAL DE EDUCACIÓN MEDIA SUPERIOR
 1. Identificación de la asignatura: UNIVERSIDAD AUTÓNOMA DEL ESTADO DE MORELOS SECRETARÍA ACADÉMICA DIRECCIÓN GENERAL DE EDUCACIÓN MEDIA SUPERIOR PROGRAMA DE ESTUDIOS PARA EL DESARROLLO DE COMPETENCIAS
1. Identificación de la asignatura: UNIVERSIDAD AUTÓNOMA DEL ESTADO DE MORELOS SECRETARÍA ACADÉMICA DIRECCIÓN GENERAL DE EDUCACIÓN MEDIA SUPERIOR PROGRAMA DE ESTUDIOS PARA EL DESARROLLO DE COMPETENCIAS
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico.
 FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
ACTIVIDADES DE RECUPERACIÓN PARA LOS ALUMNOS QUE HAYAN PROMOCIONADO A 4º ESO CON EVALUACILÓN NEGATIVA EN FÍSICA Y QUÍMICA DE 3º ESO.
 ACTIVIDADES DE RECUPERACIÓN PARA LOS ALUMNOS QUE HAYAN PROMOCIONADO A 4º ESO CON EVALUACILÓN NEGATIVA EN FÍSICA Y QUÍMICA DE 3º ESO. Para los alumnos que han promocionada a 4º ESO y tienen pendiente de
ACTIVIDADES DE RECUPERACIÓN PARA LOS ALUMNOS QUE HAYAN PROMOCIONADO A 4º ESO CON EVALUACILÓN NEGATIVA EN FÍSICA Y QUÍMICA DE 3º ESO. Para los alumnos que han promocionada a 4º ESO y tienen pendiente de
SECRETARIA DE EDUCACIÓN DE TAMAULIPAS SUBSECRETARIA DE PLANEACIÓN DIRECCIÓN DE EVALUACIÓN
 SECRETARA DE EDUCACÓN DE TAMAULPAS SUBSECRETARA DE PLANEACÓN DRECCÓN DE EVALUACÓN B Título de Bloque Las caracterí s ticas de los material es Aprendizaje Esperado Contenido Curricular ESPECFCACONES dentifica
SECRETARA DE EDUCACÓN DE TAMAULPAS SUBSECRETARA DE PLANEACÓN DRECCÓN DE EVALUACÓN B Título de Bloque Las caracterí s ticas de los material es Aprendizaje Esperado Contenido Curricular ESPECFCACONES dentifica
Diplomado Para docentes de 3 y 4 grados de primaria
 Diplomado Para docentes de 3 y 4 grados de primaria Reforma Integral de la Educación Básica Módulo 3 Planeación y evaluación para los campos de formación: Pensamiento matemático y Exploración y comprensión
Diplomado Para docentes de 3 y 4 grados de primaria Reforma Integral de la Educación Básica Módulo 3 Planeación y evaluación para los campos de formación: Pensamiento matemático y Exploración y comprensión
GUÍA DIDACTICA CURSO QUÍMICA 2º BACHILLERATO. PROFESOR: Alicia Blanco Pozos
 GUÍA DIDACTICA QUÍMICA 2º BACHILLERATO CURSO 2016-17 PROFESOR: Alicia Blanco Pozos CONTENIDOS Los contenidos se organizan en 8 unidades didácticas distribuidos en 4 bloques: BLOQUE I UNIDAD 1. Estructura
GUÍA DIDACTICA QUÍMICA 2º BACHILLERATO CURSO 2016-17 PROFESOR: Alicia Blanco Pozos CONTENIDOS Los contenidos se organizan en 8 unidades didácticas distribuidos en 4 bloques: BLOQUE I UNIDAD 1. Estructura
IDENTIFICACIÓN DEL CURSO Ubicación HCA HTI Total de horas Valor en créditos 6 semestre Tipo de curso Optativa de área
 PROGRAMA DE ESTUDIOS TEMAS SELECTOS DE EDUCACIÓN IDENTIFICACIÓN DEL CURSO Ubicación HCA HTI Total de horas Valor en créditos 6 semestre 2 2 4 4 Tipo de curso Optativa de área Matemáticas VI Inglés IV Asignaturas
PROGRAMA DE ESTUDIOS TEMAS SELECTOS DE EDUCACIÓN IDENTIFICACIÓN DEL CURSO Ubicación HCA HTI Total de horas Valor en créditos 6 semestre 2 2 4 4 Tipo de curso Optativa de área Matemáticas VI Inglés IV Asignaturas
PROGRAMA DE ESTUDIO. Básico ( ) Profesional ( x ) Especializado ( ) Horas de Práctica
 PROGRAMA DE ESTUDIO Nombre de la asignatura: LABORATORIO DE QUÍMICA ANALITICA 2 Clave: LQU07 Fecha de elaboración: Marzo 2015 Horas Semestre Horas semana Horas de Teoría Ciclo Formativo: Básico ( ) Profesional
PROGRAMA DE ESTUDIO Nombre de la asignatura: LABORATORIO DE QUÍMICA ANALITICA 2 Clave: LQU07 Fecha de elaboración: Marzo 2015 Horas Semestre Horas semana Horas de Teoría Ciclo Formativo: Básico ( ) Profesional
Prefacio... ix COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3
 ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
SUGERENCIAS DE SECUENCIA DIDÁCTICA POR MÓDULO UNIDAD DE APRENDIZAJE: FÍSICA II
 SUGERENCIAS DE SECUENCIA DIDÁCTICA POR MÓDULO UNIDAD DE APRENDIZAJE: FÍSICA II NOVIEMBRE DE 2011 1.- DATOS GENERALES. Escuela: Departamento: Ciencias de la Naturaleza y la Salud. Unidad de Aprendizaje:
SUGERENCIAS DE SECUENCIA DIDÁCTICA POR MÓDULO UNIDAD DE APRENDIZAJE: FÍSICA II NOVIEMBRE DE 2011 1.- DATOS GENERALES. Escuela: Departamento: Ciencias de la Naturaleza y la Salud. Unidad de Aprendizaje:
UNIVERSIDAD MAYOR DE SAN SIMON FACULTAD DE CIENCIAS Y TECNOLOGÍA PLAN GLOBAL QUÍMICA GENERAL
 UNIVERSIDAD MAYOR DE SAN SIMON FACULTAD DE CIENCIAS Y TECNOLOGÍA PLAN GLOBAL QUÍMICA GENERAL I. DATOS DE IDENTIFICACIÓN Nombre de la materia: Química General Código: 2004046 Grupo: 2 Carga horaria: 2 teóricas
UNIVERSIDAD MAYOR DE SAN SIMON FACULTAD DE CIENCIAS Y TECNOLOGÍA PLAN GLOBAL QUÍMICA GENERAL I. DATOS DE IDENTIFICACIÓN Nombre de la materia: Química General Código: 2004046 Grupo: 2 Carga horaria: 2 teóricas
PROGRAMA DE ESTUDIO. Horas de Práctica
 Nombre de la asignatura: BALANCE DE ENERGÍA PROGRAMA DE ESTUDIO Clave:IQM03 Ciclo Formativo: Básico ( ) Profesional ( X ) Especializado ( ) Fecha de elaboración: MARZO DE 2015 Horas Semestre Horas semana
Nombre de la asignatura: BALANCE DE ENERGÍA PROGRAMA DE ESTUDIO Clave:IQM03 Ciclo Formativo: Básico ( ) Profesional ( X ) Especializado ( ) Fecha de elaboración: MARZO DE 2015 Horas Semestre Horas semana
Plan de Estudio: Técnico Agropecuario Duración total del Plan de Estudio: 3 años Duración de cada período lectivo: Un semestre Modalidad educativa:
 Plan de Estudio: Técnico Agropecuario Duración total del Plan de Estudio: 3 años Duración de cada período lectivo: Un semestre Modalidad educativa: Escolarizada. Opción: presencial La Carrera de Técnico
Plan de Estudio: Técnico Agropecuario Duración total del Plan de Estudio: 3 años Duración de cada período lectivo: Un semestre Modalidad educativa: Escolarizada. Opción: presencial La Carrera de Técnico
