BUENOS AIRES, 2 8 ENE 2013
|
|
|
- María Antonia Romero Fidalgo
- hace 6 años
- Vistas:
Transcripción
1 ~desat«d S~deP~, "20IS-Aio de/, ~~ de taa~ ~ ~ de IfIS" ~ióie e 'l~ A.'}t, "Ht. A. 7, 0561 BUENOS AIRES, 2 8 ENE 2013 VISTO el Expediente NO del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica; y CONSIDERANDO: Que por las presentes actuaciones la firma PANALAB S.A. ARGENTINA, solicita la aprobación de nuevos proyectos de prospectos para la Especialidad Medicinal denominada DUTAPIL PANALAB / DUTASTERIDE, Forma farmacéutica y concentración: COMPRIMIDOS 0,5 S mg, aprobada por Certificado NO Que los proyectos presentados se encuadran dentro de los alcances de las normativas vigentes, Ley de Medicamentos , Decreto 150/92 Y la Disposición N : 5904/96. Que los procedimientos para las modificaciones y/o rectificaciones de los datos característicos correspondientes a un certificado de Especialidad Medicinal otorgado en los términos de la Disposición ANMAT NO 5755/96, se encuentran establecidos en la Disposición ANMAT NO 6077/97.
2 ~desaf«d S~de'P~, 1i?eIJ«ladÓn e 'l~ A.1t,?;t, A. 7, " AH4 del g'~ de ea A~ ~ ~ de 1113" Que a fojas 35 obra el informe técnico favorable de la Dirección de Evaluación de Medicamentos. Que se actúa en virtud de las facultades conferidas por los Decretos Nros.: 1.490/92 y 425/10. Por ello: EL INTERVENTOR DE LA ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA DISPONE: ARTICULO 1. - Autorízase el cambio de prospectos presentado para la Especialidad Medicinal denominada DUTAPIL PANALAB / DUTASTERIDE, U Forma farmacéutica y concentración: COMPRIMIDOS 0,5 mg, aprobada por Certificado NO Y Disposición NO 2684/08, propiedad de la firma PANALAB S.A. ARGENTINA, cuyos textos constan de fojas 10 a 21. ARTICULO Sustitúyase en el Anexo II de la Disposición autorizante ANMAT NO 2684/08 los prospectos autorizados por las fojas 10 a 13 de las aprobadas en el artículo 10, los que integrarán en el Anexo 1 de la presente. ARTICULO Acéptase el texto del Anexo de Autorización de modificaciones el cual pasa a formar parte integrante de la presente disposición y el que deberá agregarse al Certificado NO en los términos de la Disposición ANMAT NO 6077/97.
3 .& e "201S - Ai<J dd g'~ de fa A~ ~ ~ de IIIS" ~desaf«d S~ de 'PotitieM, ~adó#e e 'l~ A.1t,?;t, A. 7, ARTICULO Regístrese; por Mesa de Entradas notifíquese al interesado, haciéndole entrega de la copia autenticada de la presente disposición conjuntamente con los prospectos y Anexos, gírese al Departamento de Registro a los fines de confeccionar el legajo correspondiente, Cumplido, Archívese. EXPEDIENTE NO DISPOSICIÓN NO js 0561 ~41;" 1-, Dr. ono A.ÁRSINGHFR SUB-INTERVENTOR Á.N.M.A..':l'.
4 ~desai«d S~ de 'Potiti«u. ~e'l~ ri.1t.?1t. /1. 7. "20IS-/l~ del g'~ de l4/1~ ~ ~ de 111S" ANEXO DE AUTORIZACIÓN DE MODIFICACIONES El Interventor de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT), autorizó mediante Disposición No... O a los efectos de su anexado en el Certificado de Autorización de Especialidad Medicinal NO Y de acuerdo a lo solicitado por la firma PANALAB S.A. ARGENTINA, del producto inscripto en el registro de Especialidades Medicinales (REM) bajo: Nombre comercial/genérico/s: DUTAPIL PANALAB / DUTASTERIDE, Forma farmacéutica y concentración: COMPRIMIDOS 0,5 mg.- Disposición Autorizante de la Especialidad Medicinal NO 2684/08.-, Tramitado por expediente N DATO A MODIFICAR DATO AUTORIZADO MODIFICACION HASTA LA FECHA AUTORIZADA Prospectos. Anexo de Disposición Prospectos de fs. 10 a N 2684/ , corresponde desglosar de fs. 10 a 13.- El presente sólo tiene valor probatorio anexado al certificado de Autorización antes mencionado. Se extiende el presente Anexo de Autorización de Modificaciones del REM
5 ~desai«d S~ de 'Potiti«u. ~ e 'l1t4tit«ttj4 rl.1t. 1ít. ri. 7. "2013 -,4;0 del g'~ M ea,,4~ ~ ~ M 18'13" a la firma PANALAB S.A. ARGENTINA, Titular del Certificado de Autorización NO en la Ciudad de Buenos Aires, a los, 28 ENE 2013 dlas...,del mes de.... Expediente NO DISPOSICIÓN NO js Dr. ono A. ORSINGHFR SUB-INTERVENTOR 4.,N.lIrl.4.!l'.
6 Proyecto de Prospecto o 5 6 'lji : DUTAPIL PANALAB DUTASTERIDE 0.5 mg Comprimidos Industria Argentina Venta Bajo Receta Fórmula cualicuantitativa: Cada comprimido contiene: Dutasteride Lactosa Almidón Pregelatinizado Almidón glicolato de sodio Docusato de sodio Croscaramelosa sódica Povidona K30 Estearato de magnesio 0.5 mg 50.0 mg 25.0mg 25.0mg 5.0mg 15.0 mg 6.0mg 2.5mg Acción terapéutica: Terapia de la Hipertrofia Prostática Benigna Código A Te. G04CB02 Indicaciones: Tratamiento de la hipertrofia prostática benigna (HPB) sintomática en varones con un aumentado tamaño de próstata. Acción Farmacológica: Inhibidor sintético de la 5 alfa reductasa Mecanismo de acción Dutasteride es un 4 aza esteroide que es un inhibidor selectivo de las isoformas tipo I y 11 de la 5 alfa reductasa (una enzima intracelular) que convierte la testosterona a 5 alfa dihidrotestosterona. (DHT) Este esteroide es la causa primaria del crecimiento de la próstata. Reduciendo niveles de DHT, el dutasteride reduce el tamaño de la próstata agrandada. Esta reducción en volumen de la próstata se observa a partir del mes de tratamiento plazo en el cual se mejora el flujo urinario. Dutasteride también mejora síntomas urinarios y reduce el riesgo de AUR (la inhabilidad completa repentina para orinar) y de la cirugía Hipertrofia prostática benigna asociada (HPB) Posología: Varones adultos (incluyendo los senescentes): la posología recomendada de Dutasteride es 1 comprimido (0.5 mg) por vía oral 1 vez al día. Los comprimidos deben tragarse enteros. Dutasteride puede tomarse con o sin comida. Aunque pudiera haber una mejoría precoz, pudiera ser necesario prolongar el tratamiento como mínimo 6 meses a fin de poder evaluar objetivamente si puede obtenerse una respuesta satisfactoria. Insuficiencia renal: no se ha investigado el efecto del compromiso renal sobre la farmacocinética de dutasteride. Sin embargo, no se prevé tener que ajustar la dosis para los pacientes que lo padezcan. G... t<~. U\lIf>..,I-h.. ica Faf. TECNICP 0IRE~.~
7 o 5 6 '11 Insuficiencia hepática: no se ha investigado el efecto del compromiso hepático sobre la farmacocinética de dutasteride (ver Advertencias). Instrucciones de uso y manipulación: Dutasteride se absorbe por la piel y, por lo tanto, las mujeres y los niños tienen que evitar contacto con comprimidos con roturas (ver Precauciones: Embarazo y lactancia). De entrar en contacto con ellas, la zona afectada debe lavarse inmediatamente con jabón yagua. Reacciones Adversas: Se listan, por clase de sistema de órganos y frecuencia de ocurrencia, los efectos adversos relacionados con el medicamento. La frecuencia de ocurrencia se define como: muy común.(~11l0), común.(:::liloo y <1/10), no común.(-:::1i1000 y <1/100), rara.(~iilo,ooo y <111000) y muy rara «1/10,000) Trastornos del sistema inmunitario: Muy raros: reacción alérgica, que incluye exantema, prurito, urticaria y edema localizado. Sistema Urogenital Disminución de la líbido. Impotencia En estudios postcomercialización se ha reportado un aumento de la incidencia de cáncer de próstata de alto grado en hombres tratados con inhibidores de la 5a-reductasa. Advertencias: Dutasteride se absorbe por la piel y, por lo tanto, las mujeres y los niños tienen que evitar contacto con comprimidos con roturas (ver Precauciones: Embarazo y lactancia). De entrar en contacto con ellas, la zona afectada debe lavarse inmediatamente con jabón y agua. No se ha investigado el efecto del compromiso hepático sobre la farmacocinética de dutasteride. Debido a que es extensamente metabolizado y tiene una vida media de 3 a 5 semanas, deberá obrarse con cautela al administrar dutasteride a pacientes con hepatopatías (ver Posología). Efectos sobre el antígeno especifico a la próstata (AEP) y detección del cáncer de próstata: debe realizarse un examen digital del recto, amén de otras evaluaciones para detectar el cáncer de próstata, de los pacientes con HPB antes de instituir el tratamiento con dutasteride, y periódicamente después. La concentración sérica del antígeno específico a la próstata (AEP) es un importante componente del proceso de selección para detectar el cáncer de próstata. Generalmente, una concentración sérica total del AEP de más de 4 ng/ml (Hybritech) exige más evaluaciones y posiblemente una biopsia. El facultativo debe tener presente que un nivel del AEP en la línea base de menos de 4 ng/ml en pacientes que tomen dutasteride no excluye un diagnóstico de cáncer de próstata. A los 6 meses, Dutasteride causa una disminución de los niveles séricos del AEP (por aproximadamente un 50%) en pacientes con HPB, incluso en presencia de cáncer de próstata. Aunque pudiera haber variaciones individuales, la disminución del AEP por aproximadamente un 50% es previsible, dado que se observó a toda la escala de valores del AEP en la línea base (de 1.5 a 10 ng/ml). Por lo tanto, para interpretar un valor aislado del AEP en un yarón tratado con Dutasteride durante 6 meses o más, esos valores deben doblarse para poder compararlos con las escalas normales de los varones no tratados. Este ajuste conserva la sensibilidad y especificidad del análisis del AEP y mantiene su capacidad para detectar el cáncer de próstata. Cualquier aumento sostenido de los niveles de AEP bajo tratamiento con Dutasteride deberá ser cuidadosamente evaluado, y se tendrá en cuenta la posibilidad de que no se haya cumplido con dicho tratamiento. Los niveles séricos totales de AEP vuelven a la línea base a los 6 meses de cesar el tratamiento.
8 La relación de AEP libre a total permanece constante incluso bajo la influencia de Dutasteride. Si el médico decidiera utilizar el porcentaje de AEP libre como ayuda a la detección del cáncer de próstata en los varones sometidos a tratamiento con dutasteride, no parece ser necesario ajustar el valor Precauciones: Se desconoce la importancia clínica del efecto de la dutasteride sobre las características seminales vinculadas con la fertilidad de cada paciente. Embarazo: dutasteride está contraindicado en la mujer. No fue investigada en ella debido a que los datos preclínicos indicaban que la supresión de los niveles circulantes de dihidrotestosterona pudiera inhibir el desarrollo de los órganos genitales externos del feto de una mujer expuesta a dutasteride. Lactancia: no se recomienda el uso de Dutasteride en mujeres que están amamantando. No se sabe si dutasteride se excreta en la leche materna. Los inhibidores de la 5a-reductasa pueden aumentar el riesgo de desarrollo de cáncer de próstata de alto grado. Efectos sobre la capacidad para conducir y utilizar máquinas: en virtud de las propiedades farmacocinéticas y farmacéuticas de dutasteride, no se esperaría que ésta alterara la capacidad para conducir o manejar maquinaria Interacciones Medicamentosas: Los estudios in vitro del metabolismo del fármaco revelaron que el dutasteride es metabolizado por el isoenzíma CYP3A4 del citocromo P450 humano. Por lo tanto, las concentraciones hemáticas de dutasteride pueden aumentar en presencia de inhibidores del CYP3A4 (por ej.: ritonavir, ketoconazol, verapamilo, diltiazem, cimetidina, ciprofloxacino ). Los compuestos cuyas interacciones con dutasteride han sido comprobadas en el ser humano incluyen tamsulosina, terazosina, warfarina, digoxina y colestiramina, y no se observó ninguna interacción clínicamente importante. No se observaron interacciones adversas clínicamente importantes en los estudios clínicos cuando dutasteride se coadministró con antihiperlipidémicos, inhibidores de la enzima convertidora de la angiotensina (ACE), bloqueadores beta-adrenérgicos, bloqueadores del canal de calcio, corticosteroides, diuréticos, antiinflamatorios no esteroideos (AINE), inhibidores de la fosfodiesterasa tipo V y quinolonas. Un estudio de la interacción con los fármacos, en el que se administraron tamsulosina o terazosina en asociación con Dutasteride durante 2 semanas, no reveló indicación alguna de interacciones farmacocinéticas o farmacodinámicas. Un estudio mayor, en el que dutasteride se coadministró con tamsulosina durante hasta 9 meses, demostró que la asociación de Dutasteride con un alfa-bloqueador era bien tolerada Sobredosificación: En estudios realizados dosis únicas de dutasteride de hasta 40 mgldía (80 veces la dosis terapéutica) durante 7 días no mostraron efectos adversos. En los estudios clínicos se administraron dosis de 5 mg diarios a pacientes, durante 6 meses, sin que hubiera más efectos adversos que los observados a la dosis terapéutica de 0.5 mg. No hay un antídoto específico a dutasteride; por consiguiente, de sospecharse una sobredosis, se instituirá el tratamiento sintomático y de apoyo adecuado. Conservación: Conservar en lugar seco, a menos de 30 oc, en su estuche original. Evitar la exposición a la luz.
9 Presentaciones: Envases por 10/20/30/40/50/90 comprimidos para la venta al público y 500 Y 1000 para uso exclusivo de hospitales MANTENER FUERA DEL ALCANCE DE LOS NIÑOS "Este medicamento debe ser administrado bajo prescripción médica y no puede repetirse sin mediar una nueva receta" Especialidad Medicinal autorizada por el Ministerio de Salud Certificado N : Laboratorio Panalab S.A. Argentina Famatina 3415, CABA C1437IOK. Tel Directora Técnica: María Gabriela Palma - Farmacéutica Elaborado en Laprida 43, Avellaneda, Peía. De Buenos Aires Fecha de última revisión:....!....!.... (' I \.
BUENOS AIRES, 1 7 ASO 201! la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica;
 ~desai.«d S«JIeta!Úa de 'P~. ;;~(ió.e e 1n4tit«t04!'I.n. m.!'i. 7. OIiIPOBICIOIIII' BUENOS AIRES, 1 7 ASO 201! VISTO el Expediente NO 1-0047-0000-005152-12-3 del Registro de la Administración Nacional
~desai.«d S«JIeta!Úa de 'P~. ;;~(ió.e e 1n4tit«t04!'I.n. m.!'i. 7. OIiIPOBICIOIIII' BUENOS AIRES, 1 7 ASO 201! VISTO el Expediente NO 1-0047-0000-005152-12-3 del Registro de la Administración Nacional
DISPOSiCiÓN N } BUENOS AIRES, Disposición NO 1306/13 del registro de la Administración Nacional de
 Swzet4JÚ4 de '1'ofitiUl4, ~~e1~ r/,1t,m,r/, 7. DISPOSiCiÓN N 4-5 2 4} BUENOS AIRES, e 8 jun ZOlí VISTO el Expediente NO 1-0047-0000-002237-15-4 Y Disposición NO 1306/13 del registro de la Administración
Swzet4JÚ4 de '1'ofitiUl4, ~~e1~ r/,1t,m,r/, 7. DISPOSiCiÓN N 4-5 2 4} BUENOS AIRES, e 8 jun ZOlí VISTO el Expediente NO 1-0047-0000-002237-15-4 Y Disposición NO 1306/13 del registro de la Administración
BUENOS AIRES, 1-lMAR Z015. Administración Nacionalde Medicamentos, Alimentos y Tecnología Médica;
 DISPOSICION N 2245 BUENOS AIRES, 1-lMAR Z015 VISTO el Expediente NO 1-47-0000-9698-11-4 del registro de la Administración Nacionalde Medicamentos, Alimentos y Tecnología Médica; y CONSIDERANDO: Que por
DISPOSICION N 2245 BUENOS AIRES, 1-lMAR Z015 VISTO el Expediente NO 1-47-0000-9698-11-4 del registro de la Administración Nacionalde Medicamentos, Alimentos y Tecnología Médica; y CONSIDERANDO: Que por
Hipersensibilidad a cualquiera de los componentes de este producto.
 PROSCAR 5 mg TABLETAS RECUBIERTAS (Finasteride) PROSCAR (Finasteride) un compuesto sintético 4 azasteroide, es un inhibidor específico de la 5α - reductasa Tipo II, una enzima intracelular que metaboliza
PROSCAR 5 mg TABLETAS RECUBIERTAS (Finasteride) PROSCAR (Finasteride) un compuesto sintético 4 azasteroide, es un inhibidor específico de la 5α - reductasa Tipo II, una enzima intracelular que metaboliza
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TEALEP 2. Nombre Genérico: FINASTERIDA 3. Forma Farmacéutica y Formulación: Comprimidos. Cada comprimido contiene: Finasterida... 5 mg Excipiente
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TEALEP 2. Nombre Genérico: FINASTERIDA 3. Forma Farmacéutica y Formulación: Comprimidos. Cada comprimido contiene: Finasterida... 5 mg Excipiente
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA. Gotas Óticas. Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g.
 DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
DISPOSICiÓN N' 7 5 6 9 BUENOS AIRES, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica;
 ~desai«d S~ de ídog~4. jl ~dq.e e 'J1f4t(«t04 rl.1t.?it. ri. 7. "2011-1'1,;0 del 7..a14p 7)e«4e. ea SaI.«d 9 S~ de tm. ~~.. DISPOSICiÓN N' 7 5 6 9 BUENOS AIRES, o 7 NOV 2011 VISTO el Expediente NO 1-0047-0000-018003-11-8
~desai«d S~ de ídog~4. jl ~dq.e e 'J1f4t(«t04 rl.1t.?it. ri. 7. "2011-1'1,;0 del 7..a14p 7)e«4e. ea SaI.«d 9 S~ de tm. ~~.. DISPOSICiÓN N' 7 5 6 9 BUENOS AIRES, o 7 NOV 2011 VISTO el Expediente NO 1-0047-0000-018003-11-8
PROSTENE. FINASTERIDE 5 mg. Comprimidos recubiertos Industria Argentina Venta bajo receta
 PROSTENE FINASTERIDE 5 mg Comprimidos recubiertos Industria Argentina Venta bajo receta FORMULA: Cada comprimido recubierto contiene: Finasteride 5 mg Excipientes: lactosa, dioctilsulfosuccinato de sodio,
PROSTENE FINASTERIDE 5 mg Comprimidos recubiertos Industria Argentina Venta bajo receta FORMULA: Cada comprimido recubierto contiene: Finasteride 5 mg Excipientes: lactosa, dioctilsulfosuccinato de sodio,
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg COMPRIMIDOS RECUBIERTOS ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg COMPRIMIDOS RECUBIERTOS ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Comprimidos
; ~e'7~ A.n, 1ít,A. 7.
 ~desat«d swze:tajúa de 'P~, ; ~e'7~ A.n, 1ít,A. 7. BUENOS AIRES,! 2 MAY 1012 VISTO el Expediente NO 1-0047-0000-006700-12-2 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología
~desat«d swze:tajúa de 'P~, ; ~e'7~ A.n, 1ít,A. 7. BUENOS AIRES,! 2 MAY 1012 VISTO el Expediente NO 1-0047-0000-006700-12-2 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
BUENOSAIRES, 1 Z feb Nacional de Medicamentos, Alimentos y Tecnología Medica; EDGARDOJORGEGEZZI S.R.L. solicita la aprobación de nuevos
 C9eda~e 1~ ri.1t.?/t.ri. 7. DISPOSICION N. ~534 BUENOSAIRES, 1 Z feb 2015 VISTO el Expediente NO 1-0047-0000-002431-14-1 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología
C9eda~e 1~ ri.1t.?/t.ri. 7. DISPOSICION N. ~534 BUENOSAIRES, 1 Z feb 2015 VISTO el Expediente NO 1-0047-0000-002431-14-1 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA 3. FORMA FARMACÉUTICA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
BUENOSAIRES, 3 O ENE la Administración Nacional de Medicamentos, Alimentos y Tecnología Me1dica;
 DISPOSiCiÓN N' 1 1 8 4' BUENOSAIRES, 3 O ENE 2015 VISTO el Expediente NO 1-0047-0000-019782-13-9 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología Me1dica; y I. CONSIDERANDO:
DISPOSiCiÓN N' 1 1 8 4' BUENOSAIRES, 3 O ENE 2015 VISTO el Expediente NO 1-0047-0000-019782-13-9 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología Me1dica; y I. CONSIDERANDO:
LABORATORIOS NORMON, S.A.
 1. NOMBRE DEL MEDICAMENTO normoval 250 mg comprimidos recubiertos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto de normoval contiene: 250 mg de extracto hidroalcohólico seco de raíz
1. NOMBRE DEL MEDICAMENTO normoval 250 mg comprimidos recubiertos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto de normoval contiene: 250 mg de extracto hidroalcohólico seco de raíz
DISPOSICION N'
 "2011 - Año del Trabajo Decente, la Salud y Seguridad de los Trabajadores" Ministerio de Salud DISPOSICION N' 6 9 2 9 BUENOS AIRES, 11 OCI 2011 VISTO el Expediente N 1-47-10305-10-9 del Registro de esta
"2011 - Año del Trabajo Decente, la Salud y Seguridad de los Trabajadores" Ministerio de Salud DISPOSICION N' 6 9 2 9 BUENOS AIRES, 11 OCI 2011 VISTO el Expediente N 1-47-10305-10-9 del Registro de esta
BUENOSAIRES'1 7 JUN 2013. VISTO el Expediente NO 1-0047-0000-005887-13-5 Y. VARIFARMA SA, solicita la corrección de errores materiales que se
 8 "20/S ~eúsat«d Se
8 "20/S ~eúsat«d Se
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
Alivio de los sofocos que aparecen durante la menopausia como consecuencia de la deprivación estrogénica.
 1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Finasterida RANBAXY 5mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida RANBAXY 5mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida RANBAXY 5mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes:
DOCUMENTO DE PRODUCTO LOCAL PFIZER VENEZUELA, S.A. Preparado por Pfizer Inc. Fecha efectiva de CDS: 28 DIC Fecha CDS que reemplaza: 25 JUN 2014
 MALEATO DE TRIMEBUTINA 28 DIC 2015 DOCUMENTO DE PRODUCTO LOCAL PFIZER VENEZUELA, S.A. Preparado por Pfizer Inc. Fecha efectiva de CDS: 28 DIC 2015 Fecha CDS que reemplaza: 25 JUN 2014 MALEATO DE TRIMEBUTINA
MALEATO DE TRIMEBUTINA 28 DIC 2015 DOCUMENTO DE PRODUCTO LOCAL PFIZER VENEZUELA, S.A. Preparado por Pfizer Inc. Fecha efectiva de CDS: 28 DIC 2015 Fecha CDS que reemplaza: 25 JUN 2014 MALEATO DE TRIMEBUTINA
Prospecto: información para el usuario
 Prospecto: información para el usuario FINASTERIDA QUALIGEN 5 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
Prospecto: información para el usuario FINASTERIDA QUALIGEN 5 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
FICHA TÉCNICA. KETOISDIN 400 mg óvulos está indicado en adultos para el tratamiento local de
 1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
e~dmt e 'l~ A, 1t,m,A, 7, OISPOSICION N~ 5' 9 r
 ~desa!«d Swzetaúa de PofitúM, e~dmt e 'l~ A, 1t,m,A, 7, OISPOSICION N~ 5' 9 r BUENOS AIRES, 13 SEP 2012 VISTO el Expediente N 1-0047-0000-008209-11-9 del Registro de la Administración Nacional de Medicamentos,
~desa!«d Swzetaúa de PofitúM, e~dmt e 'l~ A, 1t,m,A, 7, OISPOSICION N~ 5' 9 r BUENOS AIRES, 13 SEP 2012 VISTO el Expediente N 1-0047-0000-008209-11-9 del Registro de la Administración Nacional de Medicamentos,
PROSPECTO. CEFTRIAXONA REIG JOFRÉ 1 g IM. Polvo y disolvente para solución inyectable. E.F.G. Ceftriaxona (D.C.I.)
 PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
GO Sildenafil Tabletas
 GO Sildenafil Tabletas FORMA FARMACÉUTICA Y FORMULACIÓN: Cada TABLETA contiene: Citrato de sildenafil equivalente a 25, 50 y 100 mg de sildenafil Excipiente cbp 1 tableta Cada TABLETA (orodispersable)
GO Sildenafil Tabletas FORMA FARMACÉUTICA Y FORMULACIÓN: Cada TABLETA contiene: Citrato de sildenafil equivalente a 25, 50 y 100 mg de sildenafil Excipiente cbp 1 tableta Cada TABLETA (orodispersable)
BUENOSAIRES, 1 3 ENE 2014. Registro de la Administración Nacional de Medicamentos, Alimentos y
 ~d
~d
~desat«d S~ de'poiltua4, ;e~e'l_ A, n,?1t,a. 7.
 ~desat«d S~ de'poiltua4, ;e~e'l_ A, n,?1t,a. 7. "2015 - AÑO DEL BICENTENARIO DEL CONGRESO DE LOS PUEBLOS LIBRES" DI8~OSI0l(\NN' BUENOSAIRES, 1'l MAY 2015 VISTO el Expediente NO 1-0047-0000-003133-15-0
~desat«d S~ de'poiltua4, ;e~e'l_ A, n,?1t,a. 7. "2015 - AÑO DEL BICENTENARIO DEL CONGRESO DE LOS PUEBLOS LIBRES" DI8~OSI0l(\NN' BUENOSAIRES, 1'l MAY 2015 VISTO el Expediente NO 1-0047-0000-003133-15-0
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Principio activo: 18,42 mg de benazepril (equivalente a 20 mg de benazepril hidrocloruro)
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BENAKOR 20 mg COMPRIMIDOS PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principio
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BENAKOR 20 mg COMPRIMIDOS PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principio
FICHA TECNICA. Tratamiento de la intoxicación por Amanita phalloides.
 FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
Ó MEJORAL PARA NIÑOS Y MEJORAL PARA NIÑOS JUNIOR / PARACETAMOL,
 ~desat«l-. Swzeta/Úa. de 'P0t/tua4, ;e~e1~ A.n.?1t. A. 7.... 2014- A.t4
~desat«l-. Swzeta/Úa. de 'P0t/tua4, ;e~e1~ A.n.?1t. A. 7.... 2014- A.t4
FICHA TÉCNICA. Por sobre: Acetato de calcio, 2,5 g (equivale a 635 mg de calcio), almidón de maíz, manitol (E421)
 FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
BUENOS AIRES, 1 3 DIe Administración Nacional de Medicamentos, Alimentos y Tecnología
 SwrdaIÚa de 'POtitiUl4. er;edadóle e 1~ A 1t.11t. A 7. 8287 BUENOS AIRES, 1 3 DIe 2 011 VISTO el Expediente NO 1-0047-0000-015934-10-3 de la Administración Nacional de Medicamentos, Alimentos y Tecnología
SwrdaIÚa de 'POtitiUl4. er;edadóle e 1~ A 1t.11t. A 7. 8287 BUENOS AIRES, 1 3 DIe 2 011 VISTO el Expediente NO 1-0047-0000-015934-10-3 de la Administración Nacional de Medicamentos, Alimentos y Tecnología
FICHA TÉCNICA. Cada comprimido recubierto con película contiene 5 mg de finasterida.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida TecniGen 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Finasterida TecniGen 5 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 5 mg
ORIFUNGAL Crema KETOCONAZOL
 ORIFUNGAL Crema KETOCONAZOL JANSSEN-CILAG Venta bajo receta Para uso externo exclusivamente Industria Brasileña FORMULA: Cada gramo de crema contiene: Ketoconazol 20 mg. Excipientes: Propilenglicol, Alcohol
ORIFUNGAL Crema KETOCONAZOL JANSSEN-CILAG Venta bajo receta Para uso externo exclusivamente Industria Brasileña FORMULA: Cada gramo de crema contiene: Ketoconazol 20 mg. Excipientes: Propilenglicol, Alcohol
FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO. URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Benzbromarona (D.C.I.)...100 mg
FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Benzbromarona (D.C.I.)...100 mg
FICHA TÉCNICA. Tratamiento de la incontinencia urinaria asociada a la insuficiencia del esfínter uretral en la perra.
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 DELTAGEL COMPRIMIDOS MASTICABLES ANTIÁCIDO Página 1 DELTAGEL Comprimidos Masticables Principio Activo Hidróxido
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 DELTAGEL COMPRIMIDOS MASTICABLES ANTIÁCIDO Página 1 DELTAGEL Comprimidos Masticables Principio Activo Hidróxido
LLD Abreviado de Zoloft. Todo medicamento debe conservarse fuera del alcance de los niños.
 LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
FICHA TÉCNICA. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada comprimido contiene: Acido ursodeoxicólico, 150 mg Excipientes: Ver 6.1.
 FICHA TÉCNICA URSOCHOL 1. NOMBRE DEL MEDICAMENTO URSOCHOL comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada comprimido contiene: Acido ursodeoxicólico, 150 mg Excipientes: Ver 6.1. 3. FORMA FARMACÉUTICA:
FICHA TÉCNICA URSOCHOL 1. NOMBRE DEL MEDICAMENTO URSOCHOL comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada comprimido contiene: Acido ursodeoxicólico, 150 mg Excipientes: Ver 6.1. 3. FORMA FARMACÉUTICA:
PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg
 PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg Lea cuidadosamente este folleto antes de la administración de este medicamento, contiene información importante acerca de su tratamiento. Si
PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg Lea cuidadosamente este folleto antes de la administración de este medicamento, contiene información importante acerca de su tratamiento. Si
BUENOSAIRES, 22 ENE de la Administración Nacional de Medicamentos, Alimentos y Tecnología
 I ~desatd Se«daIÚa de 'PoI1t«44, ~'9~e'7~ r/,n.?it.r/. 7. DISPOSIC.ON N.O 6 4 2 BUENOSAIRES, 22 ENE 2014 VISTO el Expediente NO 1-0047-0000-005613-13-8 del Registro de la Administración Nacional de Medicamentos,
I ~desatd Se«daIÚa de 'PoI1t«44, ~'9~e'7~ r/,n.?it.r/. 7. DISPOSIC.ON N.O 6 4 2 BUENOSAIRES, 22 ENE 2014 VISTO el Expediente NO 1-0047-0000-005613-13-8 del Registro de la Administración Nacional de Medicamentos,
Boletín de Actualización Farmacoterapeutica
 Cátedra de Farmacia Clínica y Asistencial Depto. de Ciencias Biológicas Facultad de Ciencias Exactas - Universidad Nacional de La Plata Calle 47 esq 115 - (1900) La Plata (54 221) 423-0121 Int.53 Boletín
Cátedra de Farmacia Clínica y Asistencial Depto. de Ciencias Biológicas Facultad de Ciencias Exactas - Universidad Nacional de La Plata Calle 47 esq 115 - (1900) La Plata (54 221) 423-0121 Int.53 Boletín
Excipientes con efecto conocido: Cada gramo de crema contiene 200 mg de propilenglicol, 75 mg de alcohol estearílico y 20 mg de alcohol cetílico.
 1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de crema contiene
1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de crema contiene
Prospecto: Información para el usuario Finasterida Bluefish 1 mg comprimidos recubiertos con película EFG
 Prospecto: Información para el usuario Finasterida Bluefish 1 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento porque contiene información
Prospecto: Información para el usuario Finasterida Bluefish 1 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento porque contiene información
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Emeprid 1 mg/ml solución oral para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Emeprid 1 mg/ml solución oral para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
"2012 - Año de Homenaje al doctor D. MANUD. /J1:"/J;IIAWr BUENOS AIRES, O 1 MAR 2012
 A.NMA.T "2012 - Año de Homenaje al doctor D. MANUD. /J1:"/J;IIAWr 11 9 4 BUENOS AIRES, O 1 MAR 2012 VISTO el Expediente N 1-47-0000-19586-11-9 del Registro de la Administración Nacional de Medicamentos,
A.NMA.T "2012 - Año de Homenaje al doctor D. MANUD. /J1:"/J;IIAWr 11 9 4 BUENOS AIRES, O 1 MAR 2012 VISTO el Expediente N 1-47-0000-19586-11-9 del Registro de la Administración Nacional de Medicamentos,
BUENOS AIRES, VISTO el Expediente NO 1-0047-0000-022126-10-5 del Registro de
 ~desai«d SeeuúvÚ4 de 'PeGtíea6. 'Rt9UÚef4.e e 1 'f4tim-tu A.1t.??t.A. 7. DISposrcrON N~ O 5 8 1 BUENOS AIRES, 25 ENE ldii VISTO el Expediente NO 1-0047-0000-022126-10-5 del Registro de la Administración
~desai«d SeeuúvÚ4 de 'PeGtíea6. 'Rt9UÚef4.e e 1 'f4tim-tu A.1t.??t.A. 7. DISposrcrON N~ O 5 8 1 BUENOS AIRES, 25 ENE ldii VISTO el Expediente NO 1-0047-0000-022126-10-5 del Registro de la Administración
FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina
 FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Hipolipemiante, inhibidor de la enzima hidroximetil-glutaril-coa-reductasa.. 1.2 Cómo actúa este fármaco: Inhibe
FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Hipolipemiante, inhibidor de la enzima hidroximetil-glutaril-coa-reductasa.. 1.2 Cómo actúa este fármaco: Inhibe
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
~desat«d SecutaJÚ4de 'P~, íl!?e9<daed.t e 1~,,4,1t,m,A. 7,
 ~desat«d SecutaJÚ4de 'P~, íl!?e9
~desat«d SecutaJÚ4de 'P~, íl!?e9
Ministerio de Salud Secretaría de Políticas, Regulación y Relaciones Sanitarias A.N.M.A.T.
 BUENOS AIRES, 24 Oct 2007 VISTO la Resolución del ex y Acción Social Nº 706/93, la Disposición Nº 5904/96, la Disposición Nº 3855/98, el Expediente Nº 1-0047- 0000-016483-07-1 del registro de esta Administración
BUENOS AIRES, 24 Oct 2007 VISTO la Resolución del ex y Acción Social Nº 706/93, la Disposición Nº 5904/96, la Disposición Nº 3855/98, el Expediente Nº 1-0047- 0000-016483-07-1 del registro de esta Administración
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CALCIO-500 D COMPRIMIDOS RECUBIERTOS SUPLEMENTO MINERAL Página 1 CALCIO-500 D Comprimidos Recubiertos Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CALCIO-500 D COMPRIMIDOS RECUBIERTOS SUPLEMENTO MINERAL Página 1 CALCIO-500 D Comprimidos Recubiertos Principio
Prospecto: Información para el usuario. Finasteridaratiopharm 5 mg comprimidos recubiertos con película EFG
 Prospecto: Información para el usuario Finasteridaratiopharm 5 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información
Prospecto: Información para el usuario Finasteridaratiopharm 5 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información
GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos
 GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos Industria Alemana EXPENDIO BAJO RECETA Nota importante: Antes de recetar este medicamento, consulte toda la información relativa a su prescripción.
GLUCEMIX VILDAGLIPTINA / METFORMINA Comprimidos recubiertos Industria Alemana EXPENDIO BAJO RECETA Nota importante: Antes de recetar este medicamento, consulte toda la información relativa a su prescripción.
BUENOS AIRES, 13 NOV 2012. concentración: COMPRIMIDOS RECUBIERTOS, 500 mg - 100 mg,
 4 e1 ~desatad SwzeúvÚa, de Pofittu4, ~e1~ 6 6 O 9 A, n.m,a. 7. DISPOSICiÓN N BUENOS AIRES, 13 NOV 2012 VISTO el Expediente NO 1-0047-0000-010756-12-0 del Registro de la Administración Nacional de Medicamentos,
4 e1 ~desatad SwzeúvÚa, de Pofittu4, ~e1~ 6 6 O 9 A, n.m,a. 7. DISPOSICiÓN N BUENOS AIRES, 13 NOV 2012 VISTO el Expediente NO 1-0047-0000-010756-12-0 del Registro de la Administración Nacional de Medicamentos,
BUENOSAIRES, 1 O MAR 2015. la Administración Nacional de Medicamentos, Alimentos y TeC~OIOgía
 Ministerio de Salud Secretaría de Políticas Regulación e nstitutos DlSPOSOÓN N" 2016 BUENOSARES 1 O MAR 2015 VSTO el Expediente NO 1-47-0000-002228-14-1 del registro de la Administración Nacional de Medicamentos
Ministerio de Salud Secretaría de Políticas Regulación e nstitutos DlSPOSOÓN N" 2016 BUENOSARES 1 O MAR 2015 VSTO el Expediente NO 1-47-0000-002228-14-1 del registro de la Administración Nacional de Medicamentos
,,. - - -j BUENOSAIRES, de la Administración Nacional de Medicamentos, Alimentos y Tecnología
 , ~desaiad Swreú/JÚ4 de 1'0fitiu4, ; ~«tadó.ee 1~ A.1t, m.a. 7, DISPOSICION,,. - - -j No 7740 BUENOSAIRES, 18 ole 2013 VISTO el Expediente NO 1-0047-0000-018483-13-1 del Registro de la Administración Nacional
, ~desaiad Swreú/JÚ4 de 1'0fitiu4, ; ~«tadó.ee 1~ A.1t, m.a. 7, DISPOSICION,,. - - -j No 7740 BUENOSAIRES, 18 ole 2013 VISTO el Expediente NO 1-0047-0000-018483-13-1 del Registro de la Administración Nacional
BUENOS AIRES, 1. 8 ENE 2013
 ~4eSat«d S~4e?~, 1!:~e'7~ rl.1t.??t. ri.,. "201S - Aio dd g'~ de ea A~ ~ ~ de 1915" BUENOS AIRES, 1. 8 ENE 2013 VISTO el Expediente NO 1-0047-0000-021121-12-4 del Registro de la Administración Nacional
~4eSat«d S~4e?~, 1!:~e'7~ rl.1t.??t. ri.,. "201S - Aio dd g'~ de ea A~ ~ ~ de 1915" BUENOS AIRES, 1. 8 ENE 2013 VISTO el Expediente NO 1-0047-0000-021121-12-4 del Registro de la Administración Nacional
BUENOS AIRES, 1 Z MAR aprobación de nueva información para el paciente para el producto APRIL
 ~desabd S~ de 'Pofitiea4. íl!?ettedaed.e e 11t4tt't«t64 A.1t.?It. A. 7. DISPOSICION N" 1, 9 6 BUENOS AIRES, 1 Z MAR 2012 VISTO el Expediente NO 1-0047-0000-011054-11-1 del Registro de la Administración
~desabd S~ de 'Pofitiea4. íl!?ettedaed.e e 11t4tt't«t64 A.1t.?It. A. 7. DISPOSICION N" 1, 9 6 BUENOS AIRES, 1 Z MAR 2012 VISTO el Expediente NO 1-0047-0000-011054-11-1 del Registro de la Administración
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR
 INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR 1. NOMBRE DEL MEDICAMENTO Disolgas 257,5 mg cápsulas blandas 2. PRINCIPIO(S) ACTIVO(S) 3. LISTA DE EXCIPIENTES Amarillo anaranjado S (E 110), azorrubina
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR 1. NOMBRE DEL MEDICAMENTO Disolgas 257,5 mg cápsulas blandas 2. PRINCIPIO(S) ACTIVO(S) 3. LISTA DE EXCIPIENTES Amarillo anaranjado S (E 110), azorrubina
KLOSARTAN LOSARTÁN POTÁSICO 50/100 mg
 KLOSARTAN LOSARTÁN POTÁSICO 50/100 mg Venta bajo receta Industria Argentina Comprimidos recubiertos FÓRMULA CUALICUANTITATIVA: Cada comprimido recubierto de 50 mg contiene: Losartán potásico 50 mg Excipientes:
KLOSARTAN LOSARTÁN POTÁSICO 50/100 mg Venta bajo receta Industria Argentina Comprimidos recubiertos FÓRMULA CUALICUANTITATIVA: Cada comprimido recubierto de 50 mg contiene: Losartán potásico 50 mg Excipientes:
BUENOSAIRES,1 7 JUN 2013. de la Administración Nacional de Medicamentos, Alimentos y Tecnología
 ~
~
PRUCAL PRUCALOPRIDE Comprimidos recubiertos Vía oral FÓRMULAS
 INDUSTRIA ARGENTINA VENTA BAJO RECETA PRUCAL PRUCALOPRIDE Comprimidos recubiertos Vía oral PRUCAL 1 FÓRMULAS Cada comprimido recubierto contiene: Prucalopride (como Prucalopride Succinato) 1,00 mg. Excipientes:
INDUSTRIA ARGENTINA VENTA BAJO RECETA PRUCAL PRUCALOPRIDE Comprimidos recubiertos Vía oral PRUCAL 1 FÓRMULAS Cada comprimido recubierto contiene: Prucalopride (como Prucalopride Succinato) 1,00 mg. Excipientes:
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Finasterida Germed 5 mg comprimidos recubiertos con película EFG Finasterida
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Finasterida Germed 5 mg comprimidos recubiertos con película EFG Finasterida Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve
PROSPECTO: INFORMACIÓN PARA EL USUARIO Finasterida Germed 5 mg comprimidos recubiertos con película EFG Finasterida Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve
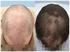
Datos: Propecia está aprobado para tratar la calvicie masculina.
 Comunicación de seguridad de Medicamentos de la FDA: la 5-alfa reductasa (5-ARI) puede aumentar el riesgo de una forma más grave de cáncer de próstata. Datos: Inhibidores de la 5-alfa-reductasa son un
Comunicación de seguridad de Medicamentos de la FDA: la 5-alfa reductasa (5-ARI) puede aumentar el riesgo de una forma más grave de cáncer de próstata. Datos: Inhibidores de la 5-alfa-reductasa son un
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERGOTAMINA + CAFEÍNA 1/100 mg COMPRIMIDOS RECUBIERTOS ANALGÉSICO, ANTIMIGRAÑOSO Página 1 ERGOTAMINA + CAFEÍNA 1/100
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERGOTAMINA + CAFEÍNA 1/100 mg COMPRIMIDOS RECUBIERTOS ANALGÉSICO, ANTIMIGRAÑOSO Página 1 ERGOTAMINA + CAFEÍNA 1/100
FICHA TECNICA. (1) Equivalente a 185,2 mg de hidróxido de magnesio.
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION Por 5 ml: Principios activos: Gel de hidróxido alumínico... 350 mg Hidróxido magnésico... 20 mg Por comprimido: Principio activo: Hidróxido alumínico...
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION Por 5 ml: Principios activos: Gel de hidróxido alumínico... 350 mg Hidróxido magnésico... 20 mg Por comprimido: Principio activo: Hidróxido alumínico...
Composición Cada 100 ml de solución oftálmica de liberación prolongada contiene:
 CARTENS 1% y 2% Clorhidrato de Carteolol Solución Oftálmica de Liberación Prolongada Industria Argentina Venta bajo receta Composición Cada 100 ml de solución oftálmica de liberación prolongada contiene:
CARTENS 1% y 2% Clorhidrato de Carteolol Solución Oftálmica de Liberación Prolongada Industria Argentina Venta bajo receta Composición Cada 100 ml de solución oftálmica de liberación prolongada contiene:
Para la lista completa de excipientes, véase la sección Indicaciones de uso, especificando las especies de destino
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
Finastar. FINASTAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA. Esta especialidad se presenta como:
 Finastar FINASTAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: FINASTAR 5 mg cuya composición es: - Principio activo: Finasterida 5 mg - Excipientes (ver
Finastar FINASTAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: FINASTAR 5 mg cuya composición es: - Principio activo: Finasterida 5 mg - Excipientes (ver
Prospecto: información para el paciente Ebastel Forte 20 mg Comprimidos recubiertos con película. Ebastina
 Prospecto: información para el paciente Ebastel Forte 20 mg Comprimidos recubiertos con película Ebastina Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
Prospecto: información para el paciente Ebastel Forte 20 mg Comprimidos recubiertos con película Ebastina Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 BROMHEXINA 4 mg/5 ml JARABE MUCOLÍTICO, EXPECTORANTE Página 1 BROMHEXINA 4 mg/5 ml Jarabe Principio Activo Bromhexina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 BROMHEXINA 4 mg/5 ml JARABE MUCOLÍTICO, EXPECTORANTE Página 1 BROMHEXINA 4 mg/5 ml Jarabe Principio Activo Bromhexina
BUENOS AIRES, 2 7 Die 2010
 !Ministerio áe Safuá Secretaria áe Pofíticas, 'i fgufación }I.J{.!M.}I. 'T. "2010 -}lño áe{(]3icentenario áe fa!j(fvo{ución áe!mayo' DISPOSIC ON N" BUENOS AIRES, 2 7 Die 2010 VISTO el Expediente no 1-47-1110-158/08-8
!Ministerio áe Safuá Secretaria áe Pofíticas, 'i fgufación }I.J{.!M.}I. 'T. "2010 -}lño áe{(]3icentenario áe fa!j(fvo{ución áe!mayo' DISPOSIC ON N" BUENOS AIRES, 2 7 Die 2010 VISTO el Expediente no 1-47-1110-158/08-8
Ministerio de Salud Secretaría de Políticas, Regulación y Relaciones Sanitarias A.N.M.A.T.
 BUENOS AIRES, 17 Sep 2007 VISTO la Resolución del ex y Acción Social Nº 706/93, la Disposición Nº 5904/96, la Disposición Nº 3855/98, el Expediente Nº 1-0047- 0000-015925-07-2 del registro de esta Administración
BUENOS AIRES, 17 Sep 2007 VISTO la Resolución del ex y Acción Social Nº 706/93, la Disposición Nº 5904/96, la Disposición Nº 3855/98, el Expediente Nº 1-0047- 0000-015925-07-2 del registro de esta Administración
Repafet. Rupatadina Tabletas. Rupatadina II.- DENOMINACIÓN GENÉRICA: III.- FORMA FARMACÉUTICA Y FORMULACIÓN:
 Repafet Rupatadina Tabletas II.- DENOMINACIÓN GENÉRICA: Rupatadina III.- FORMA FARMACÉUTICA Y FORMULACIÓN: Cada tableta contiene: Fumarato de Rupatadina equivalente a... 10 mg de Rupatadina Excipiente
Repafet Rupatadina Tabletas II.- DENOMINACIÓN GENÉRICA: Rupatadina III.- FORMA FARMACÉUTICA Y FORMULACIÓN: Cada tableta contiene: Fumarato de Rupatadina equivalente a... 10 mg de Rupatadina Excipiente
PROSCAR (finasterida) PROSCAR 5 mg cuya composición es: - Principio activo: Finasterida... 5 mg - Excipientes (ver 6.1), c.s.p...
 FICHA TÉCNICA IPC - 0199 Tracer No. PSC-E-20030237 01/03 PROSCAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: PROSCAR 5 mg cuya composición es: - Principio
FICHA TÉCNICA IPC - 0199 Tracer No. PSC-E-20030237 01/03 PROSCAR (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: PROSCAR 5 mg cuya composición es: - Principio
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VETMEDIN 5 mg COMPRIMIDOS MASTICABLES PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido masticable
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VETMEDIN 5 mg COMPRIMIDOS MASTICABLES PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido masticable
La posología recomendada es un comprimido diario de 5 mg, con o sin alimentos.
 1. NOMBRE DEL MEDICAMENTO PROSCAR 5 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes con efecto conocido: 106,40
1. NOMBRE DEL MEDICAMENTO PROSCAR 5 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de finasterida. Excipientes con efecto conocido: 106,40
BUENOS AIRES, 2 1 FEB 2013
 ~desa6td S~deP~, ~~e'l~ A.1t.??t. A. 7. "201S - Ai4 dd g'~ de f4 A~ ~ ~ de 111S" BUENOS AIRES, 2 1 FEB 2013 VISTO el Expediente NO 1-0047-0000-013887-12-2 del Registro de la Administración Nacional de
~desa6td S~deP~, ~~e'l~ A.1t.??t. A. 7. "201S - Ai4 dd g'~ de f4 A~ ~ ~ de 111S" BUENOS AIRES, 2 1 FEB 2013 VISTO el Expediente NO 1-0047-0000-013887-12-2 del Registro de la Administración Nacional de
EUCOPROST (finasterida)
 FICHA TÉCNICA para Médicos IPC 0997a Tracer No. PSC-E-14800 07/99 EUCOPROST (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: EUCOPROST 5 mg cuya composición es:
FICHA TÉCNICA para Médicos IPC 0997a Tracer No. PSC-E-14800 07/99 EUCOPROST (finasterida) 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Esta especialidad se presenta como: EUCOPROST 5 mg cuya composición es:
CLARITYNE 10 mg comprimidos Loratadina
 PROSPECTO: INFORMACIÓN PARA EL USUARIO CLARITYNE 10 mg comprimidos Loratadina Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede adquirirse sin
PROSPECTO: INFORMACIÓN PARA EL USUARIO CLARITYNE 10 mg comprimidos Loratadina Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede adquirirse sin
de la Administración Nacional de Medicamentos, Alimentos y Tecnología CABUCHI S.A., solicita la aprobación de nuevos proyectos de prospectos
 ~desatad Swr.etalÚ4 de p~, ;;ef)cd4~ e 1H4ti~ /1,n,'/1t,/1, 7, DISPOS1CIÚN N0 BUENOS AIRES, 18 Ole 2014 VISTO el Expediente N 1-0047-0000-002528-14-8 del Registro de la Administración Nacional de Medicamentos,
~desatad Swr.etalÚ4 de p~, ;;ef)cd4~ e 1H4ti~ /1,n,'/1t,/1, 7, DISPOS1CIÚN N0 BUENOS AIRES, 18 Ole 2014 VISTO el Expediente N 1-0047-0000-002528-14-8 del Registro de la Administración Nacional de Medicamentos,
FICHA TÉCNICA. ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
DiS?OSICIÚN N BUENOS AIRES, 2 2 FEB. 2016. Registro de la Administración Nacional de Medicamentos, Alimentos y
 ~desat«d S~de'P~, 'R~e1_ 1'11t?/t.,,4. 7. DiS?OSICIÚN N 16 8 Q BUENOS AIRES, 2 2 FEB. 2016 VISTO el Expediente NO 1-0047-0000-001115-15-6 del Registro de la Administración Nacional de Medicamentos, Alimentos
~desat«d S~de'P~, 'R~e1_ 1'11t?/t.,,4. 7. DiS?OSICIÚN N 16 8 Q BUENOS AIRES, 2 2 FEB. 2016 VISTO el Expediente NO 1-0047-0000-001115-15-6 del Registro de la Administración Nacional de Medicamentos, Alimentos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 AZITROMICINA 500 mg COMPRIMIDOS RECUBIERTOS ANTIBACTERIANO Página 1 AZITROMICINA 500 mg Comprimidos Recubiertos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 AZITROMICINA 500 mg COMPRIMIDOS RECUBIERTOS ANTIBACTERIANO Página 1 AZITROMICINA 500 mg Comprimidos Recubiertos
- Como disolvente de medicamentos en polvo o liofilizados, previamente a su administración. - Como diluyente de soluciones y/o medicamentos.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
BUENOS AIRES, O 7 ABO 2D15. de la Administración Nacional de Medicamentos, Alimentos y Tecnología
 ~desatad S~ de'1'dé:tiu4, ; ~e'l_ A, n,?'/t,a, 7. OISP08lr.!Ó~! N' 6 3' 7 6 BUENOS AIRES, O 7 ABO 2D15 VISTO el Expediente NO 1-0047-0000-008630-14-7 del Registro de la Administración Nacional de Medicamentos,
~desatad S~ de'1'dé:tiu4, ; ~e'l_ A, n,?'/t,a, 7. OISP08lr.!Ó~! N' 6 3' 7 6 BUENOS AIRES, O 7 ABO 2D15 VISTO el Expediente NO 1-0047-0000-008630-14-7 del Registro de la Administración Nacional de Medicamentos,
PROSPECTO: INFORMACIÓN PARA EL USUARIO. IRBESARTÁN KERN PHARMA 150 mg COMPRIMIDOS RECUBIERTOS EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO IRBESARTÁN KERN PHARMA 150 mg COMPRIMIDOS RECUBIERTOS EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto, ya
PROSPECTO: INFORMACIÓN PARA EL USUARIO IRBESARTÁN KERN PHARMA 150 mg COMPRIMIDOS RECUBIERTOS EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto, ya
FICHA TECNICA. ANASTROZOL NORMON 1 mg comprimidos recubiertos con película EFG
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ANASTROZOL NORMON 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 1 mg de anastrozol. Excipientes:
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ANASTROZOL NORMON 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 1 mg de anastrozol. Excipientes:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO: CLARITYNE FLAS 10 mg Liofilizado Oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada liofilizado oral de CLARYTINE FLAS contiene:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO: CLARITYNE FLAS 10 mg Liofilizado Oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada liofilizado oral de CLARYTINE FLAS contiene:
No hay evidencia de que un aumento de la dosis resulte en un aumento de la eficacia.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lambdaxel 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto contiene
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lambdaxel 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido recubierto contiene

 ~nisterio de Sa~ud S~ de PotttieM, í(!et}cd4~ e 1H4t
~nisterio de Sa~ud S~ de PotttieM, í(!et}cd4~ e 1H4t