Encue ntra más e ncue ntra cur s os gratis s obre s alud y me dicina e n nue s tro Ce ntro de Apre ndiz aje gratui to: / w w w.
|
|
|
- Josefa Iglesias Pereyra
- hace 5 años
- Vistas:
Transcripción
1 Encue ntra más e ncue ntra cur s os gratis s obre s alud y me dicina e n nue s tro Ce ntro de Apre ndiz aje gratui to: / w w w.e nple ni tud.com/ cur s o s
2 Sinopsis de las Técnicas de Bancos de Sangre Rafael Amadeo Mateo Capilla, Tecn. Laboratorio Clínico Indice: Grupo AB0 El fenotipo Rh-Kell La confirmación de antígeno D El grupo hemático en tubo El grupo sérico en tubo La determinación del antígeno D en placa La determinación del grupo ABO en placa La resolución de discrepancias AB0 La identificación de Anticuerpos Irregulares La investigación de anticuerpos irregulares La titulación de anticuerpos. Método en tarjeta Las pruebas cruzadas Técnica del Coombs Directo La técnica del Coombs directo monoespecífico Interpretación de la aglutinación La determinación del fenotipo del grupo Lewis La determinación del grupo MN La determinación del grupo P La determinación de los grupos acreditados Ss, Kk, KpaKpb, FyaFyb, JkaJkb, LuaLub La elución mediante R-E-S La elución con Gamma EGA La adsorción autóloga de autoanticuerpos calientes La hemoglobinuria paroxística nocturna Las autoaglutininas frías de títulos elevados
3 La especificidad de crioaglutininas La técnica de Donath-Landsteiner Capítulo 1º. GRUPO AB0 Establecer el grupo ABO (hemático/sérico) y el factor Rh (D) en tarjeta. Exposicion 1. Identificar la tarjeta con el nombre y apellidos del receptor. 2. Preparar en un tubo debidamente identificado una dilución con 10 μl de sangre total del paciente y 0.5 ml de Id-Diluent. 3. Situar 50 μl de la dilución de hematíes en los pocillos con anti-a anti-b, anti-ab, anti-d, anti- CDE y control. 4. Situar 50 μl de dilución de hematíes comerciales A1 y B en los otros dos pocillos. 5. Ampliar 50 μl de suero o plasma del paciente en los pocillos de hematíes comerciales. 6. Centrifugar en la centrífuga. 7. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura es positiva. La gradación sería:
4 La presencia de hemólisis indica igualmente positividad. Si el botón de hematíes se deposita en el fondo del pocillo la lectura es negativa. Si existe discrepancia entre grupo sérico y hemático habrá que resolverla antes de informar el resultado. Capítulo 2º. El fenotipo Rh- Kell. Establecer los antígenos del sistema Rh y Kell (D, C, c, Cw, E, e y Kell). de análisis 1. Identificar una tarjeta DiaClon Rh-subgroups+K con el nombre y apellidos del paciente. 2. Preparar en un tubo debidamente identificado una dilución con 10 μl de sangre total del paciente y 0.5 ml de Id-Diluent Situar 10 μl de la dilución de hematíes en los pocillos con anti-c, anti-c, anti-e, anti-e, anti-k y Control 4. Centrifugar en la centrífuga Diamed. 5. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura es positiva. La presencia de hemólisis indica igualmente positividad. Si el botón de hematíes baja la lectura es negativa Capítulo 3º. La confirmación de antígeno D Establecer el antígeno D
5 de análisis 1. Identificar un tarjeta Diamed anti-d con el nombre y apellidos del paciente. 2. Preparar en un tubo debidamente identificado una dilución con 10 μl de sangre total del paciente y 0.5 ml de Id-Diluent Situar 10 μl de la dilución de hematíes en los pocillos con anti-d y Control 4. Centrifugar en la centrífuga Diamed. 5. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura es positiva. La presencia de hemólisis indica igualmente positividad. Si el botón de hematíes baja la lectura es negativa. Capítulo 4º. El grupo hemático en tubo Establecer el grupo ABO en tubo. de análisis 1. Situar una gota de anti-a, anti-b, y anti-ab, en tres tubos limpios y convenientemente rotulados. 2. Ampliar una gota de hematíes problema diluidos en suero salino al 2-5% a cada tubo. 3. Mezclar suavemente agitando el contenido de los tubos y centrifugar durante 20 segundos 3000 rpm 4. Retirar de la centrífuga y resuspender suavemente el sedimento de los hematíes. 5. Examinar la presencia o ausencia de aglutinación y anotar los resultados.
6 La presencia de aglutinación o hemólisis indicará que la reacción es positiva, mientras que una suspensión uniforme de hematíes se considerará como resultado negativo. Las discrepancias entre los resultados del grupo ABO hemático y sérico deben resolverse antes de clasificar el grupo ABO del paciente. Capítulo 5º. El grupo sérico en tubo ESTUDIO DE ANÁLISIS Establecer la presencia o ausencia de anti-a y anti-b en el plasma o suero del paciente. de análisis Utilizaremos hematíes reactivo A1 y B de origen comercial. Opcionalmente podemos efectuar el grupo sérico utilizando además hematíes A2 y O. 1. Colocar una gota de hematíes reactivo en cada uno de los tubos limpios y rotulados. (A1, A2, B y O). 2. Ampliar dos gotas de suero problema a cada tubo. 3. Agitar suavemente y centrifugar durante 20 segundos a 3000 rpm ( x g). 4. Examinar los tubos en busca de hemólisis. Resuspender suavemente el sedimento de hematíes y observar la presencia o ausencia de aglutinación. Anotar resultados. La estampación de aglutinación o hemólisis revelará que La estampación de aglutinación o hemólisis revelará que la reacción es positiva, mientras que una suspensión uniforme de hematíes se considerará como resultado negativo.
7 * Las diferencias entre los resultados del grupo ABO hemático y sérico deben resolverse antes de clasificar el grupo ABO del paciente. Capítulo 6º. La determinación del antígeno D en placa Establecer la presencia del antígeno D (Rh). de análisis 1. Colocar una gota de antisuero Anti-D en un porta o placa limpio y rotulado, junto a una gota de sangre del paciente. 2. Colocar una gota de reactivo control (o en su defecto suero fisiológico) junto a otra gota de sangre del paciente, en un segundo porta o en la placa. 3. Mezclar con un palillo limpio formando un circulo de 2-3 cm de diámetro. 4. Colocar los portaobjetos sobre el visor y bascular suave y constantemente para observar la presencia de aglutinación. El máximo de observación es de dos minutos, superado ese tiempo se puede producir un fenómeno de rouleaux, que puede interpretarse erróneamente como aglutinación. Capítulo 7º. La determinación del grupo ABO en placa. Efectuar el tipaje AB0 en placa o porta. de análisis 1. Identificar el porta o la placa con el nombre y apellidos del paciente (o número de la unidad a tipar) 2. Colocar una gota de Seraclone Anti-A, Anti-B, y Anti-AB. 3. Ampliar una gota de sangre junto a cada gota de
8 los reactivo y mezclarlo en un área aproximada de 2 cm de diámetro (puede utilizarse para ello palillos higiénicos). 4. Se recomienda hacer la lectura de la posible aglutinación después de 30 a 60 segundos. La presencia de aglutinación indica la especificidad AB0. Capítulo 8. La resolución de discrepancias AB0. Acordar el grupo ABO cuando no concuerdan el grupo hemático con el grupo sérico. Se produce una discrepancia cuando los resultados del grupo hemático y sérico no concuerdan. La interpretación del grupo ABO debe retrasarse hasta que se resuelva la discrepancia. Los primeros pasos a seguir son: 1. Repetir el grupo hemático y sérico en tubo con los hematíes lavados. 2. Analizar los hematíes frente a anti-a, B, A1. 3. Analizar el suero frente a hematíes A1, A2, B. 4. Ampliar la relación suero/hematíes e incubar 30 minutos a temperatura ambiente. Centrifugar y leer. Capitulo 9º. La identificación de Anticuerpos Irregulares Identificar la especificidad (por probabilidades) del anticuerpo que descubrimos con la investigación o escrutinio de anticuerpos irregulares. Esta técnica, básicamente es similar a la detección de anticuerpos irregulares, con la diferencia de que en este
9 caso enfrentamos el suero a una batería de 11 células de grupo 0 ampliamente fenotipadas, y cuya reactividad nos indicará la probable especificidad del anticuerpo en estudio. de análisis 1. Extraer del frigorífico las cajas con los paneles comerciales de hematíes papainizados y no papainizados. Comprobar la fecha de caducidad. Dar suavemente varias vueltas a la caja entera con el fin de resuspender los hematíes de cada frasco. 2. Preparar una suspensión de 10 μl de sangre total del paciente con 0.5 ml de Id-Diluent 1 y otra suspensión de 10 μl de sangre total del paciente con 0.5 ml de Id-Diluent Rotular : 12 pocillos de tarjeta Diamed ClNa 1 al 12, 12 pocillos de tarjeta Diamed LISS/Coombs del 1 al 12, 12 pocillos de tarjeta Diamed ClNa del 1P al 12P y 12 pocillos de tarjeta Diamed LISS/Coombs del 1P al 12P. 4. Ampliar a cada pocillo 25 μl del suero problema. 5. Ampliar: 50 μl de los hematíes no papainizados del vial 1 a los pocillos rotulado 1 de las tarjetas Neutra y Coombs, y así haremos con todos los viales hasta el rotulado como 11. Al pocillo número 12 de ambas tarjetas ampliaremos 50 μl de la solución de hematíes del paciente preparada con Id-Diluent Ampliar: 50 μl de los hematíes papainizados del vial 1 a los pocillos rotulado 1P de las tarjetas Neutra y Coombs, y así haremos con todos los viales hasta el rotulado como 11. Al pocillo número 12 de ambas tarjetas ampliaremos 50 μl de la solución de hematíes del paciente preparada con Id-Diluent 1.
10 Capítulo 10º. La investigación de anticuerpos irregulares Los únicos anticuerpos de grupo que se suelen tener son los anti-a y anti-b. Los demás anticuerpos de grupo no relacionados con el sistema AB0, se les conoce como anticuerpos irregulares. Para detectar estos anticuerpos se enfrenta el suero a estudiar a una serie de hematíes de grupo 0 que poseen la mayoría de antígenos frente a los cuales estos anticuerpos son específicos. Clásicamente cuando esta prueba se utiliza como parte de los test pretransfusionales se denomina investigación de anticuerpos irregulares, y cuando se esgrime como parte del protocolo de isoinmunización materno fetal se designa Test de Coombs Indirecto. 1. Identificar la tarjeta Diamed Liss/Coombs con el nombre y apellidos del receptor y rotular cuatro pocillos en cada tarjeta con los números 1, 2 y Ampliar a cada pocillo 25 μl del suero problema. 3. Situar 50 μl de la dilución de hematíes comerciales Id Diacell I, II y III en los pocillos rotulados de la tarjeta. 4. Incubar durante 10 minutos a 37ºC la tarjeta en la incubadora Diamed. 5. Centrifugar la tarjeta en la centrífuga Diamed. Proceder a la lectura. Capítulo 11º. La titulación de anticuerpos. Método en tarjeta. El título de un anticuerpo, es la dilución máxima en la que su presencia puede ser demostrada por aglutinación, y es una forma grosera de valorar la cantidad del anticuerpo.
11 1. Rotular los tubos con la dilución del suero (1, 2, 4, 8, 16, 32, 64) y añadir 0,1 ml de Id solución 2 a todos los tubos excepto al primero. 2. Ampliar un volumen igual de suero a los dos primeros tubos. 3. Mezclar con una pipeta limpia varias veces el contenido del segundo tubo y transferir 0,1 ml al siguiente tubo. Repetir el procedimiento con todas las diluciones, utilizando una punta de pipeta nueva con cada tubo. El volumen del último tubo se guarda en un tubo limpio por si se requiriesen nuevas diluciones. 4. Rotular una tarjeta LISS/Coombs con el número de identificación del paciente y en cada pocillo con las diluciones de los tubos empezando por el segundo tubo (2, 4, 8, 16, 32, 64). 5. Dispensar en cada pocillo 50 μl de hematíes en suspensión al 0.8% (los hematíes deben tener el antígeno frente al que se dirige el anticuerpo a titular y ser compatibles ABO con el suero problema). 6. Ampliar a cada pocillo 25 μl de la dilución correspondiente. 7. Incubar durante 10 minutos la tarjeta en la incubadora Diamed. 8. Centrifugar la tarjeta en la centrífuga Diamed. Proceder a la lectura. Capítulo 12º. Las pruebas cruzadas Control final de la compatibilidad ABO entre el donante y el receptor. Demuestra la ausencia de anticuerpos irregulares que pudiera tener el receptor frente a los hematíes del donante. 1. Identificar las tarjetas (Diamed LISS/Coombs y Diamed ClNa) con el nombre y apellidos del receptor y rotular cada pocillo con el número de la unidad a cruzar. 2. Preparar una dilución con 50 μl de la unidad de concentrado de hematíes y 0.5 ml de Id-
12 Diluent 2, en un tubo rotulado con el nº de la unidad de concentrado de hematíes. 3. Situar 50 μl de la dilución de hematíes en los pocillos de la tarjeta Diamed LISS/Coombs y en la tarjeta Diamed ClNa. 4. Situar 25 μl de suero del receptor en cada pocillo de las dos tarjetas. 5. Incubar durante 15 minutos, la tarjeta Diamed LISS/Coombs, en la incubadora Diamed. Dejar ese mismo tiempo la tarjeta Diamed ClNa a temperatura ambiente. 6. Centrifugar la tarjeta en la centrífuga Diamed. 7. Proceder a la lectura. Capítulo 13º. Técnica del Coombs Directo Estudio de analisis Esta técnica detecta si los hematíes están recubiertos de anticuerpos o complemento. 1. Identificar una tarjeta Diamed LISS/Coombs con el nombre y apellidos del paciente y/o el número de identificación de la muestra. 2. Preparar una dilución con 50 μl de sangre total en 0.5 ml de Id-Diluent 2, en un tubo debidamente identificado. 3. Situar 10 μl de la dilución de hematíes en uno de los pocillos de la tarjeta. 4. Centrifugar en la centrífuga Diamed. 5. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura es positiva. Si el botón de hematíes baja la lectura es negativa.
13 Capítulo 14º. La técnica del coombs directo monoespecífico Esta técnica identifica la clase de inmunoglobulina o fracción del complemento causantes de la positividad de un test de Coombs. 1. Identificar una tarjeta DC Screning I con el nombre y apellidos del paciente y/o el número de identificación de la muestra. 2. Preparar una dilución con 30 μl de hematíes de la muestra en 1000 μl de Id Solución 2, en un tubo debidamente identificado. 3. Situar 25 μl de la dilución de hematíes en cada uno de los pocillos de la tarjeta. 4. Centrifugar 8 minutos en la centrífuga Diamed. 5. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura es positiva. Si el botón de hematíes baja la lectura es negativa. Capítulo 15º. Interpretación de la aglutinación. Valorar las reacciones de aglutinación de forma estándar.
14 Anotación Grado de aglutinación Descripción de la aglutinación Botón sólido de eritrocitos, ningún eritrocito libre; fondo claro Varios aglutinados grandes; fondo claro Muchos aglutinados de regular tamaño; fondo claro. 5 + Aglutinados pequeños; fondo turbio. 2 +/- Aglutinados muy pequeños; fondo turbio. 0 - No aglutinación ni hemólisis todos los eritrocitos libres. PH Hemólisis parcial. H Hemólisis completa; no quedan hematíes. Siempre debe buscarse la presencia de hemólisis, su presencia indicará un resultado positivo. Capítulo 16º. La determinación del fenotipo del grupo Lewis Establecer el fenotipo del grupo Lewis, en este caso para los antígenos Lea y Leb
15 1. Rotular 3 pocillos de una tarjeta Diamed ClNa correctamente identificada por cada antígeno a identificar como P, C+ y C- y ampliar por orden; 50 µl de hematíes del paciente diluido al 0.8% en el primer pocillo, 50 µl de hematíes comprobados positivos para el antígeno en el segundo pocillo y 50 µl de hematíes comprobados negativos para el antígeno en el tercer pocillo. 2. Ampliar a cada pocillo 25 µl del antisuero correspondiente al antígeno a identificar. 3. Incubar la tarjeta durante 10 minutos a 22ºC. 4. Centrifugar la tarjeta en la centrífuga Diamed. 5. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura es positiva. Si el botón de hematíes baja la lectura es negativa. Una positividad en el control negativo o negatividad en el control positivo invalida la prueba. Capítulo 17º. La determinación del grupo MN Establecer el fenotipo del sistema MN, en este caso para los antígenos M y N. 1. Rotular 3 pocillos de una tarjeta Diamed ClNa correctamente identificada por cada antígeno a identificar como P, C+ y C- y ampliar por orden; 50 µl de hematíes del paciente diluido al 0.8% en el primer pocillo, 50 µl de hematíes comprobados positivos para el antígeno en el segundo pocillo y 50 µl de hematíes comprobados negativos para el antígeno en el tercer pocillo. 2. Ampliar a cada pocillo 25 µl del antisuero correspondiente al antígeno a identificar. 3. Incubar la tarjeta durante 10 minutos a 22ºC.
16 4. Centrifugar la tarjeta en la centrífuga Diamed. 5. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura es positiva. Si el botón de hematíes baja la lectura es negativa. Una positividad en el control negativo o negatividad en el control positivo invalida la prueba. Capítulo 18º. La determinación del grupo P Establecer el fenotipo del sistema P, en este caso para el antígeno P Rotular 3 pocillos de una tarjeta Diamed ClNa correctamente identificada por cada antígeno a identificar como P, C+ y C- y ampliar por orden; 50 µl de hematíes del paciente diluido al 0.8% en el primer pocillo, 50 µl de hematíes comprobados positivos para el antígeno en el segundo pocillo y 50 µl de hematíes comprobados negativos para el antígeno en el tercer pocillo. 2. Ampliar a cada pocillo 25 µl del antisuero correspondiente al antígeno a identificar. 3. Incubar la tarjeta durante 10 minutos a 22ºC. 4. Centrifugar la tarjeta en la centrífuga Diamed. 5. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura
17 es positiva. Si el botón de hematíes baja la lectura es negativa. Una positividad en el control negativo o negatividad en el control positivo invalida la prueba. Capítulo 19º. La determinación de los grupos acreditados Ss, Kk, KpaKpb, FyaFyb, JkaJkb, LuaLub Establecer el fenotipo de los hematíes para los sistemas de grupo aludidos. 1. Rotular 3 pocillos de una tarjeta Diamed LISS/ Coombs correctamente identificada por cada antígeno a identificar como P, C+ y C- y ampliar por orden; 50 µl de hematíes del paciente diluido al 0.8% en el primer pocillo, 50 µl de hematíes comprobados positivos para el antígeno en el segundo pocillo y 50 µl de hematíes comprobados negativos para el antígeno en el tercer pocillo. 2. Ampliar a cada pocillo 25 µl del antisuero correspondiente al antígeno a identificar. 3. Incubar la tarjeta durante 10 minutos a 37ºC en la incubadora Diamed. 4. Centrifugar la tarjeta en la centrífuga Diamed. 5. Proceder a la lectura. Si el botón de hematíes queda en la parte superior del pocillo indica aglutinación y la lectura es positiva. Si el botón de hematíes baja la lectura es negativa. Una positividad en el control negativo o negatividad en el control positivo invalida la prueba.
18 Capítulo 20º. La elución mediante R-E-S Estudio de analisis Con la elución pretendemos separar los anticuerpos unidos a los hematíes para poder estudiar dichos anticuerpos. 1. Solución de Lavado. Se prepara suficiente solución para lavar cuatro veces los hematíes. Es una dilución 1/10 con disolvente y agua destilada (ej. 2ml de disolvente y 18ml de H2O destilada). 2. Lavar 1 ml (20 gotas) de hematíes concentrados 1 vez con salino, y 4 veces con solución de lavado. 3. Retirar el máximo de sobrenadante del último lavado y utilizarlo como control (en un tubo etiquetado). 4. Colocar 1 ml de células lavadas en un tubo y ampliar 1 ml de SOLUCION I (20 gotas y 20 gotas). 5. Mezclar suavemente por inversión 4-5 veces. 6. Centrifugar inmediatamente en 3400 durante 1 minuto. 7. Transferir el sobrenadante (ELUIDO) a un tubo limpio y etiquetado. 8. Ampliar 20 gotas de SOLUCION II (Azul), mezclar bien. Si el color es aún amarillo, ampliar gota a gota hasta que alcance un color azul pálido. 9. Centrifugar nuevamente para eliminar cualquier precipitado y transferir a un tubo limpio. Investigar la presencia de anticuerpos en el eluído, utilizar el sobrenadante del último lavado como control negativo.
19 Capítulo 21º. La elución con Gamma EGA El procedimiento descrito es útil para eliminar los autoanticuerpos que recubren a los hematíes, para de esta forma poder fenotiparlos. Es igualmente útil para células no recubiertas con IgG, cuando el fin es destruir los antígenos del sistema Kell para ayudar en la identificación de anticuerpos. 1. Lavar los hematíes tres veces con salino fisiológico, y resuspenderlos al 3-5%. 2. Ampliar 30 gotas de esta suspensión en un tubo limpio 3. Centrifugar 1 minuto a rpm y eliminar el sobrenadante con cuidado de no tocar los hematíes. 4. En otro tubo, preparar la solución ácida de EDTA-glicina añadiendo 4 gotas de EGA solución 1 y 16 gotas de EGA solución Ampliar inmediatamente la solución EDTAglicina recién preparada al paquete de hematíes lavados y mezclar suavemente. 6. Mantener a temperatura ambiente (23±3ºC) no más de 2 minutos (con el cronómetro en mano). Si las células están fuertemente agrupadas o teñido, debe acortarse el tiempo de incubación en períodos de 15 segundos. 7. Ampliar inmediatamente 7 gotas de solución EGA 3, mezclar bien y centrifugar 30 segundos a 3.400rpm. 8. Eliminar el sobrenadante, y resuspender las células en salino. Si en este momento del tratamiento las células no están fuertemente agrupadas o teñidas (ver paso 6), lavar las células al menos tres veces con salino.
20 Arrostración Es de máxima cautela que en el tratamiento con EGA hace que las células se puedan hemolizar con facilidad. En caso que se produzca un retraso entre el lavado y el tipaje, se requerirán mas lavados Efectuar la prueba de antiglobulina directa (Coombs Directo) de las células tratadas. Si es negativo, se procede al tipaje de los hematíes. Capítulo 22º. La adsorción autóloga de autoanticuerpos calientes Los auto-anticuerpos (Ac) calientes pueden enmascarar la presencia de alo-ac en el suero. La adsorción del suero con hematíes autólogos puede eliminar los auto- Ac y desenmascarar los posibles alo-ac. 1. Preparar dos alícuotas de 1 ml de hematíes del paciente tratados según la Técnica de Elución con GammaEGA (T-22). 2. Ampliar 2 ml de suero del paciente a una de las alícuotas, mezclar e incubar a 37ºC durante 30 minutos. 3. Centrifugar a 3400 rpm durante 2 minutos y transferir el suero a la segunda alícuota de hematíes. Mezclar e incubar a 37ºC durante 30 minutos. 4. Centrifugar a 3400 rpm 2 minutos. Transferir el SUERO ADSORBIDO, a un tubo limpio y etiquetado. 5. Efectuar una investigación de anticuerpos irregulares, y una identificación si procede. En caso de positividad puede utilizarse este suero para la realización de pruebas cruzadas. Observación primordial: No es propio para llevar a efecto la autoadsorción con hematíes de un
21 paciente recién transfundido, puesto que los hematíes transfundidos circulantes pueden adsorber los alo-ac que se están inquiriendo. Capítulo 23. La hemoglobinuria paroxística nocturna El Test de HPN (hemoglobinuria paroxística nocturna) sirve para detectar la ausencia o déficit de proteínas implicadas en la mayor sensibilidad de las células de serie roja al complemento en estos pacientes. Valora el DAF (factor acelerador del decaimiento CD55) y el MIRL (inhibidor de membrana de la lisis reactiva). 1. Recoger un tubo de sangre citratada (protrombina) del enfermo. En este caso también sirve tubo con EDTA, heparina o CPD- A. Es importante que sea sangre fresca recién extraída. 2. Preparar una solución 0,8 % con diluyente 2 de DiaMed (10 mcl de sangre y 1 ml de diluyente) para usar inmediatamente. 3. Ampliar 50 mcl de suspensión de hematíes a los pocillos DAF, MIRL y ctl de la tarjeta DiaMed. 4. Ampliar 50 mcl de cada solución (MIEL, DAF y ctl) al pocillo correspondiente 5. Repetir la operación con sangre de un paciente sin HPN, que servirá como control negativo en la misma tarjeta. 6. Incubar 15 minutos a 37º C. 7. Centrifugar en la centrífuga Dia Med (ID centrifuga 24 S) durante 10 minutos. Leer los resultados Capítulo 24º. Las autoaglutininas frías de títulos elevados
22 Precisar a que concentración se detentan anticuerpos fríos. Los autoanticuerpos fríos, si están presentes a títulos elevados tienen significación clínica y pueden causar hemólisis manifiesta, síntomas sistémicos e indicar una neoplasia subyacente. 1. Obtener suero (mantenido a 37ºC desde el momento de la extracción) separado a 37ºC de una muestra de sangre que se deja coagular a 37ºC o plasma, separado de una muestra anticoagulada después de inversiones periódicas a 37ºC durante 15 minutos. 2. Preparar una suspensión al 1% en salino de eritrocitos de los siguientes fenotipos: OI (pueden prepararse a partir de un segmento tomado de una unidad de sangre extraída dentro de los 7 días precedentes o de una muestra extraída con EDTA dentro de los tres días precedentes). Oi (Cordón) Autólogos. 3. Diluir el suero o plasma al 1/5 en salina. 4. Preparar tres hileras de doce tubos con diluciones seriadas al doble de suero o plasma diluido al 1/ 5 (1/10,...1/20.480). Utilizar volúmenes de 0,5 ml cuando se hacen las diluciones. 5. Agregar a cada tubo 0,5 ml de los hematíes correspondientes. 6. Mezclar e incubar toda la noche a 4ºC. 7. No centrifugar. Examinar los eritrocitos sedimentados macroscópicamente en busca de aglutinación. Anotar los resultados. El título es la reciproca de la dilución más alta del suero en la que se observa aglutinación. Los títulos por encima de 1/40 se consideran elevados, pero la anemia hemolítica por autoaglutininas reactivas en frío rara vez ocurre a menos que el título sea superior a 1/640.
23 Capítulo 25º. La especificidad de crioaglutininas Establecer la especificidad de las autoaglutininas que reaccionan en frío. Para ello se estudia el suero frente a eritrocitos que presenta antígenos ante los cuales reaccionan las aglutininas frías. 1. Suero (mantenido a 37ºC desde el momento de la extracción) separado a 37 ºC de una muestra de sangre que se deja coagular a 37ºC o plasma, separado de una muestra anticoagulada después de inversiones periódicas a 37ºC durante 15 minutos. 2. Suspensión al 5% en salino de eritrocitos de los siguientes fenotipos. a. Dos muestras de células OI (puede utilizarse hematíes del panel de investigación de anticuerpos). b. Una muestras de hematíes del paciente c. Una muestra de hematíes A o B si el paciente no es grupo 0 d. Una muestra OI tratada con enzimas (bromelina) e. Una muestra de hematíes Oi (cordón umbilical) 3. Preparar cinco hileras de doce tubos con diluciones seriadas al doble de suero o plasma (1/2,...1/4096) 4. Mezclar tres gotas de cada dilución con una gota de hematíes al 5% de cada muestra de eritrocitos. 5. Incubar a temperatura ambiente durante 15 minutos. Centrifugar (1000 x g 30 segundos)y examinar (golpear suavemente) macroscópicamente en busca de aglutinación. Anotar los resultados. 6. Colocar los tubos a 4ºC e incubar a esta temperatura durante 1 hora. Centrifugar y examinar macroscópicamente en busca de aglutinación. Anotar los resultados.
24 Síntesis Eritrocitos Anti-I Anti-i Anti-H A n t i - IH OI NR/ Oi NR/ < AI OI enzimas Autólogo Anti-Pr NR/ Algunos autoanticuerpos fríos pueden no mostrar especificidad aparente a temperatura de 4ºC, en estas circunstancias las pruebas pueden ser incubadas a 30-37ºC. La reactividad diferencial puede hacerse más aparente si se prolonga el tiempo de incubación y la aglutinación se evalúa después de la sedimentación sin centrifugación. Capítulo 26º. La técnica de Donath-Landsteiner Esta técnica se emplea para detectar la hemolisina bifásica responsable de la anemia hemolítica autoinmune paroxística fría. 1. Obtener suero separado de una muestra de sangre recogida y mantenida a 37 ºC y suero fresco (como fuente de complemento). 2. Preparar eritrocitos del grupo O lavados y resuspendidos al 50%. 3. Rotular tres filas de tubos como sigue:? A 1 A 2 A 3? B 1 B 2 B 3? C 1 C 2 C 3 4. A los tubos 1-2 de cada fila ampliar 10 volúmenes de suero del paciente. 5. A los tubos 2-3 de cada fila ampliar 10 volúmenes de suero fresco. 6. A todos los tubos ampliar un volumen de la
25 para jóvenes de más de Inscríbete ahora en nuestros cursos gratis Pasos para aumentar la efectividad de sus acciones comerciales Aprenda a Invertir y Administrar su Dinero Cómo tener su propio boletín electrónico Operaciones de Comercio Exterior Imagen personal para mujeres profesionales Satisfacción del cliente Ventas exitosas Planificación de la carrera profesional Manual de Organización y Regulaciones Internas Contabilidad Intermedia Prevención de Demandas Laborales Prevención del Acoso Sexual en el Trabajo suspensión de eritrocitos. Mezclar. 7. Colocar los tres tubos de la hilera A en hielo fundido durante 30 minutos y luego pasarlos a 37 ºC durante 1 hora. 8. Colocar los tres tubos de la hilera B en hielo fundido durante 90 minutos. 9. Centrifugar todos los tubos e investigar hemólisis en el liquido sobrenadante. La prueba se considera positiva cuando el suero del paciente, con complemento o sin el, produce hemólisis en los tubos que se han colocado primero en hielo y luego a 37 ºC (tubos A 1 A 2 ) y no hay hemólisis en los mantenidos a 37 ºC o en hielo. Los tubos A 3 B 3 C 3 sirven como control del complemento y deben ser negativos. Encuentra más encuentra cursos gratis sobre salud y medicina en nuestro Centro de Aprendizaje gratuito:
Nombre: Marga Alcover Cargo: Coordinadora de Enfermería Fecha: 29/01/07
 Determinación del Grupo AB0 Página 1 de 10 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
Determinación del Grupo AB0 Página 1 de 10 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Investigación de crioaglutininas Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
Investigación de crioaglutininas Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
INSTRUCCIÓN TÉCNICA. Escrutinio de anticuerpos Irregulares o Coombs Indirecto DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Página 1 de 6 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería REVISIÓN FECHA DESCRIPCIÓN
Página 1 de 6 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería REVISIÓN FECHA DESCRIPCIÓN
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Identificación de anticuerpos Página 1 de 7 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
Identificación de anticuerpos Página 1 de 7 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
Inmunohematología 2017
 Inmunohematología 2017 REACCIONES DE HEMAGLUTINACIÓN 1-Sensibilización 2-Aglutinación Ag + Ac Ag-Ac FACTORES QUE AFECTAN LA HEMAGLUTINACIÓN Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo
Inmunohematología 2017 REACCIONES DE HEMAGLUTINACIÓN 1-Sensibilización 2-Aglutinación Ag + Ac Ag-Ac FACTORES QUE AFECTAN LA HEMAGLUTINACIÓN Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo
Inmunohematología. Dra. Ana Cecilia Haro
 Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
EL TEXTO EN COLOR ROJO HA SIDO MODIFICADO
 COMENTARIOS Con fundamento en el numeral 4.11.1 de la Norma Oficial Mexicana NOM-001-SSA1-2010, se publica el presente proyecto a efecto de que los interesados, a partir del 1º de agosto y hasta el 30
COMENTARIOS Con fundamento en el numeral 4.11.1 de la Norma Oficial Mexicana NOM-001-SSA1-2010, se publica el presente proyecto a efecto de que los interesados, a partir del 1º de agosto y hasta el 30
Albúmina 22 % I.- Introducción. II.- Características. III.- Presentación
 Albúmina 22 % I.- Introducción En 1945 Cameron y Diamond establecieron que ciertos sueros anti-d(anti-rh) podían aglutinar glóbulos rojos Rho positivos en presencia de albúmina de bovino pero no aglutinaban
Albúmina 22 % I.- Introducción En 1945 Cameron y Diamond establecieron que ciertos sueros anti-d(anti-rh) podían aglutinar glóbulos rojos Rho positivos en presencia de albúmina de bovino pero no aglutinaban
Manual de Inmunohematología
 Calidad y Seguridad Del Paciente Hospital Regional Rancagua HRR Código: SGC-MIH Página: 1 de 59 INDICE / CONTENIDO Contenidos: Página Clasificación ABO y Rh D en tubo 02 Clasificación ABO y Rh D en lámina
Calidad y Seguridad Del Paciente Hospital Regional Rancagua HRR Código: SGC-MIH Página: 1 de 59 INDICE / CONTENIDO Contenidos: Página Clasificación ABO y Rh D en tubo 02 Clasificación ABO y Rh D en lámina
INSTRUCTIVO DETERMINACIÓN DE GRUPOS A,B,O Y RH-D
 1. OBJETIVO: Desarrollar la clasificación de Grupo y Rh a los usuarios del Hospital Regional de Arica Dr. Juan Noé Crevani, de acuerdo con los antígenos y anticuerpos presentes en la sangre, esto con el
1. OBJETIVO: Desarrollar la clasificación de Grupo y Rh a los usuarios del Hospital Regional de Arica Dr. Juan Noé Crevani, de acuerdo con los antígenos y anticuerpos presentes en la sangre, esto con el
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
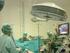 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
I.- ACTIVIDADES REALIZADAS. Administrativas
 1 I.- ACTIVIDADES REALIZADAS Administrativas Durante el mes de Octubre (de 01 al 31 de Octubre) continué en el área de serología. Las actividades que realicé fue la recolección de tubos pertenecientes
1 I.- ACTIVIDADES REALIZADAS Administrativas Durante el mes de Octubre (de 01 al 31 de Octubre) continué en el área de serología. Las actividades que realicé fue la recolección de tubos pertenecientes
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
Prueba de Antiglobulina Indirecta
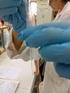 Procedimiento 1 Prueba de Antiglobulina Indirecta Principio La técnica de inmunoglobulina indirecta fue descrita por primera vez en 1945 por Coombs y colaboradores y permite observar aglutinaciones de
Procedimiento 1 Prueba de Antiglobulina Indirecta Principio La técnica de inmunoglobulina indirecta fue descrita por primera vez en 1945 por Coombs y colaboradores y permite observar aglutinaciones de
Herramientas complementarias en la investigación inmunohematológica Disociación, elución, adsorción, citometria de flujo
 Herramientas complementarias en la investigación inmunohematológica Disociación, elución, adsorción, citometria de flujo Lic. TM Edvin Santiago Trujillo Inmunohematológica Estudia los antígenos presentes
Herramientas complementarias en la investigación inmunohematológica Disociación, elución, adsorción, citometria de flujo Lic. TM Edvin Santiago Trujillo Inmunohematológica Estudia los antígenos presentes
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
> Directo... (celular) >Inverso... (Sérico) (Reverso)
 Dra. GIOVANA GARCIA > Directo... (celular) >Inverso... (Sérico) (Reverso) Discrepancias ABO La amplia mayoría de los grupos sanguíneos ABO tratados en el banco de sangre cumplen con las leyes establecidas
Dra. GIOVANA GARCIA > Directo... (celular) >Inverso... (Sérico) (Reverso) Discrepancias ABO La amplia mayoría de los grupos sanguíneos ABO tratados en el banco de sangre cumplen con las leyes establecidas
GELES FORMULADOS CON REACTIVOS MONOCLONALES DE ORIGEN MURINO O HUMANO O GEL NEUTRO
 ScanGel ABO Complete/RH/K Duo 86719 2 x 24 tarjetas 86709 2 x 144 tarjetas ScanGel ABO Complete/RH1 Duo y ScanGel Monoclonal RH/K Phenotypes Duo tarjetas GELES FORMULADOS CON REACTIVOS MONOCLONALES DE
ScanGel ABO Complete/RH/K Duo 86719 2 x 24 tarjetas 86709 2 x 144 tarjetas ScanGel ABO Complete/RH1 Duo y ScanGel Monoclonal RH/K Phenotypes Duo tarjetas GELES FORMULADOS CON REACTIVOS MONOCLONALES DE
Anemia Hemolítica Autoinmune Diagnóstico inmunohematológico
 Anemia Hemolítica Autoinmune inmunohematológico Dr. Arturo Pereira S. de Hemoterapia y Hemostasia Introducción Anemia Hemolítica Autoinmune (AHAI) Es la causa más frecuente de anemia hemolítica en el adulto.
Anemia Hemolítica Autoinmune inmunohematológico Dr. Arturo Pereira S. de Hemoterapia y Hemostasia Introducción Anemia Hemolítica Autoinmune (AHAI) Es la causa más frecuente de anemia hemolítica en el adulto.
 CALLE 102 A 47 A 64 PBX 57 (1) 6914847 BOGOTA COLOMBIA Email: proasecal@proasecal.com GP-DOC-071 PROGRAMA DE ASEGURAMIENTO DE LA CALIDAD EN EL LABORATORIO PROASECAL PROGRAMA: PRUEBA DE EFICIENCIA EN INMUNOHEMATOLOGIA
CALLE 102 A 47 A 64 PBX 57 (1) 6914847 BOGOTA COLOMBIA Email: proasecal@proasecal.com GP-DOC-071 PROGRAMA DE ASEGURAMIENTO DE LA CALIDAD EN EL LABORATORIO PROASECAL PROGRAMA: PRUEBA DE EFICIENCIA EN INMUNOHEMATOLOGIA
ACTIVIDAD PRÁCTICA No. 6 REACCIONES DE HIPERSENSIBILIDAD
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA CENTRO UNIVERSITARIO METROPOLITANO FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA DE INMUNOLOGÍA Y MICROBIOLOGÍA MÉDICA TERCER AÑO ACTIVIDAD PRÁCTICA No. 6 REACCIONES
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA CENTRO UNIVERSITARIO METROPOLITANO FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA DE INMUNOLOGÍA Y MICROBIOLOGÍA MÉDICA TERCER AÑO ACTIVIDAD PRÁCTICA No. 6 REACCIONES
ScanGel Monoclonal A - B - D Tarjetas Tarjetas
 ScanGel Monoclonal A - B - D 86491 48 Tarjetas 86481 288 Tarjetas GELES FORMULADOS CON REACTIVOS MONOCLONALES DE ORIGEN MÚRIDO O HUMANO Confirmación del tipaje ABO/D IVD Todos los productos fabricados
ScanGel Monoclonal A - B - D 86491 48 Tarjetas 86481 288 Tarjetas GELES FORMULADOS CON REACTIVOS MONOCLONALES DE ORIGEN MÚRIDO O HUMANO Confirmación del tipaje ABO/D IVD Todos los productos fabricados
NORMA OFICIAL MEXICANA. NOM-019-SSA1-93, Que Establece las Especificaciones Sanitarias del Reactivo Antiglobulina Humana para la Prueba de Coombs.
 NORMA OFICIAL MEXICANA. NOM-019-SSA1-93, Que Establece las Especificaciones Sanitarias del Reactivo Antiglobulina Humana para la Prueba de Coombs. Al margen un sello con el Escudo Nacional, que dice: Estados
NORMA OFICIAL MEXICANA. NOM-019-SSA1-93, Que Establece las Especificaciones Sanitarias del Reactivo Antiglobulina Humana para la Prueba de Coombs. Al margen un sello con el Escudo Nacional, que dice: Estados
DANAGENE SPIN GENOMIC DNA KIT
 DANAGENE SPIN GENOMIC DNA KIT Ref.0605.1 50 extracciones Ref.0605.2 250 extracciones Ref.0605.3 1000 extracciones 1. INTRODUCCION Este kit está designado para una rápida extracción y purificación de ADN
DANAGENE SPIN GENOMIC DNA KIT Ref.0605.1 50 extracciones Ref.0605.2 250 extracciones Ref.0605.3 1000 extracciones 1. INTRODUCCION Este kit está designado para una rápida extracción y purificación de ADN
CONTROL DE CALIDAD INTERNO EN INMUNOHEMATOLOGIA
 CONTROL DE CALIDAD INTERNO EN INMUNOHEMATOLOGIA DEFINICION: LAS TECNICAS OPERACIONALES Y ACTIVIDADES QUE SE USAN PARA CUMPLIR CON LOS REQUISITOS DE CALIDAD (ISO 8402:1996) REACTIVOS EQUIPOS MATERIAL CONTROL
CONTROL DE CALIDAD INTERNO EN INMUNOHEMATOLOGIA DEFINICION: LAS TECNICAS OPERACIONALES Y ACTIVIDADES QUE SE USAN PARA CUMPLIR CON LOS REQUISITOS DE CALIDAD (ISO 8402:1996) REACTIVOS EQUIPOS MATERIAL CONTROL
DANAGENE SPIN BLOOD DNA KIT
 DANAGENE SPIN BLOOD DNA KIT Ref. 0606.1 50 extracciones Ref. 0606.2 250 extracciones 1. INTRODUCCION Este kit está designado para una rápida extracción y purificación de ADN genómico de alta calidad a
DANAGENE SPIN BLOOD DNA KIT Ref. 0606.1 50 extracciones Ref. 0606.2 250 extracciones 1. INTRODUCCION Este kit está designado para una rápida extracción y purificación de ADN genómico de alta calidad a
Normas Oficiales Mexicanas SSA1
 Fuente :Diario Oficial de la Federación NOM-019-SSA1-1993 NORMA OFICIAL MEXICANA, QUE ESTABLECE LAS ESPECIFICACIONES SANITARIAS DEL REACTIVO ANTIGLOBULINA HUMANA PARA LA PRUEBA DE COOMBS. Al margen un
Fuente :Diario Oficial de la Federación NOM-019-SSA1-1993 NORMA OFICIAL MEXICANA, QUE ESTABLECE LAS ESPECIFICACIONES SANITARIAS DEL REACTIVO ANTIGLOBULINA HUMANA PARA LA PRUEBA DE COOMBS. Al margen un
ScanGel ScanBrom ml
 ScanGel ScanBrom 86445 12 ml BROMELINA PARA PRUEBAS CRUZADAS IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad se hallan bajo un sistema de garantía de calidad desde la recepción
ScanGel ScanBrom 86445 12 ml BROMELINA PARA PRUEBAS CRUZADAS IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad se hallan bajo un sistema de garantía de calidad desde la recepción
Sistemas Antigénicos eritrocitarios ABO, Lewis y P. Lourdes Torres Ribas 14 de Enero 2015 FBSTIB
 Sistemas Antigénicos eritrocitarios ABO, Lewis y P Lourdes Torres Ribas 14 de Enero 2015 FBSTIB Descubrimiento de los Antígenos -La administración intravenosa de medicamentos se hizo por vez primera en
Sistemas Antigénicos eritrocitarios ABO, Lewis y P Lourdes Torres Ribas 14 de Enero 2015 FBSTIB Descubrimiento de los Antígenos -La administración intravenosa de medicamentos se hizo por vez primera en
NORMA Oficial Mexicana NOM-019-SSA1-1993, Que establece las especificaciones sanitarias del reactivo antiglobulina humana para la prueba de coombs.
 DOF: 07/11/1994 NORMA Oficial Mexicana NOM-019-SSA1-1993, Que establece las especificaciones sanitarias del reactivo antiglobulina humana para la prueba de coombs. AUGUSTO BONDANI GUASTI, Director General
DOF: 07/11/1994 NORMA Oficial Mexicana NOM-019-SSA1-1993, Que establece las especificaciones sanitarias del reactivo antiglobulina humana para la prueba de coombs. AUGUSTO BONDANI GUASTI, Director General
CONSIDERANDO Diario Oficial de la Federación Diario Oficial de la Federación INDICE Prefacio.
 11-07-94 NORMA Oficial Mexicana NOM-019-SSA1-1993, Que establece las especificaciones sanitarias del reactivo antiglobulina humana para la prueba de coombs. Al margen un sello con el Escudo Nacional, que
11-07-94 NORMA Oficial Mexicana NOM-019-SSA1-1993, Que establece las especificaciones sanitarias del reactivo antiglobulina humana para la prueba de coombs. Al margen un sello con el Escudo Nacional, que
DANAGENE SALIVA KIT. Ref Extracciones / Ref Extracciones
 DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION Este kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras de saliva
DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION Este kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras de saliva
EL TEXTO EN COLOR ROJO HA SIDO MODIFICADO
 COMENTARIOS Con fundamento en el numeral 4.11.1 de la Norma Oficial Mexicana NOM-001-SSA1-2010, se publica el presente proyecto a efecto de que los interesados, a partir del 1º de mayo y hasta el 30 de
COMENTARIOS Con fundamento en el numeral 4.11.1 de la Norma Oficial Mexicana NOM-001-SSA1-2010, se publica el presente proyecto a efecto de que los interesados, a partir del 1º de mayo y hasta el 30 de
MDmulticard CENTÍMETROS CAPAZ DE SALVAR UN LABORATORIO DE CINCO UNA VIDA EN CINCO MINUTOS
 MDmulticard UN LABORATORIO DE CINCO CENTÍMETROS CAPAZ DE SALVAR UNA VIDA EN CINCO MINUTOS NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Corporate Communications
MDmulticard UN LABORATORIO DE CINCO CENTÍMETROS CAPAZ DE SALVAR UNA VIDA EN CINCO MINUTOS NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Corporate Communications
GUIA DE SOLUCIÓN DE ERRORES EN EL TAMIZAJE DE HEMOTRANSMISIBLES. Lic. TM. ANDRÉS LARA RODRÍGUEZ Hospital San Bartolomé
 GUIA DE SOLUCIÓN DE ERRORES EN EL TAMIZAJE DE HEMOTRANSMISIBLES Lic. TM. ANDRÉS LARA RODRÍGUEZ Hospital San Bartolomé Esquema de investigación en pruebas fallidas Revisar el procedimiento y determinar
GUIA DE SOLUCIÓN DE ERRORES EN EL TAMIZAJE DE HEMOTRANSMISIBLES Lic. TM. ANDRÉS LARA RODRÍGUEZ Hospital San Bartolomé Esquema de investigación en pruebas fallidas Revisar el procedimiento y determinar
Declaración de conflicto de intereses
 3 de noviembre de 2015 Dr. Carlos A. González Jefe de Hemoterapia Investigador Principal Prueba de compatibilidad positivas Declaración de conflicto de intereses Declaro que: No existe conflicto de interés
3 de noviembre de 2015 Dr. Carlos A. González Jefe de Hemoterapia Investigador Principal Prueba de compatibilidad positivas Declaración de conflicto de intereses Declaro que: No existe conflicto de interés
Antígenos Anticuerpo Aglutinógeno Aglutinina Es la clasificación de la sangre de acuerdo a los antígenos presentes en la membrana de los glóbulos rojo
 Grupos Sanguíneos neos Antígenos Anticuerpo Aglutinógeno Aglutinina Es la clasificación de la sangre de acuerdo a los antígenos presentes en la membrana de los glóbulos rojos y a los anticuerpos presentes
Grupos Sanguíneos neos Antígenos Anticuerpo Aglutinógeno Aglutinina Es la clasificación de la sangre de acuerdo a los antígenos presentes en la membrana de los glóbulos rojos y a los anticuerpos presentes
El laboratorio de inmunohematología
 Artículo de revisión El laboratorio de inmunohematología Lilia Rodríguez Sánchez* Introducción A lo largo de los años el trabajo del laboratorio dentro de los servicios de transfusión ha sufrido cambios
Artículo de revisión El laboratorio de inmunohematología Lilia Rodríguez Sánchez* Introducción A lo largo de los años el trabajo del laboratorio dentro de los servicios de transfusión ha sufrido cambios
TARJETA ABD/GRUPO INVERSO, MONOCLONAL
 TARJETA ABD/GRUPO INVERSO, MONOCLONAL DiaClon ABO/D + Grupo Inverso NOMBRE DiaClon ABO/D + Grupo Inverso DESCRIPCION La tarjeta DiaClon ABO/D + Reverse Grouping contiene anticuerpos monoclonales anti-a,
TARJETA ABD/GRUPO INVERSO, MONOCLONAL DiaClon ABO/D + Grupo Inverso NOMBRE DiaClon ABO/D + Grupo Inverso DESCRIPCION La tarjeta DiaClon ABO/D + Reverse Grouping contiene anticuerpos monoclonales anti-a,
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS
 1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos
 PRT-712.04-080 Página 1 de 9 1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
PRT-712.04-080 Página 1 de 9 1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
TRABAJO PRÁCTICO Nº 5 ESTUDIO DE ANEMIAS
 TRABAJO PRÁCTICO Nº 5 ESTUDIO DE ANEMIAS BIOQUÍMICA CLÍNICA I. INSTITUTO DE BIOQUÍMICA APLICADA. FACULTAD DE BIOQUÍMICA, QUÍMICA Y FARMACIA. UNT. EVALUACIÓN CLÍNICA: ESTUDIO DE LAS ANEMIAS 1) Cuándo fue
TRABAJO PRÁCTICO Nº 5 ESTUDIO DE ANEMIAS BIOQUÍMICA CLÍNICA I. INSTITUTO DE BIOQUÍMICA APLICADA. FACULTAD DE BIOQUÍMICA, QUÍMICA Y FARMACIA. UNT. EVALUACIÓN CLÍNICA: ESTUDIO DE LAS ANEMIAS 1) Cuándo fue
Cuáles son los resultados del ABO, Rh y detección de anticuerpos? Son los resultados del Coombs Indirecto significativo? Por qué?
 CASO CLINICO NRO.1 Paciente femenina de 32 años ingresada al servicio de obstetricia en trabajo de parto. Antecedentes de 2 partos normales previos en otra ciudad. El servicio de obstetricia solicita estudio
CASO CLINICO NRO.1 Paciente femenina de 32 años ingresada al servicio de obstetricia en trabajo de parto. Antecedentes de 2 partos normales previos en otra ciudad. El servicio de obstetricia solicita estudio
Pruebas de compatibilidad, qué técnica emplear?
 Pruebas de compatibilidad, qué técnica emplear? XIV Jornadas de Medicina Transfusional Dra. Carmen Buesa García Sº Hematología y Hemoterapia Hospital Universitario Central de Asturias Pruebas pretransfusionales
Pruebas de compatibilidad, qué técnica emplear? XIV Jornadas de Medicina Transfusional Dra. Carmen Buesa García Sº Hematología y Hemoterapia Hospital Universitario Central de Asturias Pruebas pretransfusionales
Discrepancias. Fuente: Manual Téfnico de la AABB (17º edición) 1
 Discrepancias ABO Tec. Graciela Deutsch - Noviembre 2015 Fuente: Manual Téfnico de la AABB (17º edición) 1 2 Antisueros conocidos GRs. de fenotipo ABO conocidos A B O Anti-A A Anti-B B Anti-AB AB 3 DETERMINACIÓN
Discrepancias ABO Tec. Graciela Deutsch - Noviembre 2015 Fuente: Manual Téfnico de la AABB (17º edición) 1 2 Antisueros conocidos GRs. de fenotipo ABO conocidos A B O Anti-A A Anti-B B Anti-AB AB 3 DETERMINACIÓN
B) Añadir al medio LB, además de la ampicilina, el IPTG (conc final, 0.5 mm) y X-Gal (conc. final 80 µg/ml). Es decir, para 100 ml de LB adicionar:
 Medios utilizados en este apartado: 1.-IPTG stock solution (0.1 M) - 0.6 g IPTG. - Añadir agua estéril a un volumen final de 25 ml. Filtrar con papel secante pasando la solución a tubos eurotubos. Guardar
Medios utilizados en este apartado: 1.-IPTG stock solution (0.1 M) - 0.6 g IPTG. - Añadir agua estéril a un volumen final de 25 ml. Filtrar con papel secante pasando la solución a tubos eurotubos. Guardar
Speed Leish K TM Kit de diagnóstico veterinario Sólo para uso in vitro
 Speed Leish K TM ES Speed Leish K TM Kit de diagnóstico veterinario Sólo para uso in vitro n INTERES CLÍNICO La leishmaniosis canina es una enfermedad causada por la proliferación de un parásito Leishmania
Speed Leish K TM ES Speed Leish K TM Kit de diagnóstico veterinario Sólo para uso in vitro n INTERES CLÍNICO La leishmaniosis canina es una enfermedad causada por la proliferación de un parásito Leishmania
D VI ce ccd VI.Ee Raro 600 Ag/GR Caucásicos. D VI Ce BARC CcD VI.ee Más frecuente Ag/GR Caucásicos y Japoneses D VI
 D VI tipo 1 D VI tipo 2 D VI tipo 3 D VI tipo 4 D VI tipo 1 D VI tipo 2 D VI tipo 3 D VI tipo 4 D VI tipo 1 D VI ce ccd VI.Ee Raro 600 Ag/GR Caucásicos D VI tipo 2 D VI Ce BARC CcD VI.ee Más frecuente
D VI tipo 1 D VI tipo 2 D VI tipo 3 D VI tipo 4 D VI tipo 1 D VI tipo 2 D VI tipo 3 D VI tipo 4 D VI tipo 1 D VI ce ccd VI.Ee Raro 600 Ag/GR Caucásicos D VI tipo 2 D VI Ce BARC CcD VI.ee Más frecuente
Al margen un sello con el Escudo Nacional, que dice: Estados Unidos Mexicanos.- Secretaría de Salud.
 NORMA OFICIAL MEXICANA NOM-017-SSA1-1993, QUE ESTABLECE LAS ESPECIFICACIONES SANITARIAS DE LOS REACTIVOS HEMOCLASIFICADORES PARA DETERMINAR GRUPOS DEL SISTEMA ABO. Al margen un sello con el Escudo Nacional,
NORMA OFICIAL MEXICANA NOM-017-SSA1-1993, QUE ESTABLECE LAS ESPECIFICACIONES SANITARIAS DE LOS REACTIVOS HEMOCLASIFICADORES PARA DETERMINAR GRUPOS DEL SISTEMA ABO. Al margen un sello con el Escudo Nacional,
Técnicas de aglutinación En estas técnicas se hacen visibles los complejos Ag-Ac por la aglutinación que producen los anticuerpos cuando el Ag forma
 Técnicas de aglutinación En estas técnicas se hacen visibles los complejos Ag-Ac por la aglutinación que producen los anticuerpos cuando el Ag forma parte, o se ha unido artificialmente, a la superficie
Técnicas de aglutinación En estas técnicas se hacen visibles los complejos Ag-Ac por la aglutinación que producen los anticuerpos cuando el Ag forma parte, o se ha unido artificialmente, a la superficie
CONSIDERANDO Diario Oficial de la Federación Diario Oficial de la Federación INDICE Prefacio Objetivo y campo de aplicación
 11-18-94 NORMA Oficial Mexicana NOM-017-SSA1-1993, Que establece las especificaciones sanitarias de los reactivos hemoclasificadores para determinar grupos del sistema ABO. Al margen un sello con el Escudo
11-18-94 NORMA Oficial Mexicana NOM-017-SSA1-1993, Que establece las especificaciones sanitarias de los reactivos hemoclasificadores para determinar grupos del sistema ABO. Al margen un sello con el Escudo
Dra. GIOVANA GARCIA Dra. Giovana García
 FUNDAMENTOS DE INMUNOHEMATOLOGÍA Dra. GIOVANA GARCIA Dra. Giovana García INMUNOHEMATOLOGIA Parte de la hematología que estudia los inmunes procesos inmunes relacionados don las células sanguíneas. Los
FUNDAMENTOS DE INMUNOHEMATOLOGÍA Dra. GIOVANA GARCIA Dra. Giovana García INMUNOHEMATOLOGIA Parte de la hematología que estudia los inmunes procesos inmunes relacionados don las células sanguíneas. Los
ScanGel ReverScan A1, B x 5 ml ReverScan A1, A2, B, O x 5 ml
 ScanGel ReverScan A1, B 86790 2 x 5 ml ReverScan A1, A2, B, O 86795 4 x 5 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PARA LA PRUEBA SÉRICA DEL TIPAJE ABO IVD Todos los productos fabricados y comercializados
ScanGel ReverScan A1, B 86790 2 x 5 ml ReverScan A1, A2, B, O 86795 4 x 5 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PARA LA PRUEBA SÉRICA DEL TIPAJE ABO IVD Todos los productos fabricados y comercializados
NORMA OFICIAL MEXICANA NOM-018-SSA1-1993, Que establece las especificaciones sanitarias del reactivo ANTI RH para identificar el ANTÍGENO D
 NORMA OFICIAL MEXICANA NOM-018-SSA1-1993, Que establece las especificaciones sanitarias del reactivo ANTI RH para identificar el ANTÍGENO D Al margen un sello con el Escudo Nacional, que dice: Estados
NORMA OFICIAL MEXICANA NOM-018-SSA1-1993, Que establece las especificaciones sanitarias del reactivo ANTI RH para identificar el ANTÍGENO D Al margen un sello con el Escudo Nacional, que dice: Estados
DANAGENE PLASMID MIDI/MAXI KIT
 REF.0702.4 25 Midis REF.0702.5 10 Maxis DANAGENE PLASMID MIDI/MAXI KIT 1. INTRODUCCION DANAGENE PLASMID Midi/Maxiprep Kit proporciona un método simple para purificar ADN plasmídico a partir de cultivos
REF.0702.4 25 Midis REF.0702.5 10 Maxis DANAGENE PLASMID MIDI/MAXI KIT 1. INTRODUCCION DANAGENE PLASMID Midi/Maxiprep Kit proporciona un método simple para purificar ADN plasmídico a partir de cultivos
NORMA Oficial Mexicana NOM-018-SSA1-1993, Que establece las especificaciones sanitarias del reactivo anti RH para identificar el antígeno D.
 01-16-95 NORMA Oficial Mexicana NOM-018-SSA1-1993, Que establece las especificaciones sanitarias del reactivo anti RH para identificar el antígeno D. Al margen un sello con el Escudo Nacional, que dice:
01-16-95 NORMA Oficial Mexicana NOM-018-SSA1-1993, Que establece las especificaciones sanitarias del reactivo anti RH para identificar el antígeno D. Al margen un sello con el Escudo Nacional, que dice:
PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013
 PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013 Este programa de control externo permite verificar el desempeño de los procesos en el área de Inmunohematología, evalúa los reactivos utilizados
PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013 Este programa de control externo permite verificar el desempeño de los procesos en el área de Inmunohematología, evalúa los reactivos utilizados
Citología General ThinPrep. Preparación de Muestras No Ginecológicas
 Citología General ThinPrep Preparación de Muestras No Ginecológicas Beneficios de la Tecnología ThinPrep El uso de Citología General ThinPrep para muestras No-ginecológicas: Optimiza la preservación celular.
Citología General ThinPrep Preparación de Muestras No Ginecológicas Beneficios de la Tecnología ThinPrep El uso de Citología General ThinPrep para muestras No-ginecológicas: Optimiza la preservación celular.
ARTRITIS REUMATOIDE. Diagnóstico de laboratorio en la clínica médica de hoy. 2 de octubre de 2018 Bioq. María Eugenia Dacharry
 ARTRITIS REUMATOIDE Diagnóstico de laboratorio en la clínica médica de hoy 2 de octubre de 2018 Bioq. María Eugenia Dacharry DEFINICIÓN La artritis reumatoidea (AR) es una enfermedad inflamatoria, crónica
ARTRITIS REUMATOIDE Diagnóstico de laboratorio en la clínica médica de hoy 2 de octubre de 2018 Bioq. María Eugenia Dacharry DEFINICIÓN La artritis reumatoidea (AR) es una enfermedad inflamatoria, crónica
ANEXOS. Anexo 1. Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v).
 ANEXOS Anexo 1 Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v). 1. Tomar 6.011mL de ácido acético y aforar a 1L de agua HPLC. 2. Pesar 13.609 g de acetato de sodio y aforar a 1L de agua
ANEXOS Anexo 1 Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v). 1. Tomar 6.011mL de ácido acético y aforar a 1L de agua HPLC. 2. Pesar 13.609 g de acetato de sodio y aforar a 1L de agua
DANAGENE microspin DNA KIT
 Ref. 0607.1 50 extracciones Ref. 0607.2 250 extracciones 1.INTRODUCCION DANAGENE microspin DNA KIT Este kit permite una eficiente extracción de ADN genómico y mitocondrial a partir de muestras de pequeño
Ref. 0607.1 50 extracciones Ref. 0607.2 250 extracciones 1.INTRODUCCION DANAGENE microspin DNA KIT Este kit permite una eficiente extracción de ADN genómico y mitocondrial a partir de muestras de pequeño
MANUAL DE NORMAS Y PROCEDIMIENTOS PROCEDIMIENTO: OPERATIVOS DE ORINAS
 SERVICIO DE LABORATORIO 1 DE 5 1. OBJETIVO El objetivo del presente documento es describir el procedimiento para determinar las características físicas, química y microscópicas de muestras de orinas. 2.
SERVICIO DE LABORATORIO 1 DE 5 1. OBJETIVO El objetivo del presente documento es describir el procedimiento para determinar las características físicas, química y microscópicas de muestras de orinas. 2.
INTRODUCCIÓN AL ELISA
 INTRODUCCIÓN AL ELISA 10 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es aportar a los estudiantes el conocimiento y metodología de la técnica del ELISA 2. COMPONENTES
INTRODUCCIÓN AL ELISA 10 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es aportar a los estudiantes el conocimiento y metodología de la técnica del ELISA 2. COMPONENTES
Técnico en Hematología y Hemoterapia. Sanidad, Dietética y Nutrición
 Técnico en Hematología y Hemoterapia Sanidad, Dietética y Nutrición Ficha Técnica Categoría Sanidad, Dietética y Nutrición Referencia 166762-1501 Precio 50.36 Euros Sinopsis La sangre es la especialidad
Técnico en Hematología y Hemoterapia Sanidad, Dietética y Nutrición Ficha Técnica Categoría Sanidad, Dietética y Nutrición Referencia 166762-1501 Precio 50.36 Euros Sinopsis La sangre es la especialidad
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar
 4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
MATERLAB S.L. Pº PONTONES 7 28005 MADRID TLF. 91/4745799 4745623 FAX.
 Técnicas de Uso 1 -INDICE- ALBÚMINA BOVINA AL 30%... 13 CONTROL-TEST ANTI-D (ANTI-RH I)... 7 PAPAÍNA LIOFILIZADA... 14 SOLUCIÓN DE BAJA FUERZA IÓNICA LISS DOPE... 12 SUERO ANTIGLOBULINA HUMANA... 10 SUERO-
Técnicas de Uso 1 -INDICE- ALBÚMINA BOVINA AL 30%... 13 CONTROL-TEST ANTI-D (ANTI-RH I)... 7 PAPAÍNA LIOFILIZADA... 14 SOLUCIÓN DE BAJA FUERZA IÓNICA LISS DOPE... 12 SUERO ANTIGLOBULINA HUMANA... 10 SUERO-
RT- PCR diagnóstica del Cotton leafroll dwarf virus (CLRDV) en plantas de algodón
 RT- PCR diagnóstica del Cotton leafroll dwarf virus (CLRDV) en plantas de algodón La identificación rápida y precisa de los patógenos que afectan a los cultivos de interés agronómico es crítica para predecir
RT- PCR diagnóstica del Cotton leafroll dwarf virus (CLRDV) en plantas de algodón La identificación rápida y precisa de los patógenos que afectan a los cultivos de interés agronómico es crítica para predecir
SISTEMA Rh. Bioquìmica: Ma. Eugenia Morales
 SISTEMA Rh Bioquìmica: Ma. Eugenia Morales El sistema Rh RH es el sistema más polimórfico Presenta mas de 45 antigenos Descubierto por Landsteiner y Wiener en 194 por un trabajo en monos Rhesus Genes RH
SISTEMA Rh Bioquìmica: Ma. Eugenia Morales El sistema Rh RH es el sistema más polimórfico Presenta mas de 45 antigenos Descubierto por Landsteiner y Wiener en 194 por un trabajo en monos Rhesus Genes RH
UNIVERSIDAD NACIONAL DEL CHIMBORAZO FACULTAD DE CIENCIAS DE LA SALUD CARRERA DE LABORATORIO CLÍNICO E HISTOPATOLÓGICO
 UNIVERSIDAD NACIONAL DEL CHIMBORAZO FACULTAD DE CIENCIAS DE LA SALUD CARRERA DE LABORATORIO CLÍNICO E HISTOPATOLÓGICO Proyecto de Investigación Previo a la Obtención del Título de Licenciada en Ciencias
UNIVERSIDAD NACIONAL DEL CHIMBORAZO FACULTAD DE CIENCIAS DE LA SALUD CARRERA DE LABORATORIO CLÍNICO E HISTOPATOLÓGICO Proyecto de Investigación Previo a la Obtención del Título de Licenciada en Ciencias
TEMA 14. Métodos inmunológicos para la identificación microbiana
 TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TRABAJO PRÁCTICO Nº 3 PROPIEDADES DE LA SANGRE DETERMINACIÓN DE GRUPOS SANGUÍNEOS INTERPRETACIÓN FISIOLÓGICA DE LAS PRUEBAS
 TRABAJO PRÁCTICO Nº 3 PROPIEDADES DE LA SANGRE DETERMINACIÓN DE GRUPOS SANGUÍNEOS INTERPRETACIÓN FISIOLÓGICA DE LAS PRUEBAS 1. OBJETIVOS Que, a partir de los conocimientos teóricos, los alumnos logren:
TRABAJO PRÁCTICO Nº 3 PROPIEDADES DE LA SANGRE DETERMINACIÓN DE GRUPOS SANGUÍNEOS INTERPRETACIÓN FISIOLÓGICA DE LAS PRUEBAS 1. OBJETIVOS Que, a partir de los conocimientos teóricos, los alumnos logren:
SON COMPATIBLES ELLOS NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Global Corporate Communications.
 NOT VALID FOR PRINTING! ELLOS SON COMPATIBLES SEGURIDAD FLEXIBILIDAD & BELLEZA NOT VALID FOR PRINTING! En Grifols, sabemos que su máxima preocupación en la transfusión sanguínea es garantizar la seguridad
NOT VALID FOR PRINTING! ELLOS SON COMPATIBLES SEGURIDAD FLEXIBILIDAD & BELLEZA NOT VALID FOR PRINTING! En Grifols, sabemos que su máxima preocupación en la transfusión sanguínea es garantizar la seguridad
A. hemolíticas extracorpusculares, métodos de estudio:
 ANEMI AS NORMOCÍ TI CAS Anemias hemolíticas A. hemolíticas intracorpusculares, métodos de estudio: MEMBRANOPATIAS: esferocitosis y eliptocitosis hereditaria ENZIMOPATIAS: G6PD y PK HEMOGLOBINOPATIAS: talasemias
ANEMI AS NORMOCÍ TI CAS Anemias hemolíticas A. hemolíticas intracorpusculares, métodos de estudio: MEMBRANOPATIAS: esferocitosis y eliptocitosis hereditaria ENZIMOPATIAS: G6PD y PK HEMOGLOBINOPATIAS: talasemias
RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA RhD
 DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA RhD 14 de enero de 2013 AUTOR TM. Andrés Aburto Almonacid. Encargado Área de Inmunohematología. Sección de
DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA RhD 14 de enero de 2013 AUTOR TM. Andrés Aburto Almonacid. Encargado Área de Inmunohematología. Sección de
Programa Formativo. Objetivos. Código: Curso: Hematología y Hemoterapia. Duración: 70h.
 Código: 40657 Curso: Hematología y Hemoterapia Modalidad: ONLINE Duración: 70h. Objetivos La sangre es un tejido líquido que circula permanentemente por el sistema vascular y está formado por vasos sanguíneos
Código: 40657 Curso: Hematología y Hemoterapia Modalidad: ONLINE Duración: 70h. Objetivos La sangre es un tejido líquido que circula permanentemente por el sistema vascular y está formado por vasos sanguíneos
Sistema de Evaluación:
 Universidad Central Del Este UCE Facultad de Ciencias de la Salud Escuela de Bioanálisis Programa de la asignatura: (BIA-061) Inmunohematología Total de Créditos: 3 Teoría: 2 Practica: 3. Prerrequisitos:
Universidad Central Del Este UCE Facultad de Ciencias de la Salud Escuela de Bioanálisis Programa de la asignatura: (BIA-061) Inmunohematología Total de Créditos: 3 Teoría: 2 Practica: 3. Prerrequisitos:
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
PLIEGO DE BASES TÉCNICAS
 PLIEGO DE BASES TÉCNICAS EXPEDIENTE Nº: G/112/20/1/1091/O491/0000/102013 OBJETO: Provisión de reactivos para Tipaje Inmunohematológico en donaciones de sangre en el Centro Vasco de Transfusión y Tejidos
PLIEGO DE BASES TÉCNICAS EXPEDIENTE Nº: G/112/20/1/1091/O491/0000/102013 OBJETO: Provisión de reactivos para Tipaje Inmunohematológico en donaciones de sangre en el Centro Vasco de Transfusión y Tejidos
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987)
 EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
Revista Salud Pública y Nutrición Edición Especial 3-2012 23 y 24 de Agosto 2011; Monterrey, N.L., México
 RESPYN Revista Salud Pública y Nutrición Edición Especial 3-2012 23 y 24 de Agosto 2011; Monterrey, N.L., México PRUEBAS Questions?! PRETRANSFUSIONALES Y SU CONTROL DE CALIDAD Pruebas Pre-transfusionales?
RESPYN Revista Salud Pública y Nutrición Edición Especial 3-2012 23 y 24 de Agosto 2011; Monterrey, N.L., México PRUEBAS Questions?! PRETRANSFUSIONALES Y SU CONTROL DE CALIDAD Pruebas Pre-transfusionales?
RECOMENDACIONES PARA LA DETECCIÓN E IDENTIFICACIÓN DE ANTICUERPOS IRREGULARES ERITROCITARIOS
 Instituto de Salud Pública Ministerio de Salud DOCUMENTOS TÉCNICOS RA EL LABORATORIO CLÍNICO RECOMENDACIONES RA LA DETECCIÓN E IDENTIFICACIÓN DE ANTICUERPOS IRREGULARES ERITROCITARIOS DERTAMENTO LABORATORIO
Instituto de Salud Pública Ministerio de Salud DOCUMENTOS TÉCNICOS RA EL LABORATORIO CLÍNICO RECOMENDACIONES RA LA DETECCIÓN E IDENTIFICACIÓN DE ANTICUERPOS IRREGULARES ERITROCITARIOS DERTAMENTO LABORATORIO
 Trascripción de la respuesta al primer examen 1) El marcaje de hematíes con 99m Tc se basa en la capacidad que posee el anión pertecnetato 99m TcO - 4 de atravesar la membrana del eritrocito, pudiendo
Trascripción de la respuesta al primer examen 1) El marcaje de hematíes con 99m Tc se basa en la capacidad que posee el anión pertecnetato 99m TcO - 4 de atravesar la membrana del eritrocito, pudiendo
P08.- DETERMINACIÓN DE LOS GRUPOS SANGUÍNEOS
 P08.- DETERMINACIÓN DE LOS GRUPOS SANGUÍNEOS Objetivos de la práctica Comprender el concepto de grupo sanguíneo y conocer los tipos sanguíneos más importantes. Conocer la importancia de determinar el grupo
P08.- DETERMINACIÓN DE LOS GRUPOS SANGUÍNEOS Objetivos de la práctica Comprender el concepto de grupo sanguíneo y conocer los tipos sanguíneos más importantes. Conocer la importancia de determinar el grupo
Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91
 Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91 NOTA Aclaratoria a la Primera Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico, publicada el
Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91 NOTA Aclaratoria a la Primera Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico, publicada el
ANALISIS CITOMETRICO DEL CONTENIDO EN DNA EN SANGRE Y MEDULA OSEA
 ANALISIS CITOMETRICO DEL CONTENIDO EN DNA EN SANGRE Y MEDULA OSEA Sistema DNA-Prep (Beckman-Coulter) DNA-Prep LPR: Reactivo de lisis de los eritrocitos y permeabilización de membranas celulares DNA-Prep
ANALISIS CITOMETRICO DEL CONTENIDO EN DNA EN SANGRE Y MEDULA OSEA Sistema DNA-Prep (Beckman-Coulter) DNA-Prep LPR: Reactivo de lisis de los eritrocitos y permeabilización de membranas celulares DNA-Prep
ScanGel ScanCell P x 10 ml
 ScanGel ScanCell P 86596 3 x 10 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PRETRATADOS CON PAPAÍNA PARA LA DETECCIÓN DE LOS ANTICUERPOS IRREGULARES ANTIERITROCITARIOS IVD Todos los productos fabricados y
ScanGel ScanCell P 86596 3 x 10 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PRETRATADOS CON PAPAÍNA PARA LA DETECCIÓN DE LOS ANTICUERPOS IRREGULARES ANTIERITROCITARIOS IVD Todos los productos fabricados y
EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDOS NUCLEICOS DE LA LEVADURA
 EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDS NUCLEICS DE LA LEVADURA bjetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la
EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDS NUCLEICS DE LA LEVADURA bjetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la
PROTOCOLO PARA EL AISLAMIENTO DE CÉLULAS DE FRACCIÓN ESTROMAL VASCULAR DERIVADAS DE TEJIDO ADIPOSO
 PROTOCOLO PARA EL AISLAMIENTO DE CÉLULAS DE FRACCIÓN ESTROMAL VASCULAR DERIVADAS DE TEJIDO ADIPOSO INDICE: 1. OBJETIVOS 2. NORMAS DE SEGURIDAD Y CONSIDERACIONES IMPORTANTES 3. LISTA DE MATERIALES 4. EQUIPOS
PROTOCOLO PARA EL AISLAMIENTO DE CÉLULAS DE FRACCIÓN ESTROMAL VASCULAR DERIVADAS DE TEJIDO ADIPOSO INDICE: 1. OBJETIVOS 2. NORMAS DE SEGURIDAD Y CONSIDERACIONES IMPORTANTES 3. LISTA DE MATERIALES 4. EQUIPOS
MANUAL DE PROCEDIMIENTOS SOLICITUD DE HEMOCOMPONENTES
 Página 1 de 7 1. Objetivo. Proporcionar hemocomponentes que cumpliendo con la Norma Oficial Mexicana, den el beneficio terapéutico al paciente, con el menor riesgo posible. 2. Alcance: Este procedimiento
Página 1 de 7 1. Objetivo. Proporcionar hemocomponentes que cumpliendo con la Norma Oficial Mexicana, den el beneficio terapéutico al paciente, con el menor riesgo posible. 2. Alcance: Este procedimiento
PROCEDIMIENTO TECNICA DE COAGULASA EN TUBO PRT
 Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
Guía del Curso Técnico en Hematología y Hemoterapia
 Guía del Curso Técnico en Hematología y Hemoterapia Modalidad de realización del curso: Titulación: A distancia y Online Diploma acreditativo con las horas del curso OBJETIVOS La sangre es un tejido líquido
Guía del Curso Técnico en Hematología y Hemoterapia Modalidad de realización del curso: Titulación: A distancia y Online Diploma acreditativo con las horas del curso OBJETIVOS La sangre es un tejido líquido
INSTRUCTIVO PARA EL DIAGNÓSTICO DE PLUM POX VIRUS MEDIANTE ELISA
 DEPARTAMENTO LABORATORIO Y ESTACIONES CUARENTENARIAS AGRÍCOLA Y PECUARIA INSTRUCTIVO PARA EL DIAGNÓSTICO DE PLUM POX VIRUS MEDIANTE ELISA Preparación Nombre Cargo Firma Marcelo Encargado Laboratorio Cabrera
DEPARTAMENTO LABORATORIO Y ESTACIONES CUARENTENARIAS AGRÍCOLA Y PECUARIA INSTRUCTIVO PARA EL DIAGNÓSTICO DE PLUM POX VIRUS MEDIANTE ELISA Preparación Nombre Cargo Firma Marcelo Encargado Laboratorio Cabrera
MANUAL DE NORMAS Y PROCEDIMIENTOS GENERALIDADES BIOQUIMICA CLINICA
 SERVICIO DE LABORATORIO 1 DE 7 Cochabamba, 2010 SERVICIO DE LABORATORIO 2 DE 7 1- Presentación El presente Manual de procedimientos de Laboratorio en Bioquímica Clínica, es una herramienta básica y fundamental
SERVICIO DE LABORATORIO 1 DE 7 Cochabamba, 2010 SERVICIO DE LABORATORIO 2 DE 7 1- Presentación El presente Manual de procedimientos de Laboratorio en Bioquímica Clínica, es una herramienta básica y fundamental
MEDIDAS DE INTERACCIÓN ANTÍGENO-ANTICUERPO DETERMINACIÓN DE GRUPO SANGUÍNEO: HEMAGLUTINACIÓN
 Departamento de Inmunología Facultad de Medicina MEDIDAS DE INTERACCIÓN ANTÍGENO-ANTICUERPO DETERMINACIÓN DE GRUPO SANGUÍNEO: HEMAGLUTINACIÓN I. Introducción. La determinación del grupo sanguíneo es una
Departamento de Inmunología Facultad de Medicina MEDIDAS DE INTERACCIÓN ANTÍGENO-ANTICUERPO DETERMINACIÓN DE GRUPO SANGUÍNEO: HEMAGLUTINACIÓN I. Introducción. La determinación del grupo sanguíneo es una
REVISTA. (Banco de Sangre. Hospital de San Juan de Dios. Bogotá). Por LORELA ENTERLINE DE F AJ ARDO,
 REVISTA FACULTAD DE LA DE MEDICINA VOLUMEN 30 ABRIL JUNIO DE 1962 METDDD ABREVIADDPARA PRUEBA [RUZADA (Banco de Sangre. Hospital de San Juan de Dios. Bogotá). Por LORELA ENTERLINE DE F AJ ARDO, M.. S.
REVISTA FACULTAD DE LA DE MEDICINA VOLUMEN 30 ABRIL JUNIO DE 1962 METDDD ABREVIADDPARA PRUEBA [RUZADA (Banco de Sangre. Hospital de San Juan de Dios. Bogotá). Por LORELA ENTERLINE DE F AJ ARDO, M.. S.
