Tema 6. ESTRUCTURA NUCLEAR
|
|
|
- Juan Francisco Sevilla Álvarez
- hace 6 años
- Vistas:
Transcripción
1 Introducción Experimento de Rutherford. Existencia del núcleo Partículas nucleares Tamaño y densidad del núcleo Energía de enlace y estabilidad nuclear Desintegración radiactiva Radiactividad α,β,γ Series radiactivas Reacciones nucleares
2 Experimento de Rutherford (1909) Bombardeo con un haz de partículas α una lámina fina de Au. Modelo de THOMPSON: la carga positiva y los electrones se distribuyen homogéneamente dentro del átomo. Las partículas α atravesarían la lámina de Au sin apenas desviarse. Las partículas α son masivas (8.000 m e ) y llevan gran velocidad. Por ello, la fuerzas eléctricas serían insuficientes para desviarlas. Observación: Un pequeño porcentaje de partículas se retrodispersan (aprox. 1 de cada 8.000). Rutherford: "tan sorprendente como si le disparases balas de cañón a una hoja de papel y rebotasen hacia ti". El que la mayoría de las partículas atraviesen la hoja metálica, indica que gran parte del átomo está vacío. Y el rebote de las partículas α indica una interacción directa con algo cargado positivamente y a la vez muy másico. MODELO ATOMICO DE RUTHERFORD : el átomo está formado por un núcleo y una corteza. El núcleo tiene carga positiva, un radio muy pequeño y en él reside casi toda la masa del átomo. La corteza está formada por una nube de electrones que orbitan alrededor del núcleo. Radio atómico del orden de 10 4 veces el Radio nuclear
3 Partículas nucleares El núcleo posee solo 2 tipos de partículas: neutrones n y protones p. Protón con carga +e y neutrón sin carga Masas muy similares: m n es 0.2% mayor que m p. Z = número atómico = nº de protones (= nº de electrones en átomos neutros) A= número másico = N + Z = nº total de nucleones Una especie nuclear se denomina nucleido Isótopos: Son aquellos nucleidos que teniendo igual número atómico Z tienen distinto nº de neutrones (distinta masa y distinto número másico A) Los isótopos de un mismo elemento poseen las mismas propiedades químicas, pues éstas solo dependen de los electrones en la corteza (nº electrones = Z) Los isótopos tienen distintas propiedades nucleares. Por ejemplo, el 12 C es estable, mientras el 14 C es radiactivo.
4 Abundancia natural: Porcentaje de cada isótopo en la naturaleza. H (Z=1): 1 H (1p): 99,985% deuterio 2 H: (1p + 1n): 0,014% tritio 3 H: (1p+ 2n): despreciable (radiactivo) U (Z=92): 238 U (92p + 146n): 99,276% 235 U (92p + 143n): 0,720% 234 U (92p + 142n): 0,0054% Todos radiactivos O (Z=8): 16 O (8p + 8n): 99,762% 17 O (8p + 9n): 0,038% 18 O (8p + 10n): 0,200% Fuerzas nucleares: Dentro del núcleo, los nucleones ejercen una fuerza atractiva muy intensa sobre sus vecinos más próximos. Fuerza nuclear fuerte o fuerza hadrónica F. Nuclear (N-N) >>> F. electr (p-p) >>> F. gravit (despreciable en F. Nuclear) FN (p-p) = FN (n-n) = FN (p-n) Muy corto alcance (Nula para distancias de algunos fm (1 fm = m))
5 Tamaño nuclear y densidad partícula El tamaño y forma de los núcleos se determina mediante experimentos de dispersión de partículas con núcleos: partícula Electrones distribución de carga Neutrones distribución de materia (nucleones) La mayoría de los núcleos son esféricos con radios nucleares dados por: núcleo R = R o A 1/3 (R 0 = 1,2-1,4 fm) La densidad nuclear es aproximadamente la misma para todos los núcleos El volumen nuclear es proporcional al nº de nucleones V = 4/3 π R 3 = 4/3 π R o3 A ρ= A / V = 3/(4 π R 3 o ) = 1,38 *10 38 nucl/cm 3 ρ aprox. 2,3 * g/cm 3 Análogo a una gota líquida: igual densidad con independencia del tamaño (fuerzas de corto alcance) Modelo de la gota liquida (fisión nuclear)
6 Estabilidad nuclear Núcleos ligeros: estabilidad con N = Z Ejemplo: A =8 8 n 4n + 4p La situación (4n + 4p) es mas estable (el ppio de exclusión de Pauli solo se da con partículas idénticas) Núcleos pesados: estabilidad con N > Z (para minimizar la repulsión culombiana entre protones)
7 Masa y energía de enlace nuclear Partículas aisladas E b = M c 2 La masa de un núcleo es menor que la suma de la masa de sus constituyentes. M N (Z, A) < Z m p + (A-Z) m n Cuando 2 o mas nucleones se unen entre sí para formar un núcleo, parte de la masa se pierde y se transforma en energía, que se desprende. Esta energía es la energía de enlace del núcleo. E b = [ Z m p + (A-Z) m n - M N (Z, A) ] c 2 Inversamente, para dividir un núcleo en sus nucleones individuales hay que aportar esa energía, que se transformará en masa, aumentando la masa de los nucleones. núcleo 1 u = (1/12) M a ( 12 C) (1 u) c 2 = 931,5 MeV Expresión aproximada E b = (Z M H + (A-Z) m n M A ) c 2 (se cancelan las masas electrónicas)
8 Ejemplo: 4 He (Z =2) M H = 1, u M A ( 4 He) = 4, u m n = 1, u Expresión aproximada E b = [ Z M H + (A-Z) m n M A ( 4 He) ] c 2 = = 0, u x 931,5 MeV/u = 28,30 MeV Energía de enlace por nucleón E b /A Grafica de E b /A frente a A Valor medio del orden 8,3 MeV Aprox. horizontal para A > 50: E b proporc.a A Cada nucleón solo es atraído por sus vecinos mas próximos (Saturación de la fuerza nuclear). Densidad nuclear constante. (Si cada nucleón se enlazara con todos los nucleones del núcleo, cada nucleón tendría A-1 enlaces y el nº total de enlaces sería A(A-1). La E b no sería cte.) A>50: pendiente negativa debida a la fuerza de Coulomb (aumenta como Z 2 ), que disminuye la energía de enlace. A<50: La función va creciendo con A como consecuencia del aumento del número de nucleones vecinos. A > 300, la fuerza ce Coulomb es tan grande que el núcleo es inestable y se fisiona espontáneamente.
9 Radiactividad Muchos núcleos son radiactivos: se desintegran en otros núcleos mediante emisión de partículas: fotones, electrones, partículas α, neutrones, protones. La desintegración radiactiva es un proceso estadístico (estocástico): solo conocemos la probabilidad de que un núcleo se desintegre en cierto intervalo de tiempo. λ = constante radiactiva de un núcleo= probabilidad de que se desintegre en un intervalo de tiempo. dn = - λ N dt Ln N = - λt + C N(t) = N o e - λt Actividad (A) = velocidad de desintegración La velocidad de desintegración no es constante, sino que va disminuyendo exponencialmente. A(t) = - dn/dt = λ N(t) = λn o e - λt = A o e - λt
10 Radiactividad Tiempo de vida media: τ = 1/λ (tiempo para que N se reduzca a N o /e) (37%) Periodo de semidesintegración: tiempo necesario para que el nº de núcleos o la actividad se reduzca a la mitad N o /2 = N o e λτ1/2 T 1/2 = ln2/λ = 0,693 τ Los T 1/2 varían desde valores muy pequeños (< µs) a valores muy grandes (10 16 años) Unidades de Actividad (SI) (Bequerelio) 1 Bq = 1 desintegracion/s ( Curie) 1 Ci = 3,7 * des/s (Bq) El Curie es equivalente a la actividad que emite 1 gramo de Radio. Es una unidad muy grande. Se usan el mci, µci, etc
11 DESINTEGRACIÓN α Naturaleza de la radiación: núcleos de 4 He (Rutherford, 1909) El núcleo con Z, A se transforma en un núcleo con (Z-2) y (A-4) Todos los núcleos pesados (Z > 83) son teóricamente inestables frente a la emisión α, ya que la masa del núcleo es mayor que la de los productos: núcleo hijo y partícula α Hijo X' Progenitor X Alfa Conservación de masa-energía Ejemplo: 232 Th 228 Ra + α m x c 2 = m x' c 2 + T x' + m alfa c 2 + T alfa (m x - ( m x' + m alfa ) ) c 2 = T x' + T alfa = Q > 0 PROCESO ESPONTÁNEO M a ( 232 Th) = 232, u M a ( 238 Ra) = 228, u M α = 4, u Q = [ 0,004382u x 931,5 MeV/u = 4,08 MeV
12 Conservación del momento p x ' = - p alfa ( T = p 2 / 2m ) m alfa T alfa = m x' T x' Q T alfa = = Q (1- (4/A)) 1 + (m alfa /m x' ) (A >> 4) T alfa (98% Q) E α ( entre 4 y 8 MeV) T 1/2 (entre 10-5 s y años): esta enorme variación fue explicada por Gamow (1928) Teoría Gamow: la partícula α se forma dentro del núcleo y luego escapa por efecto túnel a través de la barrera de Coulomb. Un incremento de Q reduce la altura y anchura de la barrera, y por tanto una mayor probabilidad de penetrarla E α aumenta λ aumenta T 1/2 disminuye ( P alfa, T alfa ) T x' (2% Q) P x = 0 X X ' ( P x', T x' )
13 DESINTEGRACIÓN β Tiene lugar en los núcleos que presentan un exceso o defecto de neutrones para conseguir la estabilidad No se modifica el número másico A. Solo el Z. Emisión β - : Este proceso ocurre espontáneamente para neutrones libres, con un T 1/2 = 10,8 min. Emisión β + : Este proceso está prohibido para protones libres. Implicaría una violación del principio de conservación de la energía (la suma de las energías de los productos resultantes es mayor que la del protón) X(A,Z) X (A, Z+1) + e - + v e Sin embargo, para protones ligados (formando parte de un núcleo), sí puede ocurrir X(A,Z) X (A, Z-1) + e + + v e 60 Co (Z=27 ) 60 Ni(Z=28 ) + e - + v e 13 N (Z=7) 13 C(Z=6) + e + + v e Los electrones y positrones no existen dentro del núcleo, sino que se crean en el proceso.
14 DESINTEGRACIÓN β La energía de los electrones o positrones emitidos por un nucleido no es un valor único fijo, sino que varia desde 0 hasta un cierto valor máximo. Es un espectro contínuo Explicación (1930, Pauli): Sugiere que una tercera partícula (neutrino) se emite simultáneamente en el proceso de desintegración. Esta partícula tiene una masa en reposo nula y no es observable. Así, la energía disponible se reparte en energía cinética de 3 partículas (y no de 2). La energía cinética que se lleva el núcleo es despreciable, debido a su gran masa. 1948: Evidencia de la existencia de una tercera partícula para confirmar la conservación de la cantidad de movimiento Q = [M(X) M(X ) m e ] c 2 = = T X +T e + T v 1957: Observación experimental del neutrino. Actualmente, sabemos que la masa del neutrino es extremadamente pequeña, pero no nula Existen tres tipos de neutrinos, con sus respectivas antipartículas: neutrino electrónico, muónico y tauónico.
15 Datación radiactiva ( 14 C) 14 C 14 N + e - + v e (T 1/2 = 5730 a) El 14 C se produce continuamente en la atmósfera terrestre a partir de reacciones nucleares originadas por los rayos cósmicos. Los organismos vivos intercambian CO 2 con la atmósfera, por lo que la relación de 14 C a 12 C en ellos es la misma relación que en la atmósfera (1,3 x 10-12). Cuando el organismo muere, la absorción de C se detiene, y la relación 14 C a 12 C va decreciendo debido a la desintegración del 14 C. Concentr. equilibrio (org. vivo): Ceq=15 dpm /gr. C C(Actual) = Ceq (0) e -λt λ = (ln 2)/5730 años T = tiempo desde defunción
16 Desintegración gamma : Un núcleo en un estado excitado se desexcita pasando a un estado de menor energía, mediante emisión de un fotón. Tras la desexcitación, el núcleo sigue siendo el mismo (Z y A no varian) Las energías entre niveles nucleares son del orden del MeV (en los átomos del orden del ev), por lo que los fotones gamma poseen energias desde 0,1 10 MeV La vida media de los emisores gamma es muy corta (del orden de s o inferiores), por lo que no se observan directamente. Habitualmente, se observa una desintegración gamma, porque antes ha habido una desintegración α ó β, produciéndose el núcleo hijo en un estado excitado. Existen algunos nucleidos emisores gamma con vidas medias muy cortas, del orden de minutos o incluso horas: Se les denomina estados metaestables. 239 Pu α 103 α 81 α 51 α 13 α 0.07 Desintegración gamma 103,04 56,83 88,70 30,04 51,62 38,66 46, U 12,96 0,077 E(keV) 103,04 81,74 51,70 46,21 13,04 0,077 0
17 Series radiactivas Desintegración alfa : Z-2, A-4 Desintegración beta: A no cambia, Z+1 o Z-1 Todos los núcleos de una serie se diferencian en 4 unidades en A La serie 4n+1, del Np no existe (desapareció), pues su nucleido de vida mas larga, el 237 Np, tiene un T 1/2 <<< edad de la Tierra (4, años)
18 Reacciones nucleares Para obtener información sobre los núcleos, éstos se bombardean con partículas y se observan los resultados. Los primeros experimentos se realizaron con fuentes de radiación natural. Después, empleando aceleradores de partículas (1931 acelerador Van de Graaf; 1932 Primer ciclotrón) Ejemplo: En 1932, Cockcroft y Walton, empleando protones acelerados artificialmente, consiguen la reacción: P + 7 Li 8 Be 4 He + 4 He Tipos de reacciones nucleares: Dispersión elástica: la partícula sufre una dispersión y el núcleo queda inalterado Dispersión inelástica: El núcleo queda en un estado excitado y, posteriormente, se desexcita emitiendo fotones. Absorción: la partícula es absorbida por el núcleo, y despueés pueden emitirse mas partículas. VALOR Q de la reacción: cantidad de energía liberada o absorbida en la reacción. Q = [ m iniciales m productos ] c 2 Reacción exotérmica: Se libera energía Q > 0. Reacción endotérmica (Q < 0) : para que la reacción se verifique hay que aportar energía En una reacción endotérmica, hace falta una energía mínima E min para que se produzca. En el sistema laboratorio, E min > IQI, (los productos deben poseer una energía cinética mínima para conservar la cantidad de movimiento. SECCION EFICAZ: σ = R / N * I I = nº de partículas incidentes por unidad de tiempo y área R = nº de reacciones nucleares producidas por unidad de tiempo N= nº de núcleos que atraviesa el haz La sección eficaz tiene unidades de área, aunque su significado es probabilidad. 1 barn = m 2
J.M.L.C. IES Aguilar y Cano ALGUNOS DERECHOS RESERVADOS
 La radiactividad o radioactividad es un fenómeno físico natural, por el cual algunas sustancias o elementos químicos llamados radiactivos, emiten radiaciones que tienen la propiedad de impresionar placas
La radiactividad o radioactividad es un fenómeno físico natural, por el cual algunas sustancias o elementos químicos llamados radiactivos, emiten radiaciones que tienen la propiedad de impresionar placas
Esta parte de la Física estudia el comportamiento de los núcleos atómicos. Física nuclear
 Esta parte de la Física estudia el comportamiento de los núcleos atómicos Física nuclear CORTEZA Electrones NÚCLEO Protones Neutrones PARTÍCULA CARGA MASA Electrón (e - ) -1,6.10-19 C 9,1.10-31 kg Protón
Esta parte de la Física estudia el comportamiento de los núcleos atómicos Física nuclear CORTEZA Electrones NÚCLEO Protones Neutrones PARTÍCULA CARGA MASA Electrón (e - ) -1,6.10-19 C 9,1.10-31 kg Protón
FÍSICA NUCLEAR. I WANT TO KNOW GOD S THOUGHTS; THE REST ARE DETAILS (Albert Einstein )
 FÍSICA NUCLEAR I WANT TO KNOW GOD S THOUGHTS; THE REST ARE DETAILS (Albert Einstein. 879 955) . INTRODUCCIÓN. RESEÑA HISTÓRICA Radiactividad propiedad de los núcleos atómicos de ciertos isótopos de modificar
FÍSICA NUCLEAR I WANT TO KNOW GOD S THOUGHTS; THE REST ARE DETAILS (Albert Einstein. 879 955) . INTRODUCCIÓN. RESEÑA HISTÓRICA Radiactividad propiedad de los núcleos atómicos de ciertos isótopos de modificar
Descubrimiento del Núcleo
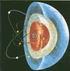 Física Nuclear Descubrimiento del Núcleo Componentes del núcleo: protones y neutrones Propiedades de la fuerza nuclear fuerte Debe ser de atracción y suficientemente grande para vencer la repulsión culombiana
Física Nuclear Descubrimiento del Núcleo Componentes del núcleo: protones y neutrones Propiedades de la fuerza nuclear fuerte Debe ser de atracción y suficientemente grande para vencer la repulsión culombiana
Resolución PRÁCTICO 9
 Resolución PRÁCTICO 9 1- Complete las siguientes ecuaciones nucleares, remplazando las X por los símbolos o números correspondientes (Nota: X toma diferentes números y símbolos en cada una de las situaciones):
Resolución PRÁCTICO 9 1- Complete las siguientes ecuaciones nucleares, remplazando las X por los símbolos o números correspondientes (Nota: X toma diferentes números y símbolos en cada una de las situaciones):
ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA.
 ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA. INDICE Qué es la materia? Modelos de la materia Fuerzas Fundamentales
ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA. INDICE Qué es la materia? Modelos de la materia Fuerzas Fundamentales
N está formado por 7 protones y 8 neutrones, luego su masa teórica debería ser:
 01. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,0001089 u. Datos: 1 u = 1, 10-2 g ; m p = 1,002 u; m n = 1,0085 u El núcleo 15 N está formado por protones y 8
01. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,0001089 u. Datos: 1 u = 1, 10-2 g ; m p = 1,002 u; m n = 1,0085 u El núcleo 15 N está formado por protones y 8
Slide 1 / 33. Slide 2 / 33. Slide 3 / El número atómico es equivalente a cuál de los siguientes? A El número de neutrones del átomo.
 Slide 1 / 33 Slide 2 / 33 3 El número atómico es equivalente a cuál de los siguientes? Slide 3 / 33 A El número de neutrones del átomo. B El número de protones del átomo C El número de nucleones del átomo.
Slide 1 / 33 Slide 2 / 33 3 El número atómico es equivalente a cuál de los siguientes? Slide 3 / 33 A El número de neutrones del átomo. B El número de protones del átomo C El número de nucleones del átomo.
EL NÚCLEO ATÓMICO. (8p, pn) y O 8. (8p, 8n), O 8. Los núcleidos O 8
 EL NÚCLEO ATÓMICO Los núcleos retienen sus identidades en los procesos químico, y las propiedades nucleares, con excepción de la carga, influyen en el comportamiento químico de modos tan sólo indirectos
EL NÚCLEO ATÓMICO Los núcleos retienen sus identidades en los procesos químico, y las propiedades nucleares, con excepción de la carga, influyen en el comportamiento químico de modos tan sólo indirectos
Problemas de Física moderna. Nuclear 2º de bachillerato. Física
 1 Problemas de Física moderna. Nuclear º de bachillerato. Física 1. El isótopo 34 U tiene un periodo de semidesintegración de 50000 años. Si partimos de una muestra de 10 gramos de dicho isótopo, determine:
1 Problemas de Física moderna. Nuclear º de bachillerato. Física 1. El isótopo 34 U tiene un periodo de semidesintegración de 50000 años. Si partimos de una muestra de 10 gramos de dicho isótopo, determine:
N está formado por 7 protones y 8 neutrones, luego su masa teórica debería ser:
 1. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,189 u. Datos: 1 u = 1,6 1-2 g ; m p = 1,26 u; m n = 1,8665 u El núcleo 15 N está formado por protones y 8 neutrones,
1. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,189 u. Datos: 1 u = 1,6 1-2 g ; m p = 1,26 u; m n = 1,8665 u El núcleo 15 N está formado por protones y 8 neutrones,
Química General III. Tema 13. Química Nuclear. Sulfato doble de K y U, emite radiación fuente de rayos radiactivos.
 Química General III. Tema 3. Química Nuclear Introducción. Reacción Química Wilhelm Röntgen Henri Becquerel solo 896 895 participan electrones. Rayos X Sulfato doble de K y U, emite radiación fuente de
Química General III. Tema 3. Química Nuclear Introducción. Reacción Química Wilhelm Röntgen Henri Becquerel solo 896 895 participan electrones. Rayos X Sulfato doble de K y U, emite radiación fuente de
Actividad y Leyes del Decaimiento Radiactivo
 ctividad y Leyes del Decaimiento Radiactivo Características del Fenómeno de la Transformación Radiactiva Se denomina radiactividad al proceso de transformación espontánea nea de núcleos atómicos mediante
ctividad y Leyes del Decaimiento Radiactivo Características del Fenómeno de la Transformación Radiactiva Se denomina radiactividad al proceso de transformación espontánea nea de núcleos atómicos mediante
Núcleo Atómico. El núcleo es una masa muy compacta formada por protones y neutrones.
 Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA
 Física P.A.U. FÍSICA MODERNA FÍSICA MODERNA PROBLEMAS MECÁNICA CUÁNTICA.. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 5 nm, el potencial de frenado para los electrones
Física P.A.U. FÍSICA MODERNA FÍSICA MODERNA PROBLEMAS MECÁNICA CUÁNTICA.. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 5 nm, el potencial de frenado para los electrones
La estructura atómica: el núcleo
 Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
BACHILLERATO FÍSICA 14. FÍSICA NUCLEAR. Dpto. de Física y Química. R. Artacho
 BACHILLERATO FÍSICA 14. FÍSICA NUCLEAR R. Artacho Dpto. de Física y Química ÍNDICE 1. El camino hacia el núcleo atómico 2. El descubrimiento del núcleo 3. Tamaño y densidad de los núcleos 4. Estabilidad
BACHILLERATO FÍSICA 14. FÍSICA NUCLEAR R. Artacho Dpto. de Física y Química ÍNDICE 1. El camino hacia el núcleo atómico 2. El descubrimiento del núcleo 3. Tamaño y densidad de los núcleos 4. Estabilidad
RADIOACTIVIDAD - (2015)
 RADIOACTIVIDAD - (2015) A- CONCEPTOS GENERALES SOBRE RADIACTIVIDAD B- ISÓTOPOS C- TIPOS Y PROPIEDADES DE LAS RADIACCIONES D- REACCIONES NUCLEARES E- VIDA MEDIA A- CONCEPTOS GENERALES SOBRE RADIACTIVIDAD
RADIOACTIVIDAD - (2015) A- CONCEPTOS GENERALES SOBRE RADIACTIVIDAD B- ISÓTOPOS C- TIPOS Y PROPIEDADES DE LAS RADIACCIONES D- REACCIONES NUCLEARES E- VIDA MEDIA A- CONCEPTOS GENERALES SOBRE RADIACTIVIDAD
TEMA 6.- EL NÚCLEO 1.- LA NATURALEZA DE LAS REACCIONES NUCLEARES 2.- ESTABILIDAD NUCLEAR. Energía de enlace nuclear 3.- RADIACTIVIDAD NATURAL
 TEMA 6.- EL NÚCLEO.- LA NATURALEZA DE LAS REACCIONES NUCLEARES 2.- ESTABILIDAD NUCLEAR Energía de enlace nuclear 3.- RADIACTIVIDAD NATURAL 4.- RADIACTIVIDAD ARTIFICIAL 5.- FISIÓN NUCLEAR 6.- FUSIÓN NUCLEAR
TEMA 6.- EL NÚCLEO.- LA NATURALEZA DE LAS REACCIONES NUCLEARES 2.- ESTABILIDAD NUCLEAR Energía de enlace nuclear 3.- RADIACTIVIDAD NATURAL 4.- RADIACTIVIDAD ARTIFICIAL 5.- FISIÓN NUCLEAR 6.- FUSIÓN NUCLEAR
Átomo. Posee protones y neutrones. Estos se llaman Nucleones. Alrededor giran los electrones en. forma de nube. Son eléctricamente neutro
 Átomo Posee protones y neutrones Estos se llaman Nucleones Alrededor giran los electrones en forma de nube Son eléctricamente neutro Por eso Z(número de Protones)=Ne(Número de Electrones) Átomo Su dimensión
Átomo Posee protones y neutrones Estos se llaman Nucleones Alrededor giran los electrones en forma de nube Son eléctricamente neutro Por eso Z(número de Protones)=Ne(Número de Electrones) Átomo Su dimensión
RADIACTIVIDAD. Alejandra Pardo Martínez 1º ESO
 RADIACTIVIDAD Alejandra Pardo Martínez 1º ESO 1. ESTRUCTURA ATÓMICA El átomo es la parte más pequeña de materia que conserva sus propiedades químicas. De forma simplificada, puede considerarse que está
RADIACTIVIDAD Alejandra Pardo Martínez 1º ESO 1. ESTRUCTURA ATÓMICA El átomo es la parte más pequeña de materia que conserva sus propiedades químicas. De forma simplificada, puede considerarse que está
Z, ( a veces se suprime Z),donde X es el símbolo químico del elemento. Así por ejemplo tenemos los isótopos del carbono:
 RADIACTIVIDAD El núcleo atómico está constituido por nucleones: Z protones y N neutrones, ( en total A ). Como sabemos los nucleones son partículas elementales y están constituidos por la agrupación de
RADIACTIVIDAD El núcleo atómico está constituido por nucleones: Z protones y N neutrones, ( en total A ). Como sabemos los nucleones son partículas elementales y están constituidos por la agrupación de
Radiactividad Medicina Nuclear (1993) Radioterapia y Radiodiagnóstico (2008) Facultad de Ingeniería, UNER
 Radiactividad Medicina Nuclear (1993) Radioterapia y Radiodiagnóstico (008) Facultad de Ingeniería, UNER 1. Ley de decaimiento En la naturaleza hay isótopos inestables y metaestables que pueden emitir
Radiactividad Medicina Nuclear (1993) Radioterapia y Radiodiagnóstico (008) Facultad de Ingeniería, UNER 1. Ley de decaimiento En la naturaleza hay isótopos inestables y metaestables que pueden emitir
Tema 1: Núcleo atómico y Desintegración
 Tema 1: Núcleo atómico y Desintegración Núcleo atómico. Radiactividad. Modos de Decaimiento N ú c l e o t ó m i c o El núcleo atómico es la parte del átomo que contiene toda la carga positiva y la mayoría
Tema 1: Núcleo atómico y Desintegración Núcleo atómico. Radiactividad. Modos de Decaimiento N ú c l e o t ó m i c o El núcleo atómico es la parte del átomo que contiene toda la carga positiva y la mayoría
Ejercicios de Física cuántica y nuclear. PAU (PAEG)
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Con respecto a la radiación gamma, cuál(es) de las siguientes afirmaciones es(son) correcta(s)?
 Nº GUÍA PRÁCTICA Fenómenos nucleares I: partículas radiactivas Ejercicios PSU 1. Con respecto a la radiación gamma, cuál(es) de las siguientes afirmaciones es(son) correcta(s)? I) Puede penetrar a través
Nº GUÍA PRÁCTICA Fenómenos nucleares I: partículas radiactivas Ejercicios PSU 1. Con respecto a la radiación gamma, cuál(es) de las siguientes afirmaciones es(son) correcta(s)? I) Puede penetrar a través
Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA
 Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA PROBLEMAS EFECTO FOTOELÉCTRICO 1. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 175 nm, el potencial de frenado para
Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA PROBLEMAS EFECTO FOTOELÉCTRICO 1. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 175 nm, el potencial de frenado para
Radiactividad y Física Nuclear (I): Radiactividad Natural diferentes tipos de radiación
 Radiactividad y Física Nuclear (I): Radiactividad Natural diferentes tipos de radiación 1896 : Becquerel descubre la Pechblenda( mineral de uranio), capaz de impresionar placas fotográficas en ausencia
Radiactividad y Física Nuclear (I): Radiactividad Natural diferentes tipos de radiación 1896 : Becquerel descubre la Pechblenda( mineral de uranio), capaz de impresionar placas fotográficas en ausencia
Teoría atómica de Dalton (1803)
 EL ÁTOMO DIVISIBLE El átomo Desde los tiempos de la antigua Grecia,los pensadores se preguntaban cómo estaba constituida la materia en su interior? Demócrito (S.V a.c.) introduce el término de átomo como
EL ÁTOMO DIVISIBLE El átomo Desde los tiempos de la antigua Grecia,los pensadores se preguntaban cómo estaba constituida la materia en su interior? Demócrito (S.V a.c.) introduce el término de átomo como
13 Física nuclear. Actividades del interior de la unidad
 13 Física nuclear ctividades del interior de la unidad 1. Indica brevemente la diferencia entre radiactividad natural y radiactividad artificial. La radiactividad natural proviene de sustancias que se
13 Física nuclear ctividades del interior de la unidad 1. Indica brevemente la diferencia entre radiactividad natural y radiactividad artificial. La radiactividad natural proviene de sustancias que se
CUESTIONES. 5. (2006) a) Cómo se puede explicar que un núcleo emita partículas β si en él sólo existen neutrones y protones? b) El
 CUESTIONES 1. (2004) a) Describa las características de los procesos de emisión radiactiva alfa, beta y gamma. b) Uno de ellos consiste en la emisión de electrones. Cómo es posible que un núcleo emita
CUESTIONES 1. (2004) a) Describa las características de los procesos de emisión radiactiva alfa, beta y gamma. b) Uno de ellos consiste en la emisión de electrones. Cómo es posible que un núcleo emita
Conceptos básicos sobre interacción de la radiación ionizante con la materia
 Conceptos básicos sobre interacción de la radiación ionizante con la materia Martín Gascón Introducción al laboratorio de Física Nuclear Técnicas experimentales avanzadas Departamento de Física de Partículas
Conceptos básicos sobre interacción de la radiación ionizante con la materia Martín Gascón Introducción al laboratorio de Física Nuclear Técnicas experimentales avanzadas Departamento de Física de Partículas
ÁTOMO ~ m NÚCLEO ~ mnucleón < m. MATERIA ~ 10-9 m. Átomo FÍSICA MATERIALES PARTÍCULAS
 ESTRUCTURA DE LA MATERIA Grupo D CURSO 20011 2012 EL NÚCLEO ATÓMICO DE QUÉ ESTÁN HECHAS LAS COSAS? MATERIA ~ 10-9 m Átomo FÍSICA MATERIALES ÁTOMO ~ 10-10 m NÚCLEO ~ 10-14 mnucleón < 10-15 m Electrón Protón
ESTRUCTURA DE LA MATERIA Grupo D CURSO 20011 2012 EL NÚCLEO ATÓMICO DE QUÉ ESTÁN HECHAS LAS COSAS? MATERIA ~ 10-9 m Átomo FÍSICA MATERIALES ÁTOMO ~ 10-10 m NÚCLEO ~ 10-14 mnucleón < 10-15 m Electrón Protón
5 DESINTEGRACIÓN NUCLEAR Y PRODUCCIÓN
 Isótopos Ambientales en el Ciclo Hidrológico IGME. Temas: Guías y manuales. ISBN: 84-7840-465-1 5 DESINTEGRACIÓN NUCLEAR Y PRODUCCIÓN Esta sección contiene una revisión breve de los aspectos relevantes
Isótopos Ambientales en el Ciclo Hidrológico IGME. Temas: Guías y manuales. ISBN: 84-7840-465-1 5 DESINTEGRACIÓN NUCLEAR Y PRODUCCIÓN Esta sección contiene una revisión breve de los aspectos relevantes
FÍSICA NUCLEAR. El núcleo atómico
 1. El núcleo atómico. 2. Energía de enlace nuclear. 3. La radiactividad nuclear. 4. Leyes de la desintegración radiactiva. 5. Reacciones nucleares: su aspecto energético. 6. Fisión nuclear: reactores nucleares.
1. El núcleo atómico. 2. Energía de enlace nuclear. 3. La radiactividad nuclear. 4. Leyes de la desintegración radiactiva. 5. Reacciones nucleares: su aspecto energético. 6. Fisión nuclear: reactores nucleares.
Unidad N 11 QUIMICA NUCLEAR
 Unidad N 11 QUIMICA NUCLEAR Estructura básica del átomo Electrones: CAMBIOS: generan las propiedades Químicas y Físicas más o menos comunes de un dado átomo. Núcleo: CAMBIOS: modifican en forma sustancial
Unidad N 11 QUIMICA NUCLEAR Estructura básica del átomo Electrones: CAMBIOS: generan las propiedades Químicas y Físicas más o menos comunes de un dado átomo. Núcleo: CAMBIOS: modifican en forma sustancial
Física Nuclear y Reacciones Nucleares Problemas de Práctica Multiopción 1 El núcleo atómico se compone de: A electrones
 Slide 1 / 58 Física Nuclear y Reacciones Nucleares Problemas de Práctica Slide 2 / 58 Multiopción 1 l núcleo atómico se compone de: Slide 3 / 58 electrones protones protones y electrones protones y neutrones
Slide 1 / 58 Física Nuclear y Reacciones Nucleares Problemas de Práctica Slide 2 / 58 Multiopción 1 l núcleo atómico se compone de: Slide 3 / 58 electrones protones protones y electrones protones y neutrones
Interacción de neutrones con la materia. Laura C. Damonte 2014
 Interacción de neutrones con la materia Laura C. Damonte 2014 Interacción de neutrones con la materia La interacción de los neutrones con la materia tiene interés tanto experimental y teórico como también
Interacción de neutrones con la materia Laura C. Damonte 2014 Interacción de neutrones con la materia La interacción de los neutrones con la materia tiene interés tanto experimental y teórico como también
TEMA 22. REACCIONES NUCLEARES.
 Tema. Segundo Cuatrimestre. TEMA. REACCIONES NUCLEARES. 1. Introducción. El concepto de reacción nuclear comprende todos los casos en los que los núcleos interaccionan mediante colisiones o desintegraciones.
Tema. Segundo Cuatrimestre. TEMA. REACCIONES NUCLEARES. 1. Introducción. El concepto de reacción nuclear comprende todos los casos en los que los núcleos interaccionan mediante colisiones o desintegraciones.
TEMA 5 Estructura del átomo. IES Sierra de San Quílez Departamento de Física y Química
 TEMA 5 Estructura del átomo IES Sierra de San Quílez Departamento de Física y Química El átomo Naturaleza eléctrica de la materia Fenómenos eléctricos Algunos fenómenos de electrización pusieron de manifiesto
TEMA 5 Estructura del átomo IES Sierra de San Quílez Departamento de Física y Química El átomo Naturaleza eléctrica de la materia Fenómenos eléctricos Algunos fenómenos de electrización pusieron de manifiesto
Elementos radiactivos
 1 Elementos radiactivos I. El núcleo atómico 1. Componentes del núcleo, nucleones, protón y neutrón. Carga masa Símbolo (u.m.a.) Protón 1+ 1,007825 1 1 P ( 1 1 H + ) Neutrón 0 1,008665 0 1 n Masa del electrón
1 Elementos radiactivos I. El núcleo atómico 1. Componentes del núcleo, nucleones, protón y neutrón. Carga masa Símbolo (u.m.a.) Protón 1+ 1,007825 1 1 P ( 1 1 H + ) Neutrón 0 1,008665 0 1 n Masa del electrón
Tema 3: Reacciones Nucleares
 Tema 3: Reacciones Nucleares I n t r o d u c c i ó n El descubrimiento de la radiactividad representó un avance muy importante para la ciencia, ya que cambió radicalmente la visión existente sobre la estructura
Tema 3: Reacciones Nucleares I n t r o d u c c i ó n El descubrimiento de la radiactividad representó un avance muy importante para la ciencia, ya que cambió radicalmente la visión existente sobre la estructura
Física nuclear. Núcleo atómico
 Física nuclear La configuración de los electrones de un átomo determina si este puede unirse a otros para formar compuestos y la manera para hacerlo. Además, los electrones causan efectos tales como la
Física nuclear La configuración de los electrones de un átomo determina si este puede unirse a otros para formar compuestos y la manera para hacerlo. Además, los electrones causan efectos tales como la
UNIDAD 3 ESTRUCTURA DE LA MATERIA
 UNIDAD 3 ESTRUCTURA DE LA MATERIA 1. ESTRUCTURA ATÓMICA DE LA MATERIA 1.1. Introducción 1.. Modelos atómicos 1.3. Estados de energía atómicos 1.4. Números cuánticos 1.5. Principio de exclusión de Pauli
UNIDAD 3 ESTRUCTURA DE LA MATERIA 1. ESTRUCTURA ATÓMICA DE LA MATERIA 1.1. Introducción 1.. Modelos atómicos 1.3. Estados de energía atómicos 1.4. Números cuánticos 1.5. Principio de exclusión de Pauli
Qué es la energía nuclear? Tema1
 Toda la materia del universo está formada por moléculas que a su vez están constituidas por átomos, pequeñísimas unidades que durante mucho tiempo se consideraron invisibles. En la actualidad sabemos que
Toda la materia del universo está formada por moléculas que a su vez están constituidas por átomos, pequeñísimas unidades que durante mucho tiempo se consideraron invisibles. En la actualidad sabemos que
Conceptos Básicos de la Energía Nuclear
 Conceptos Básicos de la Energía Nuclear El átomo En la naturaleza el átomo más simple que hay es el hidrógeno, cuenta con un protón y un electrón. Por tanto, para explicar el resto de los átomos, ha de
Conceptos Básicos de la Energía Nuclear El átomo En la naturaleza el átomo más simple que hay es el hidrógeno, cuenta con un protón y un electrón. Por tanto, para explicar el resto de los átomos, ha de
---- Debe indicarse claramente nombres y números de lista de los alumnos integrantes del grupo.
 LICEO Confederación Suiza SECTOR: Química GUÍA DE APRENDIZAJE NIVEL: 4 Medio PROFESOR(A): Genny Astudillo Castillo UNIDAD TEMÁTICA: Química Nuclear CONTENIDO: Fisión y fusión nuclear OBJETIVO DE APRENDIZAJE:
LICEO Confederación Suiza SECTOR: Química GUÍA DE APRENDIZAJE NIVEL: 4 Medio PROFESOR(A): Genny Astudillo Castillo UNIDAD TEMÁTICA: Química Nuclear CONTENIDO: Fisión y fusión nuclear OBJETIVO DE APRENDIZAJE:
Física y Tecnología Energética Energía Nuclear de Fisión. Reactores.
 Física y Tecnología Energética 12 - Energía Nuclear de Fisión. Reactores. Núcleos e Isótopos Estabilidad nuclear Masas nucleares y energía Fusión de nucleos pequeños Fisión de nucleos grandes Disminución
Física y Tecnología Energética 12 - Energía Nuclear de Fisión. Reactores. Núcleos e Isótopos Estabilidad nuclear Masas nucleares y energía Fusión de nucleos pequeños Fisión de nucleos grandes Disminución
2º Bachillerato. Química. Unidad 1 (Estructura atómica de la materia). Fotocopia 1.
 Partículas subatómicas Los átomos están formados por un núcleo (formado por protones y neutrones) rodeado por una nube de electrones, que se encuentran en la corteza. Entre núcleo y corteza hay espacio
Partículas subatómicas Los átomos están formados por un núcleo (formado por protones y neutrones) rodeado por una nube de electrones, que se encuentran en la corteza. Entre núcleo y corteza hay espacio
Masterclass Aceleradores de partículas
 Unidad de Divulgación Científica del Centro Nacional de Aceleradores (CNA) Masterclass Aceleradores de partículas 1. Técnicas experimentales empleadas en el CNA 2. Ley de decaimiento radiactivo y su aplicación
Unidad de Divulgación Científica del Centro Nacional de Aceleradores (CNA) Masterclass Aceleradores de partículas 1. Técnicas experimentales empleadas en el CNA 2. Ley de decaimiento radiactivo y su aplicación
5. ESTRUCTURA ATÓMICA
 5. ESTRUCTURA ATÓMICA 1. Qué sucede en ocasiones al ponernos o quitarnos una prenda de vestir fabricada con fibras sintéticas? La prenda se ha electrizado por frotamiento con nuestro cuerpo.. Dos cargas
5. ESTRUCTURA ATÓMICA 1. Qué sucede en ocasiones al ponernos o quitarnos una prenda de vestir fabricada con fibras sintéticas? La prenda se ha electrizado por frotamiento con nuestro cuerpo.. Dos cargas
Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO]
![Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO] Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO]](/thumbs/49/25535199.jpg) Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [2 PUNTOS /UNO] 1. Al iluminar una célula fotoeléctrica con radiación electromagnética de longitud de onda 185
Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [2 PUNTOS /UNO] 1. Al iluminar una célula fotoeléctrica con radiación electromagnética de longitud de onda 185
Interacción nuclear PONENCIA DE FÍSICA DE ANDALUCÍA. CURSO
 Interacción nuclear Cuestiones (96-E) Comente cada una de las frases siguientes: a) Isótopos son aquellos núclidos de igual número atómico pero distinto número másico. b) Si un núclido emite una partícula
Interacción nuclear Cuestiones (96-E) Comente cada una de las frases siguientes: a) Isótopos son aquellos núclidos de igual número atómico pero distinto número másico. b) Si un núclido emite una partícula
producción de energía en las estrellas interiores estelares
 producción de energía en las estrellas interiores estelares porqué brillan las estrellas? la energía emitida por las estrellas tiene su origen en reacciones termonucleares que tienen lugar en su interior
producción de energía en las estrellas interiores estelares porqué brillan las estrellas? la energía emitida por las estrellas tiene su origen en reacciones termonucleares que tienen lugar en su interior
Radiación. Tipos de radiación
 Radiación Las radiaciones son ondas electromagnéticas o partículas que se propagan con una velocidad dada. Contienen energía, carga eléctrica y magnética. Pueden ser generadas por fuentes naturales o instrumentos
Radiación Las radiaciones son ondas electromagnéticas o partículas que se propagan con una velocidad dada. Contienen energía, carga eléctrica y magnética. Pueden ser generadas por fuentes naturales o instrumentos
Curso de Radiactividad y Medioambiente clase 4
 Curso de Radiactividad y Medioambiente clase 4 Departamento de Física, Facultad de Ciencias Exactas - UNLP Instituto de Física La Plata CONICET Calle 49 y 115 La Plata Interacción de la radiación con la
Curso de Radiactividad y Medioambiente clase 4 Departamento de Física, Facultad de Ciencias Exactas - UNLP Instituto de Física La Plata CONICET Calle 49 y 115 La Plata Interacción de la radiación con la
Tema 4: Leyes de la desintegración
 Tema 4: Leyes de la desintegración 1. Ley exponencial 1.1. Constante de desintegración y ley exponencial El proceso de la desintegración es de naturaleza estadística: Imposible predecir el momento de la
Tema 4: Leyes de la desintegración 1. Ley exponencial 1.1. Constante de desintegración y ley exponencial El proceso de la desintegración es de naturaleza estadística: Imposible predecir el momento de la
Ejercicios de Física cuántica y nuclear. PAEG
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
TÉCNICAS EXPERIMENTALES V FÍSICA CUÁNTICA
 TÉCNICAS EXPERIMENTALES V FÍSICA CUÁNTICA P1 Medida de la Constante de Planck. Efecto fotoeléctrico. RNB P2 Experimento de Franck-Hertz. Niveles de energía de los átomos RNB P3 Dispersión de Rutherford
TÉCNICAS EXPERIMENTALES V FÍSICA CUÁNTICA P1 Medida de la Constante de Planck. Efecto fotoeléctrico. RNB P2 Experimento de Franck-Hertz. Niveles de energía de los átomos RNB P3 Dispersión de Rutherford
QUÍMICA COMÚN Y ELECTIVO
 QUÍMICA COMÚN Y ELECTIVO GENERALIDADES 1. MODELOS ATÓMICOS 2. EL AGUA, EL AIRE Y EL PETRÓLEO COMÚN 3. QUÍMICA ORGÁNICA 4. DISOLUCIONES QUÍMICAS 1. EQUILIBRIO QUÍMICO 2. CINÉTICA 3. ACTIVIDAD NUCLEAR ELECTIVO
QUÍMICA COMÚN Y ELECTIVO GENERALIDADES 1. MODELOS ATÓMICOS 2. EL AGUA, EL AIRE Y EL PETRÓLEO COMÚN 3. QUÍMICA ORGÁNICA 4. DISOLUCIONES QUÍMICAS 1. EQUILIBRIO QUÍMICO 2. CINÉTICA 3. ACTIVIDAD NUCLEAR ELECTIVO
FÍSICA. 2º BACHILLERATO BLOQUE V: INTRODUCCIÓN A LA FÍSICA MODERNA Examen 1
 Examen 1 1. En la explosión de una bomba atómica se produce Sr-90, que es un peligroso contaminante radiactivo, cuyo periodo de semidesintegración es de 28,8 años. Cuánto tiempo debe transcurrir para que
Examen 1 1. En la explosión de una bomba atómica se produce Sr-90, que es un peligroso contaminante radiactivo, cuyo periodo de semidesintegración es de 28,8 años. Cuánto tiempo debe transcurrir para que
El sabor de los neutrinos
 El sabor de los neutrinos Ulises Solís Hernández Nuestro planeta sufre continuamente impactos de distintos objetos que en su camino a través del espacio exterior se topan con la Tierra. Algunos de estos
El sabor de los neutrinos Ulises Solís Hernández Nuestro planeta sufre continuamente impactos de distintos objetos que en su camino a través del espacio exterior se topan con la Tierra. Algunos de estos
QUIMICA Unidad N 3 : - ESTRUCTURA ATÓMICA
 QUIMICA Unidad N 3 : - ESTRUCTURA ATÓMICA Niels BOHR John DALTON 1 Profesora Mercedes Caratini - QUIMICA- ET 28 REPÚBLICA FRANCESA MODELO ATÓMICO ACTUAL El modelo atómico actual se construye a partir de
QUIMICA Unidad N 3 : - ESTRUCTURA ATÓMICA Niels BOHR John DALTON 1 Profesora Mercedes Caratini - QUIMICA- ET 28 REPÚBLICA FRANCESA MODELO ATÓMICO ACTUAL El modelo atómico actual se construye a partir de
Estructura de la Materia
 Estructura de la Materia Antes de 1800, se pensaba que la materia era continua, es decir que podía ser dividida en infinitas partes más pequeñas sin cambiar la naturaleza del elemento. Sin embargo, alrededor
Estructura de la Materia Antes de 1800, se pensaba que la materia era continua, es decir que podía ser dividida en infinitas partes más pequeñas sin cambiar la naturaleza del elemento. Sin embargo, alrededor
Procesos nucleares en estrellas
 Procesos nucleares en estrellas # Interior estelar compuesto por núcleos de los distintos elementos # Temperaturas interior estelar Parte de los núcleos con energía térmicas (E cin ) que sobrepasan las
Procesos nucleares en estrellas # Interior estelar compuesto por núcleos de los distintos elementos # Temperaturas interior estelar Parte de los núcleos con energía térmicas (E cin ) que sobrepasan las
Interacción de la radiación con la materia
 Interacción de la radiación con la materia Fernando Mata Colodro Servicio de Radiofísica y Protección Radiológica. Hospital General Universitario Santa Lucía. Cartagena. RADIACION PARTICULAS FOTONES Colisiones
Interacción de la radiación con la materia Fernando Mata Colodro Servicio de Radiofísica y Protección Radiológica. Hospital General Universitario Santa Lucía. Cartagena. RADIACION PARTICULAS FOTONES Colisiones
Capítulo 1: El núcleo y sus radiaciones
 Capítulo 1: El núcleo y sus radiaciones En 1896, Henri Becquerel accidentalmente descubrió que placas fotográficas no expuestas a la luz y guardadas junto a cristales de una sal de uranio habían sido veladas.
Capítulo 1: El núcleo y sus radiaciones En 1896, Henri Becquerel accidentalmente descubrió que placas fotográficas no expuestas a la luz y guardadas junto a cristales de una sal de uranio habían sido veladas.
QUIMICA GENERAL. Docente : Raquel Villafrades Torres
 Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye
 Características esenciales de las reacciones químicas A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye Joseph Louis Proust (formación de CuCO 3 ): los elementos que
Características esenciales de las reacciones químicas A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye Joseph Louis Proust (formación de CuCO 3 ): los elementos que
PROBLEMAS DE FÍSICA MODERNA
 PROBLEMAS DE FÍSICA MODERNA 1.- Para un metal la frecuencia umbral es de 4,5.10 14 Hz. Cuál es la energía mínima para arrancarle un electrón?. Si el metal se ilumina con una luz de 5.10-7 m de longitud
PROBLEMAS DE FÍSICA MODERNA 1.- Para un metal la frecuencia umbral es de 4,5.10 14 Hz. Cuál es la energía mínima para arrancarle un electrón?. Si el metal se ilumina con una luz de 5.10-7 m de longitud
a Po b Po a b Po E a t t 0 tiene un punto de inflexión en t inf = 1 a Log( a b P 0
 Tarea 3 1. Las funciones Log y Exp 1. Calcule con mathematica las siguientes expresiones: a) ln 3 27 b) log 10 58 c) log 3 3 ln 52 ln 3 7 + 9 E 2 ln 4 b) Grafique las funciónes t y t 50. Cuál diverge a
Tarea 3 1. Las funciones Log y Exp 1. Calcule con mathematica las siguientes expresiones: a) ln 3 27 b) log 10 58 c) log 3 3 ln 52 ln 3 7 + 9 E 2 ln 4 b) Grafique las funciónes t y t 50. Cuál diverge a
Origen del Concepto Átomo MODELOS ATÓMICOS. Teoría o Modelo Atómico de Dalton (1808) Qué es un modelo en Ciencias?
 MODELOS ATÓMICOS Origen del Concepto Átomo Demócrito: Siglo IV (A.C.) Fundador de la Escuela Atomista los átomos son indivisibles (átomo), y se distinguen por forma, tamaño, orden y posición. Los átomos
MODELOS ATÓMICOS Origen del Concepto Átomo Demócrito: Siglo IV (A.C.) Fundador de la Escuela Atomista los átomos son indivisibles (átomo), y se distinguen por forma, tamaño, orden y posición. Los átomos
Modelo de Thomson Modelo de Rutherford. Estructura atómica. José Mariano Lucena Cruz 10 de mayo de 2010
 José Mariano Lucena Cruz chenalc@gmail.com 10 de mayo de 2010 Propiedades periódicas Aquellas cuyo valor se puede estimar según la posición que ocupen los elementos en la tabla periódica. Estas son: Tamaño
José Mariano Lucena Cruz chenalc@gmail.com 10 de mayo de 2010 Propiedades periódicas Aquellas cuyo valor se puede estimar según la posición que ocupen los elementos en la tabla periódica. Estas son: Tamaño
MODELOS ATÓMICOS. Nombre y Apellidos:... Grupo:... Correctas Incorrectas Nota
 MODELOS ATÓMICOS Nombre y Apellidos:........................................ Grupo:........... 1.- Cuestionario (7 ptos) Correctas Incorrectas Nota 1.- El siguiente dibujo corresponde al modelo de: a)
MODELOS ATÓMICOS Nombre y Apellidos:........................................ Grupo:........... 1.- Cuestionario (7 ptos) Correctas Incorrectas Nota 1.- El siguiente dibujo corresponde al modelo de: a)
EL ÁTOMO. Departamento de Física y Química 3º ESO
 EL ÁTOMO Departamento de Física y Química 3º ESO 0. Mapa conceptual Metales No metales Tabla periódica Elementos Cationes Isótopos ÁTOMO Iones Aniones Protones Núcleo Neutrones Electrones Número atómico
EL ÁTOMO Departamento de Física y Química 3º ESO 0. Mapa conceptual Metales No metales Tabla periódica Elementos Cationes Isótopos ÁTOMO Iones Aniones Protones Núcleo Neutrones Electrones Número atómico
MODELOS ATÓMICOS 2ª PARTE
 MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
Ley de Coulomb: F = Porqué el núcleo atómico no es inestable? Existen fuerzas nucleares que mantienen estable al núcleo. 1 q.
 El Núcleo N Atómico Electrones con carga negativa rodean al núcleo atómico. Porqué generalmente el átomo no tiene carga? El núcleo atómico tiene cargas positivas (protones). 1 q Ley de Coulomb: F = 1 q
El Núcleo N Atómico Electrones con carga negativa rodean al núcleo atómico. Porqué generalmente el átomo no tiene carga? El núcleo atómico tiene cargas positivas (protones). 1 q Ley de Coulomb: F = 1 q
Elemento Neutrones Protones Electrones
 PROBLEMAS DE ÁTOMOS 1. Argumenta cómo se explica la ley de conservación de la masa en las reacciones químicas mediante su teoría atómica de Dalton. Calcula cuánto carbono se necesita para reaccionar exactamente
PROBLEMAS DE ÁTOMOS 1. Argumenta cómo se explica la ley de conservación de la masa en las reacciones químicas mediante su teoría atómica de Dalton. Calcula cuánto carbono se necesita para reaccionar exactamente
BLOQUE 5.2 FÍSICA NUCLEAR
 BLOQUE 5. FÍSIC NUCLER -EL NÚCLEO TÓMICO El núcleo de los átomos se acepta universalmente que está formado por PROTONES y NEUTRONES (llamados genéricamente NUCLEONES), en una cantidad que varía de unos
BLOQUE 5. FÍSIC NUCLER -EL NÚCLEO TÓMICO El núcleo de los átomos se acepta universalmente que está formado por PROTONES y NEUTRONES (llamados genéricamente NUCLEONES), en una cantidad que varía de unos
Energía de ligadura del núcleo.
 Energía de ligadura del núcleo. Página 1 El agregado de protones y neutrones dentro del núcleo se mantiene unido por fuertes fuerzas de atracción entre los nucleones. También existen fuerzas de repulsión
Energía de ligadura del núcleo. Página 1 El agregado de protones y neutrones dentro del núcleo se mantiene unido por fuertes fuerzas de atracción entre los nucleones. También existen fuerzas de repulsión
Introducción al Análisis de Reactores Nucleares
 Objetivo Introducción al Análisis de Reactores Nucleares Esta clase tiene como objetivo que los alumnos comprendan los fenómenos básicos relacionados con el análisis y diseño de reactores nucleares, en
Objetivo Introducción al Análisis de Reactores Nucleares Esta clase tiene como objetivo que los alumnos comprendan los fenómenos básicos relacionados con el análisis y diseño de reactores nucleares, en
Un modelo atómico, por lo tanto consiste en representar de manera grafica, la dimensión atómica de la materia. El objetivo de estos modelos es que el
 Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
1. Aspectos Administrativos (10 Minutos) 2. Teoría de la Radiación (20 Minutos) 5. Sesión de Preguntas (10 Minutos)
 Radioactividad 1. Aspectos Administrativos (10 Minutos) 2. Teoría de la Radiación (20 Minutos) 3. Características de la Radiación (15 Minutos) 5. Sesión de Preguntas (10 Minutos) Aspectos Administrativos
Radioactividad 1. Aspectos Administrativos (10 Minutos) 2. Teoría de la Radiación (20 Minutos) 3. Características de la Radiación (15 Minutos) 5. Sesión de Preguntas (10 Minutos) Aspectos Administrativos
Técnico Profesional QUÍMICA
 Convenio Programa Técnico Profesional QUÍMICA Modelos atómicos, estructura atómica y tipos de átomos Nº Ejercicios PSU 1. Rutherford, luego de realizar pruebas con una lámina de oro bombardeada por partículas
Convenio Programa Técnico Profesional QUÍMICA Modelos atómicos, estructura atómica y tipos de átomos Nº Ejercicios PSU 1. Rutherford, luego de realizar pruebas con una lámina de oro bombardeada por partículas
Radiación. Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler. L. Infante 1
 Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Radiaciones Ionizantes: Utilización y Riesgos RIUR. Guía de estudio
 Radiaciones Ionizantes: Utilización y Riesgos RIUR . Estructura y radiaciones atómicas Esta guía describe el conjunto de actividades que forman el tema 2 del módulo 1: " Estructura y radiaciones atómicas"
Radiaciones Ionizantes: Utilización y Riesgos RIUR . Estructura y radiaciones atómicas Esta guía describe el conjunto de actividades que forman el tema 2 del módulo 1: " Estructura y radiaciones atómicas"
ESTRUCTURA ATÓMICA. Nomenclatura Magnesio Sodio Neón Símbolo nuclear
 ESTRUCTURA ATÓMICA 1) Confeccione una lista con el número total de electrones, neutrones y protones que hay en cada una de las siguientes especies químicas: 12 40 a) C b) Ca 6 20 2) Escriba la configuración
ESTRUCTURA ATÓMICA 1) Confeccione una lista con el número total de electrones, neutrones y protones que hay en cada una de las siguientes especies químicas: 12 40 a) C b) Ca 6 20 2) Escriba la configuración
UNIDAD 2. Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos.
 UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
Cuando el equilibrio entre las dos fuerzas de atracción y repulsión se rompe, hay emisión de radioactividad.
 PARTÍCULAS ALFA La vida media de los elementos pesados que emiten partículas alfa, varía sobre 0 órdenes de magnitud, desde 0.1 microsegundos hasta 10 billones de años. Este amplísimo rango, depende fuertemente
PARTÍCULAS ALFA La vida media de los elementos pesados que emiten partículas alfa, varía sobre 0 órdenes de magnitud, desde 0.1 microsegundos hasta 10 billones de años. Este amplísimo rango, depende fuertemente
TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA
 TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. MATERIA DIVISIBLE O INDIVISIBLE El término átomo aparece en el siglo IV a.c. para designar a la porción indivisible más pequeña que
TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. MATERIA DIVISIBLE O INDIVISIBLE El término átomo aparece en el siglo IV a.c. para designar a la porción indivisible más pequeña que
Unidad 13: Introducción a la Física Nuclear
 Unidad 13: Introducción a la Física Nuclear 1. EL NÚCLEO TÓMICO 1.1. Composición El núcleo atómico es la parte central de un átomo, tiene carga positiva, y concentra más del 99,9% de la masa total del
Unidad 13: Introducción a la Física Nuclear 1. EL NÚCLEO TÓMICO 1.1. Composición El núcleo atómico es la parte central de un átomo, tiene carga positiva, y concentra más del 99,9% de la masa total del
CLASE. Estructura de la Materia
 PROTECCION RADIOLOGICA EN line@ CLASE Estructura de la Materia Estructura de la materia El concepto del Átomo Modelos atómicos Estructura del Átomo Modelos Nucleares Estructura Nuclear Defecto de masa
PROTECCION RADIOLOGICA EN line@ CLASE Estructura de la Materia Estructura de la materia El concepto del Átomo Modelos atómicos Estructura del Átomo Modelos Nucleares Estructura Nuclear Defecto de masa
7.- Los corpúsculos de energía sin masa de la radiación electromagnética recibe el nombre de: a) Muones b) Electrones c) Rayos X d) Fotones
 EXAMEN PARCIAL 1.- El número de protones de un átomo se denomina a) número atómico A b) número másico A c) número atómico Z d) número másico Z 2.- En el núcleo se encuentran: a) Los protones y neutrones
EXAMEN PARCIAL 1.- El número de protones de un átomo se denomina a) número atómico A b) número másico A c) número atómico Z d) número másico Z 2.- En el núcleo se encuentran: a) Los protones y neutrones
Clase N 1. Modelo Atómico I
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Tema 5: Fundamentos de Física nuclear
 Tema 5: Fundamentos de Física nuclear. INTRODUCCION Aunque la primera información acerca del núcleo atómico procede del descubrimiento de la radiactividad realizada por Becquerel en 896, no fue hasta 9
Tema 5: Fundamentos de Física nuclear. INTRODUCCION Aunque la primera información acerca del núcleo atómico procede del descubrimiento de la radiactividad realizada por Becquerel en 896, no fue hasta 9
EJERCICIOS PAU FÍSICA ANDALUCÍA Autor: Fernando J. Nora Costa-Ribeiro Más ejercicios y soluciones en fisicaymat.wordpress.com
 EJERCICIOS PAU FÍSICA ANDALUCÍA Autor: Fernando J Nora Costa-Ribeiro Más ejercicios y soluciones en fisicaymatwordpresscom FÍSICA MODERNA Y NUCLEAR 1- Considere los isótopos, de masas 12,0000 u y 13,0034
EJERCICIOS PAU FÍSICA ANDALUCÍA Autor: Fernando J Nora Costa-Ribeiro Más ejercicios y soluciones en fisicaymatwordpresscom FÍSICA MODERNA Y NUCLEAR 1- Considere los isótopos, de masas 12,0000 u y 13,0034
FÍSICA MODERNA. a) Explique las transformaciones energéticas en el proceso de fotoemisión y calcule la
 FÍSICA MODERNA 2001 1. Un haz de luz de longitud de onda 546 10-9 m incide en una célula fotoeléctrica de cátodo de cesio, cuyo trabajo de extracción es de 2 ev: a) Explique las transformaciones energéticas
FÍSICA MODERNA 2001 1. Un haz de luz de longitud de onda 546 10-9 m incide en una célula fotoeléctrica de cátodo de cesio, cuyo trabajo de extracción es de 2 ev: a) Explique las transformaciones energéticas
Caracterización de los átomos
 Caracterización de los átomos Partículas subatómicas Hasta ahora hemos estudiado distintos modelos atómicos que tratan de explicar cómo son los átomos. En los modelos atómicos más modernos aparecen ciertas
Caracterización de los átomos Partículas subatómicas Hasta ahora hemos estudiado distintos modelos atómicos que tratan de explicar cómo son los átomos. En los modelos atómicos más modernos aparecen ciertas
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO. Lola Castelao
 ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
MODELOS ATOMICOS. Solución Å; Ultravioleta; 1106 m/s
 MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
