BACHILLERATO FÍSICA 14. FÍSICA NUCLEAR. Dpto. de Física y Química. R. Artacho
|
|
|
- Sergio Murillo Fernández
- hace 7 años
- Vistas:
Transcripción
1 BACHILLERATO FÍSICA 14. FÍSICA NUCLEAR R. Artacho Dpto. de Física y Química
2 ÍNDICE 1. El camino hacia el núcleo atómico 2. El descubrimiento del núcleo 3. Tamaño y densidad de los núcleos 4. Estabilidad del núcleo 5. Núcleos inestables: la radiactividad natural 6. Reacciones nucleares 7. La estructura más íntima de la materia 2
3 1 El camino hacia el núcleo atómico La radiactividad es el punto de partida para llegar a la naturaleza nuclear del átomo El físico alemán Wilhelm Konrad Roentgen ( ) descubre los Rayos X. Con el tiempo se sabrá que éste no es un fenómeno nuclear, sino que se debe a saltos de electrones de un nivel a otro En septiembre, en la ciudad de París, Marie Curie ( ), siguiendo los consejos de su esposo y tutor, Pierre Curie, decidió investigar, para su tesis doctoral, los rayos de Becquerel 1898 Joseph John Thomson ( ) descubre el electrón. Becquerel ( ), científico francés, cuando intentó determinar si las sales luminiscentes de uranio emiten Rayos X, descubrió, por azar, la radiactividad. El 18 de julio, Marie y Pierre Curie descubren dos nuevos elementos radiactivos, los bautizan con el nombre de polonio, en honor a Polonia y al otro lo llaman radio. 3
4 1 El camino hacia el núcleo atómico Ernest Rutherford ( ) reporta la existencia de las radiaciones alfa y beta. Años mas tarde se conocerá que están formadas por núcleos de helio (He 2+ ) y electrones (e - ) respectivamente. Becquerel y los esposos Curie reciben el Premio Nobel de Física Paul Villard ( ) demuestra la existencia de las radiaciones gamma constituidas por fotones de alta energía Ernest Rutherford recibe el Premio Nobel de Química. Marie Curie recibe el Nobel de Química por el establecimiento de las propiedades del radio
5 2 El descubrimiento del núcleo Modelo atómico de Thomson Tras el descubrimiento del electrón (descubierto por Thomson en el año 1897), en 1898 Thomson propuso un modelo atómico que tomaba en cuenta la existencia de dicha partícula subatómica. Thomson plantea su modelo como un pastel de frutas: los electrones estaban incrustados en una masa esférica de carga positiva. La carga negativa total de los electrones era la misma que la carga total positiva de la esfera, por lo que dedujo que el átomo era neutro. 5
6 2 El descubrimiento del núcleo Modelo atómico de Rutherford Tras el descubrimiento del protón (descubrimiento en el que Rutherford contribuyó), formuló su modelo atómico mediante un experimento que empleó las partículas alfa para determinar la estructura interna de la materia de la lámina de oro: Del análisis de los resultados observó: La mayoría de las partículas atraviesan la lámina sin desviarse (99,9 %). Algunas partículas se desvían (0,1 %). 6
7 2 El descubrimiento del núcleo Modelo atómico de Rutherford Al ver que no se cumplía el modelo propuesto por Thomson, formuló su propio modelo atómico: modelo nuclear del átomo. + Núcleo: aquí se concentra casi la totalidad de la masa del átomo, y tiene carga positiva. Corteza: está formada por los electrones, que giran alrededor del núcleo describiendo órbitas circulares (sistema solar en miniatura) 7
8 2 El descubrimiento del núcleo 2.1. Constitución básica del núcleo Él experimento de Rutherford solo demostraba que existía un núcleo positivo. Más tarde, bombardeando núcleos atómicos con partículas aceleradas, demostró que los protones resultaban ser constituyentes básicos de los núcleos. La carga nuclear es múltiplo de la carga del protón +e. Carga nuclear = +Ze Z es el número atómico Ocurría que la masa de los núcleos no coincidía con la masa de los protones presentes. Esto llevó a la hipótesis de la existencia del neutrón que se descubrió más tarde (entre 1930 y 1932). Protones Neutrones 8
9 2 El descubrimiento del núcleo 2.1. Constitución básica del núcleo Nucleones: protones (Z) y neutrones (N) Protones Neutrones Número másico, A: Número de nucleones, A = Z + N Núclido: Especie nuclear particular. Dos o más núclidos pueden tener el mismo número atómico Z, y distinto número másico A, se dice entonces que son isótopos. A ZX Todos los isótopos de un mismo elemento químico presentan idénticas propiedades químicas. Cómo pueden coexistir protones en un núcleo? Cómo se explica la emisión de electrones beta por los núcleos? Son elementales los nucleones? 9
10 2 El descubrimiento del núcleo 2.1. Constitución básica del núcleo La unidad de masa atómica 1 u = 1 12 m12 C m12 C = 12 g mol 6, átomos mol = 1, g 1 u = 1, g 12 = 1, g 1 u = 1, kg Partícula Masa (u) Masa (kg) Carga (C) Protones 1, , , Neutrones 1, , No tienen Electrones 1/1837 9, ,
11 3 Tamaño y densidad del núcleo Partícula r La energía cinética de la partícula se habrá transformado en energía potencial electrostática: 1 2 m αv 2 2e Ze α = k r = k 2Ze2 r r = 4kZe2 m α v α 2 Para el oro el radio del núcleo era del orden de m El tamaño del átomo se estimaba en unos m 11
12 3 Tamaño y densidad del núcleo Posteriormente se han empleado técnicas de dispersión de electrones de elevado momento lineal, llegándose a la siguientes conclusiones: Los núcleos atómicos son básicamente esféricos, si bien sus bordes son difusos. El tamaño de los núcleos pequeños es del orden de los m. La unidad en la que suele expresarse el tamaño del núcleo es el fentómetro o fermi, en honor a Enrico Fermi ( ). 1 fm = m Se ha podido establecer una fórmula empírica que relaciona el radio nuclear con el número másico, A: Densidad de los núcleos r 1,2 A 1 3 fm ρ = m 1, A kg 1, A kg kg = = V πr3 3 π 1,2 A1 3 fm 3 ρ = 2, m 3 Qué fuerzas son las responsables de compactar la materia hasta estas densidades? 12
13 3 Tamaño y densidad del núcleo EJERCICIO 1 Calcula el valor máximo del radio de un núcleo de oro de la lámina del experimento de Rutherford, teniendo en cuenta que las partículas alfa contienen 4 nucleones. Datos: m nucleón = 1, kg; v alfa = m/s; Z Au = 79 13
14 4 Estabilidad del núcleo Para determinar las características de la interacción responsable de la estabilidad de los núcleos debemos tener en cuenta las siguientes consideraciones: La densidad de los núcleos es constante e independiente del número de nucleones. Las fuerzas que ligan a los protones y neutrones entre sí, así como a los protones con los neutrones, son iguales. La fragmentación de un núcleo requiere una elevada cantidad de energía, lo que demuestra la fortaleza de la interacción entre los nucleones. Esta interacción recibe el nombre de interacción nuclear fuerte, y tiene las siguientes características: Es atractiva, de gran intensidad y de muy corto alcance (del orden de los m). Es independiente de la carga eléctrica. 14
15 4 Estabilidad del núcleo 4.1. La estabilidad desde el punto de vista energético: energía de enlace Mediante técnicas de espectrometría se ha podido comprobar que la masa de los núcleos es menor que la suma de la masa de los nucleones. Defecto másico m = m nucleones m núcleo E = m c 2 E = m nucleones m núcleo c 2 E = 1u m s 2 = 1, kg m s 2 = 1, J = 931,5 MeV El equivalente energético de 1 u es de 931,5 MeV 15
16 4 Estabilidad del núcleo EJERCICIO 2 Calcula el defecto de masa y la energía liberada en la formación del núcleo del átomo de carbono-12. Datos: m p = 1, u; m n = 1, u 16
17 4 Estabilidad del núcleo 4.1. La estabilidad desde el punto de vista energético: energía de enlace Energía de enlace por nucleón. Estabilidad relativa de los núcleos atómicos Los procesos radiactivos naturales finalizan con la formación de núcleos menores que el original. En la fisión nuclear (ruptura de un núcleo grande en dos medianos) conlleva una gran liberación de energía. En la fusión nuclear (fusión de dos núcleos pequeños para formar núcleos medianos) conlleva una gran liberación de energía. Los núcleos de tamaño intermedio son los más estables! Se puede comprobar calculando la energía de enlace por nucleón: E enlace nucleón = E A 17
18 Energía de enlace por nucleón (MeV) 14. FÍSICA NUCLEAR 4 Estabilidad del núcleo 4.1. La estabilidad desde el punto de vista energético: energía de enlace Energía de enlace por nucleón. Estabilidad relativa de los núcleos atómicos Número másico A 18
19 4 Estabilidad del núcleo EJERCICIO 3 Considera los núcleos de Li-6 y Li-7 de masas 6,015 2 u y 7,016 0 u, respectivamente, siendo 3 el número atómico de estos dos isótopos. Calcula para ambos núcleos: a) El defecto de masa. b) La energía de enlace. c) La energía de enlace por nucleón. Datos: 1 u = 1, kg; c = m/s; m p = 1, u; m n = 1, u 19
20 5 Núcleos inestables: radiactividad natural Si en el núcleo solo hubiera protones la repulsión coulombiana acabaría por desintegrarlo. El papel de los neutrones en los núcleos es dar estabilidad al mismo. En los núcleos pequeños, el número de protones y neutrones es el mismo. A medida que aumenta el número de protones crece el número de neutrones. Los neutrones son partículas inestables que emiten electrones beta y se convierten en protones. Los núcleos son inestables a partir del elemento número 83 (bismuto) que se estabilizan emitiendo partículas alfa o desintegrando neutrones al emitir electrones beta. 20
21 5 Núcleos inestables: radiactividad natural 5.1. Tipos de radiactividad A partir del descubrimiento de la radiactividad por parte de Becquerel, las investigaciones posteriores revelaron que: La intensidad de la radiación emitida no resulta alterada por el hecho de que la sustancia esté en disolución o participe de reacciones químicas. El fenómeno radiactivo va acompañado de emisión de energía. La emisión radiactiva se divide en tres radiaciones características: alfa, beta y gamma. El poder de penetración era muy diferente: 21
22 5 Núcleos inestables: radiactividad natural 5.1. Tipos de radiactividad -q Radiación alfa Radiación gamma +q Radiación beta Radiación alfa ( ) son núcleos de Helio emitidos una velocidad de unos km/s Radiación beta ( ) son electrones que proceden del núcleo por desintegración de un neutrón y son emitidos por el núcleo a unos km/s Radiación gamma ( ) es de naturaleza electromagnética 22
23 5 Núcleos inestables: radiactividad natural 5.2. Leyes del desplazamiento radiactivo (de Rutherford y Soddy) Cuando un núcleo radiactivo emite una partícula alfa, el elemento se desplaza dos lugares a la izquierda en el sistema periódico y su masa disminuye en aproximadamente cuatro unidades: A ZX A 4 Z 2 Y He Cuando un núcleo radiactivo emite un electrón beta, ele elemento resultante se desplaza un lugar a la derecha en el sistema periódico, esto es, se transforma en otro cuyo número atómico es una unidad mayor y cuya masa es prácticamente igual: A ZX A Z+1 Y e Cuando un núcleo radiactivo excitado emite una radiación gamma, se desexcita energéticamente, pero no sufre transmutación alguna. A ZX A Z X + γ 23
24 5 Núcleos inestables: radiactividad natural 5.2. Leyes del desplazamiento radiactivo (de Rutherford y Soddy) Mecanismo de la desintegración alfa E = m n (m n + m α ) c 2 > 0 Si aplicásemos esta expresión a un protón o a un neutrón, el valor sería negativo, lo que haría que la energía cinética transferida a las partículas sería nulo, lo cuál es imposible. 24
25 5 Núcleos inestables: radiactividad natural EJERCICIO 4 El radio-226 se desintegra emitiendo una partícula alfa. Si la masa del Ra-226 es de 226, u; la del Rn-222 es 222, u, y la de la partícula alfa, 4, u, determina: a) La energía cinética que se transfiere en el proceso de desintegración. b) La velocidad con qué es emitida la partícula alfa. 25
26 5 Núcleos inestables: radiactividad natural 5.2. Leyes del desplazamiento radiactivo (de Rutherford y Soddy) Mecanismo de la desintegración beta 0 1 n 1 1 p e + ν e Mecanismo de la desintegración beta positiva 1 1 p 1 0 n e + ν e 26
27 5 Núcleos inestables: radiactividad natural 5.3. Ley de la desintegración radiactiva: periodo de semidesintegración o semivida En 1904 Rutherford descubrió que la actividad de una sustancia radiactiva disminuía exponencialmente con el tiempo. Se entiende por actividad de una sustancia radiactiva al número de partículas emitidas por unidad de tiempo, o lo que es lo mismo, el número de núcleos que se desintegran por unidad de tiempo y es proporcional a una constante característica de cada sustancia (constante de desintegración radiactiva ) y al número de núcleos existentes en ese momento: A = dn dt = λn El número de núcleos que se desintegran en un dt será, por tanto: dn = λndt El número de núcleos existentes en un instante determinado se obtendrá: dn N t N = λdt dn N 0 N = λdt 0 N = N 0 e λt lnn lnn 0 = ln N N 0 = λt Ley de la desintegración radiactiva 27
28 5 Núcleos inestables: radiactividad natural 5.3. Ley de la desintegración radiactiva: periodo de semidesintegración o semivida N Periodo de semidesintegración o semivida es el tiempo que tarda en desintegrarse la mita de los núcleos iniciales. Vida media,, representa el promedio de vida que tenga un átomo y es: τ = 1 λ Las unidades de actividad radiactiva: 1 Becquerel (Bq) = 1 desintegración/s 1 Curie (Ci) = 3, Bq t N 0 2 = N 0e λt = e λt 1 2 ln2 = λt 1 2 T 1 = ln2 2 λ Núclido T 1/2 C años Po-214 Rn-222 Ra-225 Th-234 Np s 3,82 días 14,8 días 24,5 días 2, años U-238 4, años 28
29 5 Núcleos inestables: radiactividad natural 5.4. Datación arqueológica por el método del carbono-14 El C-14 tiene un periodo de semidesintegración de 5730 años. Se forma por los rayos cósmicos que producen neutrones en las capas altas de la atmósfera. Los neutrones colisionan con el N-14 y originan el C n N 14 6 C H El C-14 se mezcla con el isótopo estable C-12 y en el proceso de intercambio es ingerido por los seres vivos. Una vez el ser vivo fallece, finaliza el proceso de intercambio y el C-14 empieza a disminuir por desintegración beta: 14 6C 14 7 N β + ν e 29
30 5 Núcleos inestables: radiactividad natural 5.5. Series radiactivas y geocronología Las partículas alfa reducen el número másico de un isótopo en cuatro unidades y las beta no suponen variación de número másico. Ello ha permitido relacionar los distintos isótopos radiactivos que existen en la naturaleza, formando las familias o series radiactivas. Serie 4n o del Th-232: acaba en el isótopo estable Pb-208. Serie 4n+1 o del Pu-241: no se conoce más que su producto estable final Bi-209. Serie 4n+2 o del U-238: acaba en el isótopo estable Pb-206. Serie 4n+3 o del U-235: acaba en el isótopo estable Pb-207. El conocimiento de los periodos de semidesintegración de los isótopos que componen la serie permite la datación de rocas y minerales por el método antes expuesto (ley de la geocronología). 30
31 5 Núcleos inestables: radiactividad natural EJERCICIO 5 Se observa que la actividad radiactiva de una muestra de madera prehistórica es diez veces menor que la de una muestra de igual masa de madera moderna. Sabiendo que período de semidesintegración del C-14 es de años, calcula la antigüedad de la muestra. 31
32 6 Reacciones nucleares El primero que pensó en modificar artificialmente los núcleos fue Rutherford y descubrió el protón: 14 7N He 17 8 O H En 1931, Frédéric Joliot ( ) e Irène Curie ( ) descubrieron que la bombardear núcleos de berilio con partículas alfa, se producía una radiación muy penetrante que inicialmente supusieron que era radiación gamma. Análisis posteriores de James Chadwick ( ) permitió identificarla como un neutrón: 4 9 Be He 12 6 C n 32
33 6 Reacciones nucleares 6.1. Reacciones nucleares artificiales En 1932 John Cockcroft ( ) y E.T.S. Walton ( ) bombardean núcleos de Litio con protones artificialmente acelerados: Reacciones nucleares con neutrones El núcleo se transforma en un isótopo de número másico A+1 y emite radiación gamma: El núcleo emite una partícula alfa: El núcleo emite un protón: 3 7 Li H 8 4 Be He U n U + γ 10 5B n 7 3 Li He 14 7N n 14 6 C H Al capturar el neutrón, el núcleo se desestabiliza y se fragmenta en dos núcleos más pequeños: fisión nuclear. 33
34 6 Reacciones nucleares 6.2. Fisión nuclear En 1938, Otto Hahn y Frederic Strassman observaron la primera fisión nuclear del U-235 utilizando neutrones lentos: U n U Ba Kr n La energía liberada por un átomo de uranio: Q = m 931,5 MeV 200MeV 34
35 6 Reacciones nucleares 6.2. Fisión nuclear La energía que se desprendía en la fisión del uranio era enorme lo que condujo a contralar el proceso de fisión ya que cada uno de los neutrones resultante provocaba la fisión de otros núcleos produciendo así una reacción en cadena: Reacción de Fisión Nuclear en Cadena Para que se produzca la reacción en cadena es necesario que exista una cantidad de masa denominada masa crítica. 35
36 6 Reacciones nucleares 6.3. Fusión nuclear En 1929 Fritz Houtermans y Robert Atkinson explicaron la enorme energía liberada en las estrellas como resultado de un proceso de fusión nuclear: H 4 2 He e + 2ν e + γ o bien: H H 2 4 He e + ν e + γ En este proceso se libera también mucha energía: E = m 931,5 MeV 14,1 MeV El problema radica en la enorme temperatura que hay conseguir para que los núcleos venzan las repulsiones electrostáticas y que gira alrededor de los 16 millones de ºC. 36
37 6 Reacciones nucleares EJERCICIO 6 Un haz de deuterones (H-2) procedentes de un ciclotrón bombardea un blanco de C-13, con lo que se emiten protones. a) Escribe la reacción que tiene lugar. b) Cuánto vale la energía liberada en el proceso debido al defecto de masa? Datos: M (C-13) = 13, u; M (C-14) = 14, u; M (H-2) = 2, u; M (H-1) = 1, u 37
38 7 La estructura más íntima de la materia 38
39 7 La estructura más íntima de la materia 7.1. Quarks y leptones Los quarks De los seis quarks, únicamente los u y los d son constituyentes de la materia ordinaria (protón, neutrón, ) (mesón, ) 39
40 7 La estructura más íntima de la materia 40
41 7 La estructura más íntima de la materia emisión beta 41
42 7 La estructura más íntima de la materia 42
43 7 La estructura más íntima de la materia 43
Esta parte de la Física estudia el comportamiento de los núcleos atómicos. Física nuclear
 Esta parte de la Física estudia el comportamiento de los núcleos atómicos Física nuclear CORTEZA Electrones NÚCLEO Protones Neutrones PARTÍCULA CARGA MASA Electrón (e - ) -1,6.10-19 C 9,1.10-31 kg Protón
Esta parte de la Física estudia el comportamiento de los núcleos atómicos Física nuclear CORTEZA Electrones NÚCLEO Protones Neutrones PARTÍCULA CARGA MASA Electrón (e - ) -1,6.10-19 C 9,1.10-31 kg Protón
La estructura atómica: el núcleo
 Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
La física del siglo XX
 Unidad 13 La física del siglo XX chenalc@gmail.com Banda de estabilidad nuclear Posición de los nucleidos estables. Para pequeños valores de Z, los núcleos estables son aquellos en los que Z = N. A medida
Unidad 13 La física del siglo XX chenalc@gmail.com Banda de estabilidad nuclear Posición de los nucleidos estables. Para pequeños valores de Z, los núcleos estables son aquellos en los que Z = N. A medida
FÍSICA NUCLEAR. I WANT TO KNOW GOD S THOUGHTS; THE REST ARE DETAILS (Albert Einstein )
 FÍSICA NUCLEAR I WANT TO KNOW GOD S THOUGHTS; THE REST ARE DETAILS (Albert Einstein. 879 955) . INTRODUCCIÓN. RESEÑA HISTÓRICA Radiactividad propiedad de los núcleos atómicos de ciertos isótopos de modificar
FÍSICA NUCLEAR I WANT TO KNOW GOD S THOUGHTS; THE REST ARE DETAILS (Albert Einstein. 879 955) . INTRODUCCIÓN. RESEÑA HISTÓRICA Radiactividad propiedad de los núcleos atómicos de ciertos isótopos de modificar
FÍSICA MODERNA FÍSICA NUCLEAR Y DE PARTÍCULAS. José Luis Rodríguez Blanco
 FÍSICA MODERNA FÍSICA NUCLEAR Y DE PARTÍCULAS José Luis Rodríguez Blanco Fenómenos radiactivos H. Becquerel (1896): Sales de uranio emiten una radiación sumamente penetrante independiente del estado de
FÍSICA MODERNA FÍSICA NUCLEAR Y DE PARTÍCULAS José Luis Rodríguez Blanco Fenómenos radiactivos H. Becquerel (1896): Sales de uranio emiten una radiación sumamente penetrante independiente del estado de
J.M.L.C. IES Aguilar y Cano ALGUNOS DERECHOS RESERVADOS
 La radiactividad o radioactividad es un fenómeno físico natural, por el cual algunas sustancias o elementos químicos llamados radiactivos, emiten radiaciones que tienen la propiedad de impresionar placas
La radiactividad o radioactividad es un fenómeno físico natural, por el cual algunas sustancias o elementos químicos llamados radiactivos, emiten radiaciones que tienen la propiedad de impresionar placas
NUCLEO ~ m NUCLEÓN ~ m. MATERIA ~ 10-9 m. ÁTOMO ~ m. Átomo. Protón
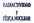 La materia está formada por átomos y moléculas que se unen para formar los sólidos. Cada átomo está compuesto de un núcleo con carga positiva y electrones que orbitan a su alrededor. El núcleo, a su vez,
La materia está formada por átomos y moléculas que se unen para formar los sólidos. Cada átomo está compuesto de un núcleo con carga positiva y electrones que orbitan a su alrededor. El núcleo, a su vez,
Qué es la energía nuclear? Tema1
 Toda la materia del universo está formada por moléculas que a su vez están constituidas por átomos, pequeñísimas unidades que durante mucho tiempo se consideraron invisibles. En la actualidad sabemos que
Toda la materia del universo está formada por moléculas que a su vez están constituidas por átomos, pequeñísimas unidades que durante mucho tiempo se consideraron invisibles. En la actualidad sabemos que
Demócrito. Modelo de Dalton. Modelo atómico de Thomson
 modelo atómico Demócrito Fue probablemente el primero en creer que la materia estaba constituida por partículas que denomino átomos, palabra que significa sin división, ya que consideraba el átomo como
modelo atómico Demócrito Fue probablemente el primero en creer que la materia estaba constituida por partículas que denomino átomos, palabra que significa sin división, ya que consideraba el átomo como
BACHILLERATO FÍSICA 12. FÍSICA NUCLEAR. Dpto. de Física y Química. R. Artacho
 BACHILLERATO FÍSICA 12. FÍSICA NUCLEAR R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. El camino hacia el núcleo atómico 2. El descubrimiento del núcleo 3. Tamaño y densidad de los núcleos 4.
BACHILLERATO FÍSICA 12. FÍSICA NUCLEAR R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. El camino hacia el núcleo atómico 2. El descubrimiento del núcleo 3. Tamaño y densidad de los núcleos 4.
Temas X y XI: Radiactividad
 Física Médica Grupo 1B Temas X y XI: Radiactividad Dpto. de Radiología (Física Médica) Facultad de Medicina Transiciones nucleares 1. Desex. gamma: A Z X * A Z X+γ 1. Emisión alfa: A Z X A 4 Z 2 Y+α 2.
Física Médica Grupo 1B Temas X y XI: Radiactividad Dpto. de Radiología (Física Médica) Facultad de Medicina Transiciones nucleares 1. Desex. gamma: A Z X * A Z X+γ 1. Emisión alfa: A Z X A 4 Z 2 Y+α 2.
PROBLEMAS DE FÍSICA NUCLEAR
 PROBLEMAS DE FÍSICA NUCLEAR 207 ) Se tiene una muestra del isótopo 226 Ra cuyo periodo de semidesintegración es de 600 años. Calcule su constante de desintegración y el tiempo que se requiere para que
PROBLEMAS DE FÍSICA NUCLEAR 207 ) Se tiene una muestra del isótopo 226 Ra cuyo periodo de semidesintegración es de 600 años. Calcule su constante de desintegración y el tiempo que se requiere para que
! " # $ " ' % () *! + ),-. /*01 ",*2 ", $ /- % $. * 1 &, * 1 " $, / " % # 1 $ 3 & + " #* 1, 4*5 1 #, " 4-6 " $*$,* 7, 4-8 $" % # $ # %$%
 Interacción nuclear Cuestiones! " # $ $%$& " ' % () *! + ),-. /*0 ",* ", $ 35 07 95U 8Pb /- % $. * &, * " $, / " % # $ 3 & + " #*, *5 #, " # #%## -6 " $*$,* 7, *0,&#%# -8 $" % # $ # %$% " # $ & & -. '
Interacción nuclear Cuestiones! " # $ $%$& " ' % () *! + ),-. /*0 ",* ", $ 35 07 95U 8Pb /- % $. * &, * " $, / " % # $ 3 & + " #*, *5 #, " # #%## -6 " $*$,* 7, *0,&#%# -8 $" % # $ # %$% " # $ & & -. '
Interacción nuclear 1
 Interacción nuclear Cuestiones. Comente cada una de las frases siguientes: a) Isótopos son aquellos núclidos de igual número atómico pero distinto número másico. b) Si un núclido emite una partícula alfa,
Interacción nuclear Cuestiones. Comente cada una de las frases siguientes: a) Isótopos son aquellos núclidos de igual número atómico pero distinto número másico. b) Si un núclido emite una partícula alfa,
Átomo. Posee protones y neutrones. Estos se llaman Nucleones. Alrededor giran los electrones en. forma de nube. Son eléctricamente neutro
 Átomo Posee protones y neutrones Estos se llaman Nucleones Alrededor giran los electrones en forma de nube Son eléctricamente neutro Por eso Z(número de Protones)=Ne(Número de Electrones) Átomo Su dimensión
Átomo Posee protones y neutrones Estos se llaman Nucleones Alrededor giran los electrones en forma de nube Son eléctricamente neutro Por eso Z(número de Protones)=Ne(Número de Electrones) Átomo Su dimensión
C U R S O: FÍSICA MENCIÓN MATERIAL: FM-35 FÍSICA MODERNA II. Radiactividad. Clases de radiación
 C U R S O: FÍSICA MENCIÓN MATERIAL: FM-35 FÍSICA MODERNA II Radiactividad Radiactividad es la propiedad que presentan los núcleos atómicos de ciertos isótopos de modificar espontáneamente su constitución,
C U R S O: FÍSICA MENCIÓN MATERIAL: FM-35 FÍSICA MODERNA II Radiactividad Radiactividad es la propiedad que presentan los núcleos atómicos de ciertos isótopos de modificar espontáneamente su constitución,
CUESTIONES. 5. (2006) a) Cómo se puede explicar que un núcleo emita partículas β si en él sólo existen neutrones y protones? b) El
 CUESTIONES 1. (2004) a) Describa las características de los procesos de emisión radiactiva alfa, beta y gamma. b) Uno de ellos consiste en la emisión de electrones. Cómo es posible que un núcleo emita
CUESTIONES 1. (2004) a) Describa las características de los procesos de emisión radiactiva alfa, beta y gamma. b) Uno de ellos consiste en la emisión de electrones. Cómo es posible que un núcleo emita
RADIOACTIVIDAD - (2015)
 RADIOACTIVIDAD - (2015) A- CONCEPTOS GENERALES SOBRE RADIACTIVIDAD B- ISÓTOPOS C- TIPOS Y PROPIEDADES DE LAS RADIACCIONES D- REACCIONES NUCLEARES E- VIDA MEDIA A- CONCEPTOS GENERALES SOBRE RADIACTIVIDAD
RADIOACTIVIDAD - (2015) A- CONCEPTOS GENERALES SOBRE RADIACTIVIDAD B- ISÓTOPOS C- TIPOS Y PROPIEDADES DE LAS RADIACCIONES D- REACCIONES NUCLEARES E- VIDA MEDIA A- CONCEPTOS GENERALES SOBRE RADIACTIVIDAD
La radioactividad es una propiedad intrínseca de los núcleos de los átomos.
 Radiactividad y Reacciones Nucleares Tema 3-1/23 1. DESCUBRIIMIIENTO DE LA RADIIACTIIVIIDAD Descubrimiento: Henri Becquerel (1896) La radioactividad es una propiedad intrínseca de los núcleos de los átomos.
Radiactividad y Reacciones Nucleares Tema 3-1/23 1. DESCUBRIIMIIENTO DE LA RADIIACTIIVIIDAD Descubrimiento: Henri Becquerel (1896) La radioactividad es una propiedad intrínseca de los núcleos de los átomos.
FÍSICA 2º Bachillerato Ejercicios: Física nuclear
 (0) Ejercicio nº 90 El período de semidesintegración del 38 Sr es de 28 años. Calcular: a) Su constante radiactiva, expresándola en /s. b) La actividad en curios de una muestra de mg. c) El tiempo necesario
(0) Ejercicio nº 90 El período de semidesintegración del 38 Sr es de 28 años. Calcular: a) Su constante radiactiva, expresándola en /s. b) La actividad en curios de una muestra de mg. c) El tiempo necesario
N está formado por 7 protones y 8 neutrones, luego su masa teórica debería ser:
 1. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,189 u. Datos: 1 u = 1,6 1-2 g ; m p = 1,26 u; m n = 1,8665 u El núcleo 15 N está formado por protones y 8 neutrones,
1. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,189 u. Datos: 1 u = 1,6 1-2 g ; m p = 1,26 u; m n = 1,8665 u El núcleo 15 N está formado por protones y 8 neutrones,
El núcleo Atómico. 10 Nuc. 1 fm = femtómetro o Fermi. 1 Aº = Angstrom.
 Física Nuclear El núcleo Atómico. Núcleo Átomo e- R 1 15 m = 1 fm 1 Nuc = A R 1 m 1 Aº 1 fm = femtómetro o Fermi. 1 Aº = Angstrom. Estructura Nuclear. Núcleo consiste de protones p y neutrones n. Z : Número
Física Nuclear El núcleo Atómico. Núcleo Átomo e- R 1 15 m = 1 fm 1 Nuc = A R 1 m 1 Aº 1 fm = femtómetro o Fermi. 1 Aº = Angstrom. Estructura Nuclear. Núcleo consiste de protones p y neutrones n. Z : Número
física física conceptual aplicada MétodoIDEA E L núcleo atómico y la radiactividad Entre la y la 1º de bachillerato Félix A.
 Entre la y la física física conceptual aplicada MétodoIDEA E L núcleo atómico y la radiactividad 1º de bachillerato Félix A. Gutiérrez Múzquiz Contenidos 1. PROPIEDADES DE LOS ÚCLEOS... 3 2. RADIACTIVIDAD
Entre la y la física física conceptual aplicada MétodoIDEA E L núcleo atómico y la radiactividad 1º de bachillerato Félix A. Gutiérrez Múzquiz Contenidos 1. PROPIEDADES DE LOS ÚCLEOS... 3 2. RADIACTIVIDAD
Preguntas de Física Nuclear. 1. Qué partículas forman el núcleo? Cuál es el término general para nombrarlas? De qué están compuestas esas partículas?
 Preguntas de Física Nuclear 1. Qué partículas forman el núcleo? Cuál es el término general para nombrarlas? De qué están compuestas esas partículas? 2. Cuál es la definición de número atómico? Cuál es
Preguntas de Física Nuclear 1. Qué partículas forman el núcleo? Cuál es el término general para nombrarlas? De qué están compuestas esas partículas? 2. Cuál es la definición de número atómico? Cuál es
CUESTIONES DE FÍSICA NUCLEAR
 CUESTIONES DE FÍSICA NUCLEAR 017 1) Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I. ) Explique cómo varía la estabilidad de los núcleos atómicos en función
CUESTIONES DE FÍSICA NUCLEAR 017 1) Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I. ) Explique cómo varía la estabilidad de los núcleos atómicos en función
BOLETÍN DE TEORÍA FÍSICA NUCLEAR (trabajo) C1: Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I.
 BOLETÍN DE TEORÍA FÍSICA NUCLEAR (trabajo) C1: Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I. La actividad de una muestra radiactiva refleja el número
BOLETÍN DE TEORÍA FÍSICA NUCLEAR (trabajo) C1: Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I. La actividad de una muestra radiactiva refleja el número
BOLETÍN DE TEORÍA FÍSICA NUCLEAR (trabajo) C1: Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I.
 BOLETÍN DE TEORÍA FÍSICA NUCLEAR (trabajo) C1: Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I. C2: Explique cómo varía la estabilidad de los núcleos atómicos
BOLETÍN DE TEORÍA FÍSICA NUCLEAR (trabajo) C1: Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I. C2: Explique cómo varía la estabilidad de los núcleos atómicos
N está formado por 7 protones y 8 neutrones, luego su masa teórica debería ser:
 01. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,0001089 u. Datos: 1 u = 1, 10-2 g ; m p = 1,002 u; m n = 1,0085 u El núcleo 15 N está formado por protones y 8
01. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,0001089 u. Datos: 1 u = 1, 10-2 g ; m p = 1,002 u; m n = 1,0085 u El núcleo 15 N está formado por protones y 8
Curso de Radioactividad y Medio Ambiente clase 2
 Curso de Radioactividad y Medio Ambiente clase 2 Departamento de Física, Facultad de Ciencias Exactas - UNLP Instituto de Física La Plata CONICET Calle 49 y 115 La Plata Qué es la radioactividad? En la
Curso de Radioactividad y Medio Ambiente clase 2 Departamento de Física, Facultad de Ciencias Exactas - UNLP Instituto de Física La Plata CONICET Calle 49 y 115 La Plata Qué es la radioactividad? En la
Núcleo Atómico. El núcleo es una masa muy compacta formada por protones y neutrones.
 Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Química General III. Tema 13. Química Nuclear. Sulfato doble de K y U, emite radiación fuente de rayos radiactivos.
 Química General III. Tema 3. Química Nuclear Introducción. Reacción Química Wilhelm Röntgen Henri Becquerel solo 896 895 participan electrones. Rayos X Sulfato doble de K y U, emite radiación fuente de
Química General III. Tema 3. Química Nuclear Introducción. Reacción Química Wilhelm Röntgen Henri Becquerel solo 896 895 participan electrones. Rayos X Sulfato doble de K y U, emite radiación fuente de
Resolución PRÁCTICO 9
 Resolución PRÁCTICO 9 1- Complete las siguientes ecuaciones nucleares, remplazando las X por los símbolos o números correspondientes (Nota: X toma diferentes números y símbolos en cada una de las situaciones):
Resolución PRÁCTICO 9 1- Complete las siguientes ecuaciones nucleares, remplazando las X por los símbolos o números correspondientes (Nota: X toma diferentes números y símbolos en cada una de las situaciones):
RADIACTIVIDAD. Alejandra Pardo Martínez 1º ESO
 RADIACTIVIDAD Alejandra Pardo Martínez 1º ESO 1. ESTRUCTURA ATÓMICA El átomo es la parte más pequeña de materia que conserva sus propiedades químicas. De forma simplificada, puede considerarse que está
RADIACTIVIDAD Alejandra Pardo Martínez 1º ESO 1. ESTRUCTURA ATÓMICA El átomo es la parte más pequeña de materia que conserva sus propiedades químicas. De forma simplificada, puede considerarse que está
Radiactividad y Física Nuclear (I): Radiactividad Natural diferentes tipos de radiación
 Radiactividad y Física Nuclear (I): Radiactividad Natural diferentes tipos de radiación 1896 : Becquerel descubre la Pechblenda( mineral de uranio), capaz de impresionar placas fotográficas en ausencia
Radiactividad y Física Nuclear (I): Radiactividad Natural diferentes tipos de radiación 1896 : Becquerel descubre la Pechblenda( mineral de uranio), capaz de impresionar placas fotográficas en ausencia
Problemas de Física moderna. Nuclear 2º de bachillerato. Física
 1 Problemas de Física moderna. Nuclear º de bachillerato. Física 1. El isótopo 34 U tiene un periodo de semidesintegración de 50000 años. Si partimos de una muestra de 10 gramos de dicho isótopo, determine:
1 Problemas de Física moderna. Nuclear º de bachillerato. Física 1. El isótopo 34 U tiene un periodo de semidesintegración de 50000 años. Si partimos de una muestra de 10 gramos de dicho isótopo, determine:
ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA.
 ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA. INDICE Qué es la materia? Modelos de la materia Fuerzas Fundamentales
ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA. INDICE Qué es la materia? Modelos de la materia Fuerzas Fundamentales
1. Con respecto a la radiación gamma, cuál(es) de las siguientes afirmaciones es(son) correcta(s)?
 Nº GUÍA PRÁCTICA Fenómenos nucleares I: partículas radiactivas Ejercicios PSU 1. Con respecto a la radiación gamma, cuál(es) de las siguientes afirmaciones es(son) correcta(s)? I) Puede penetrar a través
Nº GUÍA PRÁCTICA Fenómenos nucleares I: partículas radiactivas Ejercicios PSU 1. Con respecto a la radiación gamma, cuál(es) de las siguientes afirmaciones es(son) correcta(s)? I) Puede penetrar a través
CUESTIONES DE FÍSICA NUCLEAR
 CUESTIONES DE FÍSICA NUCLEAR 2017 1) Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I. La magnitud dn se denomina actividad de una muestra radiactiva e indica
CUESTIONES DE FÍSICA NUCLEAR 2017 1) Defina actividad de una muestra radioactiva, escriba su fórmula e indique sus unidades en el S.I. La magnitud dn se denomina actividad de una muestra radiactiva e indica
13 Física nuclear. Actividades del interior de la unidad
 13 Física nuclear ctividades del interior de la unidad 1. Indica brevemente la diferencia entre radiactividad natural y radiactividad artificial. La radiactividad natural proviene de sustancias que se
13 Física nuclear ctividades del interior de la unidad 1. Indica brevemente la diferencia entre radiactividad natural y radiactividad artificial. La radiactividad natural proviene de sustancias que se
Tema 6. ESTRUCTURA NUCLEAR
 Introducción Experimento de Rutherford. Existencia del núcleo Partículas nucleares Tamaño y densidad del núcleo Energía de enlace y estabilidad nuclear Desintegración radiactiva Radiactividad α,β,γ Series
Introducción Experimento de Rutherford. Existencia del núcleo Partículas nucleares Tamaño y densidad del núcleo Energía de enlace y estabilidad nuclear Desintegración radiactiva Radiactividad α,β,γ Series
Núcleo Atómico y Radiactividad
 Curso de Química I Núcleo Atómico y Radiactividad Es la parte del átomo que contiene toda la carga positiva y la mayoría de la masa. Ocupa una región muy pequeña dentro del átomo: radio nuclear ~ 10 15
Curso de Química I Núcleo Atómico y Radiactividad Es la parte del átomo que contiene toda la carga positiva y la mayoría de la masa. Ocupa una región muy pequeña dentro del átomo: radio nuclear ~ 10 15
INTRODUCCIÓN A LA FÍSICA MODERNA
 INTRODUCCIÓN A LA FÍSICA MODERNA CUESTIONES Física relativista (Ver Lección 12) 1. Teóricamente qué demostraba el experimento de Michelson Morley 2. Einstein desarrolló dos teorías de la relatividad: a.
INTRODUCCIÓN A LA FÍSICA MODERNA CUESTIONES Física relativista (Ver Lección 12) 1. Teóricamente qué demostraba el experimento de Michelson Morley 2. Einstein desarrolló dos teorías de la relatividad: a.
TEMA 6.- EL NÚCLEO 1.- LA NATURALEZA DE LAS REACCIONES NUCLEARES 2.- ESTABILIDAD NUCLEAR. Energía de enlace nuclear 3.- RADIACTIVIDAD NATURAL
 TEMA 6.- EL NÚCLEO.- LA NATURALEZA DE LAS REACCIONES NUCLEARES 2.- ESTABILIDAD NUCLEAR Energía de enlace nuclear 3.- RADIACTIVIDAD NATURAL 4.- RADIACTIVIDAD ARTIFICIAL 5.- FISIÓN NUCLEAR 6.- FUSIÓN NUCLEAR
TEMA 6.- EL NÚCLEO.- LA NATURALEZA DE LAS REACCIONES NUCLEARES 2.- ESTABILIDAD NUCLEAR Energía de enlace nuclear 3.- RADIACTIVIDAD NATURAL 4.- RADIACTIVIDAD ARTIFICIAL 5.- FISIÓN NUCLEAR 6.- FUSIÓN NUCLEAR
H Deuterio (1p+1n); ,02310 = = = 1uma = 1u = = 1,6610 kg
 El átomo Física uclear Es la parte más pequeña de un elemento químico que mantiene sus propiedades. Está formado por protones y neutrones, que forman el núcleo, y por electrones que giran en la corteza.
El átomo Física uclear Es la parte más pequeña de un elemento químico que mantiene sus propiedades. Está formado por protones y neutrones, que forman el núcleo, y por electrones que giran en la corteza.
PPTCEL001QM11-A16V1 Clase. Fenómenos nucleares I: partículas radiactivas
 PPTCEL001QM11-A16V1 Clase Fenómenos nucleares I: partículas radiactivas Aprendizajes esperados Conocer las partículas radiactivas. Conocer el concepto de isótopos. Aplicar el concepto de masa atómica promedio.
PPTCEL001QM11-A16V1 Clase Fenómenos nucleares I: partículas radiactivas Aprendizajes esperados Conocer las partículas radiactivas. Conocer el concepto de isótopos. Aplicar el concepto de masa atómica promedio.
Descubrimiento del Núcleo
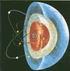 Física Nuclear Descubrimiento del Núcleo Componentes del núcleo: protones y neutrones Propiedades de la fuerza nuclear fuerte Debe ser de atracción y suficientemente grande para vencer la repulsión culombiana
Física Nuclear Descubrimiento del Núcleo Componentes del núcleo: protones y neutrones Propiedades de la fuerza nuclear fuerte Debe ser de atracción y suficientemente grande para vencer la repulsión culombiana
Z, ( a veces se suprime Z),donde X es el símbolo químico del elemento. Así por ejemplo tenemos los isótopos del carbono:
 RADIACTIVIDAD El núcleo atómico está constituido por nucleones: Z protones y N neutrones, ( en total A ). Como sabemos los nucleones son partículas elementales y están constituidos por la agrupación de
RADIACTIVIDAD El núcleo atómico está constituido por nucleones: Z protones y N neutrones, ( en total A ). Como sabemos los nucleones son partículas elementales y están constituidos por la agrupación de
A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye
 Características esenciales de las reacciones químicas A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye Joseph Louis Proust (formación de CuCO 3 ): los elementos que
Características esenciales de las reacciones químicas A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye Joseph Louis Proust (formación de CuCO 3 ): los elementos que
Física 2º Bacharelato
 Física 2º Bacharelato DEPARTAMENTO DE FÍSICA E QUÍMICA Física Moderna 16/05/08 Nombre: Problemas 1. En la alta atmósfera, el 7 N, al ser bombardeado con neutrones procedentes de la radiación cósmica, se
Física 2º Bacharelato DEPARTAMENTO DE FÍSICA E QUÍMICA Física Moderna 16/05/08 Nombre: Problemas 1. En la alta atmósfera, el 7 N, al ser bombardeado con neutrones procedentes de la radiación cósmica, se
Física nuclear. Núcleo atómico
 Física nuclear La configuración de los electrones de un átomo determina si este puede unirse a otros para formar compuestos y la manera para hacerlo. Además, los electrones causan efectos tales como la
Física nuclear La configuración de los electrones de un átomo determina si este puede unirse a otros para formar compuestos y la manera para hacerlo. Además, los electrones causan efectos tales como la
[a] Consulta el libro de Física. Recuerda que la explicación del efecto fotoeléctrico, debida a Einstein, reafirma la teoría corpuscular de la luz.
![[a] Consulta el libro de Física. Recuerda que la explicación del efecto fotoeléctrico, debida a Einstein, reafirma la teoría corpuscular de la luz. [a] Consulta el libro de Física. Recuerda que la explicación del efecto fotoeléctrico, debida a Einstein, reafirma la teoría corpuscular de la luz.](/thumbs/69/61893136.jpg) Actividad 1 [a] En qué consiste el efecto fotoeléctrico? Es una reafirmación de la teoría corpuscular o de la teoría ondulatoria? [b] Cómo es posible que los protones y neutrones que constituyen un núcleo
Actividad 1 [a] En qué consiste el efecto fotoeléctrico? Es una reafirmación de la teoría corpuscular o de la teoría ondulatoria? [b] Cómo es posible que los protones y neutrones que constituyen un núcleo
FÍSICA NUCLEAR. Tema 8 del libro (tercer tema de este bloque) 4. Modos de desintegración y leyes de desplazamiento radiactivo
 FÍSICA NUCLEAR. Tema 8 del libro (tercer tema de este bloque) 1. La radiactividad 2. Estructura y características del núcleo 3. Estabilidad 3.1 Fuerza nuclear 3.2 Energía de enlace 3.2.1 Estabilidad nuclear
FÍSICA NUCLEAR. Tema 8 del libro (tercer tema de este bloque) 1. La radiactividad 2. Estructura y características del núcleo 3. Estabilidad 3.1 Fuerza nuclear 3.2 Energía de enlace 3.2.1 Estabilidad nuclear
FÍSICA NUCLEAR. El núcleo atómico
 1. El núcleo atómico. 2. Energía de enlace nuclear. 3. La radiactividad nuclear. 4. Leyes de la desintegración radiactiva. 5. Reacciones nucleares: su aspecto energético. 6. Fisión nuclear: reactores nucleares.
1. El núcleo atómico. 2. Energía de enlace nuclear. 3. La radiactividad nuclear. 4. Leyes de la desintegración radiactiva. 5. Reacciones nucleares: su aspecto energético. 6. Fisión nuclear: reactores nucleares.
UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS. 1.3 El sol, horno nuclear
 UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS 1.3 El sol, horno nuclear RADIACTIVIDAD Y DESINTEGRACIÓN NUCLEAR HISTORIA DEL ÁTOMO Hace aproximadamente 2500 años, los filósofos griegos, afirmaron que la
UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS 1.3 El sol, horno nuclear RADIACTIVIDAD Y DESINTEGRACIÓN NUCLEAR HISTORIA DEL ÁTOMO Hace aproximadamente 2500 años, los filósofos griegos, afirmaron que la
QUÍMICA COMÚN Y ELECTIVO
 QUÍMICA COMÚN Y ELECTIVO GENERALIDADES 1. MODELOS ATÓMICOS 2. EL AGUA, EL AIRE Y EL PETRÓLEO COMÚN 3. QUÍMICA ORGÁNICA 4. DISOLUCIONES QUÍMICAS 1. EQUILIBRIO QUÍMICO 2. CINÉTICA 3. ACTIVIDAD NUCLEAR ELECTIVO
QUÍMICA COMÚN Y ELECTIVO GENERALIDADES 1. MODELOS ATÓMICOS 2. EL AGUA, EL AIRE Y EL PETRÓLEO COMÚN 3. QUÍMICA ORGÁNICA 4. DISOLUCIONES QUÍMICAS 1. EQUILIBRIO QUÍMICO 2. CINÉTICA 3. ACTIVIDAD NUCLEAR ELECTIVO
H Deuterio (1p+1n); , uma 1u 1,66 10 kg R 1 10 A
 El átomo ísica Nuclear Es la parte más pequeña de un elemento químico que mantiene sus propiedades. Está formado por protones y neutrones, que forman el núcleo, y por electrones que giran en la corteza.
El átomo ísica Nuclear Es la parte más pequeña de un elemento químico que mantiene sus propiedades. Está formado por protones y neutrones, que forman el núcleo, y por electrones que giran en la corteza.
Interacción nuclear PONENCIA DE FÍSICA DE ANDALUCÍA. CURSO
 Interacción nuclear Cuestiones (96-E) Comente cada una de las frases siguientes: a) Isótopos son aquellos núclidos de igual número atómico pero distinto número másico. b) Si un núclido emite una partícula
Interacción nuclear Cuestiones (96-E) Comente cada una de las frases siguientes: a) Isótopos son aquellos núclidos de igual número atómico pero distinto número másico. b) Si un núclido emite una partícula
Qué es la Radiactividad?
 RADIACTIVIDAD Qué es la Radiactividad? Es el fenómeno que se produce en el núcleo de algunos átomos, más concretamente en el núcleo de algunos isótopos, los cuales se modifican emitiendo radiaciones. Se
RADIACTIVIDAD Qué es la Radiactividad? Es el fenómeno que se produce en el núcleo de algunos átomos, más concretamente en el núcleo de algunos isótopos, los cuales se modifican emitiendo radiaciones. Se
Ejercicios de Física cuántica y nuclear. PAU (PAEG)
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
CENTRALES NUCLEARES CENTRALES NUCLEARES DE AGUA EN EBULLICIÓN (BWR). CENTRALES NUCLEARES DE AGUA A PRESIÓN (PWR)
 CENTRALES NUCLEARES CENTRALES NUCLEARES DE AGUA EN EBULLICIÓN (BWR). CENTRALES NUCLEARES DE AGUA A PRESIÓN (PWR) TERMINOLOGÍA NUCLEAR El núcleo atómico es la parte central de un átomo, está formado por
CENTRALES NUCLEARES CENTRALES NUCLEARES DE AGUA EN EBULLICIÓN (BWR). CENTRALES NUCLEARES DE AGUA A PRESIÓN (PWR) TERMINOLOGÍA NUCLEAR El núcleo atómico es la parte central de un átomo, está formado por
Ejercicios de Física cuántica y nuclear. PAEG
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
Unidad N 11 QUIMICA NUCLEAR
 Unidad N 11 QUIMICA NUCLEAR Estructura básica del átomo Electrones: CAMBIOS: generan las propiedades Químicas y Físicas más o menos comunes de un dado átomo. Núcleo: CAMBIOS: modifican en forma sustancial
Unidad N 11 QUIMICA NUCLEAR Estructura básica del átomo Electrones: CAMBIOS: generan las propiedades Químicas y Físicas más o menos comunes de un dado átomo. Núcleo: CAMBIOS: modifican en forma sustancial
Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA
 Física P.A.U. FÍSICA MODERNA FÍSICA MODERNA PROBLEMAS MECÁNICA CUÁNTICA.. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 5 nm, el potencial de frenado para los electrones
Física P.A.U. FÍSICA MODERNA FÍSICA MODERNA PROBLEMAS MECÁNICA CUÁNTICA.. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 5 nm, el potencial de frenado para los electrones
ENUNCIADOS. Cuestiones. Calcule el defecto de masa y la energía total de enlace del isótopo
 ENUNCIADOS Cuestiones 1 a) 15 Calcule el defecto de masa y la energía total de enlace del isótopo 7 N, de masa atómica: 15,0001089 u. b) Calcule la energía de enlace por nucleón. Datos: Masa del protón:
ENUNCIADOS Cuestiones 1 a) 15 Calcule el defecto de masa y la energía total de enlace del isótopo 7 N, de masa atómica: 15,0001089 u. b) Calcule la energía de enlace por nucleón. Datos: Masa del protón:
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
Desintegración radiactiva
 La radiactividad natural fue descubierta por H. Becquerel en 1896. Página 1 Los Curie trabajaron con un mineral (petchblenda) que contenía Uranio además de Bi, Ba y Pb. Marie Sklodowska P 193 " In recognition
La radiactividad natural fue descubierta por H. Becquerel en 1896. Página 1 Los Curie trabajaron con un mineral (petchblenda) que contenía Uranio además de Bi, Ba y Pb. Marie Sklodowska P 193 " In recognition
FÍSICA de 2º de BACHILLERATO FÍSICA NUCLEAR
 FÍSICA de 2º de BACHILLERATO FÍSICA NUCLEAR EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2015) DOMINGO
FÍSICA de 2º de BACHILLERATO FÍSICA NUCLEAR EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2015) DOMINGO
ME4010: Introducción a la Ingeniería Nuclear
 : Introducción a la Ingeniería Nuclear Sergio Courtin V. Marzo 2016 Departamento de Ingeniería Mecánica FCFM - Universidad de Chile Estabilidad Nuclear Los nucleidos que se encuentran en la naturaleza
: Introducción a la Ingeniería Nuclear Sergio Courtin V. Marzo 2016 Departamento de Ingeniería Mecánica FCFM - Universidad de Chile Estabilidad Nuclear Los nucleidos que se encuentran en la naturaleza
Hoja de Problemas 7. Física Nuclear y Física de Partículas.
 Hoja de Problemas 7. Física Nuclear y Física de Partículas. Fundamentos de Física III. Grado en Física. Curso 2015/2016. Grupo 516. UAM. 27-04-2016 Problema 1 La constante de decaimiento del 22 Na es 0.266
Hoja de Problemas 7. Física Nuclear y Física de Partículas. Fundamentos de Física III. Grado en Física. Curso 2015/2016. Grupo 516. UAM. 27-04-2016 Problema 1 La constante de decaimiento del 22 Na es 0.266
FÍSICA NUCLEAR. 3 1 H + 3 1H 4 2He n 1.13*10 7 ev
 FÍSICA NUCLEAR SEPTIEMBRE 1998: 1.- Las masas atómicas del 7 4Be y del 9 4Be son 7.01693 u y 9.012183 u respectivamente, determinar cuál es más estable. 9 4Be Masas atómicas. 1 0n = 1.008665 u; 1 1H =
FÍSICA NUCLEAR SEPTIEMBRE 1998: 1.- Las masas atómicas del 7 4Be y del 9 4Be son 7.01693 u y 9.012183 u respectivamente, determinar cuál es más estable. 9 4Be Masas atómicas. 1 0n = 1.008665 u; 1 1H =
Física Nuclear Preguntas de Opción Múltiple
 Física Nuclear Preguntas de Opción Múltiple PSI Física Nombre: 1. Un elemento químico desconocido se representa como: Z X. Cuál es el nombre de Z? A. Número de masa atómica B. Número atómico C. Número
Física Nuclear Preguntas de Opción Múltiple PSI Física Nombre: 1. Un elemento químico desconocido se representa como: Z X. Cuál es el nombre de Z? A. Número de masa atómica B. Número atómico C. Número
Física Moderna. Profesor: Ignacio J. General. 2 do cuatrimestre 2017 Escuela de Ciencia y Tecnología UNSAM
 Física Moderna Profesor: Ignacio J. General 2 do cuatrimestre 2017 Escuela de Ciencia y Tecnología UNSM Física Moderna Radiactividad Corral cuántico By Julian Voss-ndreae - Own work, CC BY-S 3.0, https://commons.wikimedia.org/w/index.php?curid=17273241
Física Moderna Profesor: Ignacio J. General 2 do cuatrimestre 2017 Escuela de Ciencia y Tecnología UNSM Física Moderna Radiactividad Corral cuántico By Julian Voss-ndreae - Own work, CC BY-S 3.0, https://commons.wikimedia.org/w/index.php?curid=17273241
E m c 2, J 1751,52 MeV. 7,453 MeV. E m c 1, J 112,86 MeV. 7,524 MeV
 1. El 235 92U tiene una masa de 235,4393 u. Calcular el defecto de masa y la energía de enlace. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,189 u. Datos: 1 u =
1. El 235 92U tiene una masa de 235,4393 u. Calcular el defecto de masa y la energía de enlace. Calcular la energía de enlace por nucleón del isótopo 15 N sabiendo que su masa es 15,189 u. Datos: 1 u =
Física Nuclear y Reacciones Nucleares
 Slide 1 / 34 Física Nuclear y Reacciones Nucleares El Núcleo Slide 2 / 34 Protón: La carga de un protón es 1,6 x10-19 C. La masa de un protón es 1,6726x10-27 kg. Neutrones: El neutrón es neutro. La masa
Slide 1 / 34 Física Nuclear y Reacciones Nucleares El Núcleo Slide 2 / 34 Protón: La carga de un protón es 1,6 x10-19 C. La masa de un protón es 1,6726x10-27 kg. Neutrones: El neutrón es neutro. La masa
Slide 1 / 34. Física Nuclear y Reacciones Nucleares
 Slide 1 / 34 Física Nuclear y Reacciones Nucleares Slide 2 / 34 El Núcleo Protón: La carga de un protón es 1,6 x10-19 C. La masa de un protón es 1,6726x10-27 kg. Neutrones: El neutrón es neutro. La masa
Slide 1 / 34 Física Nuclear y Reacciones Nucleares Slide 2 / 34 El Núcleo Protón: La carga de un protón es 1,6 x10-19 C. La masa de un protón es 1,6726x10-27 kg. Neutrones: El neutrón es neutro. La masa
4º E.S.O. FÍSICA Y QUÍMICA 2. ÁTOMOS Y SISTEMA PERIÓDICO. Dpto. de Física y Química. R. Artacho
 4º E.S.O. FÍSICA Y QUÍMICA 2. ÁTOMOS Y SISTEMA PERIÓDICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Las partículas y el átomo 2. Modelos atómicos 3. Distribución de los electrones en un
4º E.S.O. FÍSICA Y QUÍMICA 2. ÁTOMOS Y SISTEMA PERIÓDICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Las partículas y el átomo 2. Modelos atómicos 3. Distribución de los electrones en un
Física Nuclear y Reacciones Nucleares Problemas de Práctica
 Slide 1 / 58 Física Nuclear y Reacciones Nucleares Problemas de Práctica Slide 2 / 58 Multiopción Slide 3 / 58 1 El núcleo atómico se compone de: A B C D E electrones protones protones y electrones protones
Slide 1 / 58 Física Nuclear y Reacciones Nucleares Problemas de Práctica Slide 2 / 58 Multiopción Slide 3 / 58 1 El núcleo atómico se compone de: A B C D E electrones protones protones y electrones protones
Relación Problemas Tema 10: Física Nuclear
 Relación Problemas Tema 10: Física Nuclear Cuestiones y Problemas 35 1.- El Cloro tiene dos isótopos naturales. El 75,53% de los átomos es de 17Cl, cuya masa es de 34,96885 uma, y el 24,47% restante de
Relación Problemas Tema 10: Física Nuclear Cuestiones y Problemas 35 1.- El Cloro tiene dos isótopos naturales. El 75,53% de los átomos es de 17Cl, cuya masa es de 34,96885 uma, y el 24,47% restante de
Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA
 Física P.A.U. FÍSICA MODERNA FÍSICA MODERNA PROBLEMAS MECÁNICA CUÁNTICA.. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 5 nm, el potencial de frenado para los electrones
Física P.A.U. FÍSICA MODERNA FÍSICA MODERNA PROBLEMAS MECÁNICA CUÁNTICA.. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 5 nm, el potencial de frenado para los electrones
Conceptos Básicos de la Energía Nuclear
 Conceptos Básicos de la Energía Nuclear El átomo En la naturaleza el átomo más simple que hay es el hidrógeno, cuenta con un protón y un electrón. Por tanto, para explicar el resto de los átomos, ha de
Conceptos Básicos de la Energía Nuclear El átomo En la naturaleza el átomo más simple que hay es el hidrógeno, cuenta con un protón y un electrón. Por tanto, para explicar el resto de los átomos, ha de
Modelo atómico de Thomson
 Modelo atómico de Dalton. Ésta es la primera teoría científica que considera que la materia está dividida en átomos Modelo atómico de Thomson Introduce la idea de que el átomo puede dividirse en las llamadas
Modelo atómico de Dalton. Ésta es la primera teoría científica que considera que la materia está dividida en átomos Modelo atómico de Thomson Introduce la idea de que el átomo puede dividirse en las llamadas
MODELOS ATÓMICOS 2ª PARTE
 MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
---- Debe indicarse claramente nombres y números de lista de los alumnos integrantes del grupo.
 LICEO Confederación Suiza SECTOR: Química GUÍA DE APRENDIZAJE NIVEL: 4 Medio PROFESOR(A): Genny Astudillo Castillo UNIDAD TEMÁTICA: Química Nuclear CONTENIDO: Fisión y fusión nuclear OBJETIVO DE APRENDIZAJE:
LICEO Confederación Suiza SECTOR: Química GUÍA DE APRENDIZAJE NIVEL: 4 Medio PROFESOR(A): Genny Astudillo Castillo UNIDAD TEMÁTICA: Química Nuclear CONTENIDO: Fisión y fusión nuclear OBJETIVO DE APRENDIZAJE:
a) La constante de desintegración radiactiva. b) La actividad inicial de la muestra. c) La masa que quedará sindesintegrar después de años.
 Capítulo 1 SEMINARIO FÍSICA NUCLEAR 1. Si un núcleo de 6 3Li reacciona con un núcleo de un determinado elemento X, se producen dos partículas α. Escribe la reacción y determina el número atómico y elnúmeromásico
Capítulo 1 SEMINARIO FÍSICA NUCLEAR 1. Si un núcleo de 6 3Li reacciona con un núcleo de un determinado elemento X, se producen dos partículas α. Escribe la reacción y determina el número atómico y elnúmeromásico
Teoría atómica de Dalton (1803)
 EL ÁTOMO DIVISIBLE El átomo Desde los tiempos de la antigua Grecia,los pensadores se preguntaban cómo estaba constituida la materia en su interior? Demócrito (S.V a.c.) introduce el término de átomo como
EL ÁTOMO DIVISIBLE El átomo Desde los tiempos de la antigua Grecia,los pensadores se preguntaban cómo estaba constituida la materia en su interior? Demócrito (S.V a.c.) introduce el término de átomo como
BLOQUE 5.2 FÍSICA NUCLEAR
 BLOQUE 5. FÍSIC NUCLER -EL NÚCLEO TÓMICO El núcleo de los átomos se acepta universalmente que está formado por PROTONES y NEUTRONES (llamados genéricamente NUCLEONES), en una cantidad que varía de unos
BLOQUE 5. FÍSIC NUCLER -EL NÚCLEO TÓMICO El núcleo de los átomos se acepta universalmente que está formado por PROTONES y NEUTRONES (llamados genéricamente NUCLEONES), en una cantidad que varía de unos
FÍSICA NUCLEAR. Física 2º bachillerato Física nuclear 1
 FÍSICA NUCLEAR 1. Radioactividad. 2. Desintegración radioactiva. 3. El nucleo. 4. Las reacciones nucleares. 5. Partículas elementales. 6. Interacciones y unificación. Física 2º bachillerato Física nuclear
FÍSICA NUCLEAR 1. Radioactividad. 2. Desintegración radioactiva. 3. El nucleo. 4. Las reacciones nucleares. 5. Partículas elementales. 6. Interacciones y unificación. Física 2º bachillerato Física nuclear
Tema 8. Radiactividad. Fundamento físico de la atenuación de las radiaciones ionizantes
 Tema 8. Radiactividad Fundamento físico de la atenuación de las radiaciones ionizantes Qué es la radiactividad? Estructura de la materia - - NÚCLEO (Z y N) + + + + + - - electrones: q e = -1,6 10 19 C
Tema 8. Radiactividad Fundamento físico de la atenuación de las radiaciones ionizantes Qué es la radiactividad? Estructura de la materia - - NÚCLEO (Z y N) + + + + + - - electrones: q e = -1,6 10 19 C
El átomo MODELOS ATÓMICOS
 El átomo Es la porción más pequeña de la materia. Los primeros en utilizar este término fueron Leucipo y Demócrito (los atomistas), quienes creían que la materia estaba formados por pequeñas partículas
El átomo Es la porción más pequeña de la materia. Los primeros en utilizar este término fueron Leucipo y Demócrito (los atomistas), quienes creían que la materia estaba formados por pequeñas partículas
Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA
 Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA PROBLEMAS EFECTO FOTOELÉCTRICO 1. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 175 nm, el potencial de frenado para
Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA PROBLEMAS EFECTO FOTOELÉCTRICO 1. En una célula fotoeléctrica, el cátodo metálico se ilumina con una radiación de λ = 175 nm, el potencial de frenado para
Modelo de Thomson Modelo de Rutherford. Estructura atómica. José Mariano Lucena Cruz 10 de mayo de 2010
 José Mariano Lucena Cruz chenalc@gmail.com 10 de mayo de 2010 Propiedades periódicas Aquellas cuyo valor se puede estimar según la posición que ocupen los elementos en la tabla periódica. Estas son: Tamaño
José Mariano Lucena Cruz chenalc@gmail.com 10 de mayo de 2010 Propiedades periódicas Aquellas cuyo valor se puede estimar según la posición que ocupen los elementos en la tabla periódica. Estas son: Tamaño
25 12 Mg. 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores.
 MINIPRUEBA CLASE 02 25 12 Mg 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores. 25 12 Mg Z 2. Se puede afirmar que: I) La masa del electrón es aproximadamente
MINIPRUEBA CLASE 02 25 12 Mg 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores. 25 12 Mg Z 2. Se puede afirmar que: I) La masa del electrón es aproximadamente
EL ÁTOMO. Departamento de Física y Química 3º ESO
 EL ÁTOMO Departamento de Física y Química 3º ESO 0. Mapa conceptual Metales No metales Tabla periódica Elementos Cationes Isótopos ÁTOMO Iones Aniones Protones Núcleo Neutrones Electrones Número atómico
EL ÁTOMO Departamento de Física y Química 3º ESO 0. Mapa conceptual Metales No metales Tabla periódica Elementos Cationes Isótopos ÁTOMO Iones Aniones Protones Núcleo Neutrones Electrones Número atómico
Tema 1: Núcleo atómico y Desintegración
 Tema 1: Núcleo atómico y Desintegración Núcleo atómico. Radiactividad. Modos de Decaimiento N ú c l e o t ó m i c o El núcleo atómico es la parte del átomo que contiene toda la carga positiva y la mayoría
Tema 1: Núcleo atómico y Desintegración Núcleo atómico. Radiactividad. Modos de Decaimiento N ú c l e o t ó m i c o El núcleo atómico es la parte del átomo que contiene toda la carga positiva y la mayoría
Unidad II 2.1 Estructura del átomo
 Unidad II 2.1 Estructura del átomo Química general I Alfonso Rito Norma López 1 El átomo en la antigüedad Demócrito introdujo el concepto de átomo, como la constitución de la materia por partículas indivisibles.
Unidad II 2.1 Estructura del átomo Química general I Alfonso Rito Norma López 1 El átomo en la antigüedad Demócrito introdujo el concepto de átomo, como la constitución de la materia por partículas indivisibles.
QUIMICA GENERAL. Docente : Raquel Villafrades Torres
 Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
