Formato para prácticas de laboratorio
|
|
|
- Carmen Farías Martínez
- hace 6 años
- Vistas:
Transcripción
1 Fecha de efectividad: Formato para prácticas de laboratorio CARRERA PLAN DE ESTUDIO CLAVE DE UNIDAD DE APRENDIZAJE NOMBRE DE LA UNIDAD DE APRENDIZAJE Industrial Materiales de ingeniería PRÁCTICA No. 7 LABORATORIO DE NOMBRE DE LA PRÁCTICA COMPUTO INGENIERIA INDUSTRIAL DURACIÓN (HORAS) Corrosión I y II INTRODUCCIÓN En la fabricación de cierto tipo de estructuras o productos metálicos, se utilizan metales sacrificio. En esta práctica se constatará el uso de ellos como protección contra la corrosión provocada por el contacto con sustancias que favorecen la oxidación del hierro. 2. OBJETIVO (COMPETENCIA) Identificar las ventajas y desventajas del uso de recubrimientos para entender su importancia en la industria, por medio de la inspección visual de partes, con un enfoque preventivo, verificando los efectos de la corrosión en los materiales. 3. FUNDAMENTO La composición y la integridad física de un material solido se alteran en un ambiente corrosivo. Si se trata de la corrosión química, un líquido corrosivo disuelve el material. En la corrosión electroquímica se retiran átomos del metal del material solido como resultado de un circuito eléctrico producido. Los metales y ciertos materiales cerámicos reaccionan en un ambiente gaseoso, por lo general a temperaturas elevadas, y el material puede destruirse debido a la formación de óxidos y otros compuestos. Los polímeros se degradan al ser expuestos al Formuló Revisó Aprobó Autorizó Maestro Responsable de Programa Educativo Página 1 de 5 Responsable de Gestión de Calidad Director de la Facultad Código: GC-N4-017 Revisión: 3
2 oxigeno a temperaturas elevadas. Los materiales pueden alterarse si se les exponen a la radiación o incluso a las bacterias. El proceso de la corrosión se presenta con la finalidad de reducir el nivel de energía libre de un sistema; ocurre a lo largo de un periodo ya sea a altas o a bajas temperaturas. El secreto para impedir la corrosión consiste en colocar un recubrimiento que evite el contacto con el reactante o aplicar una fuerza impulsora en oposición para reducir la velocidad del proceso. La corrosión química es de especial consideración en muchos sectores incluyendo el transporte (puentes, eleoductos, automóviles, aviones, trenes y barcos) servicios públicos (energía eléctrica, agua, telecomunicaciones y plantas de energía nuclear), así como la producción y manufactura (industria alimenticia, microelectrónica y refinerías de petróleo). Corrosión química En la corrosión química, es decir, en la disolución directa, un material se disuelve en un medio corrosivo líquido. El material seguirá disolviéndose hasta que se consuma totalmente o hasta que se sature el líquido. Las aleaciones base cobre, por ejemplo, desarrollan una pátida verde a causa de la formación de carbonato e hidróxidos de cobre. Ésta es la razón por la cual, por ejemplo, la estatua de la libertad se ve verde. Corrosión electroquímica En la corrosión electroquímica la forma más común de ataques a los metales, se presenta cuando los átomos del metal pierden electrones y se convierten en iones. Conforme el metal se consume gradualmente mediante este proceso, se forma normalmente un subproducto del proceso de la corrosión. La corrosión electroquímica ocurre con mayor frecuencia en un medio acuoso, en donde los iones están presentes en el agua, la tierra o el aire húmedo. En este proceso se crea un circuito eléctrico y el sistema se conoce como celda electroquímica. Protección contra la corrosión electroquímica Se utilizan técnicas para combatir la corrosión, incluyendo el diseño, los recubrimientos, los inhibidores, la protección catódica, la pasivación y la selección de materiales. Diseño.Un adecuado diseño de las estructuras de metal puede retrasar o incluso eliminar la corrosión. Página 2 de 5
3 Pasos para combatir la corrosión. 1. Impedir la formación de celdas galvánicas. Esto se puede lograr utilizando metales o aleaciones similares. Por ejemplo, es frecuente que las tuberías de acero se conecten a los muebles de plomería de latón, lo que produce una celda galvánica que causa la corrosión del acero. Mediante el uso de acoplamientos intermedios plásticos, al aislar eléctricamente el acero del latón, este problema puede minimizarse. 2. Hacer que el área del ánodo sea mucho mayor que la del cátodo. Se pueden utilizar remaches de cobre para sujetar láminas de acero. 3. Diseñe los componentes de modo que los sistemas de fluido estén cerrados y no abiertos, y de manera que no se formen charcos estancados de liquido. Los depósitos parcialmente llenos sufren de corrosión por línea de agua. Los sistemas abiertos disuelven continuamente los gases, produciendo iones que participan en la reacción catódica y que fomentan las celdas de concentración. 4. Evitar hendiduras entre materiales ensamblados o unidos. La soldadura permanente puede resultar una mejor técnica de unión que el latonado, el estaño o la sujeción mecánica. La corrosión puede definirse como el deterioro de un metal producido por el ataque químico de su ambiente. Puesto que la corrosión es una reacción química, la velocidad a la cual ocurre dependerá hasta cierto punto de la temperatura y de la concentración de los reactivos y productos. Otros factores como el esfuerzo mecánico y la erosión también pueden contribuir a la corrosión. Cuando se habla de la corrosión, es usual referirse al proceso del ataque químico sobre los metales. Estos son susceptibles a este ataque debido a que tienen electrones libres y pueden establecer celdas electroquímicas dentro de su estructura. La mayoría de los metales son corroídos hasta cierto grado por el agua y la atmósfera. Los metales también pueden ser corroídos por el ataque químico directo de las soluciones químicas e inclusive de metales líquidos. También es posible considerar a la corrosión de los metales en algunas formas como metalurgia extractiva inversa. Página 3 de 5
4 Materiales no metálicos como las cerámicas y los polímeros no sufren el ataque electroquímico pero pueden experimentar un deterioro por ataque químico directo. 4. PROCEDIMIENTO (DESCRIPCIÓN) A) EQUIPO NECESARIO MATERIAL DE APOYO 1 sacapuntas de plástico. 1 sacapuntas de metal. Dos objetos metálicos pequeños (tuercas, N/A tornillos, etc.). Dos recipientes transparentes con tapa (vasos o botes de plástico o vidrio). Sal de cocina. Cuchara para revolver. B) DESARROLLO DE LA PRÁCTICA Procedimiento: 1. Colocar agua en uno de los recipientes y disolver un par de cucharas de sal en él. 2. Sumergir ambos sacapuntas en la solución. 3. Esperar un par de minutos y ver qué sucede. 4. Sacar ambos sacapuntas y observar el estado de las cuchillas y el metal. 5. Volver a colocar ambos sacapuntas dentro del vaso por un par de días y registrar lo que sucede. 6. Colocar agua con dos cucharadas de sal en el otro recipiente. 7. Colocar los otros dos objetos metálicos y registrar lo que sucede del mismo modo que con los sacapuntas. 8. Presentar los resultados ante el grupo. C) CÁLCULOS Y REPORTE Conclusiones: Entregar por equipo un reporte que conteste lo siguiente: 1. Por qué el comportamiento es distinto en ambas sacapuntas? 2. Es semejante el comportamiento en los otros objetos metálicos? Por qué? 3. Todos los equipos obtuvieron el mismo resultado? Por qué? Página 4 de 5
5 5. RESULTADOS Y CONCLUSIONES 6. ANEXOS 7. REFERENCIAS Fundamentos de la ciencia e ingeniería de materiales Cuarta edición William F. Smith Javad Hashemi Ciencia e ingeniería de los materiales Cuarta edición Donald R. Askeland Pradeep P. Phulé Página 5 de 5
Definición El fenómeno corrosión se define como el deterioro de los materiales a causa de alguna reacción con el medio ambiente en que son usados.
 Corrosión Definición El fenómeno corrosión se define como el deterioro de los materiales a causa de alguna reacción con el medio ambiente en que son usados. La corrosión es la destrucción lenta y progresiva
Corrosión Definición El fenómeno corrosión se define como el deterioro de los materiales a causa de alguna reacción con el medio ambiente en que son usados. La corrosión es la destrucción lenta y progresiva
UNIDAD 2. TRATAMIENTOS TÉRMICOS DE LOS ACEROS
 UNIDAD 2. TRATAMIENTOS TÉRMICOS DE LOS ACEROS 1. OXIDACIÓN... Pág. 29 2. CORROSIÓN... Pág. 34 2.1. Corrosión. Reacciones electroquímicas... Pág.34 2.2. Tipos de corrosión... Pág. 40 2.3. Medidas de protección
UNIDAD 2. TRATAMIENTOS TÉRMICOS DE LOS ACEROS 1. OXIDACIÓN... Pág. 29 2. CORROSIÓN... Pág. 34 2.1. Corrosión. Reacciones electroquímicas... Pág.34 2.2. Tipos de corrosión... Pág. 40 2.3. Medidas de protección
Me n+ + O 2- Me a O b
 4. CORROSION Oxidación Me n Me n+ a) Oxidación (con ausencia de humedad) b) Corrosión electroquímica (en ambiente corrosivo) O 2 + n O 2- Me n+ + O 2- Me a O b Fig 4-1 Velocidad de oxidación (dx/dt): temperatura
4. CORROSION Oxidación Me n Me n+ a) Oxidación (con ausencia de humedad) b) Corrosión electroquímica (en ambiente corrosivo) O 2 + n O 2- Me n+ + O 2- Me a O b Fig 4-1 Velocidad de oxidación (dx/dt): temperatura
Formato para prácticas de laboratorio
 Fecha de efectividad: Formato para prácticas de laboratorio CARRERA PLAN DE ESTUDIO CLAVE DE UNIDAD DE APRENDIZAJE NOMBRE DE LA UNIDAD DE APRENDIZAJE Industrial 2007-1 9011 Materiales de ingeniería PRÁCTICA
Fecha de efectividad: Formato para prácticas de laboratorio CARRERA PLAN DE ESTUDIO CLAVE DE UNIDAD DE APRENDIZAJE NOMBRE DE LA UNIDAD DE APRENDIZAJE Industrial 2007-1 9011 Materiales de ingeniería PRÁCTICA
Consulte nuestra página web: En ella encontrará el catálogo completo y comentado
 Ensayos físicos Consulte nuestra página web: www.sintesis.com En ella encontrará el catálogo completo y comentado Ensayos físicos Xoán Carlos Rodríguez García Xoán Carlos Rodríguez García EDITORIAL SÍNTESIS,
Ensayos físicos Consulte nuestra página web: www.sintesis.com En ella encontrará el catálogo completo y comentado Ensayos físicos Xoán Carlos Rodríguez García Xoán Carlos Rodríguez García EDITORIAL SÍNTESIS,
Efectos de corrosión y acumulación de residuos solidos en las superficies de contactos electrónicos
 Efectos de corrosión y acumulación de residuos solidos en las superficies de contactos electrónicos 1. Que es la corrosión? 2. Qué causa la corrosión en los equipos electrónicos? 3. Tipos de corrosión
Efectos de corrosión y acumulación de residuos solidos en las superficies de contactos electrónicos 1. Que es la corrosión? 2. Qué causa la corrosión en los equipos electrónicos? 3. Tipos de corrosión
Reacciones redox espontáneas
 Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA
 Trabajo Práctico Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA UNIVERSIDAD TECNOLÓGICA NACIONAL Regional Rosario En el presente se desarrolla una propuesta de trabajo práctico para realizar con los estudiantes
Trabajo Práctico Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA UNIVERSIDAD TECNOLÓGICA NACIONAL Regional Rosario En el presente se desarrolla una propuesta de trabajo práctico para realizar con los estudiantes
Unidad 6: ELECTROQUIMICA
 Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Tecnólogo en Minería Química I. PRÁCTICO DE LABORATORIO Reacciones Redox
 Tecnólogo en Minería Química I PRÁCTICO DE LABORATORIO Reacciones Redox I. INTRODUCCIÓN Las reacciones redox se encuentran entre las reacciones más comunes. Son aquellas que involucran la transferencia
Tecnólogo en Minería Química I PRÁCTICO DE LABORATORIO Reacciones Redox I. INTRODUCCIÓN Las reacciones redox se encuentran entre las reacciones más comunes. Son aquellas que involucran la transferencia
Corrosion. Tecnología de los Materiales Metálicos
 Corrosion Tecnología de los Materiales Metálicos La causa principal de todas las reacciones entre los metales y el medio ambiente es una disminución de la energía libre del sistema como resultado de la
Corrosion Tecnología de los Materiales Metálicos La causa principal de todas las reacciones entre los metales y el medio ambiente es una disminución de la energía libre del sistema como resultado de la
OXIDACIÓN Y CORROSIÓN
 OXIDACIÓN Y CORROSIÓN Tecnología Industrial II Índice 1. OXIDACIÓN... 1 1.1. Velocidad de oxidación... 1 1.2. Protección contra la oxidación... 4 2. CORROSIÓN... 4 2.1. Reacciones electroquímicas... 4
OXIDACIÓN Y CORROSIÓN Tecnología Industrial II Índice 1. OXIDACIÓN... 1 1.1. Velocidad de oxidación... 1 1.2. Protección contra la oxidación... 4 2. CORROSIÓN... 4 2.1. Reacciones electroquímicas... 4
1.2.- Factores que propician la Corrosión. M. En C. José Antonio González Moreno Enero del 2016 Ensayos Destructivos
 1.2.- Factores que propician la Corrosión M. En C. José Antonio González Moreno Enero del 2016 Ensayos Destructivos Introducción: En esta presentación, se estudiarán los factores básicos que generan o
1.2.- Factores que propician la Corrosión M. En C. José Antonio González Moreno Enero del 2016 Ensayos Destructivos Introducción: En esta presentación, se estudiarán los factores básicos que generan o
Ramírez García Pablo Torre Valenzuela Aldo Pérez Castañeda Alma Leticia 11/11/13
 Ramírez García Pablo Torre Valenzuela Aldo Pérez Castañeda Alma Leticia 11/11/13 Qué es la corrosión? Se denomina corrosión al ataque destructivo que sufre un material generalmente metálico por reacción
Ramírez García Pablo Torre Valenzuela Aldo Pérez Castañeda Alma Leticia 11/11/13 Qué es la corrosión? Se denomina corrosión al ataque destructivo que sufre un material generalmente metálico por reacción
ANODOS DE SACRIFICIO ÁNODOS DE SACRIFICIO
 ANODOS DE SACRIFICIO Protección catódica galvánica para todo tipo de aplicaciones, tanto para protección interna como externa de estructuras metálicas, tanques, pilonas de pantalanes, etc. ÁNODOS DE SACRIFICIO
ANODOS DE SACRIFICIO Protección catódica galvánica para todo tipo de aplicaciones, tanto para protección interna como externa de estructuras metálicas, tanques, pilonas de pantalanes, etc. ÁNODOS DE SACRIFICIO
CORROSION. J. M. Arroyo Rosa Página 2
 CORROSION La corrosión es la interacción de un metal con el medio que lo rodea, produciendo el consiguiente deterioro en sus propiedades tanto físicas como químicas. La característica fundamental de este
CORROSION La corrosión es la interacción de un metal con el medio que lo rodea, produciendo el consiguiente deterioro en sus propiedades tanto físicas como químicas. La característica fundamental de este
MATERIALES INDUSTRIALES II. Capitulo 4 CORROSION
 MATERIALES INDUSTRIALES II Capitulo 4 1 introducción RADIACION CALOR DEGRADACION AGRESION QUIMICA ácidos,álcalis y solventes ( polímeros ) ACUOSA agua pura Oxígeno disuelto 2 medición n de la velocidad
MATERIALES INDUSTRIALES II Capitulo 4 1 introducción RADIACION CALOR DEGRADACION AGRESION QUIMICA ácidos,álcalis y solventes ( polímeros ) ACUOSA agua pura Oxígeno disuelto 2 medición n de la velocidad
TEMA-11 Electroquímica
 QUÍMICA I TEMA-11 Electroquímica Tecnólogo en Minería 1 I n t r o d u c c i ó n Electroquímica Fenómenos eléctricos Fenómenos químicos 2 I n t r o d u c c i ó n Electroquímica Fenómenos eléctricos Fenómenos
QUÍMICA I TEMA-11 Electroquímica Tecnólogo en Minería 1 I n t r o d u c c i ó n Electroquímica Fenómenos eléctricos Fenómenos químicos 2 I n t r o d u c c i ó n Electroquímica Fenómenos eléctricos Fenómenos
CORROSIÓN EN LA INDUSTRIA DE ALIMENTOS
 CORROSIÓN EN LA INDUSTRIA DE ALIMENTOS PARTE I 1. Introducción El acero inoxidable es utilizado extensamente en la fabricación de equipos de proceso en la industria de alimentos, por su resistencia mecánica,
CORROSIÓN EN LA INDUSTRIA DE ALIMENTOS PARTE I 1. Introducción El acero inoxidable es utilizado extensamente en la fabricación de equipos de proceso en la industria de alimentos, por su resistencia mecánica,
CORROSION EN METALES. Ing. Lilian Eperjesi
 CORROSION EN METALES Qué es la Corrosión? La corrosión es la degradación que experimentan los materiales por la acción del medio que los rodea. Se puede hablar de corrosión en: - metales - hormigón - ladrillos
CORROSION EN METALES Qué es la Corrosión? La corrosión es la degradación que experimentan los materiales por la acción del medio que los rodea. Se puede hablar de corrosión en: - metales - hormigón - ladrillos
Deterioro de Materiales
 TEMA VII Deterioro de Materiales LECCIÓN 9 Oxidación y Corrosión 1 9.1 INTRODUCCIÓN Deterioro de un material por interacción química con su entorno: - Oxidación: reacción del material con el oxígeno atmosférico
TEMA VII Deterioro de Materiales LECCIÓN 9 Oxidación y Corrosión 1 9.1 INTRODUCCIÓN Deterioro de un material por interacción química con su entorno: - Oxidación: reacción del material con el oxígeno atmosférico
Serie de potenciales de reducción estándar
 Tabla 26 Cerámicas comunes usados en materiales compuestos de matriz cerámica Capítulo 9 Corrosión 1.9. Corrosión química y electroquímica 1.9.1. Serie de potenciales de reducción estándar 88 Tabla 27
Tabla 26 Cerámicas comunes usados en materiales compuestos de matriz cerámica Capítulo 9 Corrosión 1.9. Corrosión química y electroquímica 1.9.1. Serie de potenciales de reducción estándar 88 Tabla 27
Serie de potenciales de reducción estándar
 Tabla 26 Cerámicas comunes usados en materiales compuestos de matriz cerámica Capítulo 9 Corrosión 1.9. Corrosión química y electroquímica 1.9.1. Serie de potenciales de reducción estándar 101 Tabla 27
Tabla 26 Cerámicas comunes usados en materiales compuestos de matriz cerámica Capítulo 9 Corrosión 1.9. Corrosión química y electroquímica 1.9.1. Serie de potenciales de reducción estándar 101 Tabla 27
Materiales y su aplicación. Clasificación de los materiales La manera más general de clasificación de los materiales es la siguiente:
 Materiales y su aplicación Clasificación de los materiales La manera más general de clasificación de los materiales es la siguiente: Metálicos Ferrosos Los principales productos representantes de los materiales
Materiales y su aplicación Clasificación de los materiales La manera más general de clasificación de los materiales es la siguiente: Metálicos Ferrosos Los principales productos representantes de los materiales
2.5 CORROSIÓN ELECTROQUÍMICA
 2.5 CORROSIÓN ELECTROQUÍMICA La corrosión es un proceso electroquímico en el cual un metal reacciona con su medio ambiente para formar óxido o algún otro compuesto. Este proceso está formado esencialmente
2.5 CORROSIÓN ELECTROQUÍMICA La corrosión es un proceso electroquímico en el cual un metal reacciona con su medio ambiente para formar óxido o algún otro compuesto. Este proceso está formado esencialmente
OXIDACIÓN-REDUCCIÓN. PAU-tipos de problemas
 OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
Cómo se corroe el acero en el agua marina?
 Cómo se corroe el acero en el agua marina? Para entender la protección catódica, primero debemos entender el mecanismo de corrosión. Para que ocurra corrosión, se deben cumplir tres condiciones. 1. Dos
Cómo se corroe el acero en el agua marina? Para entender la protección catódica, primero debemos entender el mecanismo de corrosión. Para que ocurra corrosión, se deben cumplir tres condiciones. 1. Dos
PROTECCIÓN CATÓDICA DEFINICIÒN. MECANISMOS DE CORROSION.
 DANIEL HIDALGO DEFINICIÒN. MECANISMOS DE CORROSION. Se entiende por corrosión, todo proceso electro-químico de degradación por oxidación-reducción de los materiales de construcción de tanques, tuberías
DANIEL HIDALGO DEFINICIÒN. MECANISMOS DE CORROSION. Se entiende por corrosión, todo proceso electro-químico de degradación por oxidación-reducción de los materiales de construcción de tanques, tuberías
INDICE. XIII Acera del autor. XVII Sistema de unidades y símbolos usados en este texto
 INDICE Prefacio XIII Acera del autor XVII Sistema de unidades y símbolos usados en este texto XVIII 1 Introducción 1 1.1. Qué es manufactura? 3 1.2. los materiales en la manufactura 9 1.3. Procesos de
INDICE Prefacio XIII Acera del autor XVII Sistema de unidades y símbolos usados en este texto XVIII 1 Introducción 1 1.1. Qué es manufactura? 3 1.2. los materiales en la manufactura 9 1.3. Procesos de
CORROSIÓN PARA PRINCIPIANTES (2 de 2)
 Página 1 de 7 Si usted no puede visualizar correctamente este mensaje, presione aquí Medellín, 20 de marzo de 2009 Boletín técnico de INDISA S.A. No. 69 CORROSIÓN PARA PRINCIPIANTES (2 de 2) Ver la primera
Página 1 de 7 Si usted no puede visualizar correctamente este mensaje, presione aquí Medellín, 20 de marzo de 2009 Boletín técnico de INDISA S.A. No. 69 CORROSIÓN PARA PRINCIPIANTES (2 de 2) Ver la primera
QUÍMICA INORGÁNICA ELECTROQUIMICA CUESTIONARIO Y RESPUESTAS
 1 QUÍMICA INORGÁNICA ELECTROQUIMICA CUESTIONARIO Y RESPUESTAS 1. De qué se ocupa la electroquímica? Qué tipos de reacciones intervienen en los procesos electroquímicos? La ELECTROQUIMICA se ocupa de los
1 QUÍMICA INORGÁNICA ELECTROQUIMICA CUESTIONARIO Y RESPUESTAS 1. De qué se ocupa la electroquímica? Qué tipos de reacciones intervienen en los procesos electroquímicos? La ELECTROQUIMICA se ocupa de los
1).- La siguiente figura representa a una pila: I. galvánica. II. electrolítica. III. seca
 1).- La siguiente figura representa a una pila: I. galvánica. II. electrolítica. III. seca A) Solo I B) Solo II C) Solo III D) Solo I y III E) Solo II y III 2).- Aprovecha una reacción redox espontánea
1).- La siguiente figura representa a una pila: I. galvánica. II. electrolítica. III. seca A) Solo I B) Solo II C) Solo III D) Solo I y III E) Solo II y III 2).- Aprovecha una reacción redox espontánea
4. Un agente oxidante (2 correctas) A) Toma electrones de otra sustancia B) Da electrones a otra sustancia C) Se oxida D) Se reduce
 CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
Materiales-G704/G742. Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García. Lección 9. Oxidación y corrosión
 -G704/G742 Lección 9. Oxidación y corrosión Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García Departamento de Ciencia e Ingeniería del Terreno y de los Este tema
-G704/G742 Lección 9. Oxidación y corrosión Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García Departamento de Ciencia e Ingeniería del Terreno y de los Este tema
PRÁCTICA Nº 9 y 10 CORROSIÓN I
 PRÁCTICA Nº 9 y 10 CORROSIÓN I OBJETO DE LA PRÁCTICA: CONCEPTO DE ÁNODO Y CÁTODO APLICACIÓN A TRES REACCIONES REDOX CONCEPTO DE ENERGÍA ELÉCTRICA ASOCIADA A CAMBIOS QUÍMICOS Y VICEVERSA REACCIÓN ESPONTÁNEA
PRÁCTICA Nº 9 y 10 CORROSIÓN I OBJETO DE LA PRÁCTICA: CONCEPTO DE ÁNODO Y CÁTODO APLICACIÓN A TRES REACCIONES REDOX CONCEPTO DE ENERGÍA ELÉCTRICA ASOCIADA A CAMBIOS QUÍMICOS Y VICEVERSA REACCIÓN ESPONTÁNEA
TEMA 7.- Fallas de materiales: CORROSIÓN. Conceptos Básicos Tipos
 TEMA 7.- Fallas de materiales: CORROSIÓN Conceptos Básicos Tipos CORROSIÓN La corrosión puede ser definida como la destrucción de un sólido debido a la acción química o electroquímica que comienza en la
TEMA 7.- Fallas de materiales: CORROSIÓN Conceptos Básicos Tipos CORROSIÓN La corrosión puede ser definida como la destrucción de un sólido debido a la acción química o electroquímica que comienza en la
Celda de combustible AFC casera
 Propuesta de construcción de pila de pila AFC casera: Se trata de conseguir producir la reacción electroquímica de manera económica y sencilla para obtener energía a partir de hidrógeno y oxígeno. Para
Propuesta de construcción de pila de pila AFC casera: Se trata de conseguir producir la reacción electroquímica de manera económica y sencilla para obtener energía a partir de hidrógeno y oxígeno. Para
TEMA 3: Equilibrios redox
 TEMA 3: Equilibrios redox Índice 1) Concepto potencial redox. 2) Pila galvánica. 3) Ecuación de Nernst. 4) Espontaneidad y equilibrio. 5) Influencia del ph en el potencial de electrodo. 6) Reacciones de
TEMA 3: Equilibrios redox Índice 1) Concepto potencial redox. 2) Pila galvánica. 3) Ecuación de Nernst. 4) Espontaneidad y equilibrio. 5) Influencia del ph en el potencial de electrodo. 6) Reacciones de
OXIDACIÓN-REDUCCIÓN. PAU-tipos de problemas
 OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
Electroquímic a a tu alcance
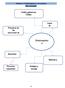 Práctica 2. Electroquímica a tu alcance Mapa conceptual Celdas galvánicas Celdas electroquímicas Principios de las reacciones de óxido reducción Leyes de Faraday Electroquímic a a tu alcance Electrólisi
Práctica 2. Electroquímica a tu alcance Mapa conceptual Celdas galvánicas Celdas electroquímicas Principios de las reacciones de óxido reducción Leyes de Faraday Electroquímic a a tu alcance Electrólisi
OXIDACIÓN Y CORROSIÓN. Julio Alberto Aguilar Schafer
 OXIDACIÓN Y CORROSIÓN Julio Alberto Aguilar Schafer Industria o sector Coste estimado (millones de libras) Ahorro potencial estimado (millones de libras) Construcción 250 ($190.000.000.000) 50 ($38.000.000.000)
OXIDACIÓN Y CORROSIÓN Julio Alberto Aguilar Schafer Industria o sector Coste estimado (millones de libras) Ahorro potencial estimado (millones de libras) Construcción 250 ($190.000.000.000) 50 ($38.000.000.000)
1. Formación de núcleos estables en el fundido. ( Nucleacion ).
 PROPIEDADES DE LOS MATERIALES. UNIDAD. IMPERFECCIONES EN SOLIDOS. Proceso de Solidificación. Es un proceso físico que consiste en el cambio de estado de materia de líquido a solido producido por la disminución
PROPIEDADES DE LOS MATERIALES. UNIDAD. IMPERFECCIONES EN SOLIDOS. Proceso de Solidificación. Es un proceso físico que consiste en el cambio de estado de materia de líquido a solido producido por la disminución
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
QUÍMICA Reactividad y equilibrio químico. Oxido - reducción. Tutora: Romina Saavedra
 QUÍMICA Reactividad y equilibrio químico Oxido - reducción Tutora: Romina Saavedra Balance de reacciones de óxido reducción Una reacción redox o de óxido reducción se caracteriza por la existencia de dos
QUÍMICA Reactividad y equilibrio químico Oxido - reducción Tutora: Romina Saavedra Balance de reacciones de óxido reducción Una reacción redox o de óxido reducción se caracteriza por la existencia de dos
REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox) 1 2 Tipos de reacciones redox (según su espontaneidad) Reacciones espontáneas: G
REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox) 1 2 Tipos de reacciones redox (según su espontaneidad) Reacciones espontáneas: G
Cambios en la Materia. Sra. Anlinés Sánchez Otero
 Cambios en la Materia Sra. Anlinés Sánchez Otero Cambios en la Materia Cambios Físicos Químicos Cambios Físicos Alteran la sustancia sin modificar su composición. Se utilizan para separar mezclas e identificar
Cambios en la Materia Sra. Anlinés Sánchez Otero Cambios en la Materia Cambios Físicos Químicos Cambios Físicos Alteran la sustancia sin modificar su composición. Se utilizan para separar mezclas e identificar
Práctica 5: Termoquímica: Celdas galvánicas
 Práctica 5: Termoquímica: Celdas galvánicas Ingeniería agrónoma grado en hortofruticultura y jardinería Jorge Cerezo Martínez Objetivos Construir, varias celdas galvánicas o voltaicas y medir el potencial
Práctica 5: Termoquímica: Celdas galvánicas Ingeniería agrónoma grado en hortofruticultura y jardinería Jorge Cerezo Martínez Objetivos Construir, varias celdas galvánicas o voltaicas y medir el potencial
Realizando una pequeña investigación
 Realizando una pequeña investigación 1. Introducción: Investigación realizada 1.1 Objetivo El Objetivo de esta investigación ha sido estudiar de qué factores depende la corrosión del hierro. 1.2 Hipótesis
Realizando una pequeña investigación 1. Introducción: Investigación realizada 1.1 Objetivo El Objetivo de esta investigación ha sido estudiar de qué factores depende la corrosión del hierro. 1.2 Hipótesis
Fabricación baterías LITIO - POLIMERO
 1 Fabricación baterías LITIO - POLIMERO FABRICACIÓN El proceso general de la fabricación de las baterías de litio polímero se resume en: Aleación del cátodo de litio, generación de un lingote, extrusión,
1 Fabricación baterías LITIO - POLIMERO FABRICACIÓN El proceso general de la fabricación de las baterías de litio polímero se resume en: Aleación del cátodo de litio, generación de un lingote, extrusión,
AISLACION DE CAÑERIAS
 Las cañerías que trabajan a baja temperatura se deben aislar en razón de: Ahorro de energía, Reducción de costos operativos Control de la condensación en la superficie externa Prevenir la condensación
Las cañerías que trabajan a baja temperatura se deben aislar en razón de: Ahorro de energía, Reducción de costos operativos Control de la condensación en la superficie externa Prevenir la condensación
INDICE. Prologo del editor
 INDICE Prologo del editor V Prologo VII 1. Morfologia de los Procesos 1 1.1. Introduccion 1 1.2. Estructura básica de los procesos de manufactura 1 1.2.1. Modelo general de los procesos 2 1.2.2. Estructura
INDICE Prologo del editor V Prologo VII 1. Morfologia de los Procesos 1 1.1. Introduccion 1 1.2. Estructura básica de los procesos de manufactura 1 1.2.1. Modelo general de los procesos 2 1.2.2. Estructura
Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante
 Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante Objetivos: Los estudiantes serán capaces de Definir oxidación y reducción en términos de pérdida o ganancia de electrones. Describir
Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante Objetivos: Los estudiantes serán capaces de Definir oxidación y reducción en términos de pérdida o ganancia de electrones. Describir
I. DATOS DE IDENTIFICACIÓN. 2. Programa (s) de estudio: (Técnico, Licenciatura (s) INGENIERO INDUSTRIAL 3. Vigencia del plan:
 UNIVERSIDAD AUTÓNOMA DE BAJA CALIFORNIA COORDINACIÓN DE FORMACIÓN BÁSICA COORDINACIÓN DE FORMACIÓN PROFESIONAL Y VINCULACIÓN UNIVERSITARIA PROGRAMA DE UNIDAD DE APRENDIZAJE I. DATOS DE IDENTIFICACIÓN 1.
UNIVERSIDAD AUTÓNOMA DE BAJA CALIFORNIA COORDINACIÓN DE FORMACIÓN BÁSICA COORDINACIÓN DE FORMACIÓN PROFESIONAL Y VINCULACIÓN UNIVERSITARIA PROGRAMA DE UNIDAD DE APRENDIZAJE I. DATOS DE IDENTIFICACIÓN 1.
Qué es la corrosión? Principio básico de la corrosión Ánodos y cátodos Proceso electroquímico electroquímico
 Qué es la corrosión? Principio básico de la corrosión Cuando un metal se expone a ciertas condiciones ambientales, tales como agua (incluyendo humedad), productos químicos (ácidos, cáusticos, sales), gases
Qué es la corrosión? Principio básico de la corrosión Cuando un metal se expone a ciertas condiciones ambientales, tales como agua (incluyendo humedad), productos químicos (ácidos, cáusticos, sales), gases
U N I V E R S I D A D D E G U A D A L A J A R A CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERIAS
 U N I V E R S I D A D D E G U A D A L A J A R A CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERIAS D I V I S I Ó N D E I N G E N I E R I A S DEPARTAMENTO DE INGENIERÍA MECÁNICA ELÉCTRICA ACADEMIA DE:
U N I V E R S I D A D D E G U A D A L A J A R A CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERIAS D I V I S I Ó N D E I N G E N I E R I A S DEPARTAMENTO DE INGENIERÍA MECÁNICA ELÉCTRICA ACADEMIA DE:
TITULACIÓN: MÁSTER EN TECNOLOGÍA E INSTRUMENTACIÓN QUÍMICA
 TITULACIÓN: MÁSTER EN TECNOLOGÍA E INSTRUMENTACIÓN QUÍMICA CURSO ACADÉMICO: 2010-2011 GUÍA DOCENTE 1. DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: DETERIORO DE LOS MATERIALES Y SU PREVENCIÓN CÓDIGO 1 : 071923007
TITULACIÓN: MÁSTER EN TECNOLOGÍA E INSTRUMENTACIÓN QUÍMICA CURSO ACADÉMICO: 2010-2011 GUÍA DOCENTE 1. DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: DETERIORO DE LOS MATERIALES Y SU PREVENCIÓN CÓDIGO 1 : 071923007
1.- DATOS DE LA ASIGNATURA. Nombre de la asignatura: Corrosión y degradación de Materiales. Carrera: Ingeniería en Materiales. Clave de la asignatura:
 1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos: Corrosión y degradación de Materiales Ingeniería en Materiales MAC 0506 4 2 10
1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos: Corrosión y degradación de Materiales Ingeniería en Materiales MAC 0506 4 2 10
Paso 2: Escribir las correspondientes semireacciones sin ajustar y. Paso 3: Ajustar en cada semireacción todos los elementos a
 Tema 21 21.1. Reacciones de oxidación-reducción Química y electricidad 21.2. Celdas electroquímicas 21.3. Potencial de electrodo 1 2 21.1. Reacciones de oxidación-reducción (redox) Son reacciones de transferencia
Tema 21 21.1. Reacciones de oxidación-reducción Química y electricidad 21.2. Celdas electroquímicas 21.3. Potencial de electrodo 1 2 21.1. Reacciones de oxidación-reducción (redox) Son reacciones de transferencia
ELECTROQUÍMICA. 1. Conceptos de oxidación-reducción
 ELECTROQUÍMICA 1. Conceptos de oxidación-reducción Oxidación: transformación en la que una especie química pierde electrones o gana oxígeno. Reducción: transformación en la que una especie química gana
ELECTROQUÍMICA 1. Conceptos de oxidación-reducción Oxidación: transformación en la que una especie química pierde electrones o gana oxígeno. Reducción: transformación en la que una especie química gana
Grupo de Investigación: Computación y Sistemas Empotrados. Tema: Electroquímica. Dr. Ernesto Bolaños Rodríguez
 Grupo de Investigación: Computación y Sistemas Empotrados Tema: Electroquímica Dr. Ernesto Bolaños Rodríguez 23 de marzo del 2012 1 Electroquímica Es la rama de la química que estudia la transformación
Grupo de Investigación: Computación y Sistemas Empotrados Tema: Electroquímica Dr. Ernesto Bolaños Rodríguez 23 de marzo del 2012 1 Electroquímica Es la rama de la química que estudia la transformación
Métodos analíticos cuantitativos basados en las propiedades eléctricas de una solución de analito cuando forma parte de una celda electroquímica
 POTENCIOMETRÍA Química electroanalítica Métodos analíticos cuantitativos basados en las propiedades eléctricas de una solución de analito cuando forma parte de una celda electroquímica Electroquímica Conversión
POTENCIOMETRÍA Química electroanalítica Métodos analíticos cuantitativos basados en las propiedades eléctricas de una solución de analito cuando forma parte de una celda electroquímica Electroquímica Conversión
PATOLOGÍA DE LA EDIFICACIÓN 24 CORROSIÓN EN LAS ESTRUCTURAS DE ACERO
 PATOLOGÍA DE LA EDIFICACIÓN 24 CORROSIÓN EN LAS ESTRUCTURAS DE ACERO 1.- GENERALIDADES INTRODUCCIÓN El acero es una aleación o combinación de hierro y carbono (alrededor de 0,05% hasta menos de un 2%),
PATOLOGÍA DE LA EDIFICACIÓN 24 CORROSIÓN EN LAS ESTRUCTURAS DE ACERO 1.- GENERALIDADES INTRODUCCIÓN El acero es una aleación o combinación de hierro y carbono (alrededor de 0,05% hasta menos de un 2%),
LIMPIEZA QUIMICA DE TUBERIAS
 LIMPIEZA QUIMICA DE TUBERIAS INTRODUCCION Las limpiezas químicas consisten habitualmente en la recirculación de un compuesto químico en disolución, con control de temperatura y una velocidad establecida,
LIMPIEZA QUIMICA DE TUBERIAS INTRODUCCION Las limpiezas químicas consisten habitualmente en la recirculación de un compuesto químico en disolución, con control de temperatura y una velocidad establecida,
Prof(a). María Angélica Sánchez Palacios
 Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea,
Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea,
TERMINALES DE CONEXIÓN PARA TOMA DE TIERRA Y SEGURIDAD
 TERMINALES DE CONEXIÓN PARA TOMA DE TIERRA Y SEGURIDAD La importancia de una conexión a tierra correcta en las instalaciones eléctricas La conexión de las instalaciones eléctricas a tierra es fundamental
TERMINALES DE CONEXIÓN PARA TOMA DE TIERRA Y SEGURIDAD La importancia de una conexión a tierra correcta en las instalaciones eléctricas La conexión de las instalaciones eléctricas a tierra es fundamental
a) b) c) d) e) f) g) e) La masa promedio de una muestra representativa de átomos en uma b) La cantidad de protones en el núcleo del átomo
 Instituto Politécnico Nacional -ESIME-UC Depto. de Ingeniería Mecánica Química Básica Guia de Estudio Grupo: 1 M Fecha: Nombre del Alumno: 1. La masa atómica de un elemento representa: a) La masa del átomo
Instituto Politécnico Nacional -ESIME-UC Depto. de Ingeniería Mecánica Química Básica Guia de Estudio Grupo: 1 M Fecha: Nombre del Alumno: 1. La masa atómica de un elemento representa: a) La masa del átomo
DEMOSTRAR LAS DIFERENTES CONDUCTIVIDADES DE LOS LIQUIDOS. Está diseñada para demostrar que el flujo de corriente eléctrica sólo es
 INFORME: CORROSIÓN ELECTROQUÍMICA NOMBRE: GRUPO: CORROSION 1 DEMOSTRAR LAS DIFERENTES CONDUCTIVIDADES DE LOS LIQUIDOS Está diseñada para demostrar que el flujo de corriente eléctrica sólo es posible a
INFORME: CORROSIÓN ELECTROQUÍMICA NOMBRE: GRUPO: CORROSION 1 DEMOSTRAR LAS DIFERENTES CONDUCTIVIDADES DE LOS LIQUIDOS Está diseñada para demostrar que el flujo de corriente eléctrica sólo es posible a
MATERIALES METALICOS
 MATERIALES METALICOS 1.- Qué es una aleación?. (1 punto) Una aleación es una mezcla de dos o más elementos químicos, al menos uno de los cuales, el que se encuentra en mayor proporción, ha de ser un metal.
MATERIALES METALICOS 1.- Qué es una aleación?. (1 punto) Una aleación es una mezcla de dos o más elementos químicos, al menos uno de los cuales, el que se encuentra en mayor proporción, ha de ser un metal.
Tema 5. Oxidación Reducción. Prof(a). María Angélica Sánchez Palacios
 Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea
Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea
Introduccion al equilibrio de reacciones de oxido-reduccion
 Introduccion al equilibrio de reacciones de oxido-reduccion laborado por: Gustavo Gomez Sosa Facultad de Quimica UNAM QU ÍM IC A A N A LÍTIC A I C LAV 142 G rupo 4, s em es tre 21-2 Resumen de celdas electroquimicas:
Introduccion al equilibrio de reacciones de oxido-reduccion laborado por: Gustavo Gomez Sosa Facultad de Quimica UNAM QU ÍM IC A A N A LÍTIC A I C LAV 142 G rupo 4, s em es tre 21-2 Resumen de celdas electroquimicas:
PILAS ELECTROQUÍMICAS
 PILAS ELECTROQUÍMICAS Las pilas electroquímicas se llaman también células galvánicas, células electroquímicas, pilas galvánicas, pilas voltaicas, pilas eléctricas o, simplemente, pilas. Como ya hemos visto,
PILAS ELECTROQUÍMICAS Las pilas electroquímicas se llaman también células galvánicas, células electroquímicas, pilas galvánicas, pilas voltaicas, pilas eléctricas o, simplemente, pilas. Como ya hemos visto,
En conjunto con la fuente de voltaje debe existir un circuito completo; este consiste en dos partes:
 La Corrosión. Podemos definir la corrosión como el deterioro que sufre un material (habitualmente un metal) en sus propiedades debido a una reacción con el medio. Si se pretenden comprender los métodos
La Corrosión. Podemos definir la corrosión como el deterioro que sufre un material (habitualmente un metal) en sus propiedades debido a una reacción con el medio. Si se pretenden comprender los métodos
LA TRIBOCORROSIÓN Y SU DESGASTE EN LOS IMPLANTES
 Máster en Ingeniería Biomédica LA TRIBOCORROSIÓN Y SU DESGASTE EN LOS IMPLANTES Franciso Company Añón. Efraím Conejero Navarro. Fernando José Quevedo González. Diciembre 2010 Qué es la tribocorrosión?
Máster en Ingeniería Biomédica LA TRIBOCORROSIÓN Y SU DESGASTE EN LOS IMPLANTES Franciso Company Añón. Efraím Conejero Navarro. Fernando José Quevedo González. Diciembre 2010 Qué es la tribocorrosión?
Materiales de uso técnico. La Madera y los Metales
 Materiales de uso técnico La Madera y los Metales El hombre a lo largo de la historia ha utilizado la naturaleza para satisfacer sus necesidades y mejorar sus condiciones de vida. Para ello ha fabricado
Materiales de uso técnico La Madera y los Metales El hombre a lo largo de la historia ha utilizado la naturaleza para satisfacer sus necesidades y mejorar sus condiciones de vida. Para ello ha fabricado
Estado de oxidación (E.O.)
 Reacciones Redox Estado de oxidación (E.O.) Es la carga que tendría un átomo si todos sus enlaces fueran iónicos. En el caso de enlaces covalentes polares habría que suponer que la pareja de electrones
Reacciones Redox Estado de oxidación (E.O.) Es la carga que tendría un átomo si todos sus enlaces fueran iónicos. En el caso de enlaces covalentes polares habría que suponer que la pareja de electrones
Tema 22 Corrosión y degradación de los materiales.
 Tema 22 Corrosión y degradación de los materiales. Sabemos que los metales poseen electrones libres. Estos electrones son el resultado del tipo de enlace que existe entre los átomos metálicos. Los electrones
Tema 22 Corrosión y degradación de los materiales. Sabemos que los metales poseen electrones libres. Estos electrones son el resultado del tipo de enlace que existe entre los átomos metálicos. Los electrones
ESTADOS DE AGREGACIÓN DE LA MATERIA
 LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
POTENCIOMETRIA KCL. Cl - CELDAS GALVANICAS DEPOSITO DE COBRE SOBRE UNA LAMINA DE ZINC CELDA GALVANICA POTENCIALES REDOX CELDA GALVANICA
 POTENCIOMETRIA TOPICOS: Celdas galvánicas Potenciales estándar de electrodo Ecuación de Nernst Electrodos de referencia: primario y secundario Medición de ph Celdas electrolíticas Titulaciones potenciométricas
POTENCIOMETRIA TOPICOS: Celdas galvánicas Potenciales estándar de electrodo Ecuación de Nernst Electrodos de referencia: primario y secundario Medición de ph Celdas electrolíticas Titulaciones potenciométricas
CENTRO DE INVESTIGACIONES AVANZADAS EN TECNOLOGÍA DEL HORMIGÓN Córdoba - Argentina CORROSIÓN DEL ACERO
 CORROSIÓN DEL ACERO A nivel macroscópico el hormigón armado puede ser considerado como un material compuesto constituido por dos fases, hormigón y acero, entre las cuales existe, además, una interfase
CORROSIÓN DEL ACERO A nivel macroscópico el hormigón armado puede ser considerado como un material compuesto constituido por dos fases, hormigón y acero, entre las cuales existe, además, una interfase
Índice general. 1. Preámbulo a la corrosión Introducción Materiales de construcción Las tuberías... 4
 Índice general 1. Preámbulo a la corrosión... 1 1.1 Introducción... 1 1.2 Materiales de construcción... 3 1.3 Las tuberías... 4 2. Corrosión de los metales... 7 2.1 Definición... 7 2.2 Mecanismo de la
Índice general 1. Preámbulo a la corrosión... 1 1.1 Introducción... 1 1.2 Materiales de construcción... 3 1.3 Las tuberías... 4 2. Corrosión de los metales... 7 2.1 Definición... 7 2.2 Mecanismo de la
ELECTROLISIS 1. OBJETIVOS 2. FUNDAMENTO TEÓRICO PROCESO ELECTROLÍTICO
 19 1. OBJETIVOS ELECTROLISIS 1.1 Observar como la electrolisis transforma la energía eléctrica en energía química. 1.2 Depositar un elemento metálico en un electrodo mediante la técnica de electrolisis.
19 1. OBJETIVOS ELECTROLISIS 1.1 Observar como la electrolisis transforma la energía eléctrica en energía química. 1.2 Depositar un elemento metálico en un electrodo mediante la técnica de electrolisis.
Presentaciones: Mario Humberto Rodriguez. Panel: COP21 una oportunidad global y nacional insoslayable.
 Presentaciones: Mario Humberto Rodriguez Panel: COP21 una oportunidad global y nacional insoslayable. Mario Humberto Rodriguez Director del proyecto de Investigación: «Recuperación de Li, Co y Al, desde
Presentaciones: Mario Humberto Rodriguez Panel: COP21 una oportunidad global y nacional insoslayable. Mario Humberto Rodriguez Director del proyecto de Investigación: «Recuperación de Li, Co y Al, desde
IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO
 IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO Tema 1: Medida y método científico. 1. Transforme las siguientes magnitudes al S.I de unidades: a) 228 Gm b) 436 ns
IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO Tema 1: Medida y método científico. 1. Transforme las siguientes magnitudes al S.I de unidades: a) 228 Gm b) 436 ns
CONTENIDO PROGRAMÁTICO
 UNE Rafael María Baralt Programa de Ingeniería y Tecnología Proyecto de Ingeniería en Mantenimiento Mecánico CONTENIDO PROGRAMÁTICO Asignatura: Preparado por: Prof. Roger Chirinos Qué es la ciencia e ingeniería
UNE Rafael María Baralt Programa de Ingeniería y Tecnología Proyecto de Ingeniería en Mantenimiento Mecánico CONTENIDO PROGRAMÁTICO Asignatura: Preparado por: Prof. Roger Chirinos Qué es la ciencia e ingeniería
PRACTICA # 2 METALES Y ALEACIONES.
 PRACTICA # 2 METALES Y ALEACIONES. 10 de 40 -INTRODUCCIÓN El ingeniero debe saber usar los materiales que satisfagan cienos requisitos en propiedades. en fabricación. etc. Por esto, deben de conocer la
PRACTICA # 2 METALES Y ALEACIONES. 10 de 40 -INTRODUCCIÓN El ingeniero debe saber usar los materiales que satisfagan cienos requisitos en propiedades. en fabricación. etc. Por esto, deben de conocer la
INHIBIDOR DE CORROSION
 GSUK3004 MANTENIMIENTO DEL INHIBIDOR DE CORROSION INHIBIDOR DE CORROSION Ejemplos de problemas Ejemplos donde no se usa un inhibidor de corrosión y donde no se hace el mantenimiento adecuado. El uso correcto
GSUK3004 MANTENIMIENTO DEL INHIBIDOR DE CORROSION INHIBIDOR DE CORROSION Ejemplos de problemas Ejemplos donde no se usa un inhibidor de corrosión y donde no se hace el mantenimiento adecuado. El uso correcto
TEMA VIII Materiales Metálicos
 TEMA VIII Materiales Metálicos LECCIÓN 12 Otras aleaciones metálicas 1 12.1 INTRODUCCIÓN Inconvenientes de las aleaciones férreas: - Densidad relativamente elevada - Conductividad eléctrica comparativamente
TEMA VIII Materiales Metálicos LECCIÓN 12 Otras aleaciones metálicas 1 12.1 INTRODUCCIÓN Inconvenientes de las aleaciones férreas: - Densidad relativamente elevada - Conductividad eléctrica comparativamente
MATERIALES METALICOS INTRODUCCION
 Materiales Metálicos 2do. Ingeniería Mecánica MATERIALES METALICOS INTRODUCCION Ing. Víctor Gómez U. T. N Facultad Regional Tucumán OBJETIVOS DE LA MATERIA -Estructuras interna y cristalográfica de los
Materiales Metálicos 2do. Ingeniería Mecánica MATERIALES METALICOS INTRODUCCION Ing. Víctor Gómez U. T. N Facultad Regional Tucumán OBJETIVOS DE LA MATERIA -Estructuras interna y cristalográfica de los
CATALOGO PARA ANODOS DE ZINC GALVANOPLASTIA
 CATALOGO PARA ANODOS DE ZINC GALVANOPLASTIA Es un proceso en el cual, por medio de la electricidad se deposita un metal sobre otro. Se dimana la corriente eléctrica de las placas sumergidas (ANODOS) hacia
CATALOGO PARA ANODOS DE ZINC GALVANOPLASTIA Es un proceso en el cual, por medio de la electricidad se deposita un metal sobre otro. Se dimana la corriente eléctrica de las placas sumergidas (ANODOS) hacia
Física y Química 4º ESO: guía interactiva para la resolución de ejercicios
 MATERIALES Y SUSTANCIAS Física y Química 4º ESO: guía interactiva para la resolución de ejercicios I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 Se dispone de láminas de varios metales y se
MATERIALES Y SUSTANCIAS Física y Química 4º ESO: guía interactiva para la resolución de ejercicios I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 Se dispone de láminas de varios metales y se
Prácticas de grupo. Práctica nº 3.
 Prácticas de grupo. Práctica nº 3. Práctica nº 3. Corrosión de armaduras de acero para hormigón. Objeto: Estudio de la oxidación acelerada de armaduras de acero usadas en hormigón. Someteremos varias probetas
Prácticas de grupo. Práctica nº 3. Práctica nº 3. Corrosión de armaduras de acero para hormigón. Objeto: Estudio de la oxidación acelerada de armaduras de acero usadas en hormigón. Someteremos varias probetas
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 REACCIONES DE TRANSFERENCIA DE ELECTRONES CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA 1 REACIONES DE OXIDACIÓNREDUCCIÓN Son aquellas en las que se produce una transferencia de electrones entre dos sustancias.
REACCIONES DE TRANSFERENCIA DE ELECTRONES CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA 1 REACIONES DE OXIDACIÓNREDUCCIÓN Son aquellas en las que se produce una transferencia de electrones entre dos sustancias.
7. Práctica 5: Celdas galvánicas.
 7. Práctica 5: Celdas galvánicas. 7.1. Fundamento teórico En esta práctica se construirán varias celdas voltaicas o galvánicas, a partir de dos semiceldas y de las conexiones apropiadas (circuito externo
7. Práctica 5: Celdas galvánicas. 7.1. Fundamento teórico En esta práctica se construirán varias celdas voltaicas o galvánicas, a partir de dos semiceldas y de las conexiones apropiadas (circuito externo
Clasificación de la materia
 Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
OBJETIVOS. General. Específicos
 OBJETIVOS General Entender y explicar la reacción que ocurre cuando se deja una puntilla en el agua, utilizando modelos atómicos y diferentes conceptos de forma clara. Específicos Investigar y estudiar
OBJETIVOS General Entender y explicar la reacción que ocurre cuando se deja una puntilla en el agua, utilizando modelos atómicos y diferentes conceptos de forma clara. Específicos Investigar y estudiar
Celdas de Combustible de Óxidos Sólidos:
 FORO ENERGÍA Y UNIVERSIDADES Celdas de Combustible de Óxidos Sólidos: Generación de Energía Eléctrica, Vía Electroquímica Noviembre 2013 ENERGÍA Las formas convencionales de generación de energía han generado
FORO ENERGÍA Y UNIVERSIDADES Celdas de Combustible de Óxidos Sólidos: Generación de Energía Eléctrica, Vía Electroquímica Noviembre 2013 ENERGÍA Las formas convencionales de generación de energía han generado
6.3.- Electroquímica
 360 Reacciones de transferencia de electrones 6.3.- Electroquímica Aspectos teóricos: Procesos electroquímicos 6.3.1. Procesos electroquímicos. Potenciales de reducción estándar. Celdas galvánicas y electrolíticas.
360 Reacciones de transferencia de electrones 6.3.- Electroquímica Aspectos teóricos: Procesos electroquímicos 6.3.1. Procesos electroquímicos. Potenciales de reducción estándar. Celdas galvánicas y electrolíticas.
CAPÍTULO 2. LAS PILAS DE COMBUSTIBLE.
 2. CAPÍTULO 2. LAS PILAS DE COMBUSTIBLE. Las pilas de combustible son equipos electroquímicos que, al igual que las baterías, convierten directamente en corriente eléctrica la energía química de un reactivo.
2. CAPÍTULO 2. LAS PILAS DE COMBUSTIBLE. Las pilas de combustible son equipos electroquímicos que, al igual que las baterías, convierten directamente en corriente eléctrica la energía química de un reactivo.
