16. El esquema simbólico de la pila anterior de todos los dados : Será el a) A b)b c) C d) D
|
|
|
- Dolores Blanco Ortega
- hace 5 años
- Vistas:
Transcripción
1 Redox 1 1.Un profesor de anatomía de la Universidad de Bolonia, va a realizar entre 1780 y 1786, las experiencias que serán el punto de partida para poder crear lo que sería el primer generador de corriente continua. Todo comenzó cuando las extremidades de una rana recién muerta, empezaron a convulsionarse, al saltar chispas de un condensador próximo, y repetirse el hecho al ser tocada por dos metales diferentes, aplicados tal como se describe en la figura. Este hecho, explicado incorrectamente por el citado profesor, Luis Galvani, fue aclarado posteriormente por su compatriota Alejandro Volta, profesor de física de la Universidad de Pavía, basándose en que: a) La rana poseía un fluido eléctrico en su estructura b) El contacto de dos metales diferentes producía una tensión eléctrica c) Había dos tipos de electricidad que al estar en contacto producían chispas d) Se había creado una fuente de electricidad que se descargaba a través de la rana 2*. Aunque inventó algunos de los aparatos más empleados en un laboratorio elemental de electricidad, como el electroscopio o el electróforo, los mayores beneficios económicos, honoríficos e incluso políticos, se los debió Volta al interés que se tomó Napoleón por su invento, que en principio llamó órgano eléctrico artificial, y que ahora conocemos como pila eléctrica. Del primer montaje realizado, cuya fotografía se adjunta, podrás concluir que: a) Se basaba en la diferente naturaleza de los metales plata y cinc b) Tenía que unir dichos metales por un aislante c) Debía comunicar los metales a través de un líquido que condujera la carga eléctrica d) Lo que realmente había creado es lo que conocemos con el nombre de una batería 3*. Debido a la participación en su creación de los profesores Galvani y Volta, el generador de corriente continua recibió los nombres de: a) Pila voltaica b) Voltámetro c) Pila galvánica d) Galvanómetro 4*. Mientras que le nombre que dio Volta al primer generador de corriente continua: órgano eléctrico artificial, se basaba en su comparación con los órganos eléctricos naturales del pez torpedo o de la anguila eléctrica, el que se emplea actualmente: pila voltaica o galvánica, surge del amontonamiento o apilamiento, tal como puede observarse de los elementos formados por discos de cobre o plata y estaño o cinc. De esta primera pila podrías decir que no funcionaría si los discos fueran: a) Todos de plata b) De cobre y plata c) De estaño y cinc d) De cobre y estaño
2 5*. Aunque la primera pila de Volta, nace con el siglo XIX, y en 1834, Grove produce energía eléctrica por unión del oxígeno con el hidrógeno, hasta 1839 no se creará la pila precursora de las de uso actual. Su montaje fue realizado por un profesor de química del Colegio del Rey, de Londres, Juan Federico Daniell. De su esquema, llegarás a concluir que : a) Está formada por dos partes o hemiceldas b) Cada hemicelda contiene un metal sumergido, en una disolución de una sal del mismo c) Las hemiceldas estaban comunicadas por una pared que permitía el intercambio iónico d) Un voltímetro intercalado indicaría una diferencia de potencial entre hemiceldas 6*. Si un montaje elemental de la pila Daniell, lo observamos en A, antes de cerrar el interruptor I y al cabo de cierto tiempo, en B, una vez cerrado I, notaremos unas claras diferencias, que nos obligarán a asegurar que: a) El cinc se ha disuelto, aumentando la concentración de Zn 2+ b) El Cu 2+, de la disolución, en su hemicelda se deposita en forma de cobre metálico c) Los átomos de cinc de la barra han ganado 2 cargas positivas, mientras que cada Cu 2+ ha tenido que perderlas d) Las cargas positivas que el Zn pierde, las gana el Cu 2+ e) Existirá un transporte de cargas eléctricas negativas, desde la barra de Zn a la de Cu 7*. Si las dos hemiceldas de la pila Daniell sólo estuvieran comunicadas por el circuito externo, la carga acumulada en las láminas al producirse las reacciones redox, impediría la continuidad del proceso, y por otra parte el uso de una pared porosa como separación, facilitaría la mezcla de disoluciones con el peligro de que ocurran fenómenos secundarios que alteren el proceso. Por eso, lo idea es emplear lo que se denomina, puente salino, esto es un tubo en U invertida, que previamente se llenó de una disolución de que facilite la propagación de la carga, bloqueándose con dos algodones en sus extremos (se puede sustituir por papel de filtro humedecido). Para que funcione correctamente, ésta deberá ser de: a) Agua destilada b) Una disolución de sal común c) Agua acidulada d) Cualquier sal 8*.En la fotografía adjunta se presenta una pila Daniell, conectada a aun voltímetro que marca 0,00V. Esto es debido a que: a) El circuito está interrumpido b) Falta el puente salino c) Están mal conectados los electrodos d) El voltímetro no funciona
3 9*. En la foto de la figura aparece una pila Daniell funcionando, con las dos hemiceldas, conectadas a un voltímetro, y un papel de filtro doblado sumergido en ambas disoluciones. Pero para que realmente el voltímetro marque una diferencia de potencial hace falta que dicho papel se impregne del líquido contenido en A, que podrá ser: a) Agua destilada b) Sal común c) Agua acidulada d) Cualquier sal 10*. El conocimiento de los procesos que tienen lugar en las pilas voltaicas, no podrá ser completo, sin el estudio de las reacciones químicas que en ellas ocurren, denominadas de oxidación-reducción, y aunque la primera definición de la oxidación fue realizada ya en 1780, por Lavoisier, como la ganancia de oxígeno por parte de una sustancia simple o compuesta, y la reducción incluso se conocía en tiempos de Geber (800 d.c.), definiéndola así por la pérdida de peso que experimentaban los compuestos metálicos al combinarse con determinadas sustancias como el carbón, actualmente debes saber que : a) La oxidación es la pérdida de electrones b) Un oxidante gana electrones c) La reducción es la pérdida de electrones d) Un reductor se oxida e) No hay oxidación sin reducción 11.Los términos ánodo y cátodo, fueron creados en 1834 por Faraday aconsejado por el profesor del Trinity College, de Cambridge, William Whewell.. Expone Faraday en Experimental Researches in Electricity de 1838: De tal forma que la electrodescomposición podía considerarse como la descomposición del cuerpo así situado de tal modo que la corriente pudiera pasar en la misma dirección y paralelamente a la que se supone existe en la Tierra. Sobre este movimiento de las cargas, propongo llamar ÁNODO, el camino hacia el este, por el cual sube el sol, y CÁTODO, la vía hacia el oeste, o el camino por el que el sol se pone. (debemos recordar que las cargas a las que hace referencia son las positivas y que ANA, en griego es ascendente, así como CATA lo es descendente). Según esto en la fotografía de la pila Daniell dada en la figura, el ánodo será: a) A b) B c) C d) D e) E 12.Las pilas electroquímicas se pueden simbolizar a través de los procesos de oxidación reducción realizados en ellas, primero lo que ocurre en el ánodo y después lo que sucede en el cátodo, teniendo en cuenta que el puente salino se representa por, dirás que la pila Daniell se representa por: a) Cu (1 M) / Cu Zn (1 M) / Zn c) 2 2 Zn / Zn (1 M) Cu (1 M) / Cu b) Zn M Zn Cu Cu M (1 ) / / (1 ) d) Cu (1 M) / Cu Zn / Zn (1 M)
4 13*. En la pila Daniell, cuyo esquema te dan, una vez transcurrido cierto tiempo podrás asegurar que a) A es una disolución de sulfato de cobre(ii), con menor concentración de la inicial b) B es el cátodo de la pila c) El Cu 2+, tomó 2 electrones oxidándose a Cu d) La reacción redox que se realizó espontáneamente sería CuSO 4 + Zn -> ZnSO 4 + Cu 14*. La interpretación del esquema que se adjunta te permitirá afirmar que: a) El comportamiento del Cu es muy diferente al presentado en la pila Daniell b) La Ag disminuyó de concentración porque se redujo c) El procedimiento se podría emplear para platear una lámina metálica d) En la disolución final también habrá Cu++ e) Por cada 2 moles de átomos de plata depositados sobre el cobre, se habrá disuelto un mol de átomos de cobre 15*.Si en la pila Daniell, analizados los fenómenos anteriores, sustituyeras la hemicelda del Zn por otra de plata sumergida en una disolución que contiene Ag+ (algunos de los fenómenos externos producidos se manifiestan en el dibujo adjunto) su observación y análisis detallado, te obligarán a decir que: a) El Cu que había actuado como oxidante frente al Zn, aquí frente a la Ag será reductor b) La circulación de la corriente por el circuito externo se hará desde la lámina de Ag a la de Cu c) La aguja del galvanómetro se desviará en sentido contrario al efectuado en la pila Daniell d) En la hemicelda de la plata ocurre una oxidación 16. El esquema simbólico de la pila anterior de todos los dados : 2 a) Cu / Cu (1 M) Ag (1 M) / Ag b) Ag (1 M) / Ag Cu / Cu (1 M) c) Ag (1 M) / Ag Cu (1 M) / Cu d) Cu (1 M) / Cu Ag / Ag (1 M) Será el a) A b)b c) C d) D
5 17. Como se ha visto, los metales tienen distintas tendencias a perder electrones, e incluso pueden ganarlos Este hecho expuesto de otra forma mas elemental era conocido mucho tiempo antes, pues ya Berzelius en 1819,había clasificado los elementos desde los más positivos, comenzando en el potasio hasta los más negativos como el oxígeno. Ahora bien, para hacer una verdadera escala, hay que establecer un patrón y una forma de medida. Esto es lo que se ha hecho con la hemicelda o electrodo de hidrógeno. En él y a la reacción 2H + + 2e- = H 2 (gas), en condiciones normal eso estándar, se le atribuyó un potencial normal E 0 dado en voltios de a) 1 b)-1 c) 0 d) 0, Si montamos 2 pilas con hemiceldas Cu ++ /Cu y Zn ++ /Zn, referidas al electrodo patrón de hidrógeno, tal como expresa el esquema adjunto y las conectamos a un voltímetro, con aguja calibrada al medio de la escala, observaremos que en el primer caso marca 0,34V, mientras que en el segundo - 0,76V.Todo ello te servirá para justificar que : a) La diferencia de potencial que proporcione la pila Daniell será de 1,1 voltios b) El Cu 2+ robe electrones al Zn 2+ c) El Zn sea mas reductor que el hidrógeno, ya que su potencial de reducción es menor d) El Cu sea mas oxidante que el hidrógeno ya que su potencial normal de reducción es mayor 19*. La interpretación del dibujo y esquema que se adjunta te permitirá afirmar que: a) El potencial normal de reducción del par Ag + /Ag, es mayor que el del Fe 3+ /Fe b) La Ag + disminuyó de concentración porque se redujo c) La hemicelda Fe 3+ /Fe es el cátodo de la pila d) La corriente circula por el conductor metálico del Fe al Ag 20. El esquema de la pila anterior, permite un simbolismo posible: 3 a) Fe / Fe (1 M) Ag (1 M) / Ag b) Ag (1 M) / Ag Fe (1 M) / Fe c) Ag (1 M) / Ag Fe / Fe (1 M) d) Fe (1 M) / Fe Ag / Ag (1 M) de todos los dados el único correcto será el a) A b) B c) C d) D
de todos los dados el correcto será el: a) A b) B c) C d) D
 Redox 3 41*. Uno de los experimentos que puedes hacer perfectamente en el laboratorio y que te permitiría recordar el proceso de la pila Daniell, sería sumergir una lámina o chapa de cinc en un vaso de
Redox 3 41*. Uno de los experimentos que puedes hacer perfectamente en el laboratorio y que te permitiría recordar el proceso de la pila Daniell, sería sumergir una lámina o chapa de cinc en un vaso de
Electroquímica. Cátedra de Geoquímica
 Electroquímica Cátedra de Geoquímica 1 ELECTROQUÍMICA: Parte de la Química que estudia las reacciones en las que hay transferencia de electrones, conocidas como REDOX Dada una reacción: Identificar el
Electroquímica Cátedra de Geoquímica 1 ELECTROQUÍMICA: Parte de la Química que estudia las reacciones en las que hay transferencia de electrones, conocidas como REDOX Dada una reacción: Identificar el
ELECTROQUÍMICA. 1. Conceptos de oxidación-reducción
 ELECTROQUÍMICA 1. Conceptos de oxidación-reducción Oxidación: transformación en la que una especie química pierde electrones o gana oxígeno. Reducción: transformación en la que una especie química gana
ELECTROQUÍMICA 1. Conceptos de oxidación-reducción Oxidación: transformación en la que una especie química pierde electrones o gana oxígeno. Reducción: transformación en la que una especie química gana
Unidad 6: ELECTROQUIMICA
 Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
-0,36-0,44 Zn 2+ +2e Zn -0,76 Mn 2+ +2e Mn -1,19 Al 3+ +3e Al -1,66 Mg 2+ +2e Mg -2,37 Na + +e Na -2,71 K + +e K -2,92 Li + +e Li -3,05
 Redox 2 21*. El número de oxidación, índice de oxidación o estado de oxidación fue definido por primera vez en 1880, por el inglés Otis Coe Johnson, como el número de cargas que un elemento aporta a la
Redox 2 21*. El número de oxidación, índice de oxidación o estado de oxidación fue definido por primera vez en 1880, por el inglés Otis Coe Johnson, como el número de cargas que un elemento aporta a la
TEMA-11 Electroquímica
 QUÍMICA I TEMA-11 Electroquímica Tecnólogo en Minería 1 I n t r o d u c c i ó n Electroquímica Fenómenos eléctricos Fenómenos químicos 2 I n t r o d u c c i ó n Electroquímica Fenómenos eléctricos Fenómenos
QUÍMICA I TEMA-11 Electroquímica Tecnólogo en Minería 1 I n t r o d u c c i ó n Electroquímica Fenómenos eléctricos Fenómenos químicos 2 I n t r o d u c c i ó n Electroquímica Fenómenos eléctricos Fenómenos
PILAS Y ELECTRÓLISIS. Foto: Gabriel Acquistapace
 PILAS Y ELECTRÓLISIS Foto: Gabriel Acquistapace En las reacciones REDOX se produce un intercambio de electrones. Para aprovechar esta circulación de carga es necesario separar las dos semireacciones y
PILAS Y ELECTRÓLISIS Foto: Gabriel Acquistapace En las reacciones REDOX se produce un intercambio de electrones. Para aprovechar esta circulación de carga es necesario separar las dos semireacciones y
PILAS ELECTROQUIMICAS
 PILAS ELECTROQUIMICAS En las reacciones de redox existe una transferencia de electrones entre en dador (especie que se oxida) y un aceptor (especie que se reduce).esta transferencia de electrones desde
PILAS ELECTROQUIMICAS En las reacciones de redox existe una transferencia de electrones entre en dador (especie que se oxida) y un aceptor (especie que se reduce).esta transferencia de electrones desde
Redox 3: Celdas electroquímicas 1
 V.Chan Celdas electroquímicas Celda electroquímica Representación simbólica de una celda Celda electroquímica: sistema en el cual se lleva a cabo una reacción redox que utiliza o consume corriente eléctrica.
V.Chan Celdas electroquímicas Celda electroquímica Representación simbólica de una celda Celda electroquímica: sistema en el cual se lleva a cabo una reacción redox que utiliza o consume corriente eléctrica.
RESUMEN DE ELECTROQUÍMICA 2ºBACH
 Toda reacción redox consiste en una transferencia de electrones desde la sustancia que se oxida (reductor)a la que se reduce (oxidante.) Una reacción redox espontánea permite obtener una corriente eléctrica.
Toda reacción redox consiste en una transferencia de electrones desde la sustancia que se oxida (reductor)a la que se reduce (oxidante.) Una reacción redox espontánea permite obtener una corriente eléctrica.
Unidad 8 Reacciones de oxidaciónreducción
 Unidad 8 Reacciones de oxidaciónreducción 1. Reacciones de Oxidación: proceso por el cual un reductor pierde electrones. Reducción: proceso por el cual un oxidante gana electrones. 2 2. Número de oxidación
Unidad 8 Reacciones de oxidaciónreducción 1. Reacciones de Oxidación: proceso por el cual un reductor pierde electrones. Reducción: proceso por el cual un oxidante gana electrones. 2 2. Número de oxidación
Tecnólogo en Minería Química I. PRÁCTICO DE LABORATORIO Reacciones Redox
 Tecnólogo en Minería Química I PRÁCTICO DE LABORATORIO Reacciones Redox I. INTRODUCCIÓN Las reacciones redox se encuentran entre las reacciones más comunes. Son aquellas que involucran la transferencia
Tecnólogo en Minería Química I PRÁCTICO DE LABORATORIO Reacciones Redox I. INTRODUCCIÓN Las reacciones redox se encuentran entre las reacciones más comunes. Son aquellas que involucran la transferencia
1. CONCEPTOS DE OXIDACIÓN Y REDUCCIÓN.
 UD. 7 REACCIONES DE TRANSFERENCIA DE ELECTRONES 1. CONCEPTOS DE OXIDACIÓN Y REDUCCIÓN. Oxidación: proceso en el que un átomo cede electrones. Reducción: proceso en el que un átomo gana electrones. Oxidante:
UD. 7 REACCIONES DE TRANSFERENCIA DE ELECTRONES 1. CONCEPTOS DE OXIDACIÓN Y REDUCCIÓN. Oxidación: proceso en el que un átomo cede electrones. Reducción: proceso en el que un átomo gana electrones. Oxidante:
Redox 7. la única correcta, sería la: a) A b)b c)c d)d
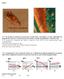 Redox 7 121*. En las fotos se muestra la reacción entre el ácido nítrico concentrado y el cobre, indicándose los productos de la reacción. La observación de las mismas y el ajuste correspondiente, te hará
Redox 7 121*. En las fotos se muestra la reacción entre el ácido nítrico concentrado y el cobre, indicándose los productos de la reacción. La observación de las mismas y el ajuste correspondiente, te hará
Oxidación-Reducción. Oxidantes y reductores
 OxidaciónReducción Inicialmente estos conceptos se relacionaban con la cantidad de oxígeno, así la oxidación comenzó a usarse para indicar que un compuesto incrementaba la proporción de átomos de este,
OxidaciónReducción Inicialmente estos conceptos se relacionaban con la cantidad de oxígeno, así la oxidación comenzó a usarse para indicar que un compuesto incrementaba la proporción de átomos de este,
FÍSICA 3 TEMA 3 Resumen teórico. Electroquímica
 Electroquímica OXIDACIÓN Y REDUCCIÓN Conceptos electrónicos de oxidación y reducción Reacciones Aplicaciones Como ya sabes, los átomos de los diversos elementos están formatos por un núcleo con protones
Electroquímica OXIDACIÓN Y REDUCCIÓN Conceptos electrónicos de oxidación y reducción Reacciones Aplicaciones Como ya sabes, los átomos de los diversos elementos están formatos por un núcleo con protones
Pilas electroquímicas
 Pilas electroquímicas El nombre de pila procede del apilamiento de monedas de cobre y cinc, que hizo Volta, en 1800. Después del descubrimiento de los reflejos eléctricos de la rana muerta de Galvani,
Pilas electroquímicas El nombre de pila procede del apilamiento de monedas de cobre y cinc, que hizo Volta, en 1800. Después del descubrimiento de los reflejos eléctricos de la rana muerta de Galvani,
1).- La siguiente figura representa a una pila: I. galvánica. II. electrolítica. III. seca
 1).- La siguiente figura representa a una pila: I. galvánica. II. electrolítica. III. seca A) Solo I B) Solo II C) Solo III D) Solo I y III E) Solo II y III 2).- Aprovecha una reacción redox espontánea
1).- La siguiente figura representa a una pila: I. galvánica. II. electrolítica. III. seca A) Solo I B) Solo II C) Solo III D) Solo I y III E) Solo II y III 2).- Aprovecha una reacción redox espontánea
PILAS ELECTROQUÍMICAS
 PILAS ELECTROQUÍMICAS Las pilas electroquímicas se llaman también células galvánicas, células electroquímicas, pilas galvánicas, pilas voltaicas, pilas eléctricas o, simplemente, pilas. Como ya hemos visto,
PILAS ELECTROQUÍMICAS Las pilas electroquímicas se llaman también células galvánicas, células electroquímicas, pilas galvánicas, pilas voltaicas, pilas eléctricas o, simplemente, pilas. Como ya hemos visto,
OXIDACIÓN-REDUCCIÓN. PAU-tipos de problemas
 OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
Paso 2: Escribir las correspondientes semireacciones sin ajustar y. Paso 3: Ajustar en cada semireacción todos los elementos a
 Tema 21 21.1. Reacciones de oxidación-reducción Química y electricidad 21.2. Celdas electroquímicas 21.3. Potencial de electrodo 1 2 21.1. Reacciones de oxidación-reducción (redox) Son reacciones de transferencia
Tema 21 21.1. Reacciones de oxidación-reducción Química y electricidad 21.2. Celdas electroquímicas 21.3. Potencial de electrodo 1 2 21.1. Reacciones de oxidación-reducción (redox) Son reacciones de transferencia
QUÍMICA INORGÁNICA ELECTROQUIMICA CUESTIONARIO Y RESPUESTAS
 1 QUÍMICA INORGÁNICA ELECTROQUIMICA CUESTIONARIO Y RESPUESTAS 1. De qué se ocupa la electroquímica? Qué tipos de reacciones intervienen en los procesos electroquímicos? La ELECTROQUIMICA se ocupa de los
1 QUÍMICA INORGÁNICA ELECTROQUIMICA CUESTIONARIO Y RESPUESTAS 1. De qué se ocupa la electroquímica? Qué tipos de reacciones intervienen en los procesos electroquímicos? La ELECTROQUIMICA se ocupa de los
Informe Electroquímica
 Informe Electroquímica Curso: Profesor: Integrante: IQ3205-1 Química Inorgánica Franciasco Santamaría Paulo Arriagada Introducción Actualmente la electricidad es la principal forma de energía utilizada
Informe Electroquímica Curso: Profesor: Integrante: IQ3205-1 Química Inorgánica Franciasco Santamaría Paulo Arriagada Introducción Actualmente la electricidad es la principal forma de energía utilizada
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 REACCIONES DE TRANSFERENCIA DE ELECTRONES CONCEPTO DE OXIDACIÓNREDUCCIÓN Oxidaciónreducción: proceso en el que se producen transferencias o intercambios de electrones de unas sustancias a otras: una sustancia
REACCIONES DE TRANSFERENCIA DE ELECTRONES CONCEPTO DE OXIDACIÓNREDUCCIÓN Oxidaciónreducción: proceso en el que se producen transferencias o intercambios de electrones de unas sustancias a otras: una sustancia
Celdas Galvánicas y Electrolíticas
 Celdas Galvánicas y Electrolíticas Reacciones de óxido-reducción Reacciones en las cuales una o más de las sustancias intervinientes modifica su estado de oxidación. Znº (s) + Cu +2 (ac) Zn 2+ (ac) + Cuº
Celdas Galvánicas y Electrolíticas Reacciones de óxido-reducción Reacciones en las cuales una o más de las sustancias intervinientes modifica su estado de oxidación. Znº (s) + Cu +2 (ac) Zn 2+ (ac) + Cuº
REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox) 1 2 Tipos de reacciones redox (según su espontaneidad) Reacciones espontáneas: G
REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox) 1 2 Tipos de reacciones redox (según su espontaneidad) Reacciones espontáneas: G
OXIDACIÓN-REDUCCIÓN. PAU-tipos de problemas
 OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
QUÍMICA 2º Bachillerato Ejercicios: Electroquímica
 1(8) Ejercicio nº 1 Considera la reacción: Cu(s) + 2Ag + (aq) Cu +2 (aq) + 2Ag(s) a) Escribe las semirreacciones de oxidación y de reducción c) Escribe el esquema de la pila que se puede formar con dicha
1(8) Ejercicio nº 1 Considera la reacción: Cu(s) + 2Ag + (aq) Cu +2 (aq) + 2Ag(s) a) Escribe las semirreacciones de oxidación y de reducción c) Escribe el esquema de la pila que se puede formar con dicha
Redox 10. Fig.1. Fig.2
 Redox 10 Foto 1 Foto 2 181. Si se dispone una moneda de cobre, sobre una disolución de nitrato de plata (foto 1), los resultados se aprecian en la foto 2. Se ha obtenido lo que fue llamado un árbol de
Redox 10 Foto 1 Foto 2 181. Si se dispone una moneda de cobre, sobre una disolución de nitrato de plata (foto 1), los resultados se aprecian en la foto 2. Se ha obtenido lo que fue llamado un árbol de
QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA
 QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA CUESTIONES RESUELTAS QUE HAN SIDO PROPUESTAS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2010) VOLUMEN
QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA CUESTIONES RESUELTAS QUE HAN SIDO PROPUESTAS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2010) VOLUMEN
Reacciones redox espontáneas
 Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
GUÍA DE REFUERZO PRUEBA DE SÍSTESIS II SEMESTRE
 Firma Apoderado GUÍA DE REFUERZO PRUEBA DE SÍSTESIS II SEMESTRE Nombre: Curso:11 th Grade Subsector: Química Fecha: Entrega 19 de noviembre Objetivos: Evaluar los contenidos y habilidades desarrollados
Firma Apoderado GUÍA DE REFUERZO PRUEBA DE SÍSTESIS II SEMESTRE Nombre: Curso:11 th Grade Subsector: Química Fecha: Entrega 19 de noviembre Objetivos: Evaluar los contenidos y habilidades desarrollados
4. Un agente oxidante (2 correctas) A) Toma electrones de otra sustancia B) Da electrones a otra sustancia C) Se oxida D) Se reduce
 CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA
 Trabajo Práctico Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA UNIVERSIDAD TECNOLÓGICA NACIONAL Regional Rosario En el presente se desarrolla una propuesta de trabajo práctico para realizar con los estudiantes
Trabajo Práctico Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA UNIVERSIDAD TECNOLÓGICA NACIONAL Regional Rosario En el presente se desarrolla una propuesta de trabajo práctico para realizar con los estudiantes
Estado de oxidación (E.O.)
 Reacciones Redox Estado de oxidación (E.O.) Es la carga que tendría un átomo si todos sus enlaces fueran iónicos. En el caso de enlaces covalentes polares habría que suponer que la pareja de electrones
Reacciones Redox Estado de oxidación (E.O.) Es la carga que tendría un átomo si todos sus enlaces fueran iónicos. En el caso de enlaces covalentes polares habría que suponer que la pareja de electrones
Problemas de electrolisis. Resueltos
 Problemas de electrolisis Resueltos Problemas 5,6 y 7 de la hoja de refuerzo Tambien estan al final de la hoja con enunciados de ejecicios PAU Serie refuerzo electroquímica 5 Se realiza la electrólisis
Problemas de electrolisis Resueltos Problemas 5,6 y 7 de la hoja de refuerzo Tambien estan al final de la hoja con enunciados de ejecicios PAU Serie refuerzo electroquímica 5 Se realiza la electrólisis
Reacciones de transferencias de electrones
 Reacciones de transferencias de electrones 5. Ajustar reacciones de oxidación-reducción y aplicarlas a problemas estequiométricos. Saber el significado de potencial estándar de reducción de un par redox,
Reacciones de transferencias de electrones 5. Ajustar reacciones de oxidación-reducción y aplicarlas a problemas estequiométricos. Saber el significado de potencial estándar de reducción de un par redox,
DEPARTAMENTO DE ELECTRÓNICA Y AUTOMÁTICA
 DEPARTAMENTO DE ELECTRÓNICA Y AUTOMÁTICA FACULTAD DE INGENIERÍA UNIVERSIDAD NACIONAL DE SAN JUAN Practica Laboratorio Nº 05 PILAS Asignatura: Química 1 Bioingeniería Autores del Grupo: Apellido, Nombre
DEPARTAMENTO DE ELECTRÓNICA Y AUTOMÁTICA FACULTAD DE INGENIERÍA UNIVERSIDAD NACIONAL DE SAN JUAN Practica Laboratorio Nº 05 PILAS Asignatura: Química 1 Bioingeniería Autores del Grupo: Apellido, Nombre
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 transparent www.profesorjrc.es REACCIONES DE TRANSFERENCIA DE ELECTRONES 29 de junio de 2016 Números de oxidación Oxidación: Reducción: Átomo o grupo de átomos que pierden e, n.o. Átomo o grupo de átomos
transparent www.profesorjrc.es REACCIONES DE TRANSFERENCIA DE ELECTRONES 29 de junio de 2016 Números de oxidación Oxidación: Reducción: Átomo o grupo de átomos que pierden e, n.o. Átomo o grupo de átomos
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2016 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 016 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 3, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción A Reserva 1, Ejercicio 6, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 016 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 3, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción A Reserva 1, Ejercicio 6, Opción
-0,36-0,44 Zn 2+ +2e Zn -0,76 Mn 2+ +2e Mn -1,19 Al 3+ +3e Al -1,66 Mg 2+ +2e Mg -2,37 Na + +e Na -2,71 K + +e K -2,92 Li + +e Li -3,05
 Redox 2 21*. El número de oxidación, índice de oxidación o estado de oxidación fue definido por primera vez en 1880, por el inglés Otis Coe Johnson, como el número de cargas que un elemento aporta a la
Redox 2 21*. El número de oxidación, índice de oxidación o estado de oxidación fue definido por primera vez en 1880, por el inglés Otis Coe Johnson, como el número de cargas que un elemento aporta a la
Tema 15: Equilibrio óxido-reducción Reacciones de oxidación-reducción (redox)
 : Equilibrio óxido-reducción 15.1 Reacciones de oxidación-reducción 15.2 Ajuste de reacciones redox: método del ión-electrón 15.3 Volumetrías redox. Indicadores. 15.4 Energía eléctrica asociada a procesos
: Equilibrio óxido-reducción 15.1 Reacciones de oxidación-reducción 15.2 Ajuste de reacciones redox: método del ión-electrón 15.3 Volumetrías redox. Indicadores. 15.4 Energía eléctrica asociada a procesos
OBJETIVOS ESPECÍFICOS. Al finalizar el Tema el estudiante:
 OBJETIVOS ESPECÍFICOS TEMA IV: ELECTROQUÍMICA: Al finalizar el Tema el estudiante: 1.1 Establecerá qué tipo de proceso es el que ocurre en una celda galvánica o pila. 1.2 Identificará los diferentes tipos
OBJETIVOS ESPECÍFICOS TEMA IV: ELECTROQUÍMICA: Al finalizar el Tema el estudiante: 1.1 Establecerá qué tipo de proceso es el que ocurre en una celda galvánica o pila. 1.2 Identificará los diferentes tipos
Unidad 7 Redox. La ecuación iónica sin ajustar con los números de oxidación:
 OPCIÓN A Unidad 7 Redox 1. Indique cual es el oxidante y cual es el reductor en los siguientes procesos de oxidación-reducción, sin ajustar: (2 p) El oxidante será aquel elemento que gane electrones (se
OPCIÓN A Unidad 7 Redox 1. Indique cual es el oxidante y cual es el reductor en los siguientes procesos de oxidación-reducción, sin ajustar: (2 p) El oxidante será aquel elemento que gane electrones (se
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 REACCIONES DE TRANSFERENCIA DE ELECTRONES CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA 1 REACIONES DE OXIDACIÓNREDUCCIÓN Son aquellas en las que se produce una transferencia de electrones entre dos sustancias.
REACCIONES DE TRANSFERENCIA DE ELECTRONES CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA 1 REACIONES DE OXIDACIÓNREDUCCIÓN Son aquellas en las que se produce una transferencia de electrones entre dos sustancias.
Examen de recuperación de la 3ª evaluación de Química de 2º de Bachillerato
 Examen de recuperación de la 3ª evaluación de Química de 2º de Bachillerato Nombre: Fecha: 1. En medio ácido, el ion permanganato (MnO - 4 ) se utiliza como agente oxidante fuerte. Conteste razonadamente
Examen de recuperación de la 3ª evaluación de Química de 2º de Bachillerato Nombre: Fecha: 1. En medio ácido, el ion permanganato (MnO - 4 ) se utiliza como agente oxidante fuerte. Conteste razonadamente
ELECTROQUÍMICA. 1- Concepto de potencial normal. Electrodo de referencia
 ELECTROQUÍMICA 1 Concepto de potencial normal. Electrodo de referencia 2 Se forma una pila con un electrodo de níquel y otro de plata. Indica el electrodo que eléctricamente es el polo positivo, el que
ELECTROQUÍMICA 1 Concepto de potencial normal. Electrodo de referencia 2 Se forma una pila con un electrodo de níquel y otro de plata. Indica el electrodo que eléctricamente es el polo positivo, el que
CÓMO RESOLVER ALGUNOS EJERCICIOS DE ELECTROQUÍMICA (Parte 1)
 M. C. Q. Alfredo Velásquez Márquez Profesor de la Facultad de Ingeniería de la UNAM velasquez777@yahoo.com.mx CÓMO RESOLVER ALGUNOS EJERCICIOS DE ELECTROQUÍMICA (Parte 1) Cuando en una reacción química
M. C. Q. Alfredo Velásquez Márquez Profesor de la Facultad de Ingeniería de la UNAM velasquez777@yahoo.com.mx CÓMO RESOLVER ALGUNOS EJERCICIOS DE ELECTROQUÍMICA (Parte 1) Cuando en una reacción química
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2001 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 001 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio, Opción A
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 001 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio, Opción A
TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX
 TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX E1A.S2012 El dióxido de manganeso reacciona en medio hidróxido potásico con clorato de potasio para dar permanganato de potasio, cloruro de potasio
TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX E1A.S2012 El dióxido de manganeso reacciona en medio hidróxido potásico con clorato de potasio para dar permanganato de potasio, cloruro de potasio
Reacciones Redox. Química General e Inorgánica Ingeniería Ambiental
 Reacciones Redox Hasta esta guía hemos aprendido a balancear ecuaciones químicas sencillas por tanteo, pero muchas ecuaciones son demasiado complejas para que este procedimiento de balanceo por tanteo
Reacciones Redox Hasta esta guía hemos aprendido a balancear ecuaciones químicas sencillas por tanteo, pero muchas ecuaciones son demasiado complejas para que este procedimiento de balanceo por tanteo
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio 5, Opción A Reserva 3, Ejercicio 3, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio 5, Opción A Reserva 3, Ejercicio 3, Opción
Reacciones de transferencia de electrones
 DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA 2º DE BACHILLERATO Actividades tema 8 Reacciones de transferencia de electrones Reacciones de oxidación-reducción 1.-Asigna el número
DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA 2º DE BACHILLERATO Actividades tema 8 Reacciones de transferencia de electrones Reacciones de oxidación-reducción 1.-Asigna el número
Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante
 Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante Objetivos: Los estudiantes serán capaces de Definir oxidación y reducción en términos de pérdida o ganancia de electrones. Describir
Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante Objetivos: Los estudiantes serán capaces de Definir oxidación y reducción en términos de pérdida o ganancia de electrones. Describir
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2005 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 005 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 5, Opción A Reserva, Ejercicio 6, Opción B Reserva 3, Ejercicio 3, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 005 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 5, Opción A Reserva, Ejercicio 6, Opción B Reserva 3, Ejercicio 3, Opción
Zn 2e Zn +2 proceso de oxidación Ánodo Polo negativo. Cu e Cu proceso de reducción Cátodo Polo positivo. Zn + Cu +2 Zn+2 + Cu
 Tema 4(II).PILAS Y CELDAS ELECTROLÍTICAS PILAS GALVÁNICAS Los procesos redox son procesos de transferencia de electrones. Podemos aprovechar tales procesos para producir corriente eléctrica si conseguimos
Tema 4(II).PILAS Y CELDAS ELECTROLÍTICAS PILAS GALVÁNICAS Los procesos redox son procesos de transferencia de electrones. Podemos aprovechar tales procesos para producir corriente eléctrica si conseguimos
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción A Reserva, Ejercicio 6, Opción B
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción A Reserva, Ejercicio 6, Opción B
Electroquímica UNIDAD XII-B QUIMICA- CPAM. 2017
 Electroquímica UNIDAD XII-B QUIMICA- CPAM. 2017 Electroquímica La electroquímica es la rama de la química que estudia la transformación entre la energía eléctrica y la energía química. Los procesos electroquímicos
Electroquímica UNIDAD XII-B QUIMICA- CPAM. 2017 Electroquímica La electroquímica es la rama de la química que estudia la transformación entre la energía eléctrica y la energía química. Los procesos electroquímicos
Métodos analíticos cuantitativos basados en las propiedades eléctricas de una solución de analito cuando forma parte de una celda electroquímica
 POTENCIOMETRÍA Química electroanalítica Métodos analíticos cuantitativos basados en las propiedades eléctricas de una solución de analito cuando forma parte de una celda electroquímica Electroquímica Conversión
POTENCIOMETRÍA Química electroanalítica Métodos analíticos cuantitativos basados en las propiedades eléctricas de una solución de analito cuando forma parte de una celda electroquímica Electroquímica Conversión
Se dispone, como ves, de tres óxidos de hierro, con diferente contenido en oxígeno.
 PVQ18-1.*** Estequiometría y redox del HIERRO Se dispone, como ves, de tres óxidos de hierro, con diferente contenido en oxígeno. a) Ordénalos por dicho contenido, de mayor a menor Fotografía 1 b) Indica
PVQ18-1.*** Estequiometría y redox del HIERRO Se dispone, como ves, de tres óxidos de hierro, con diferente contenido en oxígeno. a) Ordénalos por dicho contenido, de mayor a menor Fotografía 1 b) Indica
 REDOX 1. Dada la ecuación redox KMnO 4 + K 2 SO 3 + HCl > MnO 2 + K 2 SO 4 + KCl + H 2 O 1. a) Deduce razonadamente la sustancia oxidante y la reductora, la que oxida y la que se reduce. b) Escribe y ajusta
REDOX 1. Dada la ecuación redox KMnO 4 + K 2 SO 3 + HCl > MnO 2 + K 2 SO 4 + KCl + H 2 O 1. a) Deduce razonadamente la sustancia oxidante y la reductora, la que oxida y la que se reduce. b) Escribe y ajusta
Tema 3. Termodinámica de Procesos Electroquímicos
 Tema 3. Termodinámica de Procesos Electroquímicos 1.- Iones en disolución 2.- Reacciones Redox 3.- Celdas Electroquímicas 4.- Potencial de una celda. Ecuación de Nerst 5.- Ejemplos de Procesos Electroquímicos
Tema 3. Termodinámica de Procesos Electroquímicos 1.- Iones en disolución 2.- Reacciones Redox 3.- Celdas Electroquímicas 4.- Potencial de una celda. Ecuación de Nerst 5.- Ejemplos de Procesos Electroquímicos
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: POTENCIALES DE ELECTRODOS. PILAS 1.-/ Cuál es el potencial normal de una pila que utiliza los pares Zn 2+ /Zn y Ag + /Ag? Cuál es la polaridad de cada electrodo?
REACCIONES DE TRANSFERENCIA DE ELECTRONES: POTENCIALES DE ELECTRODOS. PILAS 1.-/ Cuál es el potencial normal de una pila que utiliza los pares Zn 2+ /Zn y Ag + /Ag? Cuál es la polaridad de cada electrodo?
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2003 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción A Reserva,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción A Reserva,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2004 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 004 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 6, Opción A Reserva, Ejercicio, Opción B
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 004 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 6, Opción A Reserva, Ejercicio, Opción B
TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN
 TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN Las reacciones químicas de óxido - reducción (reacciones redox) son aquellas en las cuales se produce una transferencia de electrones. Son las reacciones donde se producen
TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN Las reacciones químicas de óxido - reducción (reacciones redox) son aquellas en las cuales se produce una transferencia de electrones. Son las reacciones donde se producen
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2008 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 008 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 3, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción A Reserva 1, Ejercicio 6, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 008 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 3, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción A Reserva 1, Ejercicio 6, Opción
Celdas galvánicas o voltaicas
 Celdas galvánicas o voltaicas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es)
Celdas galvánicas o voltaicas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es)
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
REACCIONES DE OXIDACIÓN-REDUCCIÓN
 10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS ACTIVIDADES PRPUESTAS EN EL INTERIR DE LA UNIDAD 1 Por qué en los procesos redox no puede existir una única semirreacción de oxidación o de reducción?
10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS ACTIVIDADES PRPUESTAS EN EL INTERIR DE LA UNIDAD 1 Por qué en los procesos redox no puede existir una única semirreacción de oxidación o de reducción?
Electroquímica (II) Pilas. Potenciales redox
 Electroquímica (II) Pilas. Potenciales redox IES La Magdalena. Avilés. Asturias Las reacciones redox pueden ser utilizadas para producir diferencias de potencial entre dos puntos, entre los cuales puede
Electroquímica (II) Pilas. Potenciales redox IES La Magdalena. Avilés. Asturias Las reacciones redox pueden ser utilizadas para producir diferencias de potencial entre dos puntos, entre los cuales puede
PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO.
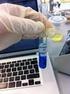 PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO. El concepto de Electroquímica implica transformaciones que requieren la presencia de electrodos. Dos electrodos sumergidos en un electrólito y unidos
PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO. El concepto de Electroquímica implica transformaciones que requieren la presencia de electrodos. Dos electrodos sumergidos en un electrólito y unidos
CUESTIONES Y PROBLEMAS DE SELECTIVIDAD EN LAS UNIVERSIDADES ANDALUZAS REACCIONES DE TRANSFERENCIA DE ELECTRONES
 CUESTIONES Y PROBLEMAS DE SELECTIVIDAD EN LAS UNIVERSIDADES ANDALUZAS 2001-2012 REACCIONES DE TRANSFERENCIA DE ELECTRONES 1. El KMnO 4, en medio ácido sulfúrico, reacciona con el H 2 O 2 para dar MnSO
CUESTIONES Y PROBLEMAS DE SELECTIVIDAD EN LAS UNIVERSIDADES ANDALUZAS 2001-2012 REACCIONES DE TRANSFERENCIA DE ELECTRONES 1. El KMnO 4, en medio ácido sulfúrico, reacciona con el H 2 O 2 para dar MnSO
PRÁCTICA Nº 9 y 10 CORROSIÓN I
 PRÁCTICA Nº 9 y 10 CORROSIÓN I OBJETO DE LA PRÁCTICA: CONCEPTO DE ÁNODO Y CÁTODO APLICACIÓN A TRES REACCIONES REDOX CONCEPTO DE ENERGÍA ELÉCTRICA ASOCIADA A CAMBIOS QUÍMICOS Y VICEVERSA REACCIÓN ESPONTÁNEA
PRÁCTICA Nº 9 y 10 CORROSIÓN I OBJETO DE LA PRÁCTICA: CONCEPTO DE ÁNODO Y CÁTODO APLICACIÓN A TRES REACCIONES REDOX CONCEPTO DE ENERGÍA ELÉCTRICA ASOCIADA A CAMBIOS QUÍMICOS Y VICEVERSA REACCIÓN ESPONTÁNEA
ELECTROQUÍMICA. Se discutirán en la clase práctica algunos de los siguientes ejercicios de Brown: Capítulo 20: 5, 7, 13, 21, 23, 33, 39, 47, 51
 REPARTIDO 8 ELECTROQUÍMICA 2007 Bibliografía: - Química, La Ciencia Central, T.L.Brown, H.E.LeMay, Jr., B. Bursten. Ed. Prentice-Hall, México, 1998, 7 ma Ed. Capítulo 20, 723-761 APENDICE E Ejercicios
REPARTIDO 8 ELECTROQUÍMICA 2007 Bibliografía: - Química, La Ciencia Central, T.L.Brown, H.E.LeMay, Jr., B. Bursten. Ed. Prentice-Hall, México, 1998, 7 ma Ed. Capítulo 20, 723-761 APENDICE E Ejercicios
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2004 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 004 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 6, Opción A Reserva, Ejercicio 3, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 004 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 6, Opción A Reserva, Ejercicio 3, Opción
ELECTROQUÍMICA. CELDAS GALVÁNICAS Y CELDAS ELECTROLÍTICAS. Reacciones de óxido reducción. Cambios de la energía libre y criterios de espontaneidad
 ELECTROQUÍMICA. CELDAS GALVÁNICAS Y CELDAS ELECTROLÍTICAS Temas previos: Reacciones de óxido reducción Cambios de la energía libre y criterios de espontaneidad REACCIONES DE OXIDO-REDUCCIÓN Oxidación:
ELECTROQUÍMICA. CELDAS GALVÁNICAS Y CELDAS ELECTROLÍTICAS Temas previos: Reacciones de óxido reducción Cambios de la energía libre y criterios de espontaneidad REACCIONES DE OXIDO-REDUCCIÓN Oxidación:
Capítulo 20: Electroquímica
 Capítulo 20: Electroquímica Dr. Alberto Santana Universidad de Puerto Rico Recinto Universitario de Mayagüez Departamento de Química Quimica general II, Electroquímica p.1 Cosas importantes Electroquímica
Capítulo 20: Electroquímica Dr. Alberto Santana Universidad de Puerto Rico Recinto Universitario de Mayagüez Departamento de Química Quimica general II, Electroquímica p.1 Cosas importantes Electroquímica
7º) En la tabla siguiente se indican los potenciales estándar de distintos pares en disolución acuosa: Fe2+/Fe = - 0,44 V Cu2+/Cu = 0,34 V
 EJERCICIOS DE OXIDACIÓN Y REDUCCIÓN 1º) Ajuste las siguientes ecuaciones iónicas, en medio ácido, por el método del ión-electrón: a) MnO4 + I Mn2+ + I2 b) VO43 + Fe2+ VO2+ + Fe3+ c) Cl2 + I Cl + I2 2º)
EJERCICIOS DE OXIDACIÓN Y REDUCCIÓN 1º) Ajuste las siguientes ecuaciones iónicas, en medio ácido, por el método del ión-electrón: a) MnO4 + I Mn2+ + I2 b) VO43 + Fe2+ VO2+ + Fe3+ c) Cl2 + I Cl + I2 2º)
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
REACCIONES DE TRANSFERENCIA DE ELECTRONES: ELECTRÓLISIS 1.-/ Calcule la intensidad de la corriente que se necesita para descomponer 18 g de cloruro de cobre (II) en disolución acuosa, en un tiempo de 50
QUÍMICA Reactividad y equilibrio químico. Oxido - reducción. Tutora: Romina Saavedra
 QUÍMICA Reactividad y equilibrio químico Oxido - reducción Tutora: Romina Saavedra Balance de reacciones de óxido reducción Una reacción redox o de óxido reducción se caracteriza por la existencia de dos
QUÍMICA Reactividad y equilibrio químico Oxido - reducción Tutora: Romina Saavedra Balance de reacciones de óxido reducción Una reacción redox o de óxido reducción se caracteriza por la existencia de dos
6.3.- Electroquímica
 360 Reacciones de transferencia de electrones 6.3.- Electroquímica Aspectos teóricos: Procesos electroquímicos 6.3.1. Procesos electroquímicos. Potenciales de reducción estándar. Celdas galvánicas y electrolíticas.
360 Reacciones de transferencia de electrones 6.3.- Electroquímica Aspectos teóricos: Procesos electroquímicos 6.3.1. Procesos electroquímicos. Potenciales de reducción estándar. Celdas galvánicas y electrolíticas.
Capítulo 4: Circuitos de corriente continua
 Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
Escuela Nacional de Ciencias Biológicas. Instituto Politécnico Nacional. Materia: Fisicoquímica II. Nombre Integrantes : González González Laura Ibeth
 Escuela Nacional de Ciencias Biológicas Instituto Politécnico Nacional Materia: Fisicoquímica II Nombre Integrantes : González González Laura Ibeth Rodríguez Ramírez Malinallitzin Prida Villagrán Angel
Escuela Nacional de Ciencias Biológicas Instituto Politécnico Nacional Materia: Fisicoquímica II Nombre Integrantes : González González Laura Ibeth Rodríguez Ramírez Malinallitzin Prida Villagrán Angel
LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II)
 LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II) Se van a presentar tres electrólisis en diferentes condiciones y con distintos electrodos, a fin de observar la influencia de estas condiciones en sus resultados
LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II) Se van a presentar tres electrólisis en diferentes condiciones y con distintos electrodos, a fin de observar la influencia de estas condiciones en sus resultados
Tema 6. Reacciones de transferencia de electrones. Oxidación-reducción
 Tema 6 Reacciones de transferencia de electrones Oxidación-reducción CONTENIDO 1.- Concepto tradicional de oxidación-reducción. 2.- Concepto electrónico de oxidación-reducción. 3.- Número de oxidación.
Tema 6 Reacciones de transferencia de electrones Oxidación-reducción CONTENIDO 1.- Concepto tradicional de oxidación-reducción. 2.- Concepto electrónico de oxidación-reducción. 3.- Número de oxidación.
BLOQUE IV- SEGUNDA PARTE. Prof. Dr. Mª del Carmen Clemente Jul
 BLOQUE IV- SEGUNDA PARTE Prof. Dr. Mª del Carmen Clemente Jul PILAS VOLTAICAS DISPOSITIVO EXPERIMENTAL QUE PERMITE A PARTIR DE UNA REACCIÓN REDOX GENERAR ELECTRICIDAD ELECTRODOS SEMICELDAS BARRAS DE LOS
BLOQUE IV- SEGUNDA PARTE Prof. Dr. Mª del Carmen Clemente Jul PILAS VOLTAICAS DISPOSITIVO EXPERIMENTAL QUE PERMITE A PARTIR DE UNA REACCIÓN REDOX GENERAR ELECTRICIDAD ELECTRODOS SEMICELDAS BARRAS DE LOS
7. Práctica 5: Celdas galvánicas.
 7. Práctica 5: Celdas galvánicas. 7.1. Fundamento teórico En esta práctica se construirán varias celdas voltaicas o galvánicas, a partir de dos semiceldas y de las conexiones apropiadas (circuito externo
7. Práctica 5: Celdas galvánicas. 7.1. Fundamento teórico En esta práctica se construirán varias celdas voltaicas o galvánicas, a partir de dos semiceldas y de las conexiones apropiadas (circuito externo
GUIA DE EJERCICIOS ELECTROQUÍMICA
 GUIA DE EJERCICIOS ELECTROQUÍMICA Ecuación de Nernst y Leyes de Faraday Resultados de aprendizaje Identifica, conecta y analiza conceptos básicos de electroquímica para la resolución de ejercicios, desarrollando
GUIA DE EJERCICIOS ELECTROQUÍMICA Ecuación de Nernst y Leyes de Faraday Resultados de aprendizaje Identifica, conecta y analiza conceptos básicos de electroquímica para la resolución de ejercicios, desarrollando
QUÍMICA. Tema 8. Reacciones Redox. Electroquímica
 Tema 8. Reacciones Redox. Electroquímica Índice - Concepto de oxidación-reducción - Número de oxidación - Oxidantes y reductores - Potencial normal de reducción - Predicción de reacciones redox Objetivos
Tema 8. Reacciones Redox. Electroquímica Índice - Concepto de oxidación-reducción - Número de oxidación - Oxidantes y reductores - Potencial normal de reducción - Predicción de reacciones redox Objetivos
Práctica 5: Termoquímica: Celdas galvánicas
 Práctica 5: Termoquímica: Celdas galvánicas Ingeniería agrónoma grado en hortofruticultura y jardinería Jorge Cerezo Martínez Objetivos Construir, varias celdas galvánicas o voltaicas y medir el potencial
Práctica 5: Termoquímica: Celdas galvánicas Ingeniería agrónoma grado en hortofruticultura y jardinería Jorge Cerezo Martínez Objetivos Construir, varias celdas galvánicas o voltaicas y medir el potencial
MADRID / JUNIO 99. LOGSE / QUÍMICA / ELECTROQUÍMICA / OPCION A/ CUESTIÓN 3
 MADRID / JUNIO 99. LOGSE / QUÍMICA / ELECTROQUÍMICA / OPCION A/ CUESTIÓN 3 3. Deduzca razonadamente y escribiendo la reacción ajustada: a) Si el hierro en su estado elemental puede ser oxidado a hierro(ii)
MADRID / JUNIO 99. LOGSE / QUÍMICA / ELECTROQUÍMICA / OPCION A/ CUESTIÓN 3 3. Deduzca razonadamente y escribiendo la reacción ajustada: a) Si el hierro en su estado elemental puede ser oxidado a hierro(ii)
CUESTIONES Y PROBLEMAS DEL TEMA 8 (ELECTROQUÍMICA)
 CUESTIONES Y PROBLEMAS DEL TEMA 8 (ELECTROQUÍMICA) 1.- Teniendo en cuenta los potenciales de reducción estándar de los pares E 0 (Cl 2 /Cl - ) = 1 36 V y E 0 (Cu 2+ /Cu) = 0 34 V: a) Escriba la reacción
CUESTIONES Y PROBLEMAS DEL TEMA 8 (ELECTROQUÍMICA) 1.- Teniendo en cuenta los potenciales de reducción estándar de los pares E 0 (Cl 2 /Cl - ) = 1 36 V y E 0 (Cu 2+ /Cu) = 0 34 V: a) Escriba la reacción
OXIDACIÓN REDUCCIÓN QCA 09 ANDALUCÍA
 OXIDACIÓN REDUCCIÓN QCA 9 ANDALUCÍA.- Sea una pila constituida, en condiciones estándar, por un electrodo de plata sumergido en una disolución de nitrato de plata y un electrodo de cadmio sumergido en
OXIDACIÓN REDUCCIÓN QCA 9 ANDALUCÍA.- Sea una pila constituida, en condiciones estándar, por un electrodo de plata sumergido en una disolución de nitrato de plata y un electrodo de cadmio sumergido en
Prof(a). María Angélica Sánchez Palacios
 Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea,
Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea,
ELECTROQUÌMICA. Zn Zn 2+ (aq) Cu 2+ (aq) Cu
 ELECTROQUÌMICA - Pilas químicas ó voltaicas, producen una corriente continua mediante la utilización de una reacción redox. - Electrólisis, produce una reacción redox por medio de una corriente eléctrica
ELECTROQUÌMICA - Pilas químicas ó voltaicas, producen una corriente continua mediante la utilización de una reacción redox. - Electrólisis, produce una reacción redox por medio de una corriente eléctrica
Procesos de Oxidación-Reducción
 2012 Procesos de Oxidación-Reducción TERMINOLOGIA La Electroquímicaes la rama de la química que estudia la transformación entre la energía eléctrica y la energía química. Material preparado por: Licda.Victoria
2012 Procesos de Oxidación-Reducción TERMINOLOGIA La Electroquímicaes la rama de la química que estudia la transformación entre la energía eléctrica y la energía química. Material preparado por: Licda.Victoria
EQUILIBRIO REDOX. Zn Zn e -
 EQUILIBRIO REDOX Con respecto a la oxidación de una sustancia, se entiende que la forma oxidada es aquella que resulta cuando la forma reducida pierde sus electrones y que se establece un equilibrio entre
EQUILIBRIO REDOX Con respecto a la oxidación de una sustancia, se entiende que la forma oxidada es aquella que resulta cuando la forma reducida pierde sus electrones y que se establece un equilibrio entre
Teoría Redox. Química III medio
 Teoría Redox Química III medio Las reacciones de oxido-reducción son aquellas en las que existe una transferencia de electrones o un cambio en los estados de oxidación de las sustancias que forman parte
Teoría Redox Química III medio Las reacciones de oxido-reducción son aquellas en las que existe una transferencia de electrones o un cambio en los estados de oxidación de las sustancias que forman parte
