Electroquímica UNIDAD XII-B QUIMICA- CPAM. 2017
|
|
|
- María Victoria Martin Martínez
- hace 6 años
- Vistas:
Transcripción
1 Electroquímica UNIDAD XII-B QUIMICA- CPAM. 2017
2 Electroquímica La electroquímica es la rama de la química que estudia la transformación entre la energía eléctrica y la energía química.
3 Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea es convertida en electricidad. o - La energía eléctrica es usada para hacer que una reacción no espontánea ocurra.
4 Reacciones REDOX Barra de Zn en una solución de CuSO 4 Los átomos de Zn pasan a la solución como Zn 2+. Iones Cu 2+ se convierten en átomos de Cu.
5 Zn (s) + CuSO 4 (ac) ZnSO 4 (ac) + Cu (s) Zn Zn e - Zn se oxida Zn es el agente reductor Cu e - Cu Cu 2+ se reduce CuSO 4 es el oxidante La transferencia de electrones de los átomos de Zn a los iones Cu 2+ para formar Zn +2 y Cu es un proceso espontáneo, y por tanto, libera energía útil (ΔG -). Esa energía puede utilizarse para producir trabajo eléctrico.
6 Celdas galvánicas o voltaicas Son dispositivos que utilizan la energía liberada por una reacción química espontánea para generar energía eléctrica. Si en la reacción anterior, se separan la semi reacción de oxidación del Zn y la semi reacción de reducción del Cu +2, y se las conecta a través de un cable conductor, se establece una corriente de electrones capaz de realizar un TRABAJO ELECTRICO.
7 Ánodo oxidación Cátodo reducción Reacción redox espontánea
8 Celdas galvánicas o voltaicas En el ANODO los átomos de Zn se oxidan, y los electrones se transportan a través del cable conductor. Los electrones llegan al CÁTODO donde los iones Cu +2 se reducen. La corriente eléctrica fluye del ánodo al cátodo porque existe una diferencia de potencial eléctrico entre el ánodo y el cátodo. Esta diferencia se llama: VOLTAJE DE CELDA
9 Potencial de celda La diferencia de potencial eléctrico entre el ánodo y el cátodo se llama: -Voltaje de la celda -Fuerza electromotriz (fem) o -Potencial de la celda El potencial de celda depende de la naturaleza de los electrodos e iones, de su concentración y de la temperatura.
10 Zn (s) + Cu 2+ (ac) Cu (s) + Zn 2+ (ac) Ánodo Diagramas de celdas [Cu 2+ ] = 1 M & [Zn 2+ ] = 1 M Zn (s) Zn 2+ (1 M) Cu 2+ (1 M) Cu (s) Cátodo
11 Potencial de celda Para la reacción: Zn (s) + Cu 2+ (ac) Cu (s) + Zn 2+ (ac) Cuando las concentraciones de los iones Cu y Zn son de 1M, el voltaje o fem de celda es de 1,10 V a 25 C. Este valor de fem debe ser la suma de los potenciales eléctricos en los electrodos de Zn y Cu. Si se conoce uno de ellos, se puede calcular el otro.
12 Potenciales estándar de reducción (E ) El potencial estándar de reducción (E 0 ) es el voltaje asociado con una reacción de reducción en un electrodo cuando todo los solutos se encuentran a 1 M y todos los gases están a 1 atm. Es imposible medir la fem de un solo electrodo, por tanto se lo mide en relación a un electrodo de referencia, el ELECTRODO DE HIDROGENO, al cual, arbitrariamente, se le ha asignado el valor 0.
13 Electrodo estándar de hidrógeno 2e - + 2H + (1 M) H 2 (1 atm) E 0 = 0 V
14 Potenciales estándar de reducción (E ) y fem de una celda. Cómo se establecen los potenciales estándar de reducción para diferentes elementos?. Cómo se calcula el voltaje de una celda (fem)?. Ejemplo: Cálculo de potencial estándar de reducción de los electrodos de Zn y Cu. Cálculo de la fem de la celda para la reacción: Zn (s) + Cu 2+ (ac) Cu (s) + Zn 2+ (ac)
15 Potencial estándar de reducción del Zn Ecelda 0 = 0.76 V Zn (s) Zn 2+ (1 M) H + (1 M) H 2 (1 atm) Pt (s)
16 Potencial estándar de reducción del Zn Zn (s) Zn 2+ (1 M) H + (1 M) H 2 (1 atm) Pt (s) Ánodo (oxidación): Zn(s) Zn +2 (1 M) + 2e - Cátodo (reducción): 2e - + 2H + (1 M) H 2 (1 atm) Zn (s) + H + (1 M) H 2 (1atm) + Zn +2 (1 M)
17 Potenciales estándar de reducción del Zn Zn (s) Zn 2+ (1 M) H + (1 M) H 2 (1 atm) Pt (s) fem estandar (E 0 ) cell E 0 celda 0 0 = E catodo E anodo E 0 = E + 0 H / H - E 2+ Zn / Zn celda V = 0 - E 2+ Zn /Zn 0 2+ E Zn /Zn = V Zn 2+ (1 M) + 2e - Zn E 0 = V
18 Potenciales estándar de reducción del Cu E 0 = 0.34 V celda Pt (s) H 2 (1 atm) H + (1 M) Cu 2+ (1 M) Cu (s)
19 Potenciales estándar de reducción del Cu Pt (s) H 2 (1 atm) H + (1 M) Cu 2+ (1 M) Cu (s) Ánodo (oxidación): H 2 (1 atm) 2H + (1 M) + 2e - Cátodo (reducción): 2e - + Cu 2+ (1 M) Cu (s) H 2 (1 atm) + Cu 2+ (1 M) Cu (s) + 2H + (1 M)
20 Potenciales estándar de reducción del Cu Pt (s) H 2 (1 atm) H + (1 M) Cu 2+ (1 M) Cu (s) E 0 celda 0 0 = E cátodo - E ánodo E celda = E 2+ Cu /Cu E H + /H = E 2+ Cu /Cu E Cu 2+ /Cu = 0.34 V
21 Reacción total de la celda de Daniell Ánodo (oxidación): Zn(s) Zn +2 (1 M) + 2e - Cátodo (reducción): 2e - + Cu 2+ (1 M) Cu (s) Zn (s) + Cu 2+ (1M) Cu (s) + Zn 2+ (1M)
22 fem de la celda E 0 celda 0 0 = E cátodo - E ánodo E celda = E 2+ Cu /Cu E +2 Zn /Zn E 0 = 0,34 V (- 0,76 V) celda E 0 celda = 1,10 V
23 El valor positivo de E indica que la reacción es favorable en ese sentido (transferencia de electrones del Zn al Cu). Al igual que con el ΔG, el signo de E permite predecir el alcance de una reacción REDOX. E positiva E negativa Equilibrio desplazado h/ productos Equilibrio desplazado h/ reactivos
24 Potenciales estándar de reducción (E ) para diferentes sustancias.
25 Entre E sea más positivo mayor será la tendencia de la sustancia a reducirse. Las sustancias que se encuentran más abajo en la tabla, oxidan espontáneamente a las que están más arriba. Las sustancias que se encuentran más arriba, reducen a las que están por debajo. Las semirreacciones son reversibles y el signo de E cambia cuando la reacción se invierte La variación de los coeficientes estequiométricos de una semireacción no altera el valor de E
26 Mayor carácter reductor Mayor tendencia a reducirse Mayor carácter oxidante Mayor tendencia a oxidarse. Química. CPAM- 2017/2018
27 Cuál es la fem estándar de una celda electroquímica hecha de un electrodo de Cd en una solución 1.0 M de Cd (NO 3 ) 2 y un electrodo de Cr en una solución 1.0 M de Cr (NO 3 ) 3? Cd 2+ (ac) + 2e - Cd (s) E 0 = V Cr 3+ (ac) + 3e - Cr (s) E 0 = V Ánodo (oxidación): Cr (s) Cr 3+ (1 M) + 3e - Cátodo (reducción): 2e - + Cd 2+ (1 M) Cd (s) x 3 x 2 2Cr (s) + 3Cd 2+ (1 M) 3Cd (s) + 2Cr 3+ (1 M) E celda = E cátodo - E ánodo E 0 = (-0.74) celda E 0 celda = 0.34 V
28 Termodinámica de las reacciones REDOX En una celda galvánica, la energía química se transforma en energía eléctrica para hacer un trabajo eléctrico. Energía eléctrica = carga x voltaje joules = coulombs x volts 1 J = 1 C x 1 V
29 Carga del electrón y constante de Faraday Energía eléctrica = carga total x potencial de celda Carga total = número de e- x carga de un e- La carga eléctrica de un mol de e- se denomina constante de Faraday (F). 1 F = 6, e- x 1, C mol e- e- 1 F = C/ mol e-
30 Trabajo eléctrico y potencial de celda La carga total se puede expresar como: Carga total = n. F n = número de moles F = constante de Faraday Y el trabajo realizado puede expresarse como: W = - n. F. E El signo indica que el trabajo lo realiza la celda sobre el entorno
31 Trabajo eléctrico y ΔG de reacción La energía disponible para realizar trabajo corresponde a la ΔG de una reacción. Entonces. ΔG = - n. F. E celda Como n y F son siempre +, a una E + corresponderá siempre una ΔG -. E + ΔG - Capacidad de realizar trabajo eléctrico
32 E y ΔG de reacción Si la reacción se realiza en condiciones estándar: ΔG = - n. F. E celda Y como ΔG se relaciona con la Keq según:. ΔG = - RT ln Keq - n. F. E celda = - RT ln Keq
33 E y ΔG de reacción Despejando en función de E celda: E celda = RT ln Keq nf
34
35 Espontaneidad de reacciones Redox DG 0 0 = -RT ln K = -n FE cell
36 Cuál es la constante de equilibrio para la reacción siguiente a 25 0 C? Fe 2+ (ac) + 2Ag (s) Fe (s) + 2Ag + (ac) E 0 celda = V n ln K Oxidación: Reducción: 2Ag 2Ag + + 2e - 2e - + Fe 2+ Fe n = 2 E 0 = E 0 Fe /Fe E0 2+ Ag + /Ag E 0 = (0.80) E 0 = V K = exp Eceldax 0 n V = exp V x V K = 1.23 x 10-42
37 Efecto de la concentración sobre la fem de la celda El cociente de masas Q influye en el valor de la ΔG según: DG = DG 0 + RT ln Q Y como la ΔG y ΔG están relacionadas con la E y la E según: DG = -nfe DG 0 = -nfe 0 -nfe = -nfe 0 + RT ln Q Ecuación de Nernst E = E 0 - RT nf ln Q A 298
38 Tendrá lugar la siguiente reacción de forma espontánea a 25 C si [Fe 2+ ] = 0.60 M y [Cd 2+ ] = M? Fe 2+ (ac) + Cd (s) Fe (s) + Cd 2+ (ac) Oxidación: Reducción: Cd Cd e - 2e - + Fe 2+ E 0 = E 0 Fe /Fe E0 2+ Cd 2+ /Cd Fe n = 2 E 0 = (-0.40) E 0 = V E = E 0 E = V V n ln Q V 2 ln E = E > 0 Espontáneo
39 IMPORTANCIA BIOLOGICA La capacidad de realizar trabajo en virtud del movimiento de electrones de especies con potenciales redox más negativos hacia otras con potenciales más positivos, constituye el principal mecanismo de obtención de energía en las mitocondrias, mediante la CADENA TRANSPORTADORA DE ELECTRONES. ΔG = - n. F. E celda E + ΔG - Capacidad de realizar trabajo eléctrico
40 IMPORTANCIA BIOLOGICA La capacidad de realizar trabajo en virtud del movimiento de electrones de especies con potenciales redox más negativos hacia otras con potenciales más positivos, constituye el principal mecanismo de obtención de energía en las mitocondrias, mediante la CADENA TRANSPORTADORA DE ELECTRONES. Mecanismo básico de obtención de energía de TODOS LOS SERES VIVOS AEROBIOS!
41 Cadena transportadora de electrones PASO 1 Oxidación de glucosa y ácidos grasos Síntesis de ATP PASO 2
42 Mayor carácter reductor Mayor carácter oxidante
43 De qué manera la CTE genera energía?. El transporte de electrones está gobernado por los potenciales de oxido reducción (E ). ΔE está relacionado con ΔG mediante la ecuación: ΔG = - n. F. ΔE Electrones fluyen de transportadores con valores de E negativos a otros con E positivos, es decir, de reductores a oxidantes (ΔE + ) Este transporte se asocia con una ΔG negativa.
44 De qué manera la CTE genera energía?. CTE se asocia con una ΔG negativa. Energía liberada se aprovecha para bombear H + de la matriz al espacio intermembrana en contra de gradiente de concentración (proceso con ΔG positivo) Gradiente protomotriz (gradiente electroquímico) Retorno de H + a través de ATP sintetasa genera ATP (fosforilación oxidativa)
45
46 Cadena transportadora de electrones PASO 1 Oxidación de glucosa y ácidos grasos Síntesis de ATP PASO 2
47 Transporte de electrones y producción de ATP La ΔG asociada al transporte de 1 mol de electrones a través de la CTE: DG = -n F E DG 0 = - 1 mol de e- x J x 1,14 V V. mol de e-. DG = J = DG = -110 kj La síntesis de ATP tiene ΔG : + 33 kj mol La energía liberada permite la síntesis de 3 moles de ATP por mol de electrones.
Unidad 6: ELECTROQUIMICA
 Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
ELECTROQUÍMICA. 1. Conceptos de oxidación-reducción
 ELECTROQUÍMICA 1. Conceptos de oxidación-reducción Oxidación: transformación en la que una especie química pierde electrones o gana oxígeno. Reducción: transformación en la que una especie química gana
ELECTROQUÍMICA 1. Conceptos de oxidación-reducción Oxidación: transformación en la que una especie química pierde electrones o gana oxígeno. Reducción: transformación en la que una especie química gana
Reacciones redox espontáneas
 Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox) 1 2 Tipos de reacciones redox (según su espontaneidad) Reacciones espontáneas: G
REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox) 1 2 Tipos de reacciones redox (según su espontaneidad) Reacciones espontáneas: G
QUÍMICA Reactividad y equilibrio químico. Oxido - reducción. Tutora: Romina Saavedra
 QUÍMICA Reactividad y equilibrio químico Oxido - reducción Tutora: Romina Saavedra Balance de reacciones de óxido reducción Una reacción redox o de óxido reducción se caracteriza por la existencia de dos
QUÍMICA Reactividad y equilibrio químico Oxido - reducción Tutora: Romina Saavedra Balance de reacciones de óxido reducción Una reacción redox o de óxido reducción se caracteriza por la existencia de dos
Tema 15: Equilibrio óxido-reducción Reacciones de oxidación-reducción (redox)
 : Equilibrio óxido-reducción 15.1 Reacciones de oxidación-reducción 15.2 Ajuste de reacciones redox: método del ión-electrón 15.3 Volumetrías redox. Indicadores. 15.4 Energía eléctrica asociada a procesos
: Equilibrio óxido-reducción 15.1 Reacciones de oxidación-reducción 15.2 Ajuste de reacciones redox: método del ión-electrón 15.3 Volumetrías redox. Indicadores. 15.4 Energía eléctrica asociada a procesos
4. Un agente oxidante (2 correctas) A) Toma electrones de otra sustancia B) Da electrones a otra sustancia C) Se oxida D) Se reduce
 CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
Celdas galvánicas o voltaicas
 Celdas galvánicas o voltaicas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es)
Celdas galvánicas o voltaicas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es)
Oxidación y Reducción
 Oxidación y Reducción Un poco de Historia En 1718 Georg Stahl propuso la existencia del Flogisto. Cuando un oxido se calienta en presencia de carbono absorben de la atmosfera al flogisto y al hacer combustión
Oxidación y Reducción Un poco de Historia En 1718 Georg Stahl propuso la existencia del Flogisto. Cuando un oxido se calienta en presencia de carbono absorben de la atmosfera al flogisto y al hacer combustión
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 REACCIONES DE TRANSFERENCIA DE ELECTRONES CONCEPTO DE OXIDACIÓNREDUCCIÓN Oxidaciónreducción: proceso en el que se producen transferencias o intercambios de electrones de unas sustancias a otras: una sustancia
REACCIONES DE TRANSFERENCIA DE ELECTRONES CONCEPTO DE OXIDACIÓNREDUCCIÓN Oxidaciónreducción: proceso en el que se producen transferencias o intercambios de electrones de unas sustancias a otras: una sustancia
Celdas Galvánicas y Electrolíticas
 Celdas Galvánicas y Electrolíticas Reacciones de óxido-reducción Reacciones en las cuales una o más de las sustancias intervinientes modifica su estado de oxidación. Znº (s) + Cu +2 (ac) Zn 2+ (ac) + Cuº
Celdas Galvánicas y Electrolíticas Reacciones de óxido-reducción Reacciones en las cuales una o más de las sustancias intervinientes modifica su estado de oxidación. Znº (s) + Cu +2 (ac) Zn 2+ (ac) + Cuº
9. Reacciones de oxidación-reducción
 9. Reacciones oxidación-reducción Conceptos básicos. Contenidos Estado de oxidación; oxidación y reducción; semirreacción; ajuste de reacciones redox; valoraciones redox Electroquímica. Serie electromotriz:
9. Reacciones oxidación-reducción Conceptos básicos. Contenidos Estado de oxidación; oxidación y reducción; semirreacción; ajuste de reacciones redox; valoraciones redox Electroquímica. Serie electromotriz:
Capítulo 18 Electroquímica
 Capítulo 18 Electroquímica Adaptado por: Ileana Nieves Martínez Corriente Eléctrica Corriente (i) de agua cantidad de agua que pasa en un periodo de tiempo Eléctrica cantidad de carga eléctrica (Q) que
Capítulo 18 Electroquímica Adaptado por: Ileana Nieves Martínez Corriente Eléctrica Corriente (i) de agua cantidad de agua que pasa en un periodo de tiempo Eléctrica cantidad de carga eléctrica (Q) que
POTENCIOMETRIA KCL. Cl - CELDAS GALVANICAS DEPOSITO DE COBRE SOBRE UNA LAMINA DE ZINC CELDA GALVANICA POTENCIALES REDOX CELDA GALVANICA
 POTENCIOMETRIA TOPICOS: Celdas galvánicas Potenciales estándar de electrodo Ecuación de Nernst Electrodos de referencia: primario y secundario Medición de ph Celdas electrolíticas Titulaciones potenciométricas
POTENCIOMETRIA TOPICOS: Celdas galvánicas Potenciales estándar de electrodo Ecuación de Nernst Electrodos de referencia: primario y secundario Medición de ph Celdas electrolíticas Titulaciones potenciométricas
ELECTROQUÍMICA. 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday.
 ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
CÓMO RESOLVER ALGUNOS EJERCICIOS DE ELECTROQUÍMICA (Parte 1)
 M. C. Q. Alfredo Velásquez Márquez Profesor de la Facultad de Ingeniería de la UNAM velasquez777@yahoo.com.mx CÓMO RESOLVER ALGUNOS EJERCICIOS DE ELECTROQUÍMICA (Parte 1) Cuando en una reacción química
M. C. Q. Alfredo Velásquez Márquez Profesor de la Facultad de Ingeniería de la UNAM velasquez777@yahoo.com.mx CÓMO RESOLVER ALGUNOS EJERCICIOS DE ELECTROQUÍMICA (Parte 1) Cuando en una reacción química
Es el análisis cuantitativo de la forma en que los organismos adquieren y utilizan la energía.
 BIOENERGÉTICA BIOENERGÉTICA Es el análisis cuantitativo de la forma en que los organismos adquieren y utilizan la energía. 1. Conservación de la energía: La energía puede cambiar de forma, pero no puede
BIOENERGÉTICA BIOENERGÉTICA Es el análisis cuantitativo de la forma en que los organismos adquieren y utilizan la energía. 1. Conservación de la energía: La energía puede cambiar de forma, pero no puede
Capítulo 19 Electroquímica
 Capítulo 19 Electroquímica En este capítulo se estudian los conceptos elaborados por la termodinámica para describir la conversión de energía química a energía eléctrica. Al terminar este capítulo, el
Capítulo 19 Electroquímica En este capítulo se estudian los conceptos elaborados por la termodinámica para describir la conversión de energía química a energía eléctrica. Al terminar este capítulo, el
Reacciones de oxido reducción
 Reacciones de oxido reducción Oxidación pérdida de electrones Reducción ganancia de electrones Las reacciones de oxido reducción tienen lugar mediante intercambio de electrones Ej.: Zn(s) + 2 H + (ac)
Reacciones de oxido reducción Oxidación pérdida de electrones Reducción ganancia de electrones Las reacciones de oxido reducción tienen lugar mediante intercambio de electrones Ej.: Zn(s) + 2 H + (ac)
LAS REACCIONES DE OXIDACIÓN-REDUCCIÓN
 LAS REACCIONES DE OXIDACIÓN-REDUCCIÓN Introducción 1.- Concepto de oxidación y reducción 1.1. Oxidantes y reductores 2.- Estado de oxidación.. 3.- Ajuste de ecuaciones redox. 3.1. Reacciones en medio ácido.
LAS REACCIONES DE OXIDACIÓN-REDUCCIÓN Introducción 1.- Concepto de oxidación y reducción 1.1. Oxidantes y reductores 2.- Estado de oxidación.. 3.- Ajuste de ecuaciones redox. 3.1. Reacciones en medio ácido.
Bioquímica Termodinámica y bioenergética.
 Bioquímica Termodinámica y bioenergética. Facultad de Enfermería Universidad de la República ESFUNO 2014 Amalia Ávila Termodinámica y bioenergética Los organismos vivos no se encuentran en equilibrio con
Bioquímica Termodinámica y bioenergética. Facultad de Enfermería Universidad de la República ESFUNO 2014 Amalia Ávila Termodinámica y bioenergética Los organismos vivos no se encuentran en equilibrio con
REACCIONES DE OXIDACIÓN-REDUCCIÓN
 10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS ACTIVIDADES PRPUESTAS EN EL INTERIR DE LA UNIDAD 1 Por qué en los procesos redox no puede existir una única semirreacción de oxidación o de reducción?
10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS ACTIVIDADES PRPUESTAS EN EL INTERIR DE LA UNIDAD 1 Por qué en los procesos redox no puede existir una única semirreacción de oxidación o de reducción?
Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA
 Trabajo Práctico Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA UNIVERSIDAD TECNOLÓGICA NACIONAL Regional Rosario En el presente se desarrolla una propuesta de trabajo práctico para realizar con los estudiantes
Trabajo Práctico Tema: Electroquímica CÁTEDRA DE FISICOQUÍMICA UNIVERSIDAD TECNOLÓGICA NACIONAL Regional Rosario En el presente se desarrolla una propuesta de trabajo práctico para realizar con los estudiantes
Reacciones de transferencia de electrones
 DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA 2º DE BACHILLERATO Actividades tema 8 Reacciones de transferencia de electrones Reacciones de oxidación-reducción 1.-Asigna el número
DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA 2º DE BACHILLERATO Actividades tema 8 Reacciones de transferencia de electrones Reacciones de oxidación-reducción 1.-Asigna el número
Electroquímica Reacciones REDOX
 QUÍMICA GENERAL 2011 Universidad Nacional de Cuyo Instituto de Ciencias Básicas Electroquímica Reacciones REDOX Prof. Dr. Rafael P. Fernandez rpfernandez@uncu.edu.ar Resumen de la Presentación Introducción
QUÍMICA GENERAL 2011 Universidad Nacional de Cuyo Instituto de Ciencias Básicas Electroquímica Reacciones REDOX Prof. Dr. Rafael P. Fernandez rpfernandez@uncu.edu.ar Resumen de la Presentación Introducción
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción. Ajuste de reacciones de oxidación-reducción.
 Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
OXIDACIÓN-REDUCCIÓN. PAU-tipos de problemas
 OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
REACCIONES DE INTERCAMBIO DE ELECTRONES EJERCICIOS PARA RESOLVER
 2010 REACCIONES DE INTERCAMBIO DE ELECTRONES EJERCICIOS PARA RESOLVER Mª Teresa Gómez Ruiz IES Politécnico Cartagena Dpto Física Química 15/09/2010 ÍNDICE Página EJERCICIOS DE ELECTROQUÍMICA (Nª 1 Nª6)
2010 REACCIONES DE INTERCAMBIO DE ELECTRONES EJERCICIOS PARA RESOLVER Mª Teresa Gómez Ruiz IES Politécnico Cartagena Dpto Física Química 15/09/2010 ÍNDICE Página EJERCICIOS DE ELECTROQUÍMICA (Nª 1 Nª6)
EJERCICIOS RESUELTOS DE REDOX
 EJERCICIOS RESUELTOS DE REDOX 1. Al hacer reaccionar cobre metálico con ácido nítrico diluido se obtiene monóxido de nitrógeno y nitrato de cobre (II). Plantee, iguale y complete la ecuación redox correspondiente,
EJERCICIOS RESUELTOS DE REDOX 1. Al hacer reaccionar cobre metálico con ácido nítrico diluido se obtiene monóxido de nitrógeno y nitrato de cobre (II). Plantee, iguale y complete la ecuación redox correspondiente,
Pilas electrolíticas
 Pilas electrolíticas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B. (smorais@qim.upv.es)
Pilas electrolíticas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B. (smorais@qim.upv.es)
QUÍMICA ANALÍTICA I. Etapa analítica. Análisis volumétrico : Titulaciones de óxido-reducción
 QUÍMICA ANALÍTICA I Etapa analítica Análisis volumétrico : Titulaciones de óxido-reducción Equilibrio Redox Ce(IV) Ce 4+ + Fe 2+ Ce 3+ + Fe 3+ Otra reacción: MnO 2-4 + 5 Fe 2+ + 8 H + Mn 2+ + 5 Fe 3+ +
QUÍMICA ANALÍTICA I Etapa analítica Análisis volumétrico : Titulaciones de óxido-reducción Equilibrio Redox Ce(IV) Ce 4+ + Fe 2+ Ce 3+ + Fe 3+ Otra reacción: MnO 2-4 + 5 Fe 2+ + 8 H + Mn 2+ + 5 Fe 3+ +
PILAS ELECTROQUÍMICAS
 PILAS ELECTROQUÍMICAS Las pilas electroquímicas se llaman también células galvánicas, células electroquímicas, pilas galvánicas, pilas voltaicas, pilas eléctricas o, simplemente, pilas. Como ya hemos visto,
PILAS ELECTROQUÍMICAS Las pilas electroquímicas se llaman también células galvánicas, células electroquímicas, pilas galvánicas, pilas voltaicas, pilas eléctricas o, simplemente, pilas. Como ya hemos visto,
TEMA 9: REACCIONES DE TRANSFERENCIA DE ELECTRONES.
 TEMA 9: REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1.- Conceptos de oxidación y reducción. Tradicionalmente decimos que un metal, o un elemento en general se oxida, cuando reacciona con oxígeno para dar
TEMA 9: REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1.- Conceptos de oxidación y reducción. Tradicionalmente decimos que un metal, o un elemento en general se oxida, cuando reacciona con oxígeno para dar
PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO.
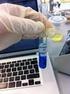 PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO. El concepto de Electroquímica implica transformaciones que requieren la presencia de electrodos. Dos electrodos sumergidos en un electrólito y unidos
PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO. El concepto de Electroquímica implica transformaciones que requieren la presencia de electrodos. Dos electrodos sumergidos en un electrólito y unidos
QUÍMICA 2º Bachillerato Ejercicios: Electroquímica
 1(8) Ejercicio nº 1 Considera la reacción: Cu(s) + 2Ag + (aq) Cu +2 (aq) + 2Ag(s) a) Escribe las semirreacciones de oxidación y de reducción c) Escribe el esquema de la pila que se puede formar con dicha
1(8) Ejercicio nº 1 Considera la reacción: Cu(s) + 2Ag + (aq) Cu +2 (aq) + 2Ag(s) a) Escribe las semirreacciones de oxidación y de reducción c) Escribe el esquema de la pila que se puede formar con dicha
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: POTENCIALES DE ELECTRODOS. PILAS 1.-/ Cuál es el potencial normal de una pila que utiliza los pares Zn 2+ /Zn y Ag + /Ag? Cuál es la polaridad de cada electrodo?
REACCIONES DE TRANSFERENCIA DE ELECTRONES: POTENCIALES DE ELECTRODOS. PILAS 1.-/ Cuál es el potencial normal de una pila que utiliza los pares Zn 2+ /Zn y Ag + /Ag? Cuál es la polaridad de cada electrodo?
PRERREQUISITOS Oxidorreducción, número de oxidación, hemirreacciones, leyes de Faraday, Ecuación de Nernst, Celdas electrolíticas y pilas voltaicas.
 CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 11 TEMA: ELECTROQUÍMICA OBJETIVOS Aplicar los conocimientos de procesos redox en ejercicios prácticos. Constatar el poder oxidante y reductor de las sustancias. Manejar
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 11 TEMA: ELECTROQUÍMICA OBJETIVOS Aplicar los conocimientos de procesos redox en ejercicios prácticos. Constatar el poder oxidante y reductor de las sustancias. Manejar
TEMA 8: REACCIONES REDOX O DE TRANSFERENCIA DE ELECTRONES
 TEMA 8: REACCIONES REDOX O DE TRANSFERENCIA DE ELECTRONES 1. Concepto de oxidación y reducción El término OXIDACIÓN comenzó a usarse para indicar que un compuesto incrementaba la proporción de átomos de
TEMA 8: REACCIONES REDOX O DE TRANSFERENCIA DE ELECTRONES 1. Concepto de oxidación y reducción El término OXIDACIÓN comenzó a usarse para indicar que un compuesto incrementaba la proporción de átomos de
Unidad 7 Redox. La ecuación iónica sin ajustar con los números de oxidación:
 OPCIÓN A Unidad 7 Redox 1. Indique cual es el oxidante y cual es el reductor en los siguientes procesos de oxidación-reducción, sin ajustar: (2 p) El oxidante será aquel elemento que gane electrones (se
OPCIÓN A Unidad 7 Redox 1. Indique cual es el oxidante y cual es el reductor en los siguientes procesos de oxidación-reducción, sin ajustar: (2 p) El oxidante será aquel elemento que gane electrones (se
FÍSICA 3 TEMA 3 Resumen teórico. Electroquímica
 Electroquímica OXIDACIÓN Y REDUCCIÓN Conceptos electrónicos de oxidación y reducción Reacciones Aplicaciones Como ya sabes, los átomos de los diversos elementos están formatos por un núcleo con protones
Electroquímica OXIDACIÓN Y REDUCCIÓN Conceptos electrónicos de oxidación y reducción Reacciones Aplicaciones Como ya sabes, los átomos de los diversos elementos están formatos por un núcleo con protones
INSTITUTO TECNOLÓGICO de Durango ELECTROQUÍMICA FISICOQUÍMICA 2. Dr. Carlos Francisco Cruz Fierro. Revisión Fisicoquímica 2.
 INSTITUTO TECNOLÓGICO de Durango ELECTROQUÍMICA FISICOQUÍMICA 2 Dr. Carlos Francisco Cruz Fierro Revisión 1 69156.17 7-ene-13 1 Electroquímica Relación entre la electricidad y la química Involucra la medición
INSTITUTO TECNOLÓGICO de Durango ELECTROQUÍMICA FISICOQUÍMICA 2 Dr. Carlos Francisco Cruz Fierro Revisión 1 69156.17 7-ene-13 1 Electroquímica Relación entre la electricidad y la química Involucra la medición
TEMA 8. Conceptos y Procesos Redox. TEMA 8. Conceptos y Procesos Redox.
 TEMA 8. Conceptos y Procesos Redox. TEMA 8. Conceptos y Procesos Redox. 1-.Oxidación-reducción. Principios Generales. 1.1. 1.1. Semireacciones. 1.2. 1.2. Reacciones de de desproporción. 2-.Procesos Redox
TEMA 8. Conceptos y Procesos Redox. TEMA 8. Conceptos y Procesos Redox. 1-.Oxidación-reducción. Principios Generales. 1.1. 1.1. Semireacciones. 1.2. 1.2. Reacciones de de desproporción. 2-.Procesos Redox
EQUILIBRIOS REDOX Estudio de reacciones redox: celdas electroquímicas -Transferencia de electrones
 EQUILIBRIOS REDOX Estudio de reacciones redox: celdas electroquímicas -Transferencia de electrones Química Analítica e Instrumental II 2012 Prof. Juan Carlos Sturm S. La pila de Volta 1801 Una reacción
EQUILIBRIOS REDOX Estudio de reacciones redox: celdas electroquímicas -Transferencia de electrones Química Analítica e Instrumental II 2012 Prof. Juan Carlos Sturm S. La pila de Volta 1801 Una reacción
TEMA 3: Equilibrios redox
 TEMA 3: Equilibrios redox Índice 1) Concepto potencial redox. 2) Pila galvánica. 3) Ecuación de Nernst. 4) Espontaneidad y equilibrio. 5) Influencia del ph en el potencial de electrodo. 6) Reacciones de
TEMA 3: Equilibrios redox Índice 1) Concepto potencial redox. 2) Pila galvánica. 3) Ecuación de Nernst. 4) Espontaneidad y equilibrio. 5) Influencia del ph en el potencial de electrodo. 6) Reacciones de
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción A Reserva, Ejercicio 6, Opción B
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción A Reserva, Ejercicio 6, Opción B
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA
 ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
Práctica: Descomponer la molécula del agua mediante el proceso de la electrólisis. Marco de referencia.
 Todo obstáculo cede al esfuerzo persistente, predeterminado. Leonardo Da Vinci. Práctica: Descomponer la molécula del agua mediante el proceso de la electrólisis. Marco de referencia. En los procesos electroquímicos,
Todo obstáculo cede al esfuerzo persistente, predeterminado. Leonardo Da Vinci. Práctica: Descomponer la molécula del agua mediante el proceso de la electrólisis. Marco de referencia. En los procesos electroquímicos,
REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015
 REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015 1- El permanganato de potasio actúa como oxidante en medio ácido, dando como producto Mn 2+. Por el contrario, como oxidante en medio básico el
REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015 1- El permanganato de potasio actúa como oxidante en medio ácido, dando como producto Mn 2+. Por el contrario, como oxidante en medio básico el
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción B Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio 5, Opción A
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción B Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio 5, Opción A
Tema 10: Oxidación-reduccción
 Tema 10: Oxidación-reduccción Francisco García Calvo-Flores Contents 21-1 Electrode Potentials and Their Measurement 21-2 Standard Electrode Potentials 21-3 E cell, ΔG, and K eq 21-4 E cell as a Function
Tema 10: Oxidación-reduccción Francisco García Calvo-Flores Contents 21-1 Electrode Potentials and Their Measurement 21-2 Standard Electrode Potentials 21-3 E cell, ΔG, and K eq 21-4 E cell as a Function
Reacciones Redox. Química General e Inorgánica Ingeniería Ambiental
 Reacciones Redox Hasta esta guía hemos aprendido a balancear ecuaciones químicas sencillas por tanteo, pero muchas ecuaciones son demasiado complejas para que este procedimiento de balanceo por tanteo
Reacciones Redox Hasta esta guía hemos aprendido a balancear ecuaciones químicas sencillas por tanteo, pero muchas ecuaciones son demasiado complejas para que este procedimiento de balanceo por tanteo
TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX
 TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX E1A.S2012 El dióxido de manganeso reacciona en medio hidróxido potásico con clorato de potasio para dar permanganato de potasio, cloruro de potasio
TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX E1A.S2012 El dióxido de manganeso reacciona en medio hidróxido potásico con clorato de potasio para dar permanganato de potasio, cloruro de potasio
UNIDAD 5. REACCIONES DE TRANSFERENCIA DE ELECTRONES
 UNIDAD 5. REACCIONES DE TRANSFERENCIA DE ELECTRONES I Oxidación y reducción Número de oxidación Ajuste de reacciones redox Cálculos estequiométricos Volumetrías redox Pilas electroquímicas Procesos electrolíticos.
UNIDAD 5. REACCIONES DE TRANSFERENCIA DE ELECTRONES I Oxidación y reducción Número de oxidación Ajuste de reacciones redox Cálculos estequiométricos Volumetrías redox Pilas electroquímicas Procesos electrolíticos.
La electroquímica es la rama de la química que estudia la conversión entre la energía eléctrica y la energía química
 7. Reacciones Redox La electroquímica es la rama de la química que estudia la conversión entre la energía eléctrica y la energía química Los procesos electroquímicos son reacciones redox en las cuales
7. Reacciones Redox La electroquímica es la rama de la química que estudia la conversión entre la energía eléctrica y la energía química Los procesos electroquímicos son reacciones redox en las cuales
TEMA 8. Conceptos y Procesos Redox. Esas reglas son las mismas que hemos empleado en formulación:
 TEMA 8. Conceptos y Procesos Redox. 1-.Oxidación-reducción. Principios Generales. 1.1. Semireacciones. 1.. Reacciones de desproporción. -.Procesos Redox espontáneos. Celdas voltaicas. 3-.Potencial y energía
TEMA 8. Conceptos y Procesos Redox. 1-.Oxidación-reducción. Principios Generales. 1.1. Semireacciones. 1.. Reacciones de desproporción. -.Procesos Redox espontáneos. Celdas voltaicas. 3-.Potencial y energía
Reacciones de transferencia de electrones
 Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
Un área importante en el estudio de las ciencias es la Termodinámica y un aspecto de este estudio, relacionado con los cambios químicos, es la
 Termoquímica. Todos los cambios que experimenta la materia, sean físicos o químicos, deben satisfacer principios fundamentales: conservación de la masa conservación de la energía Un área importante en
Termoquímica. Todos los cambios que experimenta la materia, sean físicos o químicos, deben satisfacer principios fundamentales: conservación de la masa conservación de la energía Un área importante en
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio 5, Opción A Reserva 3, Ejercicio 3, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio 5, Opción A Reserva 3, Ejercicio 3, Opción
Limitaciones de la 1ra. ley de la termodinámica
 Termodinámica Tema 9 (segunda parte) Química General e Inorgánica A Limitaciones de la 1ra. ley de la termodinámica Procesos espontáneos o irreversibles Una cascada corre cuesta abajo Un terrón de azúcar
Termodinámica Tema 9 (segunda parte) Química General e Inorgánica A Limitaciones de la 1ra. ley de la termodinámica Procesos espontáneos o irreversibles Una cascada corre cuesta abajo Un terrón de azúcar
Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante
 Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante Objetivos: Los estudiantes serán capaces de Definir oxidación y reducción en términos de pérdida o ganancia de electrones. Describir
Actividad de Química: Electroquímica Celdas Galvánicas Guía del Estudiante Objetivos: Los estudiantes serán capaces de Definir oxidación y reducción en términos de pérdida o ganancia de electrones. Describir
OXIDACIÓN-REDUCCIÓN 1. ESTADO DE OXIDACIÓN (E.O.) (O NÚMERO DE OXIDACIÓN).
 OXIDACIÓN-REDUCCIÓN 1. ESTADO DE OXIDACIÓN (E.O.) (O NÚMERO DE OXIDACIÓN). Es la carga que tendría un átomo si todos sus enlaces fueran iónicos, es decir, considerando todos los enlaces covalentes polares
OXIDACIÓN-REDUCCIÓN 1. ESTADO DE OXIDACIÓN (E.O.) (O NÚMERO DE OXIDACIÓN). Es la carga que tendría un átomo si todos sus enlaces fueran iónicos, es decir, considerando todos los enlaces covalentes polares
TEMA 6 Introducción a la Bioenergética
 TEMA 6 Introducción a la Bioenergética 1. Repaso de conceptos importantes 2. Acoplamiento entre las reacciones endergónicas y exergónicas 3. Sistema ATP/ADP 4. Termodinámica del transporte a través de
TEMA 6 Introducción a la Bioenergética 1. Repaso de conceptos importantes 2. Acoplamiento entre las reacciones endergónicas y exergónicas 3. Sistema ATP/ADP 4. Termodinámica del transporte a través de
El E.O. no tiene porqué ser la carga real que tiene un átomo, aunque a veces coincide.
 EQUILIBRIOS DE OXIDACIÓN-REDUCCIÓN (REDOX) 2º BACHILLERATO QUÍMICA 1.- Estado de oxidación. 2.- Concepto de oxidación y reducción. 3.- Ajuste de ecuaciones redox por el método del ión-electrón. 3.1. Reacciones
EQUILIBRIOS DE OXIDACIÓN-REDUCCIÓN (REDOX) 2º BACHILLERATO QUÍMICA 1.- Estado de oxidación. 2.- Concepto de oxidación y reducción. 3.- Ajuste de ecuaciones redox por el método del ión-electrón. 3.1. Reacciones
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
ELECTRÓLISIS. Electrólisis de sales fundidas
 El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
OXIDACIÓN REDUCCIÓN QCA 09 ANDALUCÍA
 OXIDACIÓN REDUCCIÓN QCA 9 ANDALUCÍA.- Sea una pila constituida, en condiciones estándar, por un electrodo de plata sumergido en una disolución de nitrato de plata y un electrodo de cadmio sumergido en
OXIDACIÓN REDUCCIÓN QCA 9 ANDALUCÍA.- Sea una pila constituida, en condiciones estándar, por un electrodo de plata sumergido en una disolución de nitrato de plata y un electrodo de cadmio sumergido en
Problemas de electrolisis. Resueltos
 Problemas de electrolisis Resueltos Problemas 5,6 y 7 de la hoja de refuerzo Tambien estan al final de la hoja con enunciados de ejecicios PAU Serie refuerzo electroquímica 5 Se realiza la electrólisis
Problemas de electrolisis Resueltos Problemas 5,6 y 7 de la hoja de refuerzo Tambien estan al final de la hoja con enunciados de ejecicios PAU Serie refuerzo electroquímica 5 Se realiza la electrólisis
MATERIAL DIDACTICO REACCIONES QUÍMICAS
 REACCIONES QUÍMICAS La ecuación química balanceada es una ecuación algebraica con todos los reaccionantes en el primer miembro y todos los productos en el segundo miembro por esta razón el signo igual
REACCIONES QUÍMICAS La ecuación química balanceada es una ecuación algebraica con todos los reaccionantes en el primer miembro y todos los productos en el segundo miembro por esta razón el signo igual
REACCIONES QUÍMICAS. Concepto Ley de Acción de masas Tipos de reacciones Ejemplos
 REACCIONES QUÍMICAS Concepto Ley de Acción de masas Tipos de reacciones Ejemplos Objetivos Apropiarse de la importancia de las reacciones químicas. Describir e identificar de reacciones químicas. los diferentes
REACCIONES QUÍMICAS Concepto Ley de Acción de masas Tipos de reacciones Ejemplos Objetivos Apropiarse de la importancia de las reacciones químicas. Describir e identificar de reacciones químicas. los diferentes
Universidad Nacional Autónoma de México Facultad de Química
 Universidad Nacional Autónoma de México Facultad de Química Departamento de Fisicoquímica Laboratorio de Termodinámica POTENCIALES TERMODINÁMICOS Elaborado por: M. en C. Gerardo Omar Hernández Segura OBJETIVO
Universidad Nacional Autónoma de México Facultad de Química Departamento de Fisicoquímica Laboratorio de Termodinámica POTENCIALES TERMODINÁMICOS Elaborado por: M. en C. Gerardo Omar Hernández Segura OBJETIVO
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES.
 TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
ELECTROQUÍMICA. 1- Concepto de potencial normal. Electrodo de referencia
 ELECTROQUÍMICA 1 Concepto de potencial normal. Electrodo de referencia 2 Se forma una pila con un electrodo de níquel y otro de plata. Indica el electrodo que eléctricamente es el polo positivo, el que
ELECTROQUÍMICA 1 Concepto de potencial normal. Electrodo de referencia 2 Se forma una pila con un electrodo de níquel y otro de plata. Indica el electrodo que eléctricamente es el polo positivo, el que
2 + b. Para oxidar el ión bromuro a bromo molecular, se necesita una reducción cuyo potencial sea superior a 1,06 v.
 Septiembre 013. Pregunta B3.- Para llevar a cabo los procesos indicados en los apartados a) y b) se dispone de cloro y iodo moleculares. Explique cuál de estas dos sustancias se podría utilizar en cada
Septiembre 013. Pregunta B3.- Para llevar a cabo los procesos indicados en los apartados a) y b) se dispone de cloro y iodo moleculares. Explique cuál de estas dos sustancias se podría utilizar en cada
Tema 12 Termoquímica. Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad En qué dirección se produce? Reacciones Químicas
 Tema 1 Estequiometría Cuánto se produce? Cuánto reacciona? Tema 15 Equilibrio Cuándo se alcanza? Cómo modificarlo? Tema 12 Termoquímica Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad
Tema 1 Estequiometría Cuánto se produce? Cuánto reacciona? Tema 15 Equilibrio Cuándo se alcanza? Cómo modificarlo? Tema 12 Termoquímica Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad
Clase 4 Metabolismo bacteriano
 Clase 4 Metabolismo bacteriano Composición química de las bacterias. Fuentes de carbono y energía. Categorías nutricionales. Catabolismo y anabolismo. Reacciones de óxido-reducción, torre de electrones,
Clase 4 Metabolismo bacteriano Composición química de las bacterias. Fuentes de carbono y energía. Categorías nutricionales. Catabolismo y anabolismo. Reacciones de óxido-reducción, torre de electrones,
TEMA 10 Corrosión Electroquímica
 TEMA 10 Corrosión Electroquímica ÍNDICE 1. Fundamentos de Corrosión 2. Corrosión electroquímica 3. Pilas de corrosión 4. Influencia de las heterogeneidades 5. Cinética de Corrosión 6. Métodos de Protección
TEMA 10 Corrosión Electroquímica ÍNDICE 1. Fundamentos de Corrosión 2. Corrosión electroquímica 3. Pilas de corrosión 4. Influencia de las heterogeneidades 5. Cinética de Corrosión 6. Métodos de Protección
Capítulo 7: Reacciones de oxidación-reducción
 Capítulo 7: Reacciones de oxidación-reducción ACTIVIDADES DE RECAPITULACIÓN 1*. Indica, razonadamente, si cada una de las siguientes transformaciones es una reacción redox, identificando, en su caso, el
Capítulo 7: Reacciones de oxidación-reducción ACTIVIDADES DE RECAPITULACIÓN 1*. Indica, razonadamente, si cada una de las siguientes transformaciones es una reacción redox, identificando, en su caso, el
PRÁCTICA Nº 9 y 10 CORROSIÓN I
 PRÁCTICA Nº 9 y 10 CORROSIÓN I OBJETO DE LA PRÁCTICA: CONCEPTO DE ÁNODO Y CÁTODO APLICACIÓN A TRES REACCIONES REDOX CONCEPTO DE ENERGÍA ELÉCTRICA ASOCIADA A CAMBIOS QUÍMICOS Y VICEVERSA REACCIÓN ESPONTÁNEA
PRÁCTICA Nº 9 y 10 CORROSIÓN I OBJETO DE LA PRÁCTICA: CONCEPTO DE ÁNODO Y CÁTODO APLICACIÓN A TRES REACCIONES REDOX CONCEPTO DE ENERGÍA ELÉCTRICA ASOCIADA A CAMBIOS QUÍMICOS Y VICEVERSA REACCIÓN ESPONTÁNEA
REACCIONES DE OXIDACIÓN-REDUCCIÓN
 10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS ACTIVIDADES DE FINAL DE UNIDAD Generales sobre oxidación-reducción 1. Determina los estados de oxidación del azufre en las siguientes sustancias: H 2 S;
10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS ACTIVIDADES DE FINAL DE UNIDAD Generales sobre oxidación-reducción 1. Determina los estados de oxidación del azufre en las siguientes sustancias: H 2 S;
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
de todos los dados el correcto será el: a) A b) B c) C d) D
 Redox 3 41*. Uno de los experimentos que puedes hacer perfectamente en el laboratorio y que te permitiría recordar el proceso de la pila Daniell, sería sumergir una lámina o chapa de cinc en un vaso de
Redox 3 41*. Uno de los experimentos que puedes hacer perfectamente en el laboratorio y que te permitiría recordar el proceso de la pila Daniell, sería sumergir una lámina o chapa de cinc en un vaso de
Actividad 4. Leccion evaluativa de la unidad UNO
 Actividad 4. Leccion evaluativa de la unidad UNO En una reacción de oxidación/reducción a veces llamadas reacciones redox, los electrones se transfieren de un reactivo a otro. Ocurren reacciones de oxidación
Actividad 4. Leccion evaluativa de la unidad UNO En una reacción de oxidación/reducción a veces llamadas reacciones redox, los electrones se transfieren de un reactivo a otro. Ocurren reacciones de oxidación
Reacciones Químicas. Cambia, todo cambia
 Reacciones Químicas Cambia, todo cambia Reacciones químicas - significado A + B C + D reactivos condiciones catalizadores productos H 2 + Cl 2 HCl Reacciones químicas - significado Ley de conservación
Reacciones Químicas Cambia, todo cambia Reacciones químicas - significado A + B C + D reactivos condiciones catalizadores productos H 2 + Cl 2 HCl Reacciones químicas - significado Ley de conservación
UD 3. Las Reacciones químicas. 1-Reacciones y ecuaciones químicas
 UD 3. Las Reacciones químicas 1- Reacciones y ecuaciones químicas. 2- Tipos de reacciones químicas y reacciones químicas importantes. 3- Cálculos estequiométricos. 1-Reacciones y ecuaciones químicas Una
UD 3. Las Reacciones químicas 1- Reacciones y ecuaciones químicas. 2- Tipos de reacciones químicas y reacciones químicas importantes. 3- Cálculos estequiométricos. 1-Reacciones y ecuaciones químicas Una
rincones.educarex.es
 rincones.educarex.es Rama de la química que estudia la energía eléctrica y la energía química. Si la reacción química es capaz de producir electricidad se habla de una pila electroquímica la relación entre
rincones.educarex.es Rama de la química que estudia la energía eléctrica y la energía química. Si la reacción química es capaz de producir electricidad se habla de una pila electroquímica la relación entre
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 014 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio, Opción A Reserva,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 014 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio, Opción A Reserva,
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Junio 2009 PRIMERA PARTE
 1 PAU Química. Junio 2009 PRIMERA PARTE Cuestión 1. La primera y segunda energía de ionización para el átomo A, cuya configuración electrónica es 1s 2 2s 1, son 520 y 7300 kj mol 1, respectivamente: a)
1 PAU Química. Junio 2009 PRIMERA PARTE Cuestión 1. La primera y segunda energía de ionización para el átomo A, cuya configuración electrónica es 1s 2 2s 1, son 520 y 7300 kj mol 1, respectivamente: a)
SISTEMAS REDOX REACCIONES REDOX
 SISTEMAS REDOX REACCIONES REDOX Existe una familia muy amplia de reacciones que se producen con la pérdida formal de electrones de un átomo y su ganancia por otro átomo. Como la ganancia de electrones
SISTEMAS REDOX REACCIONES REDOX Existe una familia muy amplia de reacciones que se producen con la pérdida formal de electrones de un átomo y su ganancia por otro átomo. Como la ganancia de electrones
Me n+ + O 2- Me a O b
 4. CORROSION Oxidación Me n Me n+ a) Oxidación (con ausencia de humedad) b) Corrosión electroquímica (en ambiente corrosivo) O 2 + n O 2- Me n+ + O 2- Me a O b Fig 4-1 Velocidad de oxidación (dx/dt): temperatura
4. CORROSION Oxidación Me n Me n+ a) Oxidación (con ausencia de humedad) b) Corrosión electroquímica (en ambiente corrosivo) O 2 + n O 2- Me n+ + O 2- Me a O b Fig 4-1 Velocidad de oxidación (dx/dt): temperatura
Reacciones redox Pedro L. Rodríguez Porca v. 1.0 2013
 Reacciones redox 1. Introducción 2. Concepto tradicional de oxidación y reducción 3. Número de oxidación 4. Concepto electrónico de oxidación-reducción 5. Ajuste de ecuaciones químicas redox 6. Estequiometría
Reacciones redox 1. Introducción 2. Concepto tradicional de oxidación y reducción 3. Número de oxidación 4. Concepto electrónico de oxidación-reducción 5. Ajuste de ecuaciones químicas redox 6. Estequiometría
METABOLISMO Y BIOENERGÉTICA BIOQUÍMICA. CAPÍTULO 14
 METABOLISMO Y BIOENERGÉTICA BIOQUÍMICA. CAPÍTULO 14 METABOLISMO Estudio de las reacciones bioquímicas que se llevan a cabo, incluidas su coordinación, regulación y necesidades energéticas. La energía que
METABOLISMO Y BIOENERGÉTICA BIOQUÍMICA. CAPÍTULO 14 METABOLISMO Estudio de las reacciones bioquímicas que se llevan a cabo, incluidas su coordinación, regulación y necesidades energéticas. La energía que
QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA
 QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
1.1 Introducción a la naturaleza corpuscular de la materia y al cambio químico.
 Unidad Educativa Monte Tabor-Nazaret Área de Ciencias Experimentales NNN Temario Exámen Supletorio Química NM II BACHILLERATO EXPERIMENTALES 1-2 2015-2016 Tema 1: Relaciones estequiométricas 1.1 Introducción
Unidad Educativa Monte Tabor-Nazaret Área de Ciencias Experimentales NNN Temario Exámen Supletorio Química NM II BACHILLERATO EXPERIMENTALES 1-2 2015-2016 Tema 1: Relaciones estequiométricas 1.1 Introducción
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre Fase específica OPCIÓN A
 1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
UNIVERSIDAD DEL ZULIA FACULTAD DE INGENIERÍA CICLO BÁSICO CONTENIDO PROGRAMÁTICO UNIDAD CURRICULAR: QUÍMICA II. CÓDIGO Nro
 UNIVERSIDAD DEL ZULIA FACULTAD DE INGENIERÍA CICLO BÁSICO CONTENIDO PROGRAMÁTICO UNIDAD CURRICULAR: QUÍMICA II CÓDIGO Nro. 200302 FECHA DE ACTUALIZACIÓN: I PERÍODO AÑO 2012 PROGRAMA DE QUÍMICA II Unidad
UNIVERSIDAD DEL ZULIA FACULTAD DE INGENIERÍA CICLO BÁSICO CONTENIDO PROGRAMÁTICO UNIDAD CURRICULAR: QUÍMICA II CÓDIGO Nro. 200302 FECHA DE ACTUALIZACIÓN: I PERÍODO AÑO 2012 PROGRAMA DE QUÍMICA II Unidad
Formación de ATP por la cadena transportadora de electrones Fotosíntesis. Capítulo 17 Bioquímica
 Formación de ATP por la cadena transportadora de electrones Fotosíntesis Capítulo 17 Bioquímica Introducción La oxidación de glucosa, por glucólisis, la oxidación del piruvato y el ciclo del ácido cítrico
Formación de ATP por la cadena transportadora de electrones Fotosíntesis Capítulo 17 Bioquímica Introducción La oxidación de glucosa, por glucólisis, la oxidación del piruvato y el ciclo del ácido cítrico
Introducción al. metabolismo
 Introducción al metabolismo H2O Para mantener su organización los sistemas vivos requieren suministro energía El Sol es la fuente original de esta energía. Al oxidar los nutrientes, convierten la energía
Introducción al metabolismo H2O Para mantener su organización los sistemas vivos requieren suministro energía El Sol es la fuente original de esta energía. Al oxidar los nutrientes, convierten la energía
Estudia la velocidad a la que ocurren las reacciones químicas
 www.clasesalacarta.com Cinética Química Estudia la velocidad a la que ocurren las reacciones químicas Termodinámica Es espontánea? Cinética A qué velocidad ocurre la reacción? Velocidad de una Reacción
www.clasesalacarta.com Cinética Química Estudia la velocidad a la que ocurren las reacciones químicas Termodinámica Es espontánea? Cinética A qué velocidad ocurre la reacción? Velocidad de una Reacción
Bloque 2: Organización y fisiología celular. Función de nutrición 2ª parte
 2.- ORGANIZACIÓN Y FISIOLOGÍA CELULAR. 2.5. CELULA EUCARIOTICA. FUNCIÓN DE NUTRICIÓN. 3ª PARTE CONTENIDOS 2.5.5. Metabolismo. 2.5.5.4.3. Respiración: ciclo de krebs, cadena respiratoria y fosforilación
2.- ORGANIZACIÓN Y FISIOLOGÍA CELULAR. 2.5. CELULA EUCARIOTICA. FUNCIÓN DE NUTRICIÓN. 3ª PARTE CONTENIDOS 2.5.5. Metabolismo. 2.5.5.4.3. Respiración: ciclo de krebs, cadena respiratoria y fosforilación
CELDAS ELECTROQUIMICAS
 CELDAS ELECTROQUIMICAS CLASIFICACION DE LAS CELDAS CELDAS ELECTROQUIMICAS Son aquellas en las cuales la energía eléctrica que procede de una fuente externa provee reacciones químicas no espontáneas. CELDAS
CELDAS ELECTROQUIMICAS CLASIFICACION DE LAS CELDAS CELDAS ELECTROQUIMICAS Son aquellas en las cuales la energía eléctrica que procede de una fuente externa provee reacciones químicas no espontáneas. CELDAS
