Materiales. Cultivos puros de hongos: Saccharomyces cerevisiae Rhodototula sp Penicillum sp Aspergillus niger Rhizopous sp Alternaria sp Fusarium sp
|
|
|
- Lucas Ortíz Vega
- hace 7 años
- Vistas:
Transcripción
1 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos algas y protozoarios Práctica 5. Técnicas de siembra y cultivo de bacterias y hongos Objetivos Aplicar las diferentes técnicas de siembra que se emplean para el estudio y asilamiento de bacterias y hongos levaduriformes y filamentosos. Relacionar la presentación del medio de cultivo con la técnica de siembra. Distinguir las condiciones de incubación para el cultivo de bacterias y hongos. Describir las características morfológicas macroscópicas y microscópicas de las bacterias y hongos (levaduriformes y filamentosos). Comprobar la pureza de los cultivos mediante tinciones simples y/o diferenciales. Introducción La identificación de microorganismos se basa en la observación de las características microscópicas y de desarrollo que presentan en medios líquidos, semisólidos y sólidos. En los últimos la formación de colonias visibles con características particulares permite diferenciar a los microorganismos, así como detectar contaminantes en los cultivos puros. Materiales Cultivos puros de bacterias: Escherichia coli Serratia marcescens Micrococcus luteus Pseudomonas aeruginosa Staphylococcus aureus Streptomyces griseus Streptomyces erythraeus Cultivos puros de hongos: Saccharomyces cerevisiae Rhodototula sp Penicillum sp Aspergillus niger Rhizopous sp Alternaria sp Fusarium sp Material por equipo ME /2 - Práctica 5 - Página 1
2 1 Microscopio 2 mecheros 2 gradillas 2 asas bacteriológicas 2 asas micológicas 1 vaso de precipitados de 250mL antes 1 juego de colorantes de Gram Lactofenol azul de algodón Azul de metileno para tinción simple Medios de cultivo 8 cajas de Petri con Agar de uso general 1 2 cajas con YPDM 4 cajas con Agar Sabouraud Material que deben tener los alumnos: 4 tubos con caldo BHI* 2 tubos con medio semisólido* 4 tubos con agar BHI inclinado* Pipetas Pasteur estériles Portaobjetos 1 Puede ser Agar Soya Tripticase (TSA), Agar Infusión de Cerebro y Corazón (BHI), Agar Nutritivo (AN), Agar Casoy (AC), etc. * Material preparado la práctica anterior Cultivo de bacterias, hongos y actinomicetos Metodología 2ª sesión de bacterias (cada equipo debe sembrar 2 bacterias diferentes) 1. A partir de la muestra problema preparar un frote, teñir con Gram y observar en 100x y registrar sus observaciones. 2. Organizar el material de modo que cada alumno cuente con lo siguiente: 4 cajas con Agar de uso general 1, 2 tubos con caldo* 2 tubos con agar inclinado* y un tubo con medio semisólido*. 3. Identificar las cajas de Petri y tubos de ensayo con plumón indeleble o con etiquetas con los siguientes datos: tener cuidado de que las anotaciones queden en la periferia de la base de la caja o cerca de la boca del tubo # de equipo Nombre del microorganismo dd/mm/aa ME /2 - Práctica 5 - Página 2
3 4. A partir de la muestra bacteriana inocular una asada en un tubo con 7mL de caldo BHI (tubo 1). 5. A partir del tubo 1 inocular el material que se muestra en el cuadro siguiendo el esquema de trabajo. 6. Sellar con las cajas dos tiras de masking tape, y colocar los tubos en un bote de metal o plástico. Incubar los dos tubos y las cajas invertidas a 37 C durante 24 horas en condiciones aeróbicas. 7. Transcurrido el tiempo de incubación, revisar y guardar en refrigeración a 4 C. 1 tubo con caldo mediante la transferencia una gota con pipeta Pasteur. 1 tubo con agar semisólido mediante picadura (emplear el asa recta o en aguja) 2 tubos con agar inclinado. Uno con estría recta y el segundo con estría ondulada. 1 caja de Petri con hisopo mediante la técnica de extendido o siembra masiva. Esta técnica también puede hacerse con asa bacteriológica. 1 caja de Petri con el asa trazar una estría simple en un cuarto de caja (cuadrante simple). Esta también puede aplicarse en el área total de la caja. 2 cajas de Petri con el asa trazar una serie de estrías con el fin de aplicar la técnica de cuadrante radial o estriado por agotamiento. ME /2 - Práctica 5 - Página 3
4 Organigrama Cepa bacteriana con asa Tinción de Gram Tubo 1 Caldo BHI Caldo BHI con pipeta Pasteur Medio semisólido con aguja de siembra por picadura Agar BHI con asa, estría recta y estría ondulada Agar BHI con asa, cuadrante simple Agar BHI con hisopo, siembra masiva Agar BHI con asa, cuadrante radial de actinomicetos o bacterias filamentosas (cada equipo debe sembrar 2 bacterias diferentes) 1. A partir de la muestra problema preparar un frote, teñir con Gram y observar a inmersión y registrar sus observaciones. 2. Con una pipeta Pasteur estéril colocar en un extremo de la placa de YPDM dos gotas del cultivo de Streptomyces griseus o de Streptomyces erythraeus. 3. Esterilizar el asa y estriar el cultivo sobre el medio con la técnica de cuadrante radial. 4. Identificar las cajas de Petri con plumón indeleble o con etiquetas con los siguientes datos: # de equipo Nombre del microorganismo dd/mm/aa 5. Sellar las cajas, invertirlas e incubar a 28 C durante 3 a 7 días. ME /2 - Práctica 5 - Página 4
5 de hongos levaduriformes (Cada equipo debe sembrar 2 levaduras diferentes) 1. Con el asa inocular una placa de Agar Sabouraud empleando la técnica de cuadrante radial con cada uno de los hongos levaduriformes. 2. Identificar las cajas de Petri con plumón indeleble o con etiquetas con los siguientes datos: # de equipo Nombre del microorganismo dd/mm/aa 3. Sellar las cajas, invertirlas e incubar a 28 C de 2 a 5 días. de hongos filamentosos (Cada equipo debe sembrar 2 hongos filamentosos diferentes) 1. Identificar las cajas de Petri con plumón indeleble o con etiquetas con los siguientes datos: # de equipo Nombre del microorganismo dd/mm/aa 2. Esterilizar el asa micológica y dejar enfriar dentro de la zona aséptica. 3. Tomar una pequeña cantidad del cultivo del hongo seleccionado y sembrar en el centro de la placa de Agar Sabouraud, para ello presionar ligeramente el asa sobre la placa. 4. Sellar las cajas e invertirlas. 5. Incubar a 28 C de 5 a 7 días. Resultados del desarrollo de bacterias, hongos y actinomicetos 2ª sesión Resultados de bacterias 1. Describir las características de desarrollo en los tubos (medio líquido, semisólido y sólido) y en las cajas de acuerdo con las guías de observación del manual de Microbiología General. 2. A partir del cultivo líquido y de dos colonias aisladas preparar 3 frotes y teñir con Gram. 3. Registrar sus resultados en el cuadro 1. Bacterias filamentosas 1. Revisar las características coloniales. 2. Preparar un frote y teñir con Gram. 3. Comparar la morfología colonial y microscópica de las bacterias estudiadas en la sesión anterior y la actual. 4. Registrar los resultados en el cuadro 2. ME /2 - Práctica 5 - Página 5
6 Hongos levaduriformes 1. Revisar las características coloniales. 2. Realizar un frote y una tinción simple de cada una de las levaduras en estudio. 3. Comparar la morfología colonial y microscópica con las características de las bacterias. 4. Registrar los resultados en el cuadro 3. La descripción de las colonias debe hacerse de acuerdo con las características indicadas en el Manual de Microbiología General. Hongos filamentosos 1. Revisar las características coloniales. 2. Mediante la técnica de impronta con diurex, hacer una preparación en fresco y teñir, observar al microscopio con los objetivos 10x y 40x. 3. Registrar los resultados en el cuadro 4, para ello describir las características de los hongos con ayuda de los esquemas del Manual de Microbiología General. Disposición de desechos 1. Verter los desechos de colorantes en los contenedores dispuestos en los laboratorios 2. Después de observar las preparaciones, sumergir los portaobjetos en una solución sanitizante durante 10 minutos, lavar con detergente, enjuagarlos y colocarlos en un frasco con alcohol al 95 %. 3. En el caso de ruptura de las preparaciones, envolver los fragmentos con papel, esterilizar el paquete en autoclave y después desecharlos en el contenedor de vidrio roto. 4. Los cultivos muestra deben ser esterilizados en autoclave, antes de ser desechados. 5. Después de observar las características de desarrollo, esterilizar los cultivos en autoclave. 6. Vaciar el agar sobre un papel y envolverlo. 7. Colocar el paquete en una bolsa de plástico y depositarla en el contenedor correspondiente. 8. Sellar las cajas de plástico con cultivos y depositarlas en el contendor rojo del laboratorio A. Registro de resultados Cuadro 1. Características microscópicas y de crecimiento en medios líquidos, semisólidos y sólidos, inoculados mediante diferentes técnicas. Nombre científico de la bacteria: Presentación del medio de cultivo y técnica de siembra Características microscópicas Caldo inoculado con asa Características de desarrollo Forma Agrupación Gram Superficial (pelicular o anillado) Sedimento Turbiedad Resultados ME /2 - Práctica 5 - Página 6
7 Picadura en medio semisólido Agar vertical inoculado con pipeta Agar inclinado Placa por extensión o masivo Placa cuadrante simple Placa estría radial (cuadrante radial o agotamiento) Características de crecimiento Movilidad (+ o -) Superficial En todo el medio En el fondo Formación de burbujas Forma del crecimiento: (filiforme, perlado o arborescente) Textura (acuosa, butirosa, cremosa, membranosa, viscosa) Consistencia (seca, húmeda) Desarrollo masivo o confluente Presencia de colonias aisladas Desarrollo a lo largo del estriado Presencia de colonias aisladas Características de las colonias: Forma (puntiforme, circular, ameboide, rizoide, fusiforme) (blanquecino, blanco opaco, amarillo etc) Borde (entero, ondulado, lobulado, crenado, filamentoso) Elevación (plana, elevada, convexa, rugosa, papilar, embonada) Textura (acuosa, butirosa, cremosa, membranosa, viscosa) Consistencia (seca, húmeda) Presencia de colonias aisladas Características de las colonias: Forma (puntiforme, circular, ameboide, rizoide, fusiforme) (blanquecino, blanco opaco, amarillo etc) Borde (entero, ondulado, lobulado, crenado, filamentoso) Elevación (plana, elevada, convexa, rugosa, papilar, embonada) Textura (acuosa, butirosa, cremosa, membranosa, viscosa) Consistencia (seca, húmeda) ME /2 - Práctica 5 - Página 7
8 Cuadro 2. Características microscópicas y de crecimiento de bacterias filamentosas. Nombre científico de la bacteria: Características coloniales Características microscópicas Forma Elevación Textura Aspecto (seco, húmedo) Forma Otras estructuras Gram Cuadro 3. Características de crecimiento y microscópicas de un hongo levaduriforme. Nombre científico: Coloniales Microscópicas Aspecto superficial (liso, rugoso, cerebriforme) Consistencia (cremosa, seca) Forma Tamaño relativo con respecto a las bacterias Presencia y distribución de blastosporas Cuadro 4. Características de crecimiento y microscópicas de un hongo filamentoso Nombre científico: Coloniales Microscópicas Desarrollo (escaso, medio, abundante) Aspecto del micelio superficial (algodonoso laxo, lanoso, aterciopelado) del micelio profundo Aspecto del micelio profundo (homogéneo, con anillos concéntricos, sectorial Tipo de hifas (cenocítica, septada) Tipo de cuerpo fructífero (esporangióforo, conidióforo) De las esporas: Morfología (esférica, oval, reniforme, fusiforme) Aspecto externo (lisas, punteadas, estriadas, verrugosas) ME /2 - Práctica 5 - Página 8
9 Bibliografía complementaria Cappuccino, James G. and Sherman Natalie Microbiology: a laboratory manual. 7 th edition. Pearson/Benjamin Cummings. USA. QR63 C Leboffe Michael J. and Burton E. Pierce Microbiology laboratory theory and application. 2 nd edition, Morton Publishing Co. USA. QR63 L Madigan, M. T. and J. M. Martinko Brock Biology of microorganisms. 11 th edition. Pearson Prentice Hall. USA. QR41.2 B Prescott Lansing M., Harley John P. and Klein Donald A Microbiology. 6 th edition. McGraw-Hill. USA. QR41.2 P Ramírez-Gama, R. M., B. Luna Millán, O. Velásquez Madrazo, L. Vierna García, A. Mejía Chávez, G. Tsuzuki Reyes, L. Hernández Gómez, I. Müggenburg, A. Camacho Cruz y M del C. Urzúa Hernández Manual de Prácticas de Microbiología General. 5ª edición. Facultad de Química, UNAM. México. Schaechter Moselio, Ingraham John L. and Neidhardt Frederick C Microbe. American Society for Microbiology. USA. QR41.2 S288 Tortora Gerard J., Funke Berdell R. and Case Christine L Microbiology : an introduction. 9th edition. Benjamin Cummings. USA. QR41.2 T ME /2 - Práctica 5 - Página 9
Materiales. Cultivos puros de bacterias: Streptomyces griseus Streptomyces erythraeus
 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
Unidad 3. Estudio de cultivos bacterianos puros Práctica 4. Técnicas de siembra y cultivo de bacterias
 Unidad 3. Estudio de cultivos bacterianos puros Práctica 4. Técnicas de siembra y cultivo de bacterias Objetivos Aplicar las diferentes técnicas de siembra que se emplean para el estudio y asilamiento
Unidad 3. Estudio de cultivos bacterianos puros Práctica 4. Técnicas de siembra y cultivo de bacterias Objetivos Aplicar las diferentes técnicas de siembra que se emplean para el estudio y asilamiento
Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos.
 Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos. Objetivos Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación
Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos. Objetivos Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación
Objetivo Describir el efecto de los factores ambientales, su concentración, así como de agentes químicos en el crecimiento de los microorganismos.
 Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Crecimiento Microbiano. Efecto de los factores ambientales y químicos Objetivo Describir el
Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Crecimiento Microbiano. Efecto de los factores ambientales y químicos Objetivo Describir el
PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión)
 PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para
PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para
PRÁCTICA 5.1 Aislamiento de Microorganismos
 PRÁCTICA 5.1 Aislamiento de Microorganismos Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
PRÁCTICA 5.1 Aislamiento de Microorganismos Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
Objetivos Describir los efectos de diferentes factores físicos en el crecimiento de bacterias.
 Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Efecto de los factores ambientales y químicos Objetivos Describir los efectos de diferentes
Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Efecto de los factores ambientales y químicos Objetivos Describir los efectos de diferentes
Práctica 3. ESTUDIO DE CULTIVOS BACTERIANOS PUROS Práctica 4. ESTUDIO MICROSCÓPICO Y CULTIVO DE HONGOS
 Práctica 3. ESTUDIO DE CULTIVOS BACTERIANOS PUROS Práctica 4. ESTUDIO MICROSCÓPICO Y CULTIVO DE HONGOS OBJETIVOS GENERALES. Al finalizar este ejercicio el alumno será capaz de: Aplicar las diferentes técnicas
Práctica 3. ESTUDIO DE CULTIVOS BACTERIANOS PUROS Práctica 4. ESTUDIO MICROSCÓPICO Y CULTIVO DE HONGOS OBJETIVOS GENERALES. Al finalizar este ejercicio el alumno será capaz de: Aplicar las diferentes técnicas
PRÁCTICA PARA EL ESTUDIO DE CULTIVOS BACTERIANOS PUROS (Siembra)
 PRÁCTICA PARA EL ESTUDIO DE CULTIVOS BACTERIANOS PUROS (Siembra) OBJETIVOS GENERALES. Al finalizar este ejercicio el alumno será capaz de: Aplicar las diferentes técnicas de siembra que se emplean para
PRÁCTICA PARA EL ESTUDIO DE CULTIVOS BACTERIANOS PUROS (Siembra) OBJETIVOS GENERALES. Al finalizar este ejercicio el alumno será capaz de: Aplicar las diferentes técnicas de siembra que se emplean para
Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas
 Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias.
 Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias. Objetivos Relacionar la actividad metabólica de los microorganismos con los cambios producidos en diferentes
Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias. Objetivos Relacionar la actividad metabólica de los microorganismos con los cambios producidos en diferentes
1ª sesión. Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo
 Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas
 Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO
 PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
1ª sesión. Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo
 Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión)
 Objetivos PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
Objetivos PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS
 PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo
 PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su utilidad en microbiología. Preparar
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su utilidad en microbiología. Preparar
PRÁCTICA 2.2 Preparaciones Microbiológicas
 PRÁCTICA 2.2 Preparaciones Microbiológicas 2.2.1 Preparaciones húmedas 2.2.2 Gota pendiente 2.2.3 Preparaciones fijas 2.2.4 Tinción simple Objetivos Al finalizar esta práctica el alumno será capaz de:
PRÁCTICA 2.2 Preparaciones Microbiológicas 2.2.1 Preparaciones húmedas 2.2.2 Gota pendiente 2.2.3 Preparaciones fijas 2.2.4 Tinción simple Objetivos Al finalizar esta práctica el alumno será capaz de:
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
 Sema na 3 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre 2014-1 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES PROTOCOLO / UNIDAD
Sema na 3 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre 2014-1 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES PROTOCOLO / UNIDAD
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Introducción
 PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
Protocolos Laboratorio de Microbiología Experimental 2014 PREPARACIONES MICROBIOLÓGICAS
 PREPARACIONES MICROBIOLÓGICAS Objetivos PREPARACIONES HÚMEDAS (EN FRESCO) Al finalizar esta práctica el alumno será capaz de: Realizar diferentes preparaciones microbiológicas a partir de muestras naturales.
PREPARACIONES MICROBIOLÓGICAS Objetivos PREPARACIONES HÚMEDAS (EN FRESCO) Al finalizar esta práctica el alumno será capaz de: Realizar diferentes preparaciones microbiológicas a partir de muestras naturales.
AISLAMIENTO DE MICROORGANISMOS
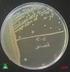 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
Aislamiento de Microorganismos (1ª Sesión)
 Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
GUIA DE TRABAJOS PRÁCTICOS MICOLOGÍA
 GUIA DE TRABAJOS PRÁCTICOS MICOLOGÍA Departamento de Microbiología Facultad de Medicina UBA 2009 Guía de Trabajos Prácticos 2009 1 Observación de escamas con micelios y levaduras. Digestión con KOH 40%.
GUIA DE TRABAJOS PRÁCTICOS MICOLOGÍA Departamento de Microbiología Facultad de Medicina UBA 2009 Guía de Trabajos Prácticos 2009 1 Observación de escamas con micelios y levaduras. Digestión con KOH 40%.
Bioseguridad en el Laboratorio de Microbiología
 Bioseguridad en el Laboratorio de Microbiología Objetivos Al finalizar la práctica el estudiante será capaz de: Aplicar las reglas básicas de higiene y seguridad para los laboratorios del área microbiológica.
Bioseguridad en el Laboratorio de Microbiología Objetivos Al finalizar la práctica el estudiante será capaz de: Aplicar las reglas básicas de higiene y seguridad para los laboratorios del área microbiológica.
UNIVERSIDAD DE CIENCIAS Y ARTES DE CHIAPAS
 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA Y PARASITOLOGÍA ELABORO: Q.F.B. MARÍA DOLORES TOLEDO MEZA ACTUALIZÓ:
FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA Y PARASITOLOGÍA ELABORO: Q.F.B. MARÍA DOLORES TOLEDO MEZA ACTUALIZÓ:
Tema 4.- Técnicas de siembra y aislamiento
 Tema 4.- Técnicas de siembra y aislamiento La siembra consiste en tomar con el asa de platino, previamente flameado, o con hisopo estéril una pequeña cantidad de muestra a estudiar y repartirla por toda
Tema 4.- Técnicas de siembra y aislamiento La siembra consiste en tomar con el asa de platino, previamente flameado, o con hisopo estéril una pequeña cantidad de muestra a estudiar y repartirla por toda
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL 2013 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA PRÁCTICA
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL 2013 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA PRÁCTICA
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA PRÁCTICA 1.
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA PRÁCTICA 1.
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL Semestre 2014-1 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL Semestre 2014-1 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA
UNIVERSIDAD AUTONOMA DE TAMAULIPAS
 R-RS-01-25-03 UNIVERSIDAD AUTONOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA-AZTLÁN NOMBRE DE LA CARRERA LICENCIADO EN NUTRICION Y CIENCIA DE LOS ALIMENTOS NOMBRE DE LA ASIGNATURA LABORATORIO
R-RS-01-25-03 UNIVERSIDAD AUTONOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA-AZTLÁN NOMBRE DE LA CARRERA LICENCIADO EN NUTRICION Y CIENCIA DE LOS ALIMENTOS NOMBRE DE LA ASIGNATURA LABORATORIO
Bioseguridad en el Laboratorio de Microbiología
 Objetivos Bioseguridad en el Laboratorio de Microbiología Al finalizar la práctica el estudiante será capaz de: Analizar la importancia que tienen las reglas básicas de higiene y seguridad, tanto en las
Objetivos Bioseguridad en el Laboratorio de Microbiología Al finalizar la práctica el estudiante será capaz de: Analizar la importancia que tienen las reglas básicas de higiene y seguridad, tanto en las
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO. OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico.
 GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL 2012 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA PRÁCTICA
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL 2012 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA PRÁCTICA
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 TRABAJO PRÁCTICO No. 7 MASTITIS CAUSADAS POR COCOS GRAM-POSITIVOS GÉNEROS STAPHYLOCOCCUS Y STREPTOCOCCUS OBJETIVOS 1. Realizar el estudio microscópico Staphylococcus y Streptococcus 2. Identificar las
TRABAJO PRÁCTICO No. 7 MASTITIS CAUSADAS POR COCOS GRAM-POSITIVOS GÉNEROS STAPHYLOCOCCUS Y STREPTOCOCCUS OBJETIVOS 1. Realizar el estudio microscópico Staphylococcus y Streptococcus 2. Identificar las
PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno
 PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno Objetivos Determinar las características nutricionales de diferentes microorganismos considerando las fuentes de carbono, energía y nitrógeno.
PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno Objetivos Determinar las características nutricionales de diferentes microorganismos considerando las fuentes de carbono, energía y nitrógeno.
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA
 PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
PRÁCTICO N 3. Técnicas para la observación, aislamiento y conservación de microorganismos
 PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
GUIA DE TRABAJOS PRÁCTICOS ÁREA DE MICOLOGÍA
 GUIA DE TRABAJOS PRÁCTICOS ÁREA DE MICOLOGÍA Departamento de Microbiología Facultad de Medicina UBA 2010 Guía de Trabajos Prácticos 2010 1 Observación de filamentos y levaduras en muestras de escamas.
GUIA DE TRABAJOS PRÁCTICOS ÁREA DE MICOLOGÍA Departamento de Microbiología Facultad de Medicina UBA 2010 Guía de Trabajos Prácticos 2010 1 Observación de filamentos y levaduras en muestras de escamas.
PRÁCTICA 2.2 Preparaciones microbiológicas
 PRÁCTICA 2.2 Preparaciones microbiológicas Objetivos Al finalizar esta práctica el alumno será capaz de: Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros.
PRÁCTICA 2.2 Preparaciones microbiológicas Objetivos Al finalizar esta práctica el alumno será capaz de: Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros.
UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II
 UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II Maye Bernal Rivera PARTE II. LECTURA E INTERPRETACION DE LOS CULTIVOS
UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II Maye Bernal Rivera PARTE II. LECTURA E INTERPRETACION DE LOS CULTIVOS
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 1 Bacteriología Veterinaria. TRABAJO PRÁCTICO No. 2 CULTIVO DE BACTERIAS OBJETIVOS 1. Manejar con destreza las diferentes técnicas empleadas para la siembra y aislamiento de bacterias. 2. Obtener cultivos
1 Bacteriología Veterinaria. TRABAJO PRÁCTICO No. 2 CULTIVO DE BACTERIAS OBJETIVOS 1. Manejar con destreza las diferentes técnicas empleadas para la siembra y aislamiento de bacterias. 2. Obtener cultivos
Varios tipos de microorganismos crecen en la piel, especialmente en los pliegues y partes húmedas asociadas a las glándulas sudoríparas.
 ACCIÓN GERMICIDA POR QUÉ NECESITAMOS DESODORANTES? Varios tipos de microorganismos crecen en la piel, especialmente en los pliegues y partes húmedas asociadas a las glándulas sudoríparas. Su actividad
ACCIÓN GERMICIDA POR QUÉ NECESITAMOS DESODORANTES? Varios tipos de microorganismos crecen en la piel, especialmente en los pliegues y partes húmedas asociadas a las glándulas sudoríparas. Su actividad
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
Cultivo Puro. Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica
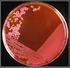 Cultivo Puro Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica Definición El cultivo puro representa las condiciones artificiales para
Cultivo Puro Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica Definición El cultivo puro representa las condiciones artificiales para
Objetivos. S Determinar la presencia de bacterias coliformes en una muestra de agua
 Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
PROCEDIMIENTO TECNICA DE COAGULASA EN TUBO PRT
 Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
ENUMERACIÓN DE ENTEROBACTERIACEAE EN ALIMENTOS SIN RESUSCITACIÓN. TÉCNICA RECUENTO EN PLACA
 PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
GUIA DE LABORATORIO PRACTICA 7 CELULAS PROCARIOTAS PROGRAMA DE INGENIERIA PECUARIA BIOLOGÍA GENERAL
 GUIA DE LABORATORIO PRACTICA 7 CELULAS PROCARIOTAS PROGRAMA DE INGENIERIA PECUARIA BIOLOGÍA GENERAL Leidy Diana Ardila Leal Docente. INTRODUCCIÓN Los organismos procariotas son por los organismos más abundantes
GUIA DE LABORATORIO PRACTICA 7 CELULAS PROCARIOTAS PROGRAMA DE INGENIERIA PECUARIA BIOLOGÍA GENERAL Leidy Diana Ardila Leal Docente. INTRODUCCIÓN Los organismos procariotas son por los organismos más abundantes
- Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio microbiológico.
 Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Técnicas de siembra para hongos y bacterias
 OBJETIVOS. UNIVERSIDAD POPULAR DEL CESAR Técnicas de siembra para hongos y bacterias - Practicar diferentes técnicas de siembra para el desarrollo de cultivos y subcultivos de hongos y bacterias, en medios
OBJETIVOS. UNIVERSIDAD POPULAR DEL CESAR Técnicas de siembra para hongos y bacterias - Practicar diferentes técnicas de siembra para el desarrollo de cultivos y subcultivos de hongos y bacterias, en medios
UNIVERSIDAD DE EL SALVADOR FACULTAD DE QUÍMICA Y FARMACIA
 1 UNIVERSIDAD DE EL SALVADOR MANUAL PARA LA CONSERVACIÓN DE CEPAS BACTERIANAS DE TRABAJO SAN SALVADOR, EL SALVADOR, CENTRO AMERICA UNIVERSIDAD DE EL SALVADOR DEPARTAMENTO DE BIOQUIMICA Y Código CONTAMINACIÓN
1 UNIVERSIDAD DE EL SALVADOR MANUAL PARA LA CONSERVACIÓN DE CEPAS BACTERIANAS DE TRABAJO SAN SALVADOR, EL SALVADOR, CENTRO AMERICA UNIVERSIDAD DE EL SALVADOR DEPARTAMENTO DE BIOQUIMICA Y Código CONTAMINACIÓN
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo
 Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
EXAMEN PRACTICO NIVEL II Tema: Microbiología General
 EXAMEN PRACTICO NIVEL II Tema: Microbiología General Puntaje Total: 50 puntos Introducción Una de las principales áreas de la Microbiología es la Microbiología diagnóstica, en la cual un microbiólogo aísla
EXAMEN PRACTICO NIVEL II Tema: Microbiología General Puntaje Total: 50 puntos Introducción Una de las principales áreas de la Microbiología es la Microbiología diagnóstica, en la cual un microbiólogo aísla
PARTE EXPERIMENTAL 1 MATERIALES, EQUIPOS Y REACTIVOS 1.1 MATERIAL Y EQUIPOS
 II PARTE EXPERIMENTAL El presente trabajo se realizó en el laboratorio del Centro Latino Americano de Enseñanza e Investigación de Bacteriología Alimentaria (CLEIBA), con sede en la Facultad de Farmacia
II PARTE EXPERIMENTAL El presente trabajo se realizó en el laboratorio del Centro Latino Americano de Enseñanza e Investigación de Bacteriología Alimentaria (CLEIBA), con sede en la Facultad de Farmacia
EVALUACIÓN DE LA CALIDAD MICROBIOLÓGICA DE LOS SERVICIOS HIDROSANITARIOS DE LA INSTITUCIÓN UNIVERSITARIA COLEGIO MAYOR DE ANTIOQUIA
 EVALUACIÓN DE LA CALIDAD MICROBIOLÓGICA DE LOS SERVICIOS HIDROSANITARIOS DE LA INSTITUCIÓN UNIVERSITARIA COLEGIO MAYOR DE ANTIOQUIA Juliana Gallego Montoya Luisa Fernanda Giraldo Vargas Valentina Acevedo
EVALUACIÓN DE LA CALIDAD MICROBIOLÓGICA DE LOS SERVICIOS HIDROSANITARIOS DE LA INSTITUCIÓN UNIVERSITARIA COLEGIO MAYOR DE ANTIOQUIA Juliana Gallego Montoya Luisa Fernanda Giraldo Vargas Valentina Acevedo
Laboratorio Nacional de Salud Pública
 1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
TRANSFERENCIAS ASÉPTICAS
 Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
Quiz #1 Repaso laboratorio #1. Características de Crecimiento Técnicas de Transferencias Técnicas asépticas
 Quiz #1 Repaso laboratorio #1 Introducción Características de Crecimiento Técnicas de Transferencias Técnicas asépticas Microscopio Importancia Mencionar tipos de Microscopios Magnificación Cuál es el
Quiz #1 Repaso laboratorio #1 Introducción Características de Crecimiento Técnicas de Transferencias Técnicas asépticas Microscopio Importancia Mencionar tipos de Microscopios Magnificación Cuál es el
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
PRÁCTICA No. 2 Métodos de cultivo y aislamiento de bacterias
 PRÁCTICA No. 2 Métodos de cultivo y aislamiento de bacterias Objetivos. Que el alumno conozca las diferentes técnicas de aislamiento en medios de cultivo sólido para la obtención de cultivos puros de bacterias.
PRÁCTICA No. 2 Métodos de cultivo y aislamiento de bacterias Objetivos. Que el alumno conozca las diferentes técnicas de aislamiento en medios de cultivo sólido para la obtención de cultivos puros de bacterias.
PROCEDIMIENTO TECNICA NMP STAPHYLOCOCCUS AUREUS EN ALIMENTOS. BAM ONLINE 2001
 PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707
 UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707 Actualizado por: DR. HÉCTOR L. AYALA DEL RÍO 2005 UPR-H Departamento de Biología-BIOL
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707 Actualizado por: DR. HÉCTOR L. AYALA DEL RÍO 2005 UPR-H Departamento de Biología-BIOL
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA Mª PAZ MERINO JIMÉNEZ MIREIA LLINARES MARCELO PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA A mi padre. M.
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA Mª PAZ MERINO JIMÉNEZ MIREIA LLINARES MARCELO PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA A mi padre. M.
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
1ª PRÁCTICA DE MICROBIOLOGÍA:
 1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
INSTRUCCIONES DE USO. USO PREVISTO Agar Cromogenico Salmonella está recomendado para el aislamiento de salmonella a partir de muestras clínicas.
 INSTRUCCIONES DE USO Revisión 2 Feb.2017 AGAR CROMOGENICO SALMONELLA Agar Cromogenico Salmonella presentación 575 gramos, 5, 25, 50 kilos. Catálogo 1122 Agar Cromogenico Salmonella presentación placas
INSTRUCCIONES DE USO Revisión 2 Feb.2017 AGAR CROMOGENICO SALMONELLA Agar Cromogenico Salmonella presentación 575 gramos, 5, 25, 50 kilos. Catálogo 1122 Agar Cromogenico Salmonella presentación placas
LICENCIATURA DE QUÍMICO EN ALIMENTOS. Microbiología General I. Tipo de Asignatura: Teórico-Práctico Área de Conocimiento: Básica de Carrera
 LICENCIATURA DE QUÍMICO EN ALIMENTOS Microbiología General I Tipo de Asignatura: Teórico-Práctico Área de Conocimiento: Básica de Carrera 111 1. DATOS GENERALES DE IDENTIFICACIÓN Nombre de la asignatura
LICENCIATURA DE QUÍMICO EN ALIMENTOS Microbiología General I Tipo de Asignatura: Teórico-Práctico Área de Conocimiento: Básica de Carrera 111 1. DATOS GENERALES DE IDENTIFICACIÓN Nombre de la asignatura
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON
 PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
PREPARACIONES Y TINCIONES
 PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
UNIVERSIDAD JUAREZ AUTONOMA DE TABASCO DIVISIÓN ACADEMICA DE CIENCIAS BIOLOGICAS LICENCIATURA EN ECOLOGIA
 UNIVERSIDAD JUAREZ AUTONOMA TABASCO DIVISIÓN ACAMICA CIENCIAS BIOLOGICAS LICENCIATURA EN ECOLOGIA ASIGNATURA: MICROBIOLOGÍA AREA : SUSTANTIVA PROFESIONAL HORAS TEÓRICAS: 2 HORAS PRÁCTICAS: 4 CRÉDITOS:
UNIVERSIDAD JUAREZ AUTONOMA TABASCO DIVISIÓN ACAMICA CIENCIAS BIOLOGICAS LICENCIATURA EN ECOLOGIA ASIGNATURA: MICROBIOLOGÍA AREA : SUSTANTIVA PROFESIONAL HORAS TEÓRICAS: 2 HORAS PRÁCTICAS: 4 CRÉDITOS:
BIORREACTRES. Estudios básicos y aplicados sobre procesos de fermentación
 BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES
 TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES 1. Objetivo del diagnóstico microbiológico 2. Toma de muestra 3. Diagnóstico directo - bacterias - hongos - protozoos -
TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES 1. Objetivo del diagnóstico microbiológico 2. Toma de muestra 3. Diagnóstico directo - bacterias - hongos - protozoos -
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA
 FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
PRÁCTICA DE NUTRICIÓN MICROBIANA Y REQUERIMIENTOS DE OXÍGENO
 PRÁCTICA DE NUTRICIÓN MICROBIANA Y REQUERIMIENTOS DE OXÍGENO INTRODUCCIÓN La nutrición es el proceso por el cual los seres vivos toman del medio donde habitan, los compuestos químicos que necesitan para
PRÁCTICA DE NUTRICIÓN MICROBIANA Y REQUERIMIENTOS DE OXÍGENO INTRODUCCIÓN La nutrición es el proceso por el cual los seres vivos toman del medio donde habitan, los compuestos químicos que necesitan para
Título de la gráfica: Crecimiento/ No crecimiento
 Resultados de la semana anterior (TSB) Título de la gráfica: # tubo TSB 1-24 Crecimiento/ No crecimiento Descripción del crecimiento Resultados de la semana anterior (TSA slant) Título de la gráfica: tubo
Resultados de la semana anterior (TSB) Título de la gráfica: # tubo TSB 1-24 Crecimiento/ No crecimiento Descripción del crecimiento Resultados de la semana anterior (TSA slant) Título de la gráfica: tubo
UNIDAD 6. Nutrición microbiana y UNIDAD 7. Requerimientos de oxígeno
 UNIDAD 6. Nutrición microbiana y UNIDAD 7. Requerimientos de oxígeno INTRODUCCIÓN La nutrición es el proceso por el cual los seres vivos toman del medio donde habitan, los compuestos químicos que necesitan
UNIDAD 6. Nutrición microbiana y UNIDAD 7. Requerimientos de oxígeno INTRODUCCIÓN La nutrición es el proceso por el cual los seres vivos toman del medio donde habitan, los compuestos químicos que necesitan
Medición del crecimiento Microbiano
 Medición del crecimiento Microbiano Determinación del número de microorganismos en una muestra. Determinación de la actividad metabólica, biomasa y proteínas. Métodos para el conteo de microorganismos
Medición del crecimiento Microbiano Determinación del número de microorganismos en una muestra. Determinación de la actividad metabólica, biomasa y proteínas. Métodos para el conteo de microorganismos
GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES
 ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
Clostridium perfringens
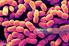 Clostridium perfringens Introducción Cuando se lanza un producto alimentario al mercado se deben tener en cuenta varios parámetros que le otorgan calidad al producto, uno de ellos es la inocuidad. Los
Clostridium perfringens Introducción Cuando se lanza un producto alimentario al mercado se deben tener en cuenta varios parámetros que le otorgan calidad al producto, uno de ellos es la inocuidad. Los
Microbiología. Carrera: PEN 0625
 1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Microbiología Ingeniería en Pesquerías PEN 0625 3 3 9 2.- HISTORIA DEL PROGRAMA
1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Microbiología Ingeniería en Pesquerías PEN 0625 3 3 9 2.- HISTORIA DEL PROGRAMA
2. Observación de hongos de interés industrial
 2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
CULTIVO DE MICROORGANISMOS
 CULTIVO DE MICROORGANISMOS OBJETIVO: El alumno aprenderá las técnicas más utilizadas para sembrar bacterias en diferentes medios de cultivo. GENERALIDADES En la naturaleza los microorganismos se presentan
CULTIVO DE MICROORGANISMOS OBJETIVO: El alumno aprenderá las técnicas más utilizadas para sembrar bacterias en diferentes medios de cultivo. GENERALIDADES En la naturaleza los microorganismos se presentan
Uso y cuidado del microscopio de campo claro.
 OBJETIVOS. Uso y cuidado del microscopio de campo claro. Al finalizar la práctica el estudiante será capaz de: Aplicar los cuidados básicos de un microscopio óptico de campo claro. Identificar las partes
OBJETIVOS. Uso y cuidado del microscopio de campo claro. Al finalizar la práctica el estudiante será capaz de: Aplicar los cuidados básicos de un microscopio óptico de campo claro. Identificar las partes
Laboratorio (#1(( Microbiolog General(
 Laboratorio (#1(( Microbiolog ía( General( Conceptos(b ásico( para(el(labo ratorio( de(microbio logía( Objetivos( 0 Técnicas(Ascépticas(y(de(Esterilización( 0 Equipo(de(laboratorio( 0 Medios(de(Cultivo(
Laboratorio (#1(( Microbiolog ía( General( Conceptos(b ásico( para(el(labo ratorio( de(microbio logía( Objetivos( 0 Técnicas(Ascépticas(y(de(Esterilización( 0 Equipo(de(laboratorio( 0 Medios(de(Cultivo(
PRACTICA 2 TINCION DE GRAM
 PRACTICA 2 TINCION DE GRAM OBJETIVOS DE APRENDIZAJE: Cuando haya completado este experimento, usted debe comprender: 1. La base teórica y química de los procedimientos de tinción diferencial. 2. La base
PRACTICA 2 TINCION DE GRAM OBJETIVOS DE APRENDIZAJE: Cuando haya completado este experimento, usted debe comprender: 1. La base teórica y química de los procedimientos de tinción diferencial. 2. La base
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUANTITATIVO DE ORINA ANÁLISIS CUALITATIVO DE ORINA M-1 M-2 M-3 M-4 Lectura de la placa de Agar CLED Identificación presuntiva
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUANTITATIVO DE ORINA ANÁLISIS CUALITATIVO DE ORINA M-1 M-2 M-3 M-4 Lectura de la placa de Agar CLED Identificación presuntiva
Universidad Autónoma Metropolitana- Iztapalapa. Academia de Microbiología, Departamento de Biotecnología
 Universidad Autónoma Metropolitana- Iztapalapa MANUAL DE PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGIA GENERAL Academia de Microbiología, Departamento de Biotecnología Participantes: Dra. María de los Angeles
Universidad Autónoma Metropolitana- Iztapalapa MANUAL DE PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGIA GENERAL Academia de Microbiología, Departamento de Biotecnología Participantes: Dra. María de los Angeles
PRACTICA Núm. 15 AISLAMIENTO E IDENTIFICACION DE MOHOS DEL AIRE
 I. OBJETIVO PRACTICA Núm. 15 AISLAMIENTO E IDENTIFICACION DE MOHOS DEL AIRE Aislar mohos del aire y conocer sus características morfológicas y estructurales para lograr su identificación. II. INTRODUCCION
I. OBJETIVO PRACTICA Núm. 15 AISLAMIENTO E IDENTIFICACION DE MOHOS DEL AIRE Aislar mohos del aire y conocer sus características morfológicas y estructurales para lograr su identificación. II. INTRODUCCION
HONGOS (fungi) A pesar de que como grupo pueden alimentarse de una gran cantidad de compuestos, tienen requerimientos nutricionales sencillos.
 07. HONGOS 1 07) HONGOS. DEFINICIÓN DEL GRUPO MICROBIANO (HONGOS MACROSCÓPICOS, FILAMENTOSOS Y LEVADURIFORMES). CARACTERÍSTICAS MORFOLÓGICAS Y FISIOLÓGICAS DE LOS HONGOS: ESTRUCTURA, NUTRICIÓN Y CRECIMIENTO.
07. HONGOS 1 07) HONGOS. DEFINICIÓN DEL GRUPO MICROBIANO (HONGOS MACROSCÓPICOS, FILAMENTOSOS Y LEVADURIFORMES). CARACTERÍSTICAS MORFOLÓGICAS Y FISIOLÓGICAS DE LOS HONGOS: ESTRUCTURA, NUTRICIÓN Y CRECIMIENTO.
1ª. Sesión. Inoculación de las muestras
 Unidad 6. Nutrición microbiana y caracterización de bacterias. Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. P11. Diversidad nutricional, fisiológica
Unidad 6. Nutrición microbiana y caracterización de bacterias. Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. P11. Diversidad nutricional, fisiológica
