UNIVERSIDAD DE CIENCIAS Y ARTES DE CHIAPAS
|
|
|
- Asunción Álvarez Ortiz de Zárate
- hace 7 años
- Vistas:
Transcripción
1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA Y PARASITOLOGÍA ELABORO: Q.F.B. MARÍA DOLORES TOLEDO MEZA ACTUALIZÓ: Q.F.B. LUIS ALBERTO MORALES MARTÍNEZ
2 Laboratorio de Microbiología y Parasitología Práctica No. 1 Objetivos ***Conocimiento y manejo del microscopio*** Conocer las partes típicas del microscopio óptico. Aprender a manejar el microscopio óptico. Conocer el manejo del microscopio estereoscópico Material: Cubreobjetos Portaobjetos Microscopio óptico Microscopio estereoscópico Reactivos: Aceite de inmersión Muestras diversas: Cabello, hojas verdes, insectos, fibras de algodón, epidermis de la cebolla, sal, frotis sanguíneo, frotis bacteriano. Procedimiento: Para microscopio óptico de campo claro 1.- Identificar cada una de las partes del microscopio. 2.- Colocar una de las muestras (excepto el frotis bacteriano y sanguíneo) en un portaobjeto y colocar encima de la muestra un cubreobjeto. 3.- Examine las muestras a través del objetivo de bajo poder (10x) y alto poder (40x). 4.- Dibuje lo observado. 5.- Al frotis bacteriano y sanguíneo colocarle una gota de aceite de inmersión y observar en el objetivo de inmersión (100x). 6.- Dibuje lo observado. Para microscopio estereoscópico: 1.- Colocar cada una de las muestras (excepto el frotis bacteriano y sanguíneo) en un portaobjeto o caja petri. 2.- Examine las muestras a través de los objetivos y dibuje lo observado. 3.- Compare esta observación con la realizada en el microscopio óptico. Cuestionario: 1.- Por medio de un dibujo, describa las partes del microscopio óptico. 2.- Describa la función de cada una de las partes del microscopio óptico. 3.- Describa las diferencias que existe entre un microscopio compuesto y un estereoscópico.
3 Laboratorio de Microbiología y Parasitología Práctica No. 2 Objetivos: ***Estudio de la morfología de los mohos*** Conocer las características microscópicas y macroscópicas de los hongos. Conocer la morfología de los mohos y distinguir microscópicamente entre un micelio, hifa y esporas. Conocer los géneros más importantes de mohos que pueden desarrollar en alimentos. Material: Cubreobjetos Portaobjetos Pinza de disección Cinta adhesiva transparente Microscopio óptico Microscopio estereoscópico. Reactivos: Colorante azul de metileno Procedimiento: Primera sesión: Previo a práctica: Dejar tortillas, pan y una fruta en un lugar húmedo durante una semana. Segunda sesión: Observación macroscópica: 1.- Anote la pigmentación del moho y su aspecto (aterciopelado, velloso, algodonoso, etc). Observación microscópica: -Para un mismo género de moho realizar el método en fresco y el de cinta adhesiva. -Realizar el método para tres mohos diferentes. Método en fresco 1.- En un portaobjetos coloque una gota de colorante. 2.- Con las pinzas, desprenda pequeñas porciones del moho y colóquelo en la gota. 3.- Colocar un cubreobjetos y observar con objetivos de 10x y 40x. 4.- Dibuje lo observado e identifique morfología del moho, ver ilustraciones. Método de cinta adhesiva
4 1.- En un portaobjetos coloque una gota de colorante. 2.- Cortar un trozo de cinta adhesiva transparente de aproximadamente 2 cm. 3.- Tocar con el lado adhesivo de la cinta la superficie del moho. 4.- Pegar la cinta adhesiva sobre la gota del portaobjetos. 5.- Eliminar el colorante sobrante con un papel. 6.- Observar con objetivos de 10x y 40x. 7.- Dibuje lo observado e identifique morfología del moho, ver ilustraciones. Cuestionario: 1.- Describa la clasificación taxonómica de hongos. 2.- Mencione dos especies de los siguientes hongos: a)hongos comestibles, b)hongos venenosos, c)hongos alucinógenos, d)levaduras, e)mohos 3.- Importancia de los hongos en la naturaleza. Esporas ILUSTRACIONES Hifas y micelio Alternaria GÉNERO DE MOHOS Alternaria Fusarium Cladosporium
5 Penicillium Aspergillus Rhizopus Geotrichum Mucor
6 Laboratorio de Microbiología y Parasitología Práctica No. 3 Objetivos: ***Los microorganismos del cuerpo y la tinción de Gram*** Realizar la tinción de Gram a microorganismos del cuerpo. Conocer el fundamento de la tinción de Gram. Diferenciar microorganismos Gram positivos de Gram negativos. Observar microorganismos del cuerpo humano. Material: Hisopos estériles o cotonetes Portaobjetos Mechero Bunsen Pinzas Asa microbiológica Papel seda Varilla de tinción Microscopio óptico Reactivos: Safranina Cristal violeta Lugol Acetona alcohol (al 30% o 3 partes de acetona y 7 de alcohol) Lugol Aceite de inmersión Material biológico: Muestra de exudado faríngeo, nasal y ótico. Procedimiento: 1.- Tomar la muestra faríngea, nasal y ótica con un hisopo estéril o cotonete y realizar un frotis en su respectivo portaobjeto. Si la muestra es muy seca, adicionar una gota de agua de la llave y realizar el frotis. 2.- Fijar la muestra con calor. 3.- Teñir con cristal violeta durante 1 minuto. 4.- Eliminar el exceso de colorante con agua de la llave. 5.- Añadir lugol durante un minuto. 6.- Lavar con acetona-alcohol, hasta decolorar. 7.- Teñir con safranina durante 1 minuto. 8.- Eliminar el exceso de colorante con agua de la llave.
7 9.- Dejar secar y observar con objetivo de inmersión (100x) Dibuje lo observado. 11.-Observar en objetivo de 100x, el frotis proporcionado por el profesor. Cuestionario: 1.- Describa la flora normal del cuerpo humano y clasifíquela por regiones. 2.- Mencione 3 diferencias entre microorganismos Gram positivos y Gram negativos. 3.- Mencione 4 microorganismos Gram positivos y Gram negativos que afecten al ser humano. 4.- Describa la función de cada uno de los reactivos que se utilizan en la tinción de Gram.
8 Laboratorio de Microbiología y Parasitología Práctica No. 4 Objetivos: ***Tinción de Ziehl-Neelsen*** Realizar la tinción de Ziehl-Neelsen en una muestra biológica. Conocer el fundamento de la tinción de Ziehl-Neelsen. Diferenciar microorganismos BAAR positivos de los BAAR negativos. Material: Portaobjetos Varilla de tinción Asa microbiológica Mechero Bunsen Papel seda Microscopio óptico Material biológico: Expectoración Material por equipo: Algodón Alcohol Reactivos: Fucsina fenicada Azul de metileno Solución ácido-alcohol (HCl al 3% en alcohol) Aceite de inmersión Procedimiento: 1.- Tomar con el asa microbiológica una cantidad de muestra y realizar un frotis en el portaobjeto. 2.- Dejar secar y fijar con calor. 3.- Coloque encima de la varilla de tinción el portaobjetos que tiene la muestra. 4.- Teñir con fucsina fenicada durante 5 minutos. Pasando debajo del portaobjetos la llama del mechero o una torunda de algodón n impregnada con alcohol prendida, de tal forma que se eliminen vapores en la tinción. No ebullición Si los borde del frotis se empiezan a secar, añada más colorante. 5.- Lavar el exceso de colorante con agua de la llave. 6.- Decolorar con solución ácido-alcohol. 7.- Lavar con agua de la llave.
9 8.- Teñir con azul de metileno durante 1 minuto. 9.- Lavar con agua de la llave. 10.-Dejar secar y observar con objetivo de inmersión (100x). Cuestionario: 1.- Describa la función de cada uno de los reactivos y el calor en la tinción de Ziehl-Neelsen. 2.- Mencione un género de microorganismos BAAR positivos que son patógenos en el ser humano. 3.- Qué significa B.A.A.R.?
10 Laboratorio de Microbiología y Parasitología Práctica No. 5 ***Esterilización y preparación de medios de cultivos*** Objetivos: Conocer los métodos de esterilización por calor seco y calor húmedo. Conocer el manejo de la autoclave, olla de presión y horno de calor seco. Preparar medios de cultivo sólidos, semisólidos y líquidos. Material y equipo: Tubos de ensayo de 16 x 150 mm con tapón de rosca Cajas Petri estériles Pipepas de 5 y 10 ml Vidrio de reloj Matraces Erlenmeyer de 125 y 250 ml Agitador de vidrio Espátula Mechero Bunsen Mechero Fisher Parilla eléctrica Balanza granataria Autoclave Horno de calor seco Por equipo traer: Papel estrasa Masking-tape Algodón Gasas Benzal Medios de cultivo: Medio SIM Agar sal manitol Agar bilis verde brillante Caldo bilis verde brillante Procedimiento: Esterilización de material de vidrio 1.- Envolver 5 pipetas de 5 ml con papel estrasa, poner masking tape y cinta testigo (se explicaran los pasos para envolver una pipeta). 2.- Esterilizar en el horno de calor seco a una temperatura de 160 a 180 o C, durante 1 hora o en autoclave durante 15 minutos a 121 o C y una presión de 15 libras in 2.
11 Preparación de medios de cultivo. 1.-Preparar en matraces los siguientes medios de cultivo: -80 ml de agar bilis verde brillante -80 ml de agar sal manitol -20 ml de caldo bilis verde brillante -20 ml de medio SIM -20 ml de agar bilis verde brillante 1) Realizar los cálculos correspondientes. 2) Pesar en un vidrio de reloj la cantidad necesaria del medio de cultivo. 3) Colocar el medio de cultivo ya pesado en un matraz Erlenmeyer. 4) Medir en una probeta graduada el agua destilada necesaria y añadir al matraz. 5) Agitar levemente tratando de disolver, sino se disuelve utilizar un agitador de vidrio. 6) Colocar un tapón de algodón al matraz y calentar hasta disolución completa del medio. Agitar frecuentemente. NO DESCUIDAR. 7) Distribuir el medio necesario en tubos con tapón de rosca o de algodón. -3 tubos con 6 ml de agar bilis verde brillante c/u -3 tubos con 6 ml medio SIM c/u -3 tubos con 6 ml de caldo bilis verde brillante c/u 8) Esterilizar los medios de cultivo en autoclave o en olla de presión durante 15 minutos a 121 o C y una presión de 15 libras in 2. 9) Sacar los medios esterilizados. 10) Dejar enfriar el agar bilis verde brillante, antes de que solidifique, vaciar en 3 cajas Petri, aproximadamente 20 a 30 ml por caja. Dejar solidificar. Realizar lo mismo con agar sal manitol. NOTA: Desinfectar el área de trabajo antes de vaciar el medio a las cajas. 11) Invertir las cajas Petri y refrigerar. 12) Inclinar en una superficie los tubos que contienen agar bilis verde brillante. Dejar solidificar. 13) Dejar los tubos con medio SIM en una gradilla y dejar solidificar. 14) Dejar enfriar los tubos con caldo bilis verde brillante. 15) Introducir todos los tubos en un vaso de precipitado y refrigerar. Cuestionario: 1.- Clasifique los medios de cultivo. 2.- Cuál es la diferencia entre un medio selectivo y un medio diferencial?. 3.- Describa los métodos de esterilización por calor seco y por calor húmedo.
12 Laboratorio de Microbiología y Parasitología Práctica No. 6 ***Cultivo y metabolismo microbiano*** Objetivos: Aprender a sembrar microorganismos por diversas técnicas. Observar características microscópicas y macroscópicas de los microorganismos aislados en cultivos sólidos y líquidos. Conocer el manejo de la incubadora. Material: Asa microbiológica Mechero Bunsen Portaobjetos Papel seda Varilla de tinción Autoclave / olla de presión Microscopio óptico Incubadora Reactivos: Medios preparados en la práctica No. 6 Colorantes para tinción de Gram Aceite de inmersión Por equipo traer: Muestra: Agua sucia y agua de frutas Cotonetes Masking-tape Benzal Procedimiento: I. Primera sesión: 1.- Antes de realizar las diversas técnicas de siembra de cultivo, desinfecte el área donde va a trabajar.
13 2- Sembrar por diversas técnicas los medios preparados en la práctica No. 6, utilizando un asa microbiológica previamente esterilizada en la flama del mechero para las muestras de agua y cotonetes para el exudado. Para cajas Petri: 1.- Numerar las cajas del 1 al 3, la número 3 será caja control, no se le pondrá muestra. 2.- Para cajas 1 y 2 de agar bilis verde brillante sembrar utilizando la técnica de estría cruzada o en cuadrante radial (ver figura No. 1) y para caja 1 y 2 de agar sal manitol sembrar utilizando la técnica de estriado continuo (ver figura No. 2.) 3.- Invertir las cajas e incubar de 24 a 48 horas a ±35 o C. AGAR BILIS VERDE BRILLANTE Cajas: Muestra Tipo de siembra Caja 1 Agua sucia Estría cruzada Caja 2 Agua de frutas Estría cruzada Caja 3 Ninguna (Caja control) Ninguna a) b) Fig. No.1 d) c)
14 AGAR SAL MANITOL Cajas: Muestra Tipo de siembra Caja 1 Exudado ótico Estría ondulada Caja 2 Exudado nasal Estría ondulada Caja 3 Ninguna (Caja control) Ninguna Fig. No.2 Para tubos: 1.- Numerar los tubos del 1 al 3 para cada medio de cultivo, el número 3 será tubo control, no se le pondrá muestra. 2.- Recuerde que antes de realizar la técnica de siembra o de inoculación, debe de esterilizar el asa con la flama del mechero. 3.- Al tubo 1 y 2 con agar bilis verde brillante, sembrar con la técnica de estría ondulada(ver fig. No.3), al tubo 1 y 2 de medio SIM, sembrar con la técnica de picadura (ver fig. No.4) y al tubo 1 y 2 de caldo bilis verde brillante, sembrar por agitación del asa (ver fig. No.5). AGAR BILIS VERDE BRILLANTE Tubos: Tipo de siembra Muestra Fig. No.3 Tubo 1 Agua sucia Estría ondulada Tubo 2 Agua de frutas Estría ondulada Tubo 3 Ninguna (Tubo control) Ninguna
15 MEDIO SIM Tubos: Muestra Tipo de siembra Tubo 1 Agua sucia Picadura Fig. No.4 Tubo 2 Agua de frutas Picadura Tubo 3 Ninguna (Tubo control) Ninguna CALDO BILIS VERDE BRILLANTE Tubos: Muestra Tipo de siembra Tubo 1 Agua sucia Agitar el asa con muestra en el caldo Fig. No.5 Tubo 2 Agua de frutas Agitar el asa con muestra en el caldo Tubo 3 Ninguna (Tubo control) Ninguna 4.- Colocar los tubos en un cesto e incubar de 24 a 48 horas a ±35 o C. II. Segunda sesión 1.- Observar y anotar las características macroscópicas de los microorganismos aislados. Para cajas: anotar el color y la forma de las colonias. Ver siguiente figura: Forma: Puntiforme Circular Amiboide Rizoide Fusiforme
16 Para tubos: Tubos sembrado con estría ondulada: Filiforme Equinulada Perlada Difusa Rizoide Arborescente Tubo sembrado por picadura Filiforme Perlada Equinulada Rizoide Arborescente Si el medio toma una coloración negra, es por H 2S liberado por la bacteria. Tubos en medio líquido: a) Crecimiento superficial: Floculento Anillado Peliculado Membranoso
17 b) Sedimento: compacto, grumoso, granular o viscoso. c) Cantidad de sedimento: abundante, escaso o nulo. 2.- Realizar la tinción de Gram de las colonias aisladas en cajas Petri donde hubo crecimiento. 3.- Observar en objetivo de inmersión (100x) las características microscópicas de la tinción realizada. 4.- Dibuje lo observado e interprete sus resultados. 5.- Esterilizar los medios utilizados. Cuestionario: 1.- Qué características macroscópicas y microscópicas se toman en cuenta en la identificación de bacterias? 2.- Escriba una lista de microorganismos patógenos que pueden transmitirse a través del aire, agua, alimentos y suelo.
18 Laboratorio de Microbiología y Parasitología Práctica No. 7 Objetivos: ***Análisis microbiológico del exudado faríngeo*** Describir la utilidad del análisis microbiológico de un exudado faríngeo. Conocer los principales agentes etiológicos de faringitis o amigdalitis. Efectuar el diagnóstico de faringitis o amigdalitis estreptocóccica, estafilocóccicas o candidiásicas. Material: Abatelenguas Asa bacteriológica Hisopos estériles Mechero Bunsen Mechero Fisher Matraces de 250 ml Espátula Portaobjetos Parrilla eléctrica Balanza granataria Autoclave Incubadora Microscopio óptico Reactivos: Aceite de inmersión. Colorantes y reactivos de Gram. Medios de cultivo: Agar Biggy Agar eosina azul de metileno Agar sal-manitol Gelosa sangre de carnero Primera sesión: I. Preparación de medios de cultivo 1.- Preparar los siguientes medios de cultivo: - 90 ml de agar eosina azul de metileno - 90 ml de agar sal-manitol - 90 ml de agar Biggy 2.- Esterilizar los medios de cultivo en autoclave o en olla de presión durante 15 minutos a 121 o C y una presión de 15 libras in 2.
19 3.- Sacar los medios esterilizados. 4.- Dejar enfriar y vaciar en 3 cajas Petri estériles ( utilizar 3 cajas para cada medio de cultivo). 5.- Dejar solidificar, invertir y refrigerar. Segunda sesión (Extraclase): 4.- Recolección de muestras de exudado faríngeo. La muestra se toma en ayuno, con ayuda de un hisopo se frota la parte posterior de la garganta, en las amígdalas o donde haya inflamación. Hisopo 5.- Descargar la muestra, realizando un estriado continuo en gelosa sangre, agar sal-manitol, agar eosina azul de metileno y agar Biggy. 6.- Incubar dichos medios, a ±35 o C durante horas. Tercera sesión: 7.- Observación de las características macroscópicas en los medios que hayan presentado crecimiento. 8.- Realizar tinción de Gram de las colonias sospechosas. Observar las características microscópicas a inmersión. 9.- Identificar los microorganismos que desarrollaron en las cajas, dependiendo de las características microscópicas, macroscópicas y bioquímicas de éstos Esterilizar los medios utilizados. Cuestionario: 1.- Describa los microorganismos que conforman la flora habitual de faringe. 2.- Describa los principales agentes etiológicos de patologías de las vías respiratorias altas. 3.- Cuáles son los microorganismos que se pueden aislar en un exudado faríngeo, en pacientes debilitados u hospitalizados?. 4.- Cuál es la utilidad de un cultivo de exudado faríngeo?
20 Laboratorio de Microbiología y Parasitología Práctica No. 8 Objetivos: ***Búsqueda de parásitos en hortalizas*** Realizar coproparasitoscópico por método directo y por concentración. Identificar parásitos intestinales (quistes, huevecillos, larvas) mediante examen microscópico. Material: Tubos de ensayo de 13 x 100 mm Pipetas transfer Vaso de precipitado de 1000 ml Portaobjetos Cubreobjetos Aplicadores de madera Papel seda Centrífuga Microscopio óptico Papel Material biológico: Hortalizas: rábano, lechuga, apio, acelga, cilantro, repollo Reactivos: Solución salina isotónica (NaCl al 0.85%) Lugol Solución de ZnSO 4 (densidad 1.18 g/ml) -Disolver 330g de sulfato de zinc en aproximadamente 670 ml de agua destilada y ajustar la densidad a 1.18 g/ml). Procedimiento: - Preparación de la muestra 1.- En un vaso de precipitado, hacer una suspensión de cada hortaliza, sumergiendo las hojas o la hortaliza en 500 ml de solución salina isotónica y dejar reposar una hora. 2.-Decantar la muestra y dividir el sedimento en dos tubos de ensayo (enumerar como tubo 1 y tubo 2). 3.-Centrifugar las muestras a 2500 rpm durante 10 minutos. 4.-Decantar la muestra. -Método directo:
21 1.- Colocar una gota del sedimento del tubo 1 en un portaobjeto y otra gota en otro portaobjeto, a este segundo adicionarle una gota de Lugol. 3.-Poner en cada muestra el cubreobjeto y observar al microscopio con el objetivo de 10x y 40x. -Método de concentración: 1.- Resuspenda el sedimento del fondo del tubo 2, con 1 2 ml de sulfato de zinc. 2.- Lleve el volumen hasta 5 mm antes de la orilla del tubo, con el sulfato de zinc. 3.- Centrifugue 1 minuto a 1000 rpm. 4.- Deje reposar por 2 3 minutos. 5.- Tome con una pipeta Pasteur o con el asa bacteriológica una o dos gotas de la película superficial. 6.- Coloque la muestra sobre el portaobjetos y añada una gota de Lugol. 10.-Coloque un cubreobjetos sobre la muestra y observe a 10x y 40x. 11.-Decante el sobrenadante y con la misma pipeta Pasteur o con el asa, tome una muestra del sedimento y añada una gota de Lugol Coloque un cubreobjetos sobre la muestra y observe a 10x y 40x. Cuestionario: 1.- Describa la clasificación taxonómica de los parásitos. 2.- De las siguientes enfermedades parasitarias, indique el agente causal y su forma de transmisión. Protozoarios:Amibiasis b) Giardiasis c) Toxoplasmosis d) Paludismo e) Enfermedad de Chagas Helmintos: a) Teniasis b) Ascariasis c) Trichuriasis d) Triquinosis e) Enterobiasis
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO. OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico.
 GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
PREPARACIONES Y TINCIONES
 PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
PRÁCTICO N 3. Técnicas para la observación, aislamiento y conservación de microorganismos
 PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión)
 PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para
PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA
 PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
MANUAL DE OPERACIONES. DIRECCIÓN DE INVESTIGACIÓN Fecha: JUN 15 SUBDIRECCIÓN DE INVESTIGACIÓN BIOMÉDICA MANUAL DE TINCIONES
 A Hoja: de 0 MANUAL DE TINCIONES Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma Hoja: 2 de 0. Propósito Establecer las técnicas y condiciones para la realización de tinciones utilizadas en
A Hoja: de 0 MANUAL DE TINCIONES Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma Hoja: 2 de 0. Propósito Establecer las técnicas y condiciones para la realización de tinciones utilizadas en
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO
 PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
 Sema na 3 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre 2014-1 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES PROTOCOLO / UNIDAD
Sema na 3 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre 2014-1 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES PROTOCOLO / UNIDAD
Semana 2. ECOLOGÍA MICROBIANA
 Semana 2. ECOLOGÍA MICROBIANA LUNES 14 DE MAYO PRACTICA # 1A. Columna de Winogradsky 1 matraz aforado de 100 ml 1 matraz Erlenmeyer de 500 ml 1 probeta de 250 ml 1 varilla de vidrio 1 vaso de precipitados
Semana 2. ECOLOGÍA MICROBIANA LUNES 14 DE MAYO PRACTICA # 1A. Columna de Winogradsky 1 matraz aforado de 100 ml 1 matraz Erlenmeyer de 500 ml 1 probeta de 250 ml 1 varilla de vidrio 1 vaso de precipitados
Materiales. Cultivos puros de bacterias: Streptomyces griseus Streptomyces erythraeus
 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos.
 Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos. Objetivos Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación
Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos. Objetivos Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Introducción
 PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
Preparaciones Microbiológicas. Preparaciones en fresco (microorganismos vivos) Preparaciones fijas y teñidas (microorganismos muertos)
 Preparaciones Microbiológicas Preparaciones en fresco (microorganismos vivos) Preparaciones fijas y teñidas (microorganismos muertos) Frotis Una capa delgada de muestra extendida sobre un portaobjetos
Preparaciones Microbiológicas Preparaciones en fresco (microorganismos vivos) Preparaciones fijas y teñidas (microorganismos muertos) Frotis Una capa delgada de muestra extendida sobre un portaobjetos
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON
 PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
EXAMEN EN FRESCO DE HECES Y PRESENCIA DE HUEVOS PRACTICA 3
 EXAMEN EN FRESCO DE HECES Y PRESENCIA DE HUEVOS PRACTICA 3 1. Introducción Examen macroscópico Es importante determinar la consistencia de las heces fecales y clasificarlas en líquidas, blandas o duras,
EXAMEN EN FRESCO DE HECES Y PRESENCIA DE HUEVOS PRACTICA 3 1. Introducción Examen macroscópico Es importante determinar la consistencia de las heces fecales y clasificarlas en líquidas, blandas o duras,
Materiales. Cultivos puros de hongos: Saccharomyces cerevisiae Rhodototula sp Penicillum sp Aspergillus niger Rhizopous sp Alternaria sp Fusarium sp
 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos algas y protozoarios Práctica 5. Técnicas de siembra y cultivo de bacterias y hongos Objetivos Aplicar
Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos algas y protozoarios Práctica 5. Técnicas de siembra y cultivo de bacterias y hongos Objetivos Aplicar
PRÁCTICA 5.1 Aislamiento de Microorganismos
 PRÁCTICA 5.1 Aislamiento de Microorganismos Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
PRÁCTICA 5.1 Aislamiento de Microorganismos Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión)
 Objetivos PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
Objetivos PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES
 ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
PRACTICA Núm. 3 PREPARACIONES DE EXTENSIONES O FROTIS Y TINCION SIMPLE
 PRACTICA Núm. 3 PREPARACIONES DE EXTENSIONES O FROTIS Y TINCION SIMPLE I. OBJETIVO Conocer el procedimiento para preparar extensiones ó frotis y los diferentes métodos de tinción, así como su utilidad
PRACTICA Núm. 3 PREPARACIONES DE EXTENSIONES O FROTIS Y TINCION SIMPLE I. OBJETIVO Conocer el procedimiento para preparar extensiones ó frotis y los diferentes métodos de tinción, así como su utilidad
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA
 FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo
 Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
PARTE EXPERIMENTAL 1 MATERIALES, EQUIPOS Y REACTIVOS 1.1 MATERIAL Y EQUIPOS
 II PARTE EXPERIMENTAL El presente trabajo se realizó en el laboratorio del Centro Latino Americano de Enseñanza e Investigación de Bacteriología Alimentaria (CLEIBA), con sede en la Facultad de Farmacia
II PARTE EXPERIMENTAL El presente trabajo se realizó en el laboratorio del Centro Latino Americano de Enseñanza e Investigación de Bacteriología Alimentaria (CLEIBA), con sede en la Facultad de Farmacia
- Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio microbiológico.
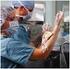 Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
OBJETIVOS CRECIMIENTO MICROBIANO EN MEDIO SÓLIDO
 UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA PROGRAMA: CIENCIAS AMBIENTALES ÁREA: AGRO Y MAR CÁTEDRA: Microbiología e Inmunología Veterinaria PROF: JOSÉ ARAUJO Actividad Prática 3 OBJETIVOS 1
UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA PROGRAMA: CIENCIAS AMBIENTALES ÁREA: AGRO Y MAR CÁTEDRA: Microbiología e Inmunología Veterinaria PROF: JOSÉ ARAUJO Actividad Prática 3 OBJETIVOS 1
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA Mª PAZ MERINO JIMÉNEZ MIREIA LLINARES MARCELO PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA A mi padre. M.
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA Mª PAZ MERINO JIMÉNEZ MIREIA LLINARES MARCELO PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA A mi padre. M.
PRACTICA 2 TINCION DE GRAM
 PRACTICA 2 TINCION DE GRAM OBJETIVOS DE APRENDIZAJE: Cuando haya completado este experimento, usted debe comprender: 1. La base teórica y química de los procedimientos de tinción diferencial. 2. La base
PRACTICA 2 TINCION DE GRAM OBJETIVOS DE APRENDIZAJE: Cuando haya completado este experimento, usted debe comprender: 1. La base teórica y química de los procedimientos de tinción diferencial. 2. La base
UNIVERSIDAD DE CIENCIAS Y ARTES DE CHIAPAS
 1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA DE ALIMENTOS ELABORO: M. EN C. GILBER VELA GUTIÉRREZ Y M.
1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA DE ALIMENTOS ELABORO: M. EN C. GILBER VELA GUTIÉRREZ Y M.
Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas
 Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
1ª PRÁCTICA DE MICROBIOLOGÍA:
 1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II
 UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II Maye Bernal Rivera PARTE II. LECTURA E INTERPRETACION DE LOS CULTIVOS
UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II Maye Bernal Rivera PARTE II. LECTURA E INTERPRETACION DE LOS CULTIVOS
UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR
 UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR Catedrático: Dra. Ana Olivia cañas Urbina. PRACTICA No. 3: TINCIONES Equipo:
UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR Catedrático: Dra. Ana Olivia cañas Urbina. PRACTICA No. 3: TINCIONES Equipo:
Laboratorio de Agroindustria II. Calidad de Leche
 Laboratorio de Agroindustria II. Calidad de Leche Medio de cultivo: Caldo lactosado biliado verde brillante (Brilliant Green Bile Lactose: BGBL) Composición - Peptona 10 g. - Lactosa 10 g. - Bilis de buey
Laboratorio de Agroindustria II. Calidad de Leche Medio de cultivo: Caldo lactosado biliado verde brillante (Brilliant Green Bile Lactose: BGBL) Composición - Peptona 10 g. - Lactosa 10 g. - Bilis de buey
EXAMEN PRACTICO NIVEL II Tema: Microbiología General
 EXAMEN PRACTICO NIVEL II Tema: Microbiología General Puntaje Total: 50 puntos Introducción Una de las principales áreas de la Microbiología es la Microbiología diagnóstica, en la cual un microbiólogo aísla
EXAMEN PRACTICO NIVEL II Tema: Microbiología General Puntaje Total: 50 puntos Introducción Una de las principales áreas de la Microbiología es la Microbiología diagnóstica, en la cual un microbiólogo aísla
EXPLICACIÓN DE TRABAJOS PRÁCTICOS COLORACIONES
 EXPLICACIÓN DE TRABAJOS PRÁCTICOS COLORACIONES Microbiología General Carrera: Tecnicatura Universitaria en Esterilización Analista Biológico 2015 DIFERENCIA ENTRE CÉLULA PROCARIOTA Y CÉLULA EUCARIOTA Morfología
EXPLICACIÓN DE TRABAJOS PRÁCTICOS COLORACIONES Microbiología General Carrera: Tecnicatura Universitaria en Esterilización Analista Biológico 2015 DIFERENCIA ENTRE CÉLULA PROCARIOTA Y CÉLULA EUCARIOTA Morfología
Tema I Introducción al estudio de los agentes biológicos de importancia médica.
 Tema I Introducción al estudio de los agentes biológicos de importancia médica. - Características de las células procarióticas y eucarióticas. - Microscopía y coloraciones. 2da Parte Esporas Se forma bajo
Tema I Introducción al estudio de los agentes biológicos de importancia médica. - Características de las células procarióticas y eucarióticas. - Microscopía y coloraciones. 2da Parte Esporas Se forma bajo
1ª sesión. Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo
 Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Técnicas de observación de microorganismos
 Fundamentos y técnicas de análisis microbiológicos Técnicas de observación de microorganismos - 1 Técnicas de observación de microorganismos El examen microscópico es el primer paso para el estudio de
Fundamentos y técnicas de análisis microbiológicos Técnicas de observación de microorganismos - 1 Técnicas de observación de microorganismos El examen microscópico es el primer paso para el estudio de
GUIA DE LABORATORIO PRACTICA 7 CELULAS PROCARIOTAS PROGRAMA DE INGENIERIA PECUARIA BIOLOGÍA GENERAL
 GUIA DE LABORATORIO PRACTICA 7 CELULAS PROCARIOTAS PROGRAMA DE INGENIERIA PECUARIA BIOLOGÍA GENERAL Leidy Diana Ardila Leal Docente. INTRODUCCIÓN Los organismos procariotas son por los organismos más abundantes
GUIA DE LABORATORIO PRACTICA 7 CELULAS PROCARIOTAS PROGRAMA DE INGENIERIA PECUARIA BIOLOGÍA GENERAL Leidy Diana Ardila Leal Docente. INTRODUCCIÓN Los organismos procariotas son por los organismos más abundantes
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS
 PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
TEMA 5: LABORATORIO PIPETA GRADUADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA PIPETA AFORADA MATRAZ DE FONDO PLANO MATRAZ DE FONDO REDONDO MATRAZ AFORADO
 TEMA 5: LABORATORIO PIPETA GRADUADA PIPETA AFORADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA BURETA DE FONDO REDONDO DE FONDO PLANO AFORADO DE DESTILACIÓN ERLENMEYER PROBETA FRASCO TRANSPARENTE FRASCOS TOPACIO
TEMA 5: LABORATORIO PIPETA GRADUADA PIPETA AFORADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA BURETA DE FONDO REDONDO DE FONDO PLANO AFORADO DE DESTILACIÓN ERLENMEYER PROBETA FRASCO TRANSPARENTE FRASCOS TOPACIO
Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Nombre: Nombre: Nombre: Nombre: Nombre:
 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 0. Ejemplos de mezcla homogénea y heterogénea Texto original: Dra. Laura María Gasque
Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 0. Ejemplos de mezcla homogénea y heterogénea Texto original: Dra. Laura María Gasque
Tema 4.- Técnicas de siembra y aislamiento
 Tema 4.- Técnicas de siembra y aislamiento La siembra consiste en tomar con el asa de platino, previamente flameado, o con hisopo estéril una pequeña cantidad de muestra a estudiar y repartirla por toda
Tema 4.- Técnicas de siembra y aislamiento La siembra consiste en tomar con el asa de platino, previamente flameado, o con hisopo estéril una pequeña cantidad de muestra a estudiar y repartirla por toda
ENUMERACIÓN DE ENTEROBACTERIACEAE EN ALIMENTOS SIN RESUSCITACIÓN. TÉCNICA RECUENTO EN PLACA
 PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL
 I. OBJETIVO PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL Determinar la presencia de coliformes totales y fecales en agua residual por el método del Número Más Probable,
I. OBJETIVO PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL Determinar la presencia de coliformes totales y fecales en agua residual por el método del Número Más Probable,
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
INSTRUMENTOS BÁSICOS DE UN LABORATORIO
 INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
2.8 Estudio microscópico de los microorganismos.
 2.8 Estudio microscópico de los microorganismos. http://es.dreamstime.com/imagenes-de-archivo-microscopio-y-bacterias-image29404744 Preparaciones Microbiológicas Preparaciones en fresco (microorganismos
2.8 Estudio microscópico de los microorganismos. http://es.dreamstime.com/imagenes-de-archivo-microscopio-y-bacterias-image29404744 Preparaciones Microbiológicas Preparaciones en fresco (microorganismos
Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas
 Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
1ª sesión. Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo
 Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
2. Observación de hongos de interés industrial
 2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO
 RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO Fundamento Los alimentos se diferencian entre sí por las sustancias o principios inmediatos que contienen y por la cantidad de cada uno
RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO Fundamento Los alimentos se diferencian entre sí por las sustancias o principios inmediatos que contienen y por la cantidad de cada uno
Universidad Autónoma Metropolitana- Iztapalapa. Academia de Microbiología, Departamento de Biotecnología
 Universidad Autónoma Metropolitana- Iztapalapa MANUAL DE PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGIA GENERAL Academia de Microbiología, Departamento de Biotecnología Participantes: Dra. María de los Angeles
Universidad Autónoma Metropolitana- Iztapalapa MANUAL DE PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGIA GENERAL Academia de Microbiología, Departamento de Biotecnología Participantes: Dra. María de los Angeles
MANUAL DE PREPARACIÓN DE REACTIVOS
 MOP-SIB-3 DIRECCIÓN DE INVESTIGACIÓN Fecha: JUN 5 Hoja: de MANUAL DE PREPARACIÓN DE REACTIVOS Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma F0-SGC-0 Rev.2 MOP-SIB-3 DIRECCIÓN DE INVESTIGACIÓN
MOP-SIB-3 DIRECCIÓN DE INVESTIGACIÓN Fecha: JUN 5 Hoja: de MANUAL DE PREPARACIÓN DE REACTIVOS Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma F0-SGC-0 Rev.2 MOP-SIB-3 DIRECCIÓN DE INVESTIGACIÓN
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo
 PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su utilidad en microbiología. Preparar
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su utilidad en microbiología. Preparar
BIORREACTRES. Estudios básicos y aplicados sobre procesos de fermentación
 BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
MANUAL DE PREPARACIÓN DE MEDIOS DE CULTIVO
 Rev. 02 Hoja: 1 de 14 MANUAL DE PREPARACIÓN DE MEDIOS DE Elaboró: Revisó: Autorizó: Puesto QUÍMICO JEFE DEL LABORATORIO SUBDIRECTOR DE INVESTIGACIÓN Firma Hoja: 2 de 14 1. Propósito Definir y describir
Rev. 02 Hoja: 1 de 14 MANUAL DE PREPARACIÓN DE MEDIOS DE Elaboró: Revisó: Autorizó: Puesto QUÍMICO JEFE DEL LABORATORIO SUBDIRECTOR DE INVESTIGACIÓN Firma Hoja: 2 de 14 1. Propósito Definir y describir
Método de flotación con sulfato de zinc de densidad. heces por flotación. Rina G. de Kaminsky
 Método de flotación con sulfato de zinc de densidad 118o120 1.18 1.20. Método de concentración de heces por flotación. Rina G. de Kaminsky Métodos de concentración Cuando el examen directo de heces resulta
Método de flotación con sulfato de zinc de densidad 118o120 1.18 1.20. Método de concentración de heces por flotación. Rina G. de Kaminsky Métodos de concentración Cuando el examen directo de heces resulta
Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias.
 Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias. Objetivos Relacionar la actividad metabólica de los microorganismos con los cambios producidos en diferentes
Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias. Objetivos Relacionar la actividad metabólica de los microorganismos con los cambios producidos en diferentes
Universidad Autónoma Metropolitana- Iztapalapa
 Universidad Autónoma Metropolitana- Iztapalapa Este manual está dirigido a estudiantes de la UEA Microbiología General, que forma parte del plan de estudio de las carreras de Ingeniería de los Alimentos
Universidad Autónoma Metropolitana- Iztapalapa Este manual está dirigido a estudiantes de la UEA Microbiología General, que forma parte del plan de estudio de las carreras de Ingeniería de los Alimentos
Material de uso frecuente en el laboratorio de química. Figura Nombre Uso / Características. Crisol. Espátula de porcelana. Capsula de porcelana
 Material de uso frecuente en el laboratorio de química. En un Laboratorio de Química se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio.
Material de uso frecuente en el laboratorio de química. En un Laboratorio de Química se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio.
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS
 PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
Clostridium perfringens
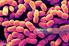 Clostridium perfringens Introducción Cuando se lanza un producto alimentario al mercado se deben tener en cuenta varios parámetros que le otorgan calidad al producto, uno de ellos es la inocuidad. Los
Clostridium perfringens Introducción Cuando se lanza un producto alimentario al mercado se deben tener en cuenta varios parámetros que le otorgan calidad al producto, uno de ellos es la inocuidad. Los
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE
 COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE PRACTICA # 1 CAMBIOS QUÍMICOS OBJETIVO DE LA PRÁCTICA: Identificar que los cambios químicos están acompañados
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE PRACTICA # 1 CAMBIOS QUÍMICOS OBJETIVO DE LA PRÁCTICA: Identificar que los cambios químicos están acompañados
PRÁCTICA 2.2 Preparaciones Microbiológicas
 PRÁCTICA 2.2 Preparaciones Microbiológicas 2.2.1 Preparaciones húmedas 2.2.2 Gota pendiente 2.2.3 Preparaciones fijas 2.2.4 Tinción simple Objetivos Al finalizar esta práctica el alumno será capaz de:
PRÁCTICA 2.2 Preparaciones Microbiológicas 2.2.1 Preparaciones húmedas 2.2.2 Gota pendiente 2.2.3 Preparaciones fijas 2.2.4 Tinción simple Objetivos Al finalizar esta práctica el alumno será capaz de:
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
Práctica nº 1. Reconocimiento del material. Objetivo: conocer todo el material que puede haber en un laboratorio.
 Práctica nº 1. Reconocimiento del material. Objetivo: conocer todo el material que puede haber en un laboratorio. Matraz aforado: tiene forma de pera con fondo plano o curvo (finalidad calentar el contenido),
Práctica nº 1. Reconocimiento del material. Objetivo: conocer todo el material que puede haber en un laboratorio. Matraz aforado: tiene forma de pera con fondo plano o curvo (finalidad calentar el contenido),
AISLAMIENTO DE MICROORGANISMOS
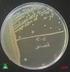 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA
 TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA 1. Competencias Industrializar materias primas a través de procesos tecnológicos, para
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA 1. Competencias Industrializar materias primas a través de procesos tecnológicos, para
CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:
 CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:55-2231189 WWW.LICEOINDUSTRIALEGM.CL GUÍA DE APRENDIZAJE Profesor Asignatura Objetivo de Aprendizaje
CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:55-2231189 WWW.LICEOINDUSTRIALEGM.CL GUÍA DE APRENDIZAJE Profesor Asignatura Objetivo de Aprendizaje
Laboratorio Nacional de Salud Pública
 1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
TRABAJO PRÁCTICO N 3 SOLUCIONES. Concepto de solución: Una solución es un sistema material homogéneo formado por dos o más componentes.
 TRABAJO PRÁCTICO N 3 SOLUCIONES Introducción Concepto de solución: Una solución es un sistema material homogéneo formado por dos o más componentes. Concentración de soluciones: En su forma más amplia de
TRABAJO PRÁCTICO N 3 SOLUCIONES Introducción Concepto de solución: Una solución es un sistema material homogéneo formado por dos o más componentes. Concentración de soluciones: En su forma más amplia de
Manual de Instrucciones
 Manual de Instrucciones 1 2 Isabel N. de Kantor (PAHO/OPS) Amelia Bernardelli (SENASA) Manual de Instrucciones Este Manual de Instrucciones presenta la metodología que se debe seguir para el cultivo de
Manual de Instrucciones 1 2 Isabel N. de Kantor (PAHO/OPS) Amelia Bernardelli (SENASA) Manual de Instrucciones Este Manual de Instrucciones presenta la metodología que se debe seguir para el cultivo de
Material y Reactivos de Laboratorio. Marcas que manejamos:
 Marcas que manejamos: Portaobjetos y Cubreobjetos Caja de Petri Sencilla, Doble y Triple Dispensador de Laminillas Jarra de Coplin Cajas para portaobjetos Pipeta Pasteur 150mm 5.75" y 229mm 9" Puntas para
Marcas que manejamos: Portaobjetos y Cubreobjetos Caja de Petri Sencilla, Doble y Triple Dispensador de Laminillas Jarra de Coplin Cajas para portaobjetos Pipeta Pasteur 150mm 5.75" y 229mm 9" Puntas para
GUIA DE LABORATORIO DE BIOLOGIA CELULAR Y MOLECULAR MEDICINA VETERINARIA Y ZOOTECNIA UNIVERSIDAD TECNOLOGICA DE PEREIRA
 GUIA DE LABORATORIO DE BIOLOGIA CELULAR Y MOLECULAR MEDICINA VETERINARIA Y ZOOTECNIA UNIVERSIDAD TECNOLOGICA DE PEREIRA NORMAS GENERALES PARA EL TRABAJO EN EL LABORATORIO 1. Usar bata de laboratorio 2.
GUIA DE LABORATORIO DE BIOLOGIA CELULAR Y MOLECULAR MEDICINA VETERINARIA Y ZOOTECNIA UNIVERSIDAD TECNOLOGICA DE PEREIRA NORMAS GENERALES PARA EL TRABAJO EN EL LABORATORIO 1. Usar bata de laboratorio 2.
B) Añadir al medio LB, además de la ampicilina, el IPTG (conc final, 0.5 mm) y X-Gal (conc. final 80 µg/ml). Es decir, para 100 ml de LB adicionar:
 Medios utilizados en este apartado: 1.-IPTG stock solution (0.1 M) - 0.6 g IPTG. - Añadir agua estéril a un volumen final de 25 ml. Filtrar con papel secante pasando la solución a tubos eurotubos. Guardar
Medios utilizados en este apartado: 1.-IPTG stock solution (0.1 M) - 0.6 g IPTG. - Añadir agua estéril a un volumen final de 25 ml. Filtrar con papel secante pasando la solución a tubos eurotubos. Guardar
PRÁCTICAS DE QUÍMICA P-11: Preparación de una disolución 0,1M de Hidróxido de sodio (sosa)
 NOTA: PRÁCTICAS DE QUÍMICA P-11: Preparación de una disolución 0,1M de Hidróxido de sodio (sosa) Alumno: Fecha: Curso: 1. OBJETIVOS - Manejo del material básico de laboratorio. - Aprender a preparar disoluciones
NOTA: PRÁCTICAS DE QUÍMICA P-11: Preparación de una disolución 0,1M de Hidróxido de sodio (sosa) Alumno: Fecha: Curso: 1. OBJETIVOS - Manejo del material básico de laboratorio. - Aprender a preparar disoluciones
UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS
 UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS INTRODUCCIÓN. Para el diagnóstico y estudio de enfermedades, en la mayoría
UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS INTRODUCCIÓN. Para el diagnóstico y estudio de enfermedades, en la mayoría
Asignaturas antecedentes y subsecuentes
 PROGRAMA DE ESTUDIOS Microbiología General Área a la que pertenece: AREA SUSTANTIVA PROFESIONAL Horas teóricas: 3 Horas practicas: 3 Créditos: 9 Clave: F0219 Ninguna. Asignaturas antecedentes y subsecuentes
PROGRAMA DE ESTUDIOS Microbiología General Área a la que pertenece: AREA SUSTANTIVA PROFESIONAL Horas teóricas: 3 Horas practicas: 3 Créditos: 9 Clave: F0219 Ninguna. Asignaturas antecedentes y subsecuentes
ESAS METAS SON RESPONSABILIDAD DE TODOS Y CADA UNO DE LOS QUE PARTICIPAN EN LABORATORIO.
 INTRODUCCION AL TRABAJO DE LABORATORIO En el trabajo cotidiano existen riesgos y con mucha más razón si el trabajo se desarrolla en el laboratorio, debido a que se experimentan una serie de situaciones
INTRODUCCION AL TRABAJO DE LABORATORIO En el trabajo cotidiano existen riesgos y con mucha más razón si el trabajo se desarrolla en el laboratorio, debido a que se experimentan una serie de situaciones
LABORATORIO GRUPO 15. NaOH NH 3
 Química Inorgánica Laboratorio Grupo 15 1 A) OBTENCIÓN DE AMONÍACO LABORATORIO GRUPO 15 Materiales: balanza granataria, un tubo de ensayos con tapón con un tubo de vidrio doblado 90,... Reactivos: cloruro
Química Inorgánica Laboratorio Grupo 15 1 A) OBTENCIÓN DE AMONÍACO LABORATORIO GRUPO 15 Materiales: balanza granataria, un tubo de ensayos con tapón con un tubo de vidrio doblado 90,... Reactivos: cloruro
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS
 DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
Microscopio y observación de células
 I.E.S. Rayuela - Departamento de Biología y Geología Práctica nº1 de Anatomía Aplicada Microscopio y observación de células Las células suelen ser de tamaño muy pequeño de modo que permanecen invisibles
I.E.S. Rayuela - Departamento de Biología y Geología Práctica nº1 de Anatomía Aplicada Microscopio y observación de células Las células suelen ser de tamaño muy pequeño de modo que permanecen invisibles
Los pasos a seguir para la toma de material a partir de abscesos de origen bucal son:
 Trabajos Prácticos Nº 6 y 7 Diagnóstico microbiológico directo Objetivos. Describir la importancia de la toma de muestra en el diagnóstico etiológico de un absceso de origen bucal. Describir los requisitos
Trabajos Prácticos Nº 6 y 7 Diagnóstico microbiológico directo Objetivos. Describir la importancia de la toma de muestra en el diagnóstico etiológico de un absceso de origen bucal. Describir los requisitos
GUÍA DE LABORATORIO. MICROBIOLOGÍA BÁSICA
 26 2017 GUÍA DE LABORATORIO. MICROBIOLOGÍA BÁSICA Documentos de docencia Course Work Coursework.ucc.edu.co N 26, diciembre de 2017 doi: https://doi.org/10.16925/greylit.2274 Maria Eugenia Castaño Orozco
26 2017 GUÍA DE LABORATORIO. MICROBIOLOGÍA BÁSICA Documentos de docencia Course Work Coursework.ucc.edu.co N 26, diciembre de 2017 doi: https://doi.org/10.16925/greylit.2274 Maria Eugenia Castaño Orozco
ACTIVIDAD EXPERIMENTAL 1 CONOCIMIENTO Y MANEJO DE LOS MICROSCOPIOS COMPUESTO Y ESTEREOSCOPICO
 ACTIVIDAD EXPERIMENTAL 1 CONOCIMIENTO Y MANEJO DE LOS MICROSCOPIOS COMPUESTO Y ESTEREOSCOPICO OBJETIVO Conocerás los diferentes microscopios que se emplean en el laboratorio de Biología para hacer uso
ACTIVIDAD EXPERIMENTAL 1 CONOCIMIENTO Y MANEJO DE LOS MICROSCOPIOS COMPUESTO Y ESTEREOSCOPICO OBJETIVO Conocerás los diferentes microscopios que se emplean en el laboratorio de Biología para hacer uso
REPÚBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD NACIONAL EXPERIMENTAL POLITÉCNICA ANTONIO JOSÉ DE SUCRE DEPARTAMNETO DE INGENIERIA QUIMICA
 Práctica Nº1: Introducción a las técnicas fundamentales del Laboratorio Químico En el laboratorio existen una variedad materiales, y cada uno de ellos debe ser utilizado apropiadamente. Por esta razón,
Práctica Nº1: Introducción a las técnicas fundamentales del Laboratorio Químico En el laboratorio existen una variedad materiales, y cada uno de ellos debe ser utilizado apropiadamente. Por esta razón,
PRÁCTICA No. 1 INSTRUMENTOS DE LABORATORIO
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA ESCUELA DE FORMACION DE PROFESORES DE ENSEÑANZA MEDIA-EFPEM- CURSO: BIOLOGÍA I CATEDRÁTICOS: LIC. JAIME TRES/LICDA. IVONNE RUANO ENCARGADOS DE LABORATORIO: PEM MOISES
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA ESCUELA DE FORMACION DE PROFESORES DE ENSEÑANZA MEDIA-EFPEM- CURSO: BIOLOGÍA I CATEDRÁTICOS: LIC. JAIME TRES/LICDA. IVONNE RUANO ENCARGADOS DE LABORATORIO: PEM MOISES
PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL
 ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL I 1. INTRODUCCION: PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL Los cambios químicos
ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL I 1. INTRODUCCION: PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL Los cambios químicos
REQUERIMIENTOS TÉCNICO ADMINISTRATIVOS POR TIPO DE ESTABLECIMIENTO
 S TÉCNICO ADMINISTRATIVOS POR TIPO DE ESTABLECIMIENTO TIPO DE ESTABLECIMIENTO LABORATORIO CLÍNICO NIVEL 2 DE REFERENCIA, PRUEBAS BÁSICAS, MICROBIOLOGIA Y PRUEBAS ESPECIALES JUNTA(S) DE VIGILANCIA RESPONSABLE(S)
S TÉCNICO ADMINISTRATIVOS POR TIPO DE ESTABLECIMIENTO TIPO DE ESTABLECIMIENTO LABORATORIO CLÍNICO NIVEL 2 DE REFERENCIA, PRUEBAS BÁSICAS, MICROBIOLOGIA Y PRUEBAS ESPECIALES JUNTA(S) DE VIGILANCIA RESPONSABLE(S)
Práctica # 2: Reconocimiento de Material de Laboratorio Y Técnicas Experimentales
 República Bolivariana de Venezuela Ministerio del poder popular para la Educación Unidad Educativa Colegio Aplicación Palo Gordo-Edo. Táchira Lcda. Katherine Gómez Práctica # 2: Reconocimiento de Material
República Bolivariana de Venezuela Ministerio del poder popular para la Educación Unidad Educativa Colegio Aplicación Palo Gordo-Edo. Táchira Lcda. Katherine Gómez Práctica # 2: Reconocimiento de Material
PRÁCTICA 3 PRINCIPIO DE CONSERVACIÓN DE LA MATERIA: TRANSFORMACIONES QUÍMICAS DE COBRE
 PRÁCTICA 3 PRINCIPIO DE CONSERVACIÓN DE LA MATERIA: TRANSFORMACIONES QUÍMICAS DE COBRE OBJETIVOS Poner de manifiesto el Principio de Conservación de la Materia mediante un ciclo de reacciones de cobre.
PRÁCTICA 3 PRINCIPIO DE CONSERVACIÓN DE LA MATERIA: TRANSFORMACIONES QUÍMICAS DE COBRE OBJETIVOS Poner de manifiesto el Principio de Conservación de la Materia mediante un ciclo de reacciones de cobre.
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS
 TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS HOJA DE ASIGNATURA CON DESGLOSE DE UNIDADES TEMÁTICAS 1. Nombre de la asignatura Microbiología. 2. Competencias a la que contribuye la asignatura
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS HOJA DE ASIGNATURA CON DESGLOSE DE UNIDADES TEMÁTICAS 1. Nombre de la asignatura Microbiología. 2. Competencias a la que contribuye la asignatura
