γ 13 C = C RMN H = ν = H o H 0 (T) ν 1 H RMN (MHz)* ν 13 C RMN (MHz)
|
|
|
- María Jesús Bustamante Martínez
- hace 7 años
- Vistas:
Transcripción
1 RMN I = 0 No observable en RMN I = ½ BSERVABLE EN RMN Abundancia natural del =.% Sensibilidad INTENSIDAD DE LAS SEÑALES RMN se basa en los mismos principios que RMN: utilizando una RF adecuada (o un pulso de RF) se provocan transiciones entre distintos niveles energéticos, de los núcleos de, creados al someter la muestra a un externo ν = γ π o γ = 6.78 = Las frecuencias necesarias para provocar transiciones en RMN son menores que las utilizadas en RMN ( /) 0 (T) ν RMN (Mz)* ν RMN (Mz) *Valor utilizado para referirnos al tipo de espectrómetro
2 INFRMAIÓN FUNDAMENTAL DE LA RMN: Número de en base al número de señales (los químicamente equivalentes tienen el mismo desplazamiento químico) Entorno magnético en base a los desplazamientos químicos Número de a los que está unido cada (,,, ) La mayoría de las señales en RMN se encuentran entre 0 y 50 ppm a campo más bajo ( δ) que en el TMS Se usa el TMS como referencia Menor probabilidad de solapamiento de señales en RMN que en RMN (el intervalo de δ es 5 veces mayor en RMN) Debido a la baja abundancia del : Inconveniente: se necesita más muestra y/o más tiempo para hacer un RMN que para un RMN Ventaja: no se observan acoplamientos - ( probabilidad de encontrar a dos contiguos) y esto simplifica mucho los espectros En RMN se observan: Acoplamientos - a un enlace ( J) de gran magnitud 5-00z que complican bastante los espectros pero que permiten distinguir entre primarios, secundarios, terciarios y cuaternarios: c t d s Acoplamientos - a dos y tres enlaces ( J y J) de menor magnitud 0-0z (J decae rápidamente con la distancia)
3 RMN A 90Mz (l ) Metilciclohexano * * 5 líneas en RMN RMN A 00Mz (l ) RMN A 00.59Mz (l ) 5 Líneas: δ = 5.8,., 6.8, 6.7 y. ppm ppm
4 Desacoplamiento de hidrógeno de banda ancha (BB decoupling) Es una técnica de DR que consiste en: irradiar la muestra con una RF intensa que cubra la ν de resonancia de todos los hidrógenos, a la vez que con otra RF se produce la resonancia de los carbonos de la muestra Así, los están en constante cambio entre sus estados (α y β) y los solo ven un promedio de los campos locales inducidos por los. Resultado: Desaparecen los acoplamientos - Señales de singletes En RMN la integral generalmente no se utiliza. La intensidad de las señales no es proporcional al número de carbonos a que corresponden en la molécula. ada tipo de presenta un tiempo de relajación diferente (generalmente al sustitución t R ). En los RMN rutinarios algunos núcleos tienen tiempo entre pulso y pulso para relajarse (por ejemplo, intensidad) y otros no (por ejemplo =, intensidad) Intensidad relativa de señales en RMN Poniendo un tiempo de espera entre pulsos se soslaya este inconveniente en muchos casos, pero aumenta considerablemente el tiempo necesario para realizar un espectro. En espectros RMN desacoplados de se produce un efecto NE sobre los de gran intensidad (hasta 00%) pero distinto en cada tipo de arbonos Intensidad relativa de señales en RMN
5 (tc) Br (ct) RMN acoplado y ampliaciones TMS ppm RMN desacoplado TMS ppm
6 Ftalato de dietilo RMN (Dl, 5. Mz) * *() Acoplado (5) 5 6 (6) ppm () * (5) RMN (Dl, 5. Mz) Desacoplado (6) ppm
7 Ftalato de dietilo 5 6 RMN (Dl, 5. Mz) Desacoplado con un tiempo de espera entre pulsos * (5) () (6) ppm () * * (5) RMN (Dl, 5. Mz ff Resonance (6) ppm
8 Este inconveniente de la no proporcionalidad entre el número de y la intensidad de la señal a que dan lugar es a veces una ventaja: De la inspección de un espectro RMN se pueden reconocer los cuaternarios por su baja intensidad. Ejemplo: Ftalato de dietilo (acoplado, desacoplado, desacoplado con mayor tiempo de espera entre pulsos y off-resonance ) Desacoplamiento ff-resonance Es una experiencia de DR en la que se utiliza una ν de irradiación fuera del rango de la resonancia del (off-resonance) y con una menor intensidad de RF De esta forma, el desacoplamiento con los no es total, queda una acoplamiento residual que permite ver la multiplicidad de cada señal y por lo tanto saber cuantos hay unidos a cada arbono. Ejemplos: Ftalato de dietilo y -butanol Jresidual < Jreal espectro más sencillo que el totalmente acoplado pues, en general, existe menos solapamiento entre multipletes de distintos El valor de la Jresidual depende de la proximidad de la señal observada a la frecuencia de irradiación Jresidual = πj ν γ ν = ν ν J = constante real = intensidad de la RF del desacoplador ν = ν de resonancia del protón desacoplado ν = ν del desacoplador
9 Dl, 50Mz Dl ff Resonance Dl Acoplado DEPT Dl Desacoplado
10 DEPT: DISTRTINLESS ENANEMENT BY PLARIZATIN TRANSFER Utilizando diferentes condiciones ( secuencias de pulsos, con ángulos de pulso, θ) se pueden obtener: Espectros en los que solo se observan: ó ó Espectros en los que aparecen los tres tipos de carbonos simultáneamente pero con distinta fase: Positivos: y Negativos: En los espectros DEPT siempre están ausentes los cuaternarios El DEPT sustituye actualmente al off resonance, generalmente se hacen: RMN totalmente desacoplado ( BB decoupling ) y DEPT uando interesa el valor de J (,) el totalmente acoplado Ejemplos: -butanol, Ipsenol y ácido neuramínico Desplazamiento químico químicamente equivalentes Igual desplamiento químico (=δ) Los diastereotópicos no son químicamente equivalentes señales Ejemplo: Ipsenol * Diastereotópicos δ
11 ' IPSENL Diastereotópicos δ Espectro DEPT del Ipsenol Dl, 75.6Mz 7 y 7 ( ) ( ) Desacoplado
12 N 8, 5, 6 y 7 Desacoplado N ÁID NEURAMÍNI. RMN, D, 00.6Mz, δ = 0-0 ppm solamente. EXPERIMENTS DEPT +
13 Rotación restringida Igual que en RMN: * N señales a T ambiente en y RMN señal al aumentar T ( 5º) RMN, 90Mz t ambiente * * RMN, desacoplado.6mz, t ambiente
14 Equilibrios a b c c AETILAETNA, Dl a temperatura ambiente a lento a' b' c' rápido ó b' c' c' c' a' a' a' a RMN b a b TMS a c RMN b c b a δ
15 Disolventes Se emplean los mismos disolventes deuterados que en RMN. Tablas: ó pág La multiplicidad que en ellos se observa se debe a acoplamientos J (,D) líneas ( M = n I + = x x + = ) l l D l D cuadruplete con J (,F) ( M = x x / + = ) 7 líneas D F F F D D D S D D 7 líneas cuadruplete con J (,F) [< J (,F)] D D singlete El número de señales que se observan en un espectro de RMN totalmente desacoplado nos puede indicar el tipo de sustitución en sistemas bencénicos: R R R' 6 R R R R' 6 R R R R R' R
16 DESPLAZAMIENT QUIMI EN RMN DE LS MPUESTS RGANIS El orden en que aparecen los distintos carbonos en RMN es similar al de aparición de los correspondientes hidrógenos en RMN: TMS Alcanos icloalcanos Alquinos Alquenos c. Aromáticos = ompuestos arbonílicos δ FATRES QUE INFLUYEN EN LS DESPLAZAMIENTS QUÍMIS DE ibridación del átomo de carbono Efectos electrónicos Efectos estéricos En general la racionalización de los desplazamientos químicos de función de efectos estructurales es más problemática que en el caso de en ibridación del átomo de δ sp < sp < sp
17 Sustituyentes en posición α ejercen un efecto desapantallante independientemente de su naturaleza Excepción: átomos pesados (I y en algunos casos Br apantallamiento) Relación entre δ y la densidad de carga del considerado Influenciada por efectos inductivos ( en α) y conjugativos En compuestos alifáticos: Sustituyentes en β ejercen también un efecto desapantallante, generalmente menor que cuando se encuentran en α Sustitutyentes en γ ejercen un efecto apantallante (Efecto γ origen estérico) Ejemplos en los que se ponen de manifiesto los efectos mencionados en distintos tipos de compuestos: Sistemas saturados: γ β α N l 5.6 Br 9.6 I -.0 l 5.0 Br. I -5.0 l 77. Br. I -9.9 l 96. Br -8.7 I -9.5
18 Alquinos y derivados N Alquenos y derivados l. (+K)8. 5.7(-I) (-K) Br 85. I ompuestos aromáticos l I N S 6..9 N
19 RRELAINES EMPÍRIAS ALANS (Tablas: 5-6 ó pág. 7-8) En RMN los distintos de un hidrocarburo saturado aparecen en un rango de desplazamiento químico muy pequeño (0.8-.0ppm) espectros complejos con señales solapadas que no son de er orden ( ν) En RMN es más raro que se produzca solapamiento de señales, suelen aparecer bien definidas las señales correspondientes a cada tipo de carbono Ejemplos: RMN y RMN del metilciclohexano y del octano El desplazamiento químico en RMN de alcanos depende del número de átomos de que hay en las posiciones α, β, γ, δ, ε,... y del grado de ramificación en la posición contigua al considerado. Los δ de estos compuestos se pueden predecir con reglas empíricas. Para un i en un alcano, el desplazamiento químico en unidades de δ se calcula según: δ i = n α + 9.n β -.5n γ + 0.n δ + 0.n ε + Σ S ij n nº de en α, β, γ, δ, ε respecto a i S ij corrección estérica (tiene en cuenta la ramificación) (Tabla 5 ó pág. 79) Ejemplo: δ = x + 9. x.5. =.0ppm (δexp =.) S: ario con α ario δ = x + 9. x.7 = 0.7ppm (δexp = 0.) S: ario con α ario
20 δ = x + 9. x.5 =.ppm (δexp =.0) S: ario con α ario δ = x + 9. x.5 x + 0 =.ppm (δexp =.8) S: ario con α ario Alcanos sustituidos (Tabla 0-5 ó pág ) δ i = -. + ΣZ i + ΣS j + ΣK k i j k Z i S K correcciones para sustituyentes en distintas posiciones α, β, γ, δ corrección estérica corrección de conformación para sustituyentes en γ Ejemplo: N-terc-butoxicarbonilalanina d b c a N δ a = = 5.8ppm (δexp = 9.0) S: ario con α ario y Nα ario δ b = = 6.ppm (δexp = 7.) S: ario con α ario δ c =. + x x.5 = 7.ppm (δexp = 78.) S: ario con α ario δ d = x = 8.7ppm (δexp = 8.) S: ario con α ario
21 RMN TAN RMN 6 RMN -METILBUTAN
22 ALQUENS δ= 80-60ppm (Tablas o pág. 8-87) Alquenos alquilsustituidos (85 ó pág. 8-8) γ γ β β α α = α β γ δsp = nα +.9nβ -.5nγ - 7.9nα -.8nβ +.5nγ + ΣS Ejemplo: cis--metil--penteno a b δ a = x 7.9 x.8 x. =.ppm (δexp =.8) α y α en cis δ b = x +.9 x 7.9 x. +. = 7.0ppm (δexp = 8.8) Alquenos sustituidos (90 ó pág. 8-8) R en β X Y δ i =. + ΣZ i Ejemplo: -Bromo--propeno a b Br δ a =. + ( 8.6) + ( 7.) = 07.ppm (δexp = 08.9 cis, 0.7 trans) δ b =. + ( 0.9) +.9 = 5.ppm (δexp = 9. cis,.7 trans) ALQUINS (Tablas 0 ó pág. 88) X a b Y Ejemplo: But--in--ol δ a = (.6) = 79.ppm δ b = = 8.ppm a b MPUESTS ALIILIS (Tablas 7-75, ó pág )
23 Br Trans--bromo--propeno Br is--bromo--propeno -Butin--ol
24 IDRARBURS ARMÁTIS (Tablas 5-0 ó pág. 96-0) δ i = ΣZ i i 5 6 X Ejemplo:,5-Dimetilnitrobenceno (0-5 ó pág ) δ = ( 0.) = 8.ppm (δexp = 8.5) δ = δ 6 = (.9) (.0) =.ppm (δexp =.7) δ = δ 5 = ( 0.) = 8.5ppm (δexp = 9.6) δ = x 0.7 = 6.0ppm (δexp = 6.) 6 5 N Ejemplo: -Metil--naftol (6-7 ó pág. 00-0) δ = ( 8.6) = 5.ppm δ = = 5.7ppm δ = ( 8.) = 8.ppm δ = (.8) = 8.0ppm δ 5 = ( 0.) + 0. = 8.0ppm δ 6 = (.) + ( 0.7) =.8ppm δ 7 = ( 0.5) = 5.9ppm δ 8 = (.7) + (.) =.ppm δ 9 = (.) =.ppm δ 0 =.6 + (.7) + ( 0.) = 8.7ppm 6 N (6) 5 5-Nitrometaxileno (5)
25 MPUESTS ETERARMÁTIS (Tablas 5-66 ó pág. 0-) Piridinas (0-5* ó pág ) 5 6 N δ = ΣZ i δ =.7 + ΣZ i δ = ΣZ i δ 5 =.7 + ΣZ i5 δ 6 = ΣZ i6 Ejemplo:,5-Dimetilpiridina 5 6 N δ = (.) = 56.ppm (δexp = 55.) 56.* δ =.7 + ( 0.5) + ( 0.9) =.ppm (δexp =.).* δ = = 6.ppm (δexp = 6.7) 6.* δ 5 =.7 + (.0) = 9.6ppm (δexp = 9.6) 9.6* δ = ( 0.7) +. = 50.ppm (δexp = 9.) 50.7* N,5-dimetilpiridina 5
26 Ejemplo: -Amino-5-metilpiridina 5 6 N N δ = (.) = 55.9ppm (δexp = 56.9) 58.8* δ =.7 + ( 5.) + ( 0.9) = 07.7ppm (δexp = 08.) 08.* δ = = 7.7ppm (δexp = 8.6) 8.* δ 5 =.7 + ( 9.7) =.9ppm (δexp =.5).0* δ 6 = (.6) +. = 9.5ppm (δexp = 7.6) 50.* N N -amino-5-metilpiridina 5 DERIVADS ALGENADS (Tablas ó pág. -6) ALLES, ÉTERES Y MPUESTS RELAINADS (Tablas 70-7 ó pág. 7-0) MPUESTS NITRGENADS (Tablas 7-79 ó pág. -7) MPUESTS N AZUFRE (Tablas 79-8 ó pág. 8-) MPUESTS ARBNÍLIS (Tablas 8-0 ó pág. 9 y -) TRS MPUESTS (Tablas 5 ó pág. -7) PRDUTS NATURALES (Tablas 05- ó pág. 8-56) DISLVENTES Y MPUESTS DE REFERENIA (Tablas ó pág )
27
28 APLAMIENTS EN RMN APLAMIENT - (Tablas ó pág. 80-8, 86-87, 89, 95, 0-0,) J (,) Su valor es siempre positivo y tanto mayor cuanto mayor es el carácter s del átomo de involucrado. 6 6 J(,)[z] ibridación sp sp sp sp Los sustituyentes electronegativos aumentan el valor de electropositivos lo disminuyen -X F Li J(,)[z] X F J(,) y los J(,)[z] En bencenos monosustituidos hay J(,) distintas: J(,) = J(6,6) J(,) = J(5,5) X J(,) 6 5 y el efecto del sustituyente R sobre la J(,) disminuye con la distancia
29 J (,) (Jgeminal) Su valor depende, entre otros, de los siguientes factores: La sustitución en los carbonos La incorporación, o no, de los carbonos a cadenas o anillos El tipo de enlace (sencillo, doble o triple) entre los dos carbonos Valores más frecuentes: J : - 0z 0-60z 0-50z J (,) (Jvecinal) Varían en el rango: 0 0z En cada caso su valor depende, entre otros, de los siguientes factores: Ángulo diedro, igual que J(,) Para φ = 0º y 80º se dan los valores mayores de J(,) = 7-9z Para φ = 90º J(,) = 0z Se sigue cumpliendo J(,) 80º > J(,) 0º Longitud de enlace Electronegatividad de los sustituyentes Ejemplo: en derivados etilénicos: Jtrans > Jcis 7.6z.z 5.0z
30 J (,) en derivados bencénicos (No suelen detectarse acoplamientos, a más de enlaces salvo en sistemas con enlaces π conjugados) En el benceno hay cuatro tipos de J(,): J(,), J(,), J(,) y J(,) En un benceno monosustituido hay 6 tipos de J(,) (excluyendo acoplamientos con sustituyentes): J(,) z 5 J(,) -..6z 5 J(,) 5.0.z J(,) z Siempre se cumple: J(,) > J(,) J J J J APLAMIENTS - En compuestos con.% de (abundancia natural) solo se observan: on grandes cantidades de muestra y tiempos de acumulación prolongados En muestras enriquecidas con 80-90% de se pueden medir J(,). Las J(,) son las de mayor magnitud, su valor aumenta con el carácter s de los carbonos: ompuesto Etano Etileno Acetileno J(,)[z]
31 APLAMIENTS N TRS NÚLES Los más importantes son: on 9 F y P por su gran abundancia natural. (Tablas 5 ó pág. - y 5-7) Ejemplos: F J(,F) = 6.z J(,F) = 9.5z J(,F) = 6.7z 6 5 F J(,F) = 5.z J(,F) =.0z J(,F) = 7.8z J(,F) =.z P J(,P) = 0.9z P J(,P) = 5z 6 J(,P) =.5 J(,P) = 0z J(,P) = 0z J(,P) = z J(,P) = z J(,P) = 0.0z 5 Acoplamientos con D en compuestos deuterados Ejemplos: Dl D D S D D J (,D) z
32 EJEMPL DE ASIGNAIN EN UN ESPETR DE RMN p-metoxibenzaldehído 6 5 En el espectro totalmente desacoplado ( BB decoupled spectra ) hay 6 señales: El del a campo bajo ( δ ) El del a campo alto ( δ ) Dos picos pequeños de los cuaternarios aromáticos y Dos picos grandes que corresponden cada uno a dos aromáticos +6 y +5 (6) (5)
33 El espectro ff-resonance confirma lo anterior d (6) (d) (5) (d) (c) s 6 5 s d d (d) c (s) (s) Las tablas permiten calcular los valores teóricos de δ y correlacionar los picos del espectro con los distintos de la molécula δ = (-7.7) = 9.0ppm δ = δ6 = = 0.7ppm δ = δ5 = (-.) =.6ppm δ = = 65.7ppm (67.8) n δ* = 9.0ppm δ = 56.0ppm (5.8) δexp 0ppm δexp ppm δexp 5ppm δexp 65ppm δexp 9ppm δexp 56ppm Tablas utilizadas: 0-5 ó pág para sp (0-5 ó pág. 7-7 para ) 0-5 ó pág para arom. 86 ó pág. 9 para
34 Volver a página docente
TEMA 2: Resonancia Magnética Nuclear RMN-1H y 13C Fundamentos
 Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Resonancia Magnética Nuclear
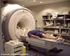 Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
Tema 11. CONCEPTOS FUNDAMENTALES EN QUÍMICA ORGÁNICA
 Tema 11. EPTS FUDAMETALES E QUÍMIA RGÁIA o metales con electronegatividad similar (,,, ). Uniones covalentes debilmente polares o apolares Reactividad: interacciones entre áreas o zonas de las moléculas
Tema 11. EPTS FUDAMETALES E QUÍMIA RGÁIA o metales con electronegatividad similar (,,, ). Uniones covalentes debilmente polares o apolares Reactividad: interacciones entre áreas o zonas de las moléculas
TEMA 10. ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR
 TEMA 10. ESPETROSOPIA DE RESONANIA MAGNÉTIA NULEAR 1. Fundamentos físicos de la espectroscopia de RMN. 2. El espectrómetro de resonancia magnética nuclear. 3. Resonancia magnética nuclear de 1. Apantallamiento
TEMA 10. ESPETROSOPIA DE RESONANIA MAGNÉTIA NULEAR 1. Fundamentos físicos de la espectroscopia de RMN. 2. El espectrómetro de resonancia magnética nuclear. 3. Resonancia magnética nuclear de 1. Apantallamiento
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS
 REATIVIDAD DE LS MPUESTS RGÁNIS 1. Reacciones inorgánicas / Reacciones orgánicas 2. Representación general de una reacción orgánica 3. Algunos aspectos a tener en cuenta en las reacciones orgánicas 4.
REATIVIDAD DE LS MPUESTS RGÁNIS 1. Reacciones inorgánicas / Reacciones orgánicas 2. Representación general de una reacción orgánica 3. Algunos aspectos a tener en cuenta en las reacciones orgánicas 4.
Química Orgánica. por átomos de carbono. A diferencia de otros
 Química Orgánica La definición moderna de la química orgánica es el estudio de los compuestos que se componen por átomos de carbono. A diferencia de otros elementos, el carbono crea enlaces muy fuertes
Química Orgánica La definición moderna de la química orgánica es el estudio de los compuestos que se componen por átomos de carbono. A diferencia de otros elementos, el carbono crea enlaces muy fuertes
Tema 9. Química Orgánica
 Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Lección 1: GENERALIDADES
 Lección 1: GENERALIDADES 1.Concepto de Química Orgánica. Introducción histórica. 2. Estructuras de Lewis. Estructuras resonantes. 3. Geometría de las moléculas. 4. Representaciones de las moléculas orgánicas
Lección 1: GENERALIDADES 1.Concepto de Química Orgánica. Introducción histórica. 2. Estructuras de Lewis. Estructuras resonantes. 3. Geometría de las moléculas. 4. Representaciones de las moléculas orgánicas
FORMULACIÓN QUÍMICA (4 o ESO) II. QUÍMICA ORGÁNICA. Prof. Jorge Rojo Carrascosa
 FRMULAIÓN QUÍMIA (4 o ES) I. QUÍMIA INRGÁNIA II. QUÍMIA RGÁNIA Prof. Jorge Rojo arrascosa Índice general I FRMULAIÓN QUÍMIA RGÁNIA 2 1. IDRARBURS 4 1.1. ALANS................................ 4 1.1.1. ALANS
FRMULAIÓN QUÍMIA (4 o ES) I. QUÍMIA INRGÁNIA II. QUÍMIA RGÁNIA Prof. Jorge Rojo arrascosa Índice general I FRMULAIÓN QUÍMIA RGÁNIA 2 1. IDRARBURS 4 1.1. ALANS................................ 4 1.1.1. ALANS
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
Lección 9: HALUROS DE ALQUILO I
 Lección 9: HALUROS DE ALQUILO I 1.Estructura y propiedades físicas. 2. Polaridad de las moléculas orgánicas: interacciones no enlazantes entre moléculas. 3. Efecto inductivo. 4. Concepto de electrófilo
Lección 9: HALUROS DE ALQUILO I 1.Estructura y propiedades físicas. 2. Polaridad de las moléculas orgánicas: interacciones no enlazantes entre moléculas. 3. Efecto inductivo. 4. Concepto de electrófilo
Reacciones de reducción
 idrogenación catalítica: reactivos y condiciones eacciones de reducción 1. atalizadores: metales nobles (Pt) ó seminobles (Pd), Ni-raney, en matriz o soporte inerte (, sulfatos, carbonatos) que adsorbe
idrogenación catalítica: reactivos y condiciones eacciones de reducción 1. atalizadores: metales nobles (Pt) ó seminobles (Pd), Ni-raney, en matriz o soporte inerte (, sulfatos, carbonatos) que adsorbe
FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS
 FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS Fórmula molecular C n H 2n+2 Sufijo ANO. Para los alcanos de cadena lineal, si tienen 1 C se utiliza el prefijo met-; 2 C et-;
FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS Fórmula molecular C n H 2n+2 Sufijo ANO. Para los alcanos de cadena lineal, si tienen 1 C se utiliza el prefijo met-; 2 C et-;
UNIDAD: Química orgánica UNIDAD DE APRENDIZAJE: Nomenclatura Orgánica. Profesora: Gladys Rivera Jerez
 UNIDAD: Química orgánica UNIDAD DE APRENDIZAJE: Nomenclatura Orgánica Profesora: Gladys Rivera Jerez Las sencillas combinaciones del carbono con algunos pocos átomos han dado origen a más de 10 millones
UNIDAD: Química orgánica UNIDAD DE APRENDIZAJE: Nomenclatura Orgánica Profesora: Gladys Rivera Jerez Las sencillas combinaciones del carbono con algunos pocos átomos han dado origen a más de 10 millones
TEMA 2 CLASIFICACION Y NOMECLATURA DE LOS COMPUESTOS ORGANICOS
 TEMA LASIFIAIN Y NMELATURA DE LS MPUESTS RGANIS. oncepto de radical y grupo funcional. Series homólogas.. Principales tipos de compuestos orgánicos. Formulación y nomenclatura. Fundamentos de Química rgánica
TEMA LASIFIAIN Y NMELATURA DE LS MPUESTS RGANIS. oncepto de radical y grupo funcional. Series homólogas.. Principales tipos de compuestos orgánicos. Formulación y nomenclatura. Fundamentos de Química rgánica
TUTORIAL PARA LA INTERPRETACIÓN DE ESPECTROS DE RESONANCIA MAGNÉTICA NUCLEAR DE PROTÓN.
 9 8 7 6 5 4 3 1 0 TUTRIAL PARA LA INTERPRETACIÓN DE ESPECTRS DE RESNANCIA MAGNÉTICA NUCLEAR DE PRTÓN. Juan A. Palop Tutorial para la interpretación de espectros de Resonancia Magnética Nuclear de protón
9 8 7 6 5 4 3 1 0 TUTRIAL PARA LA INTERPRETACIÓN DE ESPECTRS DE RESNANCIA MAGNÉTICA NUCLEAR DE PRTÓN. Juan A. Palop Tutorial para la interpretación de espectros de Resonancia Magnética Nuclear de protón
TEMA 7. 4º E.S.O. Química. 1. UN ELEMENTO MUY ESPECIAL: EL CARBONO. 2. HIDROCARBUROS.
 1 FRMULAIÓN Y NMENLATURA RGANIA TEMA 7. 4º E.S.. Química. ESQUEMA DE LA UNIDAD 2 1. UN ELEMENT MUY ESPEIAL: EL ARBN. 2. IDRARBURS. 2.1 IDRARBURS SATURADS (ALANS) 2.2 IDRARBURS INSATURADS N DBLES ENLAES
1 FRMULAIÓN Y NMENLATURA RGANIA TEMA 7. 4º E.S.. Química. ESQUEMA DE LA UNIDAD 2 1. UN ELEMENT MUY ESPEIAL: EL ARBN. 2. IDRARBURS. 2.1 IDRARBURS SATURADS (ALANS) 2.2 IDRARBURS INSATURADS N DBLES ENLAES
TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS.
 TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS. 1. Estructuras de resonancia. 1.1. Contribución de las estructuras resonantes. 1.2. Cómo dibujar estructuras resonantes 2. Efecto inductivo. 3. Efecto
TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS. 1. Estructuras de resonancia. 1.1. Contribución de las estructuras resonantes. 1.2. Cómo dibujar estructuras resonantes 2. Efecto inductivo. 3. Efecto
TEMA 2. CLASIFICACION Y NOMECLATURA DE LOS COMPUESTOS ORGANICOS.
 TEMA 2. LASIFIAIN Y NMELATURA DE LS MPUESTS RGANIS. 1. oncepto de radical y grupo funcional. Series homólogas. 2. Principales tipos de compuestos orgánicos. Formulación y nomenclatura. 2 Tema 2 TEMA 2.
TEMA 2. LASIFIAIN Y NMELATURA DE LS MPUESTS RGANIS. 1. oncepto de radical y grupo funcional. Series homólogas. 2. Principales tipos de compuestos orgánicos. Formulación y nomenclatura. 2 Tema 2 TEMA 2.
Guía del docente. 1. Descripción curricular:
 Guía del docente. 1. Descripción curricular: - Nivel: 3º medio. - Subsector: Ciencias Químicas. - Unidad temática: Reactividad en química orgánica, hidrocarburos. - Palabras claves: reacciones orgánicas,
Guía del docente. 1. Descripción curricular: - Nivel: 3º medio. - Subsector: Ciencias Químicas. - Unidad temática: Reactividad en química orgánica, hidrocarburos. - Palabras claves: reacciones orgánicas,
MOMENTO DIPOLAR DE ENLACE. La polaridad de un enlace se mide con el momento dipolar de enlace, µ.
 didactalia.net En la mayoría de los compuestos orgánicos el átomo de carbono se enlaza a átomos más electronegativos, lo que promueve que los electrones del enlace covalente sean atraídos con mayor intensidad
didactalia.net En la mayoría de los compuestos orgánicos el átomo de carbono se enlaza a átomos más electronegativos, lo que promueve que los electrones del enlace covalente sean atraídos con mayor intensidad
QUÍMICA DEL CARBONO SOLUCIONES A LAS ACTIVIDADES DE FINAL DE UNIDAD
 11 QUÍMIA DEL ARBN SLUINES A LAS ATIVIDADES DE FINAL DE UNIDAD aracterísticas del átomo de carbono 1. Explica brevemente qué es: a) una serie homóloga; b) un grupo alquilo; c) un hidrocarburo alicíclico;
11 QUÍMIA DEL ARBN SLUINES A LAS ATIVIDADES DE FINAL DE UNIDAD aracterísticas del átomo de carbono 1. Explica brevemente qué es: a) una serie homóloga; b) un grupo alquilo; c) un hidrocarburo alicíclico;
Lección 2: NOMENCLATURA Y FÓRMULAS ESTRUCTURALES
 Lección 2: NOMENCLATURA Y FÓRMULAS ESTRUCTURALES 1.Composición centesimal. Fórmula empírica y fórmula molecular. Determinación de la fórmula molecular. 2. Concepto de isomería. 3. Grupos funcionales y
Lección 2: NOMENCLATURA Y FÓRMULAS ESTRUCTURALES 1.Composición centesimal. Fórmula empírica y fórmula molecular. Determinación de la fórmula molecular. 2. Concepto de isomería. 3. Grupos funcionales y
Ejercicios variados resueltos
 Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
Susana Latorre Licenciada en Ciencias químicas
 Susana Latorre Licenciada en Ciencias químicas QUIMICA INORGANICA QUIMICA ORGANICA TIPOS DE ENLACES QUE ES UN ELEMENTO QUIMICO QUE ES UNA MOLECULA QUE ES UNA REACCION. COMO SE ESCRIBE ELEMENTO QUIMICO
Susana Latorre Licenciada en Ciencias químicas QUIMICA INORGANICA QUIMICA ORGANICA TIPOS DE ENLACES QUE ES UN ELEMENTO QUIMICO QUE ES UNA MOLECULA QUE ES UNA REACCION. COMO SE ESCRIBE ELEMENTO QUIMICO
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS QUIMICA FARMACÉUTICA ORGANICA III ACIDOS CARBOXILICOS
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS QUIMICA FARMACÉUTICA ORGANICA III ACIDOS CARBOXILICOS 1.- ESTRUCTURA La combinación de un grupo carboxilo y un grupo hidroxilo en el mismo
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS QUIMICA FARMACÉUTICA ORGANICA III ACIDOS CARBOXILICOS 1.- ESTRUCTURA La combinación de un grupo carboxilo y un grupo hidroxilo en el mismo
Química orgánica. Cuarto Medio 25/06
 Química orgánica Cuarto Medio 25/06 CARBONO Es el elemento principal de las moléculas orgánicas. Debido a que este átomo, presenta una gran estabilidad. Dado que, tiene una baja tendencia a donar y quitar
Química orgánica Cuarto Medio 25/06 CARBONO Es el elemento principal de las moléculas orgánicas. Debido a que este átomo, presenta una gran estabilidad. Dado que, tiene una baja tendencia a donar y quitar
Alcanos. Solo contienen carbono e hidrógeno Solo tienen enlaces sencillos. Todos poseen la formula: C n H 2n+2
 Alcanos Solo contienen carbono e hidrógeno Solo tienen enlaces sencillos Todos poseen la formula: C n H 2n+2 ALCANOS Ubique la cadena de átomos de carbono más larga, coloque la terminación ano Localizar
Alcanos Solo contienen carbono e hidrógeno Solo tienen enlaces sencillos Todos poseen la formula: C n H 2n+2 ALCANOS Ubique la cadena de átomos de carbono más larga, coloque la terminación ano Localizar
Singularidad del carbono
 Singularidad del carbono Su configuración electrónica y su tamaño determinan que sea el único elemento químico que puede: Formar enlaces covalentes sencillos, dobles o triples con otros átomos de carbono.
Singularidad del carbono Su configuración electrónica y su tamaño determinan que sea el único elemento químico que puede: Formar enlaces covalentes sencillos, dobles o triples con otros átomos de carbono.
QUÍMICA. 2º Bachilerrato orgánica Estereoisomería:
 TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUIMICA FARMACEUTICA CURSO DE FARMACOGNOSIA Y FITOQUIMICA PROFESOR ALEJANDRO MARTINEZ M.
 1. CONVENCIONES Y TERMINOS UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUIMICA FARMACEUTICA CURSO DE FARMACOGNOSIA Y FITOQUIMICA PROFESOR ALEJANDRO MARTINEZ M. Terminación inglesa ó término Terminación en español
1. CONVENCIONES Y TERMINOS UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUIMICA FARMACEUTICA CURSO DE FARMACOGNOSIA Y FITOQUIMICA PROFESOR ALEJANDRO MARTINEZ M. Terminación inglesa ó término Terminación en español
Las funciones orgánicas se clasifican de la siguiente manera:
 Página 1 APUNTES EJERCICIOS FORMULACIÓN ORGÁNICA Las sustancias orgánicas se clasifican en bloques que se caracterizan por tener un átomo o grupo atómico definido (grupo funcional) que le confiere a la
Página 1 APUNTES EJERCICIOS FORMULACIÓN ORGÁNICA Las sustancias orgánicas se clasifican en bloques que se caracterizan por tener un átomo o grupo atómico definido (grupo funcional) que le confiere a la
QUÍMICA ORGÁNICA BÁSICA
 QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
NOMENCLATURA QUIMICA ORGÁNICA
 NMENCLATURA QUIMICA RGÁNICA El sistema para nombrar actualmente los compuestos orgánicos, conocido como sistema IUPAC, se basa en una serie de reglas muy sencillas que permiten nombrar cualquier compuesto
NMENCLATURA QUIMICA RGÁNICA El sistema para nombrar actualmente los compuestos orgánicos, conocido como sistema IUPAC, se basa en una serie de reglas muy sencillas que permiten nombrar cualquier compuesto
QUÍMICA ORGÁNICA. Física y Química CH 3 CH CH CH 2 CH 3 CH 3 CH 2 CH 2 C CH
 1 QUÍMIA GÁNIA Física y Química 2 La química del carbono o química orgánica, estudia todas aquellas sustancias en cuyas moléculas toma parte el carbono Los átomos de carbono, tienen mucha facilidad para
1 QUÍMIA GÁNIA Física y Química 2 La química del carbono o química orgánica, estudia todas aquellas sustancias en cuyas moléculas toma parte el carbono Los átomos de carbono, tienen mucha facilidad para
La Química Orgánica es el estudio de los compuestos de carbono. El carbono puede formar más compuestos
 QUÍMICA ORGÁNICA La Química Orgánica es el estudio de los compuestos de carbono. El carbono puede formar más compuestos que ningún otro elemento, por tener la capacidad de unirse entre sí formando cadenas
QUÍMICA ORGÁNICA La Química Orgánica es el estudio de los compuestos de carbono. El carbono puede formar más compuestos que ningún otro elemento, por tener la capacidad de unirse entre sí formando cadenas
Efecto inductivo Desplazamiento parcial del par electrónico en enlace sencillo hacia el átomo más electronegativo provocando fracciones de carga.
 www.youtube.com Efecto inductivo Desplazamiento parcial del par electrónico en enlace sencillo hacia el átomo más electronegativo provocando fracciones de carga. Efecto mesómero o resonancia Desplazamiento
www.youtube.com Efecto inductivo Desplazamiento parcial del par electrónico en enlace sencillo hacia el átomo más electronegativo provocando fracciones de carga. Efecto mesómero o resonancia Desplazamiento
BIOQUÍMICA Y BIOLOGÍA MOLECULAR I CURSO 2003/04 ENLACE QUÍMICO
 BIQUÍMIA Y BILGÍA MLEULAR I URS 2003/04 Problemas 1º de Medicina UIVERSIDAD DE AVARRA DEPARTAMET DE BIQUÍMIA ELAE QUÍMI 1. rdenar por su estabilidad relativa (menor energía de ionización) los siguientes
BIQUÍMIA Y BILGÍA MLEULAR I URS 2003/04 Problemas 1º de Medicina UIVERSIDAD DE AVARRA DEPARTAMET DE BIQUÍMIA ELAE QUÍMI 1. rdenar por su estabilidad relativa (menor energía de ionización) los siguientes
SEGUNDO DE BACHILLERATO QUÍMICA. a A + b B c C + d D
 TEMA 5. CINÉTICA QUÍMICA a A + b B c C + d D 1 d[a] 1 d[b] 1 d[c] 1 d[d] mol v = = = + = + a dt b dt c dt d dt L s El signo negativo en la expresión de velocidad es debido a que los reactivos desaparecen,
TEMA 5. CINÉTICA QUÍMICA a A + b B c C + d D 1 d[a] 1 d[b] 1 d[c] 1 d[d] mol v = = = + = + a dt b dt c dt d dt L s El signo negativo en la expresión de velocidad es debido a que los reactivos desaparecen,
Espectro Electromagnético
 1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
QUÍMICA DEL CARBONO Formulación y Nomenclatura Orgánica
 1/6 El gran número de compuestos orgánicos y la complejidad de los mismos, hace imposible que cada uno de ellos tenga un nombre específico, por ello fue necesario sistematizar su nomenclatura y formulación.
1/6 El gran número de compuestos orgánicos y la complejidad de los mismos, hace imposible que cada uno de ellos tenga un nombre específico, por ello fue necesario sistematizar su nomenclatura y formulación.
TEMA 3.2 El Enlace Covalente
 TEMA 3.2 El Enlace Covalente» Estructuras de Lewis: Regla del ctete Formas resonantes Carga formal Excepciones a la regla del octete» Geometría Molecular: Teoría RPENV (Repulsión de los pares de electrones
TEMA 3.2 El Enlace Covalente» Estructuras de Lewis: Regla del ctete Formas resonantes Carga formal Excepciones a la regla del octete» Geometría Molecular: Teoría RPENV (Repulsión de los pares de electrones
Apellidos... Nombre. 1. Indique el número de señales y la multiplicidad que presentarán los compuestos siguientes en 1 H-RMN. Justificar.
 DETERMINACIN ESTRUCTURAL (5 de julio de 2005) Grupo A. TIP A Apellidos.... Nombre 1. Indique el número de señales y la multiplicidad que presentarán los compuestos siguientes en 1 H-RMN. Justificar. CH3
DETERMINACIN ESTRUCTURAL (5 de julio de 2005) Grupo A. TIP A Apellidos.... Nombre 1. Indique el número de señales y la multiplicidad que presentarán los compuestos siguientes en 1 H-RMN. Justificar. CH3
Tema 12. PREPARACIÓN DE ALQUENOS
 Tema 12. PREPARACIÓN DE ALQUENOS 2.- Principales familias de compuestos orgánicos: Tema 11. Alcanos Tema 12. Alquenos (I) Tema 13. Alquenos (II) Tema 14. Alquinos. Tema 15. Hidrocarburos aromáticos (I).
Tema 12. PREPARACIÓN DE ALQUENOS 2.- Principales familias de compuestos orgánicos: Tema 11. Alcanos Tema 12. Alquenos (I) Tema 13. Alquenos (II) Tema 14. Alquinos. Tema 15. Hidrocarburos aromáticos (I).
Introducción a la Resonancia Magnética Nuclear. Química Orgánica III Primer Semestre 2014
 Introducción a la Resonancia Magnética Nuclear Química Orgánica III Primer Semestre 2014 Referencias empleadas en esta presentación: McMurry, John. Química Orgánica. 8ª. Edición. CENGAGE. Wade, L.J. Química
Introducción a la Resonancia Magnética Nuclear Química Orgánica III Primer Semestre 2014 Referencias empleadas en esta presentación: McMurry, John. Química Orgánica. 8ª. Edición. CENGAGE. Wade, L.J. Química
DERIVADOS HALOGENADOS. Estructura
 TEMA 13.- Derivados halogenados. Reacciones S N. Clasificación y características generales. Sustitución nucleofílica. Mecanismos S N 2 y S N 1. Estereoquímica de las reacciones S N. Factores con influencia
TEMA 13.- Derivados halogenados. Reacciones S N. Clasificación y características generales. Sustitución nucleofílica. Mecanismos S N 2 y S N 1. Estereoquímica de las reacciones S N. Factores con influencia
Formulación orgánica
 Formulación orgánica Orgánico significa que procede de órganos, relacionado con la vida. Lo contrario, inorgánico, se asigna a todo lo que carece de vida. A los compuestos orgánicos se les denominó así
Formulación orgánica Orgánico significa que procede de órganos, relacionado con la vida. Lo contrario, inorgánico, se asigna a todo lo que carece de vida. A los compuestos orgánicos se les denominó así
CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS
 CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Departamento de Química Orgánica Sistemas Conjugados Los sistemas insaturados
CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Departamento de Química Orgánica Sistemas Conjugados Los sistemas insaturados
EJERCICIOS DE TERMOQUÍMICA
 EJERCICIOS DE TERMOQUÍMICA En los exámenes de Acceso a la Universidad se proponen una serie de cuestiones (más teóricas) y problemas (prácticos) para resolver. En estos apuntes vamos a resolver ambos tipos
EJERCICIOS DE TERMOQUÍMICA En los exámenes de Acceso a la Universidad se proponen una serie de cuestiones (más teóricas) y problemas (prácticos) para resolver. En estos apuntes vamos a resolver ambos tipos
UNIVERSIDAD DE PUERTO RICO RECINTO DE RÍO PIEDRAS DEPARTAMENTO DE QUÍMICA. QUíMICA 3031
 UNVERSDAD DE PUERT RC RECNT DE RÍ PEDRAS DEPARTAMENT DE QUÍMCA QUíMCA 3031 17 DE DCEMBRE DE 2004 NMBRE EXAMEN FNAL SECCÓN DE CNFERENCA Este examen se compone de 40 preguntas de selección múltiple. Se incluye
UNVERSDAD DE PUERT RC RECNT DE RÍ PEDRAS DEPARTAMENT DE QUÍMCA QUíMCA 3031 17 DE DCEMBRE DE 2004 NMBRE EXAMEN FNAL SECCÓN DE CNFERENCA Este examen se compone de 40 preguntas de selección múltiple. Se incluye
Gradientes de Campo Magnético en experimentos de RMN
 VIII Escuela de Verano RMN Jaca 16-junio junio-2009 Gradientes de Campo Magnético en experimentos de RMN Teodor Parella SeRMN UAB Secuencia de pulsos, Espectro y Estructura Experimento RMN: Secuencia de
VIII Escuela de Verano RMN Jaca 16-junio junio-2009 Gradientes de Campo Magnético en experimentos de RMN Teodor Parella SeRMN UAB Secuencia de pulsos, Espectro y Estructura Experimento RMN: Secuencia de
FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA
 FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA La fórmula empírica indica los elementos que forman la molécula y la proporción relativa de los mismos. CH (escasa información) La fórmula molecular indica el número
FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA La fórmula empírica indica los elementos que forman la molécula y la proporción relativa de los mismos. CH (escasa información) La fórmula molecular indica el número
Salvo los 4 primeros, que reciben el nombre de metano, etano, propano y butano, los demás se nombran mediante un prefijo
 ALCANOS 1A) ACÍCLICOS Salvo los 4 primeros, que reciben el nombre de metano, etano, propano y butano, los demás se nombran mediante un prefijo griego que indica el número de carbonos, y la terminación
ALCANOS 1A) ACÍCLICOS Salvo los 4 primeros, que reciben el nombre de metano, etano, propano y butano, los demás se nombran mediante un prefijo griego que indica el número de carbonos, y la terminación
JUNIO FASE GENERAL QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
TABLAS DE ESPECTROSCOPIA INFRARROJA
 Michelle Alvarez 4to Bioquímica línica TABLAS DE ESPETRSPIA INFRARRJA ALANS Forma sp3-h 2850-3000 intensa estrecha Tijera H2 y -H2 con 1450-1470 media Estrecha H3 Balanceo de H3 Balanceo de cadena de al
Michelle Alvarez 4to Bioquímica línica TABLAS DE ESPETRSPIA INFRARRJA ALANS Forma sp3-h 2850-3000 intensa estrecha Tijera H2 y -H2 con 1450-1470 media Estrecha H3 Balanceo de H3 Balanceo de cadena de al
19 Y 20 ALCOHOLES FENOLES, TIOLES Y ETERES. Licda. Lilian Judith Guzmán Melgar ALCOHOLES
 ALCOHOLES FENOLES, TIOLES Y ETERES Licda. Lilian Judith Guzmán Melgar 2016 19 Y 20 ALCOHOLES CLASIFICACIÓN Los alcoholes se pueden clasificar en tres clases Los alcoholes pueden considerarse los derivados
ALCOHOLES FENOLES, TIOLES Y ETERES Licda. Lilian Judith Guzmán Melgar 2016 19 Y 20 ALCOHOLES CLASIFICACIÓN Los alcoholes se pueden clasificar en tres clases Los alcoholes pueden considerarse los derivados
2.1. HIDROCARBUROS. Compuestos formados por Carbono e Hidrógeno unidos por enlaces simples.
 2.1. HIDROCARBUROS Alcanos Compuestos formados por Carbono e Hidrógeno unidos por enlaces simples. Se nombran con la terminación ano. Eres capaz de nombrarlo? Si es que sí, sáltate la explicación. Si es
2.1. HIDROCARBUROS Alcanos Compuestos formados por Carbono e Hidrógeno unidos por enlaces simples. Se nombran con la terminación ano. Eres capaz de nombrarlo? Si es que sí, sáltate la explicación. Si es
Resonancia Magnética Nuclear
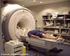 Víctor Moreno de la Cita Jesús J. Fernández Romero 25 de mayo de 2010 1 Base teórica 2 Medicina Química y análisis no destructivo Computación cuántica 3 4 Notación que emplea Kittel: µ = Momento magnético
Víctor Moreno de la Cita Jesús J. Fernández Romero 25 de mayo de 2010 1 Base teórica 2 Medicina Química y análisis no destructivo Computación cuántica 3 4 Notación que emplea Kittel: µ = Momento magnético
Conceptos basicos (III)
 erramientas de la Química rgánica erramientas de la Química rgánica ompuestos carbonílicos onceptos basicos (III) δ δ plano 120 º = polar sp 2 Z Z Z Z = ó Ar Z = ó Ar aldehídos cetonas María Font. Dpto.
erramientas de la Química rgánica erramientas de la Química rgánica ompuestos carbonílicos onceptos basicos (III) δ δ plano 120 º = polar sp 2 Z Z Z Z = ó Ar Z = ó Ar aldehídos cetonas María Font. Dpto.
UNIDAD IV ALCOHOLES. Alcoholes: Introducción y Nomenclatura. Pte. M. en C.Q. Macaria Hernández Chávez
 UNIDAD IV ALCOHOLES Alcoholes: Introducción y Nomenclatura Pte. M. en C.Q. Macaria Hernández Chávez ALCOHOLES Introducción. Los alcoholes son compuestos orgánicos que contienen grupos hidroxilo (-OH).
UNIDAD IV ALCOHOLES Alcoholes: Introducción y Nomenclatura Pte. M. en C.Q. Macaria Hernández Chávez ALCOHOLES Introducción. Los alcoholes son compuestos orgánicos que contienen grupos hidroxilo (-OH).
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
Espectroscopía de Infrarrojo (IR) y espectrometría de masas (MS)
 Espectroscopía de Infrarrojo (IR) y espectrometría de masas (MS) Elucidación Estructural de Compuestos Orgánicos Resonancia Magnética Nuclear (RMN) Espectrometría de Masa (MS) Espectroscopía de Infrarojo
Espectroscopía de Infrarrojo (IR) y espectrometría de masas (MS) Elucidación Estructural de Compuestos Orgánicos Resonancia Magnética Nuclear (RMN) Espectrometría de Masa (MS) Espectroscopía de Infrarojo
INTRODUCCIÓN A LA QUÍMICA
 INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
Tema 2. Alcanos y cicloalcanos, isomería conformacional y geométrica
 Tema 2. Alcanos y cicloalcanos, isomería conformacional y geométrica Existen tres clases principales de Hidrocarburos: Hidrocarburos saturados (alcanos y cicloalcanos) Hidrocarburos insaturados (alquenos
Tema 2. Alcanos y cicloalcanos, isomería conformacional y geométrica Existen tres clases principales de Hidrocarburos: Hidrocarburos saturados (alcanos y cicloalcanos) Hidrocarburos insaturados (alquenos
ALCANOS. Antología de química. Definición de Hidrocarburos. Clasificación de Hidrocarburos. Clasificación de los Hidrocarburos.
 Definición de idrocarburos Los hidrocarburos son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno, enlazados entre sí por uniones covalentes. Su estructura molecular comprende
Definición de idrocarburos Los hidrocarburos son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno, enlazados entre sí por uniones covalentes. Su estructura molecular comprende
QUIMICA ORGANICA 1 ALCANOS Y CICLOALCANOS 20/08/2010 ALCANOS
 0/0/00 QUIMICA ORGANICA Y CICLO Son la primera clase de hidrocarburos simples y contienen sólo enlaces sencillos de carbono carbono, solo poseen carbono e hidrogeno y no tienen grupos funcionales. El enlace
0/0/00 QUIMICA ORGANICA Y CICLO Son la primera clase de hidrocarburos simples y contienen sólo enlaces sencillos de carbono carbono, solo poseen carbono e hidrogeno y no tienen grupos funcionales. El enlace
INTRODUCCIÓN A LA QUÍMICA ORGÁNICA
 CONTENIDOS. INTRODUCCIÓN A LA QUÍMICA ORGÁNICA 1.- Primeros pasos de la Química Orgánica. 2.- Características del carbono y de los compuestos orgánicos. 3.- Tipos de enlaces del carbono. 4.- Representación
CONTENIDOS. INTRODUCCIÓN A LA QUÍMICA ORGÁNICA 1.- Primeros pasos de la Química Orgánica. 2.- Características del carbono y de los compuestos orgánicos. 3.- Tipos de enlaces del carbono. 4.- Representación
TEMA 7 ESTEREOQUIMICA I
 TEMA 7 ESTEREOQUIMIA I. oncepto de estereoquímica.. Isomería conformacional.. onformaciones y estabilidades de los cicloalcanos. Fundamentos de Química Orgánica TEMA 7. ESTEREOQUIMIA I.. oncepto de estereoquímica..
TEMA 7 ESTEREOQUIMIA I. oncepto de estereoquímica.. Isomería conformacional.. onformaciones y estabilidades de los cicloalcanos. Fundamentos de Química Orgánica TEMA 7. ESTEREOQUIMIA I.. oncepto de estereoquímica..
Quimica orgánica básica
 Quimica orgánica básica Química orgánica básica La química orgánica es el estudio de los compuestos de carbono. Los átomos de carbono son únicos en su habilidad de formar cadenas muy estables y anillos,
Quimica orgánica básica Química orgánica básica La química orgánica es el estudio de los compuestos de carbono. Los átomos de carbono son únicos en su habilidad de formar cadenas muy estables y anillos,
Dienos aislados. Dienos conjugados. Dienos acumulados (alenos)
 TEMA 10.- Hidrocarburos poliinsaturados. Clasificación. Dienos conjugados. Reacciones de adición. Cicloadiciones. Reacciones de Diels-Alder. Un dieno es un compuesto orgánico que tiene dos enlaces dobles.
TEMA 10.- Hidrocarburos poliinsaturados. Clasificación. Dienos conjugados. Reacciones de adición. Cicloadiciones. Reacciones de Diels-Alder. Un dieno es un compuesto orgánico que tiene dos enlaces dobles.
QUÍMICA. 1º A bachillerato.
 QUÍMIA. º A bachillerato. Isomería y nomenclatura 9/ebrero/05.. Establece la jerarquía, de mayor a menor, de los grupos funcionales que se formulan a continuación, nombra cada grupo funcional y la familia
QUÍMIA. º A bachillerato. Isomería y nomenclatura 9/ebrero/05.. Establece la jerarquía, de mayor a menor, de los grupos funcionales que se formulan a continuación, nombra cada grupo funcional y la familia
11. FUERZAS INTERMOLECULARES
 Las fuerzas intermoleculares son las responsables de las uniones entre las diferentes moléculas. Química 2º bachillerato Enlace químico 1 Las fuerzas de Van der Waals son interacciones entre átomos y moléculas
Las fuerzas intermoleculares son las responsables de las uniones entre las diferentes moléculas. Química 2º bachillerato Enlace químico 1 Las fuerzas de Van der Waals son interacciones entre átomos y moléculas
1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos.
 Evolución histórica de la Tabla Periódica 1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos. 1869: Mendeleev y Meyer: las propiedades
Evolución histórica de la Tabla Periódica 1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos. 1869: Mendeleev y Meyer: las propiedades
UNIDAD 2. CINÉTICA QUÍMICA
 UNIDAD 2. CINÉTICA QUÍMICA Introducción. Velocidad de reacción Cómo se producen las reacciones químicas Ecuación de la velocidad de reacción Factores que afectan a la velocidad de reacción Mecanismo de
UNIDAD 2. CINÉTICA QUÍMICA Introducción. Velocidad de reacción Cómo se producen las reacciones químicas Ecuación de la velocidad de reacción Factores que afectan a la velocidad de reacción Mecanismo de
MÓDULO A: ácido-base y espectroscópicas de los compuestos orgánicos
 MÓDULO A: Estructura t y propiedades d físicas, ácido-base y espectroscópicas de los compuestos orgánicos MÓDULO A: Estructura t y propiedades d físicas, ácido-base y espectroscópicas de los compuestos
MÓDULO A: Estructura t y propiedades d físicas, ácido-base y espectroscópicas de los compuestos orgánicos MÓDULO A: Estructura t y propiedades d físicas, ácido-base y espectroscópicas de los compuestos
TÉCNICAS INSTRUMENTALES FISICOQUÍMICAS
 DPTO. CIENCIAS Y TÉCNICAS FISICOQUÍMICAS 2ª Prueba de Evaluación a Distancia de TÉCNICAS INSTRUMENTALES FISICOQUÍMICAS Curso 2009-2010 Técnicas Instrumentales Fisicoquímicas. 2ª PED (2009-10) 1 Instrucciones
DPTO. CIENCIAS Y TÉCNICAS FISICOQUÍMICAS 2ª Prueba de Evaluación a Distancia de TÉCNICAS INSTRUMENTALES FISICOQUÍMICAS Curso 2009-2010 Técnicas Instrumentales Fisicoquímicas. 2ª PED (2009-10) 1 Instrucciones
LISTA DE SÍMBOLOS. Capítulo 2 EJEMPLOS Y TEORIA DE LAS VIBRACIONES PARAMÉTRICAS 2.1 Introducción T - Periodo Ω - Frecuencia a- parámetro b- parámetro
 LISTA DE SÍMBOLOS Capítulo 2 EJEMPLOS Y TEORIA DE LAS VIBRACIONES PARAMÉTRICAS 2.1 Introducción T - Periodo Ω - Frecuencia a- parámetro b- parámetro 2.1.1 Rigidez Flexiva que Difiere en dos Ejes x- Desplazamiento
LISTA DE SÍMBOLOS Capítulo 2 EJEMPLOS Y TEORIA DE LAS VIBRACIONES PARAMÉTRICAS 2.1 Introducción T - Periodo Ω - Frecuencia a- parámetro b- parámetro 2.1.1 Rigidez Flexiva que Difiere en dos Ejes x- Desplazamiento
Espectroscopia ultravioleta-visible (temas complementarios)
 1 Espectroscopia ultravioleta-visible (temas complementarios) Ley de Lambert y Beer Cuando se hace incidir radiación electromagnética en un medio, la energía dependerá de la longitud de onda de la radiación
1 Espectroscopia ultravioleta-visible (temas complementarios) Ley de Lambert y Beer Cuando se hace incidir radiación electromagnética en un medio, la energía dependerá de la longitud de onda de la radiación
APUNTES DE FORMULACIÓN Y NOMENCLATURA QUÍMICA ORGÁNICA JOSÉ LUIS A. EIROA MARTÍNEZ FRANCISCO J. PÉREZ GALVÁN
 APUNTES DE FRMULAIÓN Y NMENLATURA DE QUÍMIA RGÁNIA JSÉ LUIS A. EIRA MARTÍNEZ FRANIS J. PÉREZ GALVÁN 1 QUÍMIA RGÁNIA REPRESENTAIÓN DE MPUESTS RGÁNIS Fórmulas Empíricas: Fórmulas Moleculares: indican la
APUNTES DE FRMULAIÓN Y NMENLATURA DE QUÍMIA RGÁNIA JSÉ LUIS A. EIRA MARTÍNEZ FRANIS J. PÉREZ GALVÁN 1 QUÍMIA RGÁNIA REPRESENTAIÓN DE MPUESTS RGÁNIS Fórmulas Empíricas: Fórmulas Moleculares: indican la
EJEMPLOS DE PREGUNTA. Prueba de QUÍMICA. febrero 2010
 EJEMPLS DE PREGUNTA 2010 Prueba de QUÍMICA febrero 2010 PREGUNTAS DE SELECCIÓN MÚLTIPLE CN ÚNICA RESPUESTA. (TIP I) Las preguntas de este tipo constan de un enunciado y de cuatro opciones de respuesta,
EJEMPLS DE PREGUNTA 2010 Prueba de QUÍMICA febrero 2010 PREGUNTAS DE SELECCIÓN MÚLTIPLE CN ÚNICA RESPUESTA. (TIP I) Las preguntas de este tipo constan de un enunciado y de cuatro opciones de respuesta,
QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO
 QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
QUÍMICA de 2º de BACHILLERATO QUÍMICA DEL CARBONO EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica.
 SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
RESUMEN FORMULACIÓN DE QUÍMICA INORGÁNICA
 RESUMEN FORMULACIÓN DE QUÍMICA INORGÁNICA 1- SUSTANCIAS SIMPLES Las sustancias simples están constituidas por una clase única de átomos. En general, los elementos gaseosos suelen encontrarse en forma de
RESUMEN FORMULACIÓN DE QUÍMICA INORGÁNICA 1- SUSTANCIAS SIMPLES Las sustancias simples están constituidas por una clase única de átomos. En general, los elementos gaseosos suelen encontrarse en forma de
Departamento de Física y Química. I. E. S. Atenea (S. S. Reyes, Madrid)
 FRMULAIÓN Y NMENLATURA DE MPUESTS RGÁNIS SEGÚN LA IUPA 1. HIDRARBURS. ompuestos que contienen únicamente como elementos el carbono y el hidrógeno. A. HIDRARBURS LINEALES. Formados por una secuencia de
FRMULAIÓN Y NMENLATURA DE MPUESTS RGÁNIS SEGÚN LA IUPA 1. HIDRARBURS. ompuestos que contienen únicamente como elementos el carbono y el hidrógeno. A. HIDRARBURS LINEALES. Formados por una secuencia de
1 Enlace e isomería 6
 Índice vii ÍNDICE Prólogo xvii Al estudiante 1 1 Enlace e isomería 6 1.1 Cómo se encuentran ordenados los electrones en los átomos 7 1.2 Enlace iónico y covalente 8 1.2.a Compuestos iónicos 9 1.2.b Enlace
Índice vii ÍNDICE Prólogo xvii Al estudiante 1 1 Enlace e isomería 6 1.1 Cómo se encuentran ordenados los electrones en los átomos 7 1.2 Enlace iónico y covalente 8 1.2.a Compuestos iónicos 9 1.2.b Enlace
4. QUÍMICA DEL CARBONO.
 4. QUÍMICA DEL CARBONO. 4.1. FÓRMULA QUÍMICA. El número atómico del carbono es seis, contiene en su núcleo seis protones mientras seis electrones se distribuyen en orbitales a su alrededor. Su configuración
4. QUÍMICA DEL CARBONO. 4.1. FÓRMULA QUÍMICA. El número atómico del carbono es seis, contiene en su núcleo seis protones mientras seis electrones se distribuyen en orbitales a su alrededor. Su configuración
1.4.3 Nomenclatura de los compuestos
 58 Ejemplo 1.13: Calcular todos los estados de oxidación para el nitrato cúprico, Cu(NO 3 ) 2. Solución: El cobre tiene un único estado de oxidación de +2, mientras que el del oxígeno es -2 (que corresponde
58 Ejemplo 1.13: Calcular todos los estados de oxidación para el nitrato cúprico, Cu(NO 3 ) 2. Solución: El cobre tiene un único estado de oxidación de +2, mientras que el del oxígeno es -2 (que corresponde
Ác. Carboxílicos -COOH unido al número necesario de
 FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS ORGÁNICOS. Pág. Nº 1 CONTENIDOS 1.- Compuestos orgánicos. 2.- Compuestos hidrocarburos. 3.- Compuestos halogenados. 4.- Compuestos oxigenados. 5.- Compuestos
FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS ORGÁNICOS. Pág. Nº 1 CONTENIDOS 1.- Compuestos orgánicos. 2.- Compuestos hidrocarburos. 3.- Compuestos halogenados. 4.- Compuestos oxigenados. 5.- Compuestos
Técnico Profesional QUÍMICA
 Programa Técnico Profesional QUÍMICA Geometría molecular Nº Ejercicios PSU 1. La siguiente figura muestra la estructura del gas metano. C Al respecto, qué valor adopta el ángulo de enlace en este compuesto?
Programa Técnico Profesional QUÍMICA Geometría molecular Nº Ejercicios PSU 1. La siguiente figura muestra la estructura del gas metano. C Al respecto, qué valor adopta el ángulo de enlace en este compuesto?
Puntos de ebullición.
 1.-Indica el tipo de enlace de los siguientes hidruros. Ayundándote de la siguiente tabla comenta la polaridad de los enlaces. Hidruro % carácter iónico HF 43 HCl 17 HBr 11 HI 6 Representa gráficamente
1.-Indica el tipo de enlace de los siguientes hidruros. Ayundándote de la siguiente tabla comenta la polaridad de los enlaces. Hidruro % carácter iónico HF 43 HCl 17 HBr 11 HI 6 Representa gráficamente
Las que tienen relación con el de tamaño: LAS PROPIEDADES PERIÓDICAS. Se pueden separar en dos grupos: PERIODICIDAD
 LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
18 Reacciones orgánicas
 Facultad de Farmacia. Universidad de Alcalá 181 18 Reacciones orgánicas 18.1 Reacciones de adición 18.2 Reacciones de eliminación 18.3 Reacciones de sustitución 18.4 Reacciones entre ácidos y bases 18.1
Facultad de Farmacia. Universidad de Alcalá 181 18 Reacciones orgánicas 18.1 Reacciones de adición 18.2 Reacciones de eliminación 18.3 Reacciones de sustitución 18.4 Reacciones entre ácidos y bases 18.1
TEMA 4. ESTRUCTURA DE LAS MOLÉCULAS ORGÁNICAS
 W 0 J. Martínez y. Iriondo TEMA. ESTRUTURA DE LAS MLÉULAS RGÁIAS EJERIIS A. Estructuras. Dibuje las estructuras de Lewis correspondientes a los siguientes compuestos: Acetona 6 Acetonitrilo 7 Br loruro
W 0 J. Martínez y. Iriondo TEMA. ESTRUTURA DE LAS MLÉULAS RGÁIAS EJERIIS A. Estructuras. Dibuje las estructuras de Lewis correspondientes a los siguientes compuestos: Acetona 6 Acetonitrilo 7 Br loruro
NOMENCLATURA ORGÁNICA I: HIDROCARBUROS
 NOMENCLATURA ORGÁNICA I: HIDROCARBUROS ÍNDICE. Clasificación de los Hidrocarburos. Alcanos:. Lineales. Ramificados: radicales alquílicos. Cíclicos. Alquenos. Lineales. Ramificados: radicales alquenilo.
NOMENCLATURA ORGÁNICA I: HIDROCARBUROS ÍNDICE. Clasificación de los Hidrocarburos. Alcanos:. Lineales. Ramificados: radicales alquílicos. Cíclicos. Alquenos. Lineales. Ramificados: radicales alquenilo.
Espectrometría de Masas Interpretación de Espectros. Q. Georgina Duarte Lisci Facultad de Química UNAM
 Espectrometría de Masas Interpretación de Espectros Q. Georgina Duarte Lisci Facultad de Química UNAM Regiones de Información en el Espectro de Masas %Abundancia Información General Series de Iones Información
Espectrometría de Masas Interpretación de Espectros Q. Georgina Duarte Lisci Facultad de Química UNAM Regiones de Información en el Espectro de Masas %Abundancia Información General Series de Iones Información
QUÍMICA COMÚN QC-14 E JERCICIOS Q UÍMICA O RGÁNICA GRAFENO
 QUÍMIA MÚN Q-14 E JERIIS Q UÍMIA RGÁNIA GRAFEN 2014 I. La terbinafina, es una antimicótico de amplio espectro usado para tratar dermatofitosis y algunas infecciones por levaduras, es muy usado para combatir
QUÍMIA MÚN Q-14 E JERIIS Q UÍMIA RGÁNIA GRAFEN 2014 I. La terbinafina, es una antimicótico de amplio espectro usado para tratar dermatofitosis y algunas infecciones por levaduras, es muy usado para combatir
Unidad 1 (Parte XXIII) Adición de Alcoholes a Alquenos. Adición sigue la ley de Markovnikov No presenta estéreoselectividad.
 Unidad 1 (Parte XXIII) Adición de Alcoholes a Alquenos Adición sigue la ley de Markovnikov No presenta estéreoselectividad Primera Etapa: Lic. Walter de la Roca 1 Segunda Etapa: Lic. Walter de la Roca
Unidad 1 (Parte XXIII) Adición de Alcoholes a Alquenos Adición sigue la ley de Markovnikov No presenta estéreoselectividad Primera Etapa: Lic. Walter de la Roca 1 Segunda Etapa: Lic. Walter de la Roca
Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento conteste las siguientes preguntas.
 EXPERIMENTO 3 Reacción de Hidrocarburos Fecha: Sección de laboratorio: Nombre del estudiante: Grupo #: Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento conteste
EXPERIMENTO 3 Reacción de Hidrocarburos Fecha: Sección de laboratorio: Nombre del estudiante: Grupo #: Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento conteste
