Equilibrios de solubilidad
|
|
|
- Rodrigo Zúñiga Robles
- hace 6 años
- Vistas:
Transcripción
1 Equilibrios de solubilidad Apellidos, nombre Departamento Centro Atienza Boronat, Julia Morais Ezquerro, Sergi Departamento de Química ETSIAMN (Universitat Politècnica de València)
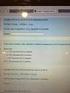
2 1 Resumen de las ideas clave Este objeto de aprendizaje te permitirá estudiar conceptos básicos sobre los equilibrios de solubilidad. El esquema a seguir es el siguiente: 1.- Producto de solubilidad 2.- Relación entre Kps, concentraciones iónicas y solubilidad 3.- Efecto de ion común 4.- Separación de iones por precipitación fraccionada 2 Introducción Diariamente tenemos contacto con compuestos que se disuelven en agua en mayor o menor medida. Por ejemplo, sales de uso común como el bicarbonato son sustancias que hemos disuelto en agua alguna vez. En este proceso se establece un equilibrio de solubilidad. Este tipo de equilibrio se aplica también en procesos de interés industrial y tiene lugar cotidianamente en nuestro entorno. Así por ejemplo, el carbonato sódico se obtiene industrialmente a partir de reacciones de precipitación; las estalactitas y estalagmitas se producen por precipitación del carbonato cálcico y las caries aparecen cuando el esmalte de los dientes, la hidroxiapatita, (Ca5(PO4)3OH) se disuelve en medio ácido. Así pues, los equilibrios de solubilidad que vamos a estudiar tienen lugar en disolución acuosa y se caracterizan por la formación de precipitados. Por ello, vamos a ver el comportamiento de distintos compuestos en disolución para responder a preguntas como: Qué es un precipitado? Cuándo comenzará a precipitar un compuesto? Existe alguna relación entre la constante del producto de solubilidad (Kps) de un soluto y su solubilidad? Qué sal será más soluble? Cuando se mezclan dos disoluciones o cuando se añade un determinado compuesto a una disolución se formará un precipitado?
3 3 Objetivos El objetivo principal de este artículo es introducir los conceptos básicos que te permitirán comprender los equilibrios de solubilidad en disolución acuosa. Este objetivo general se desglosa en los siguientes objetivos particulares: Definir qué es un precipitado Expresar la constante del producto de solubilidad Relacionar el efecto de ion común y la solubilidad de una sal Predecir la separación de iones de una disolución por precipitación fraccionada 4 Desarrollo Teniendo claro que los equilibrios de solubilidad forman parte de nuestra vida y entorno, en este aparatado vas a profundizar en su estudio, para así poder contestar a las preguntas planteadas en la introducción. La estructura de este apartado es: Producto de solubilidad Relación de la Kps con las concentraciones iónicas y la solubilidad Efecto del ion común sobre la solubilidad Separación de iones por precipitación fraccionada 4.1 Producto de solubilidad En este objeto de aprendizaje vamos a tratar con sales y compuestos poco solubles y su disociación transcurre a través de un equilibrio. Por ejemplo, el agua de la Comunidad Valenciana contiene cantidades elevadas de CaCO3, sal poco soluble que al precipitar, origina obstrucciones en los difusores de riego por goteo o en los grifos de agua. El equilibrio entre los iones Ca 2+ (ac) y CO3 2- (ac) y el CaCO3 (s) sin disolver, viene dado por la siguiente reacción de disociación: CaCO3 (s) Ca 2+ (ac) + CO3 2- (ac) Para la reacción de disociación del CaCO3, el producto de las concentraciones iónicas que intervienen en el equilibrio de solubilidad se conoce como producto iónico (PI), y se expresa como PI = [Ca 2+ ][CO3 2- ]. En el caso de que las concentraciones iónicas sean las de equilibrio, se habla de producto de solubilidad o constante del equilibrio, y se expresa como Kps = [Ca 2+ ]eq[co3 2- ]eq. Ves que la Kps de un compuesto es el producto de las concentraciones molares de los iones constituyentes, cada una elevada a su coeficiente estequiométrico en la ecuación de equilibrio. El cálculo de Kps de la reacción de disociación de la sal CaCO3 es sencillo, ya que la estequiometría es 1:1. Para otras sales como Ag2CO3 y Ba3(PO4)2, la expresión de Kps será: Ag2CO3, 2Ag + (ac) + CO3 2- (ac) Kps = [Ag + ] 2 [CO3 2- ] Ba3(PO4)2 3Ba 2+ (ac) + 2PO4 3- (ac) Kps = [Ba 2+ ] 3 [PO4 3- ] 2
4 Como habrás observado, las concentraciones molares de las especies iónicas se elevan a la potencia de su coeficiente estequiométrico. A partir de ahora podemos empezar a contestar las preguntas planteadas en la introducción Qué es un precipitado? Un sólido que se separa de la disolución. Cuándo comenzará a precipitar un compuesto? 1) Si PI < Kps la disolución no está saturada y no habrá precipitación 2) Cuando Kps = PI se trata de una disolución saturada 3) Si PI > Kps la disolución está sobresaturada y comenzará la precipitación 4.2 Relación entre la Kps, concentraciones iónicas y solubilidad La solubilidad (s) de un soluto es la concentración que se disolverá de este, expresada en mol L -1 o g L -1. Otra cuestión que se ha planteado en la introducción era saber si existía alguna relación entre Kps de un soluto y su solubilidad. Veamos por ejemplo que ocurre para una sal como el AgCl que se disocia según la reacción AgCl (s) Ag + (ac) + Cl - (ac). Se observa que por estequiometria se cumple que la solubilidad, s = [Ag + ] = [Cl - ] y por tanto, Kps = [Ag + ][Cl - ]= s 2. Así pues, fácilmente se puede calcular la Kps de esta sal a partir de la solubilidad y viceversa, ya que existe una relación directa entre ambas y la concentración iónica). Esta relación es distinta según la estequiometría de la sal (ver Tabla 1). Tabla 1 Relación entre Kps, concentración iónica y solubilidad para distintos tipos de sales Sal Reacción Relación entre Kps, concentración iónica y solubilidad AB AB2 A2B AB3 A2B3 AB(s) AB (ac) A + + B - [A + ] = [B] = s AB2(s) AB2 (ac) A + + 2B - [A + ] = s; [B - ] = 2s A2B (s) A2B (ac) 2A + + B - [A + ] = 2s; [B - ] = s AB3(s) AB3 (ac) A + + 3B - [A + ] = s; [B - ] = 3s A2B3 (s) A2B3 (ac) 2A + + 3B - [A + ] = 2s; [B - ] = 3s Kps = [A + ][B - ] = s 2 Kps = [A + ][B - ] 2 = s (2s) 2 = 4s 3 Kps = [A + ] 2 [B - ] = (2s) 2 s = 4s 3 Kps = [A + ][B - ] 3 = s (3s) 3 = 27s 4 Kps = [A + ] 2 [ B - ] 3 = (2s) 2 (3s) 3 = 108 s 5 Actividad 1: Siguiendo estas pautas, rellena la siguiente tabla
5 Sal Reacción Relación entre Kps, concentración iónica y solubilidad Ag2CO3 CaF2 Al(OH)3 Ca3(PO4)2 Observar que se puede calcular la solubilidad de una sal a partir de su Kps y viceversa, es decir determinar la Kps a partir de la solubilidad. Actividad 2: 1) La solubilidad del CuS es 7, mol L -1. Calcular el valor de su Kps 2) La Kps del Mg(OH)2 es 1, , calcula su solubilidad Otra cuestión planteada es Qué sal será más soluble? Cuando las sales tienen la misma estequiometria, sus solubilidades se relacionan de la misma forma con su Kps, y por lo tanto será más soluble la sal que tenga mayor Kps. Así, el CaCO3 (Kps = 8, ) es más soluble que el PbCO3 (Kps = 3, ), porque tiene mayor Kps. Para este tipo de compuesto con estequiometria AB se cumple que Kps = s 2. Si los solutos no tienen la misma estequiometria, habrá que calcular la solubilidad y comparar los valores (ver tabla 2). Por ejemplo, el PbCrO4, (Kps = ), tiene mayor Kps que el Cu(OH)2 (Kps = 2, ) pero su solubilidad es menor, siendo 1, y 1, mol L -1, para PbCrO4 y Cu(OH)2, respectivamente. Tabla 2 Cálculo de la solubilidad de las sales PbCrO4 y Cu(OH)2 Sal Reacción Relación entre Kps y concentración iónica Relación entre Kps y solubilidad PbCrO4 PbCrO4 Pb CrO4 2- Kps = = [Pb + 2 ][CrO4 2- ] [Pb + 2 ] =[CrO4 2- ] = s Kps = s 2 s = KKKKKK Cu(OH)2 Cu(OH)2 Cu OH - Kps = 2, = [Cu + 2 ][OH - ] 2 [Cu + 2 ] = s; [OH - ] = 2s Kps = 4s 3 s = 3 KKKKKK/4 Actividad 3: De los compuestos que a continuación se muestran Cuáles son poco solubles? Escribe sus reacciones de disociación, indicando si existe o no un
6 equilibrio NaCl, CaF2, AgNO3, BaSO4. Datos: Kps (CaF2 ) = 5, ; Kps (BaSO4 ) = 1, Efecto de ion común Una disolución saturada de TlCl en agua se representa con la siguiente reacción de equilibrio; TlCl (s) Tl + (ac) + Cl - (ac), donde [Tl + ] = [Cl - ] = s, y por tanto, Kps = [Tl + ][Cl - ]= s.s = s 2. Si a este equilibrio se le añade KCl, es decir un ion común (Cl - ), de acuerdo con el principio de Le Châtelier, el equilibrio se desplaza en el sentido de formación de TlCl ( ). Por tanto, la adición de un ion común afecta a la solubilidad de la sal, disminuyéndola al desplazar el equilibrio hacia el compuesto sin disolver. Lo podemos comprobar fácilmente: El KCl es una sal muy soluble que se disocia según la siguiente reacción: KCl K + + Cl -. Si la concentración de la sal es por ejemplo C, por estequiometría, la concentración de cloruro (Cl - ) será también C. Si esta sal se adiciona a una disolución acuosa de TlCl, el equilibrio de solubilidad se verá afectado ya que la concentración de cloruro aumenta. TlCl (s) Tl + ( ac) + Cl - (ac) s s + C En esta situación, [Tl + ] = s y [Cl - ] = s + C; es decir Kps =[Tl + ][Cl - ]= s (s + C). Como la solubilidad (s ) es mucho menor que C, esta primera es despreciable frente a C, y por tanto Kps será igual al producto de s por C (Kps = s C). Conocido el valor de Kps se puede obtener la solubilidad s por sustitución en la ecuación anterior (s = Kps/C). Actividad 4 : Calcular la solubilidad del AgCl a) en agua y b) en una disolución de KCl 0,01M. Dato: Kps (AgCl) = 1, Separación de iones por precipitación fraccionada La precipitación fraccionada es un proceso que permite separar uno o más iones de una disolución y dejar disueltos los demás, con la condición de que se formen precipitados que tengan distinta solubilidad. Vamos a considerar una disolución que contiene iones cloruro e ioduro. Estos iones se pueden separar como halogenuros de plata insolubles (AgCl y AgI), añadiendo lentamente a esta disolución un compuesto de plata soluble, como el nitrato de plata. Este concepto lo vamos a ilustrar con el siguiente ejemplo: Ejemplo: A una disolución que contiene iones cloruro (Cl - ) e ioduro (l - ) en concentración 0,1M, cada uno de ellos, se le añade nitrato de plata. Se podrán separar ambos iones por precipitación fraccionada? Datos: Kps (AgCl) = 1, Kps (AgI) = 1,
7 Para resolver este ejercicio tenemos que tener en cuenta que el ion común es Ag + y reacciona con los iones Cl - e l - para formar precipitados de AgCl y AgI, respectivamente y plantearnos las siguientes preguntas: Qué sal precipitará antes, el AgCl o el AgI? Identificado el ion común, que en este caso es el ion Ag +, se calcula la [Ag + ] necesaria para que se inicie la precipitación a partir de la Kps de cada sal, teniendo en cuenta el equilibrio de solubilidad. AgCl (s) Ag + ( ac) + Cl - (ac) AgI(s) Ag + ( ac) + I - (ac) [Ag + ]Cl- = 1, /0,1 =1, M [Ag + ] l- = 1, /0,1 =1, M Se observa que la concentración de Ag + necesaria para que precipite en forma de AgI es menor que la requerida para precipitar en forma de AgCl. Por tanto, la sal AgI será la primera en precipitar, es decir, la sal que menos concentración del ion común necesita para alcanzar la Kps. Cuándo acaban de precipitar las sales AgCl y AgI? Por convenio, una sal termina de precipitar cuando en disolución queda la milésima parte de su concentración inicial, c = 10-3.c0. Así pues, en este caso [Cl - ] = [I - ] = 0, = 10-4 M. A continuación, se determina la [Ag + ] para estas concentraciones de cloruro e ioduro con el fin de calcular las concentraciones de Ag + a la que acaban de precipitar las sales: [Ag + ]Cl- = 1, /10-4 =1, M [Ag + ]l- = 1, /10-4 =1, M Se podrán separar los precipitados de AgCl y AgI? Una manera de responder a esta pregunta es trazando una línea horizontal la cual representa la concentración del ion común [Ag + ]. A continuación se anotan las concentraciones a la que empiezan (C0) y acaban (Cf) de precipitar las sales, para así determinar el intervalo de concentración de precipitación. AgI AgCl [Ag + ] (M) C0 = 1, Cf = 1, C0 = 1, Cf = 1, Finalmente, se observa si los intervalos de concentración de precipitación de las sales se solapan o no. En este caso, como los intervalos de concentración de precipitación de AgCl (en verde) y AgI (en rojo) no se solapan se puede afirmar que estas sales si se pueden separar por precipitación fraccionada. Actividad 5: A una disolución acuosa que contiene iones Ca 2+ y Ba 2+ a una concentración 0,01M se añade lentamente sulfato de sodio. Determinar qué
8 compuesto precipitará primero y si los precipitados se podrán separar por precipitación fraccionada. Datos: Kps BaSO4 = Kps CaSO4 = Cierre En este objeto de aprendizaje hemos visto qué es el producto y la constante de solubilidad, su relación con las concentraciones iónicas y la solubilidad, cómo el efecto de ion común disminuye la solubilidad de los compuestos, y si es posible separar sales con un ion común por precipitación fraccionada. 6 Bibliografía 6.1 Libros: [1] Chang, R.: Química 10ª edición, Ed. McGraw-Hill, México, 2010, pág ; [2] Petrucci, R.H.; Herring, F.G.; Madura, J.D.; Bisonnette, C.: Química General 10ª edición, Ed. Pearson Educación, Madrid, 2011, pág
Un equilibrio heterogéneo muy especial: Equilibrio de Precipitación
 Un equilibrio heterogéneo muy especial: Equilibrio de Precipitación Los equilibrios heterogéneos son aquellos en los cuales los reactivos y productos se presentan en distintos estados de agregación (sólido,
Un equilibrio heterogéneo muy especial: Equilibrio de Precipitación Los equilibrios heterogéneos son aquellos en los cuales los reactivos y productos se presentan en distintos estados de agregación (sólido,
Reacciones de precipitación
 Reacciones de precipitación Criterios de evaluación Aplicar el concepto de equilibrio químico para predecir la evolución de un sistema y resolver problemas de equilibrios homogéneos, en particular en reacciones
Reacciones de precipitación Criterios de evaluación Aplicar el concepto de equilibrio químico para predecir la evolución de un sistema y resolver problemas de equilibrios homogéneos, en particular en reacciones
EQUILIBRIOS DE SOLUBILIDAD
 EQUILIBRIOS DE SOLUBILIDAD EJERCICIOS Y PROBLEMAS RESUELTOS 1.- Una disolución saturada de tetraoxofosfato (V) de plata, contiene 3,4 1 5 moles por litro de ion fosfato. Calcula el producto de solubilidad
EQUILIBRIOS DE SOLUBILIDAD EJERCICIOS Y PROBLEMAS RESUELTOS 1.- Una disolución saturada de tetraoxofosfato (V) de plata, contiene 3,4 1 5 moles por litro de ion fosfato. Calcula el producto de solubilidad
El hidróxido de magnesio es una sustancia ligeramente soluble en agua. El ph de una disolución saturada de dicho hidróxido es de 10,38.
 Calcula la solubilidad en g/l del fosfato de plomo (II) sabiendo que su producto de solubilidad es 1,5.10-32. Datos: Pb = 207,2; P = 31; O = 16. Sol: 1,37.10-11 g/l. Sabiendo que la solubilidad en g/l
Calcula la solubilidad en g/l del fosfato de plomo (II) sabiendo que su producto de solubilidad es 1,5.10-32. Datos: Pb = 207,2; P = 31; O = 16. Sol: 1,37.10-11 g/l. Sabiendo que la solubilidad en g/l
Tabla 4.1. Reglas de solubilidad para compuestos iónicos a 25ºC
 La disolución y la precipitación de compuestos son fenómenos que se presentan corrientemente en la naturaleza. Por ejemplo la preparación de muchos productos químicos industriales, como el Na 2 CO 3, está
La disolución y la precipitación de compuestos son fenómenos que se presentan corrientemente en la naturaleza. Por ejemplo la preparación de muchos productos químicos industriales, como el Na 2 CO 3, está
Equilibrio Químico. Aspectos Teóricos
 Equilibrio Químico Aspectos Teóricos 4.1 Introducción En los problemas de cálculos estequiométricos tratados en el tema 1, hemos supuesto que las reacciones químicas se detienen cuando uno o más reactivos
Equilibrio Químico Aspectos Teóricos 4.1 Introducción En los problemas de cálculos estequiométricos tratados en el tema 1, hemos supuesto que las reacciones químicas se detienen cuando uno o más reactivos
REACCIONES DE PRECIPITACIÓN
 TEMA 12 REACCIONES DE PRECIPITACIÓN Las reacciones de disolución/precipitación en las que un sólido pasa a la disolución o viceversa afectan profundamente la ecología de ríos, lagos y océanos ya que controlan
TEMA 12 REACCIONES DE PRECIPITACIÓN Las reacciones de disolución/precipitación en las que un sólido pasa a la disolución o viceversa afectan profundamente la ecología de ríos, lagos y océanos ya que controlan
Pilas electrolíticas
 Pilas electrolíticas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B. (smorais@qim.upv.es)
Pilas electrolíticas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B. (smorais@qim.upv.es)
EQUILIBRIO IÓNICO EN SOLUCIONES ACUOSAS
 EQUILIBRIO IÓNICO EN SOLUCIONES ACUOSAS Equilibrio entre una sal sólida poco soluble y sus iones en solución Producto de solubilidad (Kps) Muchos compuestos (sales, hidróxidos) son levemente solubles en
EQUILIBRIO IÓNICO EN SOLUCIONES ACUOSAS Equilibrio entre una sal sólida poco soluble y sus iones en solución Producto de solubilidad (Kps) Muchos compuestos (sales, hidróxidos) son levemente solubles en
ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES
 VII 1 PRÁCTICA 7 ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES FORMACIÓN DE PRECIPITADOS Y DISOLUCIÓN DE LOS MISMOS POR FORMACIÓN DE COMPLEJOS FUNDAMENTO DE LA PRÁCTICA En esta práctica llevaremos a cabo
VII 1 PRÁCTICA 7 ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES FORMACIÓN DE PRECIPITADOS Y DISOLUCIÓN DE LOS MISMOS POR FORMACIÓN DE COMPLEJOS FUNDAMENTO DE LA PRÁCTICA En esta práctica llevaremos a cabo
Tema 7: Solubilidad. (Fundamentos de Química, Grado en Física) Equilibrio químico Enero Mayo, 2011 1 / 24
 Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
] = s = 1'5 10-5 M. a) El equilibrio de ionización del compuesto es: Al(OH) 3 Al 3+ + 3 OH -
![] = s = 1'5 10-5 M. a) El equilibrio de ionización del compuesto es: Al(OH) 3 Al 3+ + 3 OH - ] = s = 1'5 10-5 M. a) El equilibrio de ionización del compuesto es: Al(OH) 3 Al 3+ + 3 OH -](/thumbs/40/21798534.jpg) 1. Se disuelve hidróxido de cobalto(ii) en agua hasta obtener una disolución saturada a una temperatura dada. Se conoce que la concentración de iones OH - es 3 10-5 M. Calcule: a) La concentración de iones
1. Se disuelve hidróxido de cobalto(ii) en agua hasta obtener una disolución saturada a una temperatura dada. Se conoce que la concentración de iones OH - es 3 10-5 M. Calcule: a) La concentración de iones
Química. Equilibrio ácido-base Nombre:
 Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
,1752'8&&,21. Ag +, Fe 2+, Cu 2+, Al 3+ HCl. AgCl Fe 2+, Cu 2+, Al 3+ NH 3. Al(OH) 3 Fe 2+, Cu 2+ NaOH. Cu 2+ (Cu(NH 3.
 (48,/,%5,26'(35(&,3,7$&,21,1752'8&&,21 62/8%,/,'$'
(48,/,%5,26'(35(&,3,7$&,21,1752'8&&,21 62/8%,/,'$'
Aspectos fundamentales sobre ácidos y bases
 Aspectos fundamentales sobre ácidos y bases Apellidos, nombre Departamento Centro Atienza Boronat, Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B.
Aspectos fundamentales sobre ácidos y bases Apellidos, nombre Departamento Centro Atienza Boronat, Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B.
Reacciones en disolución acuosa
 Reacciones en disolución acuosa (no redox) Ramón L. Hernández-Castillo, Ph.D. Química 106 (laboratorio) Objetivos Reglas de Solubilidad en medio acuoso Reacciones típicas en medio acuoso (precipitación,
Reacciones en disolución acuosa (no redox) Ramón L. Hernández-Castillo, Ph.D. Química 106 (laboratorio) Objetivos Reglas de Solubilidad en medio acuoso Reacciones típicas en medio acuoso (precipitación,
Física y Química 1ºBachillerato Ejemplo Examen. Formulación. (1 puntos) Formula correctamente los siguientes compuestos: Ioduro de Calcio:
 Física y Química 1ºBachillerato Ejemplo Examen Formulación. (1 puntos) Formula correctamente los siguientes compuestos: Óxido Fosfórico: Silano: Carburo Potásico: Ácido perclórico: Fosfato de Sodio: Hidruro
Física y Química 1ºBachillerato Ejemplo Examen Formulación. (1 puntos) Formula correctamente los siguientes compuestos: Óxido Fosfórico: Silano: Carburo Potásico: Ácido perclórico: Fosfato de Sodio: Hidruro
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO
 Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. En un recipiente de 10,0 L se introducen 0,61 moles de CO 2 y 0,39 moles de H 2 calentando hasta 1250 ºC. Una vez alcanzado
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. En un recipiente de 10,0 L se introducen 0,61 moles de CO 2 y 0,39 moles de H 2 calentando hasta 1250 ºC. Una vez alcanzado
GUIA DE ESTUDIO Nº 7: Equilibrio Químico
 Página26 GUIA DE ESTUDIO Nº 7: Equilibrio Químico I.- Conceptos básicos: Equilibrio químico y constante de equilibrio. Concentraciones en el equilibrio y evolución de un sistema hacia el equilibrio. Principio
Página26 GUIA DE ESTUDIO Nº 7: Equilibrio Químico I.- Conceptos básicos: Equilibrio químico y constante de equilibrio. Concentraciones en el equilibrio y evolución de un sistema hacia el equilibrio. Principio
Cálculo del ph en disoluciones acuosas
 Cálculo del ph en disoluciones acuosas Apellidos, nombre Departamento Centro Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B. (smorais@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es)
Cálculo del ph en disoluciones acuosas Apellidos, nombre Departamento Centro Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B. (smorais@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es)
SOLUBILIDAD 1. Solubilidad. 2. Producto de solubilidad. 3. Efecto del ion común.
 SOLUBILIDAD 1. Solubilidad. 2. Producto de solubilidad. 3. Efecto del ion común. Química 2º bachillerato Solubilidad 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que son necesarios dominar y ampliar
SOLUBILIDAD 1. Solubilidad. 2. Producto de solubilidad. 3. Efecto del ion común. Química 2º bachillerato Solubilidad 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que son necesarios dominar y ampliar
- Leyes ponderales: Las leyes ponderales relacionan las masas de las sustancias que intervienen en una reacción química.
 FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
TEMA 5.- Cinética química. Equilibrio químico
 TEMA 5.- Cinética química. Equilibrio químico CUESTIONES 41.- La siguiente tabla presenta la variación de la constante de equilibrio con la temperatura para la síntesis del amoniaco según la reacción:
TEMA 5.- Cinética química. Equilibrio químico CUESTIONES 41.- La siguiente tabla presenta la variación de la constante de equilibrio con la temperatura para la síntesis del amoniaco según la reacción:
DISOLUCIÓN Y PRECIPITACIÓN DE SALES CAPITULO V. 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada
 CAPITULO V DISOLUCIÓN Y PRECIPITACIÓN DE SALES 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada El fenómeno de precipitación, así como el de disolución de precipitados
CAPITULO V DISOLUCIÓN Y PRECIPITACIÓN DE SALES 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada El fenómeno de precipitación, así como el de disolución de precipitados
Acuerdo 286. Química. Disoluciones. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
2(OH) (aq) + Co 2+ (aq) Co(OH) 2 (s) 3) Ec. Molecular. Cu(SO 4 )(aq) + 2Na(OH) (aq) Cu(OH) 2 (s) + Na 2 (SO 4 ) (aq) Ec. Ionica.
 QUIMICA (63.01) TRABAJO PRACTICO N :2 RELACCIONES DE DOBLE DESCOMPOSICION CON FORMACIÓN DE UNA FASE SOLIDA. INTEGRANTES: REACTIVOS UTILIZADOS FORMULA NOMECLATURA COLOR KCl Cloruro de Potasio Transparente
QUIMICA (63.01) TRABAJO PRACTICO N :2 RELACCIONES DE DOBLE DESCOMPOSICION CON FORMACIÓN DE UNA FASE SOLIDA. INTEGRANTES: REACTIVOS UTILIZADOS FORMULA NOMECLATURA COLOR KCl Cloruro de Potasio Transparente
TEMA I: REACCIONES Y ESTEQUIOMETRIA
 TEMA I: REACCIONES Y ESTEQUIOMETRIA 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano que quedan. c) Los gramos
TEMA I: REACCIONES Y ESTEQUIOMETRIA 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano que quedan. c) Los gramos
Disoluciones. Química General II 2011
 Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
Capítulo 16 Equilbrio Iónico Acuoso
 apítulo 16 Equilbrio Iónico Acuoso Adaptado por: Ileana Nieves Martínez opyright 011 Pearson Education, Inc. Amortiguadores Amortiguador o Buffers Soluciones que resisten ph cuando se añade ácido base
apítulo 16 Equilbrio Iónico Acuoso Adaptado por: Ileana Nieves Martínez opyright 011 Pearson Education, Inc. Amortiguadores Amortiguador o Buffers Soluciones que resisten ph cuando se añade ácido base
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
QUIMICA ANALITICA I VOLUMETRIAS DE PRECIPITACION Y COMPLEJOS
 QUIMICA ANALITICA I VOLUMETRIAS DE PRECIPITACION Y COMPLEJOS 2016 VOLUMETRÍA DE PRECIPITACIÓN Y COMPLEJOS - QA I 2016 Nota: A continuación de la resolución de estos problemas se enumeran los métodos más
QUIMICA ANALITICA I VOLUMETRIAS DE PRECIPITACION Y COMPLEJOS 2016 VOLUMETRÍA DE PRECIPITACIÓN Y COMPLEJOS - QA I 2016 Nota: A continuación de la resolución de estos problemas se enumeran los métodos más
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA. 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué?
 REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
10.- REACCIONES DE PRECIPITACIÓN.
 Reacciones de precipitación 10.- REACCIONES DE PRECIPITACIÓN. 10.1.- Concepto de solubilidad.... 258 10.2.- Solubilidad de los compuestos iónicos.... 259 10.2.1.- Solvatación... 259 10.2.2.- Factores energéticos....
Reacciones de precipitación 10.- REACCIONES DE PRECIPITACIÓN. 10.1.- Concepto de solubilidad.... 258 10.2.- Solubilidad de los compuestos iónicos.... 259 10.2.1.- Solvatación... 259 10.2.2.- Factores energéticos....
ESTEQUIOMETRÍA. cobre(ii) y se descompone, cuántas moles de dióxido de nitrógeno se formarán? A moles B moles C moles D. 0.
 ESTEQUIOMETRÍA 1 Al calentarse fuertemente, el nitrato de cobre(ii) se descompone en óxido de cobre(ii), dióxido de nitrógeno y oxígeno elemental (O 2 ). Si calentamos 0.10 moles de nitrato de cobre(ii)
ESTEQUIOMETRÍA 1 Al calentarse fuertemente, el nitrato de cobre(ii) se descompone en óxido de cobre(ii), dióxido de nitrógeno y oxígeno elemental (O 2 ). Si calentamos 0.10 moles de nitrato de cobre(ii)
Materiales recopilados por la Ponencia Provincial de Química para Selectividad TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
DISOLUCION DE PIEZAS DENTALES
 DISOLUCION DE PIEZAS DENTALES Agua ph=7 T 20 C 1. Cuanto dura la pieza dental en contacto con agua? 2. Cuales serian los factores que determinan que se solubilice? 3. En que condiciones se disuelve en
DISOLUCION DE PIEZAS DENTALES Agua ph=7 T 20 C 1. Cuanto dura la pieza dental en contacto con agua? 2. Cuales serian los factores que determinan que se solubilice? 3. En que condiciones se disuelve en
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio
CÁLCULOS SOBRE PREPARACIÓN DE SOLUCIONES Y EXPRESIÓN DE RESULTADOS
 CÁLCULOS SOBRE PREPARACIÓN DE SOLUCIONES Y EXPRESIÓN DE RESULTADOS 1- Calcule el número de moles presentes en cada uno de los siguientes ejemplos: a) 148,2 g de Ca(HO) 2 b) 50 g de CuSO 4.5 H 2 O c) 57
CÁLCULOS SOBRE PREPARACIÓN DE SOLUCIONES Y EXPRESIÓN DE RESULTADOS 1- Calcule el número de moles presentes en cada uno de los siguientes ejemplos: a) 148,2 g de Ca(HO) 2 b) 50 g de CuSO 4.5 H 2 O c) 57
Equilibrio Químico. CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A.
 Equilibrio Químico CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Introducción Las reacciones químicas que se ha considerado hasta este punto se denominan irreversibles debido a que ellas proceden
Equilibrio Químico CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Introducción Las reacciones químicas que se ha considerado hasta este punto se denominan irreversibles debido a que ellas proceden
CAPÍTULO 6: EQUILIBRIO DE SOLUBILIDAD
 CAPÍTULO 6: EQUILIBRIO DE SOLUBILIDAD 113 CAPÍTULO 6: EQUILIBRIO DE SOLUBILIDAD El equilibrio de solubilidad es otro de los capítulos importantes que rigen el desempeño de la química analítica. Considerando
CAPÍTULO 6: EQUILIBRIO DE SOLUBILIDAD 113 CAPÍTULO 6: EQUILIBRIO DE SOLUBILIDAD El equilibrio de solubilidad es otro de los capítulos importantes que rigen el desempeño de la química analítica. Considerando
Química 2º Bach. Equilibrio químico y solubilidad 09/03/05
 Química º Bach. Equilibrio químico y solubilidad 09/03/05 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [3 PUNTOS /UNO] 1. Calcula: a) La solubilidad del hidróxido de magnesio en g/l. b) El ph de
Química º Bach. Equilibrio químico y solubilidad 09/03/05 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [3 PUNTOS /UNO] 1. Calcula: a) La solubilidad del hidróxido de magnesio en g/l. b) El ph de
Química Propedéutico para Bachillerato OBJETIVO
 Actividad 14. CÁLCULO DEL PESO MOLECULAR OBJETIVO Calcular los pesos moleculares de los compuestos químicos D.R. Universidad TecMilenio 1 INTRODUCCIÓN Las reacciones químicas son representadas mediante
Actividad 14. CÁLCULO DEL PESO MOLECULAR OBJETIVO Calcular los pesos moleculares de los compuestos químicos D.R. Universidad TecMilenio 1 INTRODUCCIÓN Las reacciones químicas son representadas mediante
REACCIONES QUÍMICAS. Cómo se simbolizan las reacciones químicas
 Capítulo 3 REACCIONES QUÍMICAS Una ecuación química es una manera abreviada de expresar una reacción química (cambio químico) con fórmulas y símbolos. Para poder escribir una ecuación para una reacción
Capítulo 3 REACCIONES QUÍMICAS Una ecuación química es una manera abreviada de expresar una reacción química (cambio químico) con fórmulas y símbolos. Para poder escribir una ecuación para una reacción
Concentración de cloruro en el suero fisiológico comercial
 Concentración de cloruro en el suero fisiológico comercial Integrantes: María Rosales 20.394298 Hécmaris Bellorin 20.263.962 Marvic Navas 20.432.075 José Escalante 19.046.898 Volumetría de precipitación
Concentración de cloruro en el suero fisiológico comercial Integrantes: María Rosales 20.394298 Hécmaris Bellorin 20.263.962 Marvic Navas 20.432.075 José Escalante 19.046.898 Volumetría de precipitación
EQUILIBRIOS DE SOLUBILIDAD
 EQUILIBRIOS DE SOLUBILIDAD EJERCICIOS Y PROBLEMAS RESUELTOS PROBLEMA 1.- Una disolución saturada de tetraoxofosfato (V) de plata, contiene, 10 5 moles por litro de ion fosfato. Calcula el producto de solubilidad
EQUILIBRIOS DE SOLUBILIDAD EJERCICIOS Y PROBLEMAS RESUELTOS PROBLEMA 1.- Una disolución saturada de tetraoxofosfato (V) de plata, contiene, 10 5 moles por litro de ion fosfato. Calcula el producto de solubilidad
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
6.2.- Reacciones de oxidación reducción
 350 Reacciones de transferencia de electrones 6.2.- Reacciones de oxidación reducción Aspectos teóricos: Valoraciones redox 6.2.1. Valoraciones redox. Equivalentes de oxidación-reducción Las reacciones
350 Reacciones de transferencia de electrones 6.2.- Reacciones de oxidación reducción Aspectos teóricos: Valoraciones redox 6.2.1. Valoraciones redox. Equivalentes de oxidación-reducción Las reacciones
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
Tecnólogo en Minería. Equilibrio Químico. Química I
 Tecnólogo en Minería Equilibrio Químico Química I Concepto de equilibrio y constante Pocas reacciones químicas se dan en un sentido Muchas veces las reacciones químicas no se completan, sino que llegan
Tecnólogo en Minería Equilibrio Químico Química I Concepto de equilibrio y constante Pocas reacciones químicas se dan en un sentido Muchas veces las reacciones químicas no se completan, sino que llegan
TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. Calcule: a) Los moles de metano que quedan. b) Las moléculas
TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. Calcule: a) Los moles de metano que quedan. b) Las moléculas
PAAU (LOXSE) Xuño 2008
 PAAU (LOXSE) Xuño 2008 Código: 31 QUÍMICA CALIFICACIÓN: CUESTIONES =2 PUNTOS CADA UNA; PROBLEMAS: 2 PUNTOS CADA UNO; PRÁCTICA: 2 PUNTOS CUESTIONES (Responda SOLAMENTE a DOS de las siguientes cuestiones)
PAAU (LOXSE) Xuño 2008 Código: 31 QUÍMICA CALIFICACIÓN: CUESTIONES =2 PUNTOS CADA UNA; PROBLEMAS: 2 PUNTOS CADA UNO; PRÁCTICA: 2 PUNTOS CUESTIONES (Responda SOLAMENTE a DOS de las siguientes cuestiones)
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE.
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
1 litro= 10 3 cm 3. TK = t ºC Tn = 10 3 Kg. 1 atm = 760mm de Hg = 760 Torr. R = 0,082 atm.l/k.mol
 Equilibrio químico 1 litro= 10 3 cm 3 1 m 3 = 10 3 litros = 10 6 cm 3 TK = t ºC + 273 1 Tn = 10 3 Kg 1 atm = 760mm de Hg = 760 Torr R = 0,082 atm.l/k.mol R= 8,31 Jul/K.mol = 2 cal/k.mol (En termoquímica
Equilibrio químico 1 litro= 10 3 cm 3 1 m 3 = 10 3 litros = 10 6 cm 3 TK = t ºC + 273 1 Tn = 10 3 Kg 1 atm = 760mm de Hg = 760 Torr R = 0,082 atm.l/k.mol R= 8,31 Jul/K.mol = 2 cal/k.mol (En termoquímica
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción B Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio 5, Opción A
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción B Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio 5, Opción A
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo.
 Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
ESTEQUIOMETRIA. H 2 SO Na Na 2 SO 4 + H 2 Acido sulfúrico Sodio Sulfato de sodio Hidrógeno
 ESTEQUIOMETRIA 1.- Se hace reaccionar 4,00 g de ácido sulfúrico con sodio metálico en condiciones estequiométricas. a) Cuántos moles de sulfato de sodio se obtienen? b) Cuántas moléculas de hidrógeno se
ESTEQUIOMETRIA 1.- Se hace reaccionar 4,00 g de ácido sulfúrico con sodio metálico en condiciones estequiométricas. a) Cuántos moles de sulfato de sodio se obtienen? b) Cuántas moléculas de hidrógeno se
TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos
 TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos ÍNDICE 1. Ecuaciones (reacciones) químicas 2. Cálculos estequiométricos. Reactivo limitante y reacciones consecutivas 3. Pureza de un reactivo 4. Rendimiento
TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos ÍNDICE 1. Ecuaciones (reacciones) químicas 2. Cálculos estequiométricos. Reactivo limitante y reacciones consecutivas 3. Pureza de un reactivo 4. Rendimiento
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II HOJAS DE TRABAJO UNIDAD IV DISOLUCIONES Libros a utilizar:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II HOJAS DE TRABAJO UNIDAD IV DISOLUCIONES Libros a utilizar:
1º) Dado el sistema de equilibrio representado por la siguiente ecuación:
 EJERCICIOS DE EQUILIBRIO QUÍMICO 1º) Dado el sistema de equilibrio representado por la siguiente ecuación: NH4HS (s) NH3 (g) + H2S (g) Indique, razonadamente, cómo varían las concentraciones de las especies
EJERCICIOS DE EQUILIBRIO QUÍMICO 1º) Dado el sistema de equilibrio representado por la siguiente ecuación: NH4HS (s) NH3 (g) + H2S (g) Indique, razonadamente, cómo varían las concentraciones de las especies
FORMAS MÁS COMUNES DE EXPRESAR LA CONCENTRACIÓN:
 CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº 4 TEMA: ESTEQUIOMETRÍA DE SOLUCIONES OBJETIVOS: Resolver problemas basados en la estequiometría de las soluciones, ampliando los conocimientos para ser aplicados criteriosamente
CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº 4 TEMA: ESTEQUIOMETRÍA DE SOLUCIONES OBJETIVOS: Resolver problemas basados en la estequiometría de las soluciones, ampliando los conocimientos para ser aplicados criteriosamente
Equilibrio químico. Qué es un equilibrio químico? Reacciones unidireccionales. Variación de la concentración con el tiempo (H 2 + I 2 2 HI)
 Equilibrio químico Carlos Paucar 010 Contenidos 1.- Concepto de equilibrio químico. 1.1. Características. Aspecto dinámico de las reacciones químicas..- Ley de acción de masas. C. 3.- Grado de disociación
Equilibrio químico Carlos Paucar 010 Contenidos 1.- Concepto de equilibrio químico. 1.1. Características. Aspecto dinámico de las reacciones químicas..- Ley de acción de masas. C. 3.- Grado de disociación
UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 9
 UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 9 NOMBRE DE LA ASIGNATURA: TÍTULO: DURACIÓN: BIBLIOGRAFÍA SUGERIDA: DOCENTES Química General SOLUCIONES 6 horas
UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 9 NOMBRE DE LA ASIGNATURA: TÍTULO: DURACIÓN: BIBLIOGRAFÍA SUGERIDA: DOCENTES Química General SOLUCIONES 6 horas
Física y Química 4 ESO REACCIONES QUÍMICAS Pág. 1
 Física y Química 4 ESO REACCIONES QUÍMICAS Pág. 1 REACCIONES QUÍMICAS Un proceso físico, o un fenómeno físico, es aquel en el que no se produce cambio en la naturaleza y las propiedades de las sustancias.
Física y Química 4 ESO REACCIONES QUÍMICAS Pág. 1 REACCIONES QUÍMICAS Un proceso físico, o un fenómeno físico, es aquel en el que no se produce cambio en la naturaleza y las propiedades de las sustancias.
REACCIONES DE IONES METÁLICOS
 Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1)
 PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1) Un gas es sometido a tres procesos identificados con las letras X, Y y Z. Estos procesos son esquematizados en los gráficos que se presentan
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1) Un gas es sometido a tres procesos identificados con las letras X, Y y Z. Estos procesos son esquematizados en los gráficos que se presentan
Problema 4 Influencia de la fuerza iónica en la solubilidad de minerales
 Problema 4 Influencia de la fuerza iónica en la solubilidad de minerales Modelización hidrogeoquímica Javier Pont Castillo Natàlia Esteve Domingo Nuria Boluda Botella a) Calcular la solubilidad de la fluorita
Problema 4 Influencia de la fuerza iónica en la solubilidad de minerales Modelización hidrogeoquímica Javier Pont Castillo Natàlia Esteve Domingo Nuria Boluda Botella a) Calcular la solubilidad de la fluorita
ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES
 VII 1 PRÁCTICA 7 ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES FORMACIÓN DE PRECIPITADOS Y DISOLUCIÓN DE LOS MISMOS POR FORMACIÓN DE COMPLEJOS FUNDAMENTO DE LA PRÁCTICA En esta práctica llevaremos a cabo
VII 1 PRÁCTICA 7 ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES FORMACIÓN DE PRECIPITADOS Y DISOLUCIÓN DE LOS MISMOS POR FORMACIÓN DE COMPLEJOS FUNDAMENTO DE LA PRÁCTICA En esta práctica llevaremos a cabo
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
A continuación se detallan cada una de las propiedades coligativas:
 PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
5/15/2013. TEMA 6: Estequiometría. Tecnicatura en Minería H 2 O. ecuaciones químicas. Representadas por
 E s t e q u i o m e t r í a Estequiometría: stoicheion ( elemento ) QUÍMICA I TEMA 6: Estequiometría metron ( medida ) Se basa en entender las masas atómicas y la Ley de conservación de la masa: la masa
E s t e q u i o m e t r í a Estequiometría: stoicheion ( elemento ) QUÍMICA I TEMA 6: Estequiometría metron ( medida ) Se basa en entender las masas atómicas y la Ley de conservación de la masa: la masa
QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g)
![QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g) QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g)](/thumbs/49/25837773.jpg) OPCIÓN A QUÍMICA. 1. (2,5 puntos) Construya el ciclo de Born-aber y calcule la energía de red (Δ red ) del KCl(s) a partir de los siguientes datos: Entalpía estándar de formación del KCl(s) [Δ f (KCl)]
OPCIÓN A QUÍMICA. 1. (2,5 puntos) Construya el ciclo de Born-aber y calcule la energía de red (Δ red ) del KCl(s) a partir de los siguientes datos: Entalpía estándar de formación del KCl(s) [Δ f (KCl)]
ESTEQUIOMETRÍA 1. Disolución. 2. La reacción química. 3. La ecuación química. 4. Clasificación de las reacciones químicas. 5. Estequiometría.
 ESTEQUIOMETRÍA 1. Disolución. 2. La reacción química. 3. La ecuación química. 4. Clasificación de las reacciones químicas. 5. Estequiometría. Química 1º bachillerato Estequiometría 1 1. DISOLUCIÓN Una
ESTEQUIOMETRÍA 1. Disolución. 2. La reacción química. 3. La ecuación química. 4. Clasificación de las reacciones químicas. 5. Estequiometría. Química 1º bachillerato Estequiometría 1 1. DISOLUCIÓN Una
, H 2 SO 4, HSO 4-. HClO 4, ClO 4-, H 2 O, H 3 O +, OH -, S =, H 2 S, HS -, NH 3, NH 4+, CO 3 =, HCO 3
 1 Aplicando la teoría de Bronsted y Lowry, razonar si son ciertas o falsas las siguientes afirmaciones a) Un ácido reacciona con su base conjugada dando lugar a una disolución neutra b) Un ácido reacciona
1 Aplicando la teoría de Bronsted y Lowry, razonar si son ciertas o falsas las siguientes afirmaciones a) Un ácido reacciona con su base conjugada dando lugar a una disolución neutra b) Un ácido reacciona
QUÍMICA - 2º DE BACHILLERATO EJERCICIOS DE SELECTIVIDAD UNIDAD 6: ÁCIDO - BASE CUESTIONES 1
 CUESTIONES 1 HOJA 6-1 2003 modelo: Conocidos los ácidos HA (K a =3,6.10-6 ), HB (K a =2,5.10-3 ) y HC (K a =1,2.10-12 ) a) Cuál es el ácido más débil. b) Cuál es el que posee la base conjugada más débil.
CUESTIONES 1 HOJA 6-1 2003 modelo: Conocidos los ácidos HA (K a =3,6.10-6 ), HB (K a =2,5.10-3 ) y HC (K a =1,2.10-12 ) a) Cuál es el ácido más débil. b) Cuál es el que posee la base conjugada más débil.
JUNIO FASE GENERAL QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
6. Reacciones de precipitación
 6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
Unidad 5 Equilibrio. 1. Razone el efecto que provocará en la síntesis de amoniaco:
 Unidad 5 Equilibrio OPCIÓN A. Razone el efecto que provocará en la síntesis de amoniaco: N (g) + 3H (g) NH 3 (g) H º 9,4 kj a) Un aumento de la presión en el reactor. Un aumento de la presión origina que
Unidad 5 Equilibrio OPCIÓN A. Razone el efecto que provocará en la síntesis de amoniaco: N (g) + 3H (g) NH 3 (g) H º 9,4 kj a) Un aumento de la presión en el reactor. Un aumento de la presión origina que
La concentración másica (C)
 La concentración másica (C) Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica de Valencia) 1 Resumen
La concentración másica (C) Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica de Valencia) 1 Resumen
2.- A la temperatura de 400 º C y 710 mm de Hg de presión, el amoniaco se encuentra disociado en un 40 % según la ecuación: 2 NH 3 (g)
 EQUILIBRIO QUÍMICO : ACTIVIDADES DE SELECTIVIDAD 1.- En un matraz de 2 l se introducen 12 g de PCl 5 y se calienta hasta 300 º C. En el equilibrio de disociación; PCl 5 (g) PCl 3 (g) + Cl 2 (g), la presión
EQUILIBRIO QUÍMICO : ACTIVIDADES DE SELECTIVIDAD 1.- En un matraz de 2 l se introducen 12 g de PCl 5 y se calienta hasta 300 º C. En el equilibrio de disociación; PCl 5 (g) PCl 3 (g) + Cl 2 (g), la presión
Tema 5. Equilibrios de solubilidad-precipitación
 En los temas anteriores has visto sistemas gaseosos en equilibrio, en los que todas las sustancias se encontraban en estado gaseoso a la temperatura de trabajo, como era el caso de la síntesis del amoniaco.
En los temas anteriores has visto sistemas gaseosos en equilibrio, en los que todas las sustancias se encontraban en estado gaseoso a la temperatura de trabajo, como era el caso de la síntesis del amoniaco.
JUNIO FASE ESPECÍFICA. QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Disponemos de los pares redox (Fe 2+ /Fe) y (O 2 /H 2 O), con potenciales estándar de reducción 0,44 V y +1,23 V, respectivamente. Con ellos
JUNIO 2011. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Disponemos de los pares redox (Fe 2+ /Fe) y (O 2 /H 2 O), con potenciales estándar de reducción 0,44 V y +1,23 V, respectivamente. Con ellos
Las sustancias reaccionan entre sí. REACCIÓN QUÍMICA: proceso en el cual una o varias sustancias cambian para formar sustancias nuevas
 Las sustancias reaccionan entre sí. REACCIÓN QUÍMICA: proceso en el cual una o varias sustancias cambian para formar sustancias nuevas LEY DE LAVOISIER: Los átomos no se crean ni se destruyen durante cualquier
Las sustancias reaccionan entre sí. REACCIÓN QUÍMICA: proceso en el cual una o varias sustancias cambian para formar sustancias nuevas LEY DE LAVOISIER: Los átomos no se crean ni se destruyen durante cualquier
Ejercicios de acceso a la Universidad Problemas de Ácidos y Bases
 Ejercicios de acceso a la Universidad Problemas de Ácidos y Bases 68 Si 10,1 ml de vinagre han necesitado 50,5 ml de una base 0,2 N para su neutralización: a) Cuál será la normalidad del ácido en el vinagre?.
Ejercicios de acceso a la Universidad Problemas de Ácidos y Bases 68 Si 10,1 ml de vinagre han necesitado 50,5 ml de una base 0,2 N para su neutralización: a) Cuál será la normalidad del ácido en el vinagre?.
Análisis Gravimétrico
 Análisis Gravimétrico Noviembre, 2012 Clasificación del Análisis Químico Análisis Químico Análisis químico cualitativo Análisis químico cuantitativo Qué hay? Cuánto hay? Identificar los componentes Cuantificar
Análisis Gravimétrico Noviembre, 2012 Clasificación del Análisis Químico Análisis Químico Análisis químico cualitativo Análisis químico cuantitativo Qué hay? Cuánto hay? Identificar los componentes Cuantificar
Molaridad y molalidad
 Molaridad y molalidad Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica de Valencia) 1 Resumen de
Molaridad y molalidad Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica de Valencia) 1 Resumen de
1010 DEPARTAMENTO DE FÍSICA Y QUÍMICA 2º Bachillerato QUÍMICA
 1.- La constante de equilibrio, K p, para la siguiente reacción química: C 2 H 4 (g) + H 2 (g) C 2 H 6 (g), vale 5 x 10 17, a 25º C. Calcula, a la misma temperatura, el valor de K c. Solución: K c = 1,22
1.- La constante de equilibrio, K p, para la siguiente reacción química: C 2 H 4 (g) + H 2 (g) C 2 H 6 (g), vale 5 x 10 17, a 25º C. Calcula, a la misma temperatura, el valor de K c. Solución: K c = 1,22
1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml.
 ESTEQUIOMETRÍA,DISOLUCIONES: ACTIVIDADES DE SELECTIVIDAD. 1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml. a) Qué volumen de esta disolución se
ESTEQUIOMETRÍA,DISOLUCIONES: ACTIVIDADES DE SELECTIVIDAD. 1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml. a) Qué volumen de esta disolución se
EQUILIBRIO QUÍMICO SOLUCIONES A LAS ACTIVIDADES DE FINAL DE UNIDAD. para cada una de las siguientes reacciones reversibles: O (g) FNO. p p.
 8 EQUILIBRIO QUÍMICO SOLUCIONES A LAS ACTIVIDADES DE FINAL DE UNIDAD Constante de equilibrio 1 Escribe la eresión de las constantes de equilibrio K y K c ara cada una de las siguientes reacciones reversibles:
8 EQUILIBRIO QUÍMICO SOLUCIONES A LAS ACTIVIDADES DE FINAL DE UNIDAD Constante de equilibrio 1 Escribe la eresión de las constantes de equilibrio K y K c ara cada una de las siguientes reacciones reversibles:
ECBTI QUIMICA GENERAL Semestre I 2016
 Fase III (actividad grupal) DESARROLLO EJERCICIOS FASE GRUPALES Desarrollo tomado del grupo 361con ajuste: Enunciados de los ejercicios. 1. Cuál es el porcentaje en masa (peso) de una solución que se preparó
Fase III (actividad grupal) DESARROLLO EJERCICIOS FASE GRUPALES Desarrollo tomado del grupo 361con ajuste: Enunciados de los ejercicios. 1. Cuál es el porcentaje en masa (peso) de una solución que se preparó
LAS REACCIONES QUÍMICAS.
 1 Ajustes de reacciones químicas. LAS REACCIONES QUÍMICAS. Ejercicios de la unidad 8 1.- Ajusta por tanteo las siguientes reacciones químicas: a) C 3 H 8 + O CO + H O; b) Na + H O NaOH + H ; c) KOH + H
1 Ajustes de reacciones químicas. LAS REACCIONES QUÍMICAS. Ejercicios de la unidad 8 1.- Ajusta por tanteo las siguientes reacciones químicas: a) C 3 H 8 + O CO + H O; b) Na + H O NaOH + H ; c) KOH + H
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Modelo 2005/2006 PRIMERA PARTE
 1 PAU Química. Modelo 2005/2006 PRIMERA PARTE Cuestión 1. Para el elemento alcalino del tercer periodo y para el segundo elemento del grupo de los halógenos: a) Escriba sus configuraciones electrónicas.
1 PAU Química. Modelo 2005/2006 PRIMERA PARTE Cuestión 1. Para el elemento alcalino del tercer periodo y para el segundo elemento del grupo de los halógenos: a) Escriba sus configuraciones electrónicas.
Propiedades ácido-base de las sales
 Propiedades ácido-base de las sales Apellidos, nombre Departamento Centro Morais Ezquerro, Sergi B. (smorais@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es) Tortajada Genaro, Luis A. (luitorge@qim.upv.es)
Propiedades ácido-base de las sales Apellidos, nombre Departamento Centro Morais Ezquerro, Sergi B. (smorais@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es) Tortajada Genaro, Luis A. (luitorge@qim.upv.es)
4.4. MOLES Y MOLÉCULAS.
 4.4. MOLES Y MOLÉCULAS. 4.4.1. MASA ATÓMICA Y MASA MOLECULAR Las moléculas están formadas por la unión de átomos que se unen mediante enlace químico. Esto significa que los átomos son difíciles de separar
4.4. MOLES Y MOLÉCULAS. 4.4.1. MASA ATÓMICA Y MASA MOLECULAR Las moléculas están formadas por la unión de átomos que se unen mediante enlace químico. Esto significa que los átomos son difíciles de separar
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016
 REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 2
 UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 2 NOMBRE DE LA ASIGNATURA: TÍTULO: DURACIÓN: BIBLIOGRAFÍA SUGERIDA: QUIMICA INORGANICA EQUILIBRIO QUIMICO 1 SEMANAS
UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 2 NOMBRE DE LA ASIGNATURA: TÍTULO: DURACIÓN: BIBLIOGRAFÍA SUGERIDA: QUIMICA INORGANICA EQUILIBRIO QUIMICO 1 SEMANAS
5. Equilibrio químico 5.1 Introducción. 5.1 Introducción
 05 Equilibrio químico Todos los procesos químicos evolucionan desde los reactivos hasta la formación de productos a una determinada velocidad hasta que la reacción se completa Llegado ese instante, lo
05 Equilibrio químico Todos los procesos químicos evolucionan desde los reactivos hasta la formación de productos a una determinada velocidad hasta que la reacción se completa Llegado ese instante, lo
CÁ LCULOS ESTEQUIOME TRICOS
 CÁ LCULOS ESTEQUIOME TRICOS 1. Cuando el carbonato de calcio sólido reacciona con el ácido clorhídrico diluido, se obtienen cloruro de calcio soluble, aua líquida y dióxido de carbono, que se desprende
CÁ LCULOS ESTEQUIOME TRICOS 1. Cuando el carbonato de calcio sólido reacciona con el ácido clorhídrico diluido, se obtienen cloruro de calcio soluble, aua líquida y dióxido de carbono, que se desprende
Física y química 1º bachillerato ESTEQUIOMETRÍA
 1.- Reacción química. Ecuación química. 2.- Tipos de reacciones. 3.- Cálculos estequiométricos. ESTEQUIOMETRÍA 1.- REACCIÓN QUÍMICA. ECUACIÓN QUÍMICA Una reacción química es cualquier proceso en el que
1.- Reacción química. Ecuación química. 2.- Tipos de reacciones. 3.- Cálculos estequiométricos. ESTEQUIOMETRÍA 1.- REACCIÓN QUÍMICA. ECUACIÓN QUÍMICA Una reacción química es cualquier proceso en el que
Cambio de color Liberación de energía en forma de luz o calor Absorción de energía (disminución de temperatura) Cambio de olor Aparición de burbujas
 Cambio de color Liberación de energía en forma de luz o calor Absorción de energía (disminución de temperatura) Cambio de olor Aparición de burbujas o sólidos (precipitados) para qué? Para describir los
Cambio de color Liberación de energía en forma de luz o calor Absorción de energía (disminución de temperatura) Cambio de olor Aparición de burbujas o sólidos (precipitados) para qué? Para describir los
GUÍA N 3: Equilibrio Químico y Cinética Química
 1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Reacción irreversible b) Reacción reversible c) Equilibrio químico d) Constante de equilibrio e) Principio de Le Chatelier
1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Reacción irreversible b) Reacción reversible c) Equilibrio químico d) Constante de equilibrio e) Principio de Le Chatelier
