1521 Química Orgánica III Prof. Mario Alfredo García Carrillo Semestre 2017-I
|
|
|
- María Victoria Crespo Blanco
- hace 6 años
- Vistas:
Transcripción
1 1521 Química rgánica III TAREA 3 1. Cómo prepararías los siguientes aminoácidos empleando la síntesis de Strecker? a) Glicina, b) Valina, c) Leucina. 2. Cómo prepararías los siguientes aminoácidos empleando la síntesis de acetamidomalonica? a) Leucina, b) Triptófano. 3. Cómo prepararías los siguientes aminoácidos empleando la síntesis de aminación reductiva? a) Metionina, b) Alanina, c) valina. 4. Muestra los pasos que se necesitan para sintetizar Fe-Ala-Val utilizando el proceso de Merrifield. 5. Dibuja las estructuras de los derivados PT que obtendrías por la degradación de Edman para los siguientes péptidos: a) Ile-Leu-Pro-Fen, b) Asp-Thr-Ser-Gli-Ala. 6. Cuáles enlaces amidicos en el siguiente polipéptido se romperán cuando se usa tripsina? 7. Serina puede ser sintetizada por una simple variación del método de amidomalonato utilizando formaldehido en ligar de un haluro de alquilo. Cómo podría ser esto hecho? 8. La reacción de ninihidrina con un α-aminoácido ocurre en varios pasos: a) el primer paso es la formación de una imina por la reacción del aminoácido con la ninihidrina. Muestra la estructura y el mecanismo de su formación. b) el segundo paso es una descarboxilación. Muestra la estructura del producto y el mecanismo de la descarboxilación. c) el tercer paso es la hidrólisis de una imina para producir una amina y un aldehído. Muestra las estructuras de ambos productos y el mecanismo de la reacción de hidrólisis. d) el paso fina es la formación de un anión que se ve de color purpura. Muestra el mecanismo de la reacción. 9. Proponga una estructura para un octapéptido que muestra la siguiente composición: Asp, 2Gli, Leu, Fen, 2Pro, Val. El reactivo de Edman muestra que la glicina es el aminoácido -terminal y carboxipeptidasa A que leucina es el aminoácido C-terminal. idrólisis parcial con Cl diluido produce los siguientes fragmentos: Val-Pro-Leu, Gli, Gli-Asp-Fen-Pro, Fen-Pro-Val. 10. Aspartame, un edulcificante no nutritivo conocido en el mercado como utrasweet, es el éster metílico de un simple dipéptido: Asp-Fe-Me. a) dibuja la estructura del aspartame. b) El punto isoeléctrico del aspartame es 5.9. Dibuja la estructura principal presente a ese p. c) dibuja la forma principal del aspartame presente a p fisiológico p= Indique para cada inciso los péptidos que resultarían de la ruptura con el reactivo indicado: a) is-lis-leu-val-glu-pro-arg-ala-gli-ala con tripsina.
2 1521 Química rgánica III b) Leu-Gli-Ser-Met-Fe-Pro-Tir-Gli-Val con quimotripsina. c) Val-Arg-Gli-Met-Arg-Ala-Ser con carboxipeptidasa A. d) Ser-Fe-Lis-Met-Pro-Ser-Ala-Asp con bromuro de cianógeno. e) Arg-Ser-Pro-Lis-Lis-Ser-Glu-Gli con tripsina. 12. Utilizando diciclohexilcarbodimida (DCC), Cómo prepararías el aspártame? 13. Los α-aminoácidos pueden ser preparados a partir de un aldehídos, amoniaco y cianuro de hidrogeno, seguido de hidrólisis acida. a) Escribe las estructuras de 2 intermediarios que se forman en esta reacción. b) Qué aminoácido resulta cuando se utiliza como aldehído 3-metilbutanal? c) Qué aldehído se usaría para preparar valina? 14. Determina la secuencia de aminoácidos de un polipéptido que se somete a: a) Una hidrólisis completa dando los siguientes aminoácidos: Ala, Arg, Gli, 2 Lis, Met, Fe, Pro, 2 Ser, Tir, Val. b) Un tratamiento con el reactivo de Edman que da TP-Val. c) Un tratamiento con carboxipeptidasa A deriva en Ala. d) Un tratamiento con bromuro de cianógeno produce los siguientes dos péptidos: 1. Ala, 2 Lis, Fe, Pro, Ser, Tir 2. Arg, Gli, Met, Ser, Val e) Un tratamiento con quimotripsina produciendo los siguientes tres péptidos: 1. 2 Lis, Fe, Pro 2. Arg, Gli, Met, Ser, Tir, Val 3. Ala, Ser f) Un tratamiento con tripsina produciendo los siguientes tres péptidos: 1. Gli, Lis, Met, Tir 2. Ala, Lis, Fen, Pro, Ser 3. Arg, Ser, Val 15. Represente la estructura de los derivados de la feniltiohidantoína de: a) alanina, b) valina, c) lisina, d) prolina, d) Angiotensina II 16. Que compuestos carbonílicos usarías para preparar los siguientes aminoácidos por medio de aminación reductiva con amoniaco y borohidruro de sodio: a) alanina y b) valina. 17. Qué aminoácido se formaría si el aldehído que se usaría en la síntesis de Strecker es: a) acetaldehído, b) 2-metilbutanal, c) 3-metilbutanal? 18. Qué aminoácido se prepararía utilizando la síntesis del ester -ftalimidomalonico cuando los siguientes compuestos son usados: 19. Investiga para qué sirve el reactivo de Sanger y cúal es dicho reactivo
3 1521 Química rgánica III 20. Muestre las estructuras de los siguientes aminoácidos en sus formas zwiteriónicas, calcula el punto isoelectronico: a) Trp b) Ile c) Cis d) is e) Ala f) Arg 21. Prediga el producto de la reacción de la valina con los siguientes reactivos: a) C 3 C 2, ácido b) dicarbonato de di-ter-butilo y Et 3 c) K, 2 d) C 3 CCl, piridina. e) alcohol bencílico, ácido f) cloroformiato de bencilo y Et Un hexapéptido con la composición Arg, Gly, Leu, 3Pro tiene prolina en los extremos C y. La hidrólisis parcial produce los siguientes fragmentos: -Gly-Pro-Arg- -Arg-Pro- -Pro-Leu-Gly- Cuál es la estructura del hexapéptido? 23. Cómo sintetizarías Valina a partir de un ácido carboxílico adecuado por el método de aminación de α-haloacidos? 24. Dibuja la estructura de la lisina a p igual a 9. Lisina pka α-c=2.18, pka α- 3 + = 8.95, pka cadena lateral=10.5. Cuál es su punto isoleléctronico? 25. Indique cada paso para sintetizar la encefalina Tir-Gli-Gli-Fen-Leu mediante la técnica en fase sólida de Merrifield. 26. La mayoría de las aminas y de los ácidos carboxílicos son solubles en éter etílico. Por qué los aminoácidos son insolubles en éter etílico? Explica tu respuesta. 27. La cisteína es el único aminoácido que tiene estereoquímica L pero una configuración R. Construya una estructura para otro aminoácido L, de su propia creación que también tenga una configuración R. 28. Escriba la estructura del ácido aspártico que predomina cuando se tienen los siguientes valores de p. a) p=1 b) p=2.6 c) p=6 d) p= Arginina, el más básico de los 20 aminoácidos comunes, contiene un grupo funcional guadinino en su cadena lateral. Explique, usando estructuras de resonancia como el grupo guadinino protonado es estabilizado.
4 1521 Química rgánica III 2 C grupo guanidino Arginina La síntesis de Gabriel también es útil para sintetizar aminoácidos. Desarrolle el mecanismo detallado de la obtención de L-glicina de acuerdo a la reacción siguiente: K Cl Et 1) K / 2 2) Cl 2 L-Glicina 31. Si el acetamidomalonato de dietilo reacciona con el acrilonitrilo en presencia de base, se forma el compuesto G, el cual produce ácido glutámico después de agregarle ácido. Desarrolle todas las transformaciones y diga quien es G. Et Et Et a G C Et (C ) Cl / 2 Acido glutámico 32. Cuando G se hidrogena, se produce una δ lactama la cual con medio ácido y calentamiento forma el aminoácido ornitina. Desarrolle todos los pasos y diga quien es y G, y dé la estructura de la ornitina. G (C ) 2 / i 1000 psi (C ) se forma una lactama Cl / 2 rnitina (C ) 33. Cierto péptido se hidroliza y los fragmentos resultantes son los que se muestran. Determine cuál era la secuencia original del péptido. Ser-Ile-Arg-Val-Val-Pro-Tyr Ser-Ile-Arg Leu-Arg Val-Val-Pro-Tyr 34. Cuál es la estructura predominante del ácido aspártico a p fisiológico (p=7.3) (α-c pka = 2.09, α- 3 + pka = 9.82, -C cadena lateral pka= 3.86)? 35. Cuál es la estructura de A para la síntesis de D, L-isoleucina por el método de Strecker? C Cl, KC 3 C A
5 1521 Química rgánica III 36. Escriba la estructura del tripéptido Val-Ser-Cis (Ser, R=C 2, Cis, R=SC 2, Val, R=isopropilo). Escriba el mecanismo de reacción y las estructuras de los productos que se forman cuando el tripéptido se trata con Cl 6M acuoso tal como ocurre en el estómago cuando ingerimos proteínas. 37. Elija la fórmula más estable que presenta de la tirosina a p=11, pka C 2 = 2.20, pka α 3 = 9.11, pka C 6 5 = Muestre cómo podría utilizar el éster acetamidomalónico para preparar el aminoácido fenilalanina. Describa el mecanismo de reacción. 39. Proponga un mecanismo de reacción para cada paso que se presenta en la síntesis a continuación. 40. Utilizando la síntesis amidomalónica, diga como obtendría la histidina. Qué estereoquímica se espera que tenga este producto sintético? aga el mecanismo de reacción para cada paso que proponga. 41. En la síntesis de péptidos, un grupo carboxilo se puede proteger formando: a) Un hemiacetal b) Un acetal c) Un éter d) Un éster 42. Qué aldehído se forma cuando la isoleucina reacciona con la ninhidrina? 43. Conque reactivo se puede saber cuál es el aminoácido -terminal de un péptido? 44. De las siguientes características de los aminoácidos, indique cuál no corresponde a dichos compuestos: a) Forman iones dipolares
6 1521 Química rgánica III b) Tienen un alto punto de fusión c) Son solubles en hidrocarburos d) Pueden formar sales cristalinas 45. Para sintetizar la encefalina Tir-Gli-Gli-Fen-Leu mediante la técnica en fase sólida de Merrifield, se debe iniciar con el compuesto indicado en el inciso: a) -Tir- b) BC-Tir- c) -Leu- d) BC-Leu- 46. Con los datos experimentales siguientes elija la estructura primaria de un tetrapéptido La leucina es el aminoácido -terminal La hidrólisis del tetrapéptido dio varios fragmentos, uno de los cuales era un tripéptido compuesto por Gli, Fe y Leu También se halló en la mezcla de hidrólisis un dipéptido que contenía Ala y Gli La estructura primaria del tetrapéptido es: a) Gli -Ala-Fe Leu b) Leu-Fe-Ala-Gli c) Leu-Fe-Gli-Ala d) Fe-Ala-Gli- Leu 47. Uno de los L-aminoácidos que sí puede prepararse mediante la Síntesis malónica es el indicado en el inciso: C S C C C 2 2 A B C D Cuál es el producto A? 2 CC C 3 CC C 2 1) C S CC 2) Cl A 49. La fórmula estructural para el dipéptido Glicil-L-alanina es: 3 C 3 C C C 2 3 C 3 C C C 2 A B C D
7 1521 Química rgánica III 50. Indique cuál descripción corresponde a la estructura terciaria de una proteína: A. Es la orientación, en un patrón regular, de los diferentes segmentos de una proteína. B. El plegamiento total de la proteína en una forma general tridimensional. C. Es la secuencia de aminoácidos en una proteína. D. Es la reunión de varios péptidos o proteínas en grandes estructuras agregadas 51. Qué reactivo es usado comúnmente para la activación del ácido carboxílico en la formación de péptidos? A. Diciclohexilurea B. Di-carbonato de di terc-butilo C. Cloruro de tionilo D. Diciclohexilcarbodiimida 52. Qué reactivo se puede emplear para determinar la estructura primaria de un péptico y/o proteína? a) BrC b) 2-Mercaptoetanol c) Ph==C=S d) Cl 53. Indique cuál de los siguientes enunciados describe los factores que determinan la estructura terciaria de una proteína a) Interacciones hidrofóbicas de las cadenas laterales b) secuencia de unión entre los aminoácidos c) formación de puentes disulfuro d) formación de puentes de hidrógeno 54. Cuáles serán los productos que se obtendrán si el siguiente tripéptido se trata con una carboxipeptidasa A? C C 3 C 3 - Carboxipeptidasa? 55. Ponga el mecanismo de reacción de la siguiente reacción. C 3 3 C C 3 R CF 3 C R 3 C C C 3 + C Los aminoácidos se pueden identificar haciéndolos reaccionar con ninhidrina. En el caso de la alanina, ocurre la reacción siguiente: C 2 + Y Donde Y es una molécula de: A. Acetaldehído
8 1521 Química rgánica III B. Acetona C. Acetato de etilo D. Ácido acético 57. Señale con qué paso se debe iniciar la síntesis del dipéptido alanil-serina, cuando la síntesis se hace en disolución: A. Proteger el grupo amino de la serina como su derivado BC B. Formar el éster metílico para proteger la alanina C. acer reaccionar la serina con DCC D. Proteger el grupo amino de la alanina como su derivado BC 58. De las siguientes afirmaciones sobre los aminoácidos, diga cuál está equivocada: a. Forman un ión bipolar (zwitterion), con carga positiva y negativa. b. Son bifuncionales, tienen un grupo amino y un carboxilo. c. Se les llama α-aminoácidos porque tienen 4 sustituyentes diferentes en el carbono alfa. d. Son anfóteros, pueden reaccionar como ácidos y como bases. 59. De las siguientes afirmaciones sobre los aminoácidos, diga cuál es correcta: a. Los aminoácidos tienen puntos de fusión bajos, generalmente inferiores a 150 C b. Los aminoácidos son más solubles en agua que en éter, diclorometano y otros disolventes orgánicos comunes. c. Los aminoácidos naturales pertenecen a la serie D d. La forma predominante del aminoácido no depende del p de la disolución 60. Muestre la estructura del dipéptido que se obtiene al realizar las siguientes reacciones. Boc-Ala Leu-C 3 1) DCC 2) CF 3 C 3) a / 2? 61. Cuál es el nombre sistemático de la L-Leucina? 62. La síntesis de aminoácidos por el método del ftalimidomalonato (malonato de dietilo y síntesis de Gabriel) utiliza como fuente de nitrógeno a: A B C D 63. La estructura del Ácido (2R)-2-amino-3-sulfanilpropanoico (L-Cisteína) es: S 2 S 2 S 2 A B C D S 2
9 1521 Química rgánica III 64. Explique porque los aminoácidos existen en su forma de zwitterion en solución acuosa pero principalmente como ácidos α aminocarboxílicos en solución clorofórmica. 3 C 2 C R R En agua En cloroformo a) Porque en el agua se dá la reacción ácido base más facilmente b) Porque el agua al ser polar, solvata facílmente a una especie cargada como el zwitterion en vez del cloroformo, que al ser poco polar disuelve mejor a una especie neutra como un α aminocarboxílico. c) Porque el cloroformo no disuelve a una especie cargada d) La forma en que se encuentre el aminoácido no depende del disolvente sino de su punto isoeléctrico. 65. Los aminoácidos se caracterizan por tener alta solubilidad en disolventes: a) o polares b) Aproticos c) Polares d) rgánicos e) Polaridad intermedia 66. Los elevados puntos de fusión de los aminoácidos se explican por qué: a) Son sales b) Tienen interacciones no covalente c) Forman puentes Disulfuro d) Son compuestos orgánicos e) Presentan resonancia del enlace amida 67. En un enlace peptídico, el átomo de nitrógeno del enlace amida tiene hibridación: a) sp 3 b) d 2 sp 3 c) sp d) dsp 3 e) sp Los aminoácidos quirales esenciales son: a) β / L b) α / D c) α / L d) β / R e) α / R 69. Un método para la degradación de péptidos es: a) Degradación de Strecker b) Método de Killiani-Fischer c) Degradación de Ruff d) Degradación de Edman e) Degradación Marker 70. La estructura correcta del tripéptido Leu-Tyr-Gly- 2 que incluye la estereoquímica de cada estereocentro es: Leu-Tyr-Gly- 2
10 1521 Química rgánica III 71. El siguiente dipéptido se sintetizó a partir de Boc-Phe. Seleccione las condiciones adecuadas para obtenerlo. Dipéptido: Phe-Leu DCC = diciclohexil carbodiimida TFA = ácido trifluoroacético A) 1) Leu + C 3, 2 S 4 cat.; 2) Boc-Phe + Leu-C 3 + DCC; 3) a, 2 ; 4) TFA B) Boc-Phe + Leu + DCC C) 1) Boc-Phe + Leu + DCC; 2) TFA D) 1) Phe + Leu + DCC; 2) TFA 72. El nombre IUPAC del aminoácido L- Ácido aspártico es: A) Ácido (2S)-2-amino-3-(4-hidroxifenil)propanóico B) Ácido (2R)-2-amino-3-(4-hidroxifenil)propanóico C) Ácido (2S)-2-amino-3-hidroxifenilpropanóico D) 1-Carboxi-1-amino-2-(4-hidroxifenil)etano 73. Cuál de las siguientes de refiere a arreglos de residuos de aminoácidos particularmente estables, en una proteína que dan lugar a patrones recurrentes? A) estructura primaria B) estructura secundaria C) estructura terciaria D) estructura cuaternaria
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
 Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
AMINOÁCIDOS Y PÉPTIDOS
 TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
CLASIFICACIÓN SEGÚN SU POLARIDAD NO POLARES POLARES NEUTROS ACIDOS BASICOS
 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
Metabolismo de AMINOÁCIDOS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
Lehninger Principles of Biochemistry Fourth Edition
 David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de
 Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO
 ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS
 EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA
 BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA
 Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
Unidad 5 (Parte 8) Análisis y Síntesis de Péptidos y Proteínas.
 Unidad 5 (Parte 8) Análisis y Síntesis de Péptidos y Proteínas. La determinación de la estructura de un péptido requiere contestar tres preguntas: Cuáles aminoácidos están presentes? Cuántos hay de cada
Unidad 5 (Parte 8) Análisis y Síntesis de Péptidos y Proteínas. La determinación de la estructura de un péptido requiere contestar tres preguntas: Cuáles aminoácidos están presentes? Cuántos hay de cada
Aminoácidos y péptidos
 Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
REACCIONES DE SÍNTESIS DE LOS ÁCIDOS CARBOXÍLICOS
 EAIES DE SÍTESIS DE LS ÁIDS ABXÍLIS 1.- xidación de los alcoholes primarios y aldehídos. En los temas anteriores ya se ha estudiado la oxidación de alcoholes primarios que mediante oxidantes fuertes se
EAIES DE SÍTESIS DE LS ÁIDS ABXÍLIS 1.- xidación de los alcoholes primarios y aldehídos. En los temas anteriores ya se ha estudiado la oxidación de alcoholes primarios que mediante oxidantes fuertes se
Estructura y propiedades de las proteínas
 Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
Tema 12. Química de los aminoácidos y péptidos
 Tema 12 Química de los aminoácidos y péptidos Estructura Átomo de carbono α Grupo amino α Un α-aminoácido Enlaces peptídicos Cadena lateral Una parte de un péptido Alanina Serina Glicina Cisteina Valina
Tema 12 Química de los aminoácidos y péptidos Estructura Átomo de carbono α Grupo amino α Un α-aminoácido Enlaces peptídicos Cadena lateral Una parte de un péptido Alanina Serina Glicina Cisteina Valina
AMINOÁCIDOS, PÉPTIDOS Y PROTEINAS. M.Sc. GABY MÓNICA FELIPE BRAVO
 AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
Tema 9. Química Orgánica
 Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Cuantificación y análisis químico de proteínas
 Cuantificación y análisis químico de proteínas Enlace peptídico R 1 R 2 Secuencia: AlaGluGlyLys o AEGK Puentes disulfuro COO- COO- COO- NH 2 NH 2 NH 2 Modificaciones Post-traduccionales I Análisis químico
Cuantificación y análisis químico de proteínas Enlace peptídico R 1 R 2 Secuencia: AlaGluGlyLys o AEGK Puentes disulfuro COO- COO- COO- NH 2 NH 2 NH 2 Modificaciones Post-traduccionales I Análisis químico
CÓMO SE PUEDE DETERMINAR LA SECUENCIA DEL DNA A PARTIR DE UNA PROTEÍNA? DR. MANUEL E. AQUINO
 Alianza para el Aprendizaje de Ciencias y Matemáticas CÓMO SE PUEDE DETERMINAR LA SECUENCIA DEL DNA A PARTIR DE UNA PROTEÍNA? DR. MANUEL E. AQUINO GUÍA DEL MAESTRO ESTÁNDARES ATENDIDOS: 1. LA NATURALEZA
Alianza para el Aprendizaje de Ciencias y Matemáticas CÓMO SE PUEDE DETERMINAR LA SECUENCIA DEL DNA A PARTIR DE UNA PROTEÍNA? DR. MANUEL E. AQUINO GUÍA DEL MAESTRO ESTÁNDARES ATENDIDOS: 1. LA NATURALEZA
QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Agua (o humedad, si se conoce)*
 QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Entregar el 21 de Mayo. Selecciona un alimento, de preferencia de los que consumes con regularidad, que contenga proteínas. 1. De acuerdo
QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Entregar el 21 de Mayo. Selecciona un alimento, de preferencia de los que consumes con regularidad, que contenga proteínas. 1. De acuerdo
GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas
 GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas I.- Conceptos básicos: Aminoácidos: Estructura y propiedades ácido base de los aminoácidos. Clasificación según su polaridad. Capacidad buffer. El
GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas I.- Conceptos básicos: Aminoácidos: Estructura y propiedades ácido base de los aminoácidos. Clasificación según su polaridad. Capacidad buffer. El
Departamento de Química Física Facultad de Ciencias
 Interacciones electrostáticas. Interacciones electrostáticas. Los fenómenos de interacción con el disolvente y cosolventes. Interacciones electrostáticas. El origen de las cargas en proteínas. Fuentes
Interacciones electrostáticas. Interacciones electrostáticas. Los fenómenos de interacción con el disolvente y cosolventes. Interacciones electrostáticas. El origen de las cargas en proteínas. Fuentes
Proteínas. Fabrizio Marcillo Morla MBA. (593-9)
 Proteínas Fabrizio Marcillo Morla MBA barcillo@gmail.com (593-9) 4194239 Otras Publicaciones del mismo autor en Repositorio ESPOL Fabrizio Marcillo Morla Guayaquil, 1966. BSc. Acuicultura. (ESPOL 1991).
Proteínas Fabrizio Marcillo Morla MBA barcillo@gmail.com (593-9) 4194239 Otras Publicaciones del mismo autor en Repositorio ESPOL Fabrizio Marcillo Morla Guayaquil, 1966. BSc. Acuicultura. (ESPOL 1991).
Figura 1: Esquema de polímero
 Eje temático: Química: Fenómenos nucleares Polímeros Procesos químicos industriales Contenido: Tipos de polímeros y polimerización Nivel: Cuarto medio Polímeros. Polímeros sintéticos y naturales Polímeros
Eje temático: Química: Fenómenos nucleares Polímeros Procesos químicos industriales Contenido: Tipos de polímeros y polimerización Nivel: Cuarto medio Polímeros. Polímeros sintéticos y naturales Polímeros
3. AMINOACIDOS. PROPIEDADES ACIDO-BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
Proteínas: Métodos para su Estudio
 Proteínas: Métodos para su Estudio Propiedades Espectroscópicas Todos los aminoácidos absorben luz en la región infraroja Sólo Phe, Tyr, & Trp absorben UV Absorbancia a 280 nm es un buen diagnóstico para
Proteínas: Métodos para su Estudio Propiedades Espectroscópicas Todos los aminoácidos absorben luz en la región infraroja Sólo Phe, Tyr, & Trp absorben UV Absorbancia a 280 nm es un buen diagnóstico para
Estructura tridimensional de proteínas
 Estructura tridimensional de proteínas 1. En solución acuosa, la conformación proteica esta determinada por dos factores prioritarios. Uno es la formación de un número máximo de enlaces de hidrógeno. El
Estructura tridimensional de proteínas 1. En solución acuosa, la conformación proteica esta determinada por dos factores prioritarios. Uno es la formación de un número máximo de enlaces de hidrógeno. El
Estructura del grupo carbonilo
 TEMA 19.- Compuestos carbonílicos. Clasificación y propiedades generales. Reacciones de adición. Características generales y factores con influencia en la velocidad de la adición. Adiciones de Michael.
TEMA 19.- Compuestos carbonílicos. Clasificación y propiedades generales. Reacciones de adición. Características generales y factores con influencia en la velocidad de la adición. Adiciones de Michael.
Holoproteínas (sólo contienen aa)
 TEMA 4: P ROTEÍNAS 1. Concepto y clasificación Las proteínas son biomoléculas orgánicas formadas por C, H, O, N y en menor medida P y S y otros elementos (Fe,Cu, Mg, ). Son polímeros no ramificados de
TEMA 4: P ROTEÍNAS 1. Concepto y clasificación Las proteínas son biomoléculas orgánicas formadas por C, H, O, N y en menor medida P y S y otros elementos (Fe,Cu, Mg, ). Son polímeros no ramificados de
Diferencias entre leche de vaca y de cabra
 Diferencias entre leche de vaca y de cabra Introducción: La leche de cabra tiene propiedades interesantes. El objetivo de este trabajo es poner de relieve algunas de las diferencias entre leche de cabra
Diferencias entre leche de vaca y de cabra Introducción: La leche de cabra tiene propiedades interesantes. El objetivo de este trabajo es poner de relieve algunas de las diferencias entre leche de cabra
METABOLISMO DEL NITRÓGENO
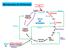 METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS.
 REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
Se encuentra separado del citoplasma por la envoltura nuclear, que está formada por varias cisternas del retículo endoplasmático, que se mantienen uni
 Se encuentra separado del citoplasma por la envoltura nuclear, que está formada por varias cisternas del retículo endoplasmático, que se mantienen unidas gracias a una red de filamentos intermedios que
Se encuentra separado del citoplasma por la envoltura nuclear, que está formada por varias cisternas del retículo endoplasmático, que se mantienen unidas gracias a una red de filamentos intermedios que
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS AMINOÁCIDOS
 ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
TEMA 4. ESTRUCTURA DE LAS MOLÉCULAS ORGÁNICAS
 W 0 J. Martínez y. Iriondo TEMA. ESTRUTURA DE LAS MLÉULAS RGÁIAS EJERIIS A. Estructuras. Dibuje las estructuras de Lewis correspondientes a los siguientes compuestos: Acetona 6 Acetonitrilo 7 Br loruro
W 0 J. Martínez y. Iriondo TEMA. ESTRUTURA DE LAS MLÉULAS RGÁIAS EJERIIS A. Estructuras. Dibuje las estructuras de Lewis correspondientes a los siguientes compuestos: Acetona 6 Acetonitrilo 7 Br loruro
4. QUÍMICA DEL CARBONO.
 4. QUÍMICA DEL CARBONO. 4.1. FÓRMULA QUÍMICA. El número atómico del carbono es seis, contiene en su núcleo seis protones mientras seis electrones se distribuyen en orbitales a su alrededor. Su configuración
4. QUÍMICA DEL CARBONO. 4.1. FÓRMULA QUÍMICA. El número atómico del carbono es seis, contiene en su núcleo seis protones mientras seis electrones se distribuyen en orbitales a su alrededor. Su configuración
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 BIOMOLÉCULAS. PROTEÍNAS BIOMOLÉCULAS Los bioelementos se unen para formar biomoléculas, también denominadas principios inmediatos. En los seres vivos las moléculas se caracterizan por presentar una gran
BIOMOLÉCULAS. PROTEÍNAS BIOMOLÉCULAS Los bioelementos se unen para formar biomoléculas, también denominadas principios inmediatos. En los seres vivos las moléculas se caracterizan por presentar una gran
AMINOACIDOS Y PROTEÍNAS
 AMINOACIDOS Y PROTEÍNAS I. OBJETIVO. Reconocer aminoácidos y proteínas a nivel de laboratorio. Analizar el tipo de estructura de los aminoácidos. II. FUNDAMENTO TEORICO. AMINOACIDOS: Cualquiera de los
AMINOACIDOS Y PROTEÍNAS I. OBJETIVO. Reconocer aminoácidos y proteínas a nivel de laboratorio. Analizar el tipo de estructura de los aminoácidos. II. FUNDAMENTO TEORICO. AMINOACIDOS: Cualquiera de los
DERIVADOS HALOGENADOS. Estructura
 TEMA 13.- Derivados halogenados. Reacciones S N. Clasificación y características generales. Sustitución nucleofílica. Mecanismos S N 2 y S N 1. Estereoquímica de las reacciones S N. Factores con influencia
TEMA 13.- Derivados halogenados. Reacciones S N. Clasificación y características generales. Sustitución nucleofílica. Mecanismos S N 2 y S N 1. Estereoquímica de las reacciones S N. Factores con influencia
Metodologías básicas del procesamiento de Proteinas
 Metodologías básicas del procesamiento de Proteinas Alejandra Kun Departamento de Proteínas y Ácidos Nucleicos-IIBCE Unidad Asociada Sección Bioquímica Facultad de Ciencias 13 de octubre 2014 Curso Introducción
Metodologías básicas del procesamiento de Proteinas Alejandra Kun Departamento de Proteínas y Ácidos Nucleicos-IIBCE Unidad Asociada Sección Bioquímica Facultad de Ciencias 13 de octubre 2014 Curso Introducción
AMINOÁCIDOS Y PROTEÍNAS
 TEMA 2 AMINOÁCIDOS Y PROTEÍNAS Antes de realizar la guía deberá revisar: 1. Concepto de ph y poder amortiguador de una solución. 2. Características químicas de los aminoácidos. Evaluación: 1. Formule la
TEMA 2 AMINOÁCIDOS Y PROTEÍNAS Antes de realizar la guía deberá revisar: 1. Concepto de ph y poder amortiguador de una solución. 2. Características químicas de los aminoácidos. Evaluación: 1. Formule la
Pagina casos de estudios:
 Libros para consulta de alumnos en el Área de Biología La Célula. De Coopers Biología Celular y Molecular G. Karp Becker.El mundo de la Célula 6Ed. Editorial Pearson Education. Alberts/Bray/Hopkin/Johnson/Lewis/Raff/Roberts/Walter.
Libros para consulta de alumnos en el Área de Biología La Célula. De Coopers Biología Celular y Molecular G. Karp Becker.El mundo de la Célula 6Ed. Editorial Pearson Education. Alberts/Bray/Hopkin/Johnson/Lewis/Raff/Roberts/Walter.
Conceptos basicos (III)
 erramientas de la Química rgánica erramientas de la Química rgánica ompuestos carbonílicos onceptos basicos (III) δ δ plano 120 º = polar sp 2 Z Z Z Z = ó Ar Z = ó Ar aldehídos cetonas María Font. Dpto.
erramientas de la Química rgánica erramientas de la Química rgánica ompuestos carbonílicos onceptos basicos (III) δ δ plano 120 º = polar sp 2 Z Z Z Z = ó Ar Z = ó Ar aldehídos cetonas María Font. Dpto.
2ª Parte: Estructura y reactividad de
 2ª Parte: Estructura y reactividad de los compuestos CMPUESTS orgánicos. CARBNÍLICS 2.- Principales familias de compuestos orgánicos: - Hidrocarburos alifáticos: alcanos, alquenos y alquinos. - Hidrocarburos
2ª Parte: Estructura y reactividad de los compuestos CMPUESTS orgánicos. CARBNÍLICS 2.- Principales familias de compuestos orgánicos: - Hidrocarburos alifáticos: alcanos, alquenos y alquinos. - Hidrocarburos
F FA AC C U ULTAD LTAD D D E
 FACULTAD DE QUÍMICA 4.1 Adición electrofílica a enlaces múltiples C-C 4.2 Adición de radicales libres a enlaces múltiples C-C 4.3 Adición nucleofílica a enlaces múltiples C-C 4.4 Adición nucleofílica a
FACULTAD DE QUÍMICA 4.1 Adición electrofílica a enlaces múltiples C-C 4.2 Adición de radicales libres a enlaces múltiples C-C 4.3 Adición nucleofílica a enlaces múltiples C-C 4.4 Adición nucleofílica a
QUÍMICA DE PROTEÍNAS
 QUÍMICA DE PROTEÍNAS COMPOSICIÓN ALIMENTO VOLATIL POR SECADO (AGUA o HUMEDAD) MATERIA SECA ORGANICA INORGANICA (CENIZAS) SOLUBLE EN DISOLVENTES ORGANICOS (GRASA O LIPIDOS) CON NITROGENO (PROTEINAS) NO
QUÍMICA DE PROTEÍNAS COMPOSICIÓN ALIMENTO VOLATIL POR SECADO (AGUA o HUMEDAD) MATERIA SECA ORGANICA INORGANICA (CENIZAS) SOLUBLE EN DISOLVENTES ORGANICOS (GRASA O LIPIDOS) CON NITROGENO (PROTEINAS) NO
Composición química de los seres vivos
 Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Estereoisomerismo en los alfaaminoácidos.
 Estructura general de un aminoácido. Esta estructura es común a todos los alfaaminoácidos, con una única excepción. (La excepción es la prolina, un aminoácido cíclico). El grupo R o cadenal lateral (en
Estructura general de un aminoácido. Esta estructura es común a todos los alfaaminoácidos, con una única excepción. (La excepción es la prolina, un aminoácido cíclico). El grupo R o cadenal lateral (en
OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo.
 1 OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo. 2 3 4 Son las moléculas que forman a los organismos o participan de su metabolismo. Orgánicas
1 OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo. 2 3 4 Son las moléculas que forman a los organismos o participan de su metabolismo. Orgánicas
ESTRUCTURA DE LA MATERIA QCA 01 ANDALUCÍA. 1.- Defina: a) Energía de ionización. b) Afinidad electrónica. c) Electronegatividad.
 1.- Defina: a) Energía de ionización. b) Afinidad electrónica. c) Electronegatividad. 2.- Razone si son verdaderas o falsas las siguientes afirmaciones: a) El punto de ebullición del butano es menor que
1.- Defina: a) Energía de ionización. b) Afinidad electrónica. c) Electronegatividad. 2.- Razone si son verdaderas o falsas las siguientes afirmaciones: a) El punto de ebullición del butano es menor que
Aminoácidos. 7. Sobre la actividad óptica de los aminoácidos es cierto que:
 Aminoácidos 1. La valoración de valina con hidróxido sódico, conduce a la obtención de dos pks. La reacción de valoración que se produce al pk2 de 9,62 es: a) COOH + OH- --> -COO- + H2O. b) COOH + -NH2
Aminoácidos 1. La valoración de valina con hidróxido sódico, conduce a la obtención de dos pks. La reacción de valoración que se produce al pk2 de 9,62 es: a) COOH + OH- --> -COO- + H2O. b) COOH + -NH2
EJEMPLOS DE PREGUNTA. Prueba de QUÍMICA. febrero 2010
 EJEMPLS DE PREGUNTA 2010 Prueba de QUÍMICA febrero 2010 PREGUNTAS DE SELECCIÓN MÚLTIPLE CN ÚNICA RESPUESTA. (TIP I) Las preguntas de este tipo constan de un enunciado y de cuatro opciones de respuesta,
EJEMPLS DE PREGUNTA 2010 Prueba de QUÍMICA febrero 2010 PREGUNTAS DE SELECCIÓN MÚLTIPLE CN ÚNICA RESPUESTA. (TIP I) Las preguntas de este tipo constan de un enunciado y de cuatro opciones de respuesta,
UNIDAD IV ALCOHOLES. Alcoholes: Usos, propiedades y aplicaciones. Pte. M. en C.Q. Macaria Hernández Chávez
 UNIDAD IV ALCOHOLES Alcoholes: Usos, propiedades y aplicaciones Pte. M. en C.Q. Macaria Hernández Chávez ALCOHOLES Introducción. La mayor parte de los alcoholes comunes, hasta con 11 ó 12 átomos de carbono,
UNIDAD IV ALCOHOLES Alcoholes: Usos, propiedades y aplicaciones Pte. M. en C.Q. Macaria Hernández Chávez ALCOHOLES Introducción. La mayor parte de los alcoholes comunes, hasta con 11 ó 12 átomos de carbono,
- Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales.
 TEMA 6. PROTEÍNAS - Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales. - Los aa son los elementos estructurales de las proteínas. Las proteínas de plantas y animales
TEMA 6. PROTEÍNAS - Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales. - Los aa son los elementos estructurales de las proteínas. Las proteínas de plantas y animales
QUÍMICA de 2º de BACHILLERATO EL ENLACE QUÍMICO
 QUÍMICA de 2º de BACHILLERATO EL ENLACE QUÍMICO EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
QUÍMICA de 2º de BACHILLERATO EL ENLACE QUÍMICO EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
Digestión y absorción de PROTEÍNAS. Marijose Artolozaga Sustacha, MSc
 Digestión y absorción de PROTEÍNAS Marijose Artolozaga Sustacha, MSc Digestión de proteínas de la dieta La mayor fuente de N de la dieta son las proteínas Unos 100g de proteína al día No se pueden absorber
Digestión y absorción de PROTEÍNAS Marijose Artolozaga Sustacha, MSc Digestión de proteínas de la dieta La mayor fuente de N de la dieta son las proteínas Unos 100g de proteína al día No se pueden absorber
TEMA 5 ESTRUCTURA Y PROPIEDADES MOLECULARES
 TEMA 5 ETRUCTURA Y PRPIEDADE MLECULARE 1. Enlaces más débiles que el enlace covalente. 1.1. Fuerzas entre dipolos. 1.2. Fuerzas de dispersión de London. 1.3. Puente de hidrógeno. 2. Influencia de la estructura
TEMA 5 ETRUCTURA Y PRPIEDADE MLECULARE 1. Enlaces más débiles que el enlace covalente. 1.1. Fuerzas entre dipolos. 1.2. Fuerzas de dispersión de London. 1.3. Puente de hidrógeno. 2. Influencia de la estructura
JUNIO FASE GENERAL QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
Las proteínas de la dieta tras ser digeridas proporcionan los aminoácidos que utilizaremos para la síntesis de proteínas endógenas, para:
 1 CONCEPTO Las proteínas son moléculas orgánicas formadas por largas cadenas lineales, no ramificadas, de más de 70 aminoácidos (monómeros o unidades que conforman las proteínas) unidos por enlaces peptídicos.
1 CONCEPTO Las proteínas son moléculas orgánicas formadas por largas cadenas lineales, no ramificadas, de más de 70 aminoácidos (monómeros o unidades que conforman las proteínas) unidos por enlaces peptídicos.
Unidad 1 (Parte XXIII) Adición de Alcoholes a Alquenos. Adición sigue la ley de Markovnikov No presenta estéreoselectividad.
 Unidad 1 (Parte XXIII) Adición de Alcoholes a Alquenos Adición sigue la ley de Markovnikov No presenta estéreoselectividad Primera Etapa: Lic. Walter de la Roca 1 Segunda Etapa: Lic. Walter de la Roca
Unidad 1 (Parte XXIII) Adición de Alcoholes a Alquenos Adición sigue la ley de Markovnikov No presenta estéreoselectividad Primera Etapa: Lic. Walter de la Roca 1 Segunda Etapa: Lic. Walter de la Roca
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1)
 PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1) Un gas es sometido a tres procesos identificados con las letras X, Y y Z. Estos procesos son esquematizados en los gráficos que se presentan
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1) Un gas es sometido a tres procesos identificados con las letras X, Y y Z. Estos procesos son esquematizados en los gráficos que se presentan
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
Proteínas fibrosas. Alfa Queratinas Beta-Queratinas Fibroína Colágeno Elastina
 Proteínas Fibrosas La mayor parte o casi toda la proteína está organizada de manera paralela a un sólo eje Las proteínas fibrosas son generalmente fuertes mecánicamente Son generalmente insolubles Generalmente
Proteínas Fibrosas La mayor parte o casi toda la proteína está organizada de manera paralela a un sólo eje Las proteínas fibrosas son generalmente fuertes mecánicamente Son generalmente insolubles Generalmente
Lección 9: HALUROS DE ALQUILO I
 Lección 9: HALUROS DE ALQUILO I 1.Estructura y propiedades físicas. 2. Polaridad de las moléculas orgánicas: interacciones no enlazantes entre moléculas. 3. Efecto inductivo. 4. Concepto de electrófilo
Lección 9: HALUROS DE ALQUILO I 1.Estructura y propiedades físicas. 2. Polaridad de las moléculas orgánicas: interacciones no enlazantes entre moléculas. 3. Efecto inductivo. 4. Concepto de electrófilo
QUÍMICA. 2º Bachilerrato orgánica Estereoisomería:
 TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
Aminoácidos y Proteínas. Bioquímica Kinesiología UNLAM 2014
 Aminoácidos y Proteínas Bioquímica Kinesiología UNLAM 2014 Proteínas Constituyen las moléculas orgánicas más abundantes de las células (50% del peso seco). Son macromoléculas, formadas por aminoácidos
Aminoácidos y Proteínas Bioquímica Kinesiología UNLAM 2014 Proteínas Constituyen las moléculas orgánicas más abundantes de las células (50% del peso seco). Son macromoléculas, formadas por aminoácidos
Biopolímero s (4831)
 Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
Proteínas. Tabla 1: Funciones de las proteínas
 Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
TEMA 5. ESTRUCTURA Y PROPIEDADES MOLECULARES
 TEMA 5. ESTRUTURA Y PRPIEDADES MLEULARES 1. Enlaces más débiles que el enlace covalente. 1.1. Fuerzas entre dipolos. 1.2. Fuerzas de dispersión de London. 1.3. Puente de hidrógeno. 2. Influencia de la
TEMA 5. ESTRUTURA Y PRPIEDADES MLEULARES 1. Enlaces más débiles que el enlace covalente. 1.1. Fuerzas entre dipolos. 1.2. Fuerzas de dispersión de London. 1.3. Puente de hidrógeno. 2. Influencia de la
I) Biomoléculas 6) Proteínas I-6 PROTEÍNAS
 I-6 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
I-6 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
ÁCIDOS NUCLEICOS. Aguanten Gregor Mendel y los guisantes!
 ÁCIDOS NUCLEICOS Aguanten Gregor Mendel y los guisantes! ÁCIDOS NUCLEICOS caracts. grales. ADN y ARN son los mensajeros químicos de la información genética de los seres vivos. Son polímeros de nucleótidos,
ÁCIDOS NUCLEICOS Aguanten Gregor Mendel y los guisantes! ÁCIDOS NUCLEICOS caracts. grales. ADN y ARN son los mensajeros químicos de la información genética de los seres vivos. Son polímeros de nucleótidos,
B1 Estructura de los aminoácidos
 SeciÓn B AMINOÁIDOS Y PROTEÍNAS B1 Estructura de los aminoácidos Notas clave Aminoácidos Enantiómeros Los 20 aminoácidos estándar Ácidos, bases y p Amortiguadores Todas las proteínas están formadas por
SeciÓn B AMINOÁIDOS Y PROTEÍNAS B1 Estructura de los aminoácidos Notas clave Aminoácidos Enantiómeros Los 20 aminoácidos estándar Ácidos, bases y p Amortiguadores Todas las proteínas están formadas por
Repaso Opción múltiple Macromoléculas Biológicas
 Repaso Opción múltiple Macromoléculas Biológicas 1. Por qué esta información sobre el carbono es tan importante para entender las moléculas de la vida? a. Es el esqueleto de las moléculas biológicas requeridas
Repaso Opción múltiple Macromoléculas Biológicas 1. Por qué esta información sobre el carbono es tan importante para entender las moléculas de la vida? a. Es el esqueleto de las moléculas biológicas requeridas
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA ESCUELA DE CIENCIAS BASICAS TECNOLOGIA E INGENIERIA
 ESCUELA DE CIENCIAS BÁSICAS, TECNOLOGÍA E INGENIERÍA - ECBTI UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA ESCUELA DE CIENCIAS BASICAS TECNOLOGIA E INGENIERIA TEXTO OVA UNIDAD 1 201103 BIOQUÍMICA ALBERTO
ESCUELA DE CIENCIAS BÁSICAS, TECNOLOGÍA E INGENIERÍA - ECBTI UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA ESCUELA DE CIENCIAS BASICAS TECNOLOGIA E INGENIERIA TEXTO OVA UNIDAD 1 201103 BIOQUÍMICA ALBERTO
PONTIFICIA UNIVERSIDAD JAVERIANA FAC. DE CIENCIAS - DPTO. DE QUIMICA FUNDAMENTOS DE BIOLOGIA I COMPUESTOS DEL CARBONO
 PNTIFICIA UNIVERSIDAD JAVERIANA FAC. DE CIENCIAS - DPT. DE QUIMICA FUNDAMENTS DE BILGIA I CMPUESTS DEL CARBN Julio A. Pedrozo Pérez 2002 FUNCINES RGANICAS 1. Funciones oxigenadas - Alcoholes, Fenoles y
PNTIFICIA UNIVERSIDAD JAVERIANA FAC. DE CIENCIAS - DPT. DE QUIMICA FUNDAMENTS DE BILGIA I CMPUESTS DEL CARBN Julio A. Pedrozo Pérez 2002 FUNCINES RGANICAS 1. Funciones oxigenadas - Alcoholes, Fenoles y
Los principales grupos funcionales son los siguientes:
 GRUPOS FUNCIONALES Qué es un grupo funcional? Hemos visto que los hidrógenos de los hidrocarburos pueden ser sustituidos por átomos de otro metal o por un agrupamiento de átomos para obtener compuestos
GRUPOS FUNCIONALES Qué es un grupo funcional? Hemos visto que los hidrógenos de los hidrocarburos pueden ser sustituidos por átomos de otro metal o por un agrupamiento de átomos para obtener compuestos
Unidad III 3.3.Enlaces simples carbonooxigeno, 3.4.carbono -azufre, 3.5. carbono- nitrógeno
 Unidad III 3.3.Enlaces simples carbonooxigeno, 3.4.carbono -azufre, 3.5. carbono- nitrógeno Química orgánica I Químicos Escuela de vacaciones junio 2016 Licda. Jaqueline Carrera. Propiedades de los éteres
Unidad III 3.3.Enlaces simples carbonooxigeno, 3.4.carbono -azufre, 3.5. carbono- nitrógeno Química orgánica I Químicos Escuela de vacaciones junio 2016 Licda. Jaqueline Carrera. Propiedades de los éteres
Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria.
 Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria. Estructura supersecundaria Motivos Dominios Estructura terciaria Fuerzas que la estabilizan Plegamiento de proteínas
Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria. Estructura supersecundaria Motivos Dominios Estructura terciaria Fuerzas que la estabilizan Plegamiento de proteínas
ENLACES QUÍMICOS. Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos.
 1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
Ejercicios variados resueltos
 Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
2.2- FENOLES. Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH.
 2.2- FENOLES Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH. Si se sustituye un solo átomo de hidrógeno, se obtienen los fenoles; si se sustituyen
2.2- FENOLES Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH. Si se sustituye un solo átomo de hidrógeno, se obtienen los fenoles; si se sustituyen
Química orgánica. Cuarto Medio 25/06
 Química orgánica Cuarto Medio 25/06 CARBONO Es el elemento principal de las moléculas orgánicas. Debido a que este átomo, presenta una gran estabilidad. Dado que, tiene una baja tendencia a donar y quitar
Química orgánica Cuarto Medio 25/06 CARBONO Es el elemento principal de las moléculas orgánicas. Debido a que este átomo, presenta una gran estabilidad. Dado que, tiene una baja tendencia a donar y quitar
Quimica orgánica básica
 Quimica orgánica básica Química orgánica básica La química orgánica es el estudio de los compuestos de carbono. Los átomos de carbono son únicos en su habilidad de formar cadenas muy estables y anillos,
Quimica orgánica básica Química orgánica básica La química orgánica es el estudio de los compuestos de carbono. Los átomos de carbono son únicos en su habilidad de formar cadenas muy estables y anillos,
Capítulo- 14 ácidos carboxílicos, esteres, aminas y amidas 14.4 Aminas
 Capítulo- 14 ácidos carboxílicos, esteres, aminas y amidas 1 14.4 Aminas Aminas 2 Aminas Son compuestos derivados orgánicos del amoniaco, NH 3 contiene un atomo de N unido a uno o más grupos alquilo o
Capítulo- 14 ácidos carboxílicos, esteres, aminas y amidas 1 14.4 Aminas Aminas 2 Aminas Son compuestos derivados orgánicos del amoniaco, NH 3 contiene un atomo de N unido a uno o más grupos alquilo o
ORGÁNICA I. 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua.
 ORGÁNICA I 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua. 2.- Escribir y nombrar el producto principal obtenido en
ORGÁNICA I 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua. 2.- Escribir y nombrar el producto principal obtenido en
ADN, ARN E INFORMACIÓN
 ADN, ARN E INFORMACIÓN LOS ÁCIDOS NUCLEICOS Los ácidos nucleicos fueron descubiertos en 1869 por Miescher, en el pus de los vendajes de heridas, pero su papel en la herencia y control de la actividad celular
ADN, ARN E INFORMACIÓN LOS ÁCIDOS NUCLEICOS Los ácidos nucleicos fueron descubiertos en 1869 por Miescher, en el pus de los vendajes de heridas, pero su papel en la herencia y control de la actividad celular
Lección 1: GENERALIDADES
 Lección 1: GENERALIDADES 1.Concepto de Química Orgánica. Introducción histórica. 2. Estructuras de Lewis. Estructuras resonantes. 3. Geometría de las moléculas. 4. Representaciones de las moléculas orgánicas
Lección 1: GENERALIDADES 1.Concepto de Química Orgánica. Introducción histórica. 2. Estructuras de Lewis. Estructuras resonantes. 3. Geometría de las moléculas. 4. Representaciones de las moléculas orgánicas
Capítulo 2. LOS AMINOÁCIDOS, EL ENLACE PEPTÍDICO Y LA ESTRUCTURA SECUNDARIA
 Capítulo 2. LOS AMINOÁCIDOS, EL ENLACE PEPTÍDICO Y LA ESTRUCTURA SECUNDARIA Javier Sancho jsancho@unizar.es Departamento de Bioquímica y Biología Molecular y Celular & Instituto de Biocomputación y Física
Capítulo 2. LOS AMINOÁCIDOS, EL ENLACE PEPTÍDICO Y LA ESTRUCTURA SECUNDARIA Javier Sancho jsancho@unizar.es Departamento de Bioquímica y Biología Molecular y Celular & Instituto de Biocomputación y Física
2.- Enuncie los principios o reglas que controlan el llenado de los niveles de energía atómicos permitidos.
 BLOQUE PRIMERO 1.- Un compuesto contiene 85,7% de carbono y 14,3% de hidrógeno y la masa de la molécula del mismo es 42. Calcule la fórmula del compuesto sabiendo que la masa atómica del carbono. 2.- Enuncie
BLOQUE PRIMERO 1.- Un compuesto contiene 85,7% de carbono y 14,3% de hidrógeno y la masa de la molécula del mismo es 42. Calcule la fórmula del compuesto sabiendo que la masa atómica del carbono. 2.- Enuncie
Tema 5: aminoácidos y proteínas
 1. Los aminoácidos 2. Propiedades de los aminoácidos 3. El enlace peptídico 4. Estructuras 1 aria y 2 aria de las proteínas 5. Estructuras 3 aria y 4 aria de las proteínas 6. Propiedades de las proteínas
1. Los aminoácidos 2. Propiedades de los aminoácidos 3. El enlace peptídico 4. Estructuras 1 aria y 2 aria de las proteínas 5. Estructuras 3 aria y 4 aria de las proteínas 6. Propiedades de las proteínas
Química Orgánica Grupos funcionales con oxígeno o nitrógeno
 Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Práctica 6. Propiedades físicas y enlace químico
 Práctica 6. Propiedades físicas y enlace químico Revisaron: M. en C. Martha Magdalena Flores Leonar Dr. Víctor Manuel Ugalde Saldívar PREGUNTA A RESPONDER AL FINAL DE LA PRÁCTICA Qué tipo de enlace predomina
Práctica 6. Propiedades físicas y enlace químico Revisaron: M. en C. Martha Magdalena Flores Leonar Dr. Víctor Manuel Ugalde Saldívar PREGUNTA A RESPONDER AL FINAL DE LA PRÁCTICA Qué tipo de enlace predomina
UNIVERSIDAD NACIONAL DEL CALLAO FACULTAD DE INGENIERIA QUIMICA AÑO 2009 AMINAS AROMATICAS
 AMINAS AROMATICAS I. OBJETIVOS Identificación de la anilina. Reconocimiento de la anilina con las diferentes pruebas. II. FUNDAMENTO TEORICO Amina, nombre que reciben los compuestos producidos a menudo
AMINAS AROMATICAS I. OBJETIVOS Identificación de la anilina. Reconocimiento de la anilina con las diferentes pruebas. II. FUNDAMENTO TEORICO Amina, nombre que reciben los compuestos producidos a menudo
QUÍMICA ORGÁNICA BÁSICA
 QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
Hibridación de orbitales.
 Hibridación de orbitales. REACCIONES ORGANICAS Las formas características de enlace del átomo de carbono en los compuestos orgánicos se describe frecuentemente de acuerdo con el modelo de hibridación de
Hibridación de orbitales. REACCIONES ORGANICAS Las formas características de enlace del átomo de carbono en los compuestos orgánicos se describe frecuentemente de acuerdo con el modelo de hibridación de
Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento, conteste las siguientes preguntas.
 EXPERIMENTO 5 ALDEHIDOS Y CETONAS Fecha: Sección de laboratorio: Nombre del estudiante: Grupo #: Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento, conteste las
EXPERIMENTO 5 ALDEHIDOS Y CETONAS Fecha: Sección de laboratorio: Nombre del estudiante: Grupo #: Preguntas de preparación para el laboratorio. Después de leer cuidadosamente el experimento, conteste las
A M I N O Á C I D O S
 A M I N O Á C I D O S Qué son? Son componentes básicos, estructurales o funcionales de los pép-dos y las proteínas. Presentan: un grupo carboxilo COOH (ácido) y un grupo amino NH2 (básico) Todos los aminoácidos
A M I N O Á C I D O S Qué son? Son componentes básicos, estructurales o funcionales de los pép-dos y las proteínas. Presentan: un grupo carboxilo COOH (ácido) y un grupo amino NH2 (básico) Todos los aminoácidos
