Universidad de El Salvador Nuevo Ingreso 2007 Facultad de Ciencias Naturales y Matemática Lic. Martín Peña
|
|
|
- Nieves Luna Castilla
- hace 8 años
- Vistas:
Transcripción
1 TEMPERATURA La temperatura de un cuerpo es una medida de su estado relativo de calentamiento o enfriamiento, cuando tocamos un cuerpo, nuestro sentido del tacto nos permite hacer una estimación del grado de calentamiento o enfriamiento del cuerpo con respecto a la parte de nuestra piel que está en contacto con dicho cuerpo. Esta estimación del tacto es demasiado limitada e imprecisa para ser de algún valor en los trabajos técnicos y científicos. Temperatura y energía cinética promedio de las moléculas o átomos de un gas. La temperatura no es una medida de "calor en el cuerpo", la temperatura es una magnitud física que nos indica cuantitativamente, el estado de "caliente" o "frío" de un cuerpo, se expresa mediante un número asociado convencionalmente al cuerpo. Realmente, en la actualidad la temperatura se considera como una medida de la mayor o menor agitación de las moléculas o átomos que constituyen un cuerpo. Para cuantificarla se relaciona la energía cinética promedio de las moléculas, de modo que una temperatura elevada corresponde una mayor energía cinética promedio de las moléculas, debido a una mayor agitación molecular. Esta relación se expresa de la siguiente manera: Tα E c La temperatura es directamente proporcional a la energía cinética media de traslación de las moléculas. La ecuación resultante es deducida de la teoría cinética de los gases, demostrándose que: 2 T= ( 3 1 )Ec K (1) En donde K es la constante de Boltzman e igual a K = 1.38 x J/ ( K molécula) PROPIEDADES TERMOMÉTRICAS DE LA MATERIA. Para medir la temperatura tenemos que hacer uso de alguna propiedad física medible, que varíe continua y sensiblemente con aquella (razón por la cual a dicha propiedad se le llama TERMOMETRICA) por ejemplo: El volumen, la resistencia eléctrica, la presión, la longitud, etc. TERMOMETRÍA. Tipos de termómetros: Termómetro es cualquier instrumento que se utiliza para medir la temperatura.
2 a) El termómetro de líquido: (puede ser mercurio o alcohol) encerrado en un tubo delgado de vidrio. La propiedad termométrica utilizada es el volumen (V) del líquido cuyo cambio, en los casos en que el área transversal del tubo es constante, resulta directamente proporcional con el cambio de longitud de la columna del líquido dentro del tubo. A su vez, ese cambio de volumen cumple una proporcionalidad directa con el cambio de temperatura ( ΔT ) del líquido. b) El termómetro de resistencia: La propiedad termométrica es la resistencia eléctrica de una pequeña bobina de hilo; el cambio de resistencia ( Δ R ) resulta directamente proporcional al cambio de temperatura ( Δ T ) del hilo. c) El termómetro de Par termoeléctrico: En el que la propiedad termoeléctrica es el voltaje producido por la diferencia de temperatura que tenga la soldadura de dos hilos de diferente metal. Escalas termométricas: Para convertir estos instrumentos en instrumentos cuantitativos es necesario introducir una escala de temperatura, y para ello se precisa disponer de un convenio internacional respecto a su calibración. Para definir una escala se eligen dos temperaturas de referencia, llamadas PUNTOS FIJOS, y se asignan valores arbitrarios a dichas temperaturas, fijando así la posición del punto cero y el tamaño de la unidad de temperatura. Una de las temperaturas de referencia, es el punto de fusión del hielo, bajo presión de una atmósfera. La otra temperatura de referencia es el punto de ebullición del agua a la presión de una atmósfera. LA ESCALA CENTIGRADA O CELSIUS: Selecciona el punto de fusión del hielo como 0 C, y el punto de ebullición del agua, como 100 C. En la escala absoluta Kelvin, estas temperaturas son K y K respectivamente y en la escala FAHRENHEIT corresponde a los valores 32 F y 212 F. Las relaciones entre estas escalas termométricas son: 5 T ( C) = [ T( F) 32] (2) 9 T ( K) = T ( C) (escala de temperatura absoluta) (3) En donde: T( C) es la temperatura en grados Celsius o centígrados. T( F) es la temperatura en grados Farenheit. T( K) es la temperatura en grados Kelvin. NOTA: Actualmente, a un grado Kelvin ( K) sólo se le llama 1 Kelvin y se simboliza únicamente por K. Energía interna La energía interna de un sistema, es el resultado de la energía cinética de las moléculas o átomos que lo constituyen, de sus energías de rotación y vibración, 2
3 además de la energía potencial intermolecular debida a las fuerzas de tipo gravitatorio, electromagnético y nuclear, que constituyen conjuntamente las interacciones fundamentales. Al aumentar la temperatura de un sistema, sin que varíe nada más, aumenta su energía interna. Convencionalmente, cuando se produce una variación de la energía interna sin que se modifique la composición química del sistema, se habla de variación de la energía interna sensible. Si se produce alteración de la estructura atómica-molecular, como es el caso de las reacciones químicas, se habla de variación de la energía interna química. Finalmente, en las reacciones de fisión y fusión se habla de energía interna nuclear. En todo sistema aislado (que no puede intercambiar energía con el exterior), la energía interna se conserva (Primer Principio de la Termodinámica). CALOR (Q). CONCEPTO DE CALOR Y SUS UNIDADES. El calor es energía en tránsito, cuando la transferencia de un cuerpo a otro sucede por medios no mecánicos, a causa de la diferencia de temperatura entre los cuerpos. El concepto de calor es similar al concepto de trabajo tomado éste como la medida de la energía que es transferida mediante un proceso mecánico. Debe distinguirse con precisión entre calor como forma de energía en tránsito y energía térmica (llamada energía interna) como propiedad del sistema, ya que no todo el calor transferido a un sistema se convierte necesariamente en energía térmica o interna. Algo de él puede quedar en forma de energía potencial o energía química. Por lo tanto, un sistema (que es cualquier conjunto de cuerpos que aislamos idealmente del universo) no puede contener calor, al igual que no puede contener trabajo. Sólo puede contener energía de varios tipos, incluida la energía térmica o interna. La cantidad de calor (Q) se mide por los efectos observables que produce, el más palpable de los cuales es la elevación de temperatura del cuerpo que recibe la energía. Si un gramo de agua recibe una cantidad de calor (Q) de modo que cambia su temperatura de 14.5 C a 15.5 C se llama a esta cantidad de calor, caloría, que es la unidad calor del sistema CGS. La kilocaloría se define análogamente para un kilogramo de agua, siendo la unidad de calor del sistema MKS. La unidad de calor del sistema inglés es la BTU (Unidad Térmica Británica) y es la cantidad de calor que es necesario suministrar a una libra de agua para elevar su temperatura de 63 F a 64 F. Equivalencias: 1 BTU = 252 Cal. = Kcal. La equivalencia entre las unidades de calor y las unidades de energía se conoce con el nombre de Equivalencia Mecánico del Calor, que fue determinado por Joule. 3
4 Los mejores resultados hasta la fecha dan esa equivalencia así: joules = 1 caloría.. Capacidad calorífica y calor específico. Las sustancias difieren entre sí en la cantidad de calor necesaria para producir una elevación determinada de temperatura sobre una masa dada. La razón entre la cantidad de calor suministrada a un cuerpo y el correspondiente incremento de temperatura (Δ T) se denomina Capacidad Calorífica del Cuerpo. Capacidad Calorífica = Cantidad de calor Incremento de Temperatura C = Q ΔT = Calorías C ó BTU F ó Caloría K (4) Para obtener un valor que sea característico de la sustancia de que está hecho el cuerpo, se define el calor específico de una sustancia (c) como la capacidad calorífica por unidad de masa de un cuerpo formado por dicha sustancia; esto es la cantidad de calor que hay que suministrar a la unidad de masa para elevar su temperatura en un grado. Calor Específico = CapacidadCalorífica Masa c = C m Q = m ΔT Q = mδt Cal BTU = ó (5) o g C Lb F De la ecuación anterior se deduce que el calor que ha de suministrarse a un cuerpo de masa m, cuyo valor específico es "c", para aumentar su temperatura en ΔT, es: Q = mcδt = mc (T f T i ). (6) Equilibrio Térmico: Si se tienen dos cuerpos A y B a temperaturas diferentes y aislados de los alrededores, al ponerlos en contacto se establecerá entre ellos un flujo de calor del objeto de mayor temperatura al de menor. El flujo de calor cesará cuando ambos alcancen una temperatura común, denominada temperatura de equilibrio. Se 4
5 dice que los objetos han alcanzado el equilibrio térmico. Como solamente se ha verificado intercambio de calor, se cumple que: Calor ganado por el cuerpo = -Calor cedido por el cuerpo. de menor temperatura de mayor temperatura Q A = - Q B M A c A ΔT A = -m B c B ΔT B (7) Calor latente. A T 1 B T 2 La materia puede existir en varios estados de agregación, entre estos los más comunes son: Sólido, Líquido y Gaseoso. Los cambios de un estado a otro van acompañados de un desprendimiento o una absorción de calor. El calor que necesita la unidad de masa de una sustancia para que pueda cambiar su estado se denomina Calor Latente y se representa simbólicamente por L. Dependiendo del cambio de estado que se realice, se puede tener calor latente de fusión L f, de solidificación L s, de vaporización L v, de condensación o licuefacción L l. El calor absorbido o liberado en el cambio de estado de una masa es: Q = ml. (8) DILATACION Todo cuerpo, por efectos del calor que recibe sufre algunos efectos, uno de ellos es la dilatación, que se produce en todas las dimensiones que posee. Según su naturaleza cada cuerpo posee lo que se llama coeficiente de dilatación térmica, cuyo símbolo es α y su unidad de medida es 1/ C o C -1, algunos valores son: Alumínio 0, Cobre 0, Acero 0, Vidrio 0, a 0, Hormigón 0, a 0, Mercurio 0, A) DILATACION LINEAL Para determinar la dilatación lineal de un cuerpo se tiene la relación donde Δ t = t f - t i l f = l i (1 + αδ t), (9) 5
6 B) DILATACION SUPERFICIAL Si se tiene una superficie de tamaño A o a una temperatura t i, al entregársele (o quitársele) un calor Q, de tal forma que su nueva temperatura sea t f, su nuevo tamaño estará expresado por A f, donde Δ t = t f - t i es la variación de temperatura que experimenta;δ A es su variación de superficie; Δa y Δb las variaciones respectivas en sus dimensiones, (estas variaciones son respecto a la figura con que se trabaja, pues si fuera un círculo, la variación sería en el radio). La relación entre las superficies A o y A f es A f = A o (1 + β Δ t) (10) Donde el coeficiente de dilatación superficial es β = 2α, siendo α el coeficiente lineal de la sustancia de la que es el objeto superficial. C) DILATACION VOLUMETRICA: Si se tiene una volumen de tamaño V o a una temperatura t i, al entregársele (o quitársele) un calor Q, de tal forma que su nueva temperatura sea t f, su nuevo tamaño estará expresado por V f, donde Δ t = t f - t i es la variación de temperatura que experimenta; Δ V es su variación de volumen; Δ a, Δb y Δc las variaciones respectivas en sus dimensiones, (estas variaciones son respecto a la figura con que se trabaja; pues si fuera una esfera, la variación sería en el radio o, si fuera un cilindro las variaciones serían en el radio y en la altura, depende de la situación!). La relación entre lo volúmenes es V o y V f es V f = V o (1 + γ Δ t) (11) Donde el coeficiente de dilatación volumétrico es γ= 3α, siendo α el coeficiente lineal de la sustancia de la que es el objeto volumétrico. Mecanismos de propagación de calor. Existen tres mecanismos mediante los cuales puede transferirse calor de un lugar a otro; ellos son: conducción, convección y radiación. Conducción. La conducción es la transferencia de calor, sin que se produzca transferencia de materia o movimiento del cuerpo a través del cual se transmite la energía. Así por ejemplo, si uno de los extremos de una cuchara metálica se introduce en un líquido caliente, el otro extremo se calienta por conducción. 6
7 En el proceso de conducción, la energía se transmite por choques a nivel molecular o atómico. La velocidad de conducción del calor varía de una sustancia a otra; generalmente los metales son buenos conductores de calor, otros como la madera, el ladrillo, asbesto, etc. son malos conductores o buenos aisladores. Considerando una lámina delgada de cierto material: sea A el área de sus caras paralelas, Δ X el espesor. Si las caras se mantienen a temperaturas distintas T 1 y T 2 habrá un flujo de calor (Q) de una cara a otra. T 2 - T 1 = Δ T: DIFERENCIA DE TEMPERATURA; Δ X ESPESOR. Δx Δ T/ Δ X = Gradiente de temperatura (dirección en la cual se obtiene el máximo o mínimo aumento de temperatura). T 1 T 2 T 1 > T 2 En estado estacionario, fluye calor desde la zona a temperatura más alta a la más baja. La ley de Fourier de la conducción térmica establece que el ritmo de flujo de calor: Q calor = Δt tiempo es proporcional con el área A de la sección transversal y con el gradiente de temperatura. En símbolos: H = Q Δ = KA T Δt ΔX (12) Donde K es la constante de proporcionalidad y se conoce como conductividad térmica del material, y Δ T es el tiempo en que ocurre el flujo de calor. El signo menos indica que el calor fluye en el sentido en que la temperatura disminuye. Algunos valores típicos de K: SUSTANCIA K (Cal/s cm. C) Agua Aire (a 0 C) Cobre
8 Hielo Grasa animal Piel humana Convección. Este tipo de transferencia de calor se manifiesta sólo en los fluidos y ocurre cuando el fluido experimenta movimiento. Esto se debe a que cuando una porción del fluido se calienta, se dilata, su densidad disminuye en relación con el resto del fluido; así el fluido caliente sube y las regiones de fluido frío descienden. Se establece así un movimiento del fluido o corrientes de convección. Si tales corrientes son originadas por la diferencia de densidad, se denomina al proceso convección natural; pero si el movimiento del fluido se incrementa por medios mecánicos (ventilador, bomba, etc.) el proceso de convección es forzada. En estas circunstancias, el calor cedido por unidad de tiempo por un cuerpo de temperatura T 1 en un ambiente de temperatura T 2 es: H = ha (T 1 -T 2 ) (13) Donde A es el área superficial y h es una constante, que en el caso del cuerpo humano rodeado de aire vale h = 1.7 x 10-3 Kcal.s -1 m -2 Kg -1 Radiación El término radiación se refiere a la energía que los cuerpos emiten en forma de ondas electromagnéticas (como la luz). Cuando las longitudes de onda se encuentran en el intervalo comprendido entre 1 um y 100 um, aproximadamente, se denomina radiación térmica o radiación infraroja. Dos cuerpos cualquiera A y B intercambiarán de energía en forma de radiación térmica, incluso cuando no hay posibilidad de que intervenga conducción o convección. La radiación térmica se propaga en el vacío y viaja a la velocidad de la luz. Algunas sustancias permiten el paso de estas radiaciones, pero absorben parte de la energía transmitida. Se define el poder emisivo total de un cuerpo como la energía radiante total de todas las longitudes de onda emitidas por el cuerpo por metro cuadrado de superficie y por segundo. Para un cuerpo negro (el mejor receptor posible, que absorbe toda la energía en forma de radiación que incide sobre el) el poder emisivo total, que se escribe es proporcional a la cuarta potencia de la temperatura absoluta (T) ξ c = σ T 4 (14) Esta es la ley de la radiación de Stefan - Boltzman, y σ es una constante universal denominada constante de Stefan -Boltzman, su valor es: σ = 5.67 x 10-8 W/m 2 K 4 El poder emisivo de cualquier otro cuerpo es una fracción de esto, 8
9 ξ c = εσ T 4 =R (15) En donde ε es llamada emisividad del cuerpo, y mide la eficiencia del cuerpo como emisor de radiación. En términos de la potencia radiada por una superficie de área A, la ecuación resulta: Dado que P = σ ε AT 4 (16) ξ = ξε = P / AΔt (energía radiada en cada unidad de tiempo por el área). La radiación de un cuerpo se produce, haya o no diferencia de temperatura entre el cuerpo y el medio que lo rodea. Si no existe diferencia de temperatura, entonces el cuerpo está absorbiendo exactamente la misma radiación que emite y no hay flujo neto de energía hacia el exterior ni hacia el interior. Sin embargo, si un cuerpo a la temperatura T está dentro de una envoltura T 0, es menor que T, la energía emitida es mayor que la absorbida y el flujo neto hacia fuera es: ε neto = εot εot = εo(t T0 ) (17) por unidad de área por segundo. Termodinámica La termodinámica puede definirse como el tema de la Física que estudia los procesos en los que se transfiere energía como calor y como trabajo. Sabemos que se efectúa trabajo cuando la energía se transfiere de un cuerpo a otro por medios mecánicos. El calor es una transferencia de energía de un cuerpo a un segundo cuerpo que está a menor temperatura. O sea, el calor es muy semejante al trabajo. Al hablar de termodinámica, con frecuencia se usa el término "sistema". Por sistema se entiende un objeto o conjunto de objetos que deseamos considerar. El resto, lo demás en el Universo, que no pertenece al sistema, se conoce como su "ambiente". Se consideran varios tipos de sistemas. En un sistema cerrado no entra ni sale masa, contrariamente a los sistemas abiertos donde sí puede entrar o salir masa. Un sistema cerrado es aislado si no pasa energía en cualquiera de sus formas por sus fronteras. Primera Ley de la Termodinámica Esta ley se expresa como: ΔE int = Q - W (18) Cambio en la energía interna en el sistema = Calor agregado (Q) - Trabajo efectuado por el sistema (W) 4 9
10 Notar que el signo menos en el lado derecho de la ecuación se debe justamente a que W se define como el trabajo efectuado por el sistema. Para entender esta ley, es útil imaginar un gas encerrado en un cilindro, una de cuyas tapas es un émbolo móvil y que mediante un mechero podemos agregarle calor. El cambio en la energía interna del gas estará dado por la diferencia entre el calor agregado y el trabajo que el gas hace al levantar el émbolo contra la presión atmosférica. Segunda Ley de la Termodinámica La primera ley nos dice que la energía se conserva. Sin embargo, podemos imaginar muchos procesos en que se conserve la energía, pero que realmente no ocurren en la naturaleza. Si se acerca un objeto caliente a uno frío, el calor pasa del caliente al frío y nunca al revés. Si pensamos que puede ser al revés, se seguiría conservando la energía y se cumpliría la primera ley. En la naturaleza hay procesos que suceden, pero cuyos procesos inversos no. Para explicar esta falta de reversibilidad se formuló la segunda ley de la termodinamica, que tiene dos enunciados equivalentes: Enunciado de Kelvin - Planck : Es imposible construir una máquina térmica que, operando en un ciclo, no produzca otro efecto que la absorción de energía desde un depósito y la realización de una cantidad igual de trabajo. Enunciado de Clausius: Es imposible construir una máquina cíclica cuyo único efecto sea la transferencia continua de energía de un objeto a otro de mayor temperatura sin la entrada de energía por trabajo. PROBLEMAS RESUELTOS 1) Transformar 175 K a grados centígrados. De la ec. 3 tenemos que: T( 0 C)= T(K)-273 T( 0 C)= =-98 0 C 2) A qué temperatura Celsius equivalen 33,8 F? De la ec. 2 tenemos que: 5 T ( C) = [ T( F) 32] 9 5 T ( C) = [ ] =1 0 C 9 10
11 3) Transformar 30 C a grados Fahrenheit. Despejando T( 0 F) de la ec. Anterior T T = 9 = ( F ) = T ( C) ( = F ) = ( 30) =86 0 C 4) Cuánto vale la energía cinética de las partículas de un gas que se encuentra a 40 0 C? De la ec. 1 y teniendo en cuenta que 60 0 C=333K y K = 1.38 x J/ ( K molécula) J E 3 C 1.38X10 23 = K E C =6.89X10-21 J ( K ) 3 E C = 2 kt 5) En un bloque de Hormigón de masa M=2 Kg a temperatura inicial T=40ºC y calor específico Ce=0.2 Kcal/Kg.ºC se introduce en un litro de Agua de masa M=1 Kg a temperatura T=20ºC y calor específico Ce=1.0 Kcal/Kg.ºC. Calcula la temperatura final Tf de equilibrio. Variación de la cantidad de calor de un cuerpo Q: Q = mcδt = mc (T f T i ). (6) Hormigón: Qh = (2Kg)( 0.2 Kcal/Kg.ºC) (Tf 40º C) = 0.4 (Tf 40ºC) [Kcal]/ ºC Agua: Qa = (1Kg)(1.0 Kcal/Kg.ºC) (Tf 20ºC) = 1.0 (Tf 20º) [Kcal]/ ºC La temperatura final Tf tendrá un valor intermedio ente 20º y 40º. El calor que pierde el hormigón (observar su valor negativo) será igual al ganado por el agua (valor positivo). Si sumamos ambas ecuaciones: Qh + Qa = 0 Hormigón+ agua: 0 = 0.4Kcal/ ºC (Tf 40.ºC) + Kcal/ ºC (Tf-20.ºC) 0 = 0.4Tf Kcal/ ºC 16Kcal + TfKcal]/ ºC 20Kcal 0 = 1.4TfKcal/ ºC 36Kcal 11
12 Despejando la Temperatura final 1.4 Tf Kcal]/ ºC = 36Kcal Tf = 36 / 1.4 = 25,71ºC Una vez hallada la temperatura final de equilibrio Tf = 25.71ºC, es fácil comprobar la cantidad de calor Q perdida (-) por el hormigón y ganada (+) por el agua: Hormigón: Qh = 0.4 ( º) = [Kcal] Agua: Qa = 1.0 ( º) = [Kcal] 6) Una masa de 250gr de agua se encuentra a 1 atmósfera de presión a 150ºC. Cuántas calorías es necesario extraer para llegar a una temperatura final de -20ºC? Recordando que: Q = mcδt Con: c=1cal/g 0 C, m=250g y ΔT=T f -T i =-20 0 C C= C Q= (250g)(1cal/g 0 C)( C) Q= cal = -42.5Kcal El signo indica que es calor perdido 7) Calcular el calor específico del mercurio si se introducen 0,2 kg del mismo a 59 C en un calorímetro con 0,37 kg de agua a 24 C y la temperatura de equilibrio térmico es de 24,7 C. Teniendo en cuenta que: Donde: Q a = - Q Hg Q Hg = m Hg c Hg ΔT=(0.2Kg)( ) 0 Cc Hg =(-6.86Kg 0 C) c Hg Q a =m a c a ΔT=(0.37Kg)(1Kcal/ 0 C)( ) 0 C=0.259 Kg 0 C(Kcal/ 0 C) Por tanto: Kg 0 C(Kcal/ 0 C)=- (-6.86Kg 0 C) c Hg c Hg = Kcal/ 0 C/6.86=0.038 Kcal/ 0 C 8) Convertir 1800J a calorías y Kcal. Recordando que 1cal=4.186J y 1Kcal=1000cal tenemos: 1cal 1800 J = 430cal = Kcal 4.186J 12
13 9) Un trozo de hielo de 583 cm 3 a 0 ºC se calienta y se convierte en agua a 4 ºC. Calcular la transferencia de calor durante el proceso Datos: densidad del hielo gr/cm 3, calor específico del agua 1 cal/g 0 C, calor de fusión del hielo 80 cal/g. Recordando que la densidad es masa entre volumen tenemos que: m=ρv m= (0.917g/cm 3 )(583cm 3 )=534.6g Para pasar de hielo a agua a 0 0 C se debe suministrar una cantidad de calor dada por: Q f =ml f Q f = (534.6g)( 80 cal/g)=42768cal Para pasar de agua a 0 ºC a agua a 4 ºC se debe agregar Q= mcδt=(534.6g)( 1 cal/g 0 C)( 4 ºC-0 ºC)=2138.4cal El calor total durante el proceso será Q T =Q f +Q= cal 10) Qué cantidad de calor absorberá un litro de agua que está a 100 C y a presión normal para vaporizarse totalmente? 1Litro =1000ml=1000cm 3, m=ρv=(1g/cm 3 )(1000cm 3 )=1000g L V = 540 cal/g Q= ml V =(1000g)( 540 cal/g)=540000cal=540kcal 11) Qué cantidad de aluminio se podrá fundir con 20 kcal si aquel está a temperatura de fusión? L f 1660cal/g m=q/l f m=20000cal/(1660cal/g)=12.04g 12) Una cinta métrica de acero (α = 0,000012/ C) es exacta a 0 C. Se efectúa una medición de 50 m un día en que la temperatura es de 32 C. Cuál es su verdadero valor? Utilizando la relación (9) para encontrar la longitud original tenemos: l f = l i (1 + αδ t) Lf li = 1+ αδt = 1+ 50m ( C ) 32 C = m 13
14 13) Cuál será la longitud que alcanza un alambre de hierro (α = 0,000012/ C) de 250 m, si sufre un aumento de temperatura de 60 C? Utilizando: l f = l i (1 + αδ t) Tenemos: L f =250m (1+ ( C -1 ) (60 0 C))=250.18m 14) Se corta un orificio con un área de sección transversal de cm 2 en un trozo de acero a 20 0 C. Cuál es el área del agujero si el acero se calienta de 20 0 C a C? El incremento en el área del orificio esta dado por: ΔA=γA 0 ΔT=2αA 0 ΔT=2(0,000012/ C)(100cm 2 )(80 0 C)=0.19cm 2 Por tanto el orificio a C es: A f =A 0 +ΔA=100.19cm 2 15) Una esfera de bronce de 33,5 cm 3 de volumen sufre un aumento de temperatura de 45 C, cuál será el aumento de volumen experimentado, si el coeficiente de dilatación lineal del bronce es de 0, / C? Se busca ΔV teniendo en cuenta que V i =33.5cm 3 De la relacion (11) tenemos: V f = V o (1 + γ Δ t) Y con γ= 3α, siendo α el coeficiente lineal de la sustancia V f =(33.5cm 3 )(1+( / C)(45 0 C))=33.57cm 3 ΔV=0.07cm 3 16) Un anillo de cobre tiene un diámetro interno de 3,98 cm a 20 C. A qué temperatura debe ser calentado para que encaje perfectamente en un eje de 4 cm de diámetro? Sabiendo que: α cobre = 17X10-6 1/ C. Teniendo en cuenta que: T i =20 0 C De la relación (9) y teniendo en cuenta que ΔT=T f -T i, despejamos T f l f = l i (1 + αδ t), 14
15 l f 1 li + Ti α = T f T f 4cm 1 0 = 20 C cm = C ) El ambiente de una caldera está separado de otro por una pared de corcho (k = 0,0001 cal/cm. C.s) de 6 cm de espesor y 2,5 m 2 de superficie y 60 0 C de diferencia de temperatura entre ambas paredes. Qué cantidad de calor ha pasado en 2,5 horas de uno a otro medio? De la ec.12. H = Q Δ = KA T Δt ΔX K= cal/cm. C.s A=2.5X10 4 cm 2 ΔT Q= KA Δt ΔX Q= 2250cal cal 0 60 C cm s C 0.06m 2 ( ) ( ) ΔT=60 0 Q= m 9000s 0 C ΔX=6cm Δt=2.5h=9000s 18) Un estudiante decide que ropa debe ponerse. El aire en su recamara esta a C. Si la temperatura de la piel del estudiante sin ropa es de C, cuánto calor pierde su cuerpo en 10.0min?suponga que la emisividad de la piel es de y que el área de la superficie del cuerpo del estudiante es 1.50m 2. De acuerdo con la relación (14) ε neto = ε neto 4 4 = AεoT AεoT = εo( T 4 T 2 8 W 4 ( 1.5m ) ( 0.900)( 310K ) ( 298K ) m 2 K ) 4 ( ) 15
16 ε neto = 143 j s Q = ε neto t j = 143 s 4 ( 600s) = J 19) Un gas esta encerrado en un recipiente dotado de un émbolo con un área de sección transversal de 0.10m 2. La presión del gas se mantiene a 8000Pa mientras se aporta calor poco a poco; en consecuencia, el gas empuja el émbolo una distancia de 4cm.(Cualquier proceso en el que la presión permanece constante se conoce como proceso isobárico)si se agregan 42J de calor al sistema durante la expansión, cuál es el cambio de energía interna del sistema? De la ec. 18. ΔE int = Q - W El trabajo realizado por el gas es: W=PΔV = ( m N ) (0.10m 2 ) (0.04m)=32J Por tanto el cambio de energía interna se calcula como: ΔE int = 42J -32J=10J 20) Un gramo de agua a la presión atmosférica (1.013X10 5 Pa) ocupa un volumen de 1.0cm 3.Cuando esta agua hierve, se convierte en 1671cm 3 de vapor de agua. Calcule el cambio de energía interna en este proceso. Para el agua el calor latente L=2.26X10 6 J/Kg Para evaporar 1.0cm 3 =1g (recordando que m=ρv) se necesita una cantidad de calor dado por: Q = ml. Q=(0.001Kg)( 2.26X10 6 J/Kg)=2260J El trabajo realizado se encuentra con la relación: W=PΔV=P(V vapor -V liquido ) Por tanto el cambio de energia interna es W=(1.013X10 5 N/m 2 )((1671)-(1))X10-6 m 3 =169J 16
17 : ΔE int = Q W=2260J-169J=20091J Ejercicios propuestos: Algunos ejercicios tienen respuestas y en otros hay que buscar el valor de las constantes físicas. 1) Transformar 175 K a grados centígrados. R/ -98 C 2) A qué temperatura Celsius equivalen 33,8 F? R/ 1 C 3) Convertir -40 C a Fahrenheit. R/ -40 F 4) A qué temperatura Celsius equivalen 33,8 F?. R/1 C 5) En un termómetro Fahrenheit se observa una marca de 125 F y en un Celsius se leen 45 C, cuál de los dos indica mayor estado térmico?. R/ el termómetro Fahrenheit 6) Cuánto calor debe absorber un cuerpo de 200 gr para aumentar su temperatura en 10 grados Celsius? (Ce = 2 cal (g ºC)-1) R/4000cal 7) Cuánto calor debe absorber un cuerpo de 200 gr para aumentar su temperatura en 10 grados Kelvin? (Ce = 2 cal (g ºC)-1) R/4000cal 8) Qué cantidad de calor cederá 1 kg de mercurio que está a 25 C para pasar a sólido? (Ts Hg =-38,87 C, Ls=-2.8Kcal/Kg,Ce=0,139J/g C) R/4,087 kcal 17
18 9) Qué cantidad de calor absorberá un litro de agua que está a 18 C y a presión normal para vaporizarse totalmente?(tv=100 0 C, Lv=540cal/g) R/ 622 kcal 19) Calcular la cantidad de cinc que se podrá fundir con 18 kcal. R/ 782,2 g 10) Se desea fundir 200 g de cinc que está a 22 C y se entregan 25 kcal. Se fundirá totalmente?, qué masa de cinc faltará fundir?(tf=420 0 C, Lf=23kcal/Kg, Ce=0.0915Kcal/Kg 0 C) 11) Qué cantidad de calor absorbe una masa de hielo de 200 kg que está a 0 C para fundirse totalmente?(lf=80kcal/kg) R/ kcal 12) Calcular la cantidad de calor que absorberá 200 g de hielo que está a -8 C para pasar a agua a 20 C. R/ 20,8 kcal 13) Si 300 g de agua (cv = 540 cal/g) están a 100 C y presión normal, qué cantidad de calor será necesaria para vaporizarlos?. R/162 kcal 14) Qué cantidad de aluminio se podrá fundir con 20 kcal si aquel está a temperatura de fusión? (Lf=92.7cal/g) R/217 g 15) Se tiene una barra de cobre de 800 g que está a 18 C, se fundirá totalmente si se le entregan 80 kcal? (Lf=51.1cal/g,Ce=0.093 cal/g ºC,Tf= C) R/no 16) Qué masa de cobre se habrá fundido en el caso del problema anterior? R/ ) La longitud de una barra de hierro (α= 0, / C) a 35 C es de 1,8 m. Si se calienta hasta 380 C, cuál es el aumento de longitud que experimentó? R/0.0073m 18) Se tienen dos varillas de acero (α = 0,000012/ C). La primera tiene exactamente un metro de longitud a los 0 C y la otra a los 30 C. Cuál será la diferencia de longitudes a los 18 C? R/0.036m 18
19 19) Cuál será el coeficiente de dilatación del cobre, si un hilo de ese metal, de 140 m de largo y a 0 C, al ser calentado a 350 C adquiere una longitud de 140,8673 m? R/ C -1 20) Un cubo de hierro (α = 0,000012/ C) lleno de mercurio (α = 0,000182/ C)es calentado de 20 C a 70 C. Si se derraman 2,7 cm 3 de mercurio, cuál es el volumen del cubo? R/9.9cm 3 21) Calcular la longitud a 0 C de un hilo de cobre que a 120 C tiene una longitud de 1200 m. R/1197.5m 22) El volumen de una esfera de plomo a 20 C es de 5 cm 3. Si se calienta a 80 C, cuál será el aumento de volumen? (α=3x C -1 ) R/0.027cm 3 23) Una masa de plomo se calienta de 20 C a 140 C. Qué aumento de volumen se verificará? R/ρ/m(3αΔT) 24) Una persona desvestida tiene una superficie de 1,5 m2 expuesta a un ambiente y a unos alrededores de 27 ºC. La temperatura de su piel es de 33 ºC y se puede considerar un emisor de radiación perfecto. Si el coeficiente de transferencia de calor por convección es de 9 W/m2 K, hállese: a) Las pérdidas de calor por convección y por radiación. b) El gasto energético en kcal/día. Cuestionario Las preguntas van seguidas por cuatro respuestas posibles de las cuales una es la correcta. Señalar con una X la respuesta que Ud. considere correcta. 1) Se dice que dos cuerpos están a la misma temperatura, cuando: a) ambos tienen la misma cantidad de calor b) la energía total de las moléculas de uno es igual a la energía total de las moléculas del otro c) ambos ganan calor en la misma proporción d) al ponerse en contacto no se transfiere calor. 2) Cuando se mide la temperatura de una persona que tiene fiebre es conveniente esperar algunos minutos para que: a) el calor que absorbe el termómetro sea igual al que absorbe el enfermo 19
20 b) el calor que cede el termómetro sea igual al que cede el enfermo c) el calor que absorbe el termómetro sea mayor al que cede el enfermo d) el termómetro llegue al equilibrio térmico con el cuerpo del enfermo. 3) Suponga una masa de hielo a 0 ºC que se encuentra dentro de un recipiente aislado que contiene agua también a 0 ºC. Qué le sucederá en este caso? a) nada b) todo el hielo se funde c) sólo una parte del hielo se funde d) toda el agua se congela. 4) Un globo con aire en su interior y con su válvula amarrada se encuentra expuesto al Sol. Después de cierto tiempo se obseva que el volumen del globo ha aumentado. Lo anterior es una evidencia de que: a) ha ingresado aire al interior del globo b) el aire aumentó su temperatura y se dilató c) la goma del globo hace menor fuerza para mantener al aire en su interior d) aumentó la masa del globo. 5) El calor que se necesita entregarle a 2 litros de agua para eleve su temperatura desde 20 ºC a 60 ºC es: a) 80 cal b) cal c) cal d) cal. 6) El calor específico del agua es 1 cal/g ºC y del cobre es de 0,09 cal/g ºC. De lo anterior se deduce que si tenemos 1 kg de agua y 1 kg de cobre resulta a) más fácil elevar o disminuir la temperatura del agua que del cobre b) más fácil elevar o disminuir la temperatura del cobre que la del agua c) que como son masas iguales, se necesita la misma cantidad de calor para cambiar la temperatura d) más fácil elevar las temperatura del agua, pero más difícil bajarla que el cobre. 7) Cuando el agua comienza a hervir, las burbujas que se forman en el fondo suben rápidamente hacia la superficie. Estas burbujas son: a) de aire y están a la misma temperatura que el agua b) de aire y están a mayor temperatura que el agua c) de vapor de agua y están a la misma temperatura que el agua d) de vapor de agua y están a mayor temperatura que el agua 8) Una cuchara de metal se encuentra dentro de una taza de café caliente. La cuchara se siente caliente pues el calor se transmite hacia la mano por: a) conducción b) convección 20
ESTADOS DE AGREGACIÓN DE LA MATERIA
 ESADOS DE AGREGACIÓN DE LA MAERIA. Propiedades generales de la materia La materia es todo aquello que tiene masa y volumen. La masa se define como la cantidad de materia de un cuerpo. Se mide en kg. El
ESADOS DE AGREGACIÓN DE LA MAERIA. Propiedades generales de la materia La materia es todo aquello que tiene masa y volumen. La masa se define como la cantidad de materia de un cuerpo. Se mide en kg. El
Elementos de Física - Aplicaciones ENERGÍA. Taller Vertical 3 de Matemática y Física Aplicadas MASSUCCO ARRARÁS MARAÑON DI LEO
 Elementos de Física - Aplicaciones ENERGÍA Taller Vertical 3 de Matemática y Física Aplicadas MASSUCCO ARRARÁS MARAÑON DI LEO Energía La energía es una magnitud física que está asociada a la capacidad
Elementos de Física - Aplicaciones ENERGÍA Taller Vertical 3 de Matemática y Física Aplicadas MASSUCCO ARRARÁS MARAÑON DI LEO Energía La energía es una magnitud física que está asociada a la capacidad
Ing. Gerardo Sarmiento CALOR Y TEMPERATURA
 Ing. Gerardo Sarmiento CALOR Y TEMPERATURA Como se mide y transporta el calor La cantidad de calor (Q) se expresa en las mismas unidades que la energía y el trabajo, es decir, en Joule. Otra unidad es
Ing. Gerardo Sarmiento CALOR Y TEMPERATURA Como se mide y transporta el calor La cantidad de calor (Q) se expresa en las mismas unidades que la energía y el trabajo, es decir, en Joule. Otra unidad es
Aire acondicionado y refrigeración
 Aire acondicionado y refrigeración CONCEPTO: El acondicionamiento del aire es el proceso que enfría, limpia y circula el aire, controlando, además, su contenido de humedad. En condiciones ideales logra
Aire acondicionado y refrigeración CONCEPTO: El acondicionamiento del aire es el proceso que enfría, limpia y circula el aire, controlando, además, su contenido de humedad. En condiciones ideales logra
Tema 7 : Trabajo, Energía y Calor
 Tema 7 : Trabajo, Energía y Calor Esquema de trabajo: 7. Trabajo. Concepto. Unidad de medida. 8. Energía. Concepto 9. Energía Cinética 10. Energía Potencial Gravitatoria 11. Ley de Conservación de la Energía
Tema 7 : Trabajo, Energía y Calor Esquema de trabajo: 7. Trabajo. Concepto. Unidad de medida. 8. Energía. Concepto 9. Energía Cinética 10. Energía Potencial Gravitatoria 11. Ley de Conservación de la Energía
ENERGÍA INTERNA DE UN SISTEMA
 ENERGÍA INTERNA DE UN SISTEMA Definimos energía interna U de un sistema la suma de las energías cinéticas de todas sus partículas constituyentes, más la suma de todas las energías de interacción entre
ENERGÍA INTERNA DE UN SISTEMA Definimos energía interna U de un sistema la suma de las energías cinéticas de todas sus partículas constituyentes, más la suma de todas las energías de interacción entre
INTERCAMBIO MECÁNICO (TRABAJO)
 Colegio Santo Ángel de la guarda Física y Química 4º ESO Fernando Barroso Lorenzo INTERCAMBIO MECÁNICO (TRABAJO) 1. Un cuerpo de 1 kg de masa se encuentra a una altura de 2 m y posee una velocidad de 3
Colegio Santo Ángel de la guarda Física y Química 4º ESO Fernando Barroso Lorenzo INTERCAMBIO MECÁNICO (TRABAJO) 1. Un cuerpo de 1 kg de masa se encuentra a una altura de 2 m y posee una velocidad de 3
EJERCICIOS PROPUESTOS. Qué le sucede al movimiento térmico de las partículas de un cuerpo cuando aumenta su temperatura?
 9 ENERGÍA Y CALOR EJERCICIOS PROPUESTOS 9.1 Qué le sucede al movimiento térmico de las partículas de un cuerpo cuando aumenta su temperatura? Al aumentar la temperatura, se mueven con mayor velocidad y
9 ENERGÍA Y CALOR EJERCICIOS PROPUESTOS 9.1 Qué le sucede al movimiento térmico de las partículas de un cuerpo cuando aumenta su temperatura? Al aumentar la temperatura, se mueven con mayor velocidad y
FISICA Y QUÍMICA 4º ESO 1.- TRABAJO MECÁNICO.
 1.- TRABAJO MECÁNICO. Si a alguien que sostiene un objeto sin moverse le preguntas si hace trabajo, probablemente te responderá que sí. Sin embargo, desde el punto de vista de la Física, no realiza trabajo;
1.- TRABAJO MECÁNICO. Si a alguien que sostiene un objeto sin moverse le preguntas si hace trabajo, probablemente te responderá que sí. Sin embargo, desde el punto de vista de la Física, no realiza trabajo;
Determinación del equivalente eléctrico del calor
 Determinación del equivalente eléctrico del calor Julieta Romani Paula Quiroga María G. Larreguy y María Paz Frigerio julietaromani@hotmail.com comquir@ciudad.com.ar merigl@yahoo.com.ar mapaz@vlb.com.ar
Determinación del equivalente eléctrico del calor Julieta Romani Paula Quiroga María G. Larreguy y María Paz Frigerio julietaromani@hotmail.com comquir@ciudad.com.ar merigl@yahoo.com.ar mapaz@vlb.com.ar
CAPITULO 3 LA TEMPERATURA
 CAPITULO 3 LA TEMPERATURA 1. CONCEPTO: La temperatura de un cuerpo indica en qué dirección se desplazará el calor al poner en contacto dos cuerpos que se encuentran a temperaturas distintas, ya que éste
CAPITULO 3 LA TEMPERATURA 1. CONCEPTO: La temperatura de un cuerpo indica en qué dirección se desplazará el calor al poner en contacto dos cuerpos que se encuentran a temperaturas distintas, ya que éste
Bases Físicas del Medio Ambiente. Sistemas Termodinámicos
 Bases Físicas del Medio Ambiente Sistemas Termodinámicos Programa VII. SISTEMAS TERMODINÁMICOS. (1h) Introducción. Sistema termodinámico. Estados de equilibrio. Procesos termodinámicos. Equilibrio termodinámico.
Bases Físicas del Medio Ambiente Sistemas Termodinámicos Programa VII. SISTEMAS TERMODINÁMICOS. (1h) Introducción. Sistema termodinámico. Estados de equilibrio. Procesos termodinámicos. Equilibrio termodinámico.
PROBLEMAS RESUELTOS EQUILIBRIO TERMICO. Para cualquier inquietud o consulta escribir a: quintere@hotmail.com quintere@gmail.com quintere2006@yahoo.
 PROBLEMAS RESUELTOS EQUILIBRIO TERMICO Para cualquier inquietud o consulta escribir a: quintere@hotmail.com quintere@gmail.com quintere2006@yahoo.com Erving Quintero Gil Ing. Electromecánico Bucaramanga
PROBLEMAS RESUELTOS EQUILIBRIO TERMICO Para cualquier inquietud o consulta escribir a: quintere@hotmail.com quintere@gmail.com quintere2006@yahoo.com Erving Quintero Gil Ing. Electromecánico Bucaramanga
LOS GASES Y SUS LEYES DE
 EMA : LOS GASES Y SUS LEYES DE COMBINACIÓN -LAS LEYES DE LOS GASES En el siglo XII comenzó a investigarse el hecho de que los gases, independientemente de su naturaleza, presentan un comportamiento similar
EMA : LOS GASES Y SUS LEYES DE COMBINACIÓN -LAS LEYES DE LOS GASES En el siglo XII comenzó a investigarse el hecho de que los gases, independientemente de su naturaleza, presentan un comportamiento similar
TERMOMETRÌA Y CALORIMETRÌA
 TERMOMETRÌA Y CALORIMETRÌA Termómetros Basados en alguna propiedad física de un sistema que cambia con la temperatura: Volumen de un líquido Longitud de un sólido Presión de un gas a volumen constante
TERMOMETRÌA Y CALORIMETRÌA Termómetros Basados en alguna propiedad física de un sistema que cambia con la temperatura: Volumen de un líquido Longitud de un sólido Presión de un gas a volumen constante
LEYES DE CONSERVACIÓN: ENERGÍA Y MOMENTO
 LEYES DE CONSERVACIÓN: ENERGÍA Y MOMENTO 1. Trabajo mecánico y energía. El trabajo, tal y como se define físicamente, es una magnitud diferente de lo que se entiende sensorialmente por trabajo. Trabajo
LEYES DE CONSERVACIÓN: ENERGÍA Y MOMENTO 1. Trabajo mecánico y energía. El trabajo, tal y como se define físicamente, es una magnitud diferente de lo que se entiende sensorialmente por trabajo. Trabajo
Estudio de la evaporación
 Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
PROBLEMAS. Segundo Principio. Problema 1
 PROBLEMAS Segundo Principio Problema 1 La figura muestra un sistema que capta radiación solar y la utiliza para producir electricidad mediante un ciclo de potencia. El colector solar recibe 0,315 kw de
PROBLEMAS Segundo Principio Problema 1 La figura muestra un sistema que capta radiación solar y la utiliza para producir electricidad mediante un ciclo de potencia. El colector solar recibe 0,315 kw de
Calibración del termómetro
 Calibración del termómetro RESUMEN En esta práctica construimos un instrumento el cual fuera capaz de relacionar la temperatura con la distancia, es decir, diseñamos un termómetro de alcohol, agua y gas
Calibración del termómetro RESUMEN En esta práctica construimos un instrumento el cual fuera capaz de relacionar la temperatura con la distancia, es decir, diseñamos un termómetro de alcohol, agua y gas
ENERGÍA INTERNA PARA GASES NO IDEALES.
 DEPARTAMENTO DE FISICA UNIERSIDAD DE SANTIAGO DE CHILE ENERGÍA INTERNA PARA GASES NO IDEALES. En el caso de los gases ideales o cualquier cuerpo en fase no gaseosa la energía interna es función de la temperatura
DEPARTAMENTO DE FISICA UNIERSIDAD DE SANTIAGO DE CHILE ENERGÍA INTERNA PARA GASES NO IDEALES. En el caso de los gases ideales o cualquier cuerpo en fase no gaseosa la energía interna es función de la temperatura
Agentes para la conservación de la energía mecánica
 Agentes para la conservación de la energía mecánica Para levantar un cuerpo verticalmente a velocidad constante, es necesario que algún agente externo realice trabajo y hemos demostrado que este trabajo
Agentes para la conservación de la energía mecánica Para levantar un cuerpo verticalmente a velocidad constante, es necesario que algún agente externo realice trabajo y hemos demostrado que este trabajo
BALANCE MÁSICO Y ENERGÉTICO DE PROBLEMAS AMBIENTALES
 BALANCE MÁSICO Y ENERGÉTICO DE PROBLEMAS AMBIENTALES Cálculos en Ingeniería, procesos y variables de procesos. Temperatura y presión Temperatura y presión La presión se define como la cantidad d fuerza
BALANCE MÁSICO Y ENERGÉTICO DE PROBLEMAS AMBIENTALES Cálculos en Ingeniería, procesos y variables de procesos. Temperatura y presión Temperatura y presión La presión se define como la cantidad d fuerza
INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA. La mecánica cuántica estudia la estructura atómica, los enlaces en moléculas y la espectroscopia.
 INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA 1. Qué es la Química Física? "La química física estudia los principios que gobiernan las propiedades el comportamiento de los sistemas químicos" El estudio de los
INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA 1. Qué es la Química Física? "La química física estudia los principios que gobiernan las propiedades el comportamiento de los sistemas químicos" El estudio de los
DEFINICIÓN DE CONCEPTOS PARA AIRE ACONDICIONADO
 DEFINICIÓN DE CONCEPTOS PARA AIRE ACONDICIONADO Glosario. (Del lat. glossarĭum). 1. m. Catálogo de palabras oscuras o desusadas, con definición o explicación de cada una de ellas. 2. m. Catálogo de palabras
DEFINICIÓN DE CONCEPTOS PARA AIRE ACONDICIONADO Glosario. (Del lat. glossarĭum). 1. m. Catálogo de palabras oscuras o desusadas, con definición o explicación de cada una de ellas. 2. m. Catálogo de palabras
PROBLEMAS DE TRNSMISIÓN DE CALOR
 TEMODINAMIA Departamento de Física - UNS arreras: Ing. Industrial y Mecánica POBLEMAS DE TNSMISIÓN DE ALO Ejemplo. Pérdida de calor a través de una pared plana onsidere una pared gruesa de 3 m de alto,
TEMODINAMIA Departamento de Física - UNS arreras: Ing. Industrial y Mecánica POBLEMAS DE TNSMISIÓN DE ALO Ejemplo. Pérdida de calor a través de una pared plana onsidere una pared gruesa de 3 m de alto,
Magnitudes y unidades
 1 Estados de agregación de la materia Magnitudes y unidades Magnitud física es toda propiedad de un objeto o de un fenómeno físico o químico que se puede medir. Medir es comparar dos magnitudes de las
1 Estados de agregación de la materia Magnitudes y unidades Magnitud física es toda propiedad de un objeto o de un fenómeno físico o químico que se puede medir. Medir es comparar dos magnitudes de las
TEMA 1 Conceptos básicos de la termodinámica
 Bases Físicas y Químicas del Medio Ambiente TEMA 1 Conceptos básicos de la termodinámica La termodinámica es el estudio de la transformación de una forma de energía en otra y del intercambio de energía
Bases Físicas y Químicas del Medio Ambiente TEMA 1 Conceptos básicos de la termodinámica La termodinámica es el estudio de la transformación de una forma de energía en otra y del intercambio de energía
La electricidad. La electricidad se origina por la separación o movimiento de los electrones que forman los átomos.
 1 La electricidad Es el conjunto de fenómenos físicos relacionados con la presencia y flujo de cargas eléctricas. Se manifiesta en una gran variedad de fenómenos como los rayos, la electricidad estática,
1 La electricidad Es el conjunto de fenómenos físicos relacionados con la presencia y flujo de cargas eléctricas. Se manifiesta en una gran variedad de fenómenos como los rayos, la electricidad estática,
TEMPERATURA: Es aquella propiedad física que permite asegurar si dos o mas sistemas están o no en equilibrio térmico.
 CONCEPTO DE CALOR: Es una forma de energía, que tiene su origen en el movimiento de las moléculas de los cuerpos y que se desarrolla por el roce o choque entre las mismas. Principales efectos del calor:
CONCEPTO DE CALOR: Es una forma de energía, que tiene su origen en el movimiento de las moléculas de los cuerpos y que se desarrolla por el roce o choque entre las mismas. Principales efectos del calor:
CAMBIO DE FASE : VAPORIZACIÓN
 CAMBIO DE FASE : VAPORIZACIÓN Un líquido no tiene que ser calentado a su punto de ebullición antes de que pueda convertirse en un gas. El agua, por ejemplo, se evapora de un envase abierto en la temperatura
CAMBIO DE FASE : VAPORIZACIÓN Un líquido no tiene que ser calentado a su punto de ebullición antes de que pueda convertirse en un gas. El agua, por ejemplo, se evapora de un envase abierto en la temperatura
Condensación y ebullición ING Roxsana Romero Ariza Junio 2013
 Condensación y ebullición ING Roxsana Romero Ariza Junio 2013 EBULLICIÓN La transferencia de calor a un líquido en ebullición es muy importante en la evaporación y destilación, así como en otros tipos
Condensación y ebullición ING Roxsana Romero Ariza Junio 2013 EBULLICIÓN La transferencia de calor a un líquido en ebullición es muy importante en la evaporación y destilación, así como en otros tipos
LÍNEAS DEL DIAGRAMA DE MOLLIER
 DIAGRAMA DE MOLLIER El refrigerante cambia de estado a lo largo del ciclo frigorífico como hemos visto en el capítulo anterior. Representaremos sobre el diagrama de p-h las distintas transformaciones que
DIAGRAMA DE MOLLIER El refrigerante cambia de estado a lo largo del ciclo frigorífico como hemos visto en el capítulo anterior. Representaremos sobre el diagrama de p-h las distintas transformaciones que
Universidad Autónoma de Nuevo León Preparatoria 8. Requisitos para presentar en 3ª, 5ª y/o 6ª Oportunidad Semestre: Agosto - Diciembre 2015
 Universidad Autónoma de Nuevo León Preparatoria 8 Requisitos para presentar en 3ª, 5ª y/o 6ª Oportunidad Semestre: Agosto - Diciembre 2015 Materia: Coordinador: Temas Selectos de Física M.A. Martín Ramírez
Universidad Autónoma de Nuevo León Preparatoria 8 Requisitos para presentar en 3ª, 5ª y/o 6ª Oportunidad Semestre: Agosto - Diciembre 2015 Materia: Coordinador: Temas Selectos de Física M.A. Martín Ramírez
DRAFT. Trabajo, Calor y Primer Principio de la Termodinámica.
 DRAFT Trabajo, Calor y Primer Principio de la Termodinámica. J.V. Alvarez Departmento de Fisica de la Materia Condensada, Universidad Autonoma de Madrid. 28049 Madrid, Spain. (Dated: October 10, 2007)
DRAFT Trabajo, Calor y Primer Principio de la Termodinámica. J.V. Alvarez Departmento de Fisica de la Materia Condensada, Universidad Autonoma de Madrid. 28049 Madrid, Spain. (Dated: October 10, 2007)
Transferencia de energía: calor
 Transferencia de energía: calor Objetivos Transferencia de energía: calor: Conocer y saber diferenciar los conceptos de calor, temperatura y energía interna. Manejar las diferentes unidades que se usan
Transferencia de energía: calor Objetivos Transferencia de energía: calor: Conocer y saber diferenciar los conceptos de calor, temperatura y energía interna. Manejar las diferentes unidades que se usan
CALOR. Q = c m (Tf - Ti) (1) Q será positivo si la temperatura final es mayor que la inicial (Tf > Ti) y negativo en el caso contrario (Tf < Ti).
 1. CANTIDADES DE CALOR CALOR Aun cuando no sea posible determinar el contenido total de energía calorífica de un cuerpo, puede medirse la cantidad que se toma o se cede al ponerlo en contacto con otro
1. CANTIDADES DE CALOR CALOR Aun cuando no sea posible determinar el contenido total de energía calorífica de un cuerpo, puede medirse la cantidad que se toma o se cede al ponerlo en contacto con otro
Determinación del calor latente de fusión del hielo
 Determinación del calor latente de usión del hielo Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica
Determinación del calor latente de usión del hielo Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica
Electricidad y calor. Temario. Temario. Webpage: http://paginas.fisica.uson.mx/qb
 Electricidad y calor Webpage: http://paginas.fisica.uson.mx/qb 2007 Departamento de Física Universidad de Sonora Temario A. Termodinámica 1. Temperatura y Ley Cero. (3horas) 1. Equilibrio Térmico y ley
Electricidad y calor Webpage: http://paginas.fisica.uson.mx/qb 2007 Departamento de Física Universidad de Sonora Temario A. Termodinámica 1. Temperatura y Ley Cero. (3horas) 1. Equilibrio Térmico y ley
14. ENTALPÍA DE FUSIÓN DEL HIELO
 14. ENTALPÍA DE FUSIÓN DEL HIELO OBJETIVO Determinar la entalpía de fusión del hielo, H f, utilizando el método de las mezclas. Previamente, ha de determinarse el equivalente en agua del calorímetro, K,
14. ENTALPÍA DE FUSIÓN DEL HIELO OBJETIVO Determinar la entalpía de fusión del hielo, H f, utilizando el método de las mezclas. Previamente, ha de determinarse el equivalente en agua del calorímetro, K,
Colegio : Liceo Miguel de Cervantes y Saavedra Dpto. Física (3 ero Medio) Profesor: Héctor Palma A.
 Tópico Generativo: La presión en vasos comunicantes. Aprendizajes Esperados: 1.-Aplicar la definir conceptual de presión y aplicarla a vasos comunicante. 2.- Caracterizar la presión en función de la fuerza
Tópico Generativo: La presión en vasos comunicantes. Aprendizajes Esperados: 1.-Aplicar la definir conceptual de presión y aplicarla a vasos comunicante. 2.- Caracterizar la presión en función de la fuerza
35 Facultad de Ciencias Universidad de Los Andes Mérida-Venezuela. Potencial Eléctrico
 q 1 q 2 Prof. Félix Aguirre 35 Energía Electrostática Potencial Eléctrico La interacción electrostática es representada muy bien a través de la ley de Coulomb, esto es: mediante fuerzas. Existen, sin embargo,
q 1 q 2 Prof. Félix Aguirre 35 Energía Electrostática Potencial Eléctrico La interacción electrostática es representada muy bien a través de la ley de Coulomb, esto es: mediante fuerzas. Existen, sin embargo,
CARACTERÍSTICAS DE LA MATERIA
 LA MATERIA CARACTERÍSTICAS DE LA MATERIA - Todo lo que existe en el universo está compuesto de Materia. - La Materia se clasifica en Mezclas y Sustancias Puras. - Las Mezclas son combinaciones de sustancias
LA MATERIA CARACTERÍSTICAS DE LA MATERIA - Todo lo que existe en el universo está compuesto de Materia. - La Materia se clasifica en Mezclas y Sustancias Puras. - Las Mezclas son combinaciones de sustancias
Ciencias Naturales 5º Primaria Tema 7: La materia
 1. La materia que nos rodea Propiedades generales de la materia Los objetos materiales tienes en común dos propiedades, que se llaman propiedades generales de la materia: Poseen masa. La masa es la cantidad
1. La materia que nos rodea Propiedades generales de la materia Los objetos materiales tienes en común dos propiedades, que se llaman propiedades generales de la materia: Poseen masa. La masa es la cantidad
TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones.
 Esquema: TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones. TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones....1 1.- Introducción...1 2.- Máquina frigorífica...1
Esquema: TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones. TEMA 4: Circuito frigorífico y bomba de calor: elementos y aplicaciones....1 1.- Introducción...1 2.- Máquina frigorífica...1
Módulo 3: Fluidos. Fluidos
 Módulo 3: Fluidos 1 Fluidos Qué es un fluido? En Física, un fluido es una sustancia que se deforma continuamente (fluye) bajo la aplicación de una tensión tangencial, por muy pequeña que sea. Es decir,
Módulo 3: Fluidos 1 Fluidos Qué es un fluido? En Física, un fluido es una sustancia que se deforma continuamente (fluye) bajo la aplicación de una tensión tangencial, por muy pequeña que sea. Es decir,
Actividad: Qué es capilaridad?
 Qué es capilaridad? Nivel: 3º medio Subsector: Ciencias físicas Unidad temática: Ver video Capilaridad Actividad: Qué es capilaridad? Los fluidos son un conjunto de moléculas distribuidas al azar que se
Qué es capilaridad? Nivel: 3º medio Subsector: Ciencias físicas Unidad temática: Ver video Capilaridad Actividad: Qué es capilaridad? Los fluidos son un conjunto de moléculas distribuidas al azar que se
TEMA 11 LA MATERIA EN EL UNIVERSO
 TEMA 11 LA MATERIA EN EL UNIVERSO TEMA 11 LA MATERIA EN EL UNIVERSO QUÉ ES LA MATERIA? Materia es todo aquello que tiene volumen (ocupa un espacio) y que tiene una determinada masa (por tanto, pesa). QUÉ
TEMA 11 LA MATERIA EN EL UNIVERSO TEMA 11 LA MATERIA EN EL UNIVERSO QUÉ ES LA MATERIA? Materia es todo aquello que tiene volumen (ocupa un espacio) y que tiene una determinada masa (por tanto, pesa). QUÉ
Completar: Un sistema material homogéneo constituido por un solo componente se llama.
 IES Menéndez Tolosa 3º ESO (Física y Química) 1 Completar: Un sistema material homogéneo constituido por un solo componente se llama. Un sistema material homogéneo formado por dos o más componentes se
IES Menéndez Tolosa 3º ESO (Física y Química) 1 Completar: Un sistema material homogéneo constituido por un solo componente se llama. Un sistema material homogéneo formado por dos o más componentes se
FÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación GAS LÍQUIDO SÓLIDO
 Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
Nombre echa de entrega ÍSICA Y QUÍMICA 3º E.S.O. - Repaso 3ª Evaluación. El aire, es materia? Por qué? Las propiedades fundamentales de la materia son la masa (cantidad de materia, expresada en kg en el
La Absorción del Agua
 La Absorción del Agua Importancia del Agua en las Plantas Es el cons5tuyente principal del protoplasma celular, en ocasiones representa hasta el 95% del peso total de la planta. Es el solvente en el que
La Absorción del Agua Importancia del Agua en las Plantas Es el cons5tuyente principal del protoplasma celular, en ocasiones representa hasta el 95% del peso total de la planta. Es el solvente en el que
DL CH12 Reactor químico combinado
 DL CH12 Reactor químico combinado Introducción La reacción química es la operación unitaria que tiene por objeto distribuir de una forma distinta los átomos de unas moléculas (compuestos reaccionantes
DL CH12 Reactor químico combinado Introducción La reacción química es la operación unitaria que tiene por objeto distribuir de una forma distinta los átomos de unas moléculas (compuestos reaccionantes
TEMA 8 CAMPO ELÉCTRICO
 TEMA 8 CAMPO ELÉCTRICO INTERACCIÓN ELECTROSTÁTICA Los antiguos griegos ya sabían que el ámbar frotado con lana adquiría la propiedad de atraer cuerpos ligeros. Todos estamos familiarizados con los efectos
TEMA 8 CAMPO ELÉCTRICO INTERACCIÓN ELECTROSTÁTICA Los antiguos griegos ya sabían que el ámbar frotado con lana adquiría la propiedad de atraer cuerpos ligeros. Todos estamos familiarizados con los efectos
Introducción al calor y la luz
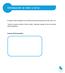 Introducción al calor y la luz El espectro electromagnético es la fuente principal de energía que provee calor y luz. Todos los cuerpos, incluído el vidrio, emiten y absorben energía en forma de ondas
Introducción al calor y la luz El espectro electromagnético es la fuente principal de energía que provee calor y luz. Todos los cuerpos, incluído el vidrio, emiten y absorben energía en forma de ondas
Tema: TEMPERATURA Y CALOR
 Tema: TEMPERATURA Y CALOR TERMOMETRÍA Consulte la bibliografía recomendada y responda: - Cómo se define los extremos 0º C y 100º C de la escala termométrica CELSIUS? - Qué relación tiene con la escala
Tema: TEMPERATURA Y CALOR TERMOMETRÍA Consulte la bibliografía recomendada y responda: - Cómo se define los extremos 0º C y 100º C de la escala termométrica CELSIUS? - Qué relación tiene con la escala
ASPECTOS GENERALES PARA LA SOLUCIÓN DE PROBLEMAS RELACIONADOS CON LA CONDUCCIÓN TRANSITORIA.
 CONDUCCIÓN TRANSITORIA Aquí encontrarás Los métodos gráficos y el análisis teórico necesario para resolver problemas relacionados con la transferencia de calor por conducción en estado transitorio a través
CONDUCCIÓN TRANSITORIA Aquí encontrarás Los métodos gráficos y el análisis teórico necesario para resolver problemas relacionados con la transferencia de calor por conducción en estado transitorio a través
PREGUNTAS FRECUENTES
 PREGUNTAS FRECUENTES ÍNDICE Qué son los Repartidores de costes de calefacción? Montaje y funcionamiento de los repartidores Base de datos de radiadores existentes. Precio de los Repartidores de Costes
PREGUNTAS FRECUENTES ÍNDICE Qué son los Repartidores de costes de calefacción? Montaje y funcionamiento de los repartidores Base de datos de radiadores existentes. Precio de los Repartidores de Costes
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire.
 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire. El proceso de secado es una de las operaciones más importantes en la industria
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire. El proceso de secado es una de las operaciones más importantes en la industria
Guía de repaso prueba de síntesis II Medio ANALIZA Y RESPONDE
 Fundación Educacional Colegio de los SS.CC. Manquehue Depto. Ciencias Profesoras: Jacky Moreno Guislaine Loayza Nivel: II medio Guía de repaso prueba de síntesis II Medio ANALIZA Y RESPONDE 1) De acuerdo
Fundación Educacional Colegio de los SS.CC. Manquehue Depto. Ciencias Profesoras: Jacky Moreno Guislaine Loayza Nivel: II medio Guía de repaso prueba de síntesis II Medio ANALIZA Y RESPONDE 1) De acuerdo
1. Calcula la energía cinética de un vehículo de 1000 kg que circula a 100 km/h. Resultado: E C = 385.802,47 J
 1.- CONCEPTOS BÁSICOS 1. Calcula la energía cinética de un vehículo de 1000 kg que circula a 100 km/h. Resultado: E C = 385.802,47 J 2. Calcula la energía potencial de una masa de 500 kg colgada a 10 m
1.- CONCEPTOS BÁSICOS 1. Calcula la energía cinética de un vehículo de 1000 kg que circula a 100 km/h. Resultado: E C = 385.802,47 J 2. Calcula la energía potencial de una masa de 500 kg colgada a 10 m
La energía y sus transformaciones
 La energía y sus transformaciones Índice 1 Definición de energía 2 Energías renovables y no renovables 2.1 Energías no renovables 2.2 Energías renovables 3 Transformaciones energéticas 4 Conservación de
La energía y sus transformaciones Índice 1 Definición de energía 2 Energías renovables y no renovables 2.1 Energías no renovables 2.2 Energías renovables 3 Transformaciones energéticas 4 Conservación de
Sistema termodinámico
 IngTermica_01:Maquetación 1 16/02/2009 17:53 Página 1 Capítulo 1 Sistema termodinámico 1.1 Introducción En sentido amplio, la Termodinámica es la ciencia que estudia las transformaciones energéticas. Si
IngTermica_01:Maquetación 1 16/02/2009 17:53 Página 1 Capítulo 1 Sistema termodinámico 1.1 Introducción En sentido amplio, la Termodinámica es la ciencia que estudia las transformaciones energéticas. Si
Cifras significativas e incertidumbre en las mediciones
 Unidades de medición Cifras significativas e incertidumbre en las mediciones Todas las mediciones constan de una unidad que nos indica lo que fue medido y un número que indica cuántas de esas unidades
Unidades de medición Cifras significativas e incertidumbre en las mediciones Todas las mediciones constan de una unidad que nos indica lo que fue medido y un número que indica cuántas de esas unidades
CAPITULO Nº 1 PODER CALORIFICO
 UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL MENDOZA CATEDRA MAQUINAS TERMICAS CARRERA INGENIERIA ELECTROMECANICA CAPITULO Nº 1 PODER CALORIFICO ELABORADO POR: ING. JORGE FELIX FERNANDEZ PROFESOR
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL MENDOZA CATEDRA MAQUINAS TERMICAS CARRERA INGENIERIA ELECTROMECANICA CAPITULO Nº 1 PODER CALORIFICO ELABORADO POR: ING. JORGE FELIX FERNANDEZ PROFESOR
EVAPORADORES Y CONDENSADORES
 AMBOS SON LOS ELEMENTOS DONDE SE PRODUCE EL INTERCAMBIO DE CALOR: EVAPORADOR: SE GANA CALOR A BAJA TEMPERATURA, GENERANDO EFECTO DE REFRIGERACIÓN MEDIANTE LA EVAPORACIÓN DEL REFRIGERANTE A BAJA PRESIÓN
AMBOS SON LOS ELEMENTOS DONDE SE PRODUCE EL INTERCAMBIO DE CALOR: EVAPORADOR: SE GANA CALOR A BAJA TEMPERATURA, GENERANDO EFECTO DE REFRIGERACIÓN MEDIANTE LA EVAPORACIÓN DEL REFRIGERANTE A BAJA PRESIÓN
Práctica II: DENSIDAD Y HUMEDAD DEL AIRE
 Física Ambiental, I.T. Agrícola Práctica II: DENSIDAD Y HUMEDAD DEL AIRE Universidad de Huelva. Dpto. de Física Aplicada. Prácticas de Física Ambiental, I.T. Agrícola 1 3. Densidad y humedad del aire 3.1.
Física Ambiental, I.T. Agrícola Práctica II: DENSIDAD Y HUMEDAD DEL AIRE Universidad de Huelva. Dpto. de Física Aplicada. Prácticas de Física Ambiental, I.T. Agrícola 1 3. Densidad y humedad del aire 3.1.
Potencial eléctrico. du = - F dl
 Introducción Como la fuerza gravitatoria, la fuerza eléctrica es conservativa. Existe una función energía potencial asociada con la fuerza eléctrica. Como veremos, la energía potencial asociada a una partícula
Introducción Como la fuerza gravitatoria, la fuerza eléctrica es conservativa. Existe una función energía potencial asociada con la fuerza eléctrica. Como veremos, la energía potencial asociada a una partícula
Contenidos Didácticos
 INDICE --------------------------------------------------------------------------------------------------------------------------------------------- 1 FUERZA...3 2 TRABAJO...5 3 POTENCIA...6 4 ENERGÍA...7
INDICE --------------------------------------------------------------------------------------------------------------------------------------------- 1 FUERZA...3 2 TRABAJO...5 3 POTENCIA...6 4 ENERGÍA...7
Transformación de trabajo en calor y calor en trabajo. Motores y Frigoríficos.
 Transformación de trabajo en calor y calor en trabajo Motores y Frigoríficos. De lo expuesto, se debe concluir que cualquier sistema que este expuesto al intercambio de trabajo y calor con el exterior
Transformación de trabajo en calor y calor en trabajo Motores y Frigoríficos. De lo expuesto, se debe concluir que cualquier sistema que este expuesto al intercambio de trabajo y calor con el exterior
ORIENTACIONES PARA LA MATERIA DE FÍSICA Convocatoria 2010
 ORIENTACIONES PARA LA MATERIA DE FÍSICA Convocatoria 2010 Prueba de Acceso para Mayores de 25 años Para que un adulto mayor de 25 años pueda incorporarse plenamente en los estudios superiores de la Física
ORIENTACIONES PARA LA MATERIA DE FÍSICA Convocatoria 2010 Prueba de Acceso para Mayores de 25 años Para que un adulto mayor de 25 años pueda incorporarse plenamente en los estudios superiores de la Física
LA ENERGÍA. La energía es una propiedad asociada a los objetos y sustancias y se manifiesta en las transformaciones que ocurren en la naturaleza.
 Objetivos: Unidad II: La energía Conocer qué es la energía Distinguir las distintas formas de energía Comprender las transformaciones de la energía Distinguir entre conservación y degradación de la energía
Objetivos: Unidad II: La energía Conocer qué es la energía Distinguir las distintas formas de energía Comprender las transformaciones de la energía Distinguir entre conservación y degradación de la energía
D E S C R I P C I O N
 SISTEMA DE REFRIGERACIÓN CON CO 2 COMO FLUIDO SECUNDARIO D E S C R I P C I O N OBJETO DE LA INVENCIÓN La presente invención se refiere a un sistema de refrigeración con CO 2 como fluido secundario que
SISTEMA DE REFRIGERACIÓN CON CO 2 COMO FLUIDO SECUNDARIO D E S C R I P C I O N OBJETO DE LA INVENCIÓN La presente invención se refiere a un sistema de refrigeración con CO 2 como fluido secundario que
Cuál es tu temperatura favorita? Cuán brillante es el Sol? Educación en el cambio global Cambios en la atmósfera - Sección CA3-1
 Educación en el cambio global Cambios en la atmósfera - Sección CA3-1 CA3 Actividades Cuál es tu temperatura favorita? Si alguien te preguntase a qué temperatura te gustaría vivir, seguramente elegirías
Educación en el cambio global Cambios en la atmósfera - Sección CA3-1 CA3 Actividades Cuál es tu temperatura favorita? Si alguien te preguntase a qué temperatura te gustaría vivir, seguramente elegirías
PRÁCTICA 5. CALORIMETRÍA
 PRÁCTICA 5. CALORIMETRÍA INTRODUCCIÓN Al mezclar dos cantidades de líquidos a distinta temperatura se genera una transferencia de energía en forma de calor desde el más caliente al más frío. Dicho tránsito
PRÁCTICA 5. CALORIMETRÍA INTRODUCCIÓN Al mezclar dos cantidades de líquidos a distinta temperatura se genera una transferencia de energía en forma de calor desde el más caliente al más frío. Dicho tránsito
Actividad V.53 Transiciones de fases Calor latente de transformación
 Actividad V.53 Transiciones de fases Calor latente de transformación Objetivo Estudio de transiciones de fase líquido vapor y sólido líquido. Medición de los calores latentes de evaporación y de fusión
Actividad V.53 Transiciones de fases Calor latente de transformación Objetivo Estudio de transiciones de fase líquido vapor y sólido líquido. Medición de los calores latentes de evaporación y de fusión
Bolilla 7: Propiedades de los Líquidos
 Bolilla 7: Propiedades de los Líquidos 1 Bolilla 7: Propiedades de los Líquidos Estudiaremos propiedades de los líquidos, derivadas de las fuerzas de cohesión entre las moléculas que lo componen. Además
Bolilla 7: Propiedades de los Líquidos 1 Bolilla 7: Propiedades de los Líquidos Estudiaremos propiedades de los líquidos, derivadas de las fuerzas de cohesión entre las moléculas que lo componen. Además
= 3600s Ec 1 =Ec 2. 36Km/h. 1000 m 1h RELACIÓN DE PROBLEMAS. ENERGÍAS 360J
 RELACIÓN DE PROBLEMAS. ENERGÍAS 1. Un objeto de 50 Kg se halla a 10 m de altura sobre la azotea de un edificio, cuya altura, respecto al suelo, es 50 m. Qué energía potencial gravitatoria posee dicho objeto?
RELACIÓN DE PROBLEMAS. ENERGÍAS 1. Un objeto de 50 Kg se halla a 10 m de altura sobre la azotea de un edificio, cuya altura, respecto al suelo, es 50 m. Qué energía potencial gravitatoria posee dicho objeto?
TRABAJO. ENERGÍA. PRINCIPIO DE CONSERVACIÓN
 TRABAJO. ENERGÍA. PRINCIPIO DE CONSERVACIÓN Un coche de 50 kg (con el conductor incluido) que funciona con gasolina está situado en una carretera horizontal, arranca y acelerando uniformemente, alcanza
TRABAJO. ENERGÍA. PRINCIPIO DE CONSERVACIÓN Un coche de 50 kg (con el conductor incluido) que funciona con gasolina está situado en una carretera horizontal, arranca y acelerando uniformemente, alcanza
Módulo 1: Electrostática Condensadores. Capacidad.
 Módulo 1: Electrostática Condensadores. Capacidad. 1 Capacidad Hemos visto la relación entre campo eléctrico y cargas, y como la interacción entre cargas se convierte en energía potencial eléctrica Ahora
Módulo 1: Electrostática Condensadores. Capacidad. 1 Capacidad Hemos visto la relación entre campo eléctrico y cargas, y como la interacción entre cargas se convierte en energía potencial eléctrica Ahora
CALENTAMIENTO DE AGUA CALIENTE SANITARIA
 CALENTAMIENTO DE AGUA CALIENTE SANITARIA De todas las formas de captación térmica de la energía solar, las que han adquirido un desarrollo comercial en España han sido los sistemas para su utilización
CALENTAMIENTO DE AGUA CALIENTE SANITARIA De todas las formas de captación térmica de la energía solar, las que han adquirido un desarrollo comercial en España han sido los sistemas para su utilización
Integración de una resistencia calefactora de SiC y un tubo de nitruro de silicio en baños de aluminio fundido
 Integración de una resistencia calefactora de SiC y un tubo de nitruro de silicio en baños de aluminio fundido Por Mitsuaki Tada Traducido por ENTESIS technology Este artículo describe la combinación de
Integración de una resistencia calefactora de SiC y un tubo de nitruro de silicio en baños de aluminio fundido Por Mitsuaki Tada Traducido por ENTESIS technology Este artículo describe la combinación de
INTERCAMBIADORES DE CALOR. Mg. Amancio R. Rojas Flores
 INTERCAMBIADORES DE CALOR Mg. Amancio R. Rojas Flores INTRODUCCIÓN Los intercambiadores de calor son aparatos que facilitan el intercambio de calor entre dos fluidos que se encuentran a temperaturas diferentes
INTERCAMBIADORES DE CALOR Mg. Amancio R. Rojas Flores INTRODUCCIÓN Los intercambiadores de calor son aparatos que facilitan el intercambio de calor entre dos fluidos que se encuentran a temperaturas diferentes
Calentadores y Sistemas de Fluido Térmico.
 Calentadores y Sistemas de Fluido Térmico. El objetivo del presente artículo es entregar información técnica para diseñar, especificar y operar sistemas de fluido térmico. Introducción Agua y vapor son
Calentadores y Sistemas de Fluido Térmico. El objetivo del presente artículo es entregar información técnica para diseñar, especificar y operar sistemas de fluido térmico. Introducción Agua y vapor son
1. INTRODUCCIÓN 1.1 INGENIERÍA
 1. INTRODUCCIÓN 1.1 INGENIERÍA Es difícil dar una explicación de ingeniería en pocas palabras, pues se puede decir que la ingeniería comenzó con el hombre mismo, pero se puede intentar dar un bosquejo
1. INTRODUCCIÓN 1.1 INGENIERÍA Es difícil dar una explicación de ingeniería en pocas palabras, pues se puede decir que la ingeniería comenzó con el hombre mismo, pero se puede intentar dar un bosquejo
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la
![CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la](/thumbs/26/7800050.jpg) 34 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO 4.1 Lecho fluidizado con vapor sobrecalentado Potter [10], ha demostrado en una planta piloto que materiales sensibles a la temperatura pueden
34 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO 4.1 Lecho fluidizado con vapor sobrecalentado Potter [10], ha demostrado en una planta piloto que materiales sensibles a la temperatura pueden
ENERGÍA (II) FUERZAS CONSERVATIVAS
 NRGÍA (II) URZAS CONSRVATIVAS IS La Magdalena. Avilés. Asturias Cuando elevamos un cuerpo una altura h, la fuerza realiza trabajo positivo (comunica energía cinética al cuerpo). No podríamos aplicar la
NRGÍA (II) URZAS CONSRVATIVAS IS La Magdalena. Avilés. Asturias Cuando elevamos un cuerpo una altura h, la fuerza realiza trabajo positivo (comunica energía cinética al cuerpo). No podríamos aplicar la
Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: LA ENERGÍA Y SU TRANSFORMACIÓN. PRODUCCIÓN DE ENERGÍA ELÉCTRICA
 TEMA 1: LA ENERGÍA Y SU TRANSFORMACIÓN. PRODUCCIÓN DE ENERGÍA ELÉCTRICA 1.- Concepto de energía y sus unidades: La energía E es la capacidad de producir trabajo. Y trabajo W es cuando al aplicar una fuerza
TEMA 1: LA ENERGÍA Y SU TRANSFORMACIÓN. PRODUCCIÓN DE ENERGÍA ELÉCTRICA 1.- Concepto de energía y sus unidades: La energía E es la capacidad de producir trabajo. Y trabajo W es cuando al aplicar una fuerza
Fundamentos de Materiales - Prácticas de Laboratorio Práctica 9. Práctica 9 DETERMINACIÓN DEL ÍNDICE DE REFRACCIÓN DE MATERIALES TRANSPARENTES
 Práctica 9 DETERMINACIÓN DEL ÍNDICE DE REFRACCIÓN DE MATERIALES TRANSPARENTES 1. Objetivos docentes Familiarizarse con las propiedades ópticas de refracción y reflexión de materiales transparentes. 2.
Práctica 9 DETERMINACIÓN DEL ÍNDICE DE REFRACCIÓN DE MATERIALES TRANSPARENTES 1. Objetivos docentes Familiarizarse con las propiedades ópticas de refracción y reflexión de materiales transparentes. 2.
P cabeza Sca 5 1 0 6 m 2 2 10 6 Pa. beza. 6 m 2 10 8 Pa unta
 Pág. 1 16 Ejercemos una fuerza de 10 N sobre un clavo. Si la superficie de su cabeza es de 5 mm y la de la punta 0,1 mm, qué presión se ejercerá al aplicar la fuerza sobre uno u otro de sus extremos? La
Pág. 1 16 Ejercemos una fuerza de 10 N sobre un clavo. Si la superficie de su cabeza es de 5 mm y la de la punta 0,1 mm, qué presión se ejercerá al aplicar la fuerza sobre uno u otro de sus extremos? La
3 Aplicaciones de primer orden
 CAPÍTULO 3 Aplicaciones de primer orden 3.4 Ley de Enfriamiento de Newton Si un cuerpo u objeto que tiene una temperatura T 0 es depositado en un medio ambiente que se mantiene a una temperatura T a constante,
CAPÍTULO 3 Aplicaciones de primer orden 3.4 Ley de Enfriamiento de Newton Si un cuerpo u objeto que tiene una temperatura T 0 es depositado en un medio ambiente que se mantiene a una temperatura T a constante,
FÍSICA APLICADA. 1- Completar el siguiente cuadro; utilizando la ecuación de conversión: CENTIGRADO FAHRENHEIT KELVIN 40 F
 UNIDAD 5: TEMPERATURA Y CALOR 5. A: Temperatura y dilatación Temperatura, energía y calor. Medición de la temperatura. Escalas de temperatura. Dilatación lineal, superficial y volumétrica. Dilatación anómala
UNIDAD 5: TEMPERATURA Y CALOR 5. A: Temperatura y dilatación Temperatura, energía y calor. Medición de la temperatura. Escalas de temperatura. Dilatación lineal, superficial y volumétrica. Dilatación anómala
LA MATERIA Materia sustancias. Propiedades Propiedades generales. Propiedades características. Densidad
 LA MATERIA La materia son todos los sólidos, líquidos, gases que nos rodean (los árboles, los perros, el agua, una mesa de madera, aire, las personas, una silla de hierro, el refresco de una botella, las
LA MATERIA La materia son todos los sólidos, líquidos, gases que nos rodean (los árboles, los perros, el agua, una mesa de madera, aire, las personas, una silla de hierro, el refresco de una botella, las
Potenciales de optimización de reacciones de laboratorio -
 Potenciales de optimización de reacciones de laboratorio - Reglas básicas para síntesis sostenibles En el curso de la investigación sobre algunas reaccione incluidas en NOP se han podido identificar algunos
Potenciales de optimización de reacciones de laboratorio - Reglas básicas para síntesis sostenibles En el curso de la investigación sobre algunas reaccione incluidas en NOP se han podido identificar algunos
1 cal = 4,18 J. 1 kwh = 1000 Wh = 1000 W 3600 s/h = 3600 1000 J = 3 6 10 6 J
 Energía Se define la energía, como la capacidad para realizar un cambio en forma de trabajo. Se mide en el sistema internacional en Julios (J), que se define como el trabajo que realiza una fuerza de 1N
Energía Se define la energía, como la capacidad para realizar un cambio en forma de trabajo. Se mide en el sistema internacional en Julios (J), que se define como el trabajo que realiza una fuerza de 1N
E t = C e. m. (T f T i ) = 1. 3,5 (T f -20) =5 Kcal
 EJERCICIOS TEMA 1: LA ENERGÍA Y SU TRANSFORMACIÓN Ejercicio 1: Calcula la energía, en KWh, que ha consumido una máquina que tiene 40 CV y ha estado funcionando durante 3 horas. Hay que pasar la potencia
EJERCICIOS TEMA 1: LA ENERGÍA Y SU TRANSFORMACIÓN Ejercicio 1: Calcula la energía, en KWh, que ha consumido una máquina que tiene 40 CV y ha estado funcionando durante 3 horas. Hay que pasar la potencia
Ejemplo 2. Velocidad de arrastre en un alambre de cobre
 Ejemplo 1 Cual es la velocidad de desplazamiento de los electrones en un alambre de cobre típico de radio 0,815mm que transporta una corriente de 1 A? Si admitimos que existe un electrón libre por átomo
Ejemplo 1 Cual es la velocidad de desplazamiento de los electrones en un alambre de cobre típico de radio 0,815mm que transporta una corriente de 1 A? Si admitimos que existe un electrón libre por átomo
La radiación es el transporte o la propagación de energía en forma de partículas u
 La radiación es el transporte o la propagación de energía en forma de partículas u ondas. Si la radiación es debida a fuerzas eléctricas o magnéticas se llama radiación electromagnética. Pero la materia
La radiación es el transporte o la propagación de energía en forma de partículas u ondas. Si la radiación es debida a fuerzas eléctricas o magnéticas se llama radiación electromagnética. Pero la materia
2. ACTIVIDAD ACADÉMICA CÁLCULO EXPERIMENTAL DE PÉRDIDAS DE CARGA EN
 . ACTIVIDAD ACADÉMICA CÁLCULO EXPERIMENTAL DE PÉRDIDAS DE CARGA EN CONDUCCIONES A PRESIÓN.1. Introducción.. Descripción de la instalación fluidomecánica.3. Descripción de la actividad práctica.4. Conceptos
. ACTIVIDAD ACADÉMICA CÁLCULO EXPERIMENTAL DE PÉRDIDAS DE CARGA EN CONDUCCIONES A PRESIÓN.1. Introducción.. Descripción de la instalación fluidomecánica.3. Descripción de la actividad práctica.4. Conceptos
TRABAJO POTENCIA Y ENERGÍA
 TRABAJO POTENCIA Y ENERGÍA TRABAJO, POTENCIA Y ENERGÍA Todos habitualmente utilizamos palabras como trabajo, potencia o energía. En esta unidad precisaremos su significado en el contexto de la física;
TRABAJO POTENCIA Y ENERGÍA TRABAJO, POTENCIA Y ENERGÍA Todos habitualmente utilizamos palabras como trabajo, potencia o energía. En esta unidad precisaremos su significado en el contexto de la física;
Bases Físicas del Medio Ambiente. Propiedades y Procesos Térmicos
 Bases Físicas del Medio Ambiente Propiedades y Procesos Térmicos Programa IX. PROPIEDADES Y PROCESOS TÉRMICOS. (1h) Introducción. Dilatación térmica. Fases. Cambios de fase. Calores latentes. Superficies
Bases Físicas del Medio Ambiente Propiedades y Procesos Térmicos Programa IX. PROPIEDADES Y PROCESOS TÉRMICOS. (1h) Introducción. Dilatación térmica. Fases. Cambios de fase. Calores latentes. Superficies
DESCRIPCIÓN GENÉRICA DE UNA INSTALACIÓN DE ENERGÍA SOLAR TÉRMICA
 DESCRIPCIÓN GENÉRICA DE UNA INSTALACIÓN DE ENERGÍA SOLAR TÉRMICA DESCRIPCIÓN GENÉRICA DE LA TECNOLOGÍA DE LA ENERGÍA SOLAR TÉRMICA Introducción Un sistema de energía solar térmica es aquel que permite
DESCRIPCIÓN GENÉRICA DE UNA INSTALACIÓN DE ENERGÍA SOLAR TÉRMICA DESCRIPCIÓN GENÉRICA DE LA TECNOLOGÍA DE LA ENERGÍA SOLAR TÉRMICA Introducción Un sistema de energía solar térmica es aquel que permite
