Enseñanza - Aprendizaje.
|
|
|
- Luz Torregrosa Vargas
- hace 7 años
- Vistas:
Transcripción
1 Desde hace siglos el hombre consideró al átomo como una partícula componente de la materia. No podía verlo ni separarlo, pero su presencia fue admitida para explicar los diferentes fenómenos que se conocían. Enseñanza - Aprendizaje Enseñanza - Aprendizaje
2 A principios de siglo XIX (1805), John Dalton da un carácter diferente a las ideas asumidas por los filósofos griegos. Concibió al átomo como una masa propia, constituida por elementos, combinables con otras masas, y esta combinación se rige bajo las Leyes de proporciones definidas y múltiples. María del Pilar Rodríguez. Química. Primer año Ciclo Diversificado. Ed. Fundación Salesiana
3 Sin embargo, siempre se consideró al átomo como una masa compacta e indivisible, lo que no explicaba la afinidad de un elemento por otro, ni la presencia de las numerosas partículas que conocemos (protón, neutrón, etc.). La idea de una materia atómica compleja surge con el descubrimiento de la electricidad yulygualdron.blogspot.com
4 En William Crookes descubre una radiación luminosa que se produce en un tubo de vidrio que contenía un gas a baja presión, después de una descarga de alto voltaje.
5
6 andresysupandilla.blogspot.com
7 Los Rayos Catódicos son una radiación originada en el cátodo, después de aplicada una descarga de alto voltaje. Viaja en línea recta hasta el ánodo, es altamente energética, puede producir efectos mecánicos, y se desvían hacia la placa positiva de un campo eléctrico, lo que demuestra su carga negativa. María del Pilar Rodríguez. Química. Primer año Ciclo Diversificado. Ed. Fundación Salesiana
8 Las partículas tienen masa y producen el movimiento de las aspas al chocar contra ella. Su carga es negativa porque el haz se desvía hacia la placa positiva de un campo eléctrico. Las partículas que componen esta radiación se originan en cualquier gas, lo que demuestra que son componentes atómicos y se les llamó electrones.
9 Los rayos canales son una luminosidad que viaja en línea recta en dirección hacia el cátodo Los rayos anódicos o también llamados canales o positivos, son haces de rayos positivos constituidos por cationes atómicos o moleculares que se desplazan hacia el electrodo negativo en un tubo de crookes (es un tubo por donde circulan una serie de gases que al aplicarle electricidad adquieren fluorescencia), es un cono de vidrio con un ánodo y un cátodo.
10 Su carga positiva es igual o múltiplo de la carga del electrón. La masa y la carga de los rayos varían según el gas encerrado en el tubo generalmente es igual a la masa atómica de dicho gas. Son desviados por campos eléctricos y magnéticos desplazados hacia la parte negativa del campo Rayos canales
11 blog.latercera.com
12 Los rayos X, descubiertos por Roentgen en 1895, se producen en forma simultánea con lo catódicos y canales. Esta radiación impresiona una placa fotográfica atravesando una cartulina negra, viaja en línea recta y puede ionizar los gases. Demuestra una naturaleza neutra desde el punto de vista eléctrico, debido a que permanece inalterable frente a un campo de naturaleza eléctrica. blogs.vanguardia.com
13 Se disparan electrones a alta velocidad sobre una placa metálica, los electrones que están en las orbitas mas bajas de la placa metálica son expulsados de sus orbitas, al alejarse absorben la energía cinética de los electrones enviados a alta velocidad, cuando los electrones que fueron despojados de sus orbitas vuelven a su lugar, emiten los rayos X.
14 A finales del siglo XIX se intensificó su estudio por Bequerel y los esposos Curie. La radiactividad es de alto contenido energético, capaz de ionizar un gas, impresionar placas fotográficas, producir destellos de luz al incidir en compuestos como el sulfuro de zinc (ZnS). Al ser sometido a la acción de un campo magnético se distinguen tres tipos de partículas: positivas, negativas y neutras. María del Pilar Rodríguez. Química. Primer año Ciclo Diversificado. Ed. Fundación Salesiana
15 didactalia.net Consecuencias de la radiactividad
16 El electrón es una partícula que se encuentra en los elementos químicos, que su salida implica un contenido energético grande. El electrón (del griego clásico λεκτρον, ámbar), comúnmente representado por el símbolo: e, es una partícula subatómica con una carga eléctrica elemental negativa. Un electrón no tiene componentes o subestructura conocidos, en otras palabras, generalmente se define como una partícula elemental. centros5.pntic.mec.es
17 La carga del electrón fue medida con más cuidado por los físicos estadounidenses Robert Millikan y Harvey Fletcher mediante su experimento de la gota de aceite (1909), cuyos resultados fueron publicados en
18 Este experimento usaba un campo eléctrico para evitar que una gota de aceite cargada cayera como resultado de la gravedad. El aparato era capaz de medir la carga eléctrica tan pequeña como de 1 a 150 iones con un margen de error del 0,3%. es.wikipedia.org Aparato diseñado por Millikan para su experimento con la gota de aceite, circa
19 Consiste en un envase de vidrio, con dos placas metálicas dispuestas horizontalmente, que funcionan de electrodos para generar un campo magnético entre ellas. En la parte superior se encuentra un atomizador con aceite; y en el orificio, una malla que se encargará de dividir la gota de aceite en otras mas pequeñas. Además, con el frotamiento, se cargarán eléctricamente. La observación de la caída de las gotas se hará con un lente que se coloca en la zona intermedia entre las placas. Mientras no se conecte el campo magnético, la caída de las gotas son gobernadas por la fuerza de gravedad.
20 Cuando no hay conexión la gota cae en caída libre, de manera que la única fuerza que domina a la gota es la fuerza de gravedad F g F g = m. g Cuando si hay conexión la gota que cae está gobernada tanto por la fuerza de gravedad F g como por la fuerza eléctrica generada por el campo eléctrico generado (E) F e. Ambas fuerzas son iguales van en sentido contrario. E. q m. q m = masa q = carga de la partícula g = fuerza de gravedad F e F g q = m. g E m. g = E. q F g = m. g F e = E. q F g = F e
21 Todas las cargas que Millikan midió, fueron múltiplos enteros de un mismo número, deduciendo así que la carga mas pequeña observada era la del electrón. Los resultados demostraron ser simples múltiplos (entre 5 y 20 veces) de una carga básica: 1,602 x culombios. Se obtuvo el valor de 1, culombios para la carga del electrón Robert Millikan ( ) nació en Morrison (U.S.A.)
22 J.J. Thomson a finales del siglo XIX. El experimento tenía por objeto demostrar que los rayos catódicos podían desviarse mediante el uso de campos cruzados, y por tanto, se componían de partículas cargadas. Midiendo la desviación de estas partículas, Thomson pudo demostrar que todas las partículas tenían la misma relación carga a masa q/m y determinar este cociente. culombios/gr
23 Una vez conocida la relación carga/masa del electrón, la masa resultó fácil de calcular a partir del valor de la carga específica del electrón determinada por Millikan 1, coul/m = 1, coul/g = g masa del electrón es = g blogs.ua.es
ELECTRONES PROTONES NEUTRONES
 C U R S O: QUÍMICA COMÚN MATERIAL QC N 01 PARTÍCULAS SUBATÓMICAS ELECTRONES Partícula subatómica de carga negativa. Se ubica fuera del núcleo y su masa es de aproximadamente 9,11 10-28 gramos. La cantidad
C U R S O: QUÍMICA COMÚN MATERIAL QC N 01 PARTÍCULAS SUBATÓMICAS ELECTRONES Partícula subatómica de carga negativa. Se ubica fuera del núcleo y su masa es de aproximadamente 9,11 10-28 gramos. La cantidad
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA:
 INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA: DOCENTE: JOSÉ ROMÁN TIPO DE GUIA: CONCEPTUAL - EJERCITACION.
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA: DOCENTE: JOSÉ ROMÁN TIPO DE GUIA: CONCEPTUAL - EJERCITACION.
LA TEORIA ATOMICA John Dalton
 LA TEORIA ATOMICA En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que llamamos átomos 1766-1844
LA TEORIA ATOMICA En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que llamamos átomos 1766-1844
Nacimiento de la teoría cuántica Antecedentes
 Estructura de la Materia Nacimiento de la teoría cuántica Antecedentes Martha M. Flores Leonar FQ UNAM 10 de febrero de 2016 CONTENIDO Magnitudes atómicas Nacimiento de la teoría cuántica Descubrimiento
Estructura de la Materia Nacimiento de la teoría cuántica Antecedentes Martha M. Flores Leonar FQ UNAM 10 de febrero de 2016 CONTENIDO Magnitudes atómicas Nacimiento de la teoría cuántica Descubrimiento
Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea?
 Introducción Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea? Por ejemplo: Podrías predecir de que están elaborados los objetos y sustancias
Introducción Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea? Por ejemplo: Podrías predecir de que están elaborados los objetos y sustancias
Modelos Atómicos Objetivo:
 CORPORACION EDUCACIONAL JUAN XXIII COLEGIO "CARDENAL RAÚL SILVA HENRÍQUEZ" DEPARTAMENTO DE CIENCIAS QUÍMICA Modelos Atómicos Objetivo: Comprender la utilidad de los modelos atómicos y la teoría atómica
CORPORACION EDUCACIONAL JUAN XXIII COLEGIO "CARDENAL RAÚL SILVA HENRÍQUEZ" DEPARTAMENTO DE CIENCIAS QUÍMICA Modelos Atómicos Objetivo: Comprender la utilidad de los modelos atómicos y la teoría atómica
Atomos, Moleculas, y Iones
 Atomos, Moleculas, y Iones La teoría atómica de la materia John Dalton: Cada elemento esta compuesto por átomos. Todos los átomos de un elemento son iguales. En las reacciones químicas los átomos no sufren
Atomos, Moleculas, y Iones La teoría atómica de la materia John Dalton: Cada elemento esta compuesto por átomos. Todos los átomos de un elemento son iguales. En las reacciones químicas los átomos no sufren
Enseñanza - Aprendizaje
 El primer modelo atómico con bases científicas, fue formulado por John Dalton descubrió a los átomos en 1804. Pensaba que eran las partículas más pequeñas de la materia, que no podían ser divididas en
El primer modelo atómico con bases científicas, fue formulado por John Dalton descubrió a los átomos en 1804. Pensaba que eran las partículas más pequeñas de la materia, que no podían ser divididas en
Complejo Educacional Joaquín Edwards Bello QUIMICA 2º MEDIO TRABAJO 2 LEA CUIDADOSAMENTE EL SIGUIENTE TEXTO Y CONTESTE LAS PREGUNTAS
 Complejo Educacional Joaquín Edwards Bello QUIMICA 2º MEDIO TRABAJO 2 NOMBRE: CURSO: LEA CUIDADOSAMENTE EL SIGUIENTE TEXTO Y CONTESTE LAS PREGUNTAS..Naturaleza Eléctrica de la Materia La electricidad fue
Complejo Educacional Joaquín Edwards Bello QUIMICA 2º MEDIO TRABAJO 2 NOMBRE: CURSO: LEA CUIDADOSAMENTE EL SIGUIENTE TEXTO Y CONTESTE LAS PREGUNTAS..Naturaleza Eléctrica de la Materia La electricidad fue
MODELOS ATÓMICOS 2ª PARTE
 MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
Un modelo atómico, por lo tanto consiste en representar de manera grafica, la dimensión atómica de la materia. El objetivo de estos modelos es que el
 Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Tercero: una reacción química incluye sólo la separación combinación o reordenamiento de átomos sin crearlos o destruirlos.
 Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
MATERIAL DIDÁCTICO HISTORIA DEL MODELO ATÓMICO
 HISTORIA DEL MODELO ATÓMICO Descubrimiento de partículas subatómicas El verdadero desarrollo se alcanzo con el estudio de las descargas eléctricas a través de gases a baja presión. En 1964 William Crookes
HISTORIA DEL MODELO ATÓMICO Descubrimiento de partículas subatómicas El verdadero desarrollo se alcanzo con el estudio de las descargas eléctricas a través de gases a baja presión. En 1964 William Crookes
Atomos, Moléculas e Iones
 Atomo Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Atomo Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B.
 CAPITULO 4 ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B. Aproximadamente 400 a.c. el filosofo griego Democrito sugirió que toda la materia esta formada por partículas minúsculas, discretas e indivisibles,
CAPITULO 4 ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B. Aproximadamente 400 a.c. el filosofo griego Democrito sugirió que toda la materia esta formada por partículas minúsculas, discretas e indivisibles,
Atomos, Moléculas e Iones. Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo
 Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Atomo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Atomo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Origen del Concepto Átomo MODELOS ATÓMICOS. Teoría o Modelo Atómico de Dalton (1808) Qué es un modelo en Ciencias?
 MODELOS ATÓMICOS Origen del Concepto Átomo Demócrito: Siglo IV (A.C.) Fundador de la Escuela Atomista los átomos son indivisibles (átomo), y se distinguen por forma, tamaño, orden y posición. Los átomos
MODELOS ATÓMICOS Origen del Concepto Átomo Demócrito: Siglo IV (A.C.) Fundador de la Escuela Atomista los átomos son indivisibles (átomo), y se distinguen por forma, tamaño, orden y posición. Los átomos
TEMA 7: ELEMENTOS Y COMPUESTOS
 TEMA 7: ELEMENTOS Y COMPUESTOS FÍSICA Y QUÍMICA 4º ESO IES ZOCO LAS PARTÍCULAS DEL ÁTOMO MODELO ATÓMICO DE DALTON Cada elemento químico se compone de partículas diminutas e indestructibles denominadas
TEMA 7: ELEMENTOS Y COMPUESTOS FÍSICA Y QUÍMICA 4º ESO IES ZOCO LAS PARTÍCULAS DEL ÁTOMO MODELO ATÓMICO DE DALTON Cada elemento químico se compone de partículas diminutas e indestructibles denominadas
Unidad II 2.1 Estructura del átomo
 Unidad II 2.1 Estructura del átomo Química general I Alfonso Rito Norma López 1 El átomo en la antigüedad Demócrito introdujo el concepto de átomo, como la constitución de la materia por partículas indivisibles.
Unidad II 2.1 Estructura del átomo Química general I Alfonso Rito Norma López 1 El átomo en la antigüedad Demócrito introdujo el concepto de átomo, como la constitución de la materia por partículas indivisibles.
UNIDAD 2. Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos.
 UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
U N A M. Facultad de Ingeniería MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON
 MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS. TEMA 7 Pág. 155 libro nuevo
 PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
- Electrización, conductividad eléctrica y calórica, emisión y absorción de luz, según el modelo atómico.
 Temas a tratar: - Constitución atómica y microscópica de la materia: átomo y molécula. - Teoría Atómica de Dalton y Modelos Atómicos. - Electrización, conductividad eléctrica y calórica, emisión y absorción
Temas a tratar: - Constitución atómica y microscópica de la materia: átomo y molécula. - Teoría Atómica de Dalton y Modelos Atómicos. - Electrización, conductividad eléctrica y calórica, emisión y absorción
TEMA 1 NATURALEZA ELÉCTRICA DE LA MATERIA
 TEMA 1 NATURALEZA ELÉCTRICA DE LA MATERIA Hoy en día el mundo científico tiene una idea lo suficientemente precisa de la estructura atómica, como para poder explicar el comportamiento de los átomos y moléculas
TEMA 1 NATURALEZA ELÉCTRICA DE LA MATERIA Hoy en día el mundo científico tiene una idea lo suficientemente precisa de la estructura atómica, como para poder explicar el comportamiento de los átomos y moléculas
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete. Núcleo. (protones y neutrones)
 Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
El concepto atomista comienza con las ideas de Leucipo y Demócrito, según ellos:
 CURSO: QUÍMICA MENCIÓN MATERIAL QM N 01 PARTÍCULAS SUBATÓMICAS LOS ELECTRONES El funcionamiento de una ampolleta es bastante simple, un haz de electrones (corriente eléctrica) atraviesa un delgado filamento
CURSO: QUÍMICA MENCIÓN MATERIAL QM N 01 PARTÍCULAS SUBATÓMICAS LOS ELECTRONES El funcionamiento de una ampolleta es bastante simple, un haz de electrones (corriente eléctrica) atraviesa un delgado filamento
Teoría atómica de la materia Demócrito ( a.c.): el mundo material está formado de pequeñas partículas indestructibles (átomos), desprovistas de
 UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
ESTRUCTURA ATOMICA FINES DEL SIGLO XIX Y COMIENZOS DEL SIGLO XX
 ESTRUCTURA ATOMICA FINES DEL SIGLO XIX Y COMIENZOS DEL SIGLO XX William Crookes, (1832-1919). Químico y Físico inglés. Inventó y diseñó el tubo electrónico conocido como «tubo de Crookes». Demostró que
ESTRUCTURA ATOMICA FINES DEL SIGLO XIX Y COMIENZOS DEL SIGLO XX William Crookes, (1832-1919). Químico y Físico inglés. Inventó y diseñó el tubo electrónico conocido como «tubo de Crookes». Demostró que
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
TEMA 5 Estructura del átomo. IES Sierra de San Quílez Departamento de Física y Química
 TEMA 5 Estructura del átomo IES Sierra de San Quílez Departamento de Física y Química El átomo Naturaleza eléctrica de la materia Fenómenos eléctricos Algunos fenómenos de electrización pusieron de manifiesto
TEMA 5 Estructura del átomo IES Sierra de San Quílez Departamento de Física y Química El átomo Naturaleza eléctrica de la materia Fenómenos eléctricos Algunos fenómenos de electrización pusieron de manifiesto
ESTRUCTURA ATÓMICA DE LA MATERIA
 ESTRUCTURA ATÓMICA DE LA MATERIA 1.MODELOS ATÓMICOS: EVOLUCIÓN HISTÓRICA. Fueron los griegos los primeros en profundizar en el conocimiento de la estructura íntima de la materia. Postularon que la materia
ESTRUCTURA ATÓMICA DE LA MATERIA 1.MODELOS ATÓMICOS: EVOLUCIÓN HISTÓRICA. Fueron los griegos los primeros en profundizar en el conocimiento de la estructura íntima de la materia. Postularon que la materia
Técnico Profesional QUÍMICA
 Convenio Programa Técnico Profesional QUÍMICA Modelos atómicos, estructura atómica y tipos de átomos Nº Ejercicios PSU 1. Rutherford, luego de realizar pruebas con una lámina de oro bombardeada por partículas
Convenio Programa Técnico Profesional QUÍMICA Modelos atómicos, estructura atómica y tipos de átomos Nº Ejercicios PSU 1. Rutherford, luego de realizar pruebas con una lámina de oro bombardeada por partículas
COMO SE DESCUBRIO EL ATOMO?
 COMO SE DESCUBRIO EL ATOMO? OBJETIVO: Caracterizar la estructura interna de la materia, basándose en los modelos atómicos desarrollados por los científicos a través del tiempo Átomo: Unidad más pequeña
COMO SE DESCUBRIO EL ATOMO? OBJETIVO: Caracterizar la estructura interna de la materia, basándose en los modelos atómicos desarrollados por los científicos a través del tiempo Átomo: Unidad más pequeña
Estructura de la Materia
 Estructura de la Materia Antes de 1800, se pensaba que la materia era continua, es decir que podía ser dividida en infinitas partes más pequeñas sin cambiar la naturaleza del elemento. Sin embargo, alrededor
Estructura de la Materia Antes de 1800, se pensaba que la materia era continua, es decir que podía ser dividida en infinitas partes más pequeñas sin cambiar la naturaleza del elemento. Sin embargo, alrededor
EL ÁTOMO Modelos Atómicos
 EL ÁTOMO Modelos Atómicos Cómo está formada la materia en su interior? Desde los tiempos de la antigua Grecia,los pensadores venían haciéndose esta pregunta, acerca de cómo estaba constituida la materia
EL ÁTOMO Modelos Atómicos Cómo está formada la materia en su interior? Desde los tiempos de la antigua Grecia,los pensadores venían haciéndose esta pregunta, acerca de cómo estaba constituida la materia
ESTRUCTURA ATÓMICA MATERIA. Todo aquello que tiene un lugar en el espacio y tiene masa
 ESTRUCTURA ATÓMICA Todo aquello que tiene un lugar en el espacio y tiene masa MATERIA Sustancia: composición constante y definida y propiedades distintivas 1 3 TIPOS DE SUSTANCIAS: MEZCLA ELEMENTO (112)
ESTRUCTURA ATÓMICA Todo aquello que tiene un lugar en el espacio y tiene masa MATERIA Sustancia: composición constante y definida y propiedades distintivas 1 3 TIPOS DE SUSTANCIAS: MEZCLA ELEMENTO (112)
Guía N 8 Modelos atómicos
 Nivel Octavo Básico Guía N 8 Modelos atómicos Nombre... Curso Eje: Materia y sus transformaciones Objetivos: Conocer los diferentes modelos atómicos que han surgido a través de los años, como también los
Nivel Octavo Básico Guía N 8 Modelos atómicos Nombre... Curso Eje: Materia y sus transformaciones Objetivos: Conocer los diferentes modelos atómicos que han surgido a través de los años, como también los
2 La carga del electrón fue determinada por primera vez en: D Difracción de electrones a partir del papel de aluminio.
 Slide 1 / 32 1 Un Tubo de Crooke (un tubo que contiene gas rarificado a través del cual se hace pasar una corriente entre un cátodo y un ánodo) fue utilizado en el descubrimiento del electrón por: A R.
Slide 1 / 32 1 Un Tubo de Crooke (un tubo que contiene gas rarificado a través del cual se hace pasar una corriente entre un cátodo y un ánodo) fue utilizado en el descubrimiento del electrón por: A R.
Teoría de DALTON. Hechos experimentales que evidencian una estructura interna de átomo.
 Teoría de DALTON. 1- Los elementos químicos están construidos por partículas denominadas átomos, que son invisibles e inalterables, en cualquier proceso, químico o físico. 2- Los átomos de un mismo elemento,
Teoría de DALTON. 1- Los elementos químicos están construidos por partículas denominadas átomos, que son invisibles e inalterables, en cualquier proceso, químico o físico. 2- Los átomos de un mismo elemento,
CONSTITUCIÓN DE LA MATERIA. Colegio San Esteban Diácono Departamento de Ciencias 8 Año Básico 2016
 CONSTITUCIÓN DE LA MATERIA Colegio San Esteban Diácono Departamento de Ciencias 8 Año Básico 2016 Qué es la Química? Es una ciencia que estudia la materia, sus propiedades, su composición, su estructura
CONSTITUCIÓN DE LA MATERIA Colegio San Esteban Diácono Departamento de Ciencias 8 Año Básico 2016 Qué es la Química? Es una ciencia que estudia la materia, sus propiedades, su composición, su estructura
25 12 Mg. 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores.
 MINIPRUEBA CLASE 02 25 12 Mg 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores. 25 12 Mg Z 2. Se puede afirmar que: I) La masa del electrón es aproximadamente
MINIPRUEBA CLASE 02 25 12 Mg 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores. 25 12 Mg Z 2. Se puede afirmar que: I) La masa del electrón es aproximadamente
Física Cuántica y Modelos atómicos. Preguntas de Capítulo. 1. Cómo se determinó que los rayos catódicos poseían una carga negativa?
 Física Cuántica y Modelos atómicos. Preguntas de Capítulo 1. Cómo se determinó que los rayos catódicos poseían una carga negativa? 2. J. J. Thomson encontró que los rayos catódicos están partículas, a
Física Cuántica y Modelos atómicos. Preguntas de Capítulo 1. Cómo se determinó que los rayos catódicos poseían una carga negativa? 2. J. J. Thomson encontró que los rayos catódicos están partículas, a
Estructura íntima de la materia
 Estructura íntima de la materia El átomo clásico José Mauricio Rodas Rodríguez Curso de Química Inorgánica Licenciatura en Biología y Química Universidad de Caldas 22 de junio de 2015 1 / J.M. Rodas www.maurorodas.com
Estructura íntima de la materia El átomo clásico José Mauricio Rodas Rodríguez Curso de Química Inorgánica Licenciatura en Biología y Química Universidad de Caldas 22 de junio de 2015 1 / J.M. Rodas www.maurorodas.com
Modelos atómicos. JOHN DALTON: Modelo atómico en forma de esfera
 M1 Modelos atómicos JOHN DALTON: Modelo atómico en forma de esfera Muchos años después de que se planteó la existencia de los átomos y que éstos eran la parte fundamental de todo lo que fuera materia,
M1 Modelos atómicos JOHN DALTON: Modelo atómico en forma de esfera Muchos años después de que se planteó la existencia de los átomos y que éstos eran la parte fundamental de todo lo que fuera materia,
El mundo material: los átomos. Física y Química 2º ESO
 El mundo material: los átomos Física y Química 2º ESO Viaje a lo más profundo de la materia Oxford University Press España, S. A. Física y Química 2º ESO 2 Hoy en día sabemos que la materia está constituida
El mundo material: los átomos Física y Química 2º ESO Viaje a lo más profundo de la materia Oxford University Press España, S. A. Física y Química 2º ESO 2 Hoy en día sabemos que la materia está constituida
DESCUBRIMIENTO DEL ÁTOMO
 C U R S O: QUÍMICA COMÚN MATERIAL QC- N 01 DESCUBRIMIENTO DEL ÁTOMO MARIE SKŁODOWSKA (1856-1940) (MADAME CURIE) Física Polaca de talento y dedicación sencillamente brillantes. Esposa de Pierre Curie, un
C U R S O: QUÍMICA COMÚN MATERIAL QC- N 01 DESCUBRIMIENTO DEL ÁTOMO MARIE SKŁODOWSKA (1856-1940) (MADAME CURIE) Física Polaca de talento y dedicación sencillamente brillantes. Esposa de Pierre Curie, un
LA LA ESTRUCTURA DE LA MATERIA. 1.-Desarrollo histórico del concepto de átomo. Teoría de Demócrito. Teoría de Dalton. Componentes del átomo
 ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
ÁTOMO..su historia y su estudio
 ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
Tema 2. Estructura atómica y sistema periódico
 Tema 2. Estructura atómica y sistema periódico Dalton: átomos par9culas indivisibles Nuevos experimentos: átomos cons>tuidos por unidades más pequeñas: par9culas subatómicas 1. Primeras evidencias de la
Tema 2. Estructura atómica y sistema periódico Dalton: átomos par9culas indivisibles Nuevos experimentos: átomos cons>tuidos por unidades más pequeñas: par9culas subatómicas 1. Primeras evidencias de la
LOS ÁTOMOS. En una reacción química, la masa total de los reactivos es igual a la masa total de las sustancias obtenidas tras el proceso.
 LOS ÁTOMOS 1. LEYES PONDERALES. MODELO ATÓMICO DE DALTON Se denominan leyes ponderales de las reacciones químicas aquellas que establecen las proporciones de los pesos en cualquier proceso químico. Son
LOS ÁTOMOS 1. LEYES PONDERALES. MODELO ATÓMICO DE DALTON Se denominan leyes ponderales de las reacciones químicas aquellas que establecen las proporciones de los pesos en cualquier proceso químico. Son
Iván Carmona Flores Prof. Química y Cs. EL ÁTOMO
 EL ÁTOMO Antecedentes históricos Lo que vemos a nuestro alrededor son materiales: el plástico, el cobre del cable eléctrico, el agua que bebemos o el azúcar del café. La palabra materia proviene del latín
EL ÁTOMO Antecedentes históricos Lo que vemos a nuestro alrededor son materiales: el plástico, el cobre del cable eléctrico, el agua que bebemos o el azúcar del café. La palabra materia proviene del latín
UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS. 1.3 El sol, horno nuclear
 UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS 1.3 El sol, horno nuclear RADIACTIVIDAD Y DESINTEGRACIÓN NUCLEAR HISTORIA DEL ÁTOMO Hace aproximadamente 2500 años, los filósofos griegos, afirmaron que la
UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS 1.3 El sol, horno nuclear RADIACTIVIDAD Y DESINTEGRACIÓN NUCLEAR HISTORIA DEL ÁTOMO Hace aproximadamente 2500 años, los filósofos griegos, afirmaron que la
3 Estructura atómica de la materia
 3 Estructura atómica de la materia 1 Las leyes fundamentales de la química onservación de la masa y proporciones definidas uando hacemos reaccionar dos elementos químicos para formar un compuesto, se cumplen
3 Estructura atómica de la materia 1 Las leyes fundamentales de la química onservación de la masa y proporciones definidas uando hacemos reaccionar dos elementos químicos para formar un compuesto, se cumplen
CENTRO DE ESTUDIOS MIRASIERRA
 El ÁTOMO TEORÏAS ATÓMICAS1 Ya hemos visto el modelo atómico de Dalton, que decía que la materia estaba formada por partículas indivisibles llamadas átomos. Actualmente, se sabe que los átomos si son divisibles
El ÁTOMO TEORÏAS ATÓMICAS1 Ya hemos visto el modelo atómico de Dalton, que decía que la materia estaba formada por partículas indivisibles llamadas átomos. Actualmente, se sabe que los átomos si son divisibles
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV
 M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
TEMA 3: Hasta el momento, hemos visto que la materia se consideraba algo continuo e indivisible hasta que se
 TEMA 3: ESTRUCTURA ATÓMICA I Hasta el momento, hemos visto que la materia se consideraba algo continuo e indivisible hasta que se confirmó que era posible dividirla en partículas más pequeñas, a las que
TEMA 3: ESTRUCTURA ATÓMICA I Hasta el momento, hemos visto que la materia se consideraba algo continuo e indivisible hasta que se confirmó que era posible dividirla en partículas más pequeñas, a las que
TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA
 TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. MATERIA DIVISIBLE O INDIVISIBLE El término átomo aparece en el siglo IV a.c. para designar a la porción indivisible más pequeña que
TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. MATERIA DIVISIBLE O INDIVISIBLE El término átomo aparece en el siglo IV a.c. para designar a la porción indivisible más pequeña que
QUIMICA GENERAL. Docente : Raquel Villafrades Torres
 Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Estructura atómica. El sistema periódico
 Estructura atómica. El sistema periódico 1. Es el átomo una esfera de materia, homogénea y maciza? Explícalo. 2. Indica la diferencia entre número atómico y másico. Define isótopo. 3. Por qué la mayoría
Estructura atómica. El sistema periódico 1. Es el átomo una esfera de materia, homogénea y maciza? Explícalo. 2. Indica la diferencia entre número atómico y másico. Define isótopo. 3. Por qué la mayoría
4ª UNIDAD LOS ÁTOMOS Y SU COMPLEJIDAD
 4ª UNIDAD LOS ÁTOMOS Y SU COMPLEJIDAD FÍSICA Y QUÍMICA 3º ESO 3º E.S.O. Grupo Apellidos: Nombre: MODELOS ATÓMICOS (Resumen de los apartados 1 y 2 del tema 4) A principios del siglo XIX John Dalton propuso
4ª UNIDAD LOS ÁTOMOS Y SU COMPLEJIDAD FÍSICA Y QUÍMICA 3º ESO 3º E.S.O. Grupo Apellidos: Nombre: MODELOS ATÓMICOS (Resumen de los apartados 1 y 2 del tema 4) A principios del siglo XIX John Dalton propuso
EXPERIMENTO DE J. J. THOMSON
 EXPERIMENTO DE J. J. THOMSON (Determinación de la Relación Carga/Masa de los Electrones) M. C. Q. Alfredo Velásquez Márquez Tubo de Geissler (~1857) Con gas a presión normal se observa poca conductividad,
EXPERIMENTO DE J. J. THOMSON (Determinación de la Relación Carga/Masa de los Electrones) M. C. Q. Alfredo Velásquez Márquez Tubo de Geissler (~1857) Con gas a presión normal se observa poca conductividad,
Clase 4:Radiación del cuerpo, efecto fotoeléctrico y modelos atómicos
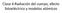 Clase 4:Radiación del cuerpo, efecto fotoeléctrico y modelos atómicos El experimento de Millikan Determina la carga del electrón 1.602 x 10-19 C Atomizador de gotas de aceite Fuente de Rayos X (ioniza
Clase 4:Radiación del cuerpo, efecto fotoeléctrico y modelos atómicos El experimento de Millikan Determina la carga del electrón 1.602 x 10-19 C Atomizador de gotas de aceite Fuente de Rayos X (ioniza
Teoría es un principio unificador que explica un conjunto de hechos y aquellas leyes que se basan en ellos.
 Página 1 de 6 Repaso de Química 105 I. Método científico Pasos Basicos Observación Representación Interpretación Hipótesis explicación tentativa de un problema. Nos guia para planear experimentos adicionales.
Página 1 de 6 Repaso de Química 105 I. Método científico Pasos Basicos Observación Representación Interpretación Hipótesis explicación tentativa de un problema. Nos guia para planear experimentos adicionales.
Evolución de los modelos atómicos
 Evolución de los modelos atómicos Un paso importante hacia el desarrollo de la química como ciencia fue el desarrollo de la comprensión de la estructura atómica. Por ejemplo, era posible comprender lo
Evolución de los modelos atómicos Un paso importante hacia el desarrollo de la química como ciencia fue el desarrollo de la comprensión de la estructura atómica. Por ejemplo, era posible comprender lo
La Teoría Cuántica Preguntas de Multiopcion
 Slide 1 / 71 La Teoría Cuántica Preguntas de Multiopcion Slide 2 / 71 1 El experimento de "rayos catódicos" se asocia con: A B C D E Millikan Thomson Townsend Plank Compton Slide 3 / 71 2 La carga del
Slide 1 / 71 La Teoría Cuántica Preguntas de Multiopcion Slide 2 / 71 1 El experimento de "rayos catódicos" se asocia con: A B C D E Millikan Thomson Townsend Plank Compton Slide 3 / 71 2 La carga del
Como esta formada la materia?
 Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Hecho por: Patricia Arroyo Gamallo nº 2 4ºeso C
 Hecho por: Patricia Arroyo Gamallo nº 2 4ºeso C La materia es todo aquello que tiene masa, ocupa un lugar en el espacio y es cuantificable (se puede medir).la Química es la ciencia que estudia su naturaleza,
Hecho por: Patricia Arroyo Gamallo nº 2 4ºeso C La materia es todo aquello que tiene masa, ocupa un lugar en el espacio y es cuantificable (se puede medir).la Química es la ciencia que estudia su naturaleza,
Tabla Periódica. Fundamentos de Química
 Tabla Periódica Fundamentos de Química Contenido La Teoría Atómica de la Materia El Descubrimiento de la Estructura Atómica La Visión Moderna de la Estructura Atómica Pesos Atómicos La Tabla Periódica
Tabla Periódica Fundamentos de Química Contenido La Teoría Atómica de la Materia El Descubrimiento de la Estructura Atómica La Visión Moderna de la Estructura Atómica Pesos Atómicos La Tabla Periódica
2º Bachillerato. Química. Unidad 1 (Estructura atómica de la materia). Fotocopia 1.
 Partículas subatómicas Los átomos están formados por un núcleo (formado por protones y neutrones) rodeado por una nube de electrones, que se encuentran en la corteza. Entre núcleo y corteza hay espacio
Partículas subatómicas Los átomos están formados por un núcleo (formado por protones y neutrones) rodeado por una nube de electrones, que se encuentran en la corteza. Entre núcleo y corteza hay espacio
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín. El átomo.
 Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
BLOQUE III Explicas el modelo atómico actual y sus aplicaciones
 Explicas el modelo atómico actual y sus aplicaciones Qué es un modelo atómico? Representación estructural de un átomo, cuyo fin es explicar sus propiedades y funcionamiento. Demócrito y Leucipo (Siglo
Explicas el modelo atómico actual y sus aplicaciones Qué es un modelo atómico? Representación estructural de un átomo, cuyo fin es explicar sus propiedades y funcionamiento. Demócrito y Leucipo (Siglo
MODELOS ATÓMICOS. Nombre y Apellidos:... Grupo:... Correctas Incorrectas Nota
 MODELOS ATÓMICOS Nombre y Apellidos:........................................ Grupo:........... 1.- Cuestionario (7 ptos) Correctas Incorrectas Nota 1.- El siguiente dibujo corresponde al modelo de: a)
MODELOS ATÓMICOS Nombre y Apellidos:........................................ Grupo:........... 1.- Cuestionario (7 ptos) Correctas Incorrectas Nota 1.- El siguiente dibujo corresponde al modelo de: a)
LiceoTolimense Química Séptimo 1 Periodo ESTRUCTURA INTERNA DE LA MATERIA
 ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
Clase N 1. Modelo Atómico I
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Teoría atómica, números cuánticos y configuración electrónica. Química 2016 PSU
 Teoría atómica, números cuánticos y configuración electrónica Química 2016 PSU Teoría atómica de Dalton. El trabajo de Dalton marcó el principio de la química moderna entre los años 1803 y 1808, proponiendo
Teoría atómica, números cuánticos y configuración electrónica Química 2016 PSU Teoría atómica de Dalton. El trabajo de Dalton marcó el principio de la química moderna entre los años 1803 y 1808, proponiendo
DEPARTAMENTO DE QUÍMICA SERIE DE EJERCICIOS. Tema 1: Estructura Atómica Semestre
 DEPARTAMENTO DE QUÍMICA SERIE DE EJERCICIOS (Basada en reactivos de exámenes colegiados) Tema 1: Estructura Atómica Semestre 2017-2 Experimento de Thomson 1. En un experimento como el de Thomson, un haz
DEPARTAMENTO DE QUÍMICA SERIE DE EJERCICIOS (Basada en reactivos de exámenes colegiados) Tema 1: Estructura Atómica Semestre 2017-2 Experimento de Thomson 1. En un experimento como el de Thomson, un haz
ORÍGENES DE LA TEORÍA ATÓMICA
 ...Naturaleza Eléctrica de la Materia MODELOS ATÓMICOS La electricidad fue por primera vez observada por Thales de Mileto en el siglo VI a.c. Frotó un trozo de ámbar con un paño y vio como las briznas
...Naturaleza Eléctrica de la Materia MODELOS ATÓMICOS La electricidad fue por primera vez observada por Thales de Mileto en el siglo VI a.c. Frotó un trozo de ámbar con un paño y vio como las briznas
ESTRUCTURA ATOMICA DESARROLLO HISTORICO
 ESTRUCTURA ATOMICA DESARROLLO HISTORICO MODELOS ATOMICOS Átomo: Partícula más pequeña de un elemento que retiene sus propiedades. DEMOCRITO Y LEUCIPO. En el Siglo V A.C. dos Filósofos Griegos Leucipo y
ESTRUCTURA ATOMICA DESARROLLO HISTORICO MODELOS ATOMICOS Átomo: Partícula más pequeña de un elemento que retiene sus propiedades. DEMOCRITO Y LEUCIPO. En el Siglo V A.C. dos Filósofos Griegos Leucipo y
Átomos, moléculas y iones
 Átomos, moléculas y iones Capítulo 2 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. La teoría atómica de Dalton (1808) 1. Los elementos están formados por partículas
Átomos, moléculas y iones Capítulo 2 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. La teoría atómica de Dalton (1808) 1. Los elementos están formados por partículas
QUÍMICA COMÚN QC-01 L O S M O D E L O S A T Ó M I C O S
 QUÍMICA COMÚN QC-01 L O S M O D E L O S A T Ó M I C O S 2013 TEORÍA ATÓMICA LA QUÍMICA EN GRECIA Hacia el 600 A.C. se inició en Grecia el primer intento por responder la composición de la materia y la
QUÍMICA COMÚN QC-01 L O S M O D E L O S A T Ó M I C O S 2013 TEORÍA ATÓMICA LA QUÍMICA EN GRECIA Hacia el 600 A.C. se inició en Grecia el primer intento por responder la composición de la materia y la
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO
 UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
Modelo atómico de la materia.
 Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
TEMA 3 LA MATERIA Y SU ESTRUCTURA
 TEMA 3 LA MATERIA Y SU ESTRUCTURA 1. Clasificación de la materia (página 58) Def. Sistema material: Es una porción de materia seleccionada para su estudio. Def. Sustancia pura: Decimos que una sustancia
TEMA 3 LA MATERIA Y SU ESTRUCTURA 1. Clasificación de la materia (página 58) Def. Sistema material: Es una porción de materia seleccionada para su estudio. Def. Sustancia pura: Decimos que una sustancia
J.J Thomson propone el primer modelo de átomo:
 MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
El átomo y el sistema periódico
 El átomo y el sistema periódico Conceptos previos Notación A-Z Conceptos previos En las reacciones químicas se cumple: 1) La ley de conservación de la masa 2) La ley de proporciones definidas Modelos atómicos
El átomo y el sistema periódico Conceptos previos Notación A-Z Conceptos previos En las reacciones químicas se cumple: 1) La ley de conservación de la masa 2) La ley de proporciones definidas Modelos atómicos
Modelo atómico de Dalton(1808)
 El átomo Modelos atómicos Como no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
El átomo Modelos atómicos Como no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO. Lola Castelao
 ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
Física Cuántica Problemas de Practica AP Física B de PSI
 Física Cuántica Problemas de Practica AP Física B de PSI Nombre 1. El experimento de "rayos catódicos" se asocia con: (A) R. A. Millikan (B) J. J. Thomson (C) J. S. Townsend (D) M. Plank (E) A. H. Compton
Física Cuántica Problemas de Practica AP Física B de PSI Nombre 1. El experimento de "rayos catódicos" se asocia con: (A) R. A. Millikan (B) J. J. Thomson (C) J. S. Townsend (D) M. Plank (E) A. H. Compton
NOME CURSO. b) El cálculo de los potenciales es simple, teniendo en cuenta que el potencial es una magnitud escalar:
 Cañiza, de abril de 004. NOM CURSO 1.- n dous dos vértices dun cadrado de 5 cm de lado están situados dúas cargas puntuais de q1 = +45 e q = -45 nc, respectivamente. Calcula: a) O campo eléctrico no vértice
Cañiza, de abril de 004. NOM CURSO 1.- n dous dos vértices dun cadrado de 5 cm de lado están situados dúas cargas puntuais de q1 = +45 e q = -45 nc, respectivamente. Calcula: a) O campo eléctrico no vértice
LA ESTRUCTURA DEL ÁTOMO
 LA ESTRUCTURA DEL ÁTOMO 1 1.- EL ÁTOMO EN LA ANTIGÜEDAD Los filósofos griegos discutieron mucho acerca de la naturaleza de la materia y concluyeron que el mundo era más simple de lo que parecía. Algunas
LA ESTRUCTURA DEL ÁTOMO 1 1.- EL ÁTOMO EN LA ANTIGÜEDAD Los filósofos griegos discutieron mucho acerca de la naturaleza de la materia y concluyeron que el mundo era más simple de lo que parecía. Algunas
RELACIÓN CARGA - MASA DEL ELECTRÓN
 Práctica 5 RELACIÓN CARGA - MASA DEL ELECTRÓN OBJETIVO Determinar la relación carga-masa del electrón (e/m e ), a partir de las trayectorias observadas de un haz de electrones que cruza una región en la
Práctica 5 RELACIÓN CARGA - MASA DEL ELECTRÓN OBJETIVO Determinar la relación carga-masa del electrón (e/m e ), a partir de las trayectorias observadas de un haz de electrones que cruza una región en la
2.- Los átomos de un mismo elemento son iguales en masa y propiedades. Y los átomos de elementos diferentes son diferentes en masa y propiedades.
 FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
4º E.S.O. FÍSICA Y QUÍMICA 2. ÁTOMOS Y SISTEMA PERIÓDICO. Dpto. de Física y Química. R. Artacho
 4º E.S.O. FÍSICA Y QUÍMICA 2. ÁTOMOS Y SISTEMA PERIÓDICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Las partículas y el átomo 2. Modelos atómicos 3. Distribución de los electrones en un
4º E.S.O. FÍSICA Y QUÍMICA 2. ÁTOMOS Y SISTEMA PERIÓDICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Las partículas y el átomo 2. Modelos atómicos 3. Distribución de los electrones en un
EL ÁTOMO. Departamento de Física y Química 3º ESO
 EL ÁTOMO Departamento de Física y Química 3º ESO 0. Mapa conceptual Metales No metales Tabla periódica Elementos Cationes Isótopos ÁTOMO Iones Aniones Protones Núcleo Neutrones Electrones Número atómico
EL ÁTOMO Departamento de Física y Química 3º ESO 0. Mapa conceptual Metales No metales Tabla periódica Elementos Cationes Isótopos ÁTOMO Iones Aniones Protones Núcleo Neutrones Electrones Número atómico
7.- Los corpúsculos de energía sin masa de la radiación electromagnética recibe el nombre de: a) Muones b) Electrones c) Rayos X d) Fotones
 EXAMEN PARCIAL 1.- El número de protones de un átomo se denomina a) número atómico A b) número másico A c) número atómico Z d) número másico Z 2.- En el núcleo se encuentran: a) Los protones y neutrones
EXAMEN PARCIAL 1.- El número de protones de un átomo se denomina a) número atómico A b) número másico A c) número atómico Z d) número másico Z 2.- En el núcleo se encuentran: a) Los protones y neutrones
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual Teoría atómica I: modelos atómicos, estructura atómica y tipos de átomos SGUICES001CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 B Aplicación
SOLUCIONARIO Guía Estándar Anual Teoría atómica I: modelos atómicos, estructura atómica y tipos de átomos SGUICES001CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 B Aplicación
Unidad I: Propiedades Periódicas: Masa y Enlace
 Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
MAGNETISMO. MsC Alexander Pérez García Video 1
 MAGNETISMO MsC Alexander Pérez García Video 1 http://www.dailymotion.com/video/xqqir9_campomagnetico-terrestre-inversion-de-los-polos_school FUERZA MAGNÉTICA SOBRE UNA CARGA EN MOVIMIENTO LA SEGUNDA
MAGNETISMO MsC Alexander Pérez García Video 1 http://www.dailymotion.com/video/xqqir9_campomagnetico-terrestre-inversion-de-los-polos_school FUERZA MAGNÉTICA SOBRE UNA CARGA EN MOVIMIENTO LA SEGUNDA
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye
 Características esenciales de las reacciones químicas A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye Joseph Louis Proust (formación de CuCO 3 ): los elementos que
Características esenciales de las reacciones químicas A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye Joseph Louis Proust (formación de CuCO 3 ): los elementos que
