GUÍA de de PRÁCTICAS de de TÉCNICAS ANALÍTICAS
|
|
|
- Óscar Ortiz de Zárate Gil
- hace 6 años
- Vistas:
Transcripción
1 GUÍA de de PRÁCTICAS de de TÉCNICAS ANALÍTICAS 1 sesión explicativa 5 sesiones prácticas 1 examen de cuestiones (último día pract.) 1 Informe (1 semana después) Salvador Sagrado sagrado@uv.es Dpto. Q. Analítica (Farmacia)
2 ANÁLISIS ANALITOS MUESTRAS 1) AMOXICILINA MEDICAMENTO 2) DUREZA (Ca, Mg) AGUA 3) QUININA TONICA 4) SULFAMIDA MEDICAMENTO 5) ALCOHOLES BEBIDAS
3 ANÁLISIS ANALITOS MUESTRAS TÉCNICA (método) 1) AMOXICILINA MEDICAMENTO VOLUMETRÍA (no acuoso) 2) DUREZA (Ca, Mg) AGUA VOLUMETRÍA 3) QUININA TONICA FLUORIMETRÍA 4) SULFAMIDA MEDICAMENTO ESPECTROFOTOMETRÍA (Vis.) 5) ALCOHOLES BEBIDAS CROMATOGRAFÍA (gases)
4 ANÁLISIS ANALITOS MUESTRAS 1) AMOXICILINA MEDICAMENTO RIESGOS: - Propipeta-pipeta - ácido acético 2) DUREZA (Ca, Mg) AGUA 3) QUININA TONICA 4) SULFAMIDA MEDICAMENTO 5) ALCOHOLES BEBIDAS
5 ANÁLISIS ANALITOS MUESTRAS 1) AMOXICILINA MEDICAMENTO ERRORES TÉCNICOS: - Pesada (m p vs. m M )*, contaminación (espátula) - perdidas (varilla) 2) DUREZA (Ca, Mg) AGUA 3) QUININA TONICA 4) SULFAMIDA MEDICAMENTO - contaminación (material) 5) ALCOHOLES BEBIDAS * pesando en un vaso limpio (EtOH), seco y a T.a: evita los errores de perdidas por trasvase del sólido
6 ORGANIZACIÓN PRACTICAS: OPCION 1: Grupo < 16 alumnos ANÁLISIS Parejas días exp. ANALITOS MUESTRAS 1º 2º 3º 4º 5º 1) AMOXICILINA MEDICAMENTO 1,2 3,4 5,6 7,8 2) DUREZA (Ca, Mg) AGUA 3,4 1,2 7,8 5,6 3) QUININA TONICA 5,6 7,8 1,2 3,4 4) SULFAMIDA MEDICAMENTO 7,8 5,6 3,4 1,2 5) ALCOHOLES BEBIDAS Todas
7 ORGANIZACIÓN PRACTICAS: OPCION 2: Grupo = 16 alumnos ANÁLISIS Parejas días exp. ANALITOS MUESTRAS 1º 2º 3º 4º 5º 1) AMOXICILINA MEDICAMENTO 1,2 3,4 5,6-7,8 2) DUREZA (Ca, Mg) AGUA 3,4 1,2 7,8-5,6 3) QUININA TONICA 5,6 7,8-1,2 3,4 4) SULFAMIDA MEDICAMENTO 7,8 5,6-3,4 1,2 5) ALCOHOLES BEBIDAS
8 INFORME (por pareja) CALIFICACIÓN (6 puntos)! RÁCTICA (ANALITO) (Intervalo previsto y unidades) RESULTADOS (Completar. Media y s con cifras significativas) MUESTRA (Código) INCIDENCIAS (Describir en la parte posterio OXICILINA -110 % Verificar Media = s = RSD(%) = n = Desv. estándar Desv. estándar Relativa (= CV%) 3 ó justificar A Pedir al profesor junto con la muestra Muestra: Medicamento Código incidencia: LFANILAMIDA -110 % Media = s = RSD(%) = n = n p = ; r= Coef. Corr. r >0.99 S Muestra: Medicamento Código incidencia: Incidencia experimental; anotar al dorso del informe Nº patrones de Calibrado: 5 ó (justificar)
9 CALCULOS: Esquemas y fórmulas (a continuación) EXAMEN (4 puntos)! HOJA EXCEL tatreg.xls (ordenadores prácticas) - Calibrado + interpolación (prácticas 3 y 4) - Media ± s, sr%, n (todas las prácticas)
10 AMOXICILINA (se recomienda el uso de guantes y trabajo en vitrina siempre) Protocolo operativo: 1) Comprobar que los 3 erlenmeyers pequeños estén secos o en la estufa (si no, lavar con etanol y secar en estufa). Lavar con etanol y secar en estufa 1 vaso para pesar en la parte (2)...mientras 2) Comprobar que el aforado de 100 ml y la pipeta de 20 ml estén secos (si no, lavar con etanol y hablar con el profesor) 3) Leer la práctica y verificar esquemas de las partes (1) y (2) 4) Sobre el primer erlenmeyer seco y a T.a. pesar el patrón (desecador) y preguntar al profesor sobre las disoluciones y el modo de trabajar. 5) Durante la práctica se irán lavando con etanol y secando los erlenmeyers pequeños gastados 6) Al finalizar la práctica, dejar los erlenmeyers en estufa. El aforado de 100 ml y la pipeta de 20 ml, enjuagados con etanol en la gradilla.
11 AMOXICILINA (Etapa-1) Calibración del método [Normalización del valorante (val.) (HClO 4 )] - Patrón (p): Biftalato (Ft H - ) (desecador) - Procedimiento (instrumentos, variables-p) Reacción volumétrica Ft H - + H + = Ft H 2 Reacc. 1:1 n (val.) = n p H + M *Material seco v. M = m p / PM p PM p v m p * Ft H - M (mol/l) = m p (g) PM p (g/mol). v (L) Media de 3 réplicas
12 AMOXICILINA (Etapa-2) Análisis de muestras (pedir al profesor) - Analito (A): Amoxicilina (C, %) Procedimiento (instrumentos, variables-a) Reacción volumétrica A + H + = A H + Reacc. 1:1 n (val.). = n A H + M v v * *Material seco * PM A m A m M * C(%) v. M = v. M A v. M = v. m A / (PM A. V) A n A * M A V Ver Nota-1 C(%) = 100 m A / m M = 100 v (L). M (mol/l). PM A (g/mol). V(L) m M (g). v(l) Media de 3 réplicas
13 DUREZA DEL AGUA Protocolo operativo: 1) Lavar con etanol y secar en estufa 1 vaso para pesar en la parte (1)...mientras 2) Leer la práctica y verificar esquemas de las partes (1) y (2) 3) Comprobar que están todas las disoluciones y que hay suficiente, en particular el EDTA (0.5 L; ver cuadernillo). Consultar en caso de duda al profesor. NOTA El HCl está en la vitrina. 4) Todo el material de vidrio está contaminado. Limpiar el material con agua desionizada a medida que se necesite (muy importante para evitar contaminar las disoluciones) 5) Al finalizar la práctica, enjuagar todo el material con agua del grifo
14 DUREZA DEL AGUA (Etapa-1) Calibración del método [Normalización del valorante (val.) (EDTA = Y 4- )] - Patrón (p): CaCO 3 (desecador) - Procedimiento (instrumentos, variables-p) Reacción volumétrica Y 4- + Ca 2+ = CaY 2- Reacc. 1:1 n (val.). = n p Y 4- M v Material NO seco PM p v. M = v. M p v. M = v. m p / PM p. V m p v * Ca 2+ n p M p V M (mol/l) = v(l). m p (g) PM p (g/mol). V(L). v (L) Media de 3 réplicas
15 DUREZA DEL AGUA (Etapa-2) Análisis de muestras (pedir al profesor) - Analito (A): CaCO 3 (C, mg. L -1 ) - Procedimiento (instrumentos, variables-a) Reacción volumétrica Y 4- + Ca 2+ = CaY 2- Reacc. 1:1 n (val.). = n A Y 4- M v Material NO seco v. M = v. M A v C(mg/L) Ca 2+ n A M A Ver Nota-1 (mg/l) = M A (mol/l). PM A (g/mol) (mg/g) = v (L). M (mol/l). PM A (g/mol) 10 3 (mg/g v(l) Media de 3 réplicas
16 QUININA Protocolo operativo: 1) Lavar con etanol y secar en estufa 2 vasos para pesar en las partes (1) y (2)...mientras 2) Leer la práctica y verificar esquemas de las partes (1) y (2) 3) Comprobar que están todas las disoluciones y que hay suficiente, en particular el H 2 SO M (1 L; ver cuadernillo). Consultar en caso de duda al profesor. 4) Todo el material de vidrio está contaminado. Limpiar el material con agua desionizada a medida que se necesite (muy importante para evitar contaminar las disoluciones) 5) Al finalizar la práctica, enjuagar todo el material con agua del grifo
17 QUININA (Etapa-1) * Calibración del método (instrumental) - Patrón (p): sulfato de quinina (desecador) - Procedimiento (instrumentos, variables-p) m p Material NO seco 0 Marcar (rotular) material Recta de calibrado : Blanco, Cero instrumento C p1 F p1 Señal Regresión Lineal m p teórica m p C pi teórica C pi C p5 F p5 Informe n p =5 (r >0.99) C pi (ppm) = m p (g). C pi teorica (ppm) m pteórica (g) NOTA: tomar m p teórica (g)
18 QUININA (Etapa-2) Análisis de muestras (pedir al profesor) - Analito (A): quinina (C, ppm) - Procedimiento (instrumentos, variables-a) aterial O seco v 1 v 2 Interpolar en la recta de calibrado F Ai C 2i (ppm) C(ppm) C 1 V 1 C 2 V 2 C. v 1 = C 1. V 1 ; C 1. v 2 = C 2i. V 2 C(ppm) = C 1 (ppm) v 1 (L). V 1 (L) = C 2i (ppm). V 2 (L). V 1 (L) v 1 (L). v 2 (L) Media de 3 réplicas (i )
19 SULFANILAMIDA Protocolo operativo: 1) Lavar con etanol y secar en estufa 2 vasos para pesar en las partes (1) y (2)...mientras 2) Leer la práctica y verificar esquemas de las partes (1) y (2) 3) Comprobar que están todas las disoluciones y que hay suficiente, en particular el HCl 0.15 M (1 L; ver cuadernillo). Consultar en caso de duda al profesor. 4) Todo el material de vidrio está contaminado. Limpiar el material con agua desionizada a medida que se necesite (muy importante para evitar contaminar las disoluciones) 5) Al finalizar la práctica, enjuagar todo el material con agua del grifo
20 SULFANILAMIDA (Etapa-1) Calibración del método (instrumental) - Patrón (p): sulfanilamida (desecador) - Procedimiento (instrumentos, variables-p) Material NO seco 0 Marcar (rotular) material Recta de calibrado : Blanco, Cero instrumento C p1 Ab p1 * v i Regresión Lineal C p m p V v C p5 Ab p5 Informe n p =5 (r >0.99) C pi (g/l) = C p v v i = m p (g). V(L) v i (L). v(l)
21 SULFANILAMIDA (Etapa-2) Análisis de muestras (pedir al profesor) - Analito (A): sulfanilamida (C, %) - Procedimiento (instrumentos, variables-a) Material NO seco C A (g/l) v a Interpolar en la recta de calibrado C (%) * V m A V v C A Ab Ai C Ai (g/l) m M C A. v a = C A. v C (%) = 100 m A (g) m M (g) = 100 C Ai (g/l). V(L) m M (g) = 100 C Ai (g/l). v(l). V(L) m M (g). v a (L) Media de 3 réplicas (i )
22 ALCOHOLES Protocolo operativo: 1) Lavar con etanol y secar en estufa 2-3 tubos y sus tapones-rosca (en total 5 + el nº de parejas)...mientras 2) Cada pareja inyecta un patrón (cuadro 3.1-cuadernillo) (por turno), empezando por el último! (Consultar al profesor). Rellenar el cuadro 3.1 (cuadernillo)...mientras 3) Leer la práctica y hacer esquemas de las partes (1) y (2) siguiendo la guía de las otras prácticas. 4) Cada pareja prepara un patrón de calibrado (por turno) en la parte (1) (Consultar al profesor) e inyecta su patrón...mientras rellenar el cuadro 3.2a (cuadernillo) 5) Cada pareja prepara e inyecta (por turno) su muestra en la parte (2) y la inyecta...mientras rellenar el cuadro 3.2b (cuadernillo) 6) Al finalizar la práctica, enjuagar todo el material con etanol y dejar en gradilla
PNT 9: DETERMINACIÓN DEL ÁCIDO ACETILSALICÍLICO EN COMPRIMIDOS MEDIANTE DIFERENTES MÉTODOS.
 PNT 9: Análisis instrumental PNT 9 ÍNDICE 1. Objetivo...Página 1 2. Fundamento teórico...página 1 y 2 3. Materiales...Página 2 4. Reactivos...Página 2 5. Equipos...Página 2 6. Procedimiento experimental...página
PNT 9: Análisis instrumental PNT 9 ÍNDICE 1. Objetivo...Página 1 2. Fundamento teórico...página 1 y 2 3. Materiales...Página 2 4. Reactivos...Página 2 5. Equipos...Página 2 6. Procedimiento experimental...página
PRÁCTICA 1 HERRAMIENTAS Y OPERACIONES BÁSICAS EN EL LABORATORIO BIOANALÍTICO
 PRÁCTICA 1 HERRAMIENTAS Y OPERACIONES BÁSICAS EN EL LABORATORIO BIOANALÍTICO INTRODUCCIÓN Todos los instrumentos de medida que se utilizan en el laboratorio tienen algún tipo de escala para medir una magnitud,
PRÁCTICA 1 HERRAMIENTAS Y OPERACIONES BÁSICAS EN EL LABORATORIO BIOANALÍTICO INTRODUCCIÓN Todos los instrumentos de medida que se utilizan en el laboratorio tienen algún tipo de escala para medir una magnitud,
LABORATORIO DE QUÍMICA ANALÍTICA I LQ-218. Práctica de Laboratorio No. 3 CALIBRACIÓN DE MATERIAL VOLUMÉTRICO ANALÍTICO
 UNIVERSIDAD NACIONAL AUTÓNOMA DE HONDURAS FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA DEPARTAMENTO DE QUÍMICA LABORATORIO DE QUÍMICA ANALÍTICA I LQ-218 Práctica de Laboratorio No. 3 COMPETENCIAS A LOGRAR:
UNIVERSIDAD NACIONAL AUTÓNOMA DE HONDURAS FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA DEPARTAMENTO DE QUÍMICA LABORATORIO DE QUÍMICA ANALÍTICA I LQ-218 Práctica de Laboratorio No. 3 COMPETENCIAS A LOGRAR:
TRBAJO PRÁCTICO N 5: ph. Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes.
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
MATERIAL VOLUMETRICO. Establecer los criterios y la metodología que se utilizarán para el verificado del material volumétrico.
 Página de 9. OBJETIVO Establecer los criterios y la metodología que se utilizarán para el verificado del material volumétrico. 2. CAMPO DE APLICACIÓN Aplica para el verificado de aparatos volumétricos,
Página de 9. OBJETIVO Establecer los criterios y la metodología que se utilizarán para el verificado del material volumétrico. 2. CAMPO DE APLICACIÓN Aplica para el verificado de aparatos volumétricos,
EXPERIMENTO 6: SÍNTESIS, PURIFICACIÓN Y ANÁLISIS DEL ÁCIDO ACETIL SALICÍCLICO (aspirina).
 EXPERIMENT 6: SÍNTESIS, PURIFIAIÓN Y ANÁLISIS DEL ÁID AETIL SALIÍLI (aspirina). BJETIV: Sintetizar ácido acetilsalicílico a partir de la reacción de esterificación del grupo hidroxílico del ácido salicílico
EXPERIMENT 6: SÍNTESIS, PURIFIAIÓN Y ANÁLISIS DEL ÁID AETIL SALIÍLI (aspirina). BJETIV: Sintetizar ácido acetilsalicílico a partir de la reacción de esterificación del grupo hidroxílico del ácido salicílico
Práctica 6. Reactivo limitante
 Práctica 6. Reactivo limitante PREGUNTA A RESPONDER AL FINAL DE LA PRÁCTICA Qué especie actúa como reactivo limitante en el siguiente proceso químico? CaCl 2 (ac) + K 2 CO 3 (ac) CaCO 3 + 2 KCl (ac) PRIMERA
Práctica 6. Reactivo limitante PREGUNTA A RESPONDER AL FINAL DE LA PRÁCTICA Qué especie actúa como reactivo limitante en el siguiente proceso químico? CaCl 2 (ac) + K 2 CO 3 (ac) CaCO 3 + 2 KCl (ac) PRIMERA
DETERMINACIÓN DE LA CANTIDAD DE ÁCIDO CLORHÍDRICO PRESENTE EN SALFUMÁN COMERCIAL
 DETERMINACIÓN DE LA CANTIDAD DE ÁCIDO CLORHÍDRICO PRESENTE EN SALFUMÁN COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen
DETERMINACIÓN DE LA CANTIDAD DE ÁCIDO CLORHÍDRICO PRESENTE EN SALFUMÁN COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen
- Matraces aforados de 25, 100, y ml.
 Página 1 de 8 1.- INTRODUCCIÓN El presente protocolo es aplicable para el análisis cuantitativo de algunos aniones en muestras de vegetales. Los analitos son extraídos de la muestra pulverizada por medio
Página 1 de 8 1.- INTRODUCCIÓN El presente protocolo es aplicable para el análisis cuantitativo de algunos aniones en muestras de vegetales. Los analitos son extraídos de la muestra pulverizada por medio
FACULTAD DE INGENIERÍA MARÍTIMA Y CIENCIAS DEL MAR FICHA DE LA PRÁCTICA PARA LABORATORIO
 CÓDIGO MATERIA Calidad de Agua (FMAR- 01677) Calidad de Agua NOMBRE DE LA PRÁCTICA OBJETIVOS GENERALES: Practica 6: Determinación de Sulfatos 1. Conocer los métodos para determinar la concentración de
CÓDIGO MATERIA Calidad de Agua (FMAR- 01677) Calidad de Agua NOMBRE DE LA PRÁCTICA OBJETIVOS GENERALES: Practica 6: Determinación de Sulfatos 1. Conocer los métodos para determinar la concentración de
PRÁCTICA 6 CINÉTICA QUÍMICA DETERMINACIÓN DE LA CONSTANTE DE VELOCIDAD DE REACCIÓN EN LA HIDRÓLISIS DEL CLORURO DE TERBUTILO
 PRÁCTICA 6 CINÉTICA QUÍMICA DETERMINACIÓN DE LA CONSTANTE DE VELOCIDAD DE REACCIÓN EN LA HIDRÓLISIS DEL CLORURO DE TERBUTILO OBJETIVO. El alumno aprenderá a comprobar experimentalmente el mecanismo de
PRÁCTICA 6 CINÉTICA QUÍMICA DETERMINACIÓN DE LA CONSTANTE DE VELOCIDAD DE REACCIÓN EN LA HIDRÓLISIS DEL CLORURO DE TERBUTILO OBJETIVO. El alumno aprenderá a comprobar experimentalmente el mecanismo de
VOLUMETRÍA DE COMPLEJACIÓN: DETERMINACIÓN DE LA DUREZA DEL AGUA
 EXPERIMENTO 5 VOLUMETRÍA DE COMPLEJACIÓN: DETERMINACIÓN DE LA DUREZA DEL AGUA Objetivo general Aplicar los principios básicos de las volumetrías de complejación en la determinación de la dureza de una
EXPERIMENTO 5 VOLUMETRÍA DE COMPLEJACIÓN: DETERMINACIÓN DE LA DUREZA DEL AGUA Objetivo general Aplicar los principios básicos de las volumetrías de complejación en la determinación de la dureza de una
TRONCO COMUN DIVISIONAL DE CIENCIAS BIOLOGICAS Y DE LA SALUD. MODULO: ENERGIA Y CONSUMO DE SUSTANCIAS FUNDAMENTALES. PRACTICA No.
 TRONCO COMUN DIVISIONAL DE CIENCIAS BIOLOGICAS Y DE LA SALUD. MODULO: ENERGIA Y CONSUMO DE SUSTANCIAS FUNDAMENTALES. PRACTICA No. 1 TITULACIÓN DE SOLUCIONES OBJETIVO: Conocer la técnica de Titulación de
TRONCO COMUN DIVISIONAL DE CIENCIAS BIOLOGICAS Y DE LA SALUD. MODULO: ENERGIA Y CONSUMO DE SUSTANCIAS FUNDAMENTALES. PRACTICA No. 1 TITULACIÓN DE SOLUCIONES OBJETIVO: Conocer la técnica de Titulación de
PNT 2 ANÁLISIS QUÍMICO MEDIOAMBIENTAL DE CONTENIDOS DE SULFATOS EN AGUA POR TURBIDIMETRÍA
 PNT 2 ANÁLISIS QUÍMICO MEDIOAMBIENTAL DE CONTENIDOS DE SULFATOS EN AGUA POR TURBIDIMETRÍA Índice Objetivo... 3 Introducción... 3 Métodos de ánalisis... 3 Fundamento... 4 Niveles admitidos... 5 Reactivos...
PNT 2 ANÁLISIS QUÍMICO MEDIOAMBIENTAL DE CONTENIDOS DE SULFATOS EN AGUA POR TURBIDIMETRÍA Índice Objetivo... 3 Introducción... 3 Métodos de ánalisis... 3 Fundamento... 4 Niveles admitidos... 5 Reactivos...
TEMA 5: LABORATORIO PIPETA GRADUADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA PIPETA AFORADA MATRAZ DE FONDO PLANO MATRAZ DE FONDO REDONDO MATRAZ AFORADO
 TEMA 5: LABORATORIO PIPETA GRADUADA PIPETA AFORADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA BURETA DE FONDO REDONDO DE FONDO PLANO AFORADO DE DESTILACIÓN ERLENMEYER PROBETA FRASCO TRANSPARENTE FRASCOS TOPACIO
TEMA 5: LABORATORIO PIPETA GRADUADA PIPETA AFORADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA BURETA DE FONDO REDONDO DE FONDO PLANO AFORADO DE DESTILACIÓN ERLENMEYER PROBETA FRASCO TRANSPARENTE FRASCOS TOPACIO
FUNDAMENTOS DE ANÁLISIS INSTRUMENTAL. 4ª RELACIÓN DE PROBLEMAS.
 FUNDAMENTOS DE ANÁLISIS INSTRUMENTAL. 4ª RELACIÓN DE PROBLEMAS. 1.- Para determinar el contenido en plomo en una muestra de leche contaminada, se toma 1.0 ml de la leche y se diluye a un volumen final
FUNDAMENTOS DE ANÁLISIS INSTRUMENTAL. 4ª RELACIÓN DE PROBLEMAS. 1.- Para determinar el contenido en plomo en una muestra de leche contaminada, se toma 1.0 ml de la leche y se diluye a un volumen final
ACTIVIDAD EXPERIMENTAL 1. CÓMO LO USO? OPERACIONES BÁSICAS EN EL LABORATORIO Versión ajustada
 ACTIVIDAD EXPERIMENTAL 1 Antes de comenzar CÓMO LO USO? OPERACIONES BÁSICAS EN EL LABORATORIO Versión ajustada En forma individual investiga lo siguiente, y posteriormente compártelo con tus compañeros
ACTIVIDAD EXPERIMENTAL 1 Antes de comenzar CÓMO LO USO? OPERACIONES BÁSICAS EN EL LABORATORIO Versión ajustada En forma individual investiga lo siguiente, y posteriormente compártelo con tus compañeros
Determinación de Alcalinidad en aguas naturales y residuales
 QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Alcalinidad en aguas naturales y residuales Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 29/09/2013 Método Titulométrico
QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Alcalinidad en aguas naturales y residuales Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 29/09/2013 Método Titulométrico
Determinación de la constante de los gases ideales
 Prácticas de Química. Determinación de la constante de los gases ideales I. Introducción teórica y objetivos........................................ 2 II. Material................................................................
Prácticas de Química. Determinación de la constante de los gases ideales I. Introducción teórica y objetivos........................................ 2 II. Material................................................................
ALCALINIDAD TOTAL- REACCIONES ACIDO-BASE Página 1
 Práctica No. 3 REACCIONES ACIDO BASE ALCALINIDAD TOTAL AL CARBONATO, BICARBONATO E HIDROXIDO FENOFTALEINA 1. OBJETIVO Determinar mediante una relación estequiometrica los carbonatos, hidróxidos y bicarbonatos
Práctica No. 3 REACCIONES ACIDO BASE ALCALINIDAD TOTAL AL CARBONATO, BICARBONATO E HIDROXIDO FENOFTALEINA 1. OBJETIVO Determinar mediante una relación estequiometrica los carbonatos, hidróxidos y bicarbonatos
VALORACIÓN REDOX (PERMANGANIMETRÍA)
 SEMINARIO DE FÍSICA Y QUÍMICA NIVEL: BACHILLERATO. FÍSICA Y QUÍMICA MATERIA: QUÍMICA CURSO 2013-2014. PRÁCTICA Nº: Nombre y apellidos:... Grupo:... Fecha:... VALORACIÓN REDOX PERMANGANIMETRÍA Introducción
SEMINARIO DE FÍSICA Y QUÍMICA NIVEL: BACHILLERATO. FÍSICA Y QUÍMICA MATERIA: QUÍMICA CURSO 2013-2014. PRÁCTICA Nº: Nombre y apellidos:... Grupo:... Fecha:... VALORACIÓN REDOX PERMANGANIMETRÍA Introducción
OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución.
 OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución. FUNDAMENTO TEÓRICO Una disolución es una mezcla homogénea
OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución. FUNDAMENTO TEÓRICO Una disolución es una mezcla homogénea
Material de uso frecuente en el laboratorio de química. Figura Nombre Uso / Características. Crisol. Espátula de porcelana. Capsula de porcelana
 Material de uso frecuente en el laboratorio de química. En un Laboratorio de Química se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio.
Material de uso frecuente en el laboratorio de química. En un Laboratorio de Química se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio.
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS
 DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
TÍTULO: Determinación colorimétrica de fenoles en agua por el método de la 4- aminoantipirina
 Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Prácticas de análisis de los vinos. Dpto. Nutrición y Bromatología II. Facultad de Farmacia. UCM
 Prácticas de análisis de los vinos. Dpto. Nutrición y Bromatología II. Facultad de Farmacia. UCM DETERMINACIONES ANALÍTICAS EN EL VINO ph ACIDEZ TOTAL ACIDEZ VOLÁTIL GRADO ALCOHÓLICO SULFUROSO ÍNDICE DE
Prácticas de análisis de los vinos. Dpto. Nutrición y Bromatología II. Facultad de Farmacia. UCM DETERMINACIONES ANALÍTICAS EN EL VINO ph ACIDEZ TOTAL ACIDEZ VOLÁTIL GRADO ALCOHÓLICO SULFUROSO ÍNDICE DE
Práctica laboratorio: Reacciones de polimerización. Determinación del peso molecular de un polímero mediante análisis de grupos finales
 Práctica laboratorio: Reacciones de polimerización. Determinación del peso molecular de un polímero mediante análisis de grupos finales Enrique Dans. Creative Commons. http://www.flickr.com/photos/edans/1239
Práctica laboratorio: Reacciones de polimerización. Determinación del peso molecular de un polímero mediante análisis de grupos finales Enrique Dans. Creative Commons. http://www.flickr.com/photos/edans/1239
PROPIEDADES ÁCIDO-BASE DE LAS SALES: HIDRÓLISIS
 IV-1 PRÁCTICA- PROPIEDADES ÁCIDO-BASE DE LAS SALES: HIDRÓLISIS En esta práctica mediremos el ph (carácter ácido, básico o neutro de disoluciones acuosas de diversas sales, y comprobaremos que estas disoluciones
IV-1 PRÁCTICA- PROPIEDADES ÁCIDO-BASE DE LAS SALES: HIDRÓLISIS En esta práctica mediremos el ph (carácter ácido, básico o neutro de disoluciones acuosas de diversas sales, y comprobaremos que estas disoluciones
CINÉTICA DE LA REACCIÓN DEL IÓN TIOSULFATO EN MEDIO ÁCIDO.
 CINÉTICA DE LA REACCIÓN DEL IÓN TIOSULFATO EN MEDIO ÁCIDO. Objetivo Medir experimentalmente el tiempo que tarda una reacción química en alcanzar una determinada concentración y a partir de las medidas
CINÉTICA DE LA REACCIÓN DEL IÓN TIOSULFATO EN MEDIO ÁCIDO. Objetivo Medir experimentalmente el tiempo que tarda una reacción química en alcanzar una determinada concentración y a partir de las medidas
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
PRÁCTICO 3: SOLUCIONES
 Curso de Laboratorio Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 3: SOLUCIONES Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall Hispanoamericana,
Curso de Laboratorio Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 3: SOLUCIONES Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall Hispanoamericana,
ESTANDARIZACIÓN DEL ACIDO NITRICO
 ESTANDARIZACIÓN DEL ACIDO NITRICO NATALI ALVAREZ MONAR 1097397966 UNIVERSIDAD DEL QUINDÍO FACULTAD DE CIENCIAS BÁSICAS Y TECNOLOGÍAS PROGRAMA DE QUÍMICA ARMENIA QUINDÍO ESTANDARIZACIÓN DEL ACIDO NITRICO
ESTANDARIZACIÓN DEL ACIDO NITRICO NATALI ALVAREZ MONAR 1097397966 UNIVERSIDAD DEL QUINDÍO FACULTAD DE CIENCIAS BÁSICAS Y TECNOLOGÍAS PROGRAMA DE QUÍMICA ARMENIA QUINDÍO ESTANDARIZACIÓN DEL ACIDO NITRICO
PRÁCTICA 3 DETERMINACIÓN DE LA DUREZA DEL AGUA POR VALORACIÓN CON EDTA
 PRÁCTICA DETERMINACIÓN DE LA DUREZA DEL AGUA POR VALORACIÓN CON EDTA INTRODUCCIÓN El contenido salino de las aguas potables es debido principalmente a las sales de calcio y magnesio y, por esta razón,
PRÁCTICA DETERMINACIÓN DE LA DUREZA DEL AGUA POR VALORACIÓN CON EDTA INTRODUCCIÓN El contenido salino de las aguas potables es debido principalmente a las sales de calcio y magnesio y, por esta razón,
Determinación de Materia Orgánica en Suelos y Sedimentos
 QUÍMICA ANALITICA APLICADA INORGÁNICA QMC-613 Determinación de Materia Orgánica en Suelos y Sedimentos Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 13/10/2013 Método de Titulométrico
QUÍMICA ANALITICA APLICADA INORGÁNICA QMC-613 Determinación de Materia Orgánica en Suelos y Sedimentos Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 13/10/2013 Método de Titulométrico
Electrodo selectivo de sodio
 96 50 Electrodo selectivo de sodio Na 2 Electrodo selectivo sodio. Manual del usuario. Indice Introducción...3 Aplicaciones...3 Especificaciones...3 Instrumentos y accesorios...3 Reactivos y disoluciones...3
96 50 Electrodo selectivo de sodio Na 2 Electrodo selectivo sodio. Manual del usuario. Indice Introducción...3 Aplicaciones...3 Especificaciones...3 Instrumentos y accesorios...3 Reactivos y disoluciones...3
PEDIDO DE PRECIOS SOLICITUD DE... PEDIDO DE PRECIOS Nº 1/14. CREDITO 60 DIAS
 1 FECHA:...28/1/14 1 1 Alcoholímetro (de 0 a 17º GL) 2 1 Alcoholímetro (de 0 a 30º GL) 3 1 Alcoholímetro (de 0 a 100º GL) 4 1 Alcoholímetro (de 10 a 20º GL) 5 1 Alcoholímetro (de 30 a 40º GL) 6 1 Alcoholímetro
1 FECHA:...28/1/14 1 1 Alcoholímetro (de 0 a 17º GL) 2 1 Alcoholímetro (de 0 a 30º GL) 3 1 Alcoholímetro (de 0 a 100º GL) 4 1 Alcoholímetro (de 10 a 20º GL) 5 1 Alcoholímetro (de 30 a 40º GL) 6 1 Alcoholímetro
PRÁCTICA 17 REACCIONES DE FORMACIÓN DE COMPLEJOS. DETERMINACIÓN DE LA DUREZA DEL AGUA.
 PRÁCTICA 17 REACCINES DE FRMACIÓN DE CMPLEJS. DETERMINACIÓN DE LA DUREZA DEL AGUA. BJETIVS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios de formación de complejos, así
PRÁCTICA 17 REACCINES DE FRMACIÓN DE CMPLEJS. DETERMINACIÓN DE LA DUREZA DEL AGUA. BJETIVS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios de formación de complejos, así
PRÁCTICA # 01 PREPARACIÓN DE DISOLUCIONES
 REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
Electrodo selectivo de calcio. Ca 2+
 96 60 Electrodo selectivo de calcio Ca 2+ Electrodo selectivo calcio. Manual del usuario. Garantía El plazo de validez es de 6 meses a partir de la fecha de expedición del electrodo. La garantía cubre
96 60 Electrodo selectivo de calcio Ca 2+ Electrodo selectivo calcio. Manual del usuario. Garantía El plazo de validez es de 6 meses a partir de la fecha de expedición del electrodo. La garantía cubre
DEPARTAMENTO DE QUÍMICA ANALÍTICA Y TECNOLOGÍA DE ALIMENTOS ANALISIS INSTRUMENTAl I
 PRIMERA RELACIÓN DE PROBLEMAS. CALIBRACIÓN EN QUÍMICA ANALÍTICA 1.- En la determinación de una especie X por un método instrumental en el que la señal analítica se define como P = kc x, se obtuvieron los
PRIMERA RELACIÓN DE PROBLEMAS. CALIBRACIÓN EN QUÍMICA ANALÍTICA 1.- En la determinación de una especie X por un método instrumental en el que la señal analítica se define como P = kc x, se obtuvieron los
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO
 PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
EJEMPLO DE ANÁLISIS POR RETROCESO: DETERMINACIÓN DEL SULFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIAL
 ISSN 1988-607 DEP. EGA: GR 9/007 Nº 1 ENERO DE 008 EJEMPO DE ANÁISIS POR RETROCESO: DETERMINACIÓN DE SUFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIA AUTORÍA JOAQUÍN RUIZ MOINA TEMÁTICA CIENCIAS EXPERIMENTAES,
ISSN 1988-607 DEP. EGA: GR 9/007 Nº 1 ENERO DE 008 EJEMPO DE ANÁISIS POR RETROCESO: DETERMINACIÓN DE SUFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIA AUTORÍA JOAQUÍN RUIZ MOINA TEMÁTICA CIENCIAS EXPERIMENTAES,
DETERMINACIÓN EXPERIMENTAL DE LA DUREZA DEL AGUA DE ARMILLA UTILIZANDO UNA VALORACIÓN CON LA FORMACIÓN DE COMPLEJOS PARA 2º DE BACHILERATO
 DETERMINACIÓN EXPERIMENTAL DE LA DUREZA DEL AGUA DE ARMILLA UTILIZANDO UNA VALORACIÓN CON LA FORMACIÓN DE COMPLEJOS PARA 2º DE BACHILERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE FORMACIÓN DE
DETERMINACIÓN EXPERIMENTAL DE LA DUREZA DEL AGUA DE ARMILLA UTILIZANDO UNA VALORACIÓN CON LA FORMACIÓN DE COMPLEJOS PARA 2º DE BACHILERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE FORMACIÓN DE
CALIBRACION DEL MATERIAL VOLUMÊTRICO
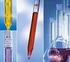 MATERIAL VOLUMÉTRICO CALIBRACION DEL MATERIAL VOLUMÊTRICO El material volumétrico tiene por finalidad la medición exacta de volúmenes y debe ser controlado antes de utilizarlo. Para ello se requiere pesar
MATERIAL VOLUMÉTRICO CALIBRACION DEL MATERIAL VOLUMÊTRICO El material volumétrico tiene por finalidad la medición exacta de volúmenes y debe ser controlado antes de utilizarlo. Para ello se requiere pesar
PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL
 PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL INTRODUCCION: Los cambios químicos implican interacciones partícula con partícula(s) y no gramo a gramo,
PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL INTRODUCCION: Los cambios químicos implican interacciones partícula con partícula(s) y no gramo a gramo,
Electrodo selectivo de nitrato NO 3
 96 62 Electrodo selectivo de nitrato NO 3 - Electrodo selectivo nitrato. Manual del usuario. Garantía El plazo de validez es de 6 meses a partir de la fecha de expedición del electrodo. La garantía cubre
96 62 Electrodo selectivo de nitrato NO 3 - Electrodo selectivo nitrato. Manual del usuario. Garantía El plazo de validez es de 6 meses a partir de la fecha de expedición del electrodo. La garantía cubre
PREPARACIÓN DE DISOLUCIONES
 SEMINARIO DE FÍSICA Y QUÍMICA NIVEL: BACHILLERATO. FÍSICA Y QUÍMICA MATERIA: QUÍMICA CURSO 2013-2014. PRÁCTICA Nº: Nombre y apellidos:... Grupo:... Fecha:... PREPARACIÓN DE DISOLUCIONES Introducción Las
SEMINARIO DE FÍSICA Y QUÍMICA NIVEL: BACHILLERATO. FÍSICA Y QUÍMICA MATERIA: QUÍMICA CURSO 2013-2014. PRÁCTICA Nº: Nombre y apellidos:... Grupo:... Fecha:... PREPARACIÓN DE DISOLUCIONES Introducción Las
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA GENERAL
 FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA GENERAL PRUEBAS DE CARACTERIZACIÓN DE ALCOHOLES Guía No: 07 Páginas: 1 a 7 1. INTRODUCCIÓN El grupo funcional
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA GENERAL PRUEBAS DE CARACTERIZACIÓN DE ALCOHOLES Guía No: 07 Páginas: 1 a 7 1. INTRODUCCIÓN El grupo funcional
PREPARACIÓN DE MUESTRAS en TÉCNICAS DE PLASMA
 PREPARACIÓN DE MUESTRAS en TÉCNICAS DE PLASMA 1. METODOLOGÍA DE TRABAJO 2. DIGESTIÓN ÁCIDA TRADICIONAL vs. DIGESTIÓN CON HORNO MICROONDAS 3. DIGESTIÓN POR MW. PARÁMETROS DE CONTROL 4. ÁCIDOS EMPLEADOS
PREPARACIÓN DE MUESTRAS en TÉCNICAS DE PLASMA 1. METODOLOGÍA DE TRABAJO 2. DIGESTIÓN ÁCIDA TRADICIONAL vs. DIGESTIÓN CON HORNO MICROONDAS 3. DIGESTIÓN POR MW. PARÁMETROS DE CONTROL 4. ÁCIDOS EMPLEADOS
Manual de laboratorio
 UNIVERSIDAD NACIONAL DE INGENIERIA UNI-Norte Sede regional en Estelí Manual de laboratorio 2008 Química de Alimentos Objetivos Generales 1. Proporcionar a los estudiantes de Ingeniería Agroindustrial las
UNIVERSIDAD NACIONAL DE INGENIERIA UNI-Norte Sede regional en Estelí Manual de laboratorio 2008 Química de Alimentos Objetivos Generales 1. Proporcionar a los estudiantes de Ingeniería Agroindustrial las
PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES
 PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES OBJETIVOS ESPECÍFICOS 1) Identificar y manejar el material básico de laboratorio. 2) Preparar
PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES OBJETIVOS ESPECÍFICOS 1) Identificar y manejar el material básico de laboratorio. 2) Preparar
PREPARACIÓN DE SOLUCIONES
 1. INTRODUCCION Las soluciones se definen como mezclas homogéneas de dos o más especies moleculares o iónicas. Las soluciones gaseosas son por lo general mezclas moleculares. Sin embargo las soluciones
1. INTRODUCCION Las soluciones se definen como mezclas homogéneas de dos o más especies moleculares o iónicas. Las soluciones gaseosas son por lo general mezclas moleculares. Sin embargo las soluciones
REGLAMENTOS. (4) Las medidas previstas en el presente Reglamento se ajustan al dictamen del Comité de la Organización Común de Mercados Agrarios,
 8.10.2016 L 273/5 REGLAMENTOS REGLAMENTO DE EJECUCIÓN (UE) 2016/1784 DE LA COMISIÓN de 30 de septiembre de 2016 que modifica el Reglamento (CEE) n. o 2568/91 relativo a las características de los aceites
8.10.2016 L 273/5 REGLAMENTOS REGLAMENTO DE EJECUCIÓN (UE) 2016/1784 DE LA COMISIÓN de 30 de septiembre de 2016 que modifica el Reglamento (CEE) n. o 2568/91 relativo a las características de los aceites
FACTORES QUE AFECTAN A LA VELOCIDAD DE REACCIÓN Y PRINCIPIO DE CONSERVACIÓN DE LA MASA DE LAVOISIER.
 FACTORES QUE AFECTAN A LA VELOCIDAD DE REACCIÓN Y PRINCIPIO DE CONSERVACIÓN DE LA MASA DE LAVOISIER. Introducción Roberto Bareas COLEGIO JULIO VERNE Torrent Esta práctica ha sido realizada como colofón
FACTORES QUE AFECTAN A LA VELOCIDAD DE REACCIÓN Y PRINCIPIO DE CONSERVACIÓN DE LA MASA DE LAVOISIER. Introducción Roberto Bareas COLEGIO JULIO VERNE Torrent Esta práctica ha sido realizada como colofón
Ley de conservación de la masa. Estequiometría
 Prácticas de laboratorio Ley de conservación de la masa. Estequiometría Introducción. En esta práctica vamos a demostrar la ley de conservación de la masa, enunciada por Lavoisier: En toda reacción química
Prácticas de laboratorio Ley de conservación de la masa. Estequiometría Introducción. En esta práctica vamos a demostrar la ley de conservación de la masa, enunciada por Lavoisier: En toda reacción química
PRACTICA No. 10 VALORACIÓN O TITULACIÓN DE LAS DISOLUCIONES
 1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 10 VALORACIÓN O TITULACIÓN DE LAS DISOLUCIONES
1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 10 VALORACIÓN O TITULACIÓN DE LAS DISOLUCIONES
INTRODUCCIÓN AL LABORATORIO
 Página: 1/10 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 1: INTRODUCCIÓN AL LABORATORIO 1- OBJETIVOS 1.1 Presentar algunas ideas generales con respecto al funcionamiento del laboratorio y a normas de trabajo
Página: 1/10 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 1: INTRODUCCIÓN AL LABORATORIO 1- OBJETIVOS 1.1 Presentar algunas ideas generales con respecto al funcionamiento del laboratorio y a normas de trabajo
LABORATORIO ANÁLISIS INSTRUMENTAL PRACTICA #7 ULTRAVIOLETA PRESENTADO POR: EMIL SON LEÓN FLORIÁN DEYMER GOMEZ PRESENTADO A: LUCAS BLANDÓN
 LABORATORIO ANÁLISIS INSTRUMENTAL PRACTICA #7 ULTRAVIOLETA PRESENTADO POR: EMIL SON LEÓN FLORIÁN DEYMER GOMEZ PRESENTADO A: LUCAS BLANDÓN UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA INGENIERÍA
LABORATORIO ANÁLISIS INSTRUMENTAL PRACTICA #7 ULTRAVIOLETA PRESENTADO POR: EMIL SON LEÓN FLORIÁN DEYMER GOMEZ PRESENTADO A: LUCAS BLANDÓN UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA INGENIERÍA
INSTRUMENTOS BÁSICOS DE UN LABORATORIO
 INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
PESADA PESADA. Indice FARMACIA. PN/L/OP/001/00 Página 1 de 6 Rev.: 0 Fecha de Edición:
 FARMACIA PROCEDIMIENTO DE OPERACIONES FARMACÉUTICAS PESADA PN/L/OP/001/00 Página 1 de 6 Rev.: 0 Fecha de Edición: Procedimientos relacionados: PESADA Indice 1. Objetivo 2. Responsabilidad de aplicación
FARMACIA PROCEDIMIENTO DE OPERACIONES FARMACÉUTICAS PESADA PN/L/OP/001/00 Página 1 de 6 Rev.: 0 Fecha de Edición: Procedimientos relacionados: PESADA Indice 1. Objetivo 2. Responsabilidad de aplicación
Grado en Química. 1 er Curso QUIMICA GENERAL II. Guiones de Prácticas
 Grado en Química 1 er Curso QUIMICA GENERAL II Guiones de Prácticas QUIMICA GENERAL II Grado en Química 1 er Curso PRÁCTICA 1: TÉCNICAS BÁSICAS EN EL LABORATORIO OBJETIVOS: Aprender a elaborar un cuaderno
Grado en Química 1 er Curso QUIMICA GENERAL II Guiones de Prácticas QUIMICA GENERAL II Grado en Química 1 er Curso PRÁCTICA 1: TÉCNICAS BÁSICAS EN EL LABORATORIO OBJETIVOS: Aprender a elaborar un cuaderno
PREPARACIÓN DE SOLUCIONES
 PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
MANUAL FAR 516 L DEL PERFIL
 BENEMÉRITA UNIVERSIDAD AUTÓNOMAA DE PUEBLA FACULTAD DE CIENCIAS QUÍMICAS LICENCIATURA: FARMACIAA ÁREA ESPECÍFICA DE: FARMACIA NOMBRE DE LA ASIGNATURA: CÓDIGO: FECHA DE ELABORACIÓN: NIVEL EN EL MAPA CURRICULAR:
BENEMÉRITA UNIVERSIDAD AUTÓNOMAA DE PUEBLA FACULTAD DE CIENCIAS QUÍMICAS LICENCIATURA: FARMACIAA ÁREA ESPECÍFICA DE: FARMACIA NOMBRE DE LA ASIGNATURA: CÓDIGO: FECHA DE ELABORACIÓN: NIVEL EN EL MAPA CURRICULAR:
ESTABLECIMIENTO DE LA TRAZABILIDAD DE LAS MEDICIONES DE HIERRO EN ALEACIONES DE COBRE POR EL MÉTODO ASTM E
 QUÍMICA ANALÍTICA EXPERIMENTAL III (1802) DEPARTAMENTO DE QUÍMICA ANALÍTICA FACULTAD DE QUÍMICA ESTABLECIMIENTO DE LA TRAZABILIDAD DE LAS MEDICIONES DE HIERRO EN ALEACIONES DE COBRE POR EL MÉTODO ASTM
QUÍMICA ANALÍTICA EXPERIMENTAL III (1802) DEPARTAMENTO DE QUÍMICA ANALÍTICA FACULTAD DE QUÍMICA ESTABLECIMIENTO DE LA TRAZABILIDAD DE LAS MEDICIONES DE HIERRO EN ALEACIONES DE COBRE POR EL MÉTODO ASTM
COLEGIO DE CIENCIAS DEPARTAMENTO DE QUÍMICA QUÍMICA (LABORATORIO) Ramón L. Hernández Castillo. Uso de materiales y cristalería del laboratorio
 COLEGIO DE CIENCIAS DEPARTAMENTO DE QUÍMICA QUÍMICA 105-106 (LABORATORIO) Ramón L. Hernández Castillo Uso de materiales y cristalería del laboratorio I. Uso de la balanza Uno de los instrumentos más utilizados
COLEGIO DE CIENCIAS DEPARTAMENTO DE QUÍMICA QUÍMICA 105-106 (LABORATORIO) Ramón L. Hernández Castillo Uso de materiales y cristalería del laboratorio I. Uso de la balanza Uno de los instrumentos más utilizados
TÍTULO: Determinación de hidrocarburos en muestras de suelo mediante espectrofotometría
 Página 1 de 7 1.- INTRODUCCIÓN El presente método es aplicable para el análisis de residuos de aceites minerales en suelo, en concentraciones superiores a 20 mg/kg. El análisis mediante espectrofotometría,
Página 1 de 7 1.- INTRODUCCIÓN El presente método es aplicable para el análisis de residuos de aceites minerales en suelo, en concentraciones superiores a 20 mg/kg. El análisis mediante espectrofotometría,
PRACTICA No. 10 VALORACIÓN O TITULACIÓN DE LAS DISOLUCIONES
 ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 10 VALORACIÓN O TITULACIÓN DE LAS DISOLUCIONES 1. INTRODUCCIÓN: VALORACIÓN es un método que se usa para encontrar o calcular
ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 10 VALORACIÓN O TITULACIÓN DE LAS DISOLUCIONES 1. INTRODUCCIÓN: VALORACIÓN es un método que se usa para encontrar o calcular
UNIVERSIDAD TECNOLÓGICA METROPOLITANA INGENIERIA EN QUIMICA LABORATORIO ANALISIS INSTRUMENTAL. INFORME N 1: ESPECTROFOTOMETRÍA UV VISIBLE INTRODUCCION
 UNIVERSIDAD TECNOLÓGICA METROPOLITANA INGENIERIA EN QUIMICA LABORATORIO ANALISIS INSTRUMENTAL. INFORME N 1: ESPECTROFOTOMETRÍA UV VISIBLE INTRODUCCION En este laboratorio utilizaremos el método de la espectrofotometría
UNIVERSIDAD TECNOLÓGICA METROPOLITANA INGENIERIA EN QUIMICA LABORATORIO ANALISIS INSTRUMENTAL. INFORME N 1: ESPECTROFOTOMETRÍA UV VISIBLE INTRODUCCION En este laboratorio utilizaremos el método de la espectrofotometría
TÍTULO: Determinación colorimétrica de compuestos fenólicos en agua mediante el reactivo de Folin-Ciocalteu
 Página 1 de 6 1.- INTRODUCCIÓN El presente método colorimétrico permite el análisis de compuestos orgánicos que presenten anillos aromáticos hidroxilados (fenoles, ácido tánico, taninos, ligninas, ácidos
Página 1 de 6 1.- INTRODUCCIÓN El presente método colorimétrico permite el análisis de compuestos orgánicos que presenten anillos aromáticos hidroxilados (fenoles, ácido tánico, taninos, ligninas, ácidos
QUÍMICA 2º BACHILLERATO
 DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
DETERMINACIÓN DE ACIDEZ TOTAL EN PRODUCTOS DE FRUTAS Método potenciométrico ME
 Página 1 de 7 1. OBJETIVO Determinar el contenido de acidez total presente en el alimento, estableciendo su acidez titulable. 2. CAMPO DE APLICACIÓN Y ALCANCE El método es aplicable a zumos o jugos, néctares,
Página 1 de 7 1. OBJETIVO Determinar el contenido de acidez total presente en el alimento, estableciendo su acidez titulable. 2. CAMPO DE APLICACIÓN Y ALCANCE El método es aplicable a zumos o jugos, néctares,
SEMANA 2 EQUIPO BÁSICO DE LABORATORIO DE QUIMICA Elaborado por: Lic. Raúl Hernández Mazariegos
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO I. INTRODUCCIÓN PRÁCTICA DE LABORATORIO 2014 SEMANA 2 EQUIPO BÁSICO DE LABORATORIO DE QUIMICA
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO I. INTRODUCCIÓN PRÁCTICA DE LABORATORIO 2014 SEMANA 2 EQUIPO BÁSICO DE LABORATORIO DE QUIMICA
6. Reacciones de precipitación
 6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
Electrodo selectivo de cloruro
 96 52 Electrodo selectivo de cloruro - Cl Código 10072 Edición Julio 2012 Electrodo selectivo de cloruro. Manual del usuario. Indice Introducción...3 Aplicaciones...3 Especificaciones...3 Instrumentos
96 52 Electrodo selectivo de cloruro - Cl Código 10072 Edición Julio 2012 Electrodo selectivo de cloruro. Manual del usuario. Indice Introducción...3 Aplicaciones...3 Especificaciones...3 Instrumentos
Titulaciones en Química Analítica. Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D.
 Titulaciones en Química Analítica Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D. Introducción En el análisis volumétrico, la concentración se determina midiendo su capacidad de reaccionar con un reactivo
Titulaciones en Química Analítica Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D. Introducción En el análisis volumétrico, la concentración se determina midiendo su capacidad de reaccionar con un reactivo
Sistema Integrado de Gestión NEUTRALIZACIÓN ACIDO-BASE TITULACIÓN DE UN ACIDO CON UNA BASE PROGRAMA FISIOTERAPIA GUIA PRÁCTICA N 4
 Sistema Integrado de Gestión NEUTRALIZACIÓN ACIDO-BASE TITULACIÓN DE UN ACIDO CON UNA BASE PROGRAMA Versión 5 Proceso: Investigación IV Febrero de 2016 Página 2 de 12 1. OBJETIVOS Valorar (titular) una
Sistema Integrado de Gestión NEUTRALIZACIÓN ACIDO-BASE TITULACIÓN DE UN ACIDO CON UNA BASE PROGRAMA Versión 5 Proceso: Investigación IV Febrero de 2016 Página 2 de 12 1. OBJETIVOS Valorar (titular) una
PRACTICA DE LABORATORIO # 1. PREPARACIÓN DE UNA SOLUCIÓN 0,1 N DE PERMANGANATO DE POTASIO Y SU ESTANDARIZACIÓN CON OXALATO DE SODIO.
 UNIVERSIDAD NACIONAL AUTONOMA DE NICARAGUA, MANAGUA RECINTO UNIVERSITARIO RUBEN DARIO FACULTAD DE CIENCIAS E INGENIERÍA DEPARTAMENTO DE QUÍMICA QUIMICA INDUSTRIAL METODOS DE ANALISIS INSTRUMENTAL PRACTICA
UNIVERSIDAD NACIONAL AUTONOMA DE NICARAGUA, MANAGUA RECINTO UNIVERSITARIO RUBEN DARIO FACULTAD DE CIENCIAS E INGENIERÍA DEPARTAMENTO DE QUÍMICA QUIMICA INDUSTRIAL METODOS DE ANALISIS INSTRUMENTAL PRACTICA
F-CGPEGI-CC-01/REV-00
 F-CGPEGI-CC-01/REV-00 UNIVERSIDAD AUTONOMA DE YUCATAN FACULTAD DE MEDICINA LABORATORIO DE CIENCIAS FISIOLOGICAS MANUAL DE PREPARACIÓN DE REACTIVOS RESPONSABLE DEL LABORATORIO DE CIENCIAS FISIOLOGICAS Q.
F-CGPEGI-CC-01/REV-00 UNIVERSIDAD AUTONOMA DE YUCATAN FACULTAD DE MEDICINA LABORATORIO DE CIENCIAS FISIOLOGICAS MANUAL DE PREPARACIÓN DE REACTIVOS RESPONSABLE DEL LABORATORIO DE CIENCIAS FISIOLOGICAS Q.
2A Reacciones de Sustitución Nucleofílica Alifática. Obtención de Cloruro de ter-butilo.
 PRÁCTICA 2A Reacciones de Sustitución Nucleofílica Alifática. Obtención de Cloruro de ter-butilo. I. OBJETIVOS. a) Conocer la preparación de un haluro de alquilo terciario a partir del alcohol correspondiente,
PRÁCTICA 2A Reacciones de Sustitución Nucleofílica Alifática. Obtención de Cloruro de ter-butilo. I. OBJETIVOS. a) Conocer la preparación de un haluro de alquilo terciario a partir del alcohol correspondiente,
CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO. Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión
 EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
Estudio cinético de la reacción entre el yodo y la acetona catalizada por ácido
 Laboratorio de Química Física 1 Curso 2011-2012 Grado en Química PRÁCTICA 5 Estudio cinético de la reacción entre el yodo y la acetona catalizada por ácido Material 1 probeta de 100 ml 1 aforado de 500
Laboratorio de Química Física 1 Curso 2011-2012 Grado en Química PRÁCTICA 5 Estudio cinético de la reacción entre el yodo y la acetona catalizada por ácido Material 1 probeta de 100 ml 1 aforado de 500
FACULTAD: CIENCIAS DE LA SALUD CARRERA PROFESIONAL: FARMACIA Y BIOQUIMICA CENTRO ULADECH CATÓLICA: TRUJILLO NOMBRE DE LA ASIGNATURA: QUÍMICA ANALITICA
 FACULTAD: CIENCIAS DE LA SALUD CARRERA PROFESIONAL: FARMACIA Y BIOQUIMICA CENTRO ULADECH CATÓLICA: TRUJILLO NOMBRE DE LA ASIGNATURA: QUÍMICA ANALITICA CICLO ACADÉMICO: II NOMBRE DEL GRUPO: LOS POSITRONES
FACULTAD: CIENCIAS DE LA SALUD CARRERA PROFESIONAL: FARMACIA Y BIOQUIMICA CENTRO ULADECH CATÓLICA: TRUJILLO NOMBRE DE LA ASIGNATURA: QUÍMICA ANALITICA CICLO ACADÉMICO: II NOMBRE DEL GRUPO: LOS POSITRONES
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS PROGRAMAS DE DEPORTE Y FISIOTERAPIA GUIA PRÁCTICA N 6
 Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Problemas disoluciones
 Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
Ácidos y bases fuertes y débiles
 9. Ácidos y bases fuertes y débiles Problemas Estimar comparativamente la acidez libre en una disolución de un ácido fuerte con la acidez libre en una disolución de un ácido débil, ambas a la misma concentración.
9. Ácidos y bases fuertes y débiles Problemas Estimar comparativamente la acidez libre en una disolución de un ácido fuerte con la acidez libre en una disolución de un ácido débil, ambas a la misma concentración.
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-302-1985. ALIMENTOS PARA USO HUMANO. AZÚCAR. DETERMINACIÓN DE SUBSTANCIAS REDUCTORAS EN MUESTRAS DE AZÚCAR CRUDO (MASCABADO). FOODS FOR HUMAN USE. DETERMINATION OF REDUCING SUBSTANCES IN RAW SUGAR
NMX-F-302-1985. ALIMENTOS PARA USO HUMANO. AZÚCAR. DETERMINACIÓN DE SUBSTANCIAS REDUCTORAS EN MUESTRAS DE AZÚCAR CRUDO (MASCABADO). FOODS FOR HUMAN USE. DETERMINATION OF REDUCING SUBSTANCES IN RAW SUGAR
Tarea Nº 5 de Química Analítica Problemas que involucran densidades
 Tarea Nº 5 de Química Analítica Problemas que involucran densidades 1.- Cuál es la densidad de una pieza moldeada y elaborada con un polímero experimental la cual pesa 4.7863 g y que al sumergirla en agua
Tarea Nº 5 de Química Analítica Problemas que involucran densidades 1.- Cuál es la densidad de una pieza moldeada y elaborada con un polímero experimental la cual pesa 4.7863 g y que al sumergirla en agua
INTRODUCCIÓN A LA ESPECTROFOTOMETRÍA
 INTRODUCCIÓN A LA ESPECTROFOTOMETRÍA Objetivos Al finalizar el trabajo práctico los estudiantes estarán en capacidad de: - Conocer el principio que rige la espectrofotometría. - Interpretar el basamento
INTRODUCCIÓN A LA ESPECTROFOTOMETRÍA Objetivos Al finalizar el trabajo práctico los estudiantes estarán en capacidad de: - Conocer el principio que rige la espectrofotometría. - Interpretar el basamento
CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN
 II PRÁCTICA 2 CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN En esta experiencia comprobaremos la influencia de la concentración de los reactivos, de la temperatura, y de
II PRÁCTICA 2 CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN En esta experiencia comprobaremos la influencia de la concentración de los reactivos, de la temperatura, y de
GUIÓN DE PRÁCTICAS PRIMER CUATRIMESTRE
 TITULACIÓN: GRADO EN QUÍMICA ASIGNATURA: QUÍMICA ANALÍTICA CURSO: º GUIÓN DE PRÁCTICAS PRIMER CUATRIMESTRE ÍNDICE 1. Introducción al laboratorio analítico. Determinación de la alcalinidad de un agua..
TITULACIÓN: GRADO EN QUÍMICA ASIGNATURA: QUÍMICA ANALÍTICA CURSO: º GUIÓN DE PRÁCTICAS PRIMER CUATRIMESTRE ÍNDICE 1. Introducción al laboratorio analítico. Determinación de la alcalinidad de un agua..
Materiales Pipetas ;Tubos de ensayo ;Vaso de precipitado ;Sistema calentador (placa calefactora) ;Probeta
 PRÁCTICA 3: Lluvia de oro Parte cualitativa En primer lugar, de forma cualitativa, se demuestra que la lluvia de oro es una reacción iónica y por tanto muy rápida. Esta parte consta de la formación de
PRÁCTICA 3: Lluvia de oro Parte cualitativa En primer lugar, de forma cualitativa, se demuestra que la lluvia de oro es una reacción iónica y por tanto muy rápida. Esta parte consta de la formación de
PRACTICA No. 9 PREPARACION DE DISOLUCIONES
 ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II 1. INTRODUCCION: PRACTICA No. 9 PREPARACION DE DISOLUCIONES Las mezclas homogéneas se originan cuando un disolvente rompe la unión
ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II 1. INTRODUCCION: PRACTICA No. 9 PREPARACION DE DISOLUCIONES Las mezclas homogéneas se originan cuando un disolvente rompe la unión
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
Quito Ecuador CARBONATO DE SODIO PARA USO INDUSTRIAL. DETERMINACIÓN DEL CONTENIDO DE BICARBONATO DE SODIO. MÉTODO VOLUMÉTRICO
 Quito Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN 1886 CARBONATO DE SODIO PARA USO INDUSTRIAL. DETERMINACIÓN DEL CONTENIDO DE BICARBONATO DE SODIO. MÉTODO VOLUMÉTRICO SODIUM CARBONATE FOR INDUSTRIAL USE.
Quito Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN 1886 CARBONATO DE SODIO PARA USO INDUSTRIAL. DETERMINACIÓN DEL CONTENIDO DE BICARBONATO DE SODIO. MÉTODO VOLUMÉTRICO SODIUM CARBONATE FOR INDUSTRIAL USE.
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: Nombre: Nombre: Nombre: Nombre:
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Práctica 9 Ácidos y bases fuertes y débiles PREGUNTAS A RESPONDER AL FINAL DE LA PRÁCTICA
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Práctica 9 Ácidos y bases fuertes y débiles PREGUNTAS A RESPONDER AL FINAL DE LA PRÁCTICA
Métodos para la cuantificación de nitrógeno y proteína
 Practica 5 Métodos para la cuantificación de nitrógeno y proteína Antecedentes Para la determinación de proteínas en muestras de alimentos se cuenta con una gran variedad de métodos, basados en diferentes
Practica 5 Métodos para la cuantificación de nitrógeno y proteína Antecedentes Para la determinación de proteínas en muestras de alimentos se cuenta con una gran variedad de métodos, basados en diferentes
PROTOCOLO DE PRÁCTICA PREPARACIÓN Y ANÁLISIS DE MUESTRAS DE AGUA
 PROTOCOLO DE PRÁCTICA PREPARACIÓN Y ANÁLISIS DE MUESTRAS DE AGUA IDENTIFICACION DE LA PRÁCTICA Nombre de curso Preparación y Análisis de Muestras de Agua Código de curso 358004 Créditos del curso Dos (2)
PROTOCOLO DE PRÁCTICA PREPARACIÓN Y ANÁLISIS DE MUESTRAS DE AGUA IDENTIFICACION DE LA PRÁCTICA Nombre de curso Preparación y Análisis de Muestras de Agua Código de curso 358004 Créditos del curso Dos (2)
Determinación de Sólidos Disueltos Totales en Aguas
 QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Sólidos Disueltos en Aguas Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 22/09/2013 Método Gravimétrico Página 2 de 7
QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Sólidos Disueltos en Aguas Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 22/09/2013 Método Gravimétrico Página 2 de 7
PRÁCTICA 3 DETERMINACIÓN ESPECTROFOTOMÉTRICA DEL pk DE UN INDICADOR
 PRÁCTICA 3 DETERMINACIÓN ESPECTROFOTOMÉTRICA DEL pk DE UN INDICADOR Material Productos 2 matraces aforados de 250 ml Hidróxido de sodio en lentejas 2 matraces aforados de 25 ml Disolución de hidróxido
PRÁCTICA 3 DETERMINACIÓN ESPECTROFOTOMÉTRICA DEL pk DE UN INDICADOR Material Productos 2 matraces aforados de 250 ml Hidróxido de sodio en lentejas 2 matraces aforados de 25 ml Disolución de hidróxido
Química Inorgánica. Profesor: Rafael Aguado Bernal. Separaciones sólido líquido
 Separaciones solido líquido: Precipitación, centrifugado, filtración, secado 1/6 INTRODUCCION: Separaciones sólido líquido Preparación de sólidos por precipitación. Separación de sólidos por filtración
Separaciones solido líquido: Precipitación, centrifugado, filtración, secado 1/6 INTRODUCCION: Separaciones sólido líquido Preparación de sólidos por precipitación. Separación de sólidos por filtración
